-
目前全球尚无预防和治疗新冠肺炎(COVID-19)确认的特效药物。有学者试图遴选已有的抗病毒药物,以期尽快开发“老药新用”的治疗方案。国家卫生健康委员会陆续发布了7版试行《新型冠状病毒肺炎诊疗方案》,其中,广谱抗病毒药物利巴韦林被作为可试用的临床治疗药物。
利巴韦林(ribavirin)常用剂型有注射剂、片剂、口服液、气雾剂等,国外临床上多以雾化剂用于成人和儿童的呼吸道合胞病毒性肺炎的治疗[1]。体外研究表明[2],利巴韦林可增强干扰素的体外活性,在治疗SARS-CoV感染者中,诊断后立即使用利巴韦林时治疗效果较好[3]。利巴韦林对DNA和RNA病毒均具有抑制作用,通常以雾化剂用于成人和儿童的呼吸道合胞病毒性肺炎的治疗。美国食品药品管理局(FDA)于1986年首次批准利巴韦林吸入溶液气雾剂(Virazole®,USP)[4],于1992年上市,而说明书中明确规定用于严重下呼吸道感染的住院患儿,且全程气雾治疗3~7 d,可见其应用的严格限制。根据国内多家临床中心的试验数据表明,与利巴韦林颗粒剂相比,国内的利巴韦林气雾剂(信韦林)达到同等的治疗效果时,虽然用药剂量大幅下降,但不良反应率无明显差异[5-8],表明利巴韦林吸入溶液气雾剂(Virazole®,USP)和利巴韦林气雾剂(信韦林)可能存在不良反应较大的缺陷,临床应用受到一定的限制。
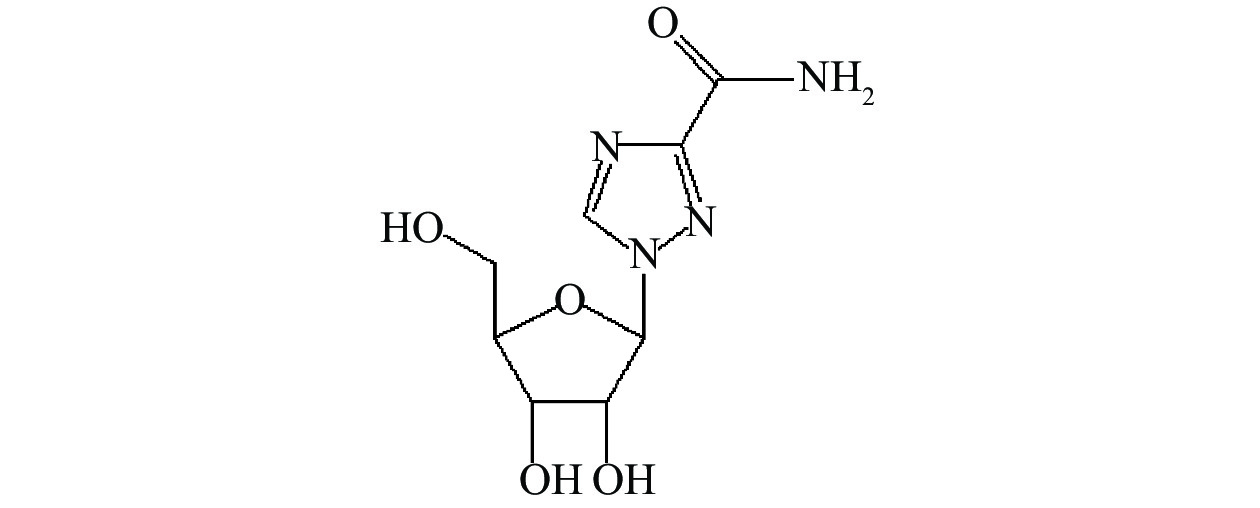
脂质体定量吸入粉雾剂(DPI)是肺部给药系统的研究热点之一。脂质体由于类似细胞结构而具有被动靶向性,作为药物载体常用于肺部给药,有利于抗病毒药物直接递送并作用于肺部细胞,抑制病毒的繁殖,特定粒径的脂质体粉雾剂可使药物不同程度地的分布于人体上、下呼吸道,从而发挥更好的临床治疗效果[9-10]。利巴韦林水溶性较好,亲脂性较差,如图1的结构式所示,不易被细胞渗透吸收,采用脂质体包裹,并制成粉雾剂给药至呼吸道或肺泡组织,可实现肺部沉积增强的作用效果,同时降低不良反应。本文根据临床急需及利巴韦林的药物理化性质,结合吸入制剂肺部给药方面的治疗优势,设计研制了一种利巴韦林脂质体吸入粉雾剂。以此开展设计研究,尝试开发抗病毒药物新型给药系统,以期为扩大利巴韦林临床使用范围,也为制剂学基础研究提供参考。
HTML
-
高效液相色谱仪(Agilent 1200);ME104E电子天平(METTLER TOLEDO);EYELA N-1000旋转蒸发仪(日本东京理化器械株式会社);Niro NS2006L高压匀质机(意大利GEA Niro Soavi公司);Nano NS90粒度检测仪(英国马尔文仪器有限公司);Hitachi S-3400N扫描电子显微镜(日本日立公司)。
-
利巴韦林原料药(纯度>98%,西安康诺化工有限公司);利巴韦林对照品(629-200202,中国食品药品检定研究院);大豆卵磷脂(SPC)、脱氧胆酸钠(SDC)(北京化学试剂公司);N,N-二甲基甲酰胺、无水乙醇、磷酸氢二钠、磷酸二氢钠(分析纯,北京化学试剂公司);蒸馏水。
1.1. 仪器
1.2. 材料
-
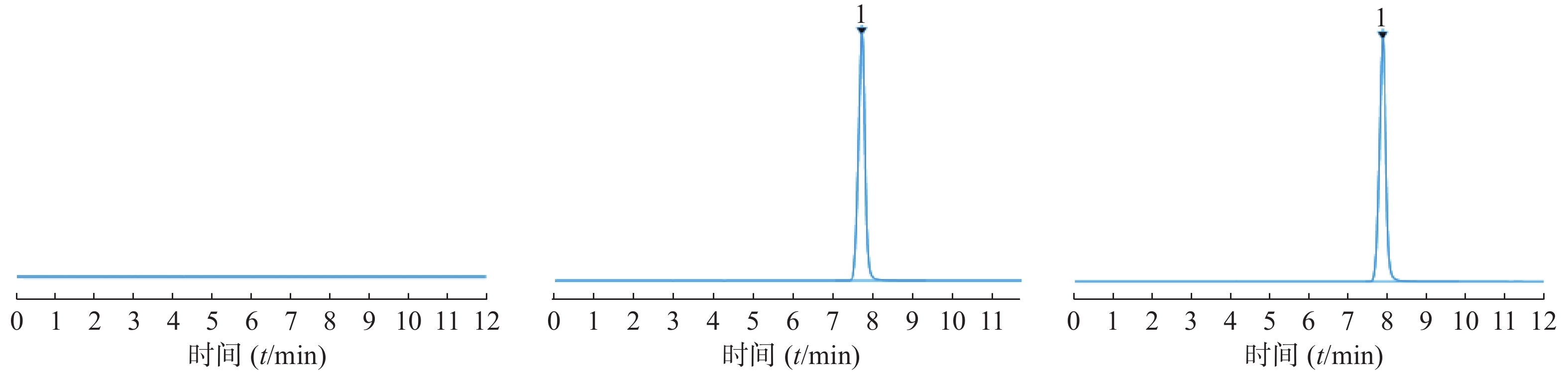
参照美国药典第40版中“利巴韦林”含量测定方法[11],采用高效液相色谱法测定。色谱条件:色谱柱为Carbomix H-NP5(7.8 mm×100 mm,5 μm);流动相硫酸溶液调整pH至2.5±0.1;流速:0.6 ml/min;柱温:60 ℃;检测波长UV 207 nm;进样量10 μl,取利巴韦林对照品适量,流动相溶解稀释至浓度为0.025 mg/ml,过滤,进样检测。取利巴韦林脂质体冻干粉适量,加入无水乙醇少量破乳,呈透明溶液后流动相稀释,制成浓度0.025 mg/ml供试品溶液;同样方式处理阴性样品溶液。在该色谱条件下得到图2的色谱图,图中利巴韦林峰型较佳,出峰时间适宜,阴性对照无干扰。
-
取大豆卵磷脂(5 mmol/L),脱氧胆酸钠(5 mmol/L),为制备具有高稳定性的双分子膜,在处方中加入适量维生素E置于250 ml的茄形瓶中,加入无水乙醇溶解,超声,至呈透明黄色溶液;将此溶液置旋转蒸发仪上旋转蒸发除去溶剂成膜;另取利巴韦林原料药溶解于磷酸盐缓冲液中(20 mg/ml),溶解完全后匀速加入至茄形瓶内,并于40 ℃水浴温度水化薄膜,直到完全水化呈近均一透明的乳白色溶液;高压均质机下将上述溶液均质,即得到粒径100~200 nm的利巴韦林脂质体溶液。加入冻干保护剂乳糖, 溶解摇匀后置西林瓶中,启动冷冻干燥程序,即得疏松利巴韦林脂质体冻干粉。
-
取载药脂质体经处理后于透射电镜下观察,呈类圆形球状物,直径约200 nm,见图3。
-
将粉末通过下孔径为5 mm 的玻璃漏斗,从10 cm的高度缓慢、均匀地落入平板上,形成圆锥体。测量圆锥体的高度(h)和基底的半径(r),按公式计算休止角(θ,tanθ=h/r)。粉末休止角为37~40°,流动性较好。取量筒,自由落体方式装入脂质体冻干粉,记录质量与体积,计算松密度约0.25 g/ml。
-
取利巴韦林脂质体冻干粉适量,纯化水溶解得脂质体复溶物,取复溶物适量加入无水乙醇少量破乳,呈透明溶液后用流动相稀释,制成0.025 mg/ml供试品溶液,按“2.1”项下色谱条件检测冻干粉含量。
经过前期实验对比,本研究采用Sephadex G-50柱层析法测定包封率。分别精密量取1 ml脂质体和冻干粉复溶物上柱,用纯化水洗脱,流速0.5 d/s,从洗脱液由澄清变乳白色开始收集至洗脱液再次变澄清(约15 ml),置50 ml容量瓶中,以乙醇定容至刻度,振摇破乳;10 μl进样分析,记录色谱图,计算包封药物含量(W包);另各取1 ml脂质体溶液及冻干粉复溶物置50 ml容量瓶中,乙醇稀释至刻度,振摇破乳,10μl进样分析,记录色谱图,计算总药量(W总)。以包封率=(W包/W总)×100%,计算结果见表1。
项目 样品 No.1 No.2 No.3 平均值 含量(mg/g) 脂质体冻干粉末 9.4 8.6 9.3 9.1 包封率 /% 冻干前脂质体溶液 64.23 63.83 66.34 64.80 脂质体冻干粉复溶液 63.43 61.65 64.10 63.06 结果表明,按照初步拟定方法制得的脂质体包封率约63%,冻干前后数据无明显差别,复溶效果较好,载药量较高,但包封率较低,处方工艺需要进一步优化。
-
取本品复溶液适量,纯化水再次稀释100倍,于马尔文粒径仪检测,如表2所示,本品冻干前后溶液粒径约160 nm,聚合物分散指数(PDI)、电位均较好,表明稳定性较好。
样品 No.1 No.2 No.3 平均值 粒径/PDI 电位 粒径/PDI 电位 粒径/PDI 电位 粒径 电位 冻干前溶液 148.3 nm/0.57 −45.4 mv 163.7 nm/0.63 −41.8 mv 172.6 nm/0.39 −40.5 mv 161.5 nm −42.6 mv 冻干复溶液 147.8 nm/0.58 −42.5 mv 161.8 nm/0.65 −38.6 mv 181.7 nm/0.41 −39.1 mv 163.8 nm −40.1 mv -
脂质体具有优良的两亲性,冻干保护剂亦有很好的亲水性。取本品冻干粉5 g置10 ml容量瓶中,加水10 ml,轻轻振摇即刻溶解完成,形成均一的乳白色胶束溶液,说明本品溶解性较好。
2.1. 利巴韦林脂质体冻干粉含量测定方法
2.2. 利巴韦林脂质体粉雾剂的制备
2.3. 外观形态
2.4. 流动性、松密度
2.5. 包封率、冻干粉含量测定
2.6. 复溶液粒径、聚合物分散指数与电位测定
2.7. 冻干粉溶解性
-
病毒通过侵入人体呼吸道黏膜上皮细胞而感染,并在细胞内进行复制与表达,再释放至细胞外感染宿主其他细胞,最终导致机体产生过度免疫反应。与一些在下呼吸道的细胞内进行复制繁殖的高致病性病毒类似,COVID-19导致下呼吸道症状较为明显。故若将抗病毒药物递送至下呼吸道,直达病灶,并进入被感染的机体上皮细胞内,可能更好地发挥抑制或清除病毒的作用。通常肺吸入给药后可直接将药物运送至肺组织,在局部起效,与全身给药治疗肺部疾病相比较,可明显减少药物用量,降低药物在其他部位分布与吸收造成的不良反应,加之粉雾剂具备给药剂量准确、无需抛射剂、方便、易用及肺部靶标部位药物沉积量高等优势,是肺部疾病治疗药物较为理想的给药途径。
将利巴韦林通过脂质体包裹技术实现粉雾剂肺部细胞靶向治疗,相比普通口服与常规气雾剂可减少用药剂量和降低不良反应,理论上具有一定的可行性。因而,对轻、中度COVID-19感染患者也许是一种潜在的抗病毒药物治疗方式。
经对利巴韦林脂质体粉雾剂的初步制剂技术探究,结果证明制备的制剂满足粉雾剂的基本要求。由于粉雾剂具有无需抛射剂、药物相对稳定的优势[12],而且给药装置易于携带,操作简单、给药剂量相对准确等优点,故适合开发研制成利巴韦林脂质体吸入粉雾剂。此外,制备的利巴韦林脂质体冻干粉还可开发为溶液气雾剂,故在药剂开发方面也有较好前景。然而,本实验尚为初步研究,仍需要对制剂处方工艺进一步优化,以进一步提高包封率与改善整体粒径分布等性能。如要进入临床试用,还需对给药装置筛选、体内外药物沉积、药效学等进行深入考察,以满足临床使用的基本要求。








 DownLoad:
DownLoad: