-
随着人口老龄化进程加快,以脑、脊髓结构或功能损伤导致的中枢神经系统(CNS)疾病的发病率和病死率逐年上升[1]。尽管对CNS疾病病因的认识已有重大进展,但是新药研发进程依旧进展缓慢,主要原因是CNS疾病发病机制复杂,以及在药物研发阶段缺少可靠有效的评价手段[2]。随着系统生物学技术的不断发展,1999年Nicholson等[3]提出的代谢组学通过研究生物体受到外界刺激或基因缺陷所导致的代谢终产物的变化情况,为研究疾病的发病机制和药物疗效评估提供了一种新手段。来源于患者或疾病动物模型的生物体样本,如血液、尿液、组织提取液等的代谢组学研究是目前的主要研究方向,但是实验研究需要大量样本数据支持,且受到伦理以及生物体内外混杂因素的影响,具有一定的局限性。细胞是构成生物体结构和功能的基本单位,体外细胞模型可建立单一症状的疾病模型、具有可控性强、有利于进行大规模药物筛选等特点而备受研究人员青睐。细胞代谢组学是以细胞为研究对象,通过现代分析方法监测细胞反应及药物作用于细胞后的代谢变化,在探寻CNS疾病的病理生理机制及治疗干预效果中展现出巨大潜力[4]。本文拟从细胞代谢组学的研究流程及其在中枢神经系统疾病中的应用进行综述,以期为从细胞层面探索中枢神经系统疾病发病机制和新药研发提供参考。
-
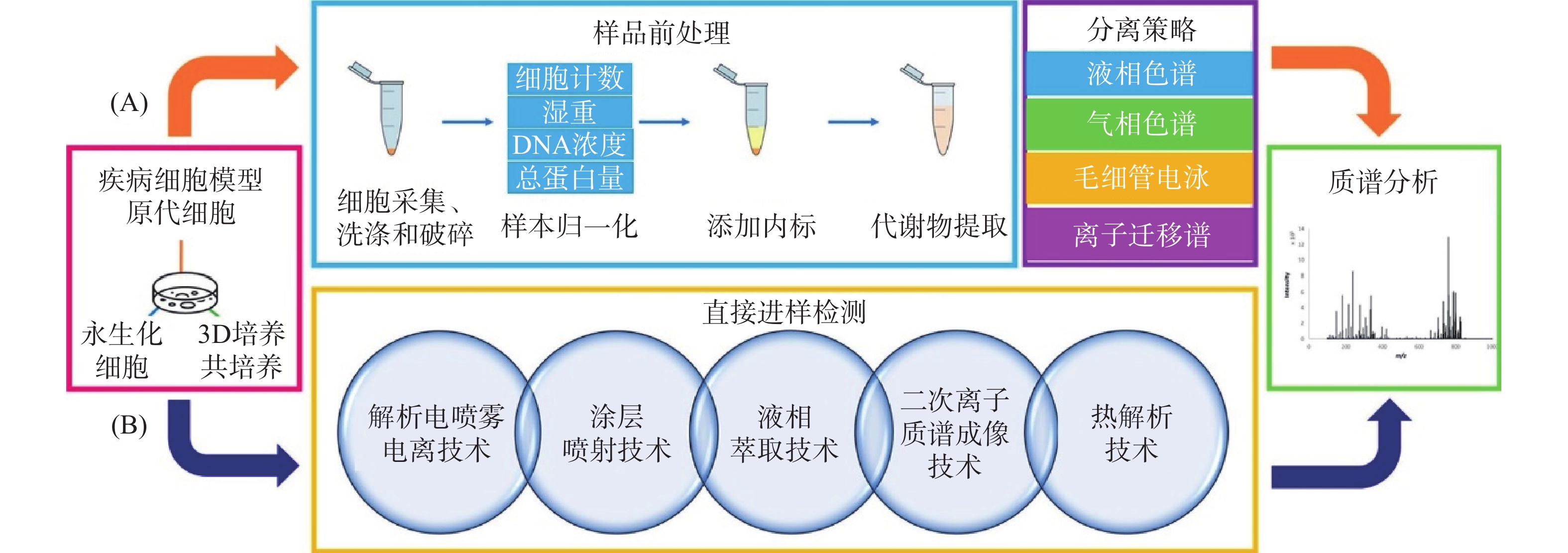
细胞代谢组学通过现代分析方法对细胞新陈代谢后产生的差异代谢物进行定性、定量研究。介于细胞内和细胞外代谢之间的密切关系,完整的细胞代谢组学研究包括细胞内指纹(细胞内所有代谢物)和细胞外足迹(细胞外介质所有代谢物)两部分[5],其主要流程为细胞培养、样品前处理、分析检测、代谢组学数据处理(图1)。
-
细胞类型和培养方法的选择对模拟疾病状态和深入了解疾病的代谢框架至关重要。来源于生物体的原代细胞是疾病研究的理想细胞模型,但其寿命有限,纵向研究具有一定挑战性。因此,能够快速分裂的癌细胞和永生化细胞被广泛用于体外模型的构建中。有研究表明,体外和体内细胞培养条件不同易导致细胞特性的改变[7]。为了能更准确地模拟体内微环境,自20世纪初建立以来,改进细胞培养技术的尝试从未停止,如在二维单层培养的基础上,研发出三维培养技术、旋转式细胞培养系统、多细胞共培养等培养模式,更加贴近细胞在生物体的生存环境[8-10]。
提取目标代谢物是细胞代谢组学分析的关键步骤。一些代谢物在样品前处理过程中受到干燥-重构的影响易产生损失或变异,因而优化样品前处理方法、建立细胞代谢组学标准化分析流程显得尤为重要[11]。Wilkins等[12]比较胰蛋白酶消化、刮刀刮取、−80 ℃甲醇淬灭以及−80 ℃甲醇淬灭后去除甲醇这4种常用的细胞代谢物提取方法,结果显示,−80 ℃甲醇快速淬灭得到的细胞代谢物稳定性和富集程度较好,且样品在−80 ℃甲醇条件下可以储存长达1个月而没有明显的代谢物降解。Ser等[13]发现温度和添加剂对细胞代谢物的影响很小,而使用磷酸盐缓冲溶液或水洗涤样品对代谢物影响较大,并提出用冷甲醇提取且不经任何洗涤可以满足绝大多数代谢物的提取。随着质谱等检测仪器的不断开发和进步,不经任何前处理将采集到的细胞代谢物直接进样分析也成为了可能[14]。
-
核磁共振波谱法(NMR)和质谱法(MS)是细胞代谢组学研究的常用分析方法。NMR可追踪代谢物流动来识别活跃的代谢途径、测量代谢通量或相应的示踪剂代谢变化,所需样品量少,具有出色的重现性、定量以及鉴定未知代谢物的能力。Saborano等[15]提出一种基于NMR法的哺乳动物细胞系和原代细胞系代谢研究框架,可用于糖酵解、戊糖磷酸循环等多种代谢途径分析。具体工作流程为将含有13C或15N标记的前体物质引入细胞培养基中培养细胞,使用甲醇-氯仿-水提取代谢物,通过异核单量子相干谱(HSQC)、二维NOE谱(NOESY)等技术采集带标记代谢物的光谱信息,探寻细胞系中健康和疾病状态的代谢差异。然而,NMR相对较低的灵敏度使其无法测量低丰度的代谢物。越来越多新型NMR方法包括多维NMR技术、快速脉冲NMR技术、核磁共振显微技术等也逐渐应用于细胞代谢组学研究,为生物标志物的寻找提供了有力手段。
MS的优势在于其灵敏度高、覆盖面广、可与多种色谱技术联用实现代谢物的有效分离。气相色谱-质谱联用法(GC-MS)可用于氨基酸、核苷酸和脂肪酸等挥发性代谢物的分析,具有较强的针对性。为简化样品制备过程中对挥发性代谢物的衍生化步骤,Araujo等[16]优化了一种基于顶空固相微萃取(HS-SPME)结合GC-MS方法,通过纤维涂层对细胞外代谢物中挥发性组分萃取后直接进样分析,可实时监测挥发性有机物的代谢过程。液相色谱-质谱联用法(LC-MS)包括反相液相色谱(RPLC)和亲水作用液相色谱(HILIC)与MS的联用,其中RPLC总体上表现出比HILIC更好的适用性和重复性,被广泛应用于细胞代谢物的分析中,尤其适用于非极性和弱极性代谢物,而HILIC对亲水性、极性和离子性代谢物如糖、氨基酸和核酸有更好的分离效果[17]。Sun等[18]采用UHPLC-QQQ/MS法对细胞外代谢物进行分析,液相分离条件的优化分别考察了7根反相UHPLC柱和5根HILIC柱,以峰面积、半峰宽、拖尾因子、峰面积CV(%)、保留时间及其SD值共6个指标评价分离效果,最终选择了其中的1根反相UHPLC柱和流动相,单次检测时间仅17 min,实现了同时检测氨基酸、糖类等93种代谢物,为开展实时监测细胞代谢物水平变化提供了可能性。
考虑到细胞间存在异质性,为获得更加丰富的细胞代谢物信息,现代生命科学研究将目光投向了单个细胞。微流控芯片可以在与细胞大小相当的微通道内进行细胞培养、样品制备、分离检测等一系列操作,是单细胞代谢组学分析的重要技术平台[19],相比于LC-MS,微流控芯片质谱法操作简单,可直接进样分析,但存在选择性差和离子抑制等问题,Xu等[20]将微流控芯片与纳米电喷雾电离质谱相联用,通过对金纳米颗粒进行特异性标记,大大提高单细胞水平内源代谢物检测的灵敏度和兼容性。得益于质谱成像仪器的快速发展,空间分辨代谢组学技术可以对目标代谢物在细胞中的分布进行定位,提供多维度代谢组学信息,是目前单细胞代谢组学研究的强有力工具[21]。
-
代谢物的存在和浓度变化可以直接体现细胞对周围化学和物理微环境的反应,具有高度动态性和未知性,庞大的数据集使得细胞代谢组学的数据分析和解释需借助生物信息学[22]。基于R、Python、C/C++ 等编程语言的代谢组学数据处理的软件资源有很多,但是尚未研发出通用的数据处理软件,需要用户根据分析目的对多种软件程序整合后优化使用[23]。Zhou等[24]在IP4M代谢组学数据分析集成平台的基础上,开发出IMAP集成代谢组学分析平台,不仅可以实现一站式完整的代谢组数据分析,而且有多种可供选择的分析方法和工作流程,可用于建立和验证预测模型以及相关的网络构建和分析,适用于批量或有特殊要求的数据分析。孙海涛等[25]提出了一种基于开源软件Mzmine和谱峰预识别算法,多个计算资源并行的云计算代谢组学数据处理方法,所提出的并行数据处理方法与单计算节点相比,计算速度得到显著提升且大大降低了研究费用,可满足海量代谢组学的数据处理需求。
-
CNS疾病影响着全球数百万患者的生命健康,其发病机制复杂,涉及神经细胞凋亡、神经炎症、氧化应激、兴奋性损伤等多种病理特征,给疾病的早期诊断和预后评估带来了很大的困难。构建单一病理状态的体外细胞模型,可以进行大规模的靶向研究和药物筛选,大大缩短了新药研发时间[26]。尽管已有各种类型的CNS疾病体外细胞模型,但其中只有少数被用于代谢组学研究。随着细胞代谢组学在探索CNS疾病发病机制以及药物作用特点中的作用日益突出,越来越多潜在的生物标志物被发现。表1归纳了2015年以来有关细胞代谢组学在CNS疾病研究的一些应用实例,包括常见CNS疾病相应的细胞模型构建、细胞代谢组学分析手段、差异代谢物筛选、通路分析及药物干预结果等。
疾病 研究对象 研究药物 检测手段 主要研究结果 参考文献 阿尔茨海默病 PC12细胞
(Aβ25~35)柚皮苷 GC-MS 筛选出甘氨酸、谷氨酸等27种AD差异代谢物,影响氨基酸代谢、碳水化合物代谢及脂质代谢等代谢通路 [27] 脑微血管内皮细胞(Aβ1~42) 丹参 UHPLC-QTOF- MS 发现了33个差异代谢物,涉及精氨酸和脯氨酸代谢、谷胱甘肽代谢等多条代谢通路 [28] SH-SY5Y细胞
(冈田酸)丹参、知母 UHPLC-QTOF- MS 发现了色氨酸、苯丙氨酸等45个潜在AD生物标志物,涉及12条代谢通路,筛选出与丹参相关的30种差异代谢物,与知母相关的7种差异代谢物 [29] SH-SY5Y细胞
(谷氨酸)人参皂苷 Rb1 1H NMR 发现谷氨酸、牛磺酸等7种差异代谢物,涉及5条不同的代谢通路 [30] 帕金森病 SH‐SY5Y细胞
(MPP+)胶质细胞源性神经营养因子 LC‐MS/MS 三酰甘油、磷脂酰胆碱等多种脂质代谢物受到影响 [31] SH-SY5Y细胞
(6-OHDA)花茶 UPLC-TOF-MS 发现多种与神经保护作用相关的代谢物 [32] SH-SY5Y细胞
(A53T基因突变)L-天冬酰胺酶 GC-MS/MS 可以调节谷氨酰胺代谢起到神经保护作用 [33] 抑郁症 PC12细胞
(皮质酮)阿魏酸 UPLC-QTOF-MS 发现24个差异代谢物,涉及氨基酸代谢、能量代谢和甘油磷脂代谢等代谢通路 [34] PC12细胞
(皮质酮)甘草苷 LC-MS 鉴定出谷氨酸、谷胱甘肽等11种潜在差异代谢物,涉及8条不同的代谢通路 [35] PC12细胞
(皮质酮)香附 UPLC-Q-TOF-MS 发现鞘磷脂、甘油磷脂等11种潜在差异代谢物 [36] PC12细胞 氯胺酮、羟基去甲氯胺酮对映体 GC-MS和CE-MS 发现甘油酸盐、柠檬酸盐、亮氨酸等49种潜在生物标志物 [37] 星形胶质细胞 氟西汀 1H NMR 发现17种潜在生物标志物,涉及脂质和氨基酸代谢通路 [38] 星形胶质细胞 文拉法辛 1H NMR 发现赖氨酸、酪氨酸、谷氨酸等31 种涉及能量、氨基酸和脂质代谢的差异代谢物 [39] -
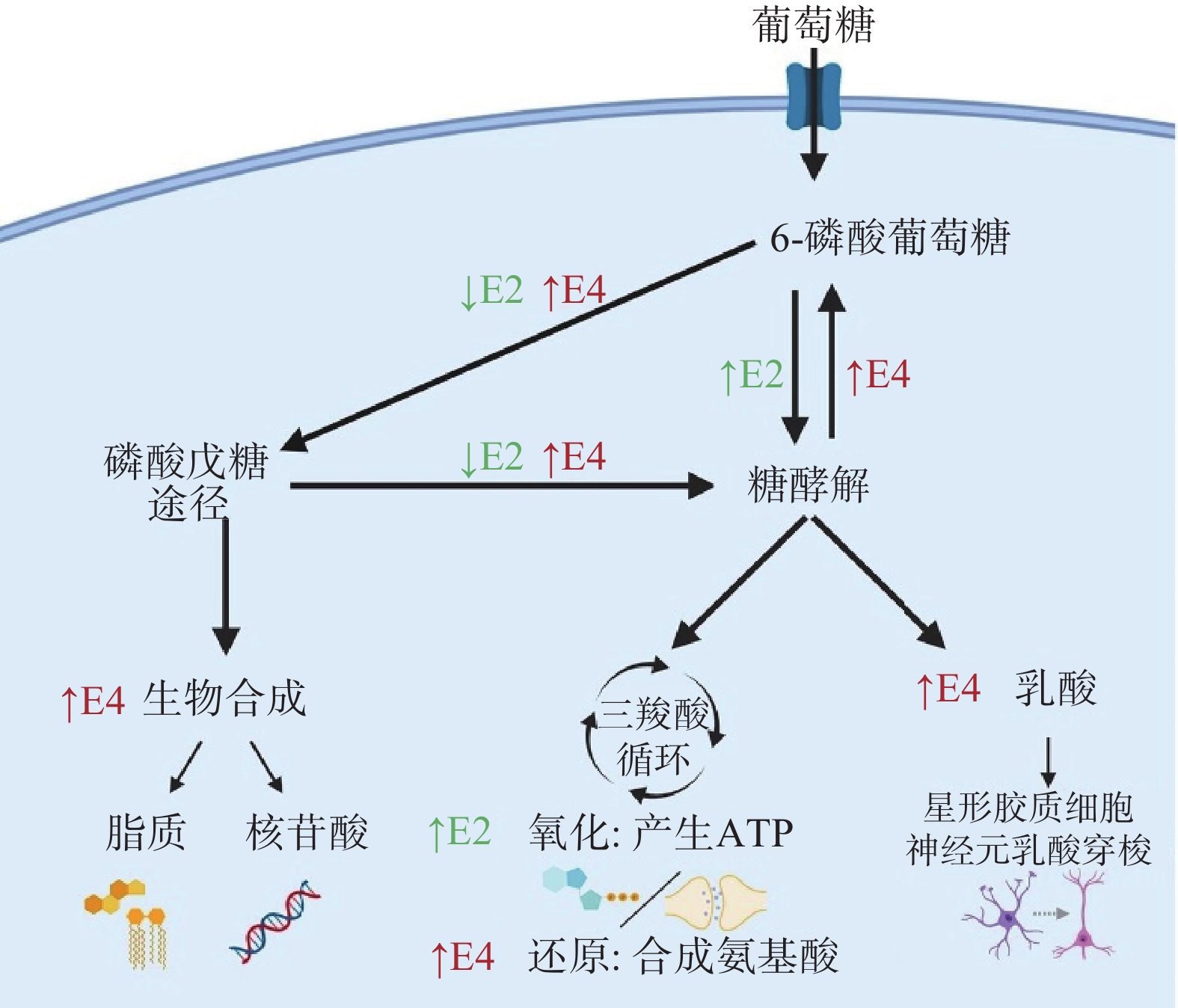
阿尔茨海默病(AD)是一种常见于老年人的神经退行性疾病,临床表现为记忆力减退、认知和交流功能障碍[40]。常用的AD细胞模型有:β淀粉样蛋白(Aβ)诱导神经毒性模型、Tau蛋白异常磷酸化模型、氧化应激模型和基因转染模型[41]。Aβ聚集沉积易使细胞产生突触受损、线粒体功能障碍以及促进Tau蛋白病理化,当前AD防治的研究热点也集中于Aβ[42]。Aβ是由淀粉样前体蛋白(APP)经分泌酶水解产生,APP的异常突变与AD的发展密切相关,Xiong等[43]对APP过表达的转基因(N2a/APP695swe)细胞用作AD体外模型的可行性进行验证,并将其应用于缬氨霉素改善AD的作用机制研究,GC-MS结果显示,缬氨霉素作用N2a/APP695swe细胞3 h后Aβ1~42和Aβ1~40水平降低,此时,三磷酸腺苷(ATP)水平和柠檬酸、苹果酸、丙酮酸等ATP相关代谢产物显著增加。但是6~12 h其ATP代谢产物却呈现水平下降趋势,提示缬氨霉素的作用时间应加以控制,才能有效促进ATP产生,起到改善AD的作用。有研究指出载脂蛋白E(APOE)不同亚型携带者患AD的风险不尽相同,可能与影响大脑葡萄糖摄取有关。为了解构成APOE相关遗传风险的分子机制,Williams等[44]采用稳定同位素示踪技术探究APOE中3种亚型基因产生的星形胶质细胞葡萄糖代谢差异,结果显示,相较于E2和E3,受E4影响的星形胶质细胞葡萄糖摄取受损,相应的糖代谢、三羧酸循环以及戊糖磷酸途径发生变化,谷胱甘肽合成增加,详见图2所示。与人类APOE表达E4基因的小鼠模型的研究结果相印证[45],证实了AD发病与遗传基因的相关性。为深入了解E4和代谢损伤对大脑影响的生物学基础,进一步阐明AD的发病机制提供了科学依据。
-
帕金森病(PD)为第二大中枢神经退行性疾病,患者常出现运动迟缓、静止性震颤和强直等症状。PD 是一种由遗传、环境和生活方式等多因素共同作用的疾病,其病理特征表现为黑质多巴胺能神经元损伤丢失和α-突触核蛋白聚集[46]。神经毒素如百草枯、6-羟基多巴胺(6-OHDA)、1-甲基-4-苯基-四氢吡啶离子(MPP+)可诱导细胞多巴胺能神经元变性死亡,从而产生类似帕金森的病理特征,所建立的细胞模型可操作性强、重复性好,是目前最常用的PD细胞造模方法。Lei等[47]采用NMR与直接输注电喷雾电离质谱(DI-ESI-MS)联用的代谢组学方法探究百草枯诱导SH-SY5Y细胞产生的代谢谱变化,结果显示,磷酸戊糖途径中6-磷酸葡萄糖、6-磷酸果糖等代谢物增加,糖酵解与TCA 循环受到抑制。Xicoy等[48]运用LC-MS法研究6-OHDA诱导的SH-SY5Y细胞的脂类代谢变化,结果发现除了磷脂酰丝氨酸水平降低外,磷脂酰胆碱、磷脂酰甘油、磷脂酰肌醇和胆固醇水平变化情况均与PD患者血浆代谢组学结果相同[49]。进一步探究降胆固醇他汀类药物对该PD模型的神经保护作用,发现他汀类药物未展现相应的保护作用,反而是低剂量的胆固醇使SH-SY5Y细胞免受6-OHDA毒性,提示该细胞模型不适用于胆固醇参与的PD发生发展机制的研究。星形胶质细胞是人脑中含量最丰富的细胞类型,在维持PD患者大脑胆固醇稳态扮演着重要角色[50]。近年来,星形胶质细胞在PD发病机制中作用开始被发现。Sonninen等[51]通过UPLC-Q-TOF-MS法探究星形胶质细胞的代谢变化,发现LRRK2和GBA基因突变的PD星形胶质细胞出现α-突触核蛋白生成增加、钙水平升高、溶血磷脂酰乙醇胺等多种氨基酸代谢改变。
-
缺血性脑卒中(IS)是中风的一种常见形式,涉及神经炎症、氧化应激、兴奋性中毒等病理机制,患病后易导致脑损伤或残疾,严重者将危及生命,对人类健康构成极大威胁[52]。IS患者因急性血管闭塞所引起的脑组织缺血、缺氧,易使细胞自由基受损、钙离子超载、能量代谢紊乱,因此保护细胞免受缺氧缺糖的影响,是体外研究IS的思路之一。脑微血管内皮细胞是IS中损伤最严重的细胞,韩晨阳等[53]采用HPLC法发现该细胞在体外缺氧缺糖环境下产生ATP、二磷酸腺苷(ADP)含量降低,磷酸腺苷(AMP)含量增加等异常能量代谢变化,而这些病理变化与IS造成的细胞损伤相似。进一步探究丁苯酞对该模型的作用机制发现,丁苯酚可以有效调节细胞在氧糖剥离条件下产生的能量紊乱、钙离子超载。Wang等[54]运用GC-MS法研究杜仲防治IS的作用,采用缺氧缺糖条件下的脑微血管内皮细胞造模,发现杜仲具有促进苯丙氨酸代谢,抑制线粒体活性氧产生的作用。上述IS体外细胞模型的构建采用的是物理方法,即将细胞置于缺糖或缺血培养基与缺氧环境下培养,对设备要求较高,需将连二亚硫酸钠(Na2S2O4)、氯化钴(CoCl2)等化学性缺氧试剂用于IS模型的构建。王宇翔[55]在PC12细胞的无糖培养基中加入Na2S2O4建立氧糖剥离模型,采用HPLC法探究染料木黄酮对所构建细胞模型的保护作用,通过测定细胞神经递质类氨基酸随时间含量变化情况,发现染料木黄酮可逆转缺氧缺糖所引起的谷氨酸、天冬氨酸等兴奋性氨基酸水平变化,发挥神经保护作用。
-
抑郁症是一种复杂的精神障碍疾病,以持续的心境低落为主要临床特征。谷氨酸循环和糖皮质激素浓度异常与抑郁症的发生发展密切相关,目前体外实验主要使用皮质酮、谷氨酸诱导细胞产生神经损伤构建抑郁症细胞模型。Zhang等[56]采用超高效液相色谱结合四极杆飞行时间质谱法(UPLC-QTOF-MS)探究皮质酮对PC12细胞的细胞毒性机制,鉴定出15种潜在生物标志物,涉及甘油磷脂代谢、鞘脂代谢、脂肪酸氧化、甘油脂代谢和甾醇脂物在内的5种代谢途径,为后续实验研究提供了有力支撑。何小燕等[57]运用1H-NMR法探究谷氨酸和皮质酮诱导下PC12细胞的代谢差异,结果显示两种刺激方式产生的代谢物不同,但影响的代谢通路却无显著差别,提示将差异代谢物与其代谢通路结合分析的重要性。中医药具有多层次、多靶点的整体调控作用,在防治抑郁症方面具有独特优势。但由于相关中医学证候模型的缺乏,在一定程度上制约了中医药防治抑郁症的进一步发展。付爽等[58]使用含10%肝郁脾虚证的血清诱导肝癌HepG2细胞构建抑郁症证候模型,对所建立的抑郁症肝郁脾虚证细胞模型与肝郁脾虚证血清进行代谢组学分析,发现了溶血磷脂酰胆碱、卵磷脂、甘油磷酰胆碱等19个相同的代谢差异物,涉及9条代谢通路,该证候细胞模型的建立为中医药辩证治疗的科学性和有效性提供了依据。
-
细胞代谢组学通过“细胞模型-生物标志物-疾病机制/作用功效”的对应关系,对细胞代谢产物进行分析,从细胞水平认识疾病,为中枢神经系统疾病的防治打开一扇新的大门。但是仍面临着一些挑战:①理想的细胞模型应该与相应疾病有高度的相似性、可重复性和可操作性,但是疾病的发生发展往往与多个细胞相关,因此需要在确保研究结果可靠的基础上选择合适的细胞造模方法。②细胞代谢物丰富但是含量少,虽然使用液氮或低温有机溶剂对细胞进行萃取可以最大程度上减少代谢物的损失,但是不同细胞模型所采用的前处理方法不尽相同,目前尚未有标准化前处理流程可以适用所有细胞代谢物的提取分析。③细胞代谢组学的分析对象是相对分子质量小于1 000的代谢物,需要不断更新、优化高通量和高分辨率的分析仪器,提高代谢物的检测灵敏度,以获取更多的细胞代谢物数据。④细胞代谢组学隶属于体外研究的范畴,与生物体复杂的代谢变化存在着一定的差异,为提高研究结果的准确性和可靠性,未来细胞代谢组学的研究方向需整合多组学和多学科的信息,以期更加全面的了解CNS病理机制,获取疾病相关生物标志物信息,进一步评价药物的药效,从而为CNS疾病的新药研发提供参考依据[59-60]。相信随着更多细胞模型的构建以及分析技术的不断发展,细胞代谢组学在CNS疾病研究中将会有更广阔的应用前景。
Application of cellular metabolomics in central nervous system diseases
doi: 10.12206/j.issn.2097-2024.202203006
- Received Date: 2022-03-01
- Rev Recd Date: 2022-07-25
- Available Online: 2023-07-14
- Publish Date: 2023-02-25
-
Key words:
- cellular metabolomics /
- central nervous system diseases /
- cell model /
- biomarkers
Abstract: Cell metabolomics is an important branch of metabolomics, which could dynamically monitor cell response and metabolic changes after drugs acting on cells, and look for potential biomarkers. Cell metabolomics has been widely used in illustration of disease mechanism, evaluation of drug efficacy and development of new drug through elucidating the pathophysiological mechanism of the disease and the effect of drug treatment intervention. The researches process of cellular metabolomics and its application in central nervous system diseases were reviewed in order to provide theoretical basis for in-depth study of the pathogenesis and prevention and treatment of central nervous system diseases.
| Citation: | HE Xiaoli, SHI Yiwei, WANG Hui, DAI Jianying, HONG Zhanying. Application of cellular metabolomics in central nervous system diseases[J]. Journal of Pharmaceutical Practice and Service, 2023, 41(2): 63-69. doi: 10.12206/j.issn.2097-2024.202203006 |







 DownLoad:
DownLoad: