-
西罗莫司(sirolimus,SRL),又称雷帕霉素,是第三代免疫抑制剂,在临床上常用于抑制肝、肾等器官移植后的免疫排斥反应。SRL属于生物药剂学分类Ⅱ类药物,在水中的溶解度极低,而渗透性良好[1-4]。SRL药理活性高,但因水溶性差,且易被肠壁和肝中的CYP3A4同工酶广泛代谢,致使其口服生物利用度较低。这是临床应用SRL的重要缺陷之一。目前,已上市的SRL制剂主要是纳米结晶片,生物利用度约为17%[5-7]。
通过适当的制剂技术提高SRL在胃肠道中的溶解度,可提高其口服生物利用度。在前期研究中,课题组分别独立进行了含SRL的自微乳(self-microemulsifying drug delivery system,SMEDDS)、固体分散体(solid dispersion,SD)和纳米结构脂质载体(nanostructured lipid carriers,NLC)的构建,均显著改善了SRL的体外溶出。本实验在前期研究的基础上,新增环糊精衍生物对SRL的增溶研究,结合体外溶出度和体内生物利用度,综合分析和评价各增溶制剂的优势和缺陷,从而为解决口服难溶性药物的研究提供参考。
HTML
-
Agilent 1200型高效液相色谱仪(美国Agilent公司);Starter 2C型pH计(上海奥豪斯仪器公司);RCZ-6BZ型药物溶出仪(上海黄海药检仪器公司);真空冷冻干燥箱(北京博医康试验仪器公司);NS1001L2K高压匀质机(意大利NiroSoavi公司);UV-2800AH型紫外可见分光光度仪(上海优尼科仪器有限公司);液相色谱-质谱联用仪(美国AB-SCIEX有限公司)。
-
SRL对照品(含量99.9%)、SRL原料药(含量99.6%),购自福建科瑞药业有限公司;子囊霉素对照品(上海齐奥化工科技有限公司),Rapamune®(美国惠氏制药)。聚乙二醇6000(PEG 6000)、聚乙烯吡咯烷酮(PVP K30)均购自国药集团化学试剂有限公司;聚氧乙烯-聚氧丙烯共聚物(Poloxamer 188)、聚氧乙烯35蓖麻油(Cremophor EL)、聚氧乙烯氢化蓖麻油(Cremophor RH40)均购自德国BASF公司;油酸聚乙二醇甘油酯(Labrafil M1944CS)、二乙二醇单乙基醚(Transcutol P)、辛酸癸酸聚乙二醇甘油酯(Labrasol)、棕榈酸硬脂酸甘油酯(Precirol ATO5)、月桂酸聚乙二醇甘油酯 (Gelucire 44/14)均购自法国GATTEFOSSE公司;HP-β-CD、DM-β-CD、SBE-β-CD(山东滨州智源生物科技有限公司)。
1.1. 仪器
1.2. 试剂
-
采用高效液相色谱仪(HPLC)测定样品中的SRL含量[8]。色谱柱为Eclipse XDB-C18(150 mm×4.6 mm,5 μm),流动相为乙腈-甲醇-水(45∶34∶21),流速为1 ml/min,检测波长为278 nm,柱温为50 ℃,进样量为20 μl。配制浓度为2、4、8、12、16、20 μg/ml的SRL对照品溶液,得标准曲线为Y=54.712X+1.221,r=0.999 9,表明在2~20 μg/ml浓度范围内线性关系良好。另外,精密度、回收率符合要求。
-
参考前期研究[9],称取1 g SRL原料药,加入19 g的助乳化剂Transcutol HP,超声至全部溶解后,加入22 g油相Labrafil M1944CS及39 g乳化剂Cremophor EL,涡旋混匀,得到淡黄色澄清溶液,即SRL-SMEDDS。
-
参考前期研究[10-11],取Gelucire44/14和Crodamol GTCC在75 ℃水浴中完全熔融后,加入SRL原料药搅拌均匀成澄明油相,再将同温度吐温−80的水溶液迅速倒入油相,以300 r/min搅拌30 min制备初乳,再经高压匀质机90 MPa乳匀5次,即得SRL-NLC分散液,其中SRL为0.21%,Gelucire44/14:Crodamol GTCC(1∶2.1),脂质总量为10%,吐温−80为7.33%。随后,将SRL-NLC(42.6%)加入微晶纤维素和聚乙烯吡咯烷酮(50%,4∶1)中,研磨混合并放置过夜以充分吸附,加入甘露醇(冻干保护剂,3%),经冷冻干燥过夜后,所得固体粉末中加入低取代羟丙基纤维素(崩解剂,4%)和二氧化硅(助流剂,0.4%)即得固化纳米脂质体。
-
采用溶剂-熔融法制备SRL-SD。称取载体材料,于80 ℃水浴加热熔融,滴入SRL乙醇溶液,充分混匀,待乙醇挥发完全后,迅速将其倾倒于冰浴条件下的不锈钢板上成薄膜,固化,再于−18 ℃放置4 h后,将固体分散体从不锈钢板上刮下,置真空干燥器中干燥,待脆化后研细,过80目筛,即得SRL-SD。以载体种类、药物-载体比例为考察因素,以0.4% SDS中的溶出度为指标,对SRL-SD进行单因素分析。
-
称取适量β-环糊精衍生物溶于去离子水中,缓慢滴加SRL乙醇溶液,在一定温度下磁力搅拌至澄清透明,减压挥发4 h,使乙醇挥发完全,再置于4 ℃冰箱冷藏12 h,降低SRL的溶解度,从而使游离的SRL发生结晶。经0.22 μm微孔滤膜过滤除去结晶,滤液冷冻干燥24 h,所得固体研磨细化,过80目筛,即得SRL-IC。
称取一定量的SRL-IC置10 ml容量瓶中,加入50%甲醇水溶液,超声至全部溶解后,定容至刻度,并采用HPLC测定SRL含量,根据公式:包封率(%)=[(SRL投入量-SRL测定量)/ SRL投入量]×100%,进行计算。以环糊精衍生物的种类、浓度、温度、乙醇体积和投药量为考察因素,以包封率为指标,对SRL-IC进行单因素分析。
-
参考《中国药典》2015年版四部通则0931项下溶出度与释放度测定法,考察SRL原料药、市售片(Rapamune®)、SRL-SMEDDS、SRL-NLC、SRL-IC及SRL-SD的溶出曲线。除市售片外,其余样品均装入硬胶囊中,每个胶囊含1 mg SRL。采用桨法,搅拌速度为100 r/min,溶出介质体积为250 ml,分别以0.4% SDS、水、pH 1.2盐酸溶液、pH 4.5醋酸盐缓冲液、pH 6.8磷酸盐缓冲液、pH 7.4磷酸盐缓冲液为溶出介质。将两颗胶囊或药片置于沉降篮中,投入溶出介质,在10、30、45、60、90、120 min,吸取2 ml介质,并补充等温等体积的介质,采用HPLC测定样品中的药物含量,绘制溶出曲线。
-
选用比格犬为实验动物,采用6周期6交叉实验设计,进行SRL原料药、市售片(Rapamune®)、SRL-SMEDDS、SRL-NLC、SRL-IC及SRL-SD的药代动力学试验。给药剂量为1 mg SRL,实验动物试验开始前12 h禁食不禁水,给药4 h后自由饮水,2次给药间隔2周以上的清洗期。于给药前,0.25、0.5、0.75、1、1.5、2、3、4、6、8、10、12、24、36、48及72 h分别经前肢小静脉采血2 ml,置于含肝素和EDTA的抗凝管中,−20 ℃保存备用。血样处理与测定方法参照课题组前期研究[12]。
2.1. SRL含量测定方法
2.2. SRL增溶方法
2.2.1. SRL-SMEDDS的制备
2.2.2. SRL-NLC的制备
2.2.3. SRL-SD的制备
2.2.4. SRL-IC的制备
2.3. 体外溶出试验
2.4. 体内药代动力学试验
-
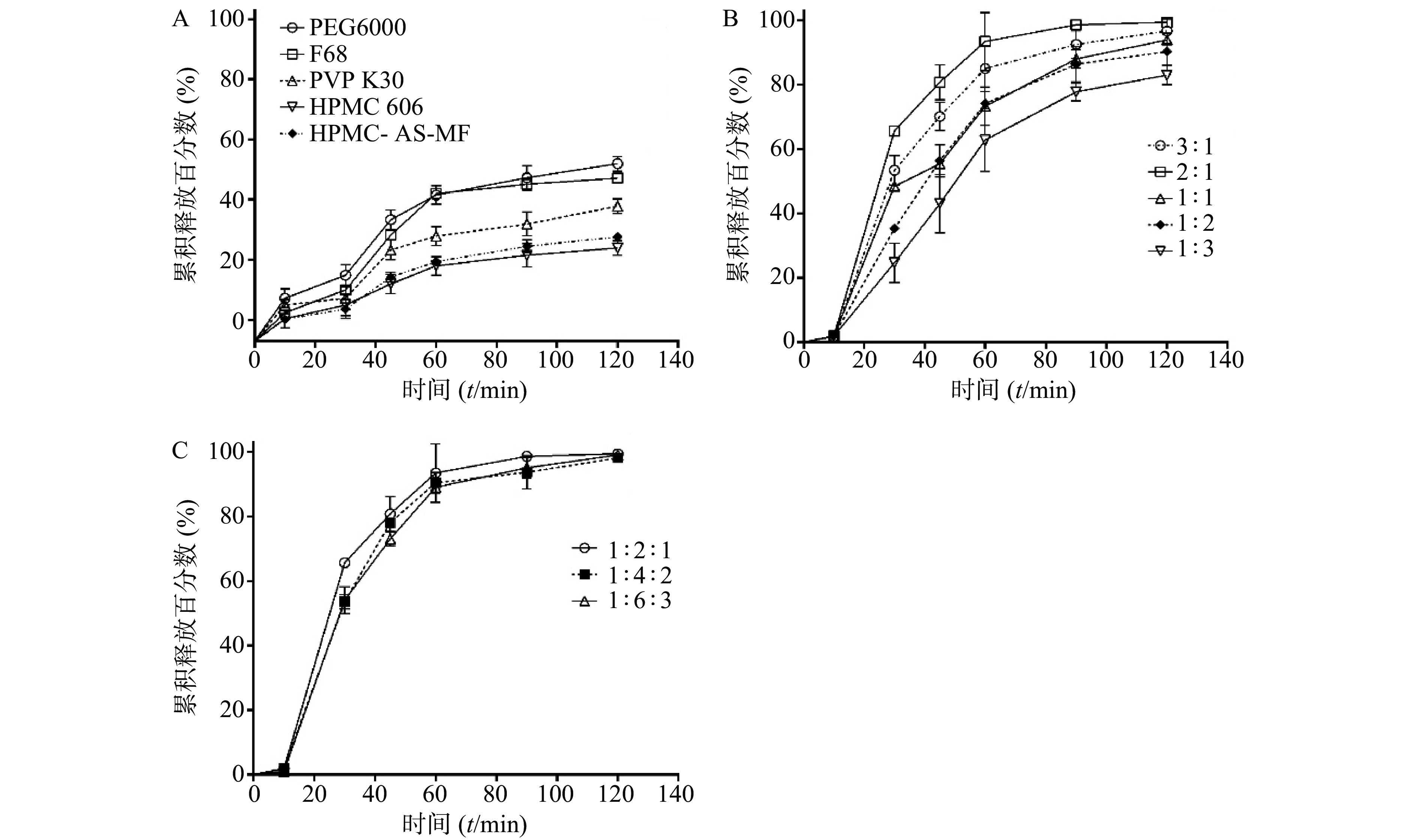
如图1A所示,不同载体材料制备的SRL-SD的溶出曲线显示了明显的差异,溶出速率为PEG6000>F68>PVP K30>HPMC606>HPMC-AS-MF。同时,各载体材料的溶出度均不理想(≤50%),因此进一步考察采用二元载体制备SRL-SD。
选择PEG6000联合F68制备二元载体固体分散体[13],两者比例为3∶1、2∶1、1∶1、1∶2、1∶3。随PEG6000/F68比例的增大,则SRL溶出度呈增大趋势,在PEG6000/F68为2∶1时的溶出度达到最大(图1B)。
-
在PEG6000/F68=2∶1的基础上,进一步考察药物-载体比例对SRL-SD溶出的影响。药物-PEG6000/F68载体比例为1∶2∶1、1∶4∶2及1∶6∶3所制的SRL-SD的溶出曲线相似,没有明显差别,2 h的溶出度都接近100%(图1C)。因此优选载药量最大,即药物- PEG6000/F68载体比例为1∶2∶1。
-
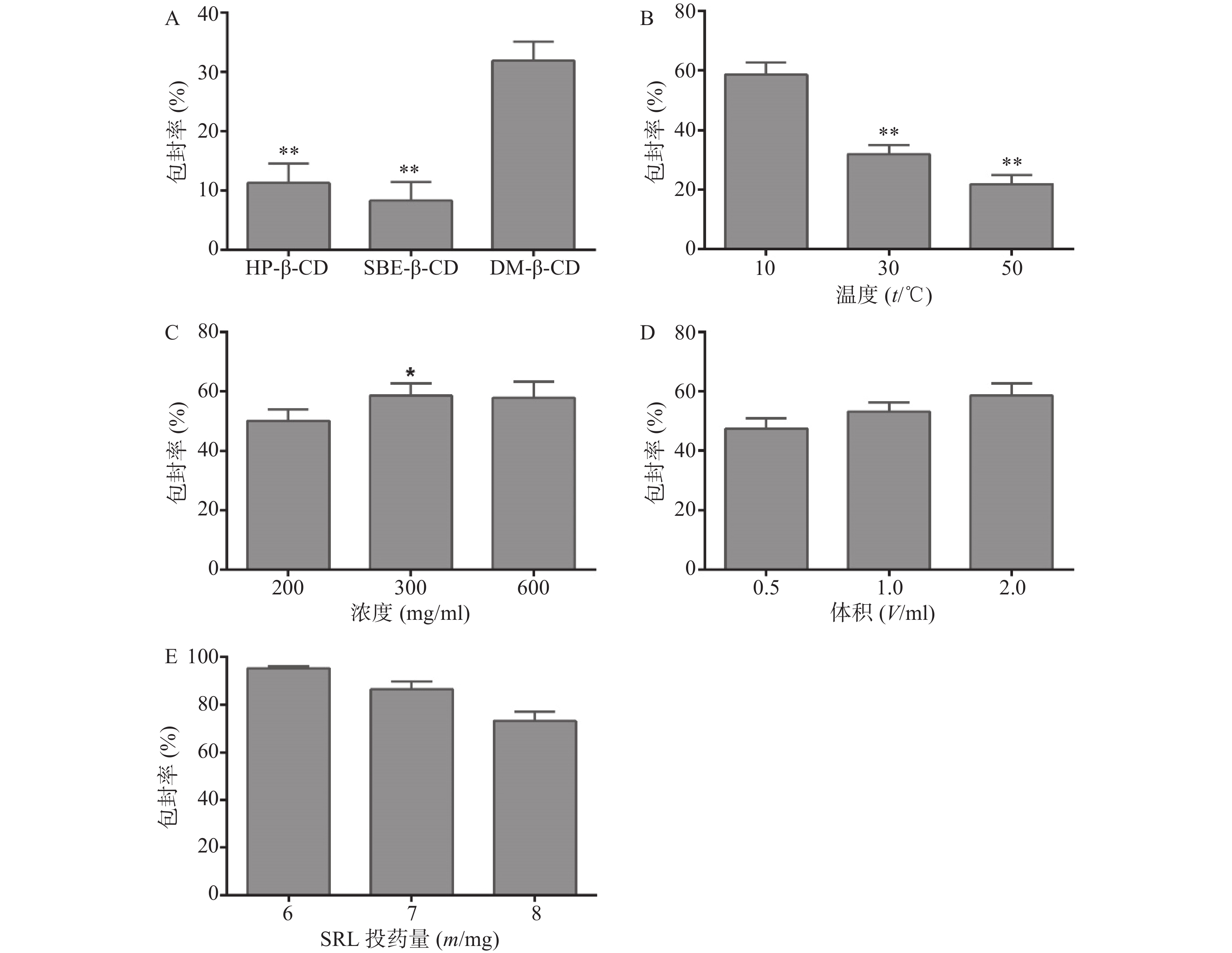
在其他条件相同的情况下,HP-β-CD、SBE-β-CD和DM-β-CD对SRL的包封率分别为(11.21±3.35)%、(8.24±3.11)%和(31.86±3.26)%,见图2A。因此,优选DM-β-CD制备SRL-IC。
-
采用DM-β-CD制备SRL-IC,考察不同温度对包封率的影响。结果显示(图2B),温度越低,包封率越高,10 ℃条件下制备的SRL-IC的包封率显著高于30 ℃和50 ℃(P<0.01),为(58.61±4.16)%。因此,优选10 ℃制备SRL-IC。
-
DM-β-CD的浓度由200 mg/ml增大至300 mg/ml,SRL的包封率由(52.12±4.17)%增大至(58.61±4.11)%(P<0.05,图2C)。进一步增大DM-β-CD的浓度至600 mg/ml,包封率没有明显变化(P>0.05)。因此,优选DM-β-CD的浓度为300 mg/ml制备SRL-IC。
-
乙醇体积由0.5 ml增大至2 ml,包封率呈增大趋势(图2D)。因此,优选乙醇体积为0.5 ml制备SRL-IC。
-
SRL的投药量6 mg增大至8 mg,包封率显著降低,6 mg SRL的包封率为(95.21±1.10)%,见图2E。因此,优选SRL的投药量为6 mg。
-
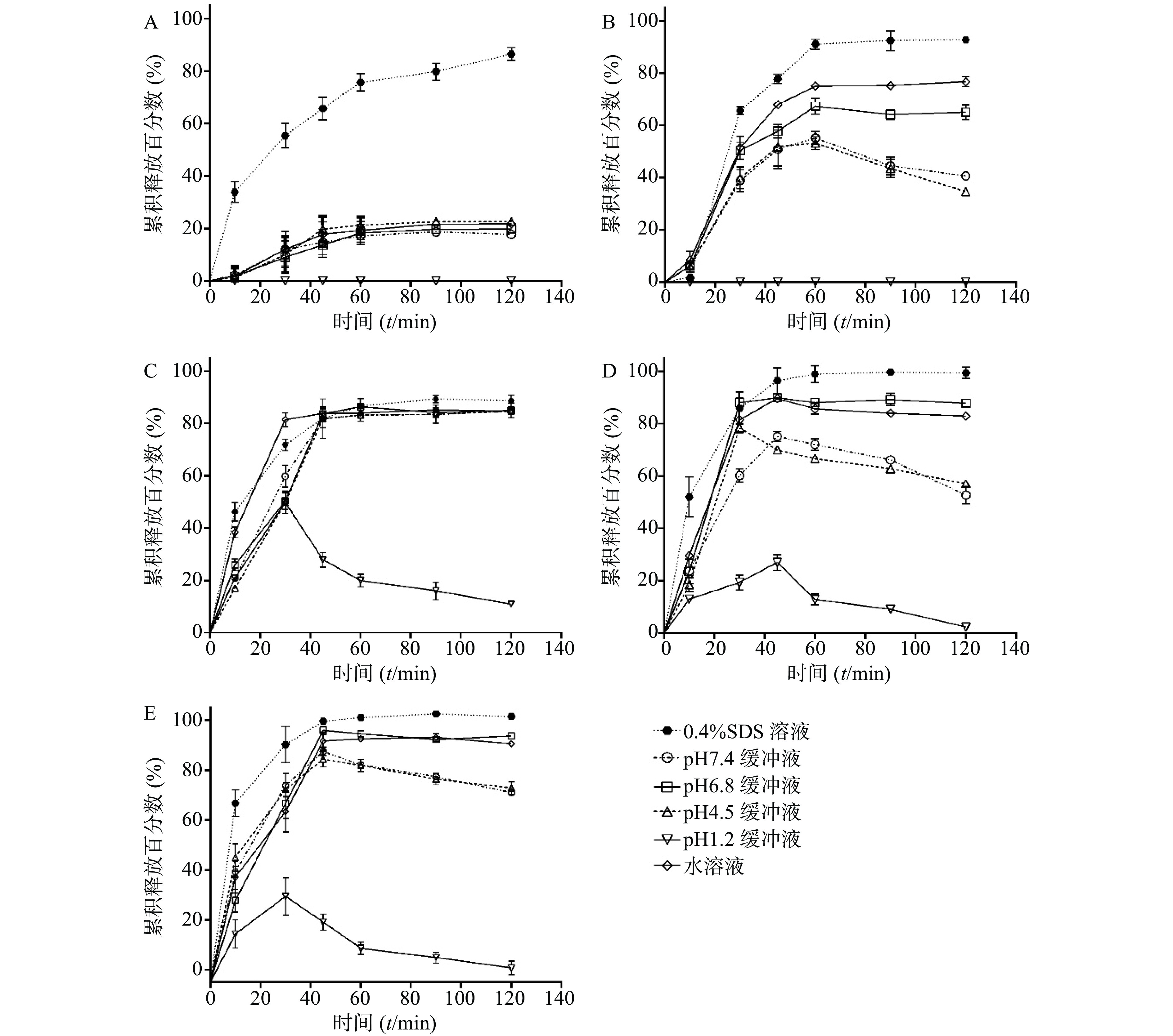
考察SRL-SD、SRL-IC、SRL-SMEDDS及SRL-NLC在不同介质中的溶出曲线。如图3所示,在0.4% SDS中,各制剂在2 h的溶出度均超过80%,尤其是SMEDDS和NLC的溶出度接近100%。
在pH 6.8和水中,SRL-SD的溶出速率减小,2 h的溶出度分别为(65.00±4.90)%和(76.70±1.95)%。在pH 4.5和pH 7.4的介质中,SRL-SD的溶出在1 h达到最大值,分别为(53.20±4.34)%和(55.20±4.34)%,随后溶出度逐渐降低。在pH 1.2的介质中,未检测到SRL。
在水、pH 4.5、pH 6.8和pH 7.4中,SRL-IC在40 min内的溶出速率有所减小,但2 h的累积溶出没有明显变化,均在80%以上。在pH 1.2的介质中,SRL-IC的溶出度在30 min达到最大值,为(49.84±7.21)%,随后溶出度逐渐降低。
SRL-SMEDDS和SRL-NLC显示了与SRL-SD相似的溶出趋势,即在水和pH 6.8中的溶出度低于0.4% SDS,但大于80%。在pH 4.5和pH 7.4的介质中,溶出达到峰值(约80%)后逐渐降低。
-
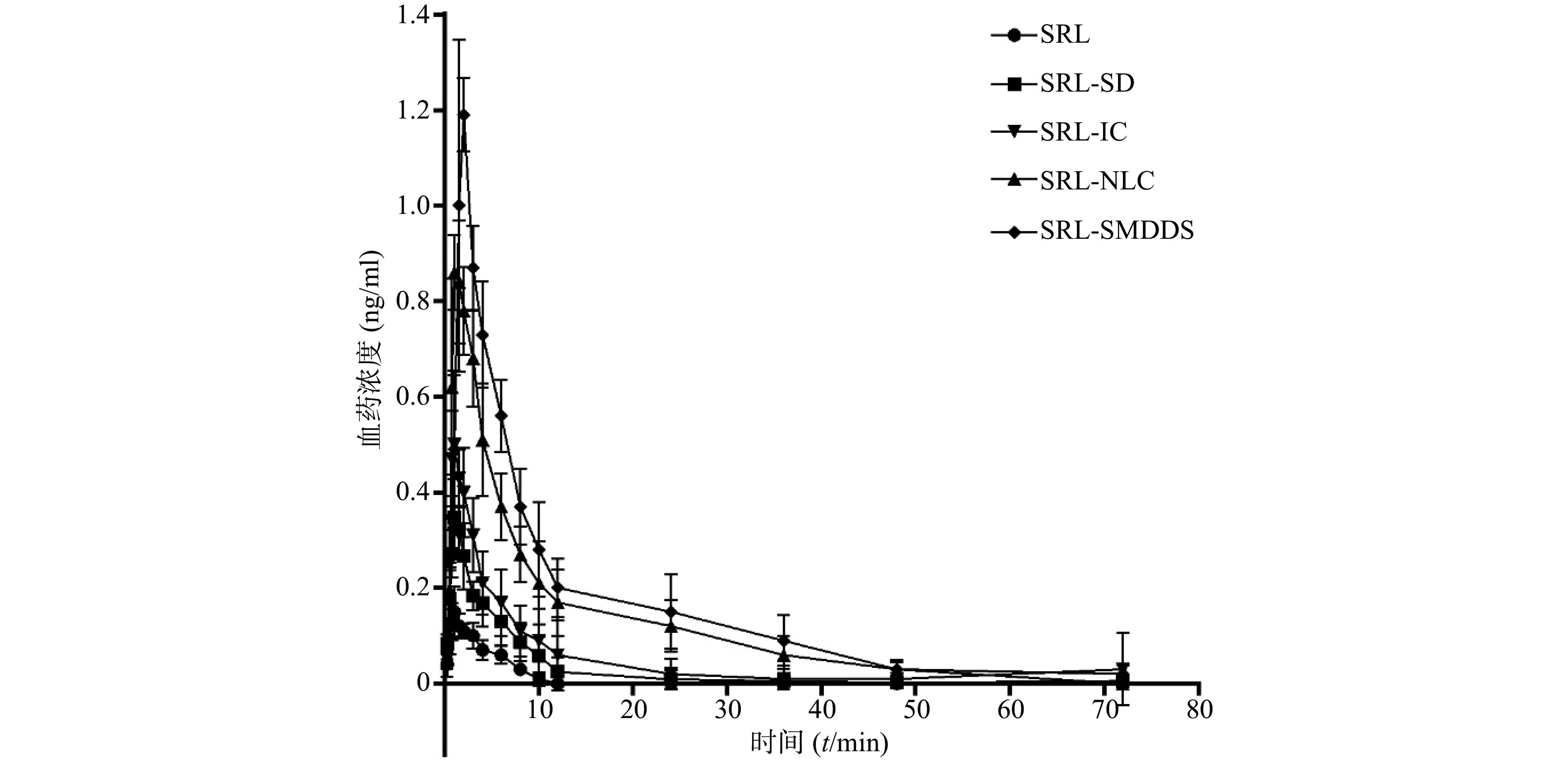
SRL血药浓度-时间曲线见图4,经DAS 3.2.6软件处理后,具体参数见表 1。
参数 SRL SRL-SD SRL-IC SRL- NLC SRL-SMEDDS Rapamune® AUC0→72(µg·h/ml) 0.70±0.13 2.06±0.79 3.66±2.64 8.60±2.03 10.76±1.57 11.02±2.73 AUC0→t(µg·h/ml) 0.73±0.15 2.07±0.81 3.78±2.84 8.67±1.95 11.15±2.11 11.75±3.13 t1/2 (t/h) 16.53±1.50 14.50±2.15 20.64±5.45 8.97±6.87 12.97±5.67 14.54±5.67 tmax(t/h) 1.04±0.25 1.25±0.28 1.04±0.25 1.13±0.31 1.50±0.38 1.83±0.26 cmax (ng/ml) 0.16±0.05 0.36±0.05 0.53±0.13 0.90±0.09 1.23±0.07 1.28±0.13 以原料药为参比制剂,SRL-SD、SRL-IC、SRL-SMEDDS、SRL-NLC、Rapamune®的相对生物利用度分别为332.8%、522.9%、1 228.6%、1 537.1%、1 574.3%,表明各增溶方法都显著提高了SRL的生物利用度。
以市售纳米晶片Rapamune®为参比制剂,SRL-SD、SRL-IC、SRL-NLC、SRL-SMEDDS的相对生物利用度分别为18.7%、33.2%、78.0%、97.6%,可见在各增溶方法中,SMEDDS对SRL体内吸收的作用最显著,与市售制剂相当。
3.1. SRL-SD的制备
3.1.1. 载体种类
3.1.2. 药物-载体比例
3.2. SRL-IC的制备
3.2.1. β-环糊精衍生物种类
3.2.2. 温度
3.2.3. 环糊精衍生物浓度
3.2.4. 乙醇体积
3.2.5. 投药量
3.3. 体外溶出度
3.4. 比格犬体内药动学试验
-
本研究同时制备和比较了SRL的4种增溶制剂,均显示了良好的体外溶出度。同时,各制剂都提高了SRL的生物利用度,但体内吸收程度有较明显的差异。
首先,SRL本身的性质是影响体内吸收的重要因素。在理化性质方面,SRL在电解质溶液中可发生开环水解,特别是在强酸和碱性条件下,降解速率显著增加[14]。在生理因素方面,SRL是肠道内CYP3A4酶和P糖蛋白的底物,对肠道吸收有较大影响[15]。
其次,制剂本身的特点对体内吸收有重要影响。SMEDDS和NLC均可形成纳米级的脂质微粒,在胃肠道消化后可形成乳糜胶束[16-17]均减轻了胃肠液的pH对SRL的降解作用,因此SMEDDS和NLC对脂质微粒中的SRL有一定的保护作用。相比之下,SD中的SRL快速释放后,载体材料失去了对药物的隔离保护作用,导致SRL在极短的时间内发生降解。另外,环糊精的空腔可以容纳药物分子[18],不仅提高了SRL的溶解度,而且降低了H+和OH-对SRL的作用概率,减缓了SRL的降解。本研究的体外溶出试验也证实了不同增溶制剂中SRL稳定性的差异。
同时,SMEDDS的辅料Labrafil M1944 CS和Cremophor EL[9, 19-21]和NLC中的脂质及其代谢产物能够抑制CYP3A4酶的代谢和P糖蛋白外排,消化后形成的乳糜胶束还可通过淋巴途径吸收[22],从而提高了生物利用度[10-11]。
另外,由于SRL分子量较大,分子结构可能仅有部分插入环糊精的空腔中。因此,尽管环糊精提高了SRL的溶出度,但包合物的稳定性较差,进入胃肠道后,药物可被胃肠液中的成分替换[23],导致SRL加速降解或发生重结晶,进而生物利用度下降。







 DownLoad:
DownLoad: