-
结直肠癌,又称大肠癌,好发于大肠黏膜,是常见消化系统恶性肿瘤,早期症状不明显不易发现,晚期则表现贫血、体重减轻等。由于现代生活节奏加快及各种不良饮食、作息、环境和遗传等因素的影响,使得我国的发病率逐年增加[1]。据《中国肿瘤登记年报》内容显示:2015年我国肿瘤登记地区结直肠癌发病率和病死率分别为17.1/10万和7.9/10万,发病率男女性别比和城乡比分别为1.5和1.4,病死率分别为1.6和1.4。与年报数据接近的《中国死因监测数据集》显示,2017年我国结直肠癌病死率为6.9/10万[2]。虽然,目前已有各种化疗、外科手术、中医治疗等诊治方法,但是仍然存在早期诊查率低、预后差等问题,患者术后5年的生存率仍没有得到较大的改善,故针对结直肠癌的诊疗研究亦成为现在的热点[3]。
卡培他滨(Cap)是结直肠癌辅助化疗及一线治疗药物,通常与多西他赛、奥沙利铂、爱必妥等联合应用,常见结直肠癌化疗方案是联合奥沙利铂。Cap是前体药,体内转化成氟尿嘧啶,并在肿瘤组织中代谢为5-氟尿嘧啶,从而抑制核苷酸的合成,发挥抗肿瘤作用。肿瘤组织中5-氟尿嘧啶的浓度是血液中的100倍以上,靶向性好,不良反应轻微,且大部分患者都可耐受[4]。手足综合征(HFS)是服用Cap后出现的常见药物不良反应,多为1~2级,少数达到3级。临床主要表现为进展性症状变化,早期症状主要发生在手掌和足底,出现不同程度的瘙痒,指尖、手掌和足底充血,之后会持续发展为手掌和足底的暗红和肿胀,随后产生水泡,最终发展为脱皮,极大影响患者用药依从性及生存质量,成为后期持续治疗效果不佳的严重因素之一[5]。Cap导致HFS的发病机制尚不清楚,但病理特征表现为不同程度的细胞点片坏死、轻度的海绵状水肿、血管扩张、表皮与真皮交界处有炎性渗出。有研究表明[6-8],显微镜镜下观察到血管舒张和水肿,类似于炎症反应,而炎症发生时,活跃的炎症因子主要有白介素类中的IL-1β、IL-6、IL-10、IL-12、IL-17、IL-23,肿瘤坏死因子(TNF-α)、干扰素(IFN-γ)、C-反应蛋白(CPR)以及趋化性细胞因子(CCL-5)。因此,本研究对出现HFS的结直肠癌患者血浆中的主要炎症因子进行考察,推测其中涉及到的炎症因子,建立炎症因子含量变化与HFS发生的相关性,为Cap发生HFS的防治提供一定参考。
-
选取2018年9月至2019年2月海军军医大学附属长征医院普外科接受卡培他滨化疗方案的35例结直肠癌患者作为本次研究对象。纳入标准:①年龄≥18周岁;②经临床确诊为结直肠癌的患者;③接受了以Cap为基础的化疗;④预计生存期≥3个月,无主要器官的功能障碍;⑤有化疗指证,包括心肝肾等脏器功能正常,骨髓造血功能正常;⑥治疗前病情评估应有完整的体格检查和实验室检查,包括全血细胞计数、生化功能检查等;⑦生活质量:首次出现先写中文名(KPS)评分≥60分;⑧自愿签署知情同意书。排除标准:①孕、哺乳期患者;②5年内患过其他恶性肿瘤者;③经临床确定,对FU类药物过敏或严重代谢不良的患者;④有严重感染的患者;⑤经临床确定,患有其他会影响实验结果的恶性疾病;⑥不符合纳入标准,未按规定用药,无法判断疗效,或资料不全等影响疗效或安全性判断者。HFS事件评价标准:根据美国卫生及公共服务部2009年出版的常见不良反应事件评价标准4.0(CTCAE v4.0)分级,1级:轻微皮肤改变或皮肤炎(红斑、水肿、角化过度、不痛);2级:皮肤改变(剥落、水泡、出血、肿胀、角化过度),疼痛,影响工具性日常生活活动;3级:重度皮肤改变(剥落、水泡、出血、水肿、角化过度),疼痛,个人自理能力受限。自患者服用Cap后进行临床观察,直到患者出现HFS后停止,收集患者出现HFS时的血液样本,采用EDTA-3K抗凝管采集血样,储存于−80 ℃冰箱冻存。本研究经过海军军医大学附属长征医院伦理委员会批准,35例患者基本信息及HFS信息见表1。
表 1 患者一般资料及HFS分级情况
例数 性别 年龄(岁) 肿瘤部位 HFS分级 男 女 均值 中位数 直肠 结肠 未发生 1级 2级 3级 35 23 12 55.9 61 14 21 12 16 3 4 (65.7%) (34.3%) — — (29.9%) (70.1%) (34.2%) (45.7%) (8.5%) (11.4%) -
Human IL-6 ELISA kit试剂盒、 Human IL-1β ELISA kit试剂盒、Human IL-10 ELISA kit试剂盒、Human IL-12p70 ELISA kit试剂盒、Human IL-17/IL-17A ELISA kit试剂盒、Human IL-23 ELISA kit试剂盒、Human IFN-γ ELISA kit试剂盒、Human CRP ELISA kit试剂盒、Human TNF-α ELISA kit试剂盒以及Human RANTES ELISA kit试剂盒均购自国润医疗供应链服务(上海)有限公司。酶标仪(Biotek,型号:800TSI)购自美国伯腾仪器(北京代表处)有限公司。37 ℃孵箱(型号:FYL-YS-151L,温度:0 ℃~100 ℃)由北京福意电器有限公司提供。
-
参照试剂盒说明书测定35例结直肠癌患者服用卡培他滨后血浆中各炎症因子包括白介素类中的IL-1β、IL-6、IL-10、IL-12、IL-17、IL-23, TNF-α,IFN-γ,CPR和CCL-5含量水平。将血液样本4 000 r/min离心15 min, 收集血浆样本,按照试剂盒说明书测定各炎症因子的含量。
-
使用 Microsoft Excel 软件进行统计结果分析,采用Graphpad Prism 8.3.0作图。
-
IL-23标准曲线的浓度为2 000、1 000、500、250、125、62.5、31.25 pg/ml;IFN-γ、IL-17、TNF-α、IL-12标准曲线的浓度为1 000、500、250、125、62.5、31.25、15.6 pg/ml;CCL-5、IL-1β的标准曲线的浓度为500、250、125、62.5、31.25、15.6、7.8 pg/ml;IL-6、CRP的标准曲线的标准品浓度为200、150、50、25、12.5、6.25、3.125 pg/ml;IL-10的标准曲线的浓度为50、25、12.5、6.25、3.125、1.56、0.78 pg/ml。各炎症因子标准曲线呈现良好线性关系,可为样本的检测提供阳性对照,见表2。
表 2 炎症因子线性范围及标准曲线
炎症因子 线性范围pg/ml 标准曲线 r IL-23 0~2 000 Y=594.66X−23.268 0.994 8 IFN-γ 0~1 000 Y=384.31X+7.9709 0.999 3 IL-17 Y=1379X−12.849 0.997 9 TNF-α Y=352.02X+5.7229 0.999 7 IL-12 Y=448.55X+8.5172 0.994 6 CCL-5 0~500 Y=168.42X−12.215 0.997 2 IL-1β Y=206.82X−4.5823 0.999 6 IL-6 0~200 Y=67.278X−6.6851 0.996 7 CRP Y=90.523X -3.228 0.990 5 IL-10 0~50 Y=27.541X−0.403 0.997 5 -
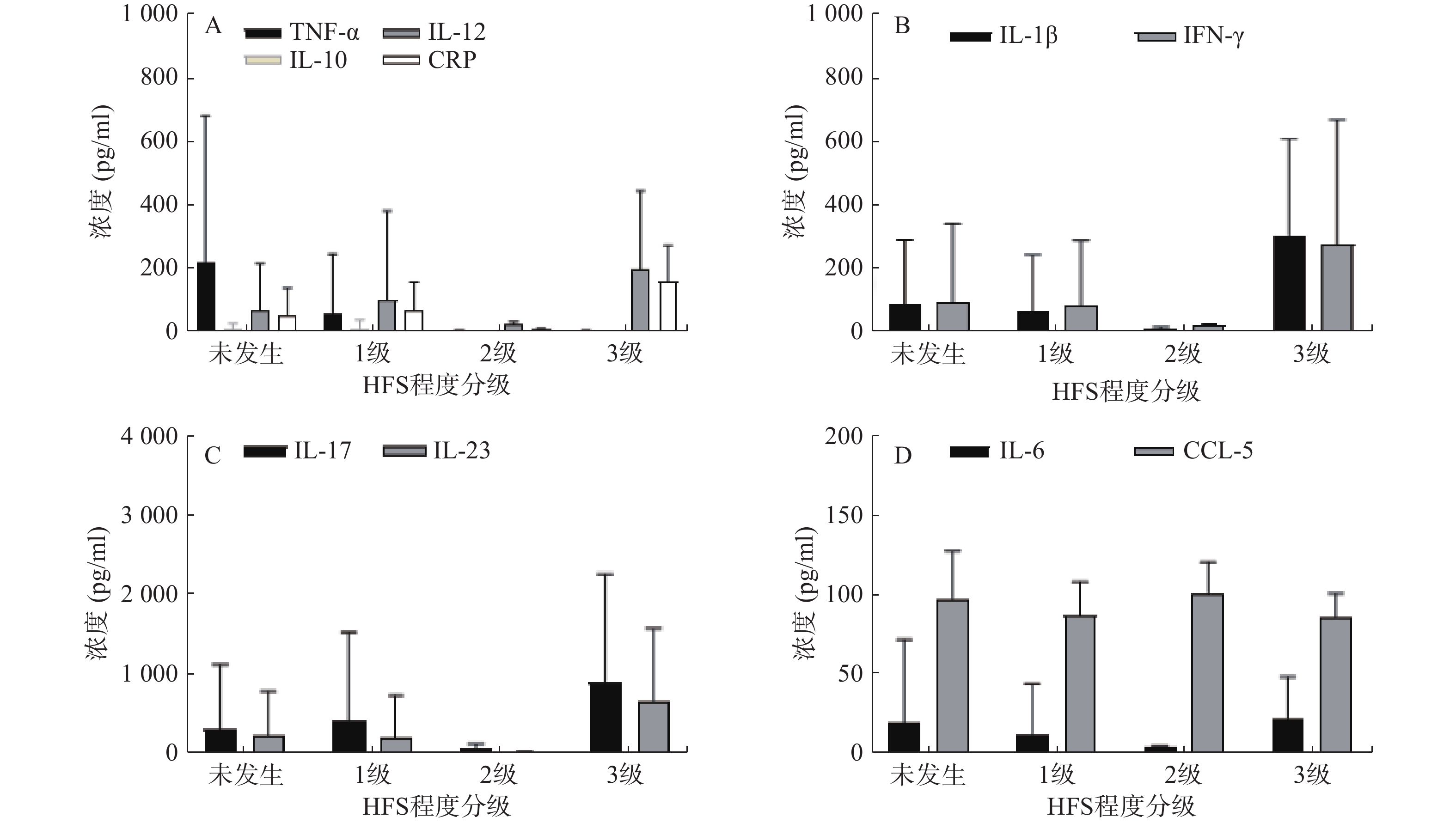
35例服用Cap后未发生与发生各级HFS的两类结直肠癌患者,其血浆中各炎症因子含量水平见表3。结果显示,不同级别的HFS各炎症因子含量存在一定的差异性,提示Cap诱发HFS会导致血浆中不同炎症因子相互作用发生级联反应。其中,TNF-α 的含量水平在发生HPS呈整体下调状态,且明显低于未发生者的含量水平。其余炎症因子含量水平变化则无规律可循(图1)。
表 3 不同分级HFS患者中的各炎症因子含量测定结果(pg/ml,
$\bar x $ ±s)炎症因子 未发生 1级 2级 3级 浓度平均值 标准差 浓度平均值 标准差 浓度平均值 标准差 浓度平均值 标准差 IL-1β 83.64 203.67 60.98 180.17 8.96 5.03 303.17 303.50 IL-6 19.57 52.35 12.29 31.84 4.68 0.34 22.60 25.96 IL-10 8.280 17.19 10.53 26.67 0.17 0.11 0.10 0.03 IL-12 67.80 148.40 99.40 282.18 22.87 9.42 195.11 250.89 IL-17 316.96 807.82 413.09 1118.61 76.79 46.93 905.52 1361.64 IL-23 218.06 566.46 190.55 542.33 12.11 5.95 663.67 911.80 IFN-γ 89.87 248.25 77.82 209.39 17.36 5.01 274.05 392.16 CRP 52.99 85.03 65.77 91.81 6.91 3.49 157.98 114.55 TNF-α 221.01 461.14 58.98 186.95 2.67 2.51 2.64 1.54 CCL-5 98.11 30.01 87.84 20.60 101.78 19.20 85.93 15.49 注:未发生HFS 12例;1级HFS 16例;2级HFS 3例;3级HFS 4例 -
随着结直肠癌发病率的上升,Cap的临床应用越来越广泛,其带来的不良反应也急剧增加,其中,HFS严重影响患者生活质量以及用药依从性,更甚者则终止治疗,故必须对Cap诱发HFS进行药学监护[9-10]。临床常见的监护策略主要有减少给药剂量、中断药物治疗以及使用其他药物(如塞来昔布胶囊200 mg,po,bid +尿素乳膏涂抹患处,tid)干预HFS严重程度等方法。肿瘤坏死因子(TNF-α)是机体重要的炎性细胞因子之一,具有多生物学效应及生理病理性功能,且TNF-α在HFS发生的不同程度时血浆中含量有显著变化,推测TNF-α 血浆中含量水平越低发生HFS的程度越严重,并在进行药学监护时具有一定参考价值。
本实验以HFS为主要研究方向,对患者血浆中炎症因子进行检测,结果发现Cap诱发不同程度HFS血浆中的炎症因子含量有一定的差异性。由于临床化疗治疗医生很少让患者的HFS进展到2、3级再进行处理,所以患者例数较少,数据不能支撑比较。但对未发生与1级HFS比较发现,1级HFS患者血浆中IL-1β、IL-6、IL-23、IFN-γ、TNF-α、CCL-5的含量明显低于未发生HFS患者;而IL-10、IL-12、IL-17、CRP血浆中含量明显高于未发生HFS患者,且TNF-α浓度水平变化较为明显。目前,Cap诱发HFS的发生机制尚不清楚,可能是多途径炎症因子相互作用的结果。因此,关注定血浆炎症因子含量水平变化,在一定程度上可以反应Cap诱导HFS的严重程度,通过测定血浆中炎症因子含量的变化,有利于防治Cap诱发HFS情况,并对临床有重要的指导意义。
Analysis of association between severity of capecitabine-induced hand-foot syndrome and inflammatory factors
-
摘要:
目的 检测并分析服用卡培他滨后出现手足综合征的结直肠癌患者血浆中主要炎症因子(IL-1β、IL-6、IL-10、IL-12、IL-17、IL-23、TNF-α、IFN-γ、CPR和CCL-5)与手足综合征之间的相关性。 方法 收集35例服用卡培他滨的结直肠癌患者血浆样本,根据手足综合征分级诊断标准对其轻重程度进行划分,用ELISA试剂盒检测血浆中各炎症因子的含量。 结果 所有炎症因子的标准曲线呈线性(r>0.9900),并测定了不同结直肠癌患者血浆中炎症因子的含量,其中,TNF-α 含量水平变化较为明显,且具有参考价值。 结论 不同的炎症因子在不同分级的手足综合征患者血浆中浓度存在一定差异,且TNF-α 炎症因子含量水平与其发生手足综合症的轻重程度密切相关。 Abstract:Objective To investigate the correlation between plasma inflammatory factors [IL-1β, IL-6, IL-10, IL-12, IL-17, IL-23, TNF-α, TGF-β, IFN-γ, C-reactive protein (CPR) CCL-5] and hand-foot syndrome in colorectal cancer patients after taking capecitabine. Methods 35 colorectal cancer patients treated with capecitabine were collected and the degree of severity was divided according to the hand-foot syndrome grading diagnostic criteria. The concentrations of inflammatory factors in plasma were determined by ELISA kits. Results The standard curve of all inflammatory cytokines were linear (r>0.9900), and plasma concentrations of inflammatory cytokines in patients with colorectal cancer were determined. The concentration of TNF-α changed obviously, which had reference value. Conclusion The concentrations of different inflammatory factors were different and the concentration of TNF-α was closely correlated with the severity of hand-foot syndrome. -
Key words:
- colorectal cancer /
- capecitabine /
- hand-foot syndrome /
- inflammatory factors
-
近年来随着医药行业的快速发展,治疗药物监测愈益成为临床药物治疗工作的一项重要内容,也是个体化用药指导的重要手段之一。治疗药物监测[1](therapeutic drug monitoring,TDM),其目的是通过测定血液中或其他体液中药物的浓度并利用药动学的原理相应调整药物剂量,使给药方案个体化,以提高药物的疗效,避免或减少毒副反应;同时也为药物过量中毒的诊断和处理提供实验室依据,简而言之就是对药物浓度的评估[2]。药物治疗窗(therapeutic drug window)指药物产生最小治疗效应与机体能耐受的最小中毒反应间的血药浓度范围,是TDM的临床用药依据。目前临床上开展TDM的药物涉及多种类、多监测方法,但TDM的治疗窗和血样却没有很好的分析、归纳及总结。前期课题组研究表明[3-4],高原环境对药物代谢酶、转运体的活性及蛋白表达均有一定的影响,导致高原环境下药动学参数发生变化,而药动学参数是指导临床合理用药的重要理论依据,直接关系到给药的剂量及给药时间,那么高原低氧环境对临床常用监测药物的代谢是否会产生影响?本文将对临床上常用的治疗监测药物种类、治疗窗、以及检测血样进行归纳和总结,分析高原环境下对临床常用监测药物代谢的影响,一方面有利于指导临床合理用药、毒性反应评估、引导个体化用药;另一方面,为本课题组进一步研究高原环境下开展TDM提供理论指导。
1. TDM药物种类及治疗窗
随着TDM研究的不断深入,王菁等人[5]归纳了临床上遴选TDM遵循的八条原则。即行TDM的药物具有自身治疗指数低、治疗窗窄、毒性较大、非线性药动学特征和个体差异较大,以及联合用药时会发生相互作用,导致血药浓度变化等特点。目前,需TDM的药物种类主要包括免疫抑制剂,如他克莫司(FK506)、环孢霉素(CsA);抗菌药,如万古霉素、替考拉宁;平喘药,如氨茶碱;抗癫痫药,如丙戊酸(VPA)、卡马西平(CBZ)、苯巴比妥;心血管系统药物,如地高辛;抗心律失常药物,如普鲁卡因胺、利多卡因、奎尼丁;抗肿瘤药,如甲氨蝶呤(MTX);抗抑郁药,如丙咪嗪、阿米替林、碳酸锂,等等。由于这些药物个体差异大,容易在同等剂量出现毒副反应或达不到相应的疗效,因此,临床上需要做TDM。使监测药物的血药浓度控制在治疗窗内,是保证患者安全、有效的用药关键。以下将临床上常用TDM药物的治疗窗及血样进行分类(表1)。
表 1 临床常用治疗监测药物的治疗窗类别 代表药物 血样 治疗窗 免疫抑制剂 他克莫司 全血 5−10 ng/ml 环孢霉素 全血 150−400 ng/ml 抗菌药 万古霉素 血清 10−15 μg/ml 替考拉宁 血浆 ρmin≥10 μg/ml(非复杂感染) 20−60 μg/ml(深部复杂感染) 平喘药 氨茶碱 血清 10−20 mg/ml 血浆 55−110 μmol/L 抗癫痫药 丙戊酸 血清 50−100 μg/ml 苯巴比妥 血清 10−40 μg/ml 卡马西平 血清 4−12 μg/ml 心血管系统药物 地高辛 血清 0.8−2.0 ng/ml 并非所有的药物都需要做血药浓度监测,一些有显著效果指标的药物,如降压药(如硝苯地平、厄贝沙坦、卡托普利等),其临床的治疗效果可以直接通过测定患者血压数值来反映降压的程度,进而根据血压数值调整用药的剂量;新型广谱唑类药物艾沙康唑(isavuconazole)目前也不需要TDM[6]。对于上述治疗窗宽、安全范围广的药物进行血药浓度监测和药代动力学参数的研究并没有多少实际意义。
进行监测的药物血样[7]主要有全血、血浆及血清等,监测血样的确定主要根据药物与血浆蛋白、红细胞结合率,以及游离状态来决定,以便更好的评价血药浓度,指导临床个体用药剂量。当药物主要与血液中红细胞结合时,监测的血样一般选择全血;药物与血浆蛋白结合率高时,主要以游离态来发挥作用时,选择血清为监测的血样结果会更加准确。例如,免疫抑制剂他克莫司、环孢霉素,监测的血样为全血,因为多数他克莫司与血液中红细胞结合,少数与血浆中的脂蛋白结合[8-9];环孢霉素也在血浆中与血浆蛋白和红细胞的结合率高[10]。由于他克莫司、环孢霉素与红细胞有较高的结合率,因此,必须以全血为血样,以保证监测的浓度结果更加可靠、准确、稳定,但在测定全血时干扰物质较多,全血处理也要有严格的要求[雅培公司所产的全自动免疫分析仪(型号:AR i1000SR)在测定血样前需加入全血沉淀试剂];而抗癫痫药丙戊酸的监测血样为血清,因为丙戊酸80%~90%处于与血浆蛋白结合状态,主要以游离态发挥作用[11],因此,丙戊酸以血清来评价血药浓度。研究表明[12],在血清中加入适量的高丰度蛋白质去除试剂乙腈,不仅能够有效沉淀蛋白,减少对血药浓度的影响,还能减弱加入内标提取液引起的乳化现象,使临床监测更加简便、经济。
2. 高原环境对TDM药物代谢的影响
高原环境具有低氧、低温、低气压、高辐射等基本特点,其中低氧是影响药物代谢的主要因素,低氧环境中药物蛋白结合率、器官血流量、代谢酶及转运体的表达及功能均会发生变化[13-14]。而这些变化会导致高原环境下药动学参数的改变,而药动学参数是指导临床合理用药的重要理论依据,直接关系到给药的剂量及间隔。TDM药物的代谢与血浆蛋白结合率、局部器官的血流量、代谢酶及转运体有直接的关系,也就是说高原环境的特殊性对TDM代谢也会有很大的影响,这些因素影响会使TDM药物的血药浓度发生改变,进而导致药动学参数发生变化,使高原人群的用药剂量存在风险。因此探究高原环境下TDM代谢发生的变化,对保证高原人群安全、合理、有效的用药具有重大意义。
2.1 高原环境对TDM血浆蛋白结合率的影响
药物与血浆蛋白结合率是影响药物在体内分布的重要因素,蛋白结合率高的药物在体内消除慢,作用维持时间长。药物进入循环后首先与血浆蛋白成为结合型药物,未被结合的药物称为游离型药物,两种类型的药物处于动态的平衡状态,仅游离型药物才能转运到作用部位产生药理效应。药物的血浆蛋白结合率会严重影响机体对药物的分布、排泄和代谢,从而影响药物作用强度和持续时间,加大了不良反应的发生率。高原环境对不同药物的血浆蛋白结合率具有不同的影响。如呋塞米、美托洛尔的蛋白结合率无显著性差异;而醋甲唑胺、普萘洛尔蛋白结合率显著性增高[15]。
临床上常用的监测药物种类多,不同药物在高原环境中血浆蛋白结合率不同,导致药物临床药效不同。课题组前期研究表明[16],监测药物氨茶碱平原组与高原组Wistar大鼠血浆蛋白结合率分别为37.05%和74.17%,急进高原组的血浆蛋白结合率比平原组显著高37.12%,具有较高的血浆蛋白结合率,导致药物的浓度增大,体内驻留时间缩短,若按照平原给药的标准很有可能发生不良反应。高原环境对TDM药物的血浆蛋白结合率的影响会使体内药物浓度发生改变,进而导致TDM药动学参数的变化。
2.2 高原环境对局部器官血流量的影响
人体脏器的血流量分布以肝最多,肾、脑、脾、心次之。肝是代谢药物的主要场所,进入高原机体对器官的血流增多,红细胞对血管的黏附也增强[17],血液黏稠度会增高,肾血流量减少,尿量减少,导致药物在体内的蓄积;脾是重要的免疫器官,其血流量显著增加到6.70±1.84(P<0.01)[18],使脾脏过负荷,导致脾肿大生理功能下降。
高原环境对器官血流量的影响,导致TDM药物的排泄发生变化。如地高辛在体内消除主要是以原型药经肾小球滤过或肾小管分泌排泄,尿中排出量为用量的50%~70%,仅约10%左右在肝代谢,另有7%左右处于肠肝循环。因此,高原环境中,地高辛经尿液的排出量减少,造成其在体内造成大量的蓄积,毒副作用也随之产生,即主要经肾排泄的TDM药物(VPA、苯巴比妥),在高原低氧的状态下应对可能产生的毒副反应进行监测,防止不良反应的发生。高原环境对器官血流量产生的影响,导致TDM药物的排泄发生改变。
2.3 高原环境对TDM代谢酶的影响
大多数药物代谢主要在肝脏中进行,肝细胞中的药物代谢酶会参与药物的代谢,肝脏微粒体酶系(细胞色素P450酶系)是促进药物转化的主要酶系统。CYP450酶系是一个基因超家族,临床中90%以上经肝脏代谢的药物是经过CYP450酶系亚酶代谢的,已有大量研究表明高原低氧导致酶的活性或表达降低,影响机体对大部分药物的生物转化率及清除率,减缓药物在体内的代谢,可能增加药物的毒副作用。
治疗监测药物的代谢也需要代谢酶的参与。如免疫抑制剂、环孢霉素主要通过CYP3A4和CYP3A5代谢[19-20];氨茶碱通过CYP1A2代谢[21];抗癫痫药丙戊酸的代谢过程受到尿苷二磷酸葡萄糖醛酸基转移酶(UGT酶)和细胞色素酶(CYP)影响[22];苯巴比妥在肝脏中主要被CYP2C9代谢,而CYP2C19和CYP2E1代谢较少[23]。课题组前期研究表明[3-4, 24-25],在高原低氧环境中,上述药物的代谢亚酶CYP3A4、CYP3A5、CYP1A2、CYP2C9及 UGT的mRNA与蛋白表达均下降,导致酶活性降低,这会使体内TDM药物的代谢减慢,半衰期延长,甚至使体内的药物浓度过大,造成药物及其代谢物在体内的大量蓄积,直接关系到患者用药的剂量及间隔。因此,高原环境对不同代谢酶的影响,TDM药物的代谢参数也将发生变化。
2.4 高原环境对TDM转运体的影响
药物转运体是转运药物透过细胞膜进入体内和产生药效的关键因素,其广泛分布在小肠绒毛上皮细胞、肾小管上皮细胞、肝细胞,其在药物代谢的各个环节中发挥着重要的作用。同一个转运体可在多个正常器官和组织中表达,而同一个组织和器官也可表达多个转运体。药物转运体分两类:ABC族转运蛋白和SLC族载体转运蛋白。P-糖蛋白(P-gp)是人体重要的ABC族外运蛋白,其存在于肝、肾、小肠、胎盘屏障和血脑屏障等组织器官中,其主要功能是将药物摄取或外排出细胞,从而影响体内代谢的各个过程。Rohwer等[26]总结了不同肿瘤细胞中P-gp 的变化,发现低氧诱导因子使转运体蛋白高表达,从而影响化疗药物的疗效。本课题组[4,27-28]研究了高原实地低氧环境中大鼠体内转运体的变化情况,高原低氧组小肠组织中P-gp mRNA与蛋白的相对表达水平分别下调50.80%和71.30%(P<0.05),高原低氧会导致小肠中P-gp的表达下调,使其底物的外排减少,增加其底物在肠道的吸收;肝脏中P-gp mRNA与蛋白的相对表达量分别上调了1.15倍和1.33倍;肾脏中分别上调了49.0%和1.83倍;高原组(海拔4 010 m)与平原组比,大鼠血脑屏障(BBB)组织中P-gp mRNA与蛋白相对表达量分别显著上调了2.18倍和2.58倍(P<0.05),随着表达量的升高,介导药物的外排增多,进入脑内的药量减少,疗效减弱。这些研究表明高原低氧条件下各组织中P-gp表达量均会发生明显的变化,影响药物在体内各组织的转运,代谢发生变化。
临床常用TDM:他克莫司、环孢霉素、卡马西平、丙戊酸都是P-gp的底物药物[29],也会受到高原环境的影响,导致药物在不同组织中发生不同的变化。如,抗癫痫药丙戊酸、苯巴比妥、卡马西平需要通过血脑屏障来发挥作用,高原环境会使这类药物进入脑内的药量减少、导致药效大大减弱。如果沿用平原的给药标准那么很有可能无法达到预期疗效。因此,必要研究TDM药物在高原低氧环境下的代谢变化,保证高原人群用药安全性和有效性。
2.5 高原环境中TDM药代参数的改变
高原环境对器官血流量及药物血浆蛋白结合率、代谢酶、转运体的活性及蛋白表达均有一定的影响,这些将导致高原环境下药动学参数发生变化,而药动学参数是临床用药剂量及间隔的重要依据。如大鼠灌胃给予氨茶碱剂量为3.6 mg/200 g,高原组氨茶碱体内消除减慢、Tmax显著减小(高原组0.44±0.191;平原组0.887±0.196),药物半衰期和滞留时间延长(高原组2.944±0.694;平原组2.365±0.448),Cmax增大到1.22倍,AUC增到1.35倍[20]。这些表明氨茶碱在高原低氧环境中生物利用度升高,那么人体中其用药剂量应适当的降低,防止体内浓度过高。若明确高原环境下TDM药物的药代参数,用药的剂量也会有所明确,以确保TDM药物的疗效。
3. 总结与展望
高原低氧环境中不仅使器官的血流量发生改变,而且严重影响TDM血浆蛋白结合率、代谢酶和药物转运体,使监测血药浓度值存在误差;药动学参数也会发生改变,而药代参数的改变会导致TDM剂量受到影响。目前,TDM的监测及代谢研究多在低海拔地区进行,而高原低氧环境下TDM的代谢鲜有文献报道。高原人群TDM的用药剂量及间隔是否可以沿用平原用药标准?因此,高原环境下TDM药物代谢是一个亟待解决的问题,更是临床有效性和安全性用药的重要前提。解决这问题将为高原临床治疗监测药物提供参考,在保证高原人群合理用药、减少毒副反应发生、提高生活质量等方面具有重大意义。
-
表 1 患者一般资料及HFS分级情况
例数 性别 年龄(岁) 肿瘤部位 HFS分级 男 女 均值 中位数 直肠 结肠 未发生 1级 2级 3级 35 23 12 55.9 61 14 21 12 16 3 4 (65.7%) (34.3%) — — (29.9%) (70.1%) (34.2%) (45.7%) (8.5%) (11.4%) 表 2 炎症因子线性范围及标准曲线
炎症因子 线性范围pg/ml 标准曲线 r IL-23 0~2 000 Y=594.66X−23.268 0.994 8 IFN-γ 0~1 000 Y=384.31X+7.9709 0.999 3 IL-17 Y=1379X−12.849 0.997 9 TNF-α Y=352.02X+5.7229 0.999 7 IL-12 Y=448.55X+8.5172 0.994 6 CCL-5 0~500 Y=168.42X−12.215 0.997 2 IL-1β Y=206.82X−4.5823 0.999 6 IL-6 0~200 Y=67.278X−6.6851 0.996 7 CRP Y=90.523X -3.228 0.990 5 IL-10 0~50 Y=27.541X−0.403 0.997 5 表 3 不同分级HFS患者中的各炎症因子含量测定结果(pg/ml,
$\bar x $ ±s)炎症因子 未发生 1级 2级 3级 浓度平均值 标准差 浓度平均值 标准差 浓度平均值 标准差 浓度平均值 标准差 IL-1β 83.64 203.67 60.98 180.17 8.96 5.03 303.17 303.50 IL-6 19.57 52.35 12.29 31.84 4.68 0.34 22.60 25.96 IL-10 8.280 17.19 10.53 26.67 0.17 0.11 0.10 0.03 IL-12 67.80 148.40 99.40 282.18 22.87 9.42 195.11 250.89 IL-17 316.96 807.82 413.09 1118.61 76.79 46.93 905.52 1361.64 IL-23 218.06 566.46 190.55 542.33 12.11 5.95 663.67 911.80 IFN-γ 89.87 248.25 77.82 209.39 17.36 5.01 274.05 392.16 CRP 52.99 85.03 65.77 91.81 6.91 3.49 157.98 114.55 TNF-α 221.01 461.14 58.98 186.95 2.67 2.51 2.64 1.54 CCL-5 98.11 30.01 87.84 20.60 101.78 19.20 85.93 15.49 注:未发生HFS 12例;1级HFS 16例;2级HFS 3例;3级HFS 4例 -
[1] 付卫, 黄坤蓉, 付敏, 等. CD73在结直肠癌组织中的表达及其与临床病理参数的关系[J]. 现代肿瘤医学, 2019, 27(10):1753-1757. doi: 10.3969/j.issn.1672-4992.2019.10.022 [2] 王红, 曹梦迪, 刘成成, 等. 中国人群结直肠癌疾病负担: 近年是否有变?[J]. 中华流行病学杂志, 2020, 41(10):1633-1642. doi: 10.3760/cma.j.cn112338-20200306-00273 [3] 陈诚, 熊亚立, 张敬, 等. 转移性结直肠癌一线化疗控制后卡培他滨维持的临床疗效评价[J]. 重庆医学, 2019, 48(8):1416-1419. doi: 10.3969/j.issn.1671-8348.2019.08.037 [4] 彭雪, 杨文博, 张寒, 等. 抗肿瘤药物诱导的手足综合征的诊疗进展[J]. 现代肿瘤医学, 2019, 27(8):1461-1464. doi: 10.3969/j.issn.1672-4992.2019.08.043 [5] NG C Y, CHEN C B, WU M Y, et al. Anticancer drugs induced severe adverse cutaneous drug reactions: an updated review on the risks associated with anticancer targeted therapy or immunotherapies[J]. J Immunol Res, 2018, 2018:5376476. [6] 张丽, 姚希. 血清肿瘤标志物及炎症因子在结直肠癌中的表达及意义[J]. 川北医学院学报, 2018, 33(5):766-769. doi: 10.3969/j.issn.1005-3697.2018.05.034 [7] 李鸿飞, 黄客增, 吴向华. 原发性胃肠道肿瘤合并轻型地中海贫血患者外周血白细胞介素6、肿瘤坏死因子α、干扰素γ及铁调素25水平及其临床意义[J]. 广西医学, 2018, 40(18):2156-2158. [8] 朱聪聪, 潘会君, 朱全刚. Th2相关炎症因子在湿疹发病中的作用机制[J]. 药学实践杂志, 2019, 37(1):9-13. [9] 漆婷婷, 胡志强, 马雪, 等. 1例卡培他滨致晚期结肠癌患者手足综合征循证干预与药学监护[J]. 中国药业, 2021, 30(17):119-123. doi: 10.3969/j.issn.1006-4931.2021.17.032 [10] CHEN J X, WANG Z. How to conduct integrated pharmaceutical care for patients with hand-foot syndrome associated with chemotherapeutic agents and targeted drugs[J]. J Oncol Pharm Pract, 2021, 27(4):919-929. doi: 10.1177/10781552211009291 -





 下载:
下载:
 下载:
下载:



