-
延胡索为罂粟科植物延胡索(Corydalis yanhusuo W.T.Wang)的干燥块茎,主产地为浙江、安徽、江苏等地,中医药应用历史悠久。其具有活血、行气、止痛之功效,用于胸胁,脘腹疼痛,胸痹心痛,经闭痛经,产后淤阻,跌扑肿痛[1]。现代科学研究发现延胡索主要含有生物碱、有机酸、甾体、挥发油、糖类、氨基酸等活性成分[2-3],具有镇痛、镇静催眠、抗溃疡、抗菌、抗炎、抗肿瘤、扩张冠状动脉,增加冠脉血流量,抑制血小板聚集,抗心律失常,改善心肌供氧,增加心输出量等药理作用[4]。含延胡索的中药处方及延胡索乙素制剂广泛应用于胃痛、伤痛、心绞痛、痛经等多种痛症。延胡索临床应用常以炮制品入药,目前常用的炮制方法主要有炒制、醋制、酒制等[5],其中又以醋制为主,醋制可以提高主要活性成分延胡索乙素的含量[6-7],《中国药典》(2015年版)收载醋制延胡索为醋炙和醋煮,醋蒸法始载于明代卢之颐的《本草乘雅半偈》,但药典及其他炮制规范等地方标准也无收载。本实验是在《安徽省中药饮片炮制规范》(2019年版)修订课题的基础上完成,实验数据及操作过程,符合中药标准制定规范要求。
-
超声波清洗仪(德国Elma公司);分析天平(METTLER TOLEDO公司);多功能振荡器(山东申仪电子科技有限公司);高温箱型电炉、数显鼓风干燥箱(上海博讯实业有限公司);普利菲尔超纯水机(上海富诗特仪器设备有限公司);赛默飞U3000系列液相色谱仪(赛默飞世尔科技有限公司)。
-
本实验共收集10批延胡索药材,经海军军医大学药学系中药鉴定学教研室张成中老师鉴定为罂粟科植物延胡索的干燥块茎。延胡索乙素(中国食品药品检定研究院,批号:110726-201516,纯度:99.8%);食用醋(江苏恒顺醋业股份有限公司);自制超纯水;色谱级甲醇、氨水(国药集团)。
-
取净制、切制后的延胡索,大小分档,加醋拌匀、润透,置蒸制容器内,用蒸汽加热蒸透、内无硬心,取出,干燥。炮制操作主药与辅料按延胡索与米醋的质量比为100∶20(kg/kg)制备醋蒸延胡索。
-
取10批醋蒸延胡索分别编号为CYHS-01-01~10,观察其大小、形状、色泽、质地、气、味等总结其共性特征。本品呈不规则的圆形厚片,表面黄褐色,有不规则网状皱纹。质硬而脆,断面黄褐色,角质样,有蜡样光泽。微具醋香气,味苦。
-
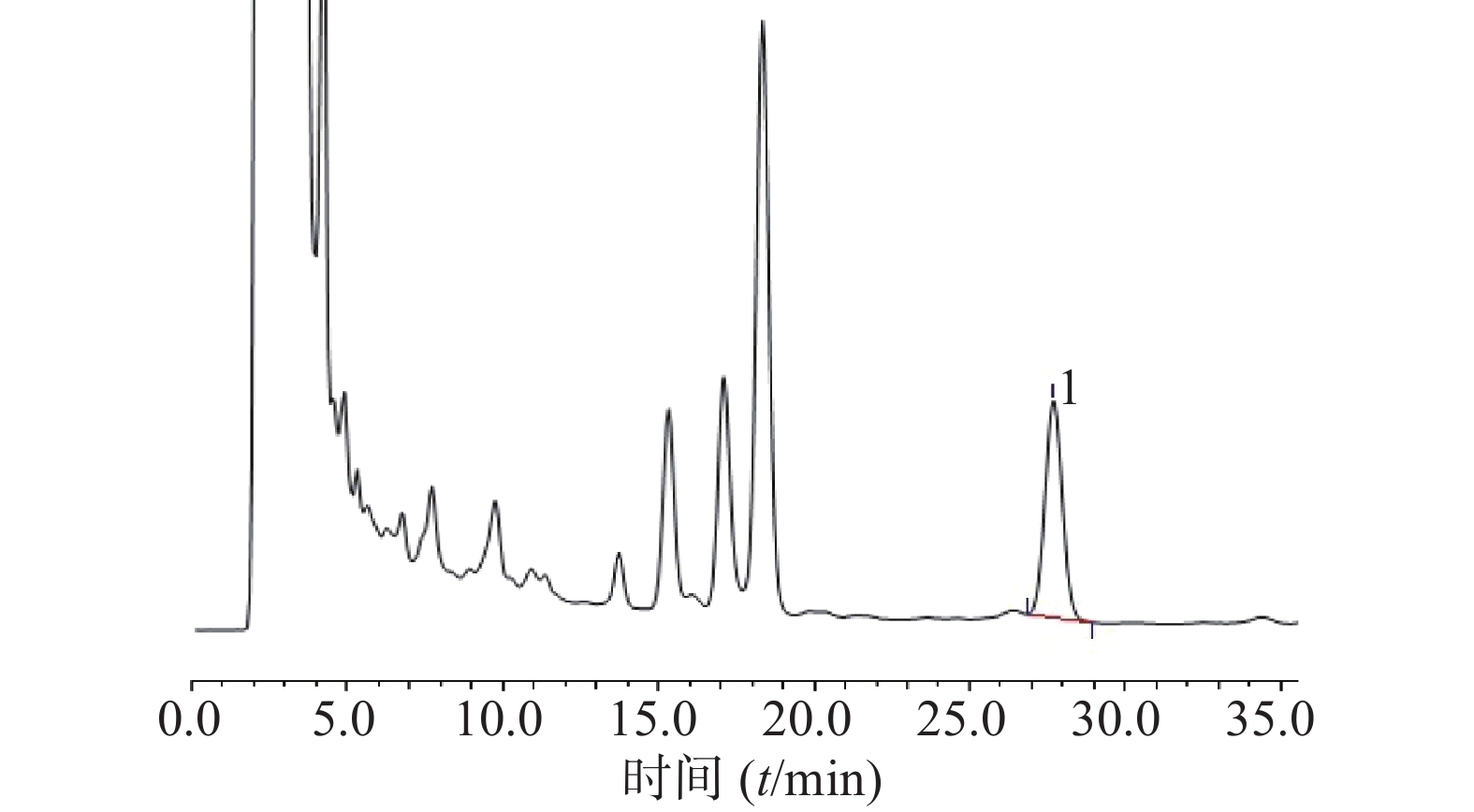
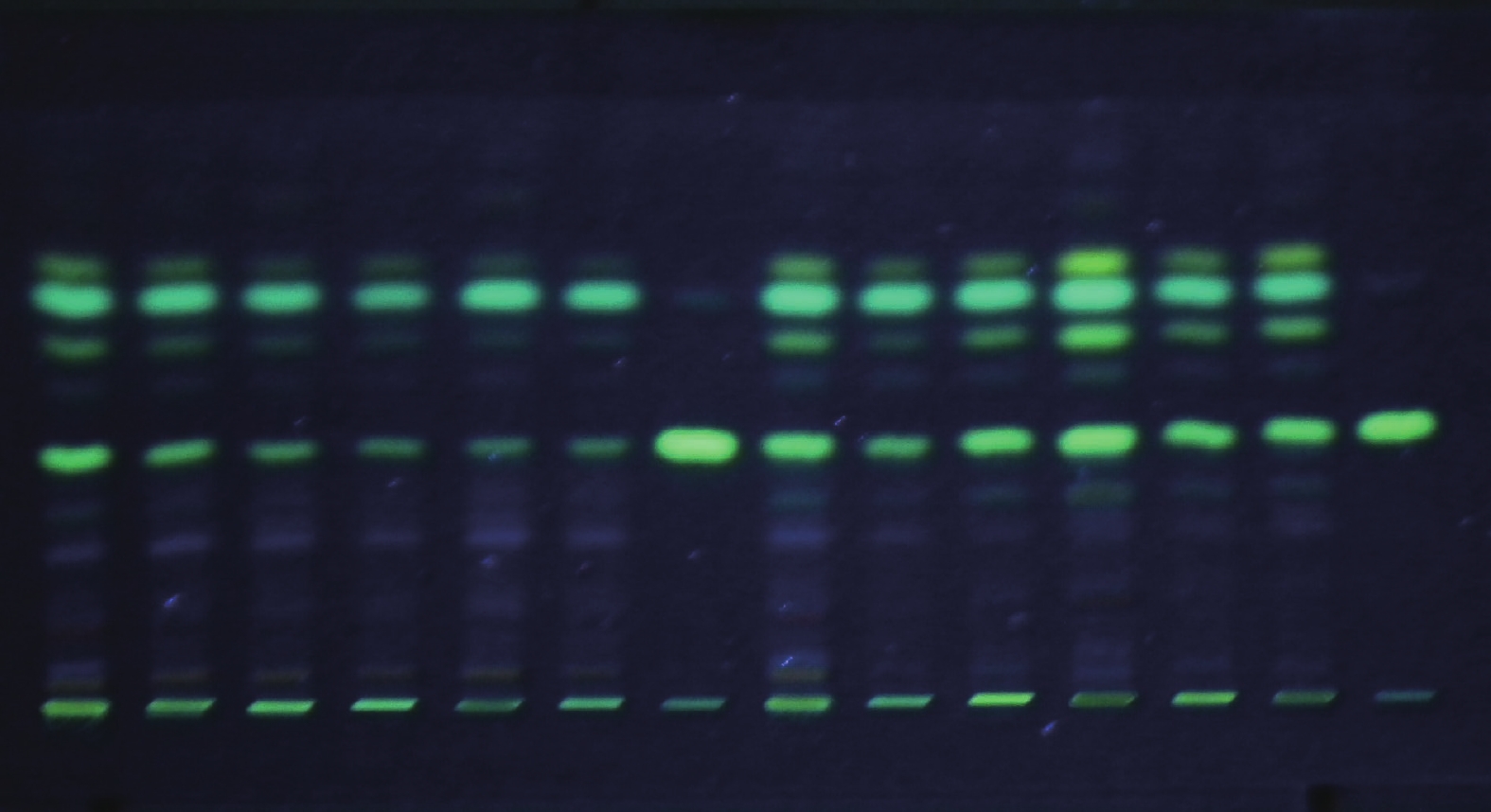
取醋蒸延胡索粉末1 g,参照《中国药典》(一部)2015年版延胡索薄层鉴别项下制备供试品溶液。另取延胡索对照药材l g,同法制成对照药材溶液。再取延胡索乙素对照品,加甲醇制成每l ml含0.5 mg 的溶液,制成对照品溶液。吸取上述3种溶液各2~3μl分别点于用1%氢氧化钠溶液制备的同一硅胶G 薄层板上,以甲苯-丙酮(9∶2)为展开剂,展开,取出,晾干,置碘缸中显色约3 min后取出,待板上吸附的碘挥尽后,置紫外光灯(365 nm)下检视。从色谱图上可以看出,供试品色谱中,在与对照药材及对照品色谱相应的位置上,显相同颜色的斑点和荧光斑点(图1)。
-
参照《中国药典》(四部)2015年版0832水分测定法第二法共测定10批次醋蒸延胡索饮片,水分最低值11.87%,最高值15.74%(表1),根据数据及公式μ=
$ \bar x $ + ts/$\sqrt{n} $ +MU[注:$\bar x $ 是样本的平均数;t是置信水平为99%的学生t检测值(单尾);s是样本的标准偏差;n是样本的批数;MU是不确定度评估(MU=0.1270×$\bar x $ )]计算,限度应为15.61%,参照《中国药典》(一部)2015年版延胡索项下,拟定水分限度不得超过15.0%。表 1 10批醋蒸延胡索水分测定结果(%)
序号 含水量A 含水量B 平均值 相对偏差 CYHS-01-01 13.62 13.45 13.54 0.63 CYHS-01-02 12.12 12.35 12.24 0.94 CYHS-01-03 12.39 12.62 12.51 0.92 CYHS-01-04 12.15 12.04 12.10 0.45 CYHS-01-05 12.50 12.15 12.33 1.42 CYHS-01-06 14.09 13.86 13.98 0.82 CYHS-01-07 11.97 11.76 11.87 0.88 CYHS-01-08 16.09 15.38 15.74 2.26 CYHS-01-09 12.40 12.06 12.23 1.39 CYHS-01-10 13.07 12.72 12.90 1.36 -
参照《中国药典》(四部)2015年版2302灰分测定法共测定10批次醋制延胡索饮片,总灰分最低值2.77%,最高值3.80%(表2),根据数据参照《中国药典》(一部)2015年版延胡索项下,根据公式μ=
$\bar x $ +ts/$\sqrt{n} $ +MU计算,限度应为:3.53%,参考《中国药典》(一部)2015年版延胡索项下总灰分限度,拟定不得超过4.0%。表 2 10批醋蒸延胡索总灰分测定结果(%)
序号 灰分A 灰分B 平均值 相对偏差 CYHS-01-01 3.15 3.04 3.10 1.78 CYHS-01-02 2.76 2.80 2.78 0.72 CYHS-01-03 2.89 2.93 2.91 0.69 CYHS-01-04 3.78 3.82 3.80 0.53 CYHS-01-05 2.88 2.95 2.92 1.20 CYHS-01-06 2.74 2.79 2.77 0.90 CYHS-01-07 3.24 3.20 3.22 0.62 CYHS-01-08 3.20 3.23 3.22 0.47 CYHS-01-09 3.25 3.29 3.27 0.61 CYHS-01-10 3.22 3.19 3.21 0.47 -
按照《中国药典》(四部)2015年版2201醇溶性浸出物测定法热浸法,用稀乙醇作溶剂,共测定10批次醋延胡索浸出物, 10批醋延胡索的浸出物在11.68%~18.20%之间(表3)。以统计学方法分析测试数据, 基于测试数据, 设定浸出物限度的公式如下:μ=
$\bar x $ −ts/$\sqrt{n}$ −MU(其中,$\bar x $ 是样本的平均数;t是置信水平为99%的学生t检测值(单尾)t0.01,9=2.821;s是样本的标准偏差;n是样本的批数;MU是不确定度评估MU=0.1413×$\bar x $ )。浸出物测定限度为:10.41%。拟定醇溶性浸出物测定法,参照《中国药典》2015年版(四部)2201测定,用稀乙醇作溶剂,浸出物不得少于11.0%。表 3 10批醋蒸延胡索浸出物测定结果(%)
序号 浸出物A 浸出物B 平均值 相对偏差 CYHS-01-01 13.69 13.48 13.59 0.77 CYHS-01-02 18.51 18.20 18.36 0.84 CYHS-01-03 14.06 14.15 14.11 0.32 CYHS-01-04 13.87 13.67 13.77 0.73 CYHS-01-05 14.39 14.05 14.22 1.20 CYHS-01-06 16.46 16.21 16.34 0.77 CYHS-01-07 14.66 14.50 14.58 0.55 CYHS-01-08 11.43 11.68 11.56 1.08 CYHS-01-09 13.68 13.79 13.74 0.40 CYHS-01-10 11.78 11.92 11.85 0.59 -
以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.1%磷酸溶液(三乙胺调pH至6.0)(55∶45)为流动相;检测波长为280 mn。理论板数按延胡索乙素峰计算应不低于3 000。
-
取P2O5减压干燥12 h后延胡索乙素对照品适量,精密称定,加甲醇制成每1 ml含46 μg的溶液,即得。
-
取醋蒸延胡索粉末(过三号筛)约0.5 g,精密称定,置平底烧瓶中,精密加入浓氨试液-甲醇(1∶20)混合溶液50 ml,称定重量,浸渍1 h后加热回流1 h,放冷,再称定重量,用浓氨试液-甲醇(1∶20)混合溶液补足减失的重量,摇匀,滤过。精密量取续滤液25 ml,蒸干,残渣加甲醇溶解,转移至5 ml量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得。
-
精密称取纯度为99.8%的延胡索乙素对照品适量置50 ml容量瓶中,加甲醇稀释至刻度,摇匀,得对照品溶液储备液,分别精密量取一定量的对照品储备液稀释成浓度分别为0.0101、0.0202、0.0404、0.0809、0.1213、0.1618 mg/ml的对照品溶液,注入液相色谱仪,测定含量,以浓度为纵坐标、峰面积为横坐标得标准曲线Y=931.64X+5.1405 (r=0.99995)。
-
取CYHS-01-010样品约0.5 g,精密称定,按供试品溶液制备方法处理,测定含量,平行取样测定6次,计算每次测定延胡索乙素的含量为0.097%,RSD为2.4%,符合要求。
-
精密称取延胡索乙素对照品溶液10 μl注入液相色谱仪,测定峰面积,平行测定8次,计算RSD为1.1%,符合要求。
-
取CYHS-01-010样品约0.5 g,精密称定,按供试品溶液制备方法处理,分别在0、2、4、6、8、12、24 h测定含量,计算每次测定延胡索乙素的RSD为1.8%,符合规定。
-
取CYHS-01-010样品约0.25 g,精密称定,精密加入含延胡素乙素0.202 2 mg的对照品溶液,按供试品溶液制备方法处理,得相关溶液,进液相色谱仪处理,计算含量及加样回收率,理论要求加样回收率85%~110%(CYHS-01-010含量为0.097%),RSD<5%(表4)。
表 4 加样回收率试验结果
编号 取样量(m/g) 加样量(m/mg) 回收率(%) RSD(%) 1 0.2418 0.2022 100.4 3.3 2 0.2417 0.2022 106.7 3 0.2427 0.2022 104.6 4 0.2462 0.2022 105.7 5 0.2453 0.2022 100.0 6 0.2440 0.2022 98.5 -
测定10批样品,根据数据计算,结果参照《中国药典》(一部)2015年版延胡索项下制订,拟定含量限度为:不得少于0.050%(10批检品含量差别不大,最大值与最小值差别接近1倍),见表5。根据公式μ=
$\bar x $ -ts/$\sqrt{n} $ -MU计算,限度应不得少于0.060%,醋蒸为醋制延胡索的一个炮制规格,结合《中国药典》(2015年版)一部延胡索项下的含量限度,设定按干燥品计算,延胡索乙素(C21H25NO4)不少于 0.050%。表 5 10批醋蒸延胡索含量测定结果
样品 含量(%) 平均值(%) CYHS-01-01 0.064 0.077 CYHS-01-02 0.068 CYHS-01-03 0.055 CYHS-01-04 0.058 CYHS-01-05 0.072 CYHS-01-06 0.092 CYHS-01-07 0.068 CYHS-01-08 0.100 CYHS-01-09 0.098 CYHS-01-10 0.098 -
辛、苦、温,归肝、脾经。具有活血,行气,止痛之功。性味与归经、功能与主治、用法与用量、储藏等项目参照现行版《中国药典》(一部)2015年版延胡索项下制定。
-
蒸法炮制药材早在2000多年前的医药文献《五十二病方》中就有“陈藿,蒸而取其汁”记载,汉代张仲景的《伤寒论》中有“乌梅...蒸之”,至明代缪希雍《炮炙大法》中已有近百味药材的蒸制记载。蒸法的广泛应用使其成为中药炮制最常用的炮制工艺之一。中药延胡索的炮制在宋代出现了醋炒、醋煮、盐炒等工艺,及至明清时又出现了醋纸煨、酒煮等工艺,延胡索醋蒸始载于明代《本草乘雅半偈》“醋润,蒸之,从巳至亥,俟冷取出,焙干,研细用”。现在主要炮制方法为醋炙、醋煮、酒炙、醋蒸等,醋蒸延胡索临床上虽广泛应用,但尚缺法定质量标准。
延胡索经过醋炙后,饮片中延胡索乙素的含量较醋炙前变化较小,但醋炙后延胡索煎剂中延胡索乙素的含量变化较大,溶出会显著增加,表明延胡索醋制后大量生物碱和醋酸反应生成生物碱盐,可提高煎出量,继而提高延胡索止痛作用[8-9]。江国荣等将延胡索生品分别经醋炙、醋煮、醋烘、酒炙后,测定生物碱的含量,发现延胡索经不同炮制后生物碱含量均有所升高,说明临床上可以根据治疗需要,对延胡索采用醋烘、醋炙、酒炙等炮制方法来提高有效成分的含量[10]。李春等采用正交试验法优化延胡索醋蒸炮制工艺,以延胡索粗粉为原料,加醋量30%,闷润2 h,蒸制2 h后,延胡索乙素的含量明显提高[11]。郑军献等对新采集的延胡索进行加工炮制,发现通过不同炮制方法制备延胡索药材,水煮法、蒸制法、烘干法在外形、性状基本一致,但延胡索乙素及成品折干率相差较大,蒸制延胡索乙素含量比水煮高出16.35%,成品折干率比煮法高出3.52%,说明蒸制法优于水煮法。蒸制时间10 min,延胡索乙素含量达到最高,当蒸制时间延长时,其含量反而降低[12]。龙全江等研究发现,经煮制加工的延胡索药材样品中3 种生物碱的含量总体低于蒸制加工所得的延胡索药材,其结果为延胡索药材蒸制炮制工艺的确定提供了物质基础和研究依据 [13]。
在现有文献的基础上,经实验研究分析,醋蒸延胡索具备现行版《中国药典》一部收载的醋炙延胡索质量要求,且延胡索乙素的含量明显高于药典中醋炙延胡索的要求,延胡索乙素可以作用于中枢神经系统,止痛、镇静,降低成瘾性、保护大脑的作用;也可以作用于心血管系统,抗心律失常、改善血流动力学、降低血脂[14]。延胡索乙素含量的增加符合醋制增强行气、止痛之功的炮制目的。因此制定醋蒸延胡索质量标准要求应为:性状为不规则的圆形厚片,表面黄褐色,有不规则网状皱纹。质硬而脆,断面黄褐色,角质样,有蜡样光泽,微具醋香气,味苦;水分不超过15%;总灰分不超过5%;以稀乙醇作溶剂,浸出物不少于11.0%;延胡索乙素(C21H25NO4)含量,按干燥品计算不少于 0. 050%。
Study on quality standard for vinegar-steamed Corydalis rhizoma
-
摘要:
目的 制定符合《中国药典》要求的醋蒸延胡索质量标准,用于延胡索醋蒸炮制品种的生产、监督、流通及使用等各环节的质量控制。 方法 参照《中国药典》(四部)2015年版通用检测方法分别对醋蒸延胡索的水分、总灰分、浸出物、主要有效成分含量进行测定。 结果 依据中药质量标准制定指导原则及相关检测方法,根据实验数据,醋蒸延胡索呈不规则的圆形厚片,表面深黄色或黄褐色,有不规则细皱纹。质较硬,断面黄色或黄褐色,角质样,有蜡样光泽,微具醋香气,味苦。其水分含量不超过15.0%,总灰分不得超过4.0%,醇溶性浸出物不少于11.0%,按干燥品计算,含延胡索乙素(C21H25NO4)不少于0.050%。 结论 实验所建立的醋蒸延胡索质量标准符合国家有关中药饮片质量标准制定要求,能够以标准的形式对醋蒸延胡索的质量进行控制。 Abstract:Objective To set up the quality standards for vinegar-steamed Corydalis rhizome, which can be used for the quality control of production, supervision, circulation and application of the steam processed Corydalis rhizoma with vinegar. Methods The moisture content, total ash, ethanol extract content and active ingredients of the steam processed Corydalis rhizoma with vinegar were determined according to the related assay method in Part IV of Chinese Pharmacopeia 2015. Results According to the guidelines from the traditional Chinese medicine quality standards and related testing methods, the moisture content of steam processed Corydalis rhizoma with vinegar should be less than 15.0%, the total ash content less than 4.0%, the ethanol extract content more than 11.0%, and the representative component of tetrahydropalmatine more than 0.05%. Conclusion The established process with this study for the quality standard of vinegar-steamed Corydalis rhizoma was conformed to the state requirements for traditional Chinese medicine. It can be used as a reference for the quality standard of vinegar-steamed Corydalis rhizoma. -
Key words:
- vinegar-steamed Corydalis rhizoma /
- identify /
- quality standard
-
类风湿关节炎(RA) 是一种以滑膜关节病变为主的慢性全身性、进行性自身免疫性疾病。疾病最早开始表现是滑膜炎,继而引发骨损伤及侵蚀,直至骨关节畸形及功能障碍[1-2],RA动物模型中广泛使用的是佐剂性关节炎模型和胶原诱导的关节炎模型。佐剂性关节炎又称弗氏佐剂性关节炎,是建立免疫性关节炎动物模型的基本方法[3]。RA发病机制还不明确,目前缺乏理想的治疗方案。临床上治疗RA主要是非甾体类抗炎药、抗风湿药物及糖皮质激素等[4],但往往因为药物的不良反应、价格等因素,难以坚持长期服药。
茵连痛风颗粒是上海中医药大学附属岳阳中西医结合医院院内制剂,由菌陈、连钱草、伸筋草组成,具有清热利湿、通络的功效。其处方是依据沪上著名夏氏外科传人夏涵教授数年临床经验方制成,用于治疗痛风性关节炎,临床具有显著疗效[5]。本实验通过弗氏完全佐剂诱导大鼠关节炎模型,观察茵连痛风颗粒对佐剂性关节炎的影响,为茵连痛风颗粒的临床应用提供科学依据。
1. 材料
1.1 药物与试剂
茵连痛风颗粒(上海中医药大学附属岳阳中西医结合医院药剂科自制,沪药制字:Z05050342,批号:1811001);塞来昔布胶囊(辉瑞制药有限公司,批号:AN8171);弗氏完全佐剂(Sigma 公司); IL-10、IL-4、前动力蛋白(PK1、2)酶联免疫分析试剂盒均购自上海威奥生物科技有限公司。
1.2 动物
SD 大鼠,雄性,体重(160±10)g,[上海斯莱克实验动物有限责任公司,实验动物生产许可证号:SCXK(沪)2017-0005]。
1.3 仪器
酶标仪(型号:DENLEY DRAGON Wellscan MK3,公司:Thermo);离心机(型号:TGL-168,公司:上海安亭科学仪器厂);数字显示隔水式电热恒温培养箱(型号:PYX-DHS,公司:上海跃进医疗器械厂);自制刻度软尺。
2. 方法
2.1 分组给药和模型建立
将48只SD雄性大鼠适应性饲养1周后,随机分为6组,每组8只。分别为正常组,模型组,塞来昔布阳性组(0.017 g/kg),茵连痛风颗粒高剂量组(15.4 g/kg),茵连痛风颗粒中剂量组(7.7 g/kg),茵连痛风颗粒低剂量组(3.8 g/kg)。除正常组外,其余各组大鼠右后足皮内注射弗氏完全佐剂 0.1 ml/足。注射弗氏完全佐剂后第8天,按照如上剂量灌胃给予相应浓度的受试药品,正常组和模型组给予等体积蒸馏水,每天给药1次,连续给药28 d。
模型鉴定:造模后各组大鼠的皮肤肿胀,皮肤温度及踝关节肿胀度与正常组之间是否有统计学差异,是模型成功与否的判定标准。
2.2 实验方法
2.2.1 大鼠一般情况和关节炎症状评分
分别在大鼠给药后7、14、28 d记录大鼠四肢关节病变程度,采用关节炎指数(AI)评分分级法评价大鼠病变程度。关节炎指数分为 5级(0~4分):0分,关节无红肿;l分,单个趾关节明显红肿;2分,发红并(或)肿胀关节>l个;3分,整个足及跖关节明显红肿;4分,严重的关节肿胀或畸形。根据未注射佐剂的余下肢体的病变程度累计积分,计算出AI(各个关节的积分累计起来,即为每只大鼠的 AI)。
2.2.2 茵连痛风颗粒对大鼠踝关节肿胀度影响
分别于造模前、给药后1 d、以及每间隔8 d,用刻度软尺测量大鼠右后踝关节周长,并观察各组动物关节病变情况。按照下列公式计算踝关节肿胀率:踝关节肿胀率=(致炎后踝关节周长-致炎前踝关节周长) /致炎前踝关节周长×100% 。
2.2.3 对大鼠甲醛致痛的影响[6]
末次给药后2 h,于大鼠左足趾皮下注射50 μl 2.5%甲醛,观察1~10 min(第I时相)和10~30 min(第II时相)的行为反应。评分标准:第I时相抬足1次,计1分;第II时相舔足、咬足或抖足1次,计2分。计算30 min内的总得分。
2.2.4 血清炎症指标检测和病理组织观察
末次给药后禁食、禁水12 h,大鼠注射10%水合氯醛(0.3 ml/100 g)进行麻醉,腹主动脉取血,离心取血清,用ELISA 法检测血清中IL-10、IL-4、PK1、PK2含量; 各组大鼠取左侧足掌肉垫,福马林固定,乙醇梯度脱水,石蜡包埋、切片和HE染色,病理组织学观察。
2.3 统计学分析
采用 SPSS 21.0 统计软件进行分析,实验数据以(
$ \bar x \pm s $ )表示,组间比较采用单因素方差分析。3. 结果
3.1 茵连痛风颗粒对大鼠一般情况及关节炎指数的影响
造模前各组大鼠毛色光亮,动作敏捷,精神状态和饮食均良好。模型组大鼠在造模后,自主活动减少、足底局部出现红肿,后期整只爪和关节均有不同程度肿胀,最初表现为足部肿胀,而后肿胀向上到达踝关节,肿胀部位皮肤发红,温度升高。随着时间延长,大鼠食欲减退,毛色暗黄,且运动功能逐渐减退。给予茵连痛风颗粒高、中、低剂量组及塞来昔布阳性组大鼠精神状态有所好转,关节肿胀度、食欲等有不同程度的缓解。表1结果表明,与模型组比较,给药7、14、28 d后,茵连痛风颗粒高、中剂量组和阳性组大鼠关节炎指数显著降低(P<0.01)。
表 1 茵连痛风颗粒对大鼠关节炎指数的影响 ($ \bar x \pm s $ ,n=8)组别 剂量(g/kg) 给药后关节炎指数 第7天 第14天 第28天 正常组 — 0.00±0.00 0.00±0.00 0.00±0.00 模型组 — 6.37±0.52## 9.63±0.74## 8.38±0.92## 阳性组 0.017 5.63±0.51** 6.50±0.93** 4.38±0.52** 高剂量组 15.4 5.50±0.53** 7.13±0.0.83** 4.13±0.64** 中剂量组 7.7 5.75±0.46** 8.13±0.0.83** 5.63±0.52** 低剂量组 3.8 5.88±0.35* 9.13±0.81 8.13±0.74 *P<0.05,**P<0.01,与模型组比较;##P<0.01,与正常组比较。 3.2 茵连痛风颗粒对大鼠踝关节肿胀度影响
表2结果显示,与同期正常组比较,模型组在给药第9天时肿胀率达峰值, 17d开始,肿胀逐日减轻,给药第9天开始,阳性组和茵连痛风颗粒高剂量组足肿胀与模型组比较,肿胀明显减轻,有显著统计学差异(P<0.01);在给药第25、28天,茵连痛风颗粒中剂组与模型组有显著性差异(P<0.05),茵连痛风颗粒低剂组无明显差异。结果显示了茵连痛风颗粒对佐剂性关节炎大鼠原发足踝关节肿胀有剂量依赖性抑制作用。
表 2 茵连痛风颗粒对大鼠踝关节肿胀率的影响 ($ \bar x \pm s $ ,n=8)组 别
踝关节周长(l/cm)给药后踝关节肿胀率(%) 第1天 第9天 第17天 第25天 第28天 正常组 2.24±0.05 2.77±0.71 3.36±1.87 3.56±4.70 3.94±6.89 4.31±7.95 模型组 2.26±0.06 28.75±6.36## 30.09±8.24## 26.51±10.43## 25.44±12.90## 23.31±13.26## 阳性组 2.27±0.08 27.00 ±0.00 22.63±1.77** 20.61±1.45** 19.33±4.31** 18.45±4.67** 高剂量 2.22±0.05 27.54 ±1.03 23.85±1.56** 20.01±0.04** 18.14±1.52** 17.85±2.40** 中剂量 2.24±0.06 28.24 ±0.67 28.68±0.92 25.19±0.88 22.26±1.52* 21.85±2.40* 低剂量 2.28±0.07 29.48 ±0.21 29.49±2.23 26.05±0.99 25.01±0.32 24.10±0.28 *P<0.05,**P<0.01,与模型组比较; ##P<0.01,与正常组比较。 3.3 茵连痛风颗粒对大鼠甲醛致痛的影响
与模型组比较,在I时相和II时相,阳性组和茵连痛风颗粒高、中、低剂量组可显著降低甲醛致痛分值(P<0.01),表明茵连痛风颗粒具有很好的镇痛作用(表3)。
表 3 茵连痛风颗粒对大鼠甲醛致痛的影响 ($ \bar x \pm s $ ,n=8)组 别 剂量 (g/kg) 甲醛致痛分值 1~10 min(Ⅰ时相) 10~30 min(Ⅱ时相) 正常组 — 2.38±0.52 1.38±0.52 模型组 — 33.63±1.41## 14.88±1.64## 阳性组 0.017 11.38±1.06** 3.50±0.93** 高剂量组 15.4 12.13±0.99** 3.25±1.04** 中剂量组 7.7 16.00±1.60** 5.25±0.89** 低剂量组 3.8 19.38±1.19** 6.50±1.20** **P<0.01;与模型组比较; ##P<0.01,与正常组比较。 3.4 茵连痛风颗粒对IL-4、IL-10、PK1、PK2的影响
模型组大鼠IL-10,IL-4与正常组相比显著降低(P<0.01),炎性反应较明显;茵连痛风颗粒各组和阳性组均能升高IL-10,IL-4水平。同时,模型组大鼠 PK1、PK2水平与正常组相比显著升高(P<0.01),阳性组和茵连痛风颗粒各组均能降低两者水平,与模型组比较有显著差异 (P<0.01),其中,茵连痛风颗粒高剂量组更明显(表4)。
表 4 茵连痛风颗粒对大鼠血清IL-4、IL-10、PK1、PK2的影响 ($ \bar x \pm s $ ,n=8)组别 剂量 (g/kg)
IL-4
IL-10
PK1
PK2正常组 — 79.49±4.38 97.07±2.97 491.76±8.56 926.24±25.38 模型组 — 59.89±3.45## 20.99±2.78## 706.31±67.83## 1455.40±147.81## 阳性组 0.017 139.69±13.78** 98.94±6.72** 567.10±20.58** 1099.60±63.63** 高剂量组 15.4 101.45±7.05** 90.36±5.43** 365.49±27.65** 656.07±194.68** 中剂量组 7.7 95.60±4.52** 82.75±8.49** 433.91±22.29** 866.73±21.57** 低剂量组 3.8 72.50±3.09** 78.15±5.47** 529.20±12.79** 1015.51±18.36** **P<0.01,与模型组比较; ##P<0.01,与正常组比较。 3.5 病理观察
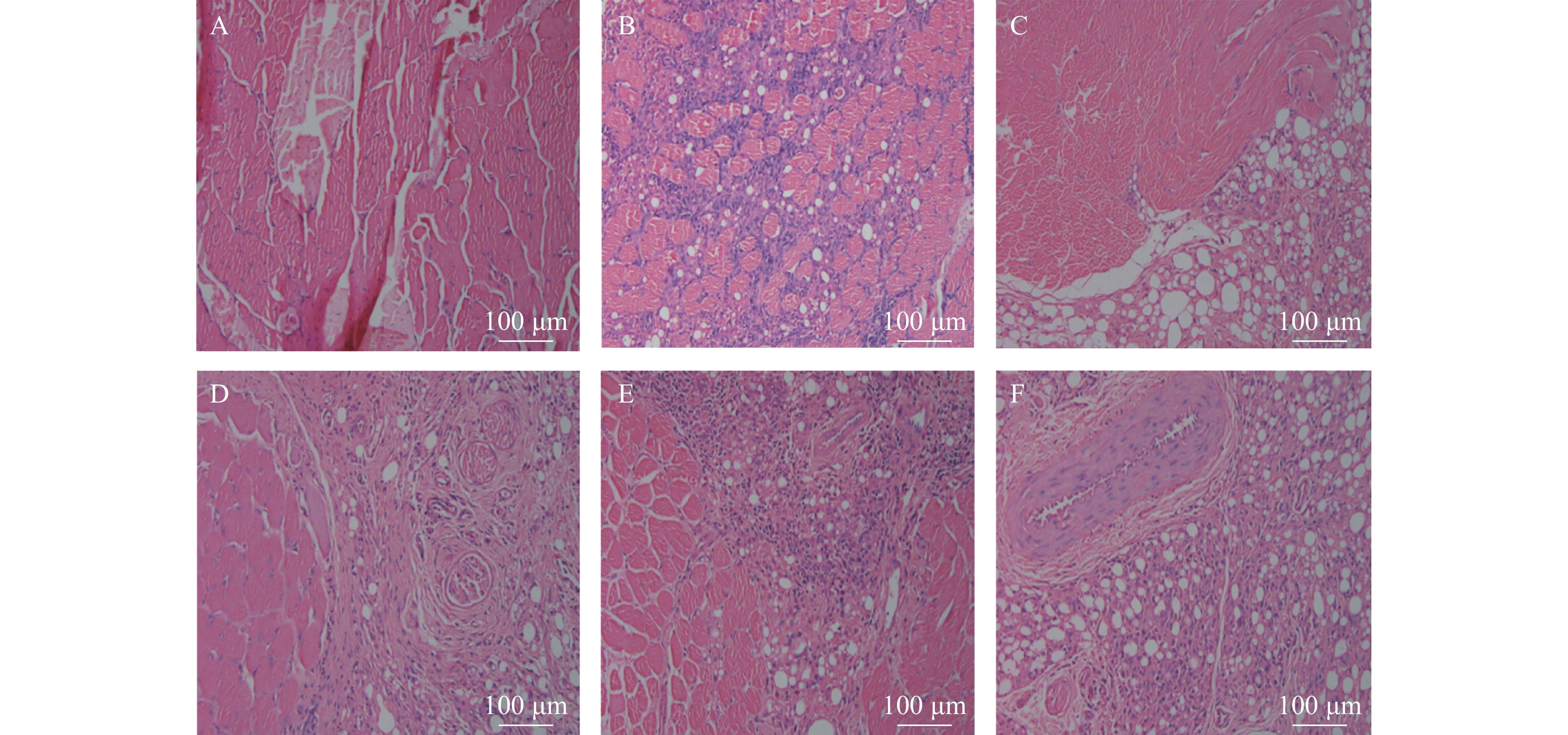
由图1可见,正常对照组足趾肉垫无炎症细胞浸润,而模型组可见大量淋巴细胞浸润。塞来昔布组可见淋巴细胞浸润程度的大幅度降低,而茵连痛风颗粒高、中、低剂量组均可降低淋巴细胞浸润,而以茵连痛风颗粒高剂量组最为显著。
4. 讨论
类风湿关节炎在中医归属“痹症”范畴,治疗以祛风除湿、散寒通络、扶正固本、清热解毒为主[7]。茵连痛风颗粒有茵陈、连钱草、伸筋草三味药材组成。茵陈作为君药,具有清利湿热、芳香舒脾、透表畅气之效;臣药连钱草,取其消石之功,防止痛风性尿路结石的产生,具有利湿通淋、清热解毒、散瘀消肿之功效;佐药伸筋草具有祛风除湿、舒筋活血之效,为治痹痛拘挛及伤损瘀肿之要药,配伍茵陈可以增强该复方利湿通络的作用。该方配伍符合中医理论对类风湿性关节炎的认识[8]。
弗氏佐剂关节炎动物模型是经典的类风湿关节炎模型,与类风湿性关节炎模型的病因、病症更接近。它能较为真实地反映类风湿关节炎的病理进程,与痛风性关节炎同属中医 “痹证”“白虎历节风”范畴,而且制备方法简便、易重复。常用于关节炎药物的药效评估[9]。IL-4、IL-10细胞因子在类风湿性关节炎患者中,起到十分重要的作用。这类细胞因子与滑膜炎性反应、增生及关节变形有着密切的关系。PK信号通路是近年新发现的调节通路,包括两种结构上关联的小分子肽PK1和PK2及相应的G蛋白偶联受体PK(PKR1和PKR2),PKs及其受体PKRs广泛分布在许多人体组织中。在免疫细胞中参与炎症发生和疼痛传递的重要环节,如PK2参与免疫调节,诱导骨髓细胞分化为单核细胞系和巨噬细胞系,并通过激活单核细胞、巨噬细胞和树突状细胞上的 PKRs,释放IL-1、IL-6、TNF-a等炎性细胞因子,触发和维持炎性疼痛,调节免疫炎症反应[10-11]。研究发现在前动力蛋白信号通路中加入PKRs激动剂可以显著降低IL-10和IL-4生成[12]。损伤组织中释放的PKs是免疫-炎症反应的一种自分泌或旁分泌的调节剂,能够刺激神经元中PKRs而增强伤害性感受器的敏感性,说明PKs信号通路在调节伤害性感受阈方面发挥重要功能,因此阻断PKs信号通路是目前治疗炎性疼痛的新策略[11]。然而,关于PK信号通路在中药镇痛方面的研究报道较少,其干预中药镇痛的具体机制有待进一步研究证实。本实验结果显示,茵连痛风颗粒可明显减轻RA大鼠足踝关节肿胀,按照人和大鼠之间的体表面积换算成大鼠的给药中剂量,并设置高、中、低3个剂量组。以高剂量组改善最为明显,并呈现剂量依赖性。同时,病理结果显示,茵连痛风颗粒高中低剂量组均可降低淋巴细胞浸润,以茵连痛风颗粒高剂量组最为显著。其作用机制可能是通过PK信号通路抑制PK1、PK2分泌,以及促进细胞因子IL-4、IL-10等分泌达到抗类风湿性关节炎的作用。为茵连痛风颗粒作用机制的阐明打下了基础。这些研究结果表明,茵连痛风颗粒对佐剂关节炎具有明显抑制作用,暗示其对类风湿关节炎的治疗前景,作用机制有待进一步研究。
-
表 1 10批醋蒸延胡索水分测定结果(%)
序号 含水量A 含水量B 平均值 相对偏差 CYHS-01-01 13.62 13.45 13.54 0.63 CYHS-01-02 12.12 12.35 12.24 0.94 CYHS-01-03 12.39 12.62 12.51 0.92 CYHS-01-04 12.15 12.04 12.10 0.45 CYHS-01-05 12.50 12.15 12.33 1.42 CYHS-01-06 14.09 13.86 13.98 0.82 CYHS-01-07 11.97 11.76 11.87 0.88 CYHS-01-08 16.09 15.38 15.74 2.26 CYHS-01-09 12.40 12.06 12.23 1.39 CYHS-01-10 13.07 12.72 12.90 1.36 表 2 10批醋蒸延胡索总灰分测定结果(%)
序号 灰分A 灰分B 平均值 相对偏差 CYHS-01-01 3.15 3.04 3.10 1.78 CYHS-01-02 2.76 2.80 2.78 0.72 CYHS-01-03 2.89 2.93 2.91 0.69 CYHS-01-04 3.78 3.82 3.80 0.53 CYHS-01-05 2.88 2.95 2.92 1.20 CYHS-01-06 2.74 2.79 2.77 0.90 CYHS-01-07 3.24 3.20 3.22 0.62 CYHS-01-08 3.20 3.23 3.22 0.47 CYHS-01-09 3.25 3.29 3.27 0.61 CYHS-01-10 3.22 3.19 3.21 0.47 表 3 10批醋蒸延胡索浸出物测定结果(%)
序号 浸出物A 浸出物B 平均值 相对偏差 CYHS-01-01 13.69 13.48 13.59 0.77 CYHS-01-02 18.51 18.20 18.36 0.84 CYHS-01-03 14.06 14.15 14.11 0.32 CYHS-01-04 13.87 13.67 13.77 0.73 CYHS-01-05 14.39 14.05 14.22 1.20 CYHS-01-06 16.46 16.21 16.34 0.77 CYHS-01-07 14.66 14.50 14.58 0.55 CYHS-01-08 11.43 11.68 11.56 1.08 CYHS-01-09 13.68 13.79 13.74 0.40 CYHS-01-10 11.78 11.92 11.85 0.59 表 4 加样回收率试验结果
编号 取样量(m/g) 加样量(m/mg) 回收率(%) RSD(%) 1 0.2418 0.2022 100.4 3.3 2 0.2417 0.2022 106.7 3 0.2427 0.2022 104.6 4 0.2462 0.2022 105.7 5 0.2453 0.2022 100.0 6 0.2440 0.2022 98.5 表 5 10批醋蒸延胡索含量测定结果
样品 含量(%) 平均值(%) CYHS-01-01 0.064 0.077 CYHS-01-02 0.068 CYHS-01-03 0.055 CYHS-01-04 0.058 CYHS-01-05 0.072 CYHS-01-06 0.092 CYHS-01-07 0.068 CYHS-01-08 0.100 CYHS-01-09 0.098 CYHS-01-10 0.098 -
[1] 国家药典委员会. 中华人民共和国药典(一部)2015年版 [S]. 北京: 中国医药科技出版社, 2015. [2] 冯自立, 赵正栋, 刘建欣. 延胡索化学成分及药理活性研究进展[J]. 天然产物研究与开发, 2018, 30(11):2000-2008. [3] 何晓凤, 张晶, 张梅. 延胡索化学成分、药理活性及毒副作用研究进展[J]. 上海中医药杂志, 2017, 51(11):97-100. [4] 董庆海, 吴福林, 王涵, 等. 延胡索药学研究进展[J]. 中国野生植物资源, 2019, 38(1):48-53,79. [5] 龚千锋. 中药炮制学[M]. 4版. 北京: 中国中医药出版社, 2016. [6] 黄小平. 不同的炮制方法对延胡索中延胡索乙素含量的影响[J]. 当代医药论丛, 2019, 17(18):167-168. doi: 10.3969/j.issn.2095-7629.2019.18.127 [7] 肖辉. 不同炮制方法对延胡索中延胡索乙素含量的影响[J]. 中国药业, 2016, 25(4):29-31. [8] 孟德阳. 延胡索醋炙前后饮片和煎剂中延胡索乙素含量变化对比[J]. 吉林中医药, 2018, 38(2):198-201. [9] 谢明. 延胡索醋制前后总生物碱含量测定及对小鼠的镇痛作用比较[J]. 海峡药学, 2014, 26(3):33-34. [10] 江国荣, 禤雪梅, 潘雪莲, 等. 不同炮制方法对中药延胡索中有效成分含量的影响[J]. 北方药学, 2016, 13(11):5,121. [11] 李春, 蒋晓煌, 蒋孟良, 等. 正交试验优选延胡索醋蒸法炮制工艺[J]. 中医药导报, 2015, 21(6):53-55. [12] 郑军献, 徐雁, 洪春霞, 等. 延胡索不同加工工艺的研究[J]. 浙江中医杂志, 2012, 47(5):379-380. doi: 10.3969/j.issn.0411-8421.2012.05.058 [13] 龙全江, 张颖, 徐雪琴. 不同加工方法对延胡索3种生物碱含量的影响[J]. 中国中医药信息杂志, 2017, 24(7):90-93. doi: 10.3969/j.issn.1005-5304.2017.07.021 [14] 王安铸, 马晓昌. 延胡索乙素的研究进展[J]. 中华中医药杂志(原中国医药学报), 2020, 35(4):1927-1929. -







 下载:
下载:



 下载:
下载: