-
癫痫在神经科的发病率较高,仅次于脑血管疾病,患者首次发病后,经常会反复发作,彻底治愈难度大,一般需要长期服药以控制病情。在长期的抗癫痫治疗过程中,患者受到药物﹑气候及周围环境的影响,免疫功能下降,在治疗期间易获得院内细菌性感染[1]。癫痫合并耐药阳性菌感染的住院患者(尤其是ICU患者)常联合使用丙戊酸钠和万古霉素,以达到治疗效果。但丙戊酸钠治疗指数低、体内过程和疗效存在较大个体差异,其有效血药浓度范围为50~100 μg/ml,而且该药需要长期服用,易产生耐受,血药浓度相对不稳定,特别是与其他药物联用时,常发生相互作用而影响疗效[2-3]。另外,万古霉素疗效与其血药浓度密切相关[4],2011年美国感染病学会(IDSA)刊文指出,万古霉素的血药浓度应达到10 μg/ml以上,对于复杂、严重的感染应达到15~20 μg/ml方能起到更好的治疗效果,同时万古霉素的治疗窗相对狭窄,血药浓度过高可能导致肾功能损害及耳毒性发生。所以临床用药时需要对两者进行血药浓度监测。
目前对丙戊酸钠和万古霉素进行血药浓度监测主要有高效液相色谱法和免疫分析法。采用高效液相色谱串联质谱法(HPLC-MS/MS)对两者进行浓度检测的文献亦有报道,但均为对其单独检测,未见对两者同时进行浓度检测的报道。本研究拟建立同时测定血清中丙戊酸钠和万古霉素浓度的HPLC-MS/MS法,并应用于两者联合用药时的血药浓度监测,该研究结果会对两者在临床的安全合理使用、节省医疗资源和减少患者医疗费用等方面起到积极作用。
-
Agilent 1260 高效液相色谱仪(美国 Agilent),包括G1322A自动脱气机,G1318B自动调配四元泵,G1367E自动进样器,G1316A可调柱温箱;Agilent 6420 triple quad LC/MS,图谱分析软件MassHunter Workstation Software(版本号B. 06.00);XW-80A型旋涡混合器(原上海医科大学仪器厂);BP110S 型电子分析天平(德国 Sartorius);MIKRO12-24 型高速离心机(德国 Hettich)。
-
丙戊酸钠对照品、丙戊酸钠-d6对照品、万古霉素对照品、卡那霉素B对照品(European Directorate for the Quality of Medicines & HealthCare),甲醇、乙腈、甲酸(质谱纯,默克公司),水为重蒸去离子水。
-
色谱柱为美国Agilent ZORBAX Eclipse Plus C18(4.6 mm×100 mm, 3.5 μm),流速0.5 ml/min,柱温25 ℃,进样量4 µl,流动相为0.1%甲酸水溶液(A)-乙腈(B),梯度洗脱见表1。
表 1 梯度洗脱信息
时间(t/min) A(%) B(%) 0~1.5 85 15 1.5~4.5 30 70 4.5~5.5 10 90 5.5~12 85 15 -
离子源为电喷雾离子化源(ESI),用多反应监测模式(MRM)进行定量分析,用正负离子检测模式。毛细管电压4 000 V,喷雾气压力45 psi,干燥气体流速10 L/min,干燥气体温度350 ℃。丙戊酸钠和内标丙戊酸钠-d6,选择负离子模式检测,离子反应对[M-H]−分别为m/z 143→143和m/z 149→149,碰撞能量均为0 V,裂解电压均为110 V。万古霉素和内标卡那霉素B,选择正离子模式检测,离子反应对[M+H]+分别为m/z 725→100和m/z 484→324,碰撞能量分别为46 V和14 V,裂解电压分别为142 V和130 V。4种药物的四级杆捕捉时间均为0.2 s,电子倍增器300 V。
-
分别精密称取丙戊酸钠对照品和万古霉素对照品20 mg和10 mg,置于10 ml棕色容量瓶中,用乙腈-水(50∶50)溶液定容至刻度,得到浓度分别为2 000 μg/ml和1 000 μg/ml的丙戊酸钠和万古霉素混合对照品储备液,贮存于4 ℃冰箱备用。配制浓度均为100 μg/ml丙戊酸钠-d6和卡那霉素B内标溶液,置于4 ℃冰箱保存备用。
-
取血清样品200 µl,置于1.5 ml的EP管中,分别加入内标丙戊酸钠-d6和卡那霉素B溶液各20 µl,涡旋混匀30 s,加入乙腈200 µl,涡旋混匀60 s,于室温下以14 000 r/min离心5 min,吸取上清液300 µl,加入乙腈-水(50∶50)溶液500 µl,涡旋混匀30 s,进样分析,分析时间12 min。
-
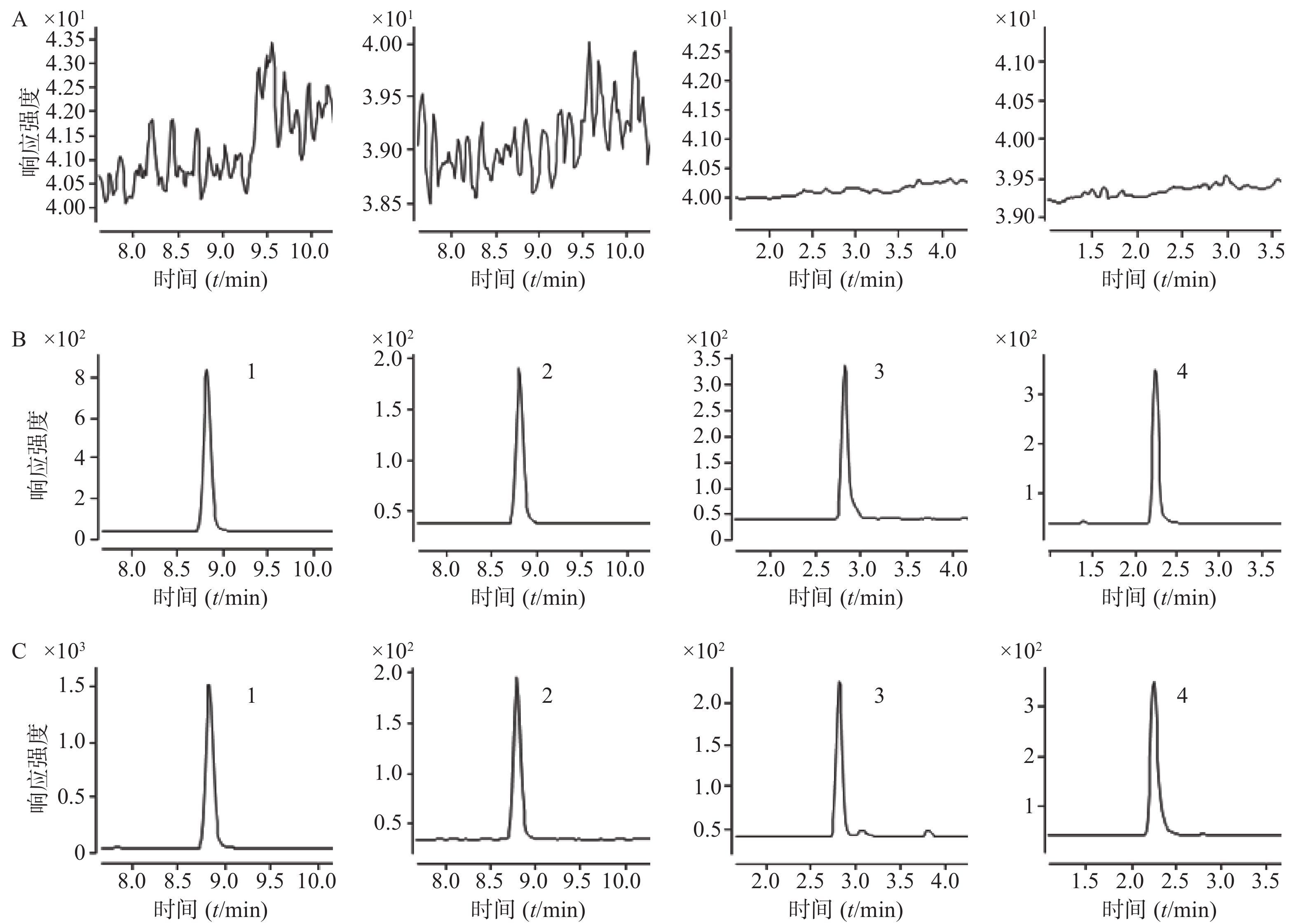
取空白血清200 µl置1.5 ml的EP管中,不加入内标溶液,按“2.4”项下操作进样分析,获得空白血清样品的色谱图;将一定浓度的标准溶液及内标加入空白血清中,依同法操作获得相应的色谱图;另取临床血清样品,依同法操作得色谱图。在该色谱质谱条件下得到的丙戊酸钠、万古霉素和内标物的色谱峰良好,无明显的杂质峰干扰,丙戊酸钠与丙戊酸钠-d6的保留时间均为8.81 min,万古霉素和卡那霉素B的保留时间分别为2.82、2.24 min。结果表明,空白血清中内源性物质不干扰丙戊酸钠和万古霉素的测定。色谱图见图1。
-
取空白血清180 µl,加入用乙腈-水(50:50)溶液将丙戊酸钠和万古霉素混合对照品储备液逐级稀释成相应的混合对照品系列溶液,按“2.4”项下操作法配制成血清中丙戊酸钠浓度分别为1、2、4、10、20、100和200 μg/ml,万古霉素质量浓度分别为 0.5、1、2、5、10、50和100 μg/ml的血清样品,进样分析。以待测物与内标质量浓度的比值为横坐标轴(X),以待测物与内标峰面积的比值为纵坐标轴(Y),绘制标准曲线。用权重系数为1/χ2计算线性回归方程。丙戊酸钠和万古霉素分别在1~200 μg/ml和0.5~100 μg/ml内具有良好的线性关系,标准曲线方程分别为Y=2.71X+0.003和Y=2.83X+0.19(r均>0.999)。丙戊酸钠定量下限为1.00 μg/ml,方法回收率为113.81%,RSD为1.64%;万古霉素定量下限为0.50 μg/ml,方法回收率为107.34%,RSD为4.20%。
-
按“3.2”项方法分别配制低、中、高3个浓度的丙戊酸钠(2、10和100 μg/ml)和万古霉素(1、5和50 μg/ml)的质控血清样品各15份,分为3批,每批5份,并与每批的标准曲线同时进行,按“2.4”项同法操作进样,求得本法的精密度和准确度。结果表明,低、中、高浓度的丙戊酸钠和万古霉素的批内、批间精密度RSD均小于15%,结果见表2。
表 2 丙戊酸钠和万古霉素的精密度与准确度(
$ \overline{\text{x}}\text{±}\text{s} $ ,n=5)分析物 浓度值(μg/ml) 准确度
(%)精密度RSD(%) 标示浓度 实测浓度 批内(n=5) 批间(n=15) 丙戊酸钠 2 2.06±0.09 102.78 0.87 5.05 10 9.27±0.32 92.67 0.21 3.71 100 99.55±1.99 99.54 0.23 2.15 万古霉素 1 1.07±0.09 106.87 7.54 9.93 5 5.03±0.13 100.69 1.07 2.86 50 50.64±2.49 101.28 3.54 5.32 -
按“3.2”项方法分别配制低、中、高3个浓度的丙戊酸钠(2、10和100 μg/ml)和万古霉素(1、5和50 μg/ml)的质控血清样品,按“2.4”项同法操作进样得峰面积A1。另取3份空白血清200 µl,先用200 µl乙腈沉淀蛋白,经14 000 r/min,5 min离心沉淀后,取180 µl该上清液,加入相应浓度的丙戊酸钠与万古霉素混合标准液和内标溶液各20 µl,得3个浓度的标准样品,进样得峰面积A2。再取3份180 µl重蒸去离子水,分别向其中加相应浓度的丙戊酸钠与万古霉素混合标准液和内标溶液各20 µl,得到3个浓度的标准样品,进样得峰面积A3。提取回收率即A1/A2×100%,基质效应即A2/A3×100%。结果表明,丙戊酸钠和万古霉素的基质影响均在85%~115%之间,RSD均小于15%,提取回收率平均值均达到70%以上,结果见表3。
表 3 丙戊酸钠和万古霉素的基质效应与提取回收率(
$ \overline{\text{x}}\text{±}\text{s} $ ,n=5)分析物 标示浓度
(μg/ml)基质效应
(%)RSD
(%)提取回收率 RSD
(%)丙戊酸钠 2 106.60±2.95 2.77 78.23±5.39 6.89 10 92.63±2.69 2.91 73.76±3.58 4.85 100 92.82±1.59 1.72 75.83±3.53 4.66 万古霉素 1 96.90±1.88 1.94 71.62±7.99 11.16 5 99.07±1.79 1.80 73.08±4.99 6.82 50 99.19±0.84 0.85 71.23±4.87 6.84 -
按“3.2”项方法分别配制低、中、高 3个浓度的丙戊酸钠和万古霉素的质控血清样品,考察样品经室温放置24 h、4 ℃冷藏24 h、反复冻融3次以及-80 ℃冻存30 d的稳定性。结果表明,以上条件下3个浓度样品检测结果的RSD值均小于15%。结果见表4。
表 4 丙戊酸钠和万古霉素的稳定性(
$ \overline{\text{x}}\text{±}\text{s} $ ,n=5)分析物 标示浓度
(μg/ml)25 ℃放置24 h 4 ℃放置24 h 反复冻融3次 -80 ℃冻存30 d 实测浓度(μg/ml) RSD(%) 实测浓度(μg/ml) RSD(%) 实测浓度(μg/ml) RSD(%) 实测浓度(μg/ml) RSD(%) 丙戊酸钠 2 2.16±0.14 6.55 1.86±4.73 7.38 1.77±0.18 10.23 1.83±0.12 6.34 10 10.71±0.38 3.56 10.18±0.37 4.32 8.97±0.69 7.72 9.49±0.64 6.79 100 104.30±1.50 1.44 107.40±2.70 2.48 91.63±10.81 11.79 88.58±4.91 5.55 万古霉素 1 1.20±0.07 5.62 1.04±0.05 9.11 0.96±0.13 13.37 0.84±0.08 9.39 5 5.43±0.31 5.63 5.03±0.25 6.51 4.78±0.43 9.06 4.59±0.34 7.51 50 52.72±2.70 5.12 46.26±0.78 7.85 44.69±3.69 8.26 44.57±3.22 7.23 -
近年来,有报道[5-8]使用HPLC-MS/MS法测定丙戊酸钠和万古霉素的血药浓度,但都是分别单独检测,对它们同时检测的HPLC-MS/MS法尚未见报道。目前HPLC-MS/MS法同时测定多种药物血药浓度的技术主要被用于测定同类药物。同类药物的理化性质相似,方法的建立更简单快速。但本实验测定的丙戊酸钠脂溶性强,而万古霉素则为水溶性药物,理化性质存在差异,方法建立难度较大。在血清样品的处理方法上,本实验考虑了包括液-液萃取法、固相萃取法及蛋白沉淀法多种处理方法,液-液萃取法及固相萃取法操作复杂,时间较长,本实验最终选择使用蛋白沉淀法。通过对比甲醇、乙腈、10%三氯乙酸、10%三氯乙酸-甲醇(50∶50)等沉淀剂的蛋白沉淀效果,确定乙腈作为有机蛋白沉淀剂效果最好,此方法稳定性好,同时也避免了引入新的杂质对实验结果产生影响。另外,样本单纯经乙腈沉淀蛋白后直接进样分析,会导致万古霉素提取回收率较低,因此我们在乙腈沉淀蛋白后尝试了按不同比例加入纯化水稀释,虽然万古霉素提取回收率得到了改善,但稳定性下降且峰形较差,杂峰较多。最后尝试比较了不同比例的甲醇-水溶液和乙腈-水溶液稀释法,确定了以乙腈-水(50∶50)溶液稀释乙腈沉淀蛋白后的提取液,不仅提取回收率得到了提高,且稳定性良好,可以满足临床样本检测的需要。在流动相的选择上,本实验选择了0.1%甲酸水溶液-乙腈作为流动相,与文献报道[5-8]使用的乙腈-20 mmol/L乙酸铵水溶液、0.1%甲酸水溶液-0.1%甲酸甲醇溶液等相比,该流动相配制简单,更适合用于丙戊酸钠和万古霉素2种药物的同时检测,峰形较好,无拖尾现象。
在临床上,丙戊酸钠和万古霉素均为监测其血药谷浓度,采血时间相同。采用本方法对丙戊酸钠和万古霉素同时进行血药浓度监测,不仅可以避免两次抽血给患者带来的不适,提高患者依从性,同时降低了检测成本,有利于节约医疗成本,减少患者医疗支出。
Determination of sodium valproate and vancomycin in human serum by HPLC-MS/MS
-
摘要:
目的 建立同时测定人血清中丙戊酸钠和万古霉素浓度的高效液相色谱串联质谱法(HPLC-MS/MS)。 方法 以丙戊酸-d6和卡那霉素B分别作为丙戊酸钠和万古霉素的内标,用乙腈沉淀蛋白法处理血清样品,以0.1%甲酸水溶液-乙腈为流动相进行梯度洗脱,流速为0.5 ml/min,柱温25 ℃,进样量4 μl,总分析时间12 min。采用电喷雾离子源进行正负离子模式监测,多反应监测模式进行定量分析。考察该方法的专属性、标准曲线、定量下限、精密度、回收率、基质效应以及稳定性。 结果 丙戊酸钠和万古霉素分别在1~200 μg/ml和0.5~100 μg/ml范围内具有良好的线性关系,定量下限分别为1 μg/ml和0.5 μg/ml,提取回收率均达到70%以上,批间、批内精密度RSD值均小于10%,稳定性良好,无明显基质效应。 结论 该方法操作简便、快捷、专属性好、灵敏度高、结果准确,可用于临床对两者同时进行血药浓度监测。 -
关键词:
- 丙戊酸钠 /
- 万古霉素 /
- 血药浓度监测 /
- 高效液相色谱串联质谱法
Abstract:Objective To establish a high performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS) method for simultaneous determination of sodium valproate and vancomycin in human serum. Methods Valproic acid-d6 and kanamycin B were used as the internal standard of sodium valproate and vancomycin, the serum samples were treated by acetonitrile precipitation protein method. The mobile phase was 0.1% formic acid aqueous solution-acetonitrile for gradient elution. The flow rate was 0.5 ml/min, with column temperature at 25 ℃. The sample volume was 4 μl and total analysis time was 12 min. The positive and negative ion mode was monitored by electrospray ion source and the multiple reaction monitoring mode was used for quantitative analysis. The specificity, standard curve, lower limit of quantification, precision, recovery, matrix effect, and stability of the method were examined. Results Sodium valproate and vancomycin had good linear relationships in the range of 1 - 200 μg/ml and 0.5 - 100 μg/ml, respectively. The quantitative lower limits were 1 μg/ml and 0.5 μg/ml, respectively. The extraction recoveries were above 70%. The inter- and intra-batch precision RSD values were less than 10%. The stability was good and there was no obvious matrix effect. Conclusion This method is simple, quick, sensitive, specific and accurate, which could be used to simultaneously determine the concentration of sodium valproate and vancomycin in human serum. -
Key words:
- sodium valproate /
- vancomycin /
- blood concentration monitoring /
- HPLC-MS/MS
-
根据世界卫生组织最新统计显示,心脑血管疾病如心肌梗死、缺血性卒中等是目前全球最主要的致死原因[1]。血小板作为动脉血栓形成的一项重要介质,其高反应性是导致动脉血栓事件发病率和病死率增加的重要危险因素[2, 3]。尽管现有的抗血栓药物可有效减少心血管疾病患者的动脉血栓形成,但出血的不良反应也极大限制了它们的使用。因此为了开发出能在抗血栓形成效果和出血之间取得更好平衡的新一代安全有效的抗血栓药物,迫切需要了解导致血管血栓闭塞的致病机制,开展新靶标的基础研究[4, 5]。
分泌蛋白可由机体各种组织器官分泌,在生理、病理过程中起关键作用,具备良好的研究前景,有望开发成为心脑血管疾病防治的药物、靶标、生物标志物[6, 7]。近期有多项研究表明部分分泌蛋白大量存在于血液之中,可直接作用于血栓调控[8-10]。Metrnl是本实验室前期通过构建限食模型筛选获得的一种与神经营养因子Metrn同源的新型分泌蛋白[11]。迄今为止,多项研究结果表明Metrnl在免疫炎症及代谢性心脑血管疾病中发挥重要作用,例如调节胰岛素敏感性、维持肠道稳态、对抗动脉粥样硬化、促进血管新生等[12-17]。此外,临床研究显示,血液Metrnl水平与冠心病、心肌梗死、缺血性脑卒中等多种血栓性疾病存在相关性[18-20]。以上结果均提示Metrnl在心脑血管疾病病理过程中扮演重要角色,但是Metrnl在血栓形成特别是其对血小板的直接作用尚未可知。
前期,本实验室通过使用Metrnl全身性敲除小鼠,已在多种血栓模型下证明Metrnl缺乏会导致血栓形成能力增强,并且在进一步的血小板功能检测中,证实Metrnl缺乏会导致血小板活性增强[21]。然而,我们尚未证明究竟是循环Metrnl还是血小板Metrnl的缺乏在促进血栓形成中扮演主要角色,且血小板Metrnl是否可以直接调控血小板活性改变,从而在血小板高活性与动脉血栓形成事件发生率增加之间建立联系,目前尚不清楚。
因此,本研究使用Metrnlloxp/loxp小鼠和Pf4-Cre小鼠进行交配繁殖,旨在构建血小板特异性Metrnl敲除小鼠模型,作为深入研究血小板内源性Metrnl在动脉血栓中的作用及调控机制的工具,并对该敲除小鼠的构建成功与否展开验证工作。
1. 材料与方法
1.1 实验试剂和仪器
鼠尾DNA提取试剂盒(CW2094S)购自北京康为世纪生物科技有限公司,5×Evo M-MLV RT Master Mix(AG11706)、通用型RNA提取试剂盒(AG21022)购自湖南艾科瑞生物工程有限公司,小鼠Actin抗体(
66009 -1-IG)购自武汉三鹰技术有限公司,Anti-METRNL抗体(ab235775)购自Abcam公司,辣根过氧化物酶标记山羊抗小鼠IgG(H+L)(A0216)、辣根过氧化物酶标记山羊抗兔IgG(H+L)(A0208)购自上海碧云天生物技术有限公司,红细胞裂解液(BL503B)购自北京兰杰柯科技有限公司。实时荧光定量PCR仪(LightCycler96)来自Roche公司,PCR仪(TP600)来自Takara公司,化学发光分析系统(5200S)来自Tanon公司,动物全血计数仪(pocH-100iV)来自希森美康公司。
1.2 实验动物
Metrnlloxp/loxp小鼠为实验室前期构建所得。SPF级8周龄Pf4-Cre小鼠购自上海南方模式生物技术有限公司。
所有实验小鼠均饲养在独立通气笼盒(IVC)系统中,温度(24±2) ℃,相对湿度为40%~60%,饲养期间笼盒内保持清洁,小鼠在笼内自由活动、进食及饮水,动物房内照明系统为自动控制(12 h照明、12 h黑暗)。动物实验标准均依照国家《实验动物护理使用卫生指南》,并经过海军军医大学大学医学研究伦理委员会批准指导。
1.3 实验方法
1.3.1 动物基因型鉴定
将剪刀消毒后剪取小鼠尾尖约3 mm,剪碎,按照DNA提取试剂盒的说明书方法提取DNA。之后,对目的基因进行PCR扩增,各引物序列如表1。
表 1 PCR扩增实验中的引物序列基因名称 上游引物(5’→3’) 下游引物(5’→3’) Metrnl loxp TGAGGGTTGGAGGCTCCTAGC GGATGAGCGTTTGAGCACAGC Pf4-Cre CCAAGTCCTACTGTTTCTCACTC TGCACAGTCAGCAGGTT 内参基因 CAAATGTTGCTTGTCTGGTG GTCAGTCGAGTGCACAGTTT 将PCR产物进行1.2% 琼脂糖凝胶电泳,上样量为每孔6 μl,电泳条件为100 V×30 min,结束后进行拍照、分析。
1.3.2 小鼠取材
将小鼠称重后,腹腔注射1%戊巴比妥钠溶液(100 mg/kg),待小鼠处于深度麻醉后,打开其腹腔,用1 ml注射器吸取约100 μl 2%枸橼酸钠溶液(枸橼酸钠0.2 g,蒸馏水定容至10 ml),自腹主动脉处缓慢抽取抗凝血液,并转移至15 ml离心管中。组织灌流后迅速剪取小鼠心、肝、脾、肺、肾、脑、结肠组织,放入组织冻存管扔进液氮速冻,待取材结束后及时转入−80 ℃超低温冰箱储存。骨髓提取分离小鼠股骨并剪去多余肌肉和纤维组织,剪掉股骨两端,在干净PBS中反复冲洗骨髓腔,收集冲洗液室温离心
1000 r/min×5 min获得骨髓细胞,用1 ml Triozl溶液重悬混匀,储存至−80 ℃超低温冰箱。1.3.3 小鼠洗涤血小板制备
向小鼠抗凝全血中加入等体积0.9%生理盐水,并加入Apyrase(终浓度2 U/ml),快速颠倒混匀后室温离心800 r/min×10 min;离心后收集最上层富血小板血浆(PRP),转移至新的15 ml离心管,室温离心
1700 r/min×5 min,弃去上清液,取适量台式液重悬。1.3.4 小鼠外周血细胞制备
小鼠心脏采抗凝血后,室温离心
1000 r/min×5 min,弃去上清液后加入5 ml的红细胞裂解液,室温作用10 min,室温离心1000 r/min×5 min,重复1次,在血细胞沉淀中加入5 ml PBS洗涤,室温离心1000 r/min×5 min,弃去上清后根据白细胞沉淀的量加入100~500 μl PBS重悬。红细胞提取在全血中加入等体积红细胞保存液(枸橼酸钠0.8 g,葡萄糖2.05 g,枸橼酸0.0325 g,氯化钠0.42 g,蒸馏水定容至100 ml), 室温离心2 000 r/min×10 min,连续离心洗涤3次后,取压积红细胞加入100~500 μl红细胞保存液重悬。1.3.5 实时荧光定量PCR实验
使用RNA提取试剂盒提取组织RNA,Triozl法提取骨髓RNA,将得到的RNA进行浓度测定与吸光度测定后进行逆转录,得到cDNA用于实时荧光定量PCR实验,各引物序列如表2。
表 2 实时荧光定量PCR实验中的引物序列基因名称 上游引物(5′→3′) 下游引物(5′→3′) Mouse Metrnl CTGGAGCAGGGAGGCTTATTT GGACAACAAAGTCACTGGTACAG Mouse Gapdh GTATGACTCCACTCACGGCAAA GGTCTCGCTCCTGGAAGATG 1.3.6 蛋白免疫印迹实验
取适量组织至2 ml高速离心管,加入蛋白裂解液后,使用高通量匀浆仪匀浆240 s。取出高速离心管,离心:
12000 g×15 min。将上清液转移至另一干净1.5 ml EP管中,进行蛋白浓度测定,剩余样品加入5×蛋白上样缓冲液,97 ℃变性10 min得到蛋白样品。使用10% SDS-PAGE凝胶进行电泳,电泳条件为:150 V×60 min。使用PVDF膜进行转膜,转膜条件为100 V×60 min。
转膜结束后,使用快速封闭液封闭20 min,之后使用1 × TBST缓冲液洗膜,5 min×3次。加入一抗孵育液(1∶
1000 稀释)4 ℃孵育过夜。次日去除一抗孵育液,使用1×TBST缓冲液洗膜,10 min×3次。加入二抗孵育液(1∶1000 稀释)常温孵育1 h,用1×TBST缓冲液洗去二抗,10 min×2次,结束后即可进行扫膜。1.3.7 统计学分析
实验数据使用GraphPad Prism 9.5进行统计分析。两组间的比较使用two-tailed Student’s t test检验,P<0.05视为结果存在统计学意义。
2. 结果
2.1 血小板特异性Metrnl敲除小鼠的构建和基因型鉴定
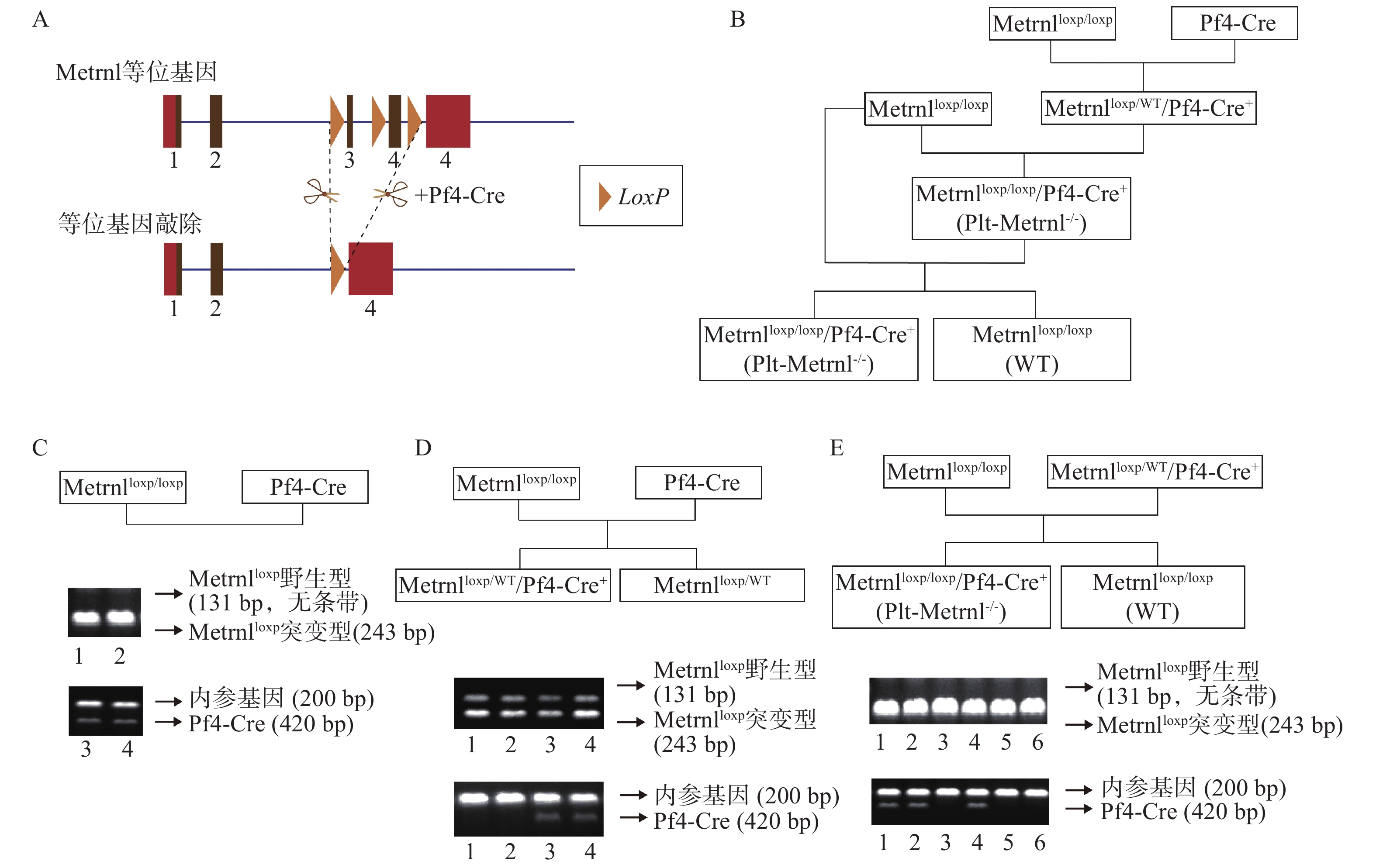
本研究构建策略基于前期构建的Metrnlloxp/loxp小鼠和Cre-LoxP重组酶系统,所构建血小板特异性Metrnl敲除小鼠(Metrnlloxp/loxp/Pf4-Cre+)简称Plt-Metrnl-/-小鼠,具体构建策略如图1A所示。
Metrnlloxp/loxp小鼠是前期构建而成,该小鼠Metrnl基因的3号外显子两侧和4号外显子编码区的都插有同向LoxP位点(即图1A中所示“等位基因”),可基于Cre-LoxP系统在Cre酶的作用下,将LoxP位点之间的序列切除(图1A)[12]。
Pf4-Cre小鼠是由Pf4基因启动子Cre重组酶在巨核细胞及血小板谱系表达的工具鼠,最初开发用于研究APC-Wnt调节途径在巨核细胞生成和血小板产生中的作用,其Cre重组酶的表达受巨核细胞特异性受体Pf4基因的启动子介导,在巨核细胞的成熟Ⅰ期(最早可识别形态期)中即开始发生转录激活,之后广泛表达于成熟的血小板[22, 23]。
将Metrnlloxp/loxp小鼠和Pf4-Cre小鼠进行交配繁殖,巨核细胞特异性表达的Cre酶可将Metrnl同向LoxP位点之间的序列切除,以达到在巨核细胞及血小板谱系特异性敲除Metrnl基因的目的,具体构建繁殖流程如图1B所示,最终可以获得Plt-Metrnl-/-小鼠及其对照小鼠(WT)。
繁殖过程中进行基因型鉴定时,需确认Metrnlloxp基因和Pf4-Cre基因的表达情况。采用相应基因上下游引物分别进行鼠尾基因型鉴定,Metrnlloxp突变型基因阳性条带为243bp,对应野生型序列条带为131bp,Pf4-Cre基因阳性条带为420bp,内参基因阳性条带为200bp。对培育繁殖过程中的母代及子代小鼠均进行了基因型鉴定,如图1C、D、E中DNA电泳条带图所示:图1C中泳道1、2为母代Metrnlloxp/loxp小鼠,泳道3、4为母代Pf4-Cre小鼠;图1D中泳道1、2为Metrnlloxp/WT小鼠,泳道3、4为Metrnlloxp/WT/Pf4-Cre+小鼠;图1E泳道1、2、4为Plt-Metrnl-/-小鼠,泳道3、5、6为WT小鼠。
2.2 血小板特异性Metrnl敲除小鼠血小板蛋白表达情况
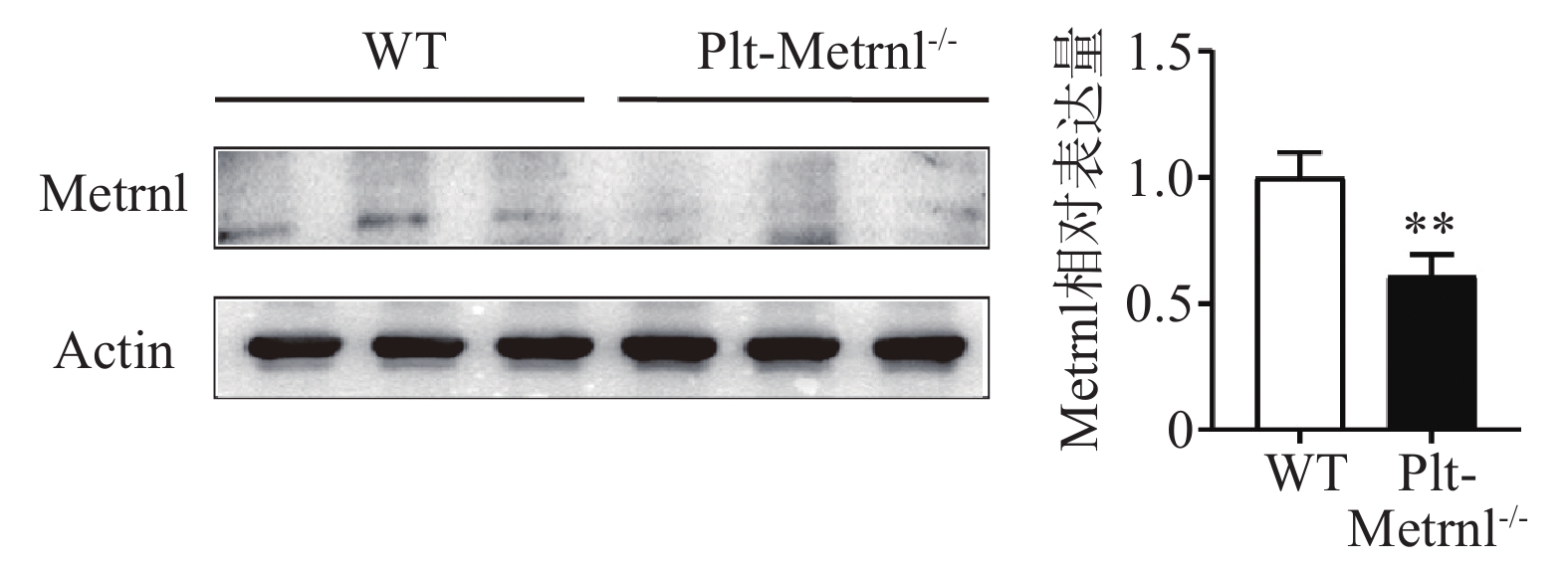
为验证血小板特异性Metrnl敲除小鼠是否实现血小板特异性Metrnl基因敲除,分别提取Plt-Metrnl-/-小鼠及对照WT小鼠血小板蛋白,使用蛋白免疫印迹实验方法验证敲除情况,结果如图2所示,Plt-Metrnl-/-小鼠血小板蛋白Metrnl表达较对照WT小鼠明显降低,提示Plt-Metrnl-/-小鼠血小板Metrnl成功敲除。
2.3 血小板特异性Metrnl敲除小鼠各组织Metrnl mRNA及蛋白表达情况
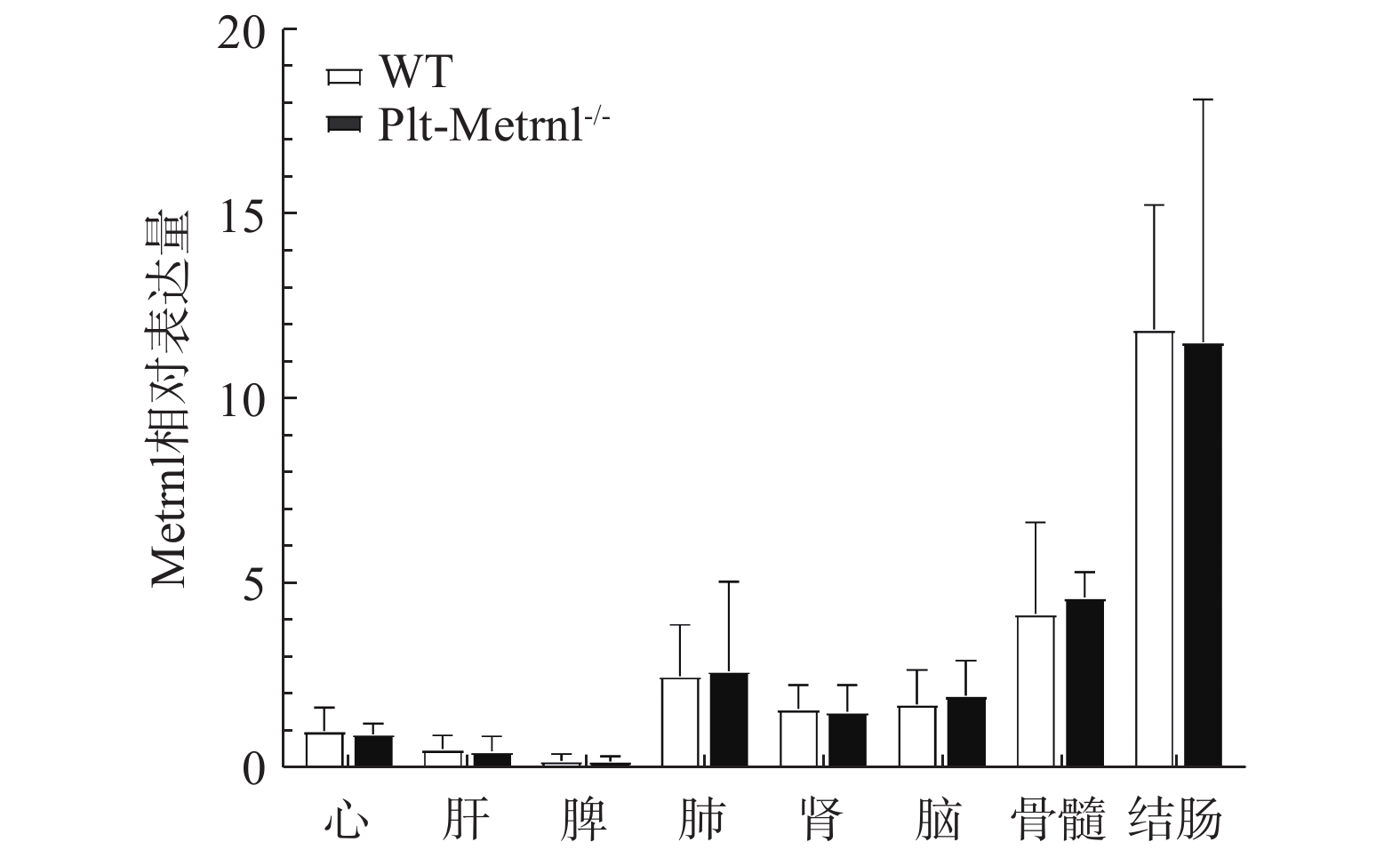
为验证血小板特异性Metrnl敲除小鼠是否存在其他组织非特异性敲除,本研究首先利用实时荧光定量PCR技术检测了该小鼠各组织中Metrnl mRNA的表达情况。如图3所示,以WT对照小鼠的心脏Metrnl mRNA表达量为1,Plt-Metrnl-/-小鼠在心、肝、脾、肺、肾、脑、结肠、骨髓组织mRNA水平上并未存在显著差异。该结果说明,血小板特异性Metrnl基因敲除小鼠在组织mRNA水平上并未发生其他组织非特异性敲除。
然后,本研究提取血细胞及各组织的蛋白,使用蛋白免疫印迹实验方法验证Plt-Metrnl-/-小鼠各血细胞及组织中Metrnl蛋白表达情况。如图4所示,并未发现Metrnl蛋白在Plt-Metrnl-/-小鼠和对照WT小鼠各组织中存在显著差异,该结果提示,Plt-Metrnl-/-小鼠在其他血细胞蛋白水平及各组织蛋白水平上并未发生非特异性敲除。
2.4 血小板特异性Metrnl敲除小鼠外周血常规指标情况
分别对Plt-Metrnl-/-小鼠及对照WT小鼠外周血进行血常规指标检测,结果如表3所示,外周血血常规计数红细胞、白细胞、血小板数量未见明显改变,血小板大小及分布未见显著差异,提示血小板特异性敲除Metrnl后不影响外周血细胞数量,且对血小板形态没有明显影响。
表 3 Plt-Metrnl-/-小鼠及对照WT小鼠血常规指标对比(n=6)血常规检验项目 WT Plt-Metrnl-/- 白细胞计数(109/L) 2.10±0.50 2.25±0.30 淋巴细胞计数(109/L) 1.28±0.20 1.52±0.20 淋巴细胞比率(%) 63±3 68±3 嗜酸性粒细胞计数(109/L) 0.10±0.05 0.05±0.02 嗜酸性粒细胞比率(%) 3.0±1.8 1.0±0.3 其他细胞计数(109/L) 0.72±0.20 0.68±0.10 其他细胞比率(%) 34.0±3.3 31±3 红细胞计数(1012/L) 8.49±0.40 7.83±0.40 血红蛋白(g/L) 122.0±5.5 113.0±4.6 红细胞压积(%) 42±2 37±2 平均红细胞体积(fL) 49.1±0.8 47.7±0.9 平均血红蛋白含量(pg) 14.30±0.08 14.5±0.1 平均血红蛋白浓度(g/L) 292±5 304.0±7.7 红细胞分布宽度-SD(fL) 27.6±0.4 26.2±0.6 红细胞分布宽度-CV(%) 13.2±0.4 12.4±0.3 血小板计数(109/L) 1121 ±581049 ±132血小板平均宽度(fL) 6.7±0.4 6.1±0.1 平均血小板体积(fL) 6.20±0.26 5.80±0.08 大型血小板比率(%) 1.9±1.0 3.5±0.3 2.5 血小板特异性Metrnl敲除小鼠一般繁殖情况
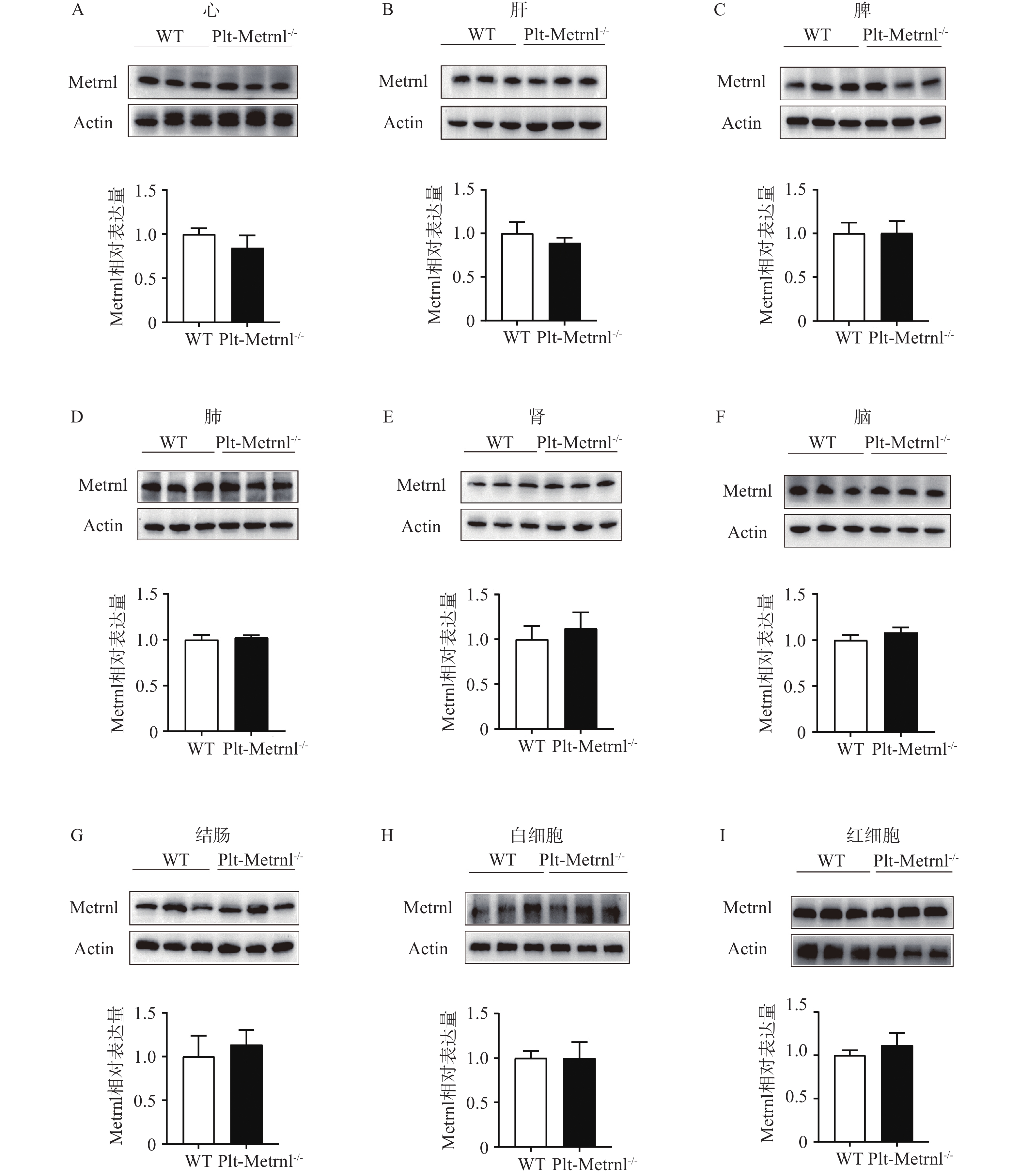
Metrnlloxp/loxp/Pf4-Cre+(Plt-Metrnl-/-)小鼠和对照WT小鼠为首次繁殖培育的转基因动物,在生理状态下,血小板Metrnl缺失是否影响动物繁殖情况尚未见报道,因此,本研究统计记录了小鼠基因型分布情况。Plt-Metrnl-/-小鼠扩大繁殖流程如图5A所示,按照遗传学规律,Metrnlloxp/loxp/Pf4-Cre+(Plt-Metrnl-/-)小鼠和Metrnlloxp/loxp小鼠杂交繁殖获得子代鼠中Plt-Metrnl-/-小鼠和WT小鼠的比例应为1∶1。如图5B、5C所示,对繁殖过程中所获得的16窝次共计130只目的鼠进行统计,Plt-Metrnl-/-小鼠共有67只,其中雄鼠31只,雌鼠36只;WT小鼠共有63只,其中雄鼠37只,雌鼠26只。结果表明繁殖鼠遗传规律基本符合预期,无明显差异,提示血小板特异性敲除Metrnl对小鼠胚胎发育和性别比例无明显影响。
3. 讨论与总结
Cre-LoxP重组酶系统主要用于构建条件性基因敲除小鼠模型,是当前阐释基因功能的最直接的方式之一。Pf4-Cre工具鼠长期以来应用于巨核谱系基因敲除动物的构建,虽然有研究表明Pf4-Cre表达不仅限于巨核细胞/血小板谱系,也表达于其他骨髓造血干细胞以及远端肠道的上皮细胞中,但是该小鼠目前仍是巨核细胞谱系遗传修饰的最佳工具,且不影响血小板和血栓形成功能的考察[22-24]。因此本研究利用Pf4-Cre工具鼠和实验室前期构建的Metrnlloxp/loxp小鼠进行杂交繁殖,最终获得血小板特异性Metrnl敲除小鼠,即Plt-Metrnl-/-小鼠。
本研究从mRNA水平、组织蛋白水平、外周血常规水平考察了Plt-Metrnl-/-小鼠血小板Metrnl敲除的情况。本研究结果显示,Plt-Metrnl-/-小鼠血小板Metrnl蛋白表达较对照WT小鼠减低约50%,可能是由于本实验室前期构建的Metrnlloxp/loxp小鼠插入的loxp序列位点在3、4号外显子,因此Pf4-Cre仅介导3、4号外显子间的同向基因序列切除,并未实现Metrnl基因全长敲除。另外,血小板是骨髓巨核细胞分化形成的“细胞碎片”,由于无法获得原代骨髓巨核细胞,本研究并未对骨髓巨核细胞的Metrnl敲除情况进行验证,未证实Metrnl敲除是否会对骨髓巨核细胞的生成和形态产生影响,仅从血常规计数中初步得知血小板的生成未受到明显影响。Metrnl与骨髓巨核细胞之间的关系也可作为下一步的研究方向。
在小鼠培育的过程中,尚未发现Plt-Metrnl-/-小鼠和同窝对照WT小鼠在体重、形态等方面的差异。基于孟德尔遗传定律,Plt-Metrnl-/-小鼠和Metrnlloxp/loxp小鼠杂交进行扩大繁殖和保种的得率也接近50%,说明血小板Metrnl缺失不影响小鼠繁殖情况。
前期本课题组已证实Metrnl全身敲除小鼠血栓形成能力增强,血小板活性明显增强,构建Plt-Metrnl-/-小鼠可考虑用于血小板内源性Metrnl与血小板功能相关性的研究,并且该小鼠可与Metrnl全身敲除小鼠进行血栓形成能力比较,比较全身Metrnl和局部血小板Metrnl的作用,深入研究其作用方式及机制,为血栓性疾病的防治提供新靶点。
-
表 1 梯度洗脱信息
时间(t/min) A(%) B(%) 0~1.5 85 15 1.5~4.5 30 70 4.5~5.5 10 90 5.5~12 85 15 表 2 丙戊酸钠和万古霉素的精密度与准确度(
$ \overline{\text{x}}\text{±}\text{s} $ ,n=5)分析物 浓度值(μg/ml) 准确度
(%)精密度RSD(%) 标示浓度 实测浓度 批内(n=5) 批间(n=15) 丙戊酸钠 2 2.06±0.09 102.78 0.87 5.05 10 9.27±0.32 92.67 0.21 3.71 100 99.55±1.99 99.54 0.23 2.15 万古霉素 1 1.07±0.09 106.87 7.54 9.93 5 5.03±0.13 100.69 1.07 2.86 50 50.64±2.49 101.28 3.54 5.32 表 3 丙戊酸钠和万古霉素的基质效应与提取回收率(
$ \overline{\text{x}}\text{±}\text{s} $ ,n=5)分析物 标示浓度
(μg/ml)基质效应
(%)RSD
(%)提取回收率 RSD
(%)丙戊酸钠 2 106.60±2.95 2.77 78.23±5.39 6.89 10 92.63±2.69 2.91 73.76±3.58 4.85 100 92.82±1.59 1.72 75.83±3.53 4.66 万古霉素 1 96.90±1.88 1.94 71.62±7.99 11.16 5 99.07±1.79 1.80 73.08±4.99 6.82 50 99.19±0.84 0.85 71.23±4.87 6.84 表 4 丙戊酸钠和万古霉素的稳定性(
$ \overline{\text{x}}\text{±}\text{s} $ ,n=5)分析物 标示浓度
(μg/ml)25 ℃放置24 h 4 ℃放置24 h 反复冻融3次 -80 ℃冻存30 d 实测浓度(μg/ml) RSD(%) 实测浓度(μg/ml) RSD(%) 实测浓度(μg/ml) RSD(%) 实测浓度(μg/ml) RSD(%) 丙戊酸钠 2 2.16±0.14 6.55 1.86±4.73 7.38 1.77±0.18 10.23 1.83±0.12 6.34 10 10.71±0.38 3.56 10.18±0.37 4.32 8.97±0.69 7.72 9.49±0.64 6.79 100 104.30±1.50 1.44 107.40±2.70 2.48 91.63±10.81 11.79 88.58±4.91 5.55 万古霉素 1 1.20±0.07 5.62 1.04±0.05 9.11 0.96±0.13 13.37 0.84±0.08 9.39 5 5.43±0.31 5.63 5.03±0.25 6.51 4.78±0.43 9.06 4.59±0.34 7.51 50 52.72±2.70 5.12 46.26±0.78 7.85 44.69±3.69 8.26 44.57±3.22 7.23 -
[1] VEZZANI A, FUJINAMI R S, WHITE H S, et al. Infections, inflammation and epilepsy[J]. Acta Neuropathol,2016,131(2):211-234. doi: 10.1007/s00401-015-1481-5 [2] 周婷, 蔡建, 段晶晶, 等. 丙戊酸钠用药差错致肝损伤: 病例分析[J]. 药学实践杂志, 2019, 37(5):466-469. doi: 10.3969/j.issn.1006-0111.2019.05.016 [3] 周浔, 陈顺, 宗传峰, 等. 丙戊酸钠及其代谢产物与肝损伤的相关性分析[J]. 药学实践杂志, 2020, 38(3):273-276. doi: 10.12206/j.issn.1006-0111.201910080 [4] 万古霉素临床应用中国专家共识(2011版)[J]. 中国新药与临床杂志, 2011, 30(8): 561-573. [5] CASS R T, VILLA J S, KARR D E, et al. Rapid bioanalysis of vancomycin in serum and urine by high-performance liquid chromatography tandem mass spectrometry using on-line sample extraction and parallel analytical columns[J]. Rapid Commun Mass Spectrom,2001,15(6):406-412. doi: 10.1002/rcm.246 [6] OYAERT M, PEERSMAN N, KIEFFER D, et al. Novel LC-MS/MS method for plasma vancomycin: comparison with immunoassays and clinical impact[J]. Clin Chim Acta,2015,441:63-70. doi: 10.1016/j.cca.2014.12.012 [7] WEN D, CHEN Z, YANG C, et al. A rapid and simple HPLC-MS/MS method for the simultaneous quantification of valproic acid and its five metabolites in human plasma and application to study pharmacokinetic interaction in Chinese epilepsy pati-ents[J]. J Pharm Biomed Anal,2018,149:448-456. doi: 10.1016/j.jpba.2017.11.042 [8] CHENG H, LIU Z, BLUM W, et al. Quantification of valproic acid and its metabolite 2-propyl-4-pentenoic acid in human plasma using HPLC-MS/MS[J]. J Chromatogr B Analyt Technol Biomed Life Sci,2007,850(1-2):206-212. doi: 10.1016/j.jchromb.2006.11.027 -





 下载:
下载:
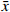
 下载:
下载:





