-
河豚毒素是一种钠通道阻滞剂,可以导致人类中毒和死亡[1]。河豚毒素不仅存在于河豚科的河豚中,而且在海洋和陆地环境的多种生物中均有发现[2-4]。河豚毒素作用时具有选择性,其与心肌NaV通道缺乏亲和力,且无法穿透血脑屏障,这些特性使其成为麻醉和镇痛药物设计的有吸引力的候选者[5]。河豚毒素的毒理作用在神经性、急性和炎症性疼痛模型中得到证实[6-8]。在远低于半数致死剂量(LD50)的浓度下,河豚毒素对神经系统的急性和瞬时作用使其在最低浓度时即可达到预期结果[9]。然而,河豚毒素的高毒性引发人们对其安全性问题的关注,本文利用斑马鱼模型研究河豚毒素的急性毒性,旨在为评价河豚毒素的安全性提供依据。
-
河豚毒素[中洋生物科技(上海)股份有限公司,批号:2020102307],用醋酸盐缓冲液配制成10.0 mmol/L母液,冷藏避光储存。斑马鱼饲养于28 ℃的养鱼用水中(水质:每1 L反渗透水中加入200 mg速溶海盐,电导率为450~550 μS/cm,pH为6.5~8.5,硬度为50~100 mg/L CaCO3),由杭州环特生物科技股份有限公司养鱼中心繁殖提供,实验动物使用许可证号为:SYXK(浙)2012-0171,饲养管理符合国际AAALAC认证(编号:001458)的要求。野生型AB品系斑马鱼,以自然成对交配繁殖方式进行,年龄为受精后2 d(2 dpf)。
-
随机选取2 dpf野生型AB品系斑马鱼于6孔板中,每孔(实验组)均处理30尾斑马鱼。分别水溶给予河豚毒素(浓度为0.125、0.250、0.500、1.00、2.00、4.00、8.00、16.0、32.0、64.0 µmol/L),同时设置正常对照组和溶剂对照组,每孔容量为3 ml。28 ℃处理72 h,每天统计各实验组的斑马鱼死亡数量并及时移除。
-
实验结束后,在解剖显微镜下观察并记录斑马鱼心脏、循环系统、出血及血栓、脑、下颌、眼睛、肝脏、肾脏、肠道、躯干/尾/脊索、肌肉/体节、身体着色、体长等变化情况,采集典型毒性器官照片。以各器官的毒性发生率评价河豚毒素样品对斑马鱼的急性毒性,并鉴别毒性靶器官。
-
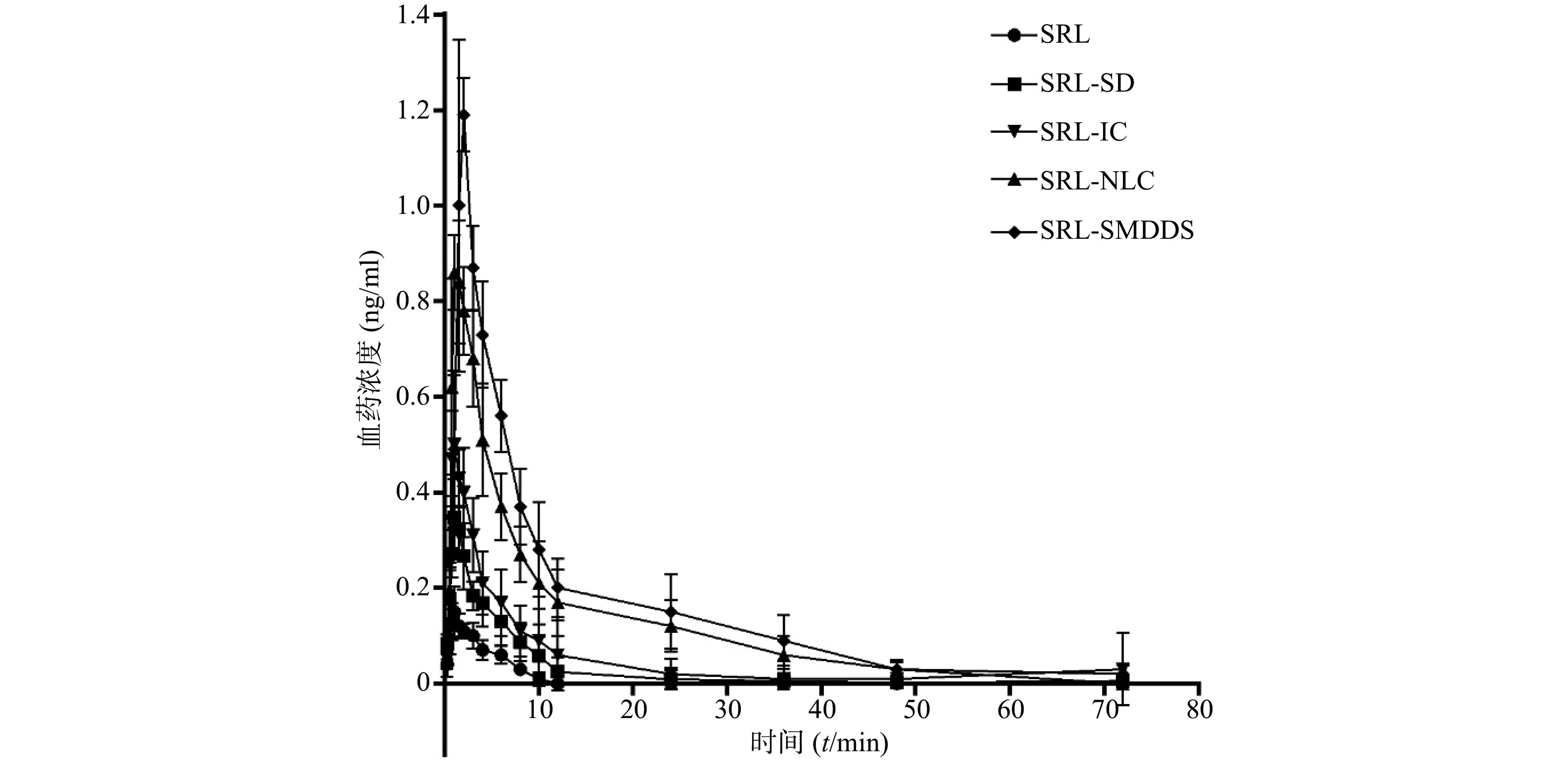
用Origin 8.0统计学软件绘制“浓度-死亡率”效应曲线,并计算河豚毒素对斑马鱼的MNLC和LC10。
-
研究结果显示,正常对照组和溶剂对照组斑马鱼的死亡率均为0;0.125~8.00 µmol/L的河豚毒素处理后斑马鱼的死亡率均为0;当河豚毒素的浓度达到16.0 µmol/L时,斑马鱼死亡4尾,死亡率为13%,当河豚毒素的浓度达到32.0 µmol/L时,斑马鱼死亡29尾,死亡率为97%,而当河豚毒素的浓度达到64.0µmol/L时,斑马鱼死亡30尾,死亡率为100%。经Origin 8.0软件模拟得出河豚毒素对斑马鱼急性毒性MNLC为8.62 μmol/L,LC10为15.2 µmol/L,详见图1。
-
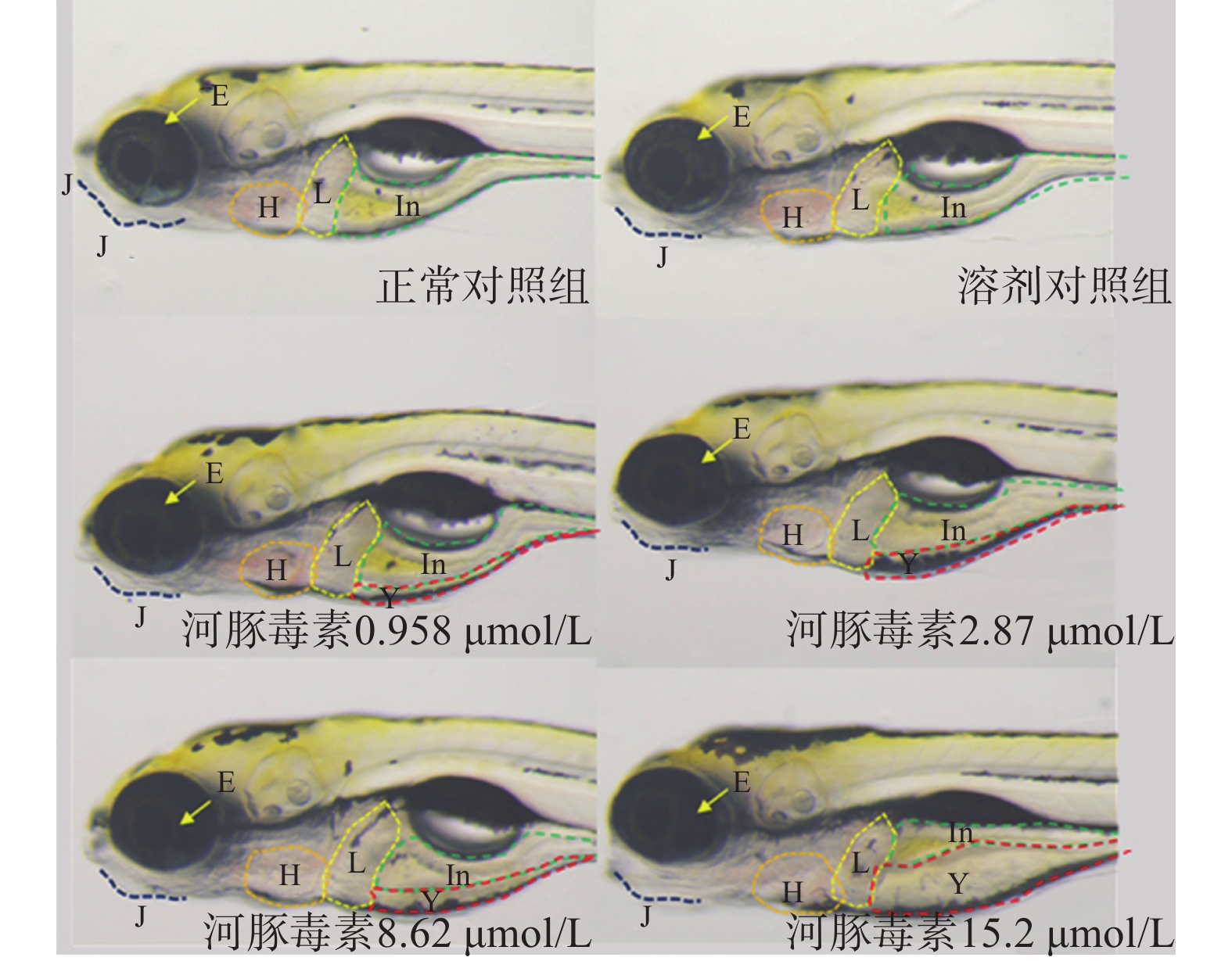
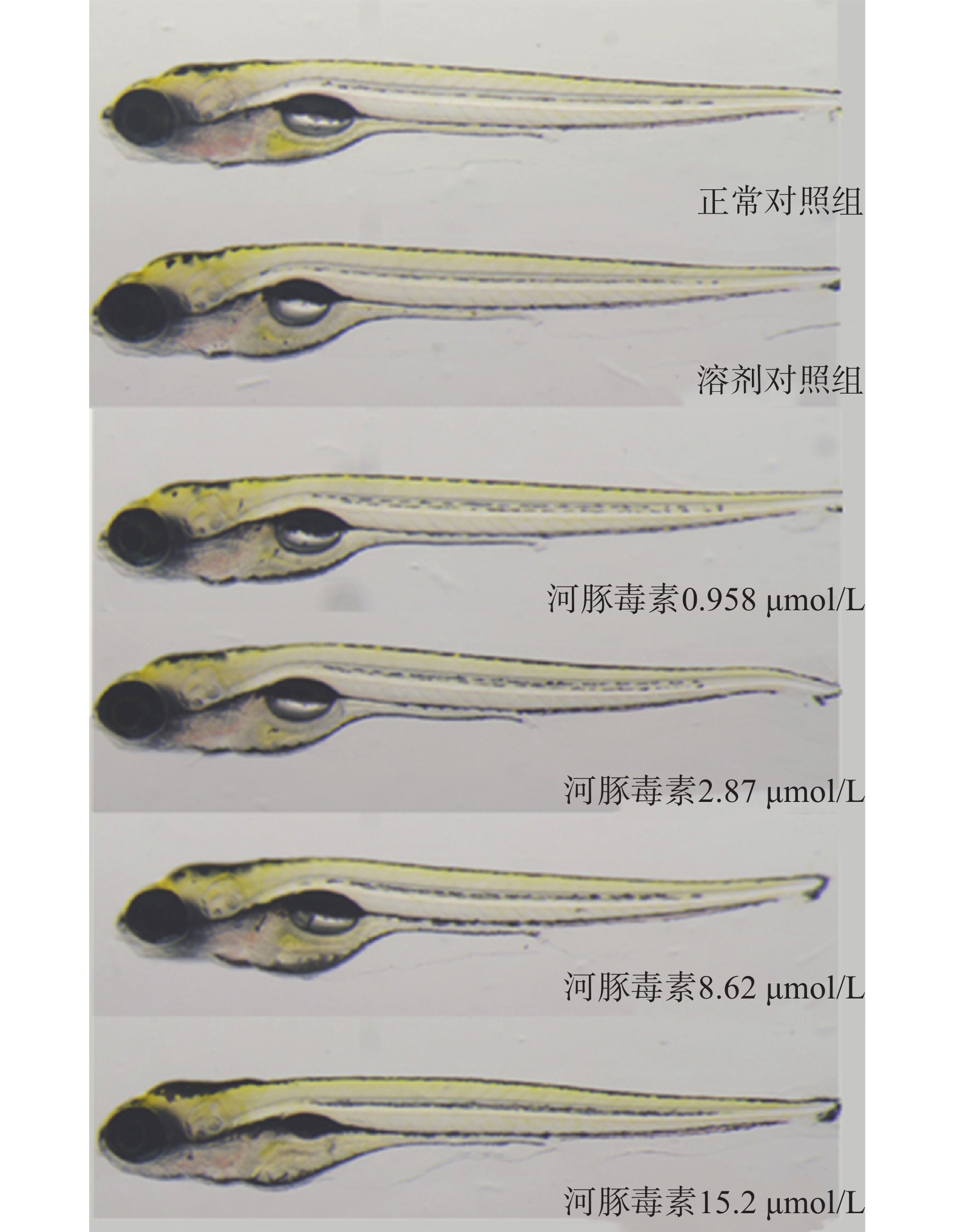
在本实验条件下浓度摸索过程中,16.0 μmol/L及以上浓度诱发心包水肿和心律异常,河豚毒素处理后72 h出现部分或全部死亡。如表1和图2、图3所示,河豚毒素急性毒性靶器官是心脏和肝脏,当河豚毒素的浓度达到0.958 µmol/L及以上时,斑马鱼表现出卵黄囊吸收延迟。当河豚毒素的浓度达到2.87 µmol/L及以上时斑马鱼表现出心律异常和肠腔异常。当河豚毒素浓度达到8.62 µmol/L及以上时斑马鱼表现出心包水肿。不同浓度的河豚毒素均未发现躯干/尾/脊索、肌肉/体节、身体着色以及体长生长等异常。
表 1 河豚毒素急性毒性发生率统计(n=30)
毒性类型 正常对照组 溶剂对照组 河豚毒素浓度(μmol/L) 0.958 2.87 8.62 15.2 心脏 心包水肿 - - - - 7(2/30) 13(4/30) 房室缺失 - - - - - - 心律异常 - - - 7(2/30) 7(2/30) 17(5/30) 循环系统 血流变慢 - - - - - - 循环缺失 - - - - - - 出血及血栓 - - - - - - 脑 畸形 - - - - - - 下颌 短小 - - - - - - 眼睛 眼变小 - - - - - - 肝脏 缺失 - - - - - - 肝肿大 - - - - - - 肝变性 - - - - - - 卵黄囊吸收延迟 - - 80(24/30) 80(24/30) 87(26/30) 93(28/30) 肾脏 水肿 - - - - - - 肠道 肠腔异常 - - - 7(2/30) 13(4/30) 13(4/30) 躯干/尾/脊索 弯曲 - - - - - - 肌肉/体节 肌肉变性 - - - - - - 身体着色 异常 - - - - - - 体长变短 - - - - - 死亡 - - - - - 注:“-”表示未见明显异常 -
河豚毒素是一种致命的神经毒素,作为一种选择性Na+通道阻滞剂,其在生物医学中的应用引起了广泛关注[10]。日本传统医学中曾使用河豚鱼来治疗麻风病患者的神经痛,后来河豚毒素被发现、提取和纯化,并用于抑制破伤风患者的痉挛[11]。近年来,在双壳贝类中也发现了河豚毒素。例如,2011年在新西兰发现一种蛤类中的河豚毒素(0.8 mg/kg)[12],2014年英国学者发现贻贝和太平洋牡蛎样本中的河豚毒素(0.003~0.12 mg/kg)[13]。这些证据表明,河豚毒素对于食品安全来说具有一定的威胁,因此,国际食品和药品监管机构将河豚毒素作为一种新的风险。
在本研究中我们通过使用MNLC和LC10这两个指标,以评估河豚毒素对斑马鱼的急性毒性。研究发现,当河豚毒素的浓度达到16.0 μmol/L时,斑马鱼出现了心包水肿和心律异常,导致部分或者全部的斑马鱼死亡。有研究证实,选择性激活河豚毒素敏感的神经元钠通道可以安全地增加心脏收缩力[14]。还有研究结果显示,河豚毒素的肌肉内给药改变了肝脏中参与各种信号通路的肝脏基因的表达[15]。由此可见,河豚毒素对斑马鱼具有明显的心脏和肝脏毒性,且其毒性随着河豚毒素浓度的升高而增强。
目前,尚无针对河豚毒素的解毒剂,一旦摄入河豚毒素,严重中毒者可发生心力衰竭甚至死亡[16]。多年前有研究者收治了5例河豚毒素中毒者,患者出现了肾脏损害,表现为多尿,经过治疗后仍有患者死亡[17]。在日本,监管规定了河豚毒素的摄入浓度不得超过2 mg/kg[11]。目前,关于河豚毒素急性毒性的可用数据非常少,而且现有的大部分数据都缺乏足够的实验细节。有研究者发现,在昆明小鼠腹膜内(ip)、皮下(sc)和胃内(ig)注射的中位致死剂量(LD50)分别为10.7、12.5、532 μg/kg[18]。我们在斑马鱼模型中研究发现,河豚毒素对斑马鱼急性毒性MNLC为8.62 μmol/L,LC10为15.2 µmol/L,急性毒性靶器官是心脏和肝脏,主要表现为心包水肿、心律异常和卵黄囊吸收延迟,毒性出现浓度为0.958 µmol/L。
本研究还存在一定的不足。作为一种常用于药物毒性评价的模式生物,斑马鱼具有易养殖、繁殖快、成本低等优势,但斑马鱼被用于药物毒性检测时易存在假阳性和假阴性。因此,本研究的结论还需要在其他动物模型中进一步研究。
The acute toxicity of tetrodotoxin to zebra fish
-
摘要:
目的 研究河豚毒素对斑马鱼的急性毒性。 方法 在斑马鱼中用最大非致死浓度(MNLC)和10%致死浓度(LC10)测定和评估河豚毒素的急性毒性。 结果 经Origin 8.0软件模拟,得出河豚毒素对斑马鱼急性毒性MNLC为8.62 μmol/L,LC10为15.2 μmol/L。在本实验条件下,16.0 μmol/L及以上浓度河豚毒素可诱发斑马鱼心包水肿和心律异常,终点时出现部分或全部死亡。河豚毒素的急性毒性靶器官是心脏和肝脏,主要表现为心包水肿、心律异常和卵黄囊吸收延迟,毒性出现浓度为0.958 μmol/L。 结论 河豚毒素对斑马鱼具有一定的心脏和肝脏毒性,且其毒性与河豚毒素的浓度相关。 Abstract:Objective To study the acute toxicity of tetrodotoxin to zebra fish. Methods The maximum non-lethal concentration (MNLC) and 10% lethal concentration (LC10) determinations were used to assess the acute toxicity of tetrodotoxin. Results According to the simulation calculation of Origin 8.0 software, the MNLC was 8.62 µmol/L and 15.2 µmol/L for LC10. Under the experimental conditions, tetrodotoxin at a concentration of 16.0 µmol/L and above induced pericardial edema and arrhythmia, leading to the death of zebra fish. The target organs for acute toxicity of tetrodotoxin were the heart and liver. The main manifestations were pericardial edema, arrhythmia, and delayed yolk sac absorption. The toxicity appeared at a concentration of 0.958 µmol/L. Conclusion Tetrodotoxin has heart and liver toxicity to zebra fish, and its toxicity is dose-dependent. -
Key words:
- tetrodotoxin /
- zebra fish /
- acute toxicity
-
西罗莫司(sirolimus,SRL),又称雷帕霉素,是第三代免疫抑制剂,在临床上常用于抑制肝、肾等器官移植后的免疫排斥反应。SRL属于生物药剂学分类Ⅱ类药物,在水中的溶解度极低,而渗透性良好[1-4]。SRL药理活性高,但因水溶性差,且易被肠壁和肝中的CYP3A4同工酶广泛代谢,致使其口服生物利用度较低。这是临床应用SRL的重要缺陷之一。目前,已上市的SRL制剂主要是纳米结晶片,生物利用度约为17%[5-7]。
通过适当的制剂技术提高SRL在胃肠道中的溶解度,可提高其口服生物利用度。在前期研究中,课题组分别独立进行了含SRL的自微乳(self-microemulsifying drug delivery system,SMEDDS)、固体分散体(solid dispersion,SD)和纳米结构脂质载体(nanostructured lipid carriers,NLC)的构建,均显著改善了SRL的体外溶出。本实验在前期研究的基础上,新增环糊精衍生物对SRL的增溶研究,结合体外溶出度和体内生物利用度,综合分析和评价各增溶制剂的优势和缺陷,从而为解决口服难溶性药物的研究提供参考。
1. 仪器与试剂
1.1 仪器
Agilent 1200型高效液相色谱仪(美国Agilent公司);Starter 2C型pH计(上海奥豪斯仪器公司);RCZ-6BZ型药物溶出仪(上海黄海药检仪器公司);真空冷冻干燥箱(北京博医康试验仪器公司);NS1001L2K高压匀质机(意大利NiroSoavi公司);UV-2800AH型紫外可见分光光度仪(上海优尼科仪器有限公司);液相色谱-质谱联用仪(美国AB-SCIEX有限公司)。
1.2 试剂
SRL对照品(含量99.9%)、SRL原料药(含量99.6%),购自福建科瑞药业有限公司;子囊霉素对照品(上海齐奥化工科技有限公司),Rapamune®(美国惠氏制药)。聚乙二醇6000(PEG 6000)、聚乙烯吡咯烷酮(PVP K30)均购自国药集团化学试剂有限公司;聚氧乙烯-聚氧丙烯共聚物(Poloxamer 188)、聚氧乙烯35蓖麻油(Cremophor EL)、聚氧乙烯氢化蓖麻油(Cremophor RH40)均购自德国BASF公司;油酸聚乙二醇甘油酯(Labrafil M1944CS)、二乙二醇单乙基醚(Transcutol P)、辛酸癸酸聚乙二醇甘油酯(Labrasol)、棕榈酸硬脂酸甘油酯(Precirol ATO5)、月桂酸聚乙二醇甘油酯 (Gelucire 44/14)均购自法国GATTEFOSSE公司;HP-β-CD、DM-β-CD、SBE-β-CD(山东滨州智源生物科技有限公司)。
2. 方法
2.1 SRL含量测定方法
采用高效液相色谱仪(HPLC)测定样品中的SRL含量[8]。色谱柱为Eclipse XDB-C18(150 mm×4.6 mm,5 μm),流动相为乙腈-甲醇-水(45∶34∶21),流速为1 ml/min,检测波长为278 nm,柱温为50 ℃,进样量为20 μl。配制浓度为2、4、8、12、16、20 μg/ml的SRL对照品溶液,得标准曲线为Y=54.712X+1.221,r=0.999 9,表明在2~20 μg/ml浓度范围内线性关系良好。另外,精密度、回收率符合要求。
2.2 SRL增溶方法
2.2.1 SRL-SMEDDS的制备
参考前期研究[9],称取1 g SRL原料药,加入19 g的助乳化剂Transcutol HP,超声至全部溶解后,加入22 g油相Labrafil M1944CS及39 g乳化剂Cremophor EL,涡旋混匀,得到淡黄色澄清溶液,即SRL-SMEDDS。
2.2.2 SRL-NLC的制备
参考前期研究[10-11],取Gelucire44/14和Crodamol GTCC在75 ℃水浴中完全熔融后,加入SRL原料药搅拌均匀成澄明油相,再将同温度吐温−80的水溶液迅速倒入油相,以300 r/min搅拌30 min制备初乳,再经高压匀质机90 MPa乳匀5次,即得SRL-NLC分散液,其中SRL为0.21%,Gelucire44/14:Crodamol GTCC(1∶2.1),脂质总量为10%,吐温−80为7.33%。随后,将SRL-NLC(42.6%)加入微晶纤维素和聚乙烯吡咯烷酮(50%,4∶1)中,研磨混合并放置过夜以充分吸附,加入甘露醇(冻干保护剂,3%),经冷冻干燥过夜后,所得固体粉末中加入低取代羟丙基纤维素(崩解剂,4%)和二氧化硅(助流剂,0.4%)即得固化纳米脂质体。
2.2.3 SRL-SD的制备
采用溶剂-熔融法制备SRL-SD。称取载体材料,于80 ℃水浴加热熔融,滴入SRL乙醇溶液,充分混匀,待乙醇挥发完全后,迅速将其倾倒于冰浴条件下的不锈钢板上成薄膜,固化,再于−18 ℃放置4 h后,将固体分散体从不锈钢板上刮下,置真空干燥器中干燥,待脆化后研细,过80目筛,即得SRL-SD。以载体种类、药物-载体比例为考察因素,以0.4% SDS中的溶出度为指标,对SRL-SD进行单因素分析。
2.2.4 SRL-IC的制备
称取适量β-环糊精衍生物溶于去离子水中,缓慢滴加SRL乙醇溶液,在一定温度下磁力搅拌至澄清透明,减压挥发4 h,使乙醇挥发完全,再置于4 ℃冰箱冷藏12 h,降低SRL的溶解度,从而使游离的SRL发生结晶。经0.22 μm微孔滤膜过滤除去结晶,滤液冷冻干燥24 h,所得固体研磨细化,过80目筛,即得SRL-IC。
称取一定量的SRL-IC置10 ml容量瓶中,加入50%甲醇水溶液,超声至全部溶解后,定容至刻度,并采用HPLC测定SRL含量,根据公式:包封率(%)=[(SRL投入量-SRL测定量)/ SRL投入量]×100%,进行计算。以环糊精衍生物的种类、浓度、温度、乙醇体积和投药量为考察因素,以包封率为指标,对SRL-IC进行单因素分析。
2.3 体外溶出试验
参考《中国药典》2015年版四部通则0931项下溶出度与释放度测定法,考察SRL原料药、市售片(Rapamune®)、SRL-SMEDDS、SRL-NLC、SRL-IC及SRL-SD的溶出曲线。除市售片外,其余样品均装入硬胶囊中,每个胶囊含1 mg SRL。采用桨法,搅拌速度为100 r/min,溶出介质体积为250 ml,分别以0.4% SDS、水、pH 1.2盐酸溶液、pH 4.5醋酸盐缓冲液、pH 6.8磷酸盐缓冲液、pH 7.4磷酸盐缓冲液为溶出介质。将两颗胶囊或药片置于沉降篮中,投入溶出介质,在10、30、45、60、90、120 min,吸取2 ml介质,并补充等温等体积的介质,采用HPLC测定样品中的药物含量,绘制溶出曲线。
2.4 体内药代动力学试验
选用比格犬为实验动物,采用6周期6交叉实验设计,进行SRL原料药、市售片(Rapamune®)、SRL-SMEDDS、SRL-NLC、SRL-IC及SRL-SD的药代动力学试验。给药剂量为1 mg SRL,实验动物试验开始前12 h禁食不禁水,给药4 h后自由饮水,2次给药间隔2周以上的清洗期。于给药前,0.25、0.5、0.75、1、1.5、2、3、4、6、8、10、12、24、36、48及72 h分别经前肢小静脉采血2 ml,置于含肝素和EDTA的抗凝管中,−20 ℃保存备用。血样处理与测定方法参照课题组前期研究[12]。
3. 结果
3.1 SRL-SD的制备
3.1.1 载体种类
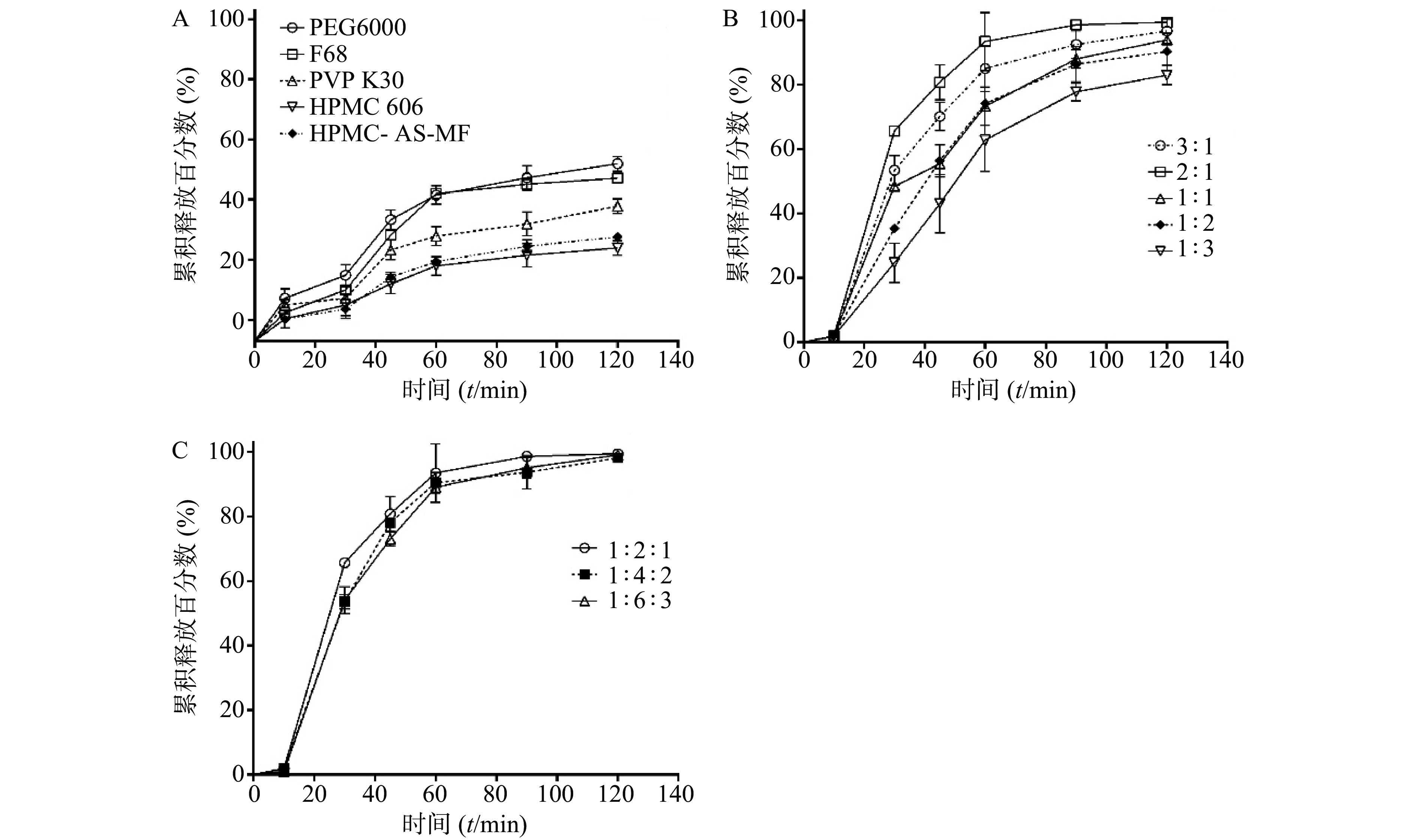
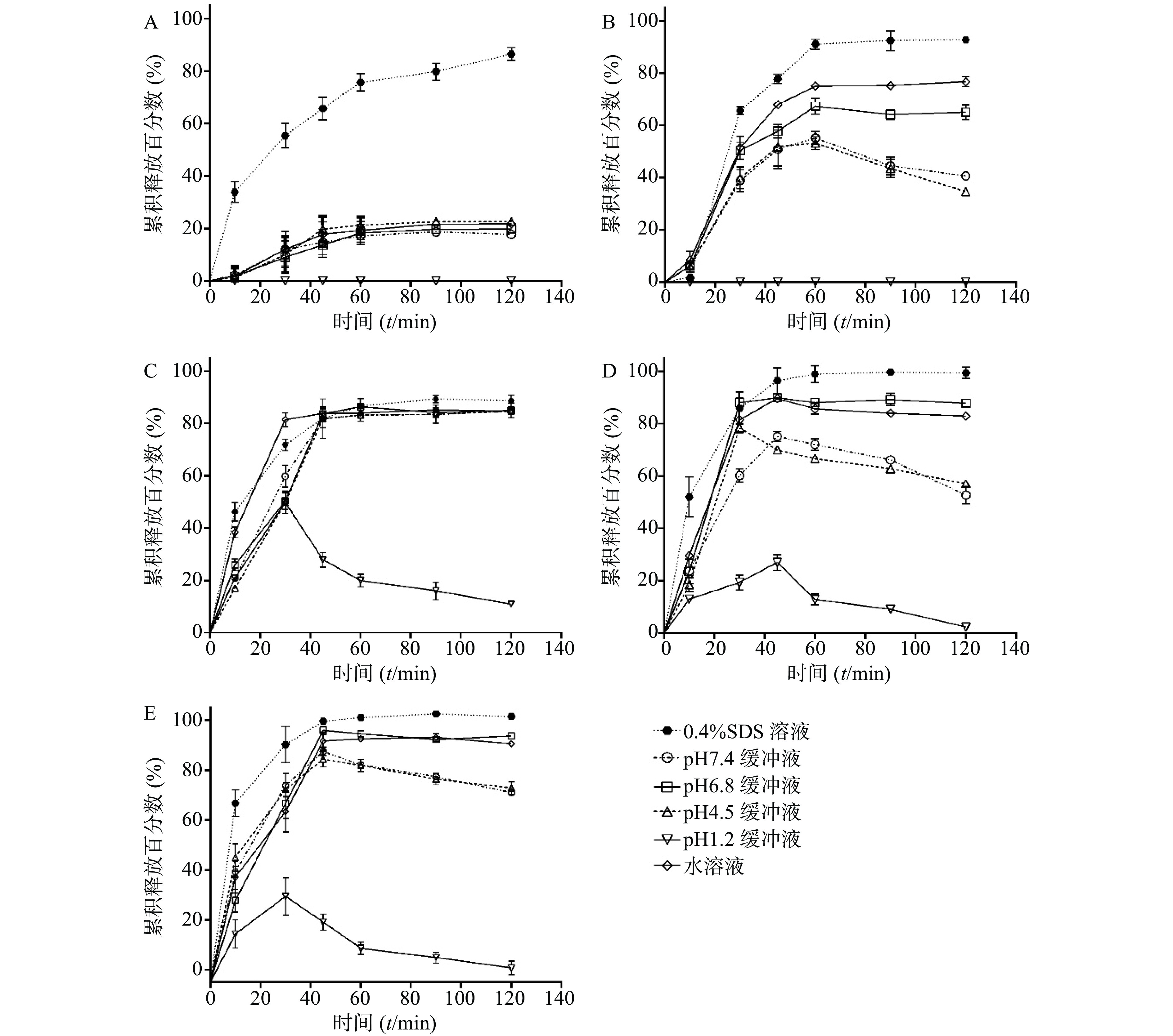
如图1A所示,不同载体材料制备的SRL-SD的溶出曲线显示了明显的差异,溶出速率为PEG6000>F68>PVP K30>HPMC606>HPMC-AS-MF。同时,各载体材料的溶出度均不理想(≤50%),因此进一步考察采用二元载体制备SRL-SD。
选择PEG6000联合F68制备二元载体固体分散体[13],两者比例为3∶1、2∶1、1∶1、1∶2、1∶3。随PEG6000/F68比例的增大,则SRL溶出度呈增大趋势,在PEG6000/F68为2∶1时的溶出度达到最大(图1B)。
3.1.2 药物-载体比例
在PEG6000/F68=2∶1的基础上,进一步考察药物-载体比例对SRL-SD溶出的影响。药物-PEG6000/F68载体比例为1∶2∶1、1∶4∶2及1∶6∶3所制的SRL-SD的溶出曲线相似,没有明显差别,2 h的溶出度都接近100%(图1C)。因此优选载药量最大,即药物- PEG6000/F68载体比例为1∶2∶1。
3.2 SRL-IC的制备
3.2.1 β-环糊精衍生物种类
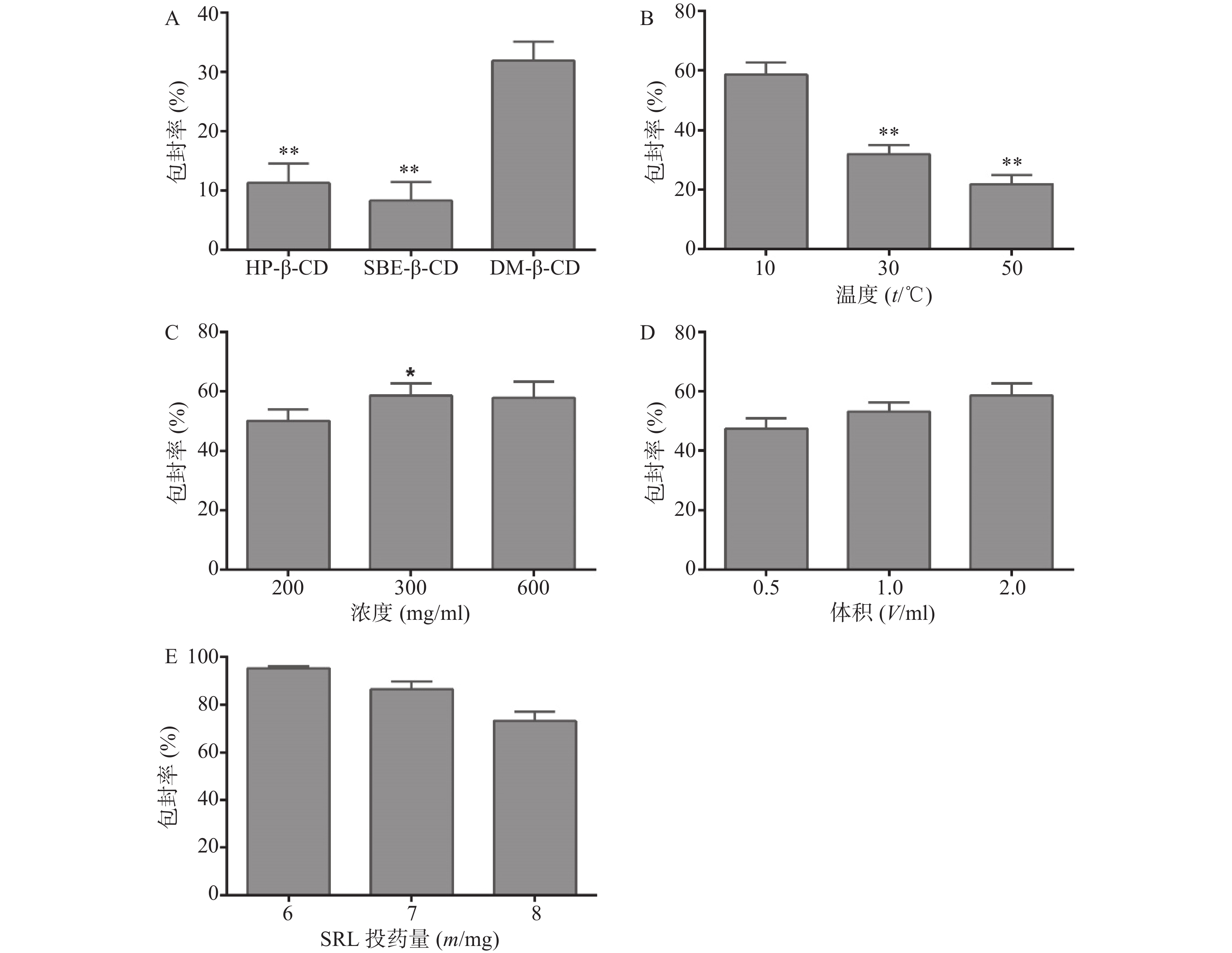
在其他条件相同的情况下,HP-β-CD、SBE-β-CD和DM-β-CD对SRL的包封率分别为(11.21±3.35)%、(8.24±3.11)%和(31.86±3.26)%,见图2A。因此,优选DM-β-CD制备SRL-IC。
3.2.2 温度
采用DM-β-CD制备SRL-IC,考察不同温度对包封率的影响。结果显示(图2B),温度越低,包封率越高,10 ℃条件下制备的SRL-IC的包封率显著高于30 ℃和50 ℃(P<0.01),为(58.61±4.16)%。因此,优选10 ℃制备SRL-IC。
3.2.3 环糊精衍生物浓度
DM-β-CD的浓度由200 mg/ml增大至300 mg/ml,SRL的包封率由(52.12±4.17)%增大至(58.61±4.11)%(P<0.05,图2C)。进一步增大DM-β-CD的浓度至600 mg/ml,包封率没有明显变化(P>0.05)。因此,优选DM-β-CD的浓度为300 mg/ml制备SRL-IC。
3.2.4 乙醇体积
乙醇体积由0.5 ml增大至2 ml,包封率呈增大趋势(图2D)。因此,优选乙醇体积为0.5 ml制备SRL-IC。
3.2.5 投药量
SRL的投药量6 mg增大至8 mg,包封率显著降低,6 mg SRL的包封率为(95.21±1.10)%,见图2E。因此,优选SRL的投药量为6 mg。
3.3 体外溶出度
考察SRL-SD、SRL-IC、SRL-SMEDDS及SRL-NLC在不同介质中的溶出曲线。如图3所示,在0.4% SDS中,各制剂在2 h的溶出度均超过80%,尤其是SMEDDS和NLC的溶出度接近100%。
在pH 6.8和水中,SRL-SD的溶出速率减小,2 h的溶出度分别为(65.00±4.90)%和(76.70±1.95)%。在pH 4.5和pH 7.4的介质中,SRL-SD的溶出在1 h达到最大值,分别为(53.20±4.34)%和(55.20±4.34)%,随后溶出度逐渐降低。在pH 1.2的介质中,未检测到SRL。
在水、pH 4.5、pH 6.8和pH 7.4中,SRL-IC在40 min内的溶出速率有所减小,但2 h的累积溶出没有明显变化,均在80%以上。在pH 1.2的介质中,SRL-IC的溶出度在30 min达到最大值,为(49.84±7.21)%,随后溶出度逐渐降低。
SRL-SMEDDS和SRL-NLC显示了与SRL-SD相似的溶出趋势,即在水和pH 6.8中的溶出度低于0.4% SDS,但大于80%。在pH 4.5和pH 7.4的介质中,溶出达到峰值(约80%)后逐渐降低。
3.4 比格犬体内药动学试验
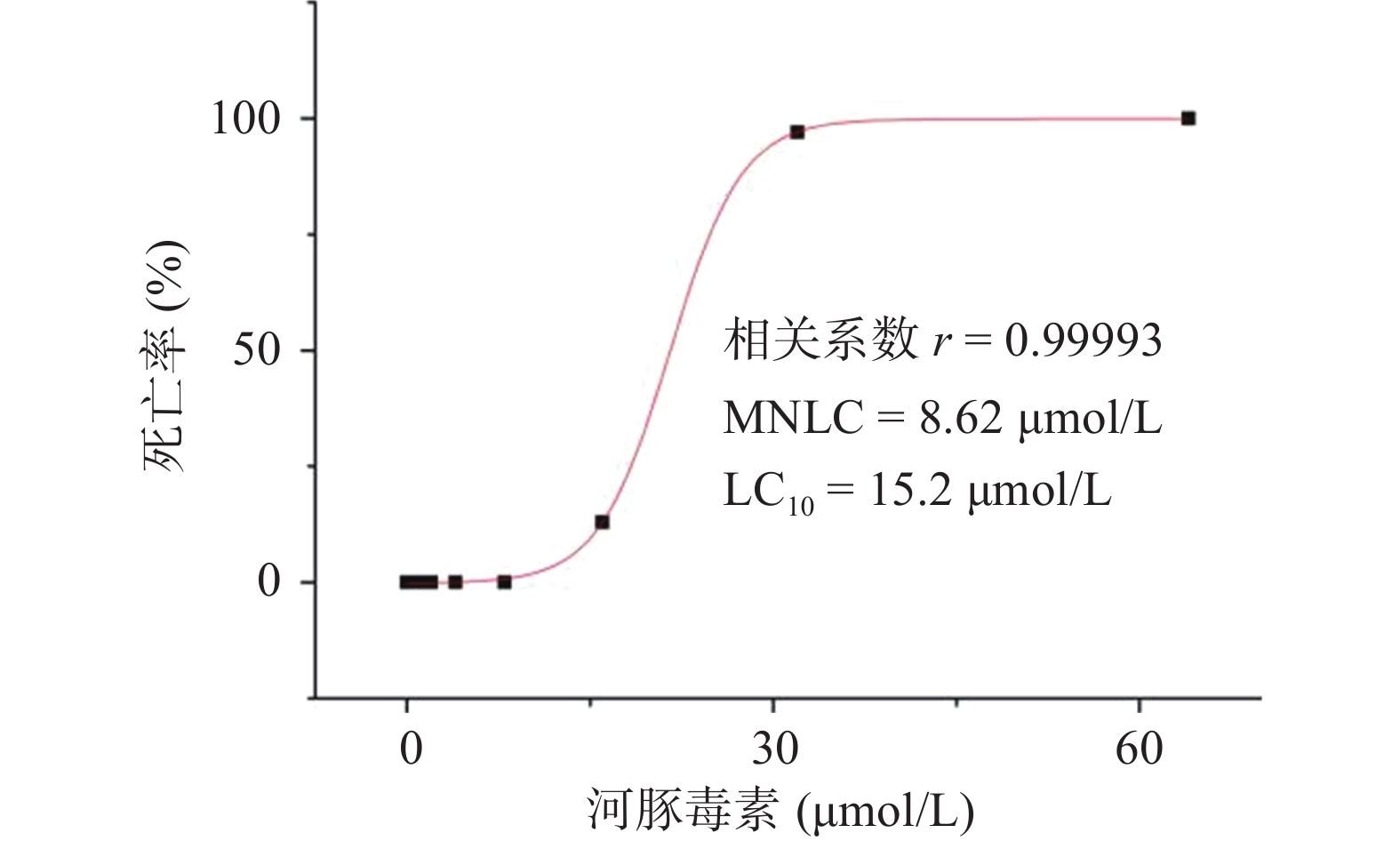
SRL血药浓度-时间曲线见图4,经DAS 3.2.6软件处理后,具体参数见表 1。
表 1 非房室模型体内药动学参数($ \bar x$ ±s)参数 SRL SRL-SD SRL-IC SRL- NLC SRL-SMEDDS Rapamune® AUC0→72(µg·h/ml) 0.70±0.13 2.06±0.79 3.66±2.64 8.60±2.03 10.76±1.57 11.02±2.73 AUC0→t(µg·h/ml) 0.73±0.15 2.07±0.81 3.78±2.84 8.67±1.95 11.15±2.11 11.75±3.13 t1/2 (t/h) 16.53±1.50 14.50±2.15 20.64±5.45 8.97±6.87 12.97±5.67 14.54±5.67 tmax(t/h) 1.04±0.25 1.25±0.28 1.04±0.25 1.13±0.31 1.50±0.38 1.83±0.26 cmax (ng/ml) 0.16±0.05 0.36±0.05 0.53±0.13 0.90±0.09 1.23±0.07 1.28±0.13 以原料药为参比制剂,SRL-SD、SRL-IC、SRL-SMEDDS、SRL-NLC、Rapamune®的相对生物利用度分别为332.8%、522.9%、1 228.6%、1 537.1%、1 574.3%,表明各增溶方法都显著提高了SRL的生物利用度。
以市售纳米晶片Rapamune®为参比制剂,SRL-SD、SRL-IC、SRL-NLC、SRL-SMEDDS的相对生物利用度分别为18.7%、33.2%、78.0%、97.6%,可见在各增溶方法中,SMEDDS对SRL体内吸收的作用最显著,与市售制剂相当。
4. 讨论
本研究同时制备和比较了SRL的4种增溶制剂,均显示了良好的体外溶出度。同时,各制剂都提高了SRL的生物利用度,但体内吸收程度有较明显的差异。
首先,SRL本身的性质是影响体内吸收的重要因素。在理化性质方面,SRL在电解质溶液中可发生开环水解,特别是在强酸和碱性条件下,降解速率显著增加[14]。在生理因素方面,SRL是肠道内CYP3A4酶和P糖蛋白的底物,对肠道吸收有较大影响[15]。
其次,制剂本身的特点对体内吸收有重要影响。SMEDDS和NLC均可形成纳米级的脂质微粒,在胃肠道消化后可形成乳糜胶束[16-17]均减轻了胃肠液的pH对SRL的降解作用,因此SMEDDS和NLC对脂质微粒中的SRL有一定的保护作用。相比之下,SD中的SRL快速释放后,载体材料失去了对药物的隔离保护作用,导致SRL在极短的时间内发生降解。另外,环糊精的空腔可以容纳药物分子[18],不仅提高了SRL的溶解度,而且降低了H+和OH-对SRL的作用概率,减缓了SRL的降解。本研究的体外溶出试验也证实了不同增溶制剂中SRL稳定性的差异。
同时,SMEDDS的辅料Labrafil M1944 CS和Cremophor EL[9, 19-21]和NLC中的脂质及其代谢产物能够抑制CYP3A4酶的代谢和P糖蛋白外排,消化后形成的乳糜胶束还可通过淋巴途径吸收[22],从而提高了生物利用度[10-11]。
另外,由于SRL分子量较大,分子结构可能仅有部分插入环糊精的空腔中。因此,尽管环糊精提高了SRL的溶出度,但包合物的稳定性较差,进入胃肠道后,药物可被胃肠液中的成分替换[23],导致SRL加速降解或发生重结晶,进而生物利用度下降。
-
表 1 河豚毒素急性毒性发生率统计(n=30)
毒性类型 正常对照组 溶剂对照组 河豚毒素浓度(μmol/L) 0.958 2.87 8.62 15.2 心脏 心包水肿 - - - - 7(2/30) 13(4/30) 房室缺失 - - - - - - 心律异常 - - - 7(2/30) 7(2/30) 17(5/30) 循环系统 血流变慢 - - - - - - 循环缺失 - - - - - - 出血及血栓 - - - - - - 脑 畸形 - - - - - - 下颌 短小 - - - - - - 眼睛 眼变小 - - - - - - 肝脏 缺失 - - - - - - 肝肿大 - - - - - - 肝变性 - - - - - - 卵黄囊吸收延迟 - - 80(24/30) 80(24/30) 87(26/30) 93(28/30) 肾脏 水肿 - - - - - - 肠道 肠腔异常 - - - 7(2/30) 13(4/30) 13(4/30) 躯干/尾/脊索 弯曲 - - - - - - 肌肉/体节 肌肉变性 - - - - - - 身体着色 异常 - - - - - - 体长变短 - - - - - 死亡 - - - - - 注:“-”表示未见明显异常 -
[1] ZIMMER T. Effects of tetrodotoxin on the mammalian cardiovascular system[J]. Mar Drugs, 2010, 8(3): 741-762. https://pubmed.ncbi.nlm.nih.gov/20411124/ [2] BIESSY L, BOUNDY M J, SMITH K F, et al. Tetrodotoxin in marine bivalves and edible gastropods: a mini-review[J]. Chemosphere, 2019, 236: 124404. https://pubmed.ncbi.nlm.nih.gov/31545201/ [3] TAMELE I J, SILVA M, VASCONCELOS V. The incidence of tetrodotoxin and its analogs in the Indian Ocean and the red sea[J]. Mar Drugs, 2019, 17(1): 28. https://pubmed.ncbi.nlm.nih.gov/30621279/ [4] MAGARLAMOV T Y, MELNIKOVA D I, CHERNYSHEV A V. Tetrodotoxin-producing bacteria: detection, distribution and migration of the toxin in aquatic systems[J]. Toxins, 2017, 9(5): 166. https://pubmed.ncbi.nlm.nih.gov/28513564/ [5] NIETO F R, COBOS E J, TEJADA M Á, et al. Tetrodotoxin (TTX) as a therapeutic agent for pain[J]. Mar Drugs, 2012, 10(2): 281-305. https://pubmed.ncbi.nlm.nih.gov/22412801/ [6] MATTEI C. Tetrodotoxin, a candidate drug for Nav1.1-induced mechanical pain? [J]. Mar Drugs, 2018, 16(2): E72. https://pubmed.ncbi.nlm.nih.gov/29470418/ [7] SALAS M M, MCINTYRE M K, PETZ L N, et al. Tetrodotoxin suppresses thermal hyperalgesia and mechanical allodynia in a rat full thickness thermal injury pain model[J]. Neurosci Lett, 2015, 607: 108-113. https://pubmed.ncbi.nlm.nih.gov/26424077/ [8] QIU F, JIANG Y G, ZHANG H, et al. Increased expression of tetrodotoxin-resistant sodium channels Nav1.8 and Nav1.9 within dorsal root Ganglia in a rat model of bone cancer pain[J]. Neurosci Lett, 2012, 512(2): 61-66. https://pubmed.ncbi.nlm.nih.gov/22342308/ [9] NEWMAN D J, CRAGG G M. Drugs and drug candidates from marine sources: an assessment of the current “state of play”[J]. Planta Med, 2016, 82(9-10): 775-789. https://pubmed.ncbi.nlm.nih.gov/26891002/ [10] JAL S, KHORA S S. An overview on the origin and production of tetrodotoxin, a potent neurotoxin[J]. J Appl Microbiol, 2015, 119(4): 907-916. https://pubmed.ncbi.nlm.nih.gov/26178523/ [11] LAGO J, RODRÍGUEZ L P, BLANCO L, et al. Tetrodotoxin, an extremely potent marine neurotoxin: distribution, toxicity, origin and therapeutical uses[J]. Mar Drugs, 2015, 13(10): 6384-6406. https://pubmed.ncbi.nlm.nih.gov/26492253/ [12] MCNABB P S, TAYLOR D I, OGILVIE S C, et al. First detection of tetrodotoxin in the bivalve Paphies australis by liquid chromatography coupled to triple quadrupole mass spectrometry with and without precolumn reaction[J]. J AOAC Int, 2014, 97(2): 325-333. https://pubmed.ncbi.nlm.nih.gov/24830143/ [13] TURNER A D, POWELL A, SCHOFIELD A, et al. Detection of the pufferfish toxin tetrodotoxin in European bivalves, England, 2013 to 2014[J]. Euro Surveill, 2015, 20(2): 21009. https://pubmed.ncbi.nlm.nih.gov/25613778/ [14] KIRCHHOF P, TAL T, FABRITZ L, et al. First report on an inotropic peptide activating tetrodotoxin-sensitive, “neuronal” sodium currents in the heart[J]. Circ Heart Fail, 2015, 8(1): 79-88. https://pubmed.ncbi.nlm.nih.gov/25424392/ [15] MATSUMOTO T, FEROUDJ H, KIKUCHI R, et al. DNA microarray analysis on the genes differentially expressed in the liver of the pufferfish, Takifugu rubripes, following an intramuscular administration of tetrodotoxin[J]. Microarrays (Basel), 2014, 3(4): 226-244. https://pubmed.ncbi.nlm.nih.gov/27600346/ [16] 王敏, 臧奎, 尚福泰, 等. 河豚毒素中毒致心跳呼吸骤停1例[J]. 临床急诊杂志, 2014, 15(1): 54-55. https://kns.cnki.net/KCMS/detail/detail.aspx?filename=ZZLC201401024&dbname=CJFD&dbcode=CJFQ [17] 张桦, 赵剑. 河豚毒素中毒致急性肾脏损害5例报告[J]. 中国实用内科杂志, 2002, 22(5): 303. https://kns.cnki.net/KCMS/detail/detail.aspx?filename=SYNK200205028&dbname=CJFD&dbcode=CJFQ [18] 徐勤惠, 黄凯, 高莉莎, 张翰, 荣康泰. 河豚毒素对小鼠和家兔的毒性研究[J]. 卫生研究, 2003, 32(4): 371-374. https://kns.cnki.net/KCMS/detail/detail.aspx?filename=WSYJ200304022&dbname=CJFD&dbcode=CJFQ -





 下载:
下载:
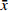
 下载:
下载: