-
心力衰竭具有高发病率和病死率,是绝大多数终末期心脏病的最终归宿[1]。近几十年来,HF的治疗在医疗和设备方面有了很大的创新,但其发病率仍在不断增加,HF患者的生活质量和预期寿命依然出现不同程度的损害[2]。心脏能量需求是非常高的,需要源源不断消耗ATP来维持收缩舒张的功能。研究发现,HF患者会出现严重的能量代谢紊乱,包括底物吸收和利用、氧化磷酸化和ATP穿梭障碍,最终,导致心脏能量供应不足[3]。目前,关于HF疗法主要是通过降低心率、前负荷和后负荷来减轻心脏负荷,从而治疗和延缓疾病进展。关于影响心脏能量代谢的药物有很多基础研究,而能用于临床治疗的却少之又少。本综述将简单概述健康心脏和HF期间的心脏能量代谢,及通过调节能量代谢降低HF的潜在药物。
-
心脏可利用葡萄糖、脂质、氨基酸和酮体等各种底物来提供能量以维持正常的工作,它对底物的利用随生命周期生理、病理和外部环境的变化而变化[4]。胎儿由于在缺氧和低脂肪酸的环境中生存,此时,心肌主要依靠葡萄糖和乳酸代谢来产能[5]。出生后的新生儿不仅心脏血流动力学负荷和氧分压增加,且线粒体数量也在快速增加,这样会显著提高心脏的氧化能力。此时,心脏对葡萄糖的依赖减少,血乳酸水平开始下降。随着三酰甘油含量的增加,脂肪酸氧化成为心脏能量的主要来源[6]。脂肪酸是成人心脏主要的能量来源,占60%~90%,其余10%~40%来源于葡萄糖、氨基酸、丙酮酸、乳酸、酮体等[7]。其中,线粒体的氧化磷酸化可供给约95%的心肌所需的ATP,剩下的5%由糖酵解提供[8]。
-
在正常情况下,脂肪酸和葡萄糖能否得到充分利用,取决于代谢底物和氧气的浓度。1 mol的20碳脂肪酸完全氧化产生的ATP量(约134 mol)远大于1 mol葡萄糖产生的ATP量(约30 mol)。研究发现,当它们产生相同数量的ATP时,脂肪酸氧化比葡萄糖氧化需要更多的氧气。而在氧气缺少的情况下,脂肪酸氧化的生产效率明显低于葡萄糖氧化[9]。HF后的低氧环境将心脏的能量代谢逆转为胎儿期的能量代谢,葡萄糖代谢将是主要的能量来源[10]。在HF期间,葡萄糖摄入量和糖酵解速率显著增加,以补偿脂肪酸氧化以提供能量。由于HF期间,心肌细胞对游离脂肪酸的利用显著降低,血浆中游离脂肪酸浓度升高,这样可能会进一步加重能量代谢紊乱和心肌损伤[11]。
正常成人心脏中90%的能量是由线粒体的氧化磷酸化提供的。许多研究证实,心血管疾病,如心律失常、心肌病和HF,与线粒体功能和结构的改变有关[12]。研究表明,HF时心肌细胞线粒体基因突变率显著增加,引起线粒体畸变,从而影响线粒体氧化呼吸链相关酶复合物的活性和线粒体蛋白的合成[13]。这些变化导致线粒体功能障碍,影响线粒体能量代谢,耗尽心肌细胞中的能量,加快HF的进程。
-
激素是人体必需的物质,在调节新陈代谢、生长、发育、繁殖等过程中发挥着重要作用。一些激素类药物,包括甲状腺素、松弛肽和雌激素,已被用于治疗心脑血管疾病。甲状腺素是体内不可或缺的激素,与生长、细胞凋亡和能量代谢息息相关。最近的研究表明,甲状腺素可通过LKB1/AMPK/mTOR 通路来减少心肌细胞凋亡、减少能量损失和预防多柔比星引起的心脏损伤[14]。因此,甲状腺素有望成为临床预防多柔比星化疗所致心脏损害的新药。临床研究表明,怀孕期间给予松弛肽-2,可以延长急性HF患者的生存期[15]。松弛肽抗HF的分子机制目前尚不清楚,可能与内源性长链多不饱和脂肪酸的合成、氨基酸修饰中的能量代谢和心血管结构调节有关[16]。雌激素促进女性副性器官的发育、成熟和第二性征的出现,帮助维持正常的性欲和生殖功能。研究表明,雌激素可以通过保护线粒体含量和氧化能力来保护肺动脉高压模型小鼠的右心室功能。
-
有临床观察表明,二甲双胍可提高非糖尿病HF患者的心肌效率,降低耗氧量,改善心功能[17]。研究表明,二甲双胍可在一定程度上恢复左心室舒张功能,并降低免疫和炎症反应[18]。它还可以增加梗死后心力衰竭小鼠的收缩功能,同时减少心肌细胞的凋亡[19]。二甲双胍改善心功能的机制可能与调节葡萄糖吸收、线粒体功能和氧化应激有关。二甲双胍通过刺激活化 PI3K–PKB/AKT和AMPK的通路来增加葡萄糖摄取,这种积极作用已在胰岛素抵抗心肌细胞和正常胰岛素敏感心肌细胞中得到了验证[20]。二甲双胍还可以通过调节SIRT3降低PGC-1α乙酰化水平、降低受损的线粒体膜电位和增加线粒体呼吸功能来改善小鼠的心脏功能[19]。
-
钠-葡萄糖转运蛋白2(SGLT2)抑制剂是最近研发的一类抗糖尿病药物,如达格列净、卡格列净和恩格列净。有研究发现SGLT2抑制剂是潜在的心血管保护药物,在临床评估心血管安全性时可用于治疗HF[21]。临床研究表明,达格列净可降低2型糖尿病和HF患者的糖尿病性心肌病的风险,并有利于改善左心室功能。此外,达格列净还可以减轻HF患者的症状,改善身体功能和生活质量,降低心血管疾病HF进展和病死率[22]。此外,还观察到卡格列净和恩格列净也可改善HF患者的状况[23]。
-
吡格列酮是一种胰岛素增敏的噻唑烷二酮和PPARγ激动剂。研究发现,吡格列酮可逆转严重肺动脉高压和血管重构,预防右心室HF,这与通过 miRNA/mRNA 网络调节心脏肥大、纤维化、心肌收缩力、脂肪酸转运/氧化和转化生长因子信号转导有关[24]。
-
辛伐他汀是一种羟甲基戊二酰辅酶A(HMG-CoA)抑制剂,常用于高血脂的治疗,主要用于降低胆固醇。临床观察发现,服用辛伐他汀20 d可显着降低慢性HF患者的促炎标志物IL-6和C反应蛋白水平[25]。它还可以诱导脂滴积累,为维持线粒体功能提供能量,并抑制线粒体损伤和心肌细胞凋亡[26]。此外,辛伐他汀还通过降低心房诱导的一氧化氮合酶、钠钙交换剂来降低缺血性HF大鼠的氧化应激、内皮血栓形成和心房颤动[27]。
-
非诺贝特属于苯氧芳酸类降脂药,主要用于降低三酰甘油。它是一种高度选择性PPARα配体,可降低低密度脂蛋白、总胆固醇和三酰甘油的水平,并增加高密度脂蛋白[28]。研究发现,非诺贝特可防止HF模型犬心脏代谢底物的转化,并适度改善心脏功能[29]。还有研究发现,在异丙肾上腺素诱导的HF大鼠身上,非诺贝特可增加线粒体中的脂肪酸氧化,增加心肌能量代谢和氧化应激,从而保护心脏功能[30]。
-
曲美他嗪常用于治疗心绞痛,是代谢治疗中研究最广泛的药物之一。临床研究发现,它可以改善 HF患者的心脏功能、运动耐量、生活质量、左心室射血分数和心脏容量[31]。它还可以通抑制脂肪酸氧化,促进葡萄糖代谢,并维持细胞中的 PCr/ATP 比率[32]。
-
卡维地洛是一种α 1和β受体阻断剂,具有扩张血管的作用。常用于治疗轻度或中度高血压,或肾功能不全和糖尿病患者。一项临床研究表明,长期使用卡维地洛可以提高非缺血性HF患者的生存率,而更高剂量(7.5 mg/d)的卡维地洛可以提高低心率和低射血分数HF患者的生存率,但对射血分数保留的患者无效[33]。卡维地洛可降低充血性HF患者的心肌脂肪酸利用,但对葡萄糖利用没有影响[34]。它还可以增加射血分数,降低纽约心脏协会的心脏分级,增加PCr/ATP比率和代谢当量,并维持心肌高能磷酸盐水平[35]。此外,它可以增加心肌缺血模型大鼠的线粒体能量电荷,减少磷酸化滞后阶段的长度,改善心肌缺血期间的线粒体功能[36]。
已经发现这些治疗HF的合成药物在治疗其他疾病时可以改善能量代谢并保护心肌,而不是专门开发用于改善HF的能量代谢。这表明我们可以通过这些药物在体内的作用机制找到新的或最佳的HF治疗靶点,为临床药物开发治疗HF的药物提供了可能。同时,需要进一步研究这些合成药物及其衍生物治疗不同因素所致HF的特异性和安全性,为其临床应用提供更多参考。
-
多酚是一大类植物化学物质,存在于各种食物中,例如,水果、蔬菜、豆类、谷物、可可或巧克力,以及红酒、咖啡和茶等饮料。按其结构特点,大致可分为黄酮类、酚酸类、木脂素类和芪类。白藜芦醇、槲皮素、姜黄素和表没食子儿茶素没食子酸酯等多酚类物质对动脉粥样硬化、高血压、心肌梗死、蒽环类药物引起的心肌病、血管生成和HF有明显的保护作用[37]。大量多酚已被证明可有效通过能量代谢减少心血管疾病,但只有白藜芦醇进入了系统化、标准化的临床试验。此外,一些富含多酚的提取物值得关注。例如,长期使用绿茶提取物可以改善正常心肌细胞的细胞力学性能和细胞内钙动力学,提高能量利用率,并消除受磷蛋白对肌浆网Ca2+依赖性ATPase 2a的抑制作用。
-
目前,人参皂苷是用于治疗HF的主要皂苷,又称三萜皂苷。人参总皂苷通过激活TCA循环中的特定蛋白来增加心脏能量代谢[38]。阿江榄仁酸是一种天然存在的手性三萜皂苷,可以降低心肌细胞中的氧化磷酸化活性、活性氧水平和氧化应激,以减少线粒体功能障碍和增加糖酵解速率。此外,它还可以上调PPARα,降低TAK1的磷酸化水平,抑制p38 MAPK和NF-κB P65的活化,减少胶原合成和心脏肥大,从而保护心脏[39]。黄芪甲苷是黄芪提取物。它可以增加PPARα、中链酰基辅酶A脱氢酶(MCAD)和肌肉肉碱棕榈酰转移酶-1(MCP1)的表达,并增加慢性HF大鼠对游离脂肪酸的利用,从而改善心脏功能和抑制心室重构[40]。同时,它还能刺激脂肪酸β氧化并改善HF动物的线粒体功能,是一种抑制HF进展的潜在药物[41]。
-
从植物中提取的多糖对心血管疾病具有治疗作用,这与其抗炎和抗氧化作用有关[42]。但关于多糖是否调节心脏能量代谢的报道有限,仅有麦冬多糖、枸杞多糖和黄芪多糖有报道。麦冬多糖可显著降低转氨酶、乳酸脱氢酶、肌酸激酶和肌酸激酶同工酶水平,提高ATP酶活性,对缺血性心肌损伤具有保护作用[43]。枸杞的提取物枸杞多糖可以通过上调线粒体生物基因调节因子促进肌肉分化和能量代谢,通过减少HF小鼠的炎性细胞因子和脂质过氧化来发挥心脏保护作用[44]。有报道,黄芪多糖可以调节TNF -α/PGC-1信号通路介导的能量生物合成,降低ANP的mRNA和蛋白表达,增加ATP/ADP和ATP/AMP的比值,降低游离脂肪酸含量和抑制心肌细胞肥大[45]。
-
猪毛菜酚是一种来自乌头植物的生物碱。它可降低多柔比星诱导的慢性HF,降低血清心肌损伤标志物水平,减少对心脏的组织损伤,并增加TCA循环下游关键酶的mRNA 表达水平,从而增加心脏能量代谢[46]。和乌胺是一种典型的β2-肾上腺素选择性受体激动剂,也是乌头植物中的一种生物碱,可显着增加心肌收缩力[47]。川芎嗪又名四甲基吡嗪,是从川芎中分离得到的生物碱。它可以促进BCL-2向线粒体的转移,改善线粒体功能,从而防止脂多糖引起的心肌损伤[48]。它还可以通过下调miR-499a、上调SIRT1和激活 PI3K/AKT通路来减轻缺氧诱导的H9c2细胞凋亡[49]。
-
中药中,不同机制的天然产物,甚至几种药材,按照一定的规律进行组合,可以最大限度地发挥药效,减少毒副作用。这种做法即为临床补充和替代疗法。临床研究发现,口服参附颗粒可显著改善慢性HF患者的生活质量[50]。参附注射液通过刺激抗氧化剂和改变磷脂水平、分布以及牛磺酸、谷胱甘肽和磷脂的水平来减少心肌梗死的面积并保护心肌[51]。此外,临床观察发现,由十一味草药(黄芪、人参、附子、丹参、葶苈子、泽泻、玉竹、桂枝、红花、香加皮、陈皮)提取物组成的芪苈强心胶囊可以改善HF患者的生活质量,降低了心血管疾病的发生率和再住院率[52]。目前,一些天然成分和草药的联合使用和安全性仍在研究中,但它们为HF的替代和补充治疗以及HF药物的开发提供了可能。
我们对上述激素、合成药物和天然药物(表1)研究发现,大多数药物或成分可以作用于多种途径或靶点,并调节多种底物代谢。这表明我们可以考虑不同药物的组合,特别是一些大剂量、安全窗口窄的药物,可以减少剂量、耐药性和副作用。这些组成部分应进一步研究,并为其开发和应用提供可靠的数据。此外,我们还应该专注于利用这些药物的体内机制来寻找新的或最佳的HF治疗靶点。然后,应将研究结果应用于临床实践,开发更有效的治疗HF的药物和合理的治疗策略。
表 1 药物的已知途径、靶点和代谢途径摘要
药物类别 药物名称 已知通路或靶点 已知的代谢途径 激素 甲状腺素 LKB1/AMPK/mTOR 脂肪酸代谢 松弛素 – 脂肪酸合成、氨基酸代谢 雌激素 – 线粒体功能 合成药物 二甲双胍 PI3K-PKB/AKT、AMPK、PGC-1α 葡萄糖代谢、线粒体功能、氧化应激 SGLT2抑制剂 AMPK、 Na+/H+ 交换剂、NLRP3 炎症小体 酮代谢、线粒体功能、细胞内钠稳态、胰岛素信号传导、氧化应激 吡格列酮 PPAR γ 脂肪酸氧化,线粒体功能 辛伐他汀 iNOSitol、INCX、Rac1 线粒体功能,氧化应激 非诺贝特 PPARα 脂肪酸代谢 曲美他嗪 长链3-酮酰基辅酶A硫溶酶 葡萄糖代谢、脂肪酸代谢 卡维地洛 α1、β受体 脂肪酸代谢,线粒体功能 天然药物 白藜芦醇 SIRT1、CYP1B2 葡萄糖代谢、脂肪酸代谢、线粒体功能、胰岛素信号、钙2+浓度 人参皂苷Rb1 TGF-β1/SMAD ERK、AKT 葡萄糖代谢 人参皂苷Rb3 PPARα 脂肪酸代谢,线粒体功能 阿江榄仁酸 P47phox、ERK、PPARα、TAK1、p38 MAPK、NF-κB P65 葡萄糖代谢、线粒体功能、氧化应激 黄芪甲苷 PPARα、MCAD、MCP1 脂肪酸代谢,线粒体功能 麦冬多糖 AST、 LDH、CK、CK-MB、ATPase 线粒体功能 枸杞多糖 线粒体生物基因调控因子 脂肪酸代谢,线粒体功能 黄芪多糖 TNF-α/PGC-1 脂肪酸代谢 猪毛菜酚 – 线粒体功能 和乌胺 PPAR α/PGC-1α/SIRT3 线粒体功能 川芎嗪 miR-499a、SIRT1、PI3K/AKT 线粒体功能 -
大量证据表明,优化心肌能量代谢,尤其是调节底物代谢,可以保持或改善心肌机械功能,延缓HF进展,改善心功能分级、运动耐量、生活质量、左心室射血评分甚至存活率。然而,如何根据不同的病理情况选择合适的底物进行充分代谢,促进心肌代谢物的活性,增加整体供能,是HF药物的研究方向,也是亟待解决的问题。此外,大多数治疗HF的药物的开发通过能量代谢仍处于基础研究阶段,这些药物的疗效和应用变化也缺乏临床数据支持。研究人员应进一步探索HF发病机制与心肌能量代谢变化的关系,阐明影响HF能量代谢的信号通路和关键调控因素,研发有效的新方法,包括天然药物,以预防HF的发生和发展。
Advances in potential drugs for improvement of energy metabolism in heart failure
-
摘要: 心力衰竭(HF)是一个全球性的公共卫生问题,发病率和死亡率都很高。研究表明,HF是由严重的能量代谢紊乱引起的,导致心脏能量供应不足。这种能量缺乏会导致心脏泵血功能障碍和全身其他器官能量代谢的衰竭。针对HF的疗法主要通过降低心率和心脏前负荷和后负荷、对症治疗或延缓疾病的发展来发挥作用。然而,针对心脏能量代谢的药物却尚未研发出来。本文概述健康心脏中能量代谢的主要特征、HF期间的代谢变化,并讨论通过能量代谢来改善心脏功能的药物,为治疗HF药物的研发和应用提供新的研究方向。Abstract: Heart failure (HF) is a global public health problem with high morbidity and mortality. Numerous studies have shown that HF is caused by severe disturbance of energy metabolism, resulting in insufficient cardiac energy supply. This lack of energy could lead to a failure of the heart to pump blood and a failure of energy metabolism in other organs throughout the body. Currently, therapeutics of HF work by reducing heart rate and cardiac preload and afterload, symptomatic treatment, or delaying the progression of the disease. However, drugs targeting heart energy metabolism have not been developed. the main characteristics of cardiac energy metabolism, metabolic changes during HF were summarized and drugs that improve cardiac function through energy metabolism were discussed, which could provide a new research direction for the development and application of drugs in treatment of heart failure.
-
Key words:
- heart failure /
- energy metabolism /
- anti-heart failure drugs
-
西红花为名贵药材,来源于鸢尾科植物番红花Crocus sativus L.的干燥柱头。原产于地中海地区、希腊、小亚细亚和伊朗,后经西藏传入国内,故又名藏红花[1]。《本草纲目》中记载番红花“主治心忧郁积、气闷不散,活血,亦治惊悸”[2]。2020版《中国药典》描述西红花具有活血化瘀、凉血解毒、解郁安神的功效[3]。越来越多的现代药理研究表明,西红花具有抗肿瘤、抗血小板聚集与凋亡、抗心血管细胞凋亡、降血脂和降血糖等活性[4–6],在健康和医疗领域具有重要作用。
世界卫生组织国际癌症研究机构(IARC)发布的最新数据,2020年全球癌症新发患者病例数超过1 930万例,癌症死亡患者接近1 000万例[7]。天然活性成分是抗肿瘤药物研发的重要来源[8]。有研究表明,西红花中特有的西红花酸、西红花苷等具有抗肿瘤活性[9],已有学者在西红花治疗结直肠癌、乳腺癌等的抗肿瘤作用方面进行了相关研究[10-11],但其主要活性成分及抗肿瘤作用机制仍需进一步探索。
网络药理学[12]将系统生物学、生物信息学、计算生物学、网络科学和靶向药理学相结合,从系统层次和生物网络的整体角度探讨成分—靶标—通路的相互作用关系,为中药多靶点、多成分、系统性、整体性的作用机制研究提供了有力的技术支撑,从而指导新药研发和临床诊疗。因此,本研究应用网络药理学结合反向分子对接的方法,对西红花的抗肿瘤作用成分及靶点机制进行研究,为深入探索西红花抗肿瘤药效物质基础及作用机制提供参考。
1. 方法
1.1 西红花化学成分获取
利用TCMSP平台获取西红花化学成分,口服生物利用度(oral bioavailability,OB)和类药性(drug-likeness,DL) 是药物筛选的关键参数,一般设置OB≥30%和DL≥0.18的化学成分作为候选药效成分,并结合文献报道[13–15]补充4个西红花化学成分。
1.2 西红花活性成分和肿瘤疾病相关靶点整理
应用TCMSP平台和PharmMapper[16]工具获取西红花活性成分的作用靶点,并借助UniProt数据库将靶点转换为对应基因。以“tumor”、“cancer”为关键词,在GeneCards(https://www.genecards.org/)、OMIM数据库(https://www.omim.org/)和TTD数据库(http://db.idrblab.net/ttd/)进行检索。将得到的疾病靶点和药物靶点取交集,作为药物作用于疾病的预测靶点。
1.3 “成分-靶点”网络的构建
根据预测的西红花药效成分、交集靶点,使用Cytoscape 3.9.1软件建立“成分-靶点”的网络图。
1.4 蛋白质相互作用网络(protein-protein interaction,PPI)的构建与分析
将药物疾病交集靶点输入String数据库构建PPI网络进行初步筛选,再将PPI网络导入Cytoscape 3.9.1中,以半数degree为参考标准,选取关键靶点。
1.5 基因功能注释和富集通路分析
将筛选获得的37个核心靶点录入Metascape平台(http://metascape.org/gp/index.html),物种设置为人,选择Custom Analysis,设置P<0.01,进行基因本体(gene ontology,GO)功能富集分析及京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes,KEGG)通路富集分析。
1.6 分子对接
将筛选出的西红花主要活性成分通过PubChem下载SDF格式;利用RCSB PDB数据库下载关键蛋白靶点,优先选择有配体、结构相对完整的晶体结构,并采用AutoDock Tools对获取的PDB蛋白分子进行除水、加氢、计算电荷预处理;使用AutoDock Vina进行分子对接,计算结合能;选取最优构象,使用PyMOL软件做出3D结合模式图。
2. 结果
2.1 西红花化学成分获取
通过TCMSP获得70个西红花化学成分,设置OB≥30%且DL≥0.18进行筛选,再添加文献检索相关成分,共获得9个西红花活性成分,见表1。
表 1 西红花活性成分序号 化合物编号 化合物英文名 中文名 OB (%) DL 1 MOL001389 n-heptanal 庚醛 79.74 0.59 2 MOL001406 crocetin 西红花酸 35.3 0.26 3 MOL000354 isorhamnetin 异鼠李素 49.6 0.31 4 MOL000422 kaempferol 山柰酚 41.88 0.24 5 MOL000098 quercetin 槲皮素 46.43 0.28 6 MOL001405 crocin Ⅰ 西红花苷Ⅰ 2.54 0.12 7 MOL001407 crocin Ⅱ 西红花苷Ⅱ 1.65 0.21 8 MOL000720 safranal 藏红花醛 39.56 0.04 9 MOL001409 picrocrocin 苦番红花素 33.71 0.04 2.2 西红花活性成分和肿瘤疾病靶点
将TCMSP平台和PharmMapper获取结果进行整理,并借助UniProt数据库进行靶基因匹配,获得201个潜在靶点。以“tumor”和“cancer”为关键词,在GeneCards、OMIM和TTD数据库进行预测整理,剔除重复,筛选得到5896个潜在疾病靶点。将得到的疾病靶点和药物靶点取交集,共得到可作为药物作用于疾病的179个预测靶点。
2.3 “成分-靶点”网络的构建与分析
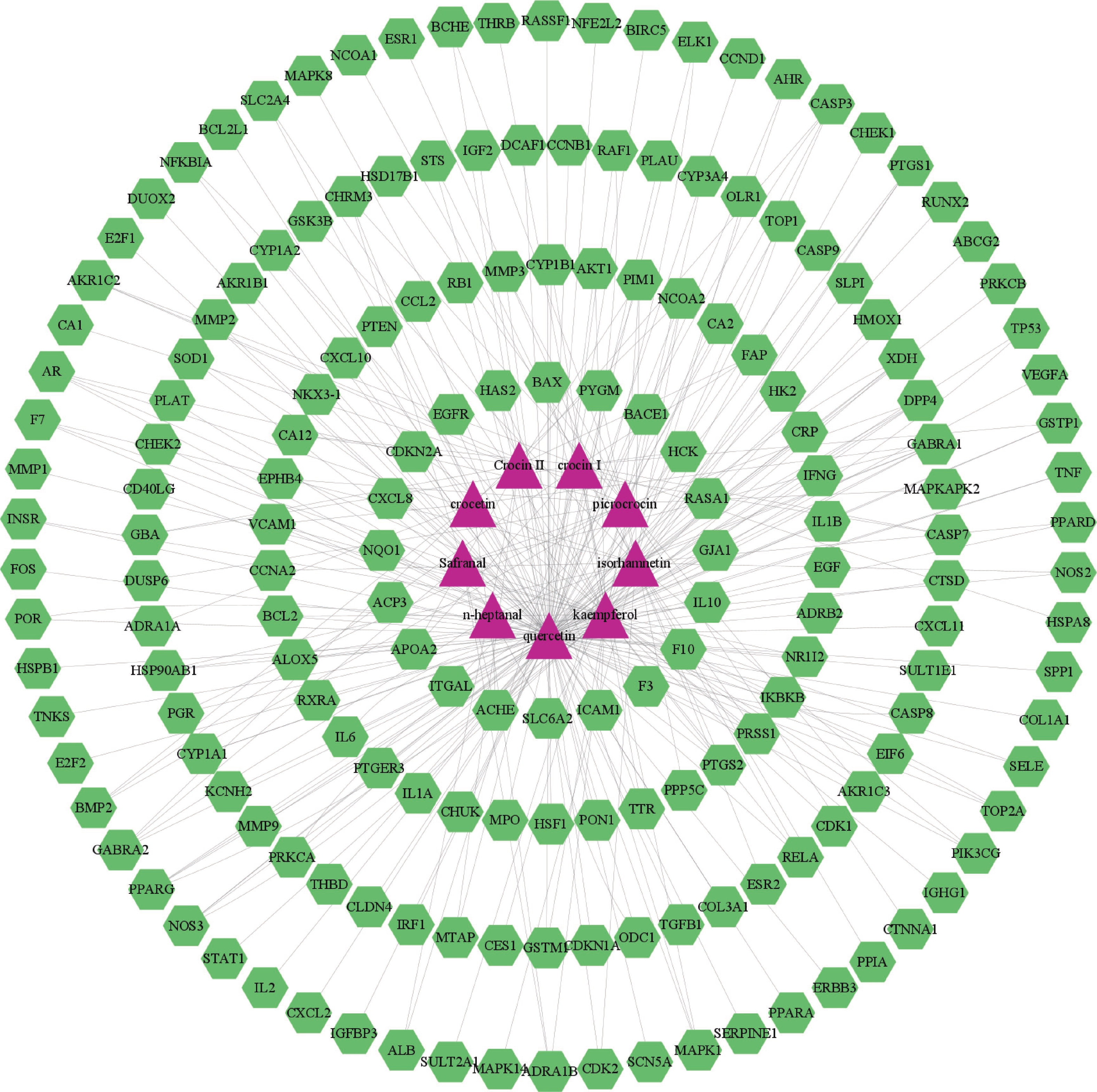
将西红花的9个活性成分与预测到的179个潜在靶点导入Cytoscape 3.9.1软件,构建“药物-活性成分-靶点”网络(图1),网络中绿色代表药物作用于疾病的靶点,蓝色代表西红花活性成分,全图包括189个节点、299条边,其中degree值排名靠前的活性成分为槲皮素、山柰酚、异鼠李素、苦番红花素和西红花苷Ⅰ,这些可能是西红花发挥抗肿瘤作用的潜在活性成分。
2.4 蛋白相互作用PPI的构建与分析
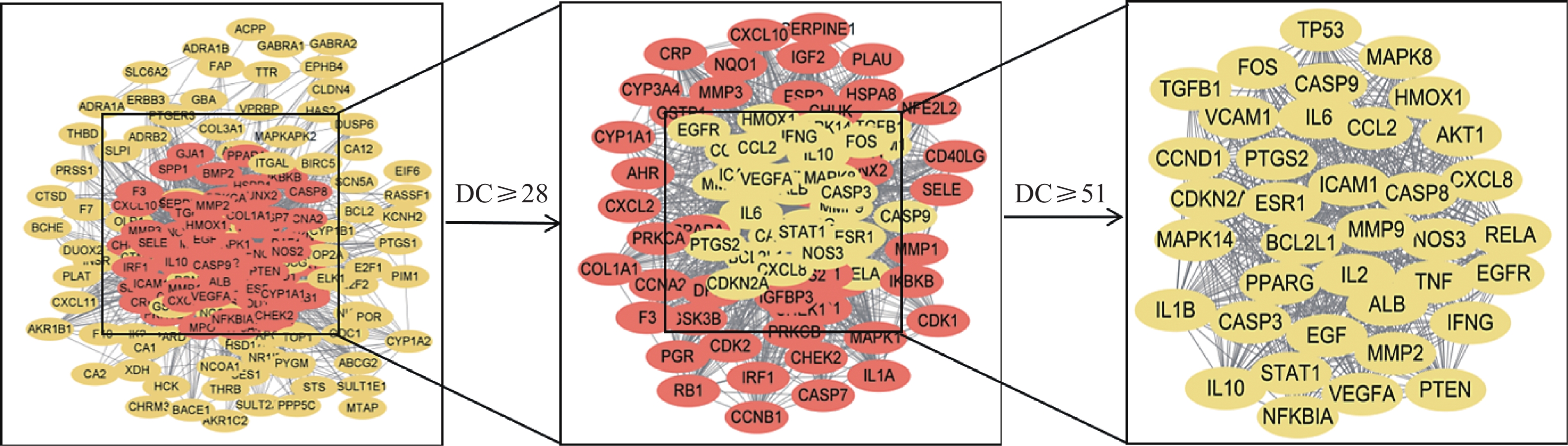
将疾病与活性成分的潜在靶点导入String数据库,采用Cytoscape 3.9.1软件绘制PPI网络图,依据degree值进行排序,以大于半数degree值为标准进行两次筛选,获取核心靶点37个(图2)。度值排名前5的靶点分别为EGF、MMP9、NFKBIA、IL-1B和IL-10,提示这些靶点可能是西红花发挥抗肿瘤作用的关键潜在靶点。
2.5 基因功能注释和富集通路分析
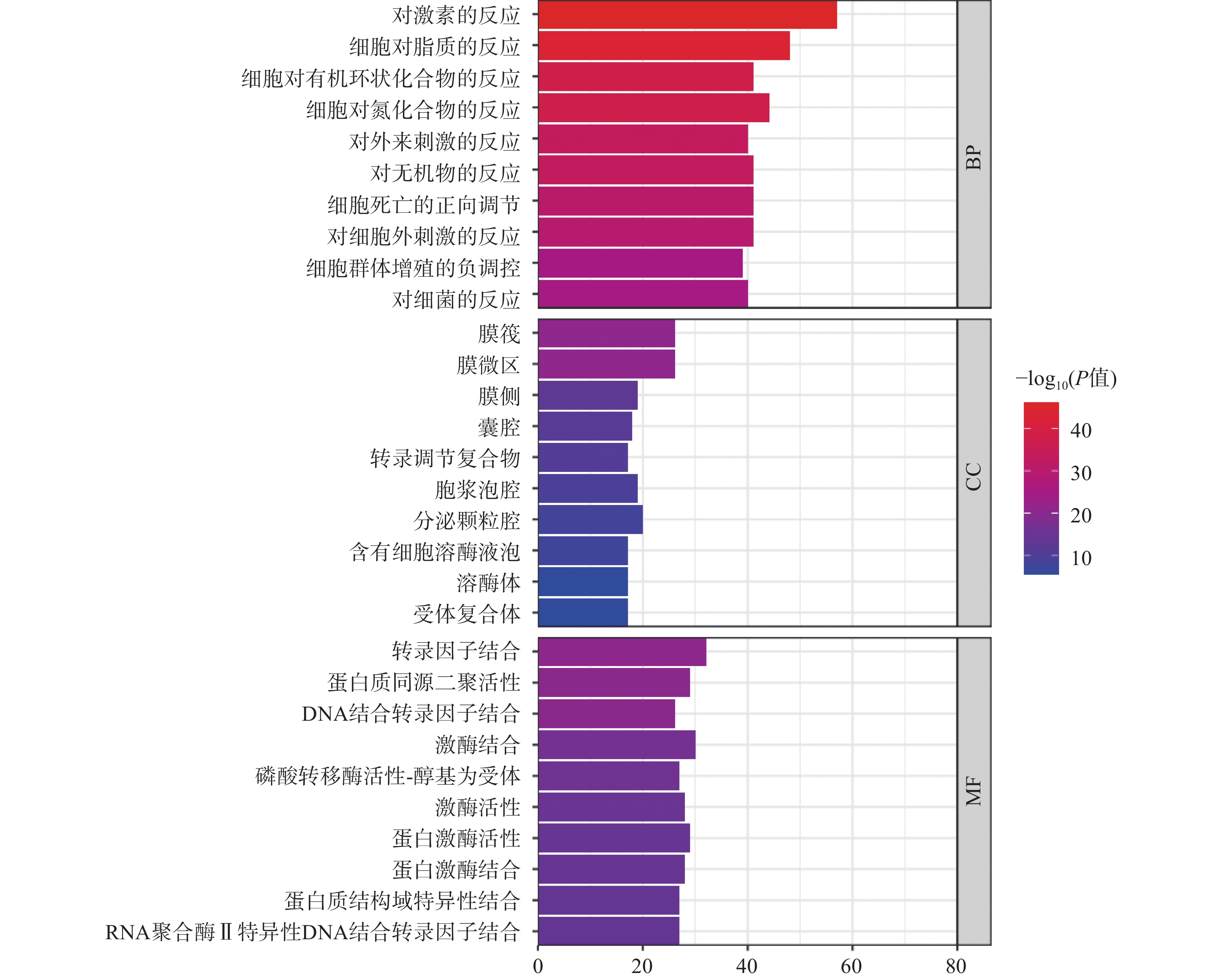
GO分析常用于注释基因和基因产物生物功能,分析包括生物过程(biological process,BP)、分子功能(molecular function,MF)和细胞组成(cellular component,CC)三部分。此次GO富集分析共得到BP富集结果193个、CC富集结果83个和MF富集结果123个,选取排名前10的条目绘制GO功能分析图(图3)。如图3所示,BP主要涉及对激素的反应、对脂质的反应、对异源刺激的反应等;CC主要涉及膜筏、膜微区、囊腔、细胞质囊泡腔等;MF主要涉及转录因子结合、DNA结合转录因子结合、RNA聚合酶Ⅱ特异性DNA结合转录因子结合等。通过比较发现,细胞生物过程富集的基因数较多,说明西红花可能主要通过调节生物过程发挥抗肿瘤作用。
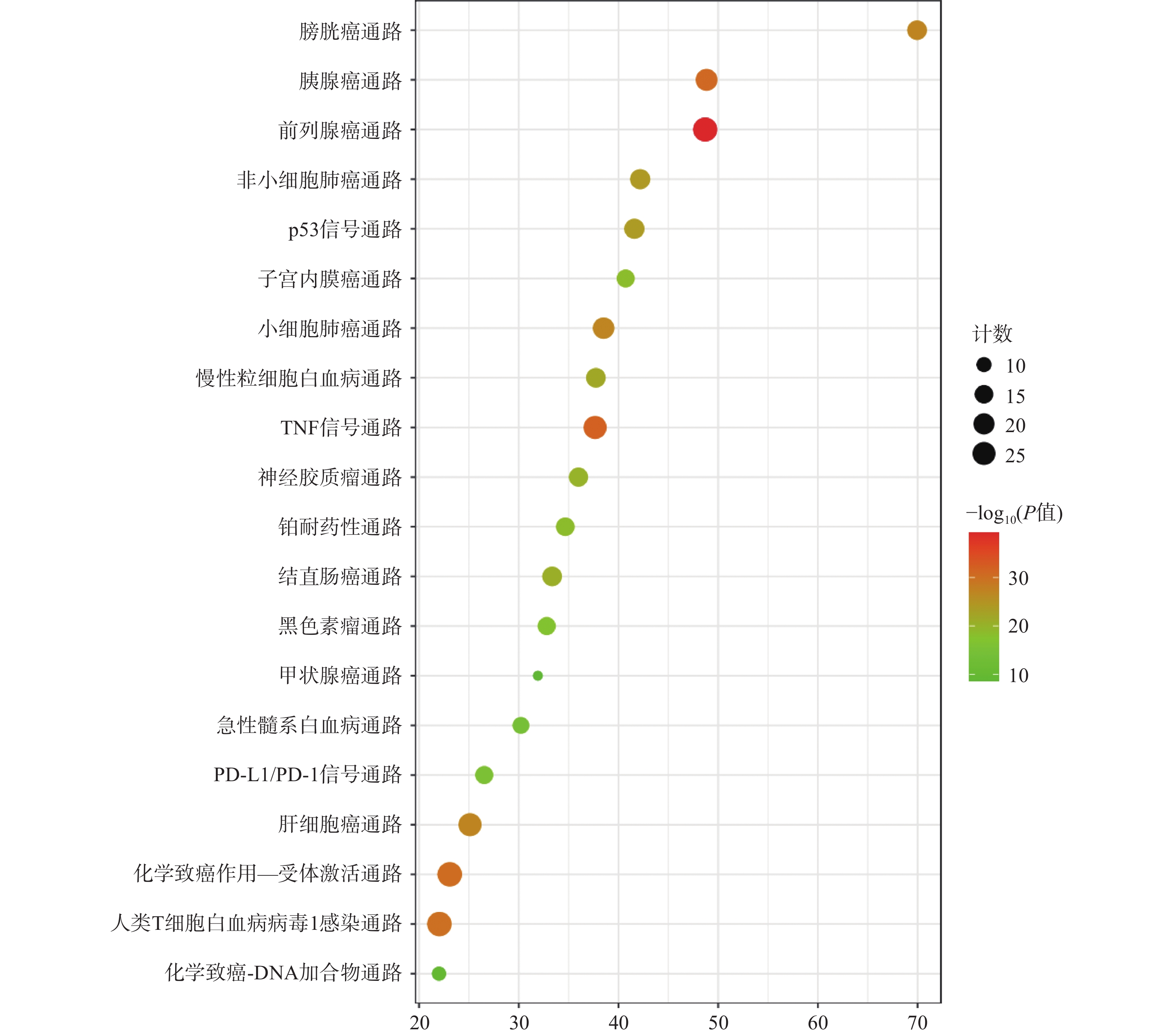
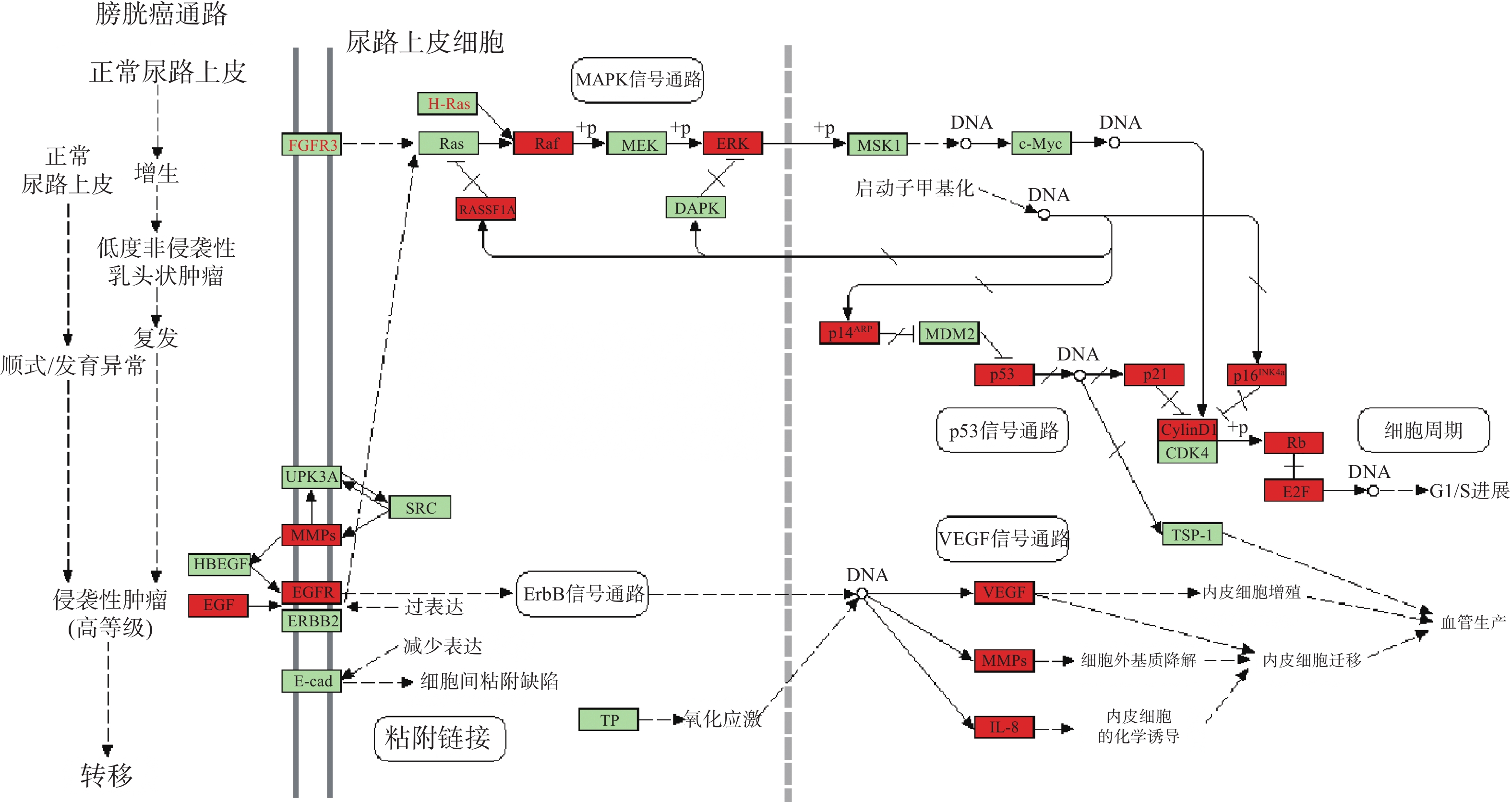
KEGG分析共富集到194条信号通路,其中34条癌症相关通路,并对前20条通路绘制气泡图(图4)。依据KEGG分析,西红花可能通过p53信号通路、TNF通路发挥抗肿瘤作用,可能对膀胱癌、胰腺癌、前列腺癌、非小细胞肺癌等肿瘤具有治疗作用,西红花靶点-通路相互作用网络见图5,红色三角形代表与肿瘤相关的信号通路,蓝色矩形代表关键靶点。其中,西红花通过膀胱癌信号通路调控EGF、MMPs、Raf、VEGF、ERK等基因发挥抗肿瘤作用(图6),红色矩形代表西红花可能干预的关键靶点。
2.6 分子对接
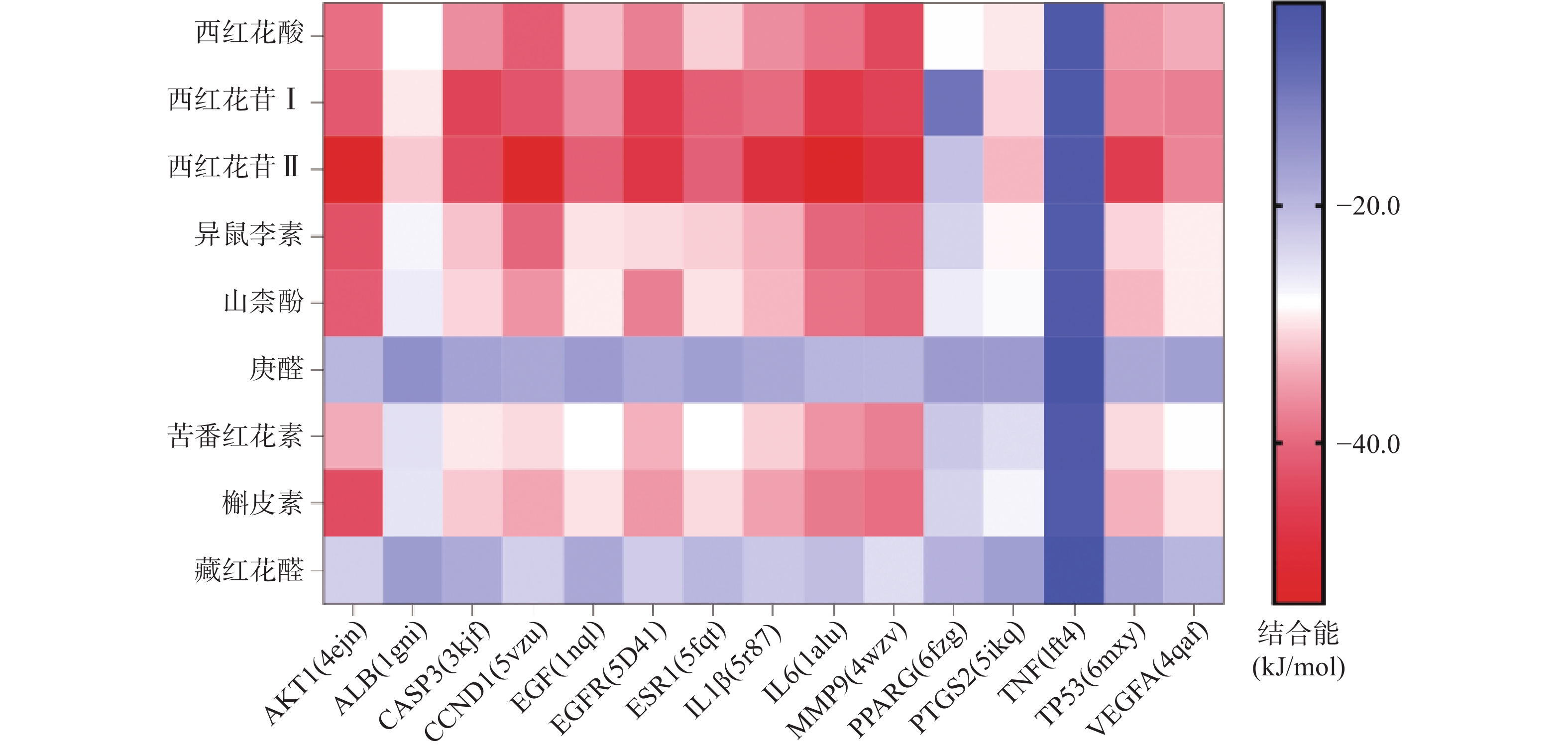
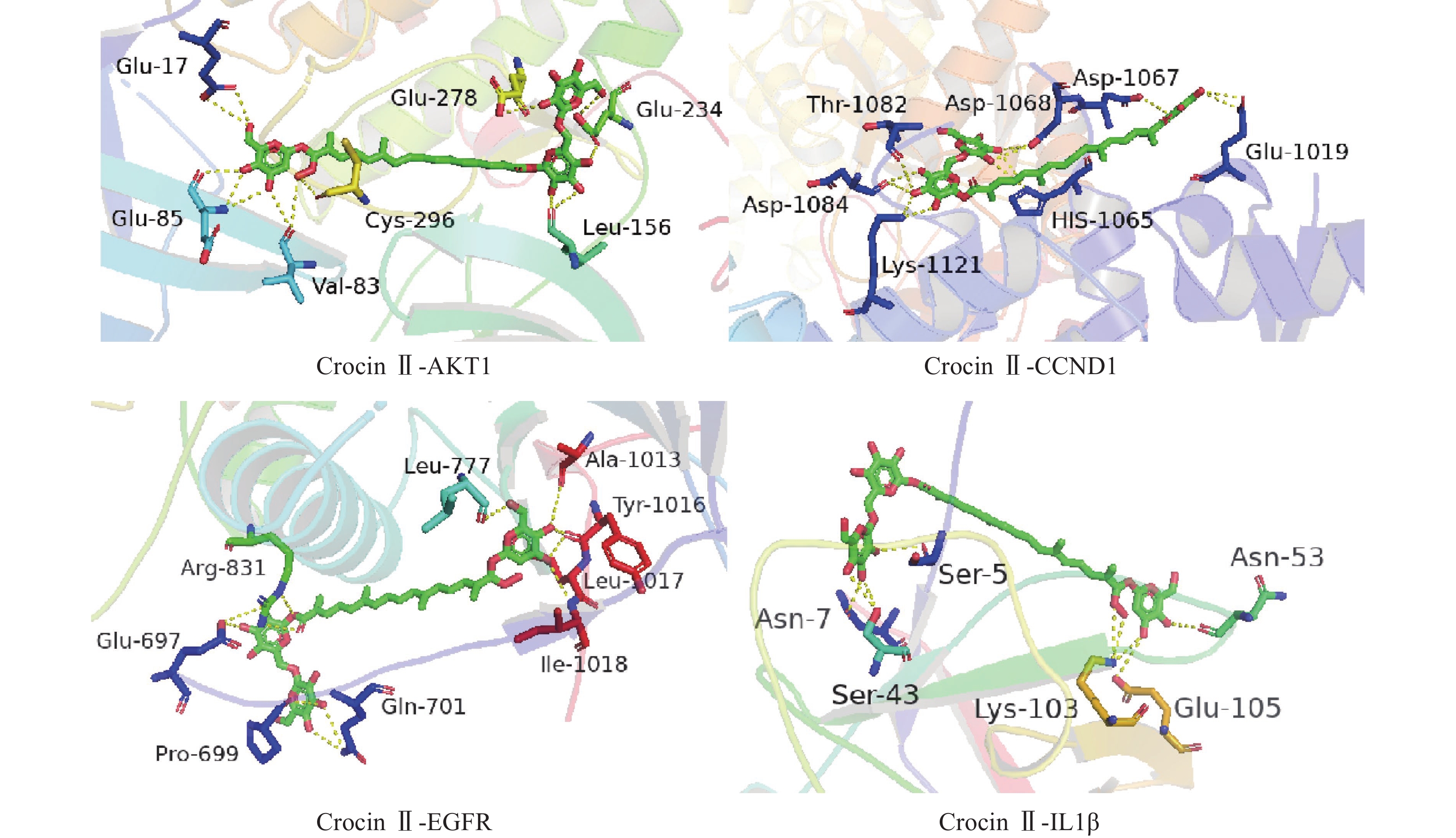
将前15个潜在核心靶点与西红花活性成分进行分子对接。结合能(affinity)<0表明配体分子能够与受体蛋白自发结合,结合能≤−17.78 kJ/mol表明配体与受体有一定的结合活性,结合能≤−20.92 kJ/mol 表明配体与受体有较好的结合活性,结合能≤−29.29 kJ/mol 表明配体与受体有强的结合活性[17],且结合能越低,表明对接的效果越好,结合的构象越稳定[18]。经AutoDock Vina对接,将得到的结合能数据使用热图展示(图7)。本研究结合自由能小于−20.92kJ/mol 的活性成分有102个,占75.6%;小于−29.29kJ/mol 的活性成分有73个,占54.1%,可见这些核心化合物与受体结合活性较高,结构相对稳定。选取结合能力最好的4个组合用Pymol软件进行可视化处理(图8)。
3. 讨论
肿瘤的发生和发展是多基因、多步骤的结果。中药多成分、多靶点的特点使其在肿瘤治疗方面有独特的优势。大量的临床实践表明,中药在治疗肿瘤中能够改善症状、提高患者生存质量、延长生存期等,有着其他治疗药物及手段不可替代的作用[19-20]。以中药黄芪为例,不仅可以通过Wnt5/β-catenin信号通路抑制肿瘤生长[21],同时具有通过PD-L1下调诱导耐药黑色素瘤的干性抑制和化疗敏感性增强的作用,可以减少化疗药物用量[22],还能充当免疫佐剂,提高患者免疫力,改善生存质量[23]。网络药理学最大的优势在于可以运用系统生物学的分析,为中药多成分、多靶点、多通路的机制研究提供有力的技术支撑[12],其分析理念和技术路径又与中医药治疗疾病的整体观相契合,已用于多种中药和中药复方作用机制的研究,如灯盏细辛、半枝莲等中药和茵陈蒿汤、桃红四物汤等中药复方,利用网络药理学的方法得到治疗机制的详细阐述和证明[24–27],为中药药理作用机制的探索提供了很好的参考。
本研究发现西红花中多种成分,如西红花酸、西红花苷等可与IL-6、AKT1、CCND1、IL-1β、MMP9、EGFR、TP53靶点产生适度结合,提示这些靶点可能是西红花中活性成分发挥抗肿瘤作用的关键靶点。研究发现,AKT1是PI3K-AKT-mTOR信号通路中的重要靶点,被磷酸化激活后可以促进细胞的增殖与存活,与肿瘤细胞的生长密切相关[28]。多项研究表明,通过抑制AKT1可以治疗肺癌、结肠癌、卵巢癌等多种实体癌[29]。EGFR与一些全球发病率和致死率高的癌症发病机制直接或间接相关,包括肺癌、乳腺癌和结直肠癌等[30]。当EGFR过度表达时,细胞表面会出现过量的受体,诱导正常的细胞转化为癌细胞,并为癌细胞持续生存提供条件[31]。CCND1是细胞周期家族的一员[32],公认的原癌基因,在甲状旁腺瘤、乳腺癌、肝癌及食管、肺、头颈部鳞状细胞癌的发生、发展过程中均起着重要作用[33-34]。西红花苷是由西红花酸和龙胆二糖或葡萄糖结合形成的二萜苷类化合物,西红花苷Ⅰ和西红花苷Ⅱ的差别在于分子中糖苷基数目的多少 [35]。西红花酸已具有抗肿瘤作用,以其为苷元形成的西红花苷同样也表现出较好的抗肿瘤活性,其中西红花苷Ⅱ的表现最好。西红花苷可以通过P53途径下调细胞周期蛋白d1和p21的表达,诱导细胞凋亡和细胞周期停滞,从而抑制肿瘤生长[36]。分子对接的结果与GO富集分析、KEGG通路富集分析结果一致,验证了网络药理学分析结果的正确性。
Buyun等学者在肝癌Hep3B和HepG2细胞中使用西红花苷抑制了IL-6对STAT3以及细胞周期蛋白D1的激活,验证了西红花对肝癌细胞的抗增殖,凋亡和阻断入侵作用[37]。在转移性乳腺癌的研究中,Ali等研究人员在体内和体外实验中均证明了西红花苷可以通过VEGF和MMP9下调发挥抗肿瘤作用,而且对乳腺癌的转移扩散有较好的抑制作用[38]。这些研究成果在一定程度上验证了利用网络药理学探究发现的西红花抗肿瘤作用机制的可行性。
综上所述,本研究利用网络药理学结合分子对接技术,探究西红花抗肿瘤作用的活性成分、作用靶点及信号通路。发现西红花抗肿瘤的作用具有多成分、多靶点、多通路、多机制的特点,其中以西红花苷为代表的西红花特有化学成分显示出了良好的抗肿瘤活性,可以在多条肿瘤发生通路中发挥作用,为西红花治疗肿瘤的深入研究提供了理论基础。但这些结果受限于各个数据库信息的片面性,而且只关注了成分,没有考量到成分的含量及其之间是否存在相互作用,预测的结果存在一定的片面性和局限性,需要进一步进行体内、外实验验证。
-
表 1 药物的已知途径、靶点和代谢途径摘要
药物类别 药物名称 已知通路或靶点 已知的代谢途径 激素 甲状腺素 LKB1/AMPK/mTOR 脂肪酸代谢 松弛素 – 脂肪酸合成、氨基酸代谢 雌激素 – 线粒体功能 合成药物 二甲双胍 PI3K-PKB/AKT、AMPK、PGC-1α 葡萄糖代谢、线粒体功能、氧化应激 SGLT2抑制剂 AMPK、 Na+/H+ 交换剂、NLRP3 炎症小体 酮代谢、线粒体功能、细胞内钠稳态、胰岛素信号传导、氧化应激 吡格列酮 PPAR γ 脂肪酸氧化,线粒体功能 辛伐他汀 iNOSitol、INCX、Rac1 线粒体功能,氧化应激 非诺贝特 PPARα 脂肪酸代谢 曲美他嗪 长链3-酮酰基辅酶A硫溶酶 葡萄糖代谢、脂肪酸代谢 卡维地洛 α1、β受体 脂肪酸代谢,线粒体功能 天然药物 白藜芦醇 SIRT1、CYP1B2 葡萄糖代谢、脂肪酸代谢、线粒体功能、胰岛素信号、钙2+浓度 人参皂苷Rb1 TGF-β1/SMAD ERK、AKT 葡萄糖代谢 人参皂苷Rb3 PPARα 脂肪酸代谢,线粒体功能 阿江榄仁酸 P47phox、ERK、PPARα、TAK1、p38 MAPK、NF-κB P65 葡萄糖代谢、线粒体功能、氧化应激 黄芪甲苷 PPARα、MCAD、MCP1 脂肪酸代谢,线粒体功能 麦冬多糖 AST、 LDH、CK、CK-MB、ATPase 线粒体功能 枸杞多糖 线粒体生物基因调控因子 脂肪酸代谢,线粒体功能 黄芪多糖 TNF-α/PGC-1 脂肪酸代谢 猪毛菜酚 – 线粒体功能 和乌胺 PPAR α/PGC-1α/SIRT3 线粒体功能 川芎嗪 miR-499a、SIRT1、PI3K/AKT 线粒体功能 -
[1] VIRANI S S, ALONSO A, APARICIO H J, et al. Heart disease and stroke statistics-2021 update: a report from the American heart association[J]. Circulation,2021,143(8):e254-e743. [2] PONIKOWSKI P, VOORS A A, ANKER S D, et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC[J]. Eur J Heart Fail,2016,18(8):891-975. doi: 10.1002/ejhf.592 [3] GUPTA A, HOUSTON B. A comprehensive review of the bioenergetics of fatty acid and glucose metabolism in the healthy and failing heart in nondiabetic condition[J]. Heart Fail Rev,2017,22(6):825-842. doi: 10.1007/s10741-017-9623-6 [4] RITTERHOFF J, TIAN R. Metabolism in cardiomyopathy: every substrate matters[J]. Cardiovasc Res,2017,113(4):411-421. doi: 10.1093/cvr/cvx017 [5] SANO H I, TOKI T, NAITO Y, et al. Developmental changes in the balance of glycolytic ATP production and oxidative phosphorylation in ventricular cells: a simulation study[J]. J Theor Biol,2017,419:269-277. doi: 10.1016/j.jtbi.2017.02.019 [6] LOPASCHUK G D, JASWAL J S. Energy metabolic phenotype of the cardiomyocyte during development, differentiation, and postnatal maturation[J]. J Cardiovasc Pharmacol,2010,56(2):130-140. doi: 10.1097/FJC.0b013e3181e74a14 [7] DE CARVALHO A E T S, BASSANEZE V, FORNI M F, et al. Early postnatal cardiomyocyte proliferation requires high oxidative energy metabolism[J]. Sci Rep,2017,7(1):15434. doi: 10.1038/s41598-017-15656-3 [8] HEGGERMONT W A, PAPAGEORGIOU A P, HEYMANS S, et al. Metabolic support for the heart: complementary therapy for heart failure? Eur J Heart Fail,2016,18(12):1420-1429. doi: 10.1002/ejhf.678 [9] WISNESKI J A, STANLEY W C, NEESE R A, et al. Effects of acute hyperglycemia on myocardial glycolytic activity in humans[J]. J Clin Invest,1990,85(5):1648-1656. doi: 10.1172/JCI114616 [10] MURTHY M S, PANDE S V. Malonyl-CoA binding site and the overt carnitine palmitoyltransferase activity reside on the opposite sides of the outer mitochondrial membrane[J]. Proc Natl Acad Sci USA,1987,84(2):378-382. doi: 10.1073/pnas.84.2.378 [11] PETERZAN M A, LYGATE C A, NEUBAUER S, et al. Metabolic remodeling in hypertrophied and failing myocardium: a review[J]. Am J Physiol Heart Circ Physiol,2017,313(3):H597-H616. doi: 10.1152/ajpheart.00731.2016 [12] DOENST T, NGUYEN T D, ABEL E D. Cardiac metabolism in heart failure: implications beyond ATP production[J]. Circ Res,2013,113(6):709-724. doi: 10.1161/CIRCRESAHA.113.300376 [13] AERNI-FLESSNER L, ABI-JAOUDE M, KOENIG A, et al. GLUT4, GLUT1, and GLUT8 are the dominant GLUT transcripts expressed in the murine left ventricle[J]. Cardiovasc Diabetol,2012,11:63. doi: 10.1186/1475-2840-11-63 [14] WANG Y, ZHU S, LIU H T, et al. Thyroxine alleviates energy failure, prevents myocardial cell apoptosis, and protects against doxorubicin-induced cardiac injury and cardiac dysfunction via the LKB1/AMPK/mTOR axis in mice[J]. Dis Markers,2019,2019:7420196. [15] MIRÓ Ò, HERRERO-PUENTE P, PRIETO B, et al. The subset of patients with acute heart failure able to secrete relaxin-2 at pregnancy concentrations could have a longer survival: a pilot study[J]. Biomarkers,2018,23(6):573-579. doi: 10.1080/1354750X.2018.1463564 [16] ARAGÓN-HERRERA A, FEIJÓO-BANDÍN S, ABELLA V, et al. Serelaxin (recombinant human relaxin-2) treatment affects the endogenous synthesis of long chain poly-unsaturated fatty acids and induces substantial alterations of lipidome and metabolome profiles in rat cardiac tissue[J]. Pharmacol Res,2019,144:51-65. doi: 10.1016/j.phrs.2019.04.009 [17] LARSEN A H, JESSEN N, NØRRELUND H, et al. A randomised, double-blind, placebo-controlled trial of metformin on myocardial efficiency in insulin-resistant chronic heart failure patients without diabetes[J]. Eur J Heart Fail,2020,22(9):1628-1637. doi: 10.1002/ejhf.1656 [18] JO W, KANG K K, CHAE S, et al. Metformin alleviates left ventricular diastolic dysfunction in a rat myocardial ischemia reperfusion injury model[J]. Int J Mol Sci,2020,21(4):1489. doi: 10.3390/ijms21041489 [19] SUN D, YANG F. Metformin improves cardiac function in mice with heart failure after myocardial infarction by regulating mitochondrial energy metabolism[J]. Biochem Biophys Res Commun,2017,486(2):329-335. doi: 10.1016/j.bbrc.2017.03.036 [20] BERTRAND L, GINION A, BEAULOYE C, et al. AMPK activation restores the stimulation of glucose uptake in an in vitro model of insulin-resistant cardiomyocytes via the activation of protein kinase B[J]. Am J Physiol Heart Circ Physiol,2006,291(1):H239-H250. doi: 10.1152/ajpheart.01269.2005 [21] CUSTODIO J S Jr, DURAES A R, ABREU M, et al. SGLT2 inhibition and heart failure-current concepts[J]. Heart Fail Rev,2018,23(3):409-418. doi: 10.1007/s10741-018-9703-2 [22] KOSIBOROD M N, JHUND P S, DOCHERTY K F, et al. Effects of dapagliflozin on symptoms, function, and quality of life in patients with heart failure and reduced ejection fraction: results from the DAPA-HF trial[J]. Circulation,2020,141(2):90-99. doi: 10.1161/CIRCULATIONAHA.119.044138 [23] DE BOER R A, NÚÑEZ J, KOZLOVSKI P, et al. Effects of the dual sodium-glucose linked transporter inhibitor, licogliflozin vs placebo or empagliflozin in patients with type 2 diabetes and heart failure[J]. Br J Clin Pharmacol,2020,86(7):1346-1356. doi: 10.1111/bcp.14248 [24] LEGCHENKO E, CHOUVARINE P, BORCHERT P, et al. PPARγ agonist pioglitazone reverses pulmonary hypertension and prevents right heart failure via fatty acid oxidation[J]. Sci Transl Med,2018,10(438):eaao0303. doi: 10.1126/scitranslmed.aao0303 [25] CHONG C R, CLARKE K, LEVELT E. Metabolic remodelling in diabetic cardiomyopathy[J]. Cardiovasc Res,2017,113(4):422-430. doi: 10.1093/cvr/cvx018 [26] HSIEH C C, LI C Y, HSU C H, et al. Mitochondrial protection by simvastatin against angiotensin II-mediated heart failure[J]. Br J Pharmacol,2019,176(19):3791-3804. doi: 10.1111/bph.14781 [27] CHO K I, KOO S H, CHA T J, et al. Simvastatin attenuates the oxidative stress, endothelial thrombogenicity and the inducibility of atrial fibrillation in a rat model of ischemic heart failure[J]. Int J Mol Sci,2014,15(8):14803-14818. doi: 10.3390/ijms150814803 [28] LI P, LUO S K, PAN C J, et al. Modulation of fatty acid metabolism is involved in the alleviation of isoproterenol-induced rat heart failure by fenofibrate[J]. Mol Med Rep,2015,12(6):7899-7906. doi: 10.3892/mmr.2015.4466 [29] LABINSKYY V, BELLOMO M, CHANDLER M P, et al. Chronic activation of peroxisome proliferator-activated receptor-alpha with fenofibrate prevents alterations in cardiac metabolic phenotype without changing the onset of decompensation in pacing-induced heart failure[J]. J Pharmacol Exp Ther,2007,321(1):165-171. doi: 10.1124/jpet.106.116871 [30] DHYANI N, SAIDULLAH B, FAHIM M, et al. Fenofibrate ameliorates neural, mechanical, chemical, and electrical alterations in the murine model of heart failure[J]. Hum Exp Toxicol,2019,38(10):1183-1194. doi: 10.1177/0960327119860173 [31] UNNO K, ISOBE S, IZAWA H, et al. Relation of functional and morphological changes in mitochondria to myocardial contractile and relaxation reserves in asymptomatic to mildly symptomatic patients with hypertrophic cardiomyopathy[J]. Eur Heart J,2009,30(15):1853-1862. doi: 10.1093/eurheartj/ehp184 [32] DALAL J J, MISHRA S. Modulation of myocardial energetics: an important category of agents in the multimodal treatment of coronary artery disease and heart failure[J]. Indian Heart J,2017,69(3):393-401. doi: 10.1016/j.ihj.2017.04.001 [33] NAGARA K, SUZUKI A, SHIGA T, et al. Long-term outcome of carvedilol therapy in Japanese patients with nonischemic heart failure[J]. Heart Vessels,2020,35(7):957-966. doi: 10.1007/s00380-020-01560-w [34] PODBREGAR M, VOGA G. Effect of selective and nonselective beta-blockers on resting energy production rate and total body substrate utilization in chronic heart failure[J]. J Card Fail,2002,8(6):369-378. doi: 10.1054/jcaf.2002.130238 [35] SPOLADORE R, FRAGASSO G, PERSEGHIN G, et al. Beneficial effects of beta-blockers on left ventricular function and cellular energy reserve in patients with heart failure[J]. Fundam Clin Pharmacol,2013,27(4):455-464. doi: 10.1111/j.1472-8206.2012.01029.x [36] CARAFA V, ROTILI D, FORGIONE M, et al. Sirtuin functions and modulation: from chemistry to the clinic[J]. Clin Epigenetics,2016,8:61. doi: 10.1186/s13148-016-0224-3 [37] SANTOS C N, GOMES A, OUDOT C, et al. Pure polyphenols applications for cardiac health and disease[J]. Curr Pharm Des,2018,24(19):2137-2156. doi: 10.2174/1381612824666180608102344 [38] WANG J R, ZHOU H, YI X Q, et al. Total ginsenosides of Radix Ginseng modulates tricarboxylic acid cycle protein expression to enhance cardiac energy metabolism in ischemic rat heart tissues[J]. Molecules,2012,17(11):12746-12757. doi: 10.3390/molecules171112746 [39] BANSAL T, CHATTERJEE E, SINGH J, et al. Arjunolic acid, a peroxisome proliferator-activated receptor α agonist, regresses cardiac fibrosis by inhibiting non-canonical TGF-β signaling[J]. J Biol Chem,2017,292(40):16440-16462. doi: 10.1074/jbc.M117.788299 [40] TANG B, ZHANG J G, TAN H Y, et al. Astragaloside IV inhibits ventricular remodeling and improves fatty acid utilization in rats with chronic heart failure[J]. Biosci Rep,2018,38(3):BSR20171036. doi: 10.1042/BSR20171036 [41] DONG Z W, ZHAO P, XU M, et al. Astragaloside IV alleviates heart failure via activating PPARα to switch glycolysis to fatty acid β-oxidation[J]. Sci Rep,2017,7:2691. doi: 10.1038/s41598-017-02360-5 [42] ZHANG R, XU Y, NIU H F, et al. Lycium barbarum polysaccharides restore adverse structural remodelling and cardiac contractile dysfunction induced by overexpression of microRNA-1[J]. J Cell Mol Med,2018,22(10):4830-4839. doi: 10.1111/jcmm.13740 [43] FAN S R, ZHANG J F, XIAO Q, et al. Cardioprotective effect of the polysaccharide from Ophiopogon japonicus on isoproterenol-induced myocardial ischemia in rats[J]. Int J Biol Macromol,2020,147((1):233-240. [44] MA J N, MENG X L, KANG S Y, et al. Regulatory effects of the fruit extract of Lycium chinense and its active compound, betaine, on muscle differentiation and mitochondrial biogenesis in C2C12 cells[J]. Biomed Pharmacother,2019,118:109297. doi: 10.1016/j.biopha.2019.109297 [45] LUAN A, TANG F, YANG Y, et al. Astragalus polysaccharide attenuates isoproterenol-induced cardiac hypertrophy by regulating TNF-α/PGC-1α signaling mediated energy biosynthesis[J]. Environ Toxicol Pharmacol,2015,39(3):1081-1090. doi: 10.1016/j.etap.2015.03.014 [46] VAKHRUSHEVA O, SMOLKA C, GAJAWADA P, et al. Sirt7 increases stress resistance of cardiomyocytes and prevents apoptosis and inflammatory cardiomyopathy in mice[J]. Circ Res,2008,102(6):703-710. doi: 10.1161/CIRCRESAHA.107.164558 [47] ZHANG N N, LIAN Z Q, PENG X Y, et al. Applications of higenamine in pharmacology and medicine[J]. J Ethnopharmacol,2017,196:242-252. doi: 10.1016/j.jep.2016.12.033 [48] HUANG B W, YOU J G, QIAO Y, et al. Tetramethylpyrazine attenuates lipopolysaccharide-induced cardiomyocyte injury via improving mitochondrial function mediated by 14-3-3γ[J]. Eur J Pharmacol,2018,832:67-74. doi: 10.1016/j.ejphar.2018.05.019 [49] QI D K, YOUNG L H. AMPK: energy sensor and survival mechanism in the ischemic heart[J]. Trends Endocrinol Metab,2015,26(8):422-429. doi: 10.1016/j.tem.2015.05.010 [50] WEI H M, WU H J, YU W, et al. Shenfu Decoction as adjuvant therapy for improving quality of life and hepatic dysfunction in patients with symptomatic chronic heart failure[J]. J Ethnopharmacol,2015,169:347-355. doi: 10.1016/j.jep.2015.04.016 [51] RUSSELL R R 3rd, LI J, COVEN D L, et al. AMP-activated protein kinase mediates ischemic glucose uptake and prevents postischemic cardiac dysfunction, apoptosis, and injury[J]. J Clin Invest,2004,114(4):495-503. doi: 10.1172/JCI19297 [52] SUN J, ZHANG K, XIONG W J, et al. Clinical effects of a standardized Chinese herbal remedy, Qili Qiangxin, as an adjuvant treatment in heart failure: systematic review and meta-analysis[J]. BMC Complement Altern Med,2016,16:201. doi: 10.1186/s12906-016-1174-1 -





 下载:
下载:

 下载:
下载: 

