-
尿石症的微创碎石术包括体外冲击波碎石术(ESWL),经输尿管镜碎石术(URL)和经皮肾镜取石术(PCNL)[1-3]。尿路感染是以上碎石术的最常见并发症,细菌或内毒素进入血流都可能导致败血症,这可能是致命的并发症[3-5]。近年来国内外有不少关于尿石症微创碎石术围手术期抗菌药物使用的指南共识和高质量研究结果发表,为围手术期抗菌药物使用提供了依据。但在泌尿外科碎石术临床实际工作中,仍存在多种不合理用药情况,如预防用药级别过高、联合用药不适宜,用药疗程过长等问题。为了遏制泌尿外科碎石术预防使用抗菌药物不合理使用现象的蔓延,在医院医务处牵头下,药剂科临床药师自2019年起协助泌尿外科管理碎石术预防使用的抗菌药物,并提供技术支持,经过4年的合理管控,产生了良好的效果。
-
优化目录和加大限量力度,先后将11个品规每月消耗金额上限分次逐步下调至12.5%;剔除异常增长品种;将8个与“三网”推荐目录相符性欠佳的品规,从本院供应目录剔除;要求科室主任组织科室人员学习抗菌药物合理使用,并签订抗菌药物使用强度逐步降低的目标责任状,每年结合医院整体的目标,根据各临床科室不同专业特点和上一年指标完成情况,个性化定制下一年的目标。
-
每月开展抗菌药物使用强度点评,每季度开展特殊使用级抗菌药物专项点评和异常增长抗菌药物的专项点评。临床药师进行逐个点评,分析科室用药特点,与临床科室沟通,分析不合理原因,最终形成报告。点评结果以合理用药点评简报和长海药学服务(药讯)的方式通过大周会、企业微信等多渠道向全院进行通报,并对部分不合理用药问题较为突出的科室和医生要求重新学习《抗菌药物临床应用指导原则( 2015 年版)》等指南规范。
-
强化事前审方规则基础维护工作,发动全科药师利用业余时间积极审核和拟定评价规则,调整、新增处方前置审核规则
3874 条,其中新增以抗菌药物为重点的规则195条,其中拦截性规则28条,提醒性规则167条。重点有计划地审核和设“用药适应证”及“禁忌证”这些非常重要但原有系统因技术困难却缺乏的规则,力求从合理用药系统的基础维护方面步步推进、打牢基础,不断完善信息化手段,在合理用药管理中发挥应有的作用。 -
抗菌药物科学化管理得到全院各科室的重视,临床科室主动要求临床药师开展抗菌药物合理应用系列专题讲座,如《泌尿相关的抗菌药物使用及强度分享》《药敏报告的解读》《头孢菌素过敏性休克不良反应的案例介绍》等。了解科室抗菌药物使用的盲点、弱点和担忧点,根据科室具体情况分析如何合理使用抗菌药物。
临床药师在全院多科室轮转,包括急诊科、呼吸科、肝胆胰腺外科、泌尿外科、脑外科、胃肠外科、肾内科、微生物室等,和医生一起解决临床实际问题。临床药师多次参加抗感染会诊,对特殊病理生理状态下患者抗菌药物选择,抗菌药物剂量、疗程把握以及不良反应判断和处理提供参考意见。
在《泌尿相关的抗菌药物使用及强度分享》中临床药师除向泌尿外科医生讲解抗菌药物使用强度的定义、临床意义、计算方法、影响因素等基础内容外,着重讲解了泌尿外科碎石术预防使用抗菌药物的合理选择。后续临床药师与泌尿外科医生持续保持沟通,及时解决泌尿外科提出的碎石术预防使用抗菌药物相关问题。
-
⑴临床药师开展临床路径用药规则审核完善工作,针对全院360余个临床路径涉及的抗菌药物品种选择、给药剂量和用药疗程等一系列问题进行评价和反馈。涉及泌尿系统碎石术预防用药的临床路径有3个,分别为经皮肾镜碎石术、输尿管结石行输尿管镜碎石术、肾结石行输尿管软镜碎石术治疗。
⑵抗菌药物临时采购审批启用企业微信,流程中增加临床药师审核。
⑶特殊使用级抗菌药物申请需通过企业微信进行审批,进一步提高院内信息化手段在合理用药管理中的作用。
-
临床科室积极配合整改。通过完善院前检查和抗菌药物治疗,降低HALF分类方法[6]中高危组患者的尿路细菌负荷后,再收入院开展碎石术。通过合理预防使用抗菌药物,有效的降低了抗菌药物使用率和使用强度。
-
从大数据中心的医院运营管理系统(Rbase系统)提取2019−2022年泌尿外科抗菌药物相关指标数据,主要分析泌尿外科住院抗菌药物使用率、微生物送检率、抗菌药物使用强度(AUD),以及泌尿系统碎石术预防使用抗菌药物消耗量排名和泌尿外科碳青霉烯类抗菌药物消耗量排名在管控前后的变化。数据采用 Microsoft Excel 16 统计和分析。
-
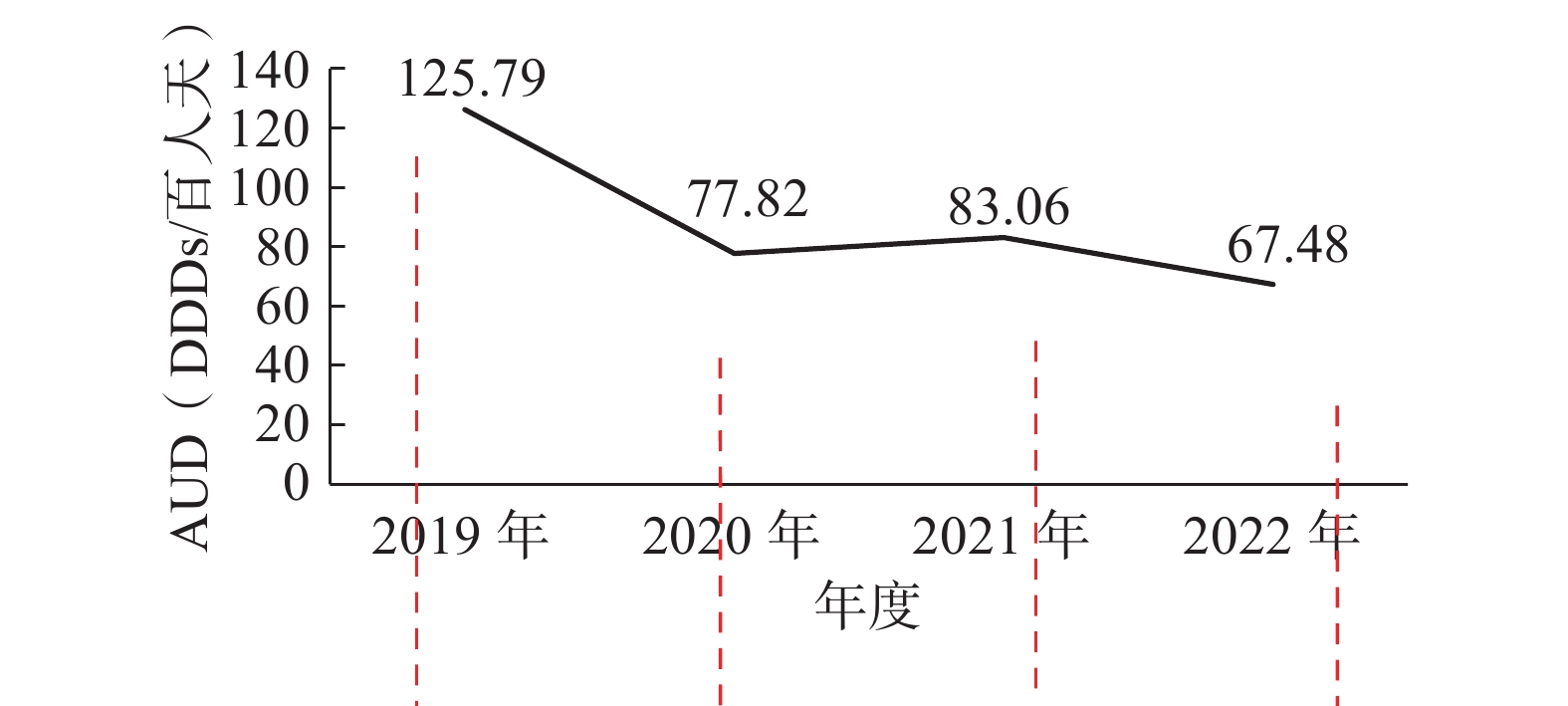
与2019年相比,2022年泌尿外科抗菌药物多项指标趋于达标,各项指标目标值来自于《关于进一步加强抗菌药物临床应用管理工作的通知》(国卫办医发〔2015〕42号)。住院抗菌药物使用率由94.27%下降为77.47%,但未达标(见表1);自2019年住院抗菌药物使用强度呈逐年下降趋势,如图1所示;由125.79 DDDs/百人天下降为67.48 DDDs/百人天,但未达标(见表1);微生物送检率(限制类)由2019年的42.71%上升至60.91%,符合要求(见表1)。
表 1 2019年和2022年泌尿外科抗菌药物指标详情
项目 2019 2022 目标值 住院抗菌药物使用率(%) 94.27 77.47 60 住院抗菌药物使用强度(DDDs/百人天) 125.79 67.48 40 微生物送检率(%) 39 52.74 30 微生物送检率(特殊类)(%) 91.69 93.66 80 微生物送检率(限制类)(%) 42.71 60.91 50 注:微生物送检率指接受抗菌药物治疗的住院患者微生物送检率;微生物送检率(特殊类)指接受特殊使用级抗菌药物治疗的住院患者微生物送检率;微生物送检率(限制类)指接受限制使用级抗菌药物治疗的住院患者微生物送检率。 -
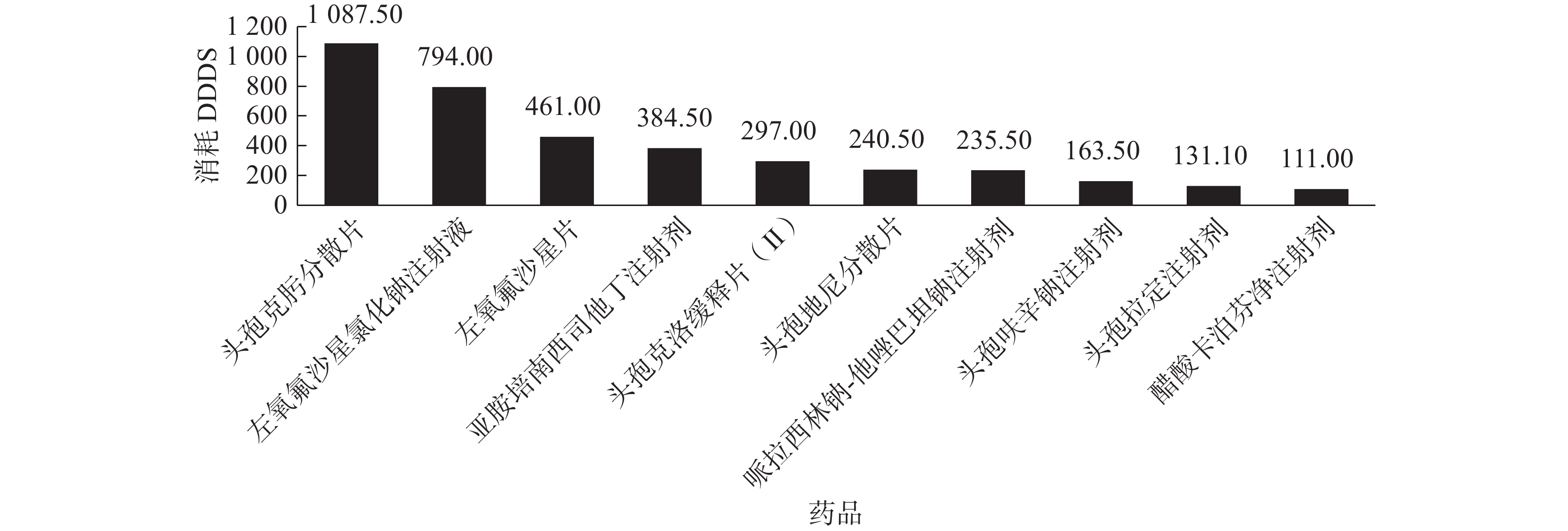
2019年泌尿系统碎石术预防使用抗菌药物消耗DDDs排名第一位的是头孢克肟分散片(
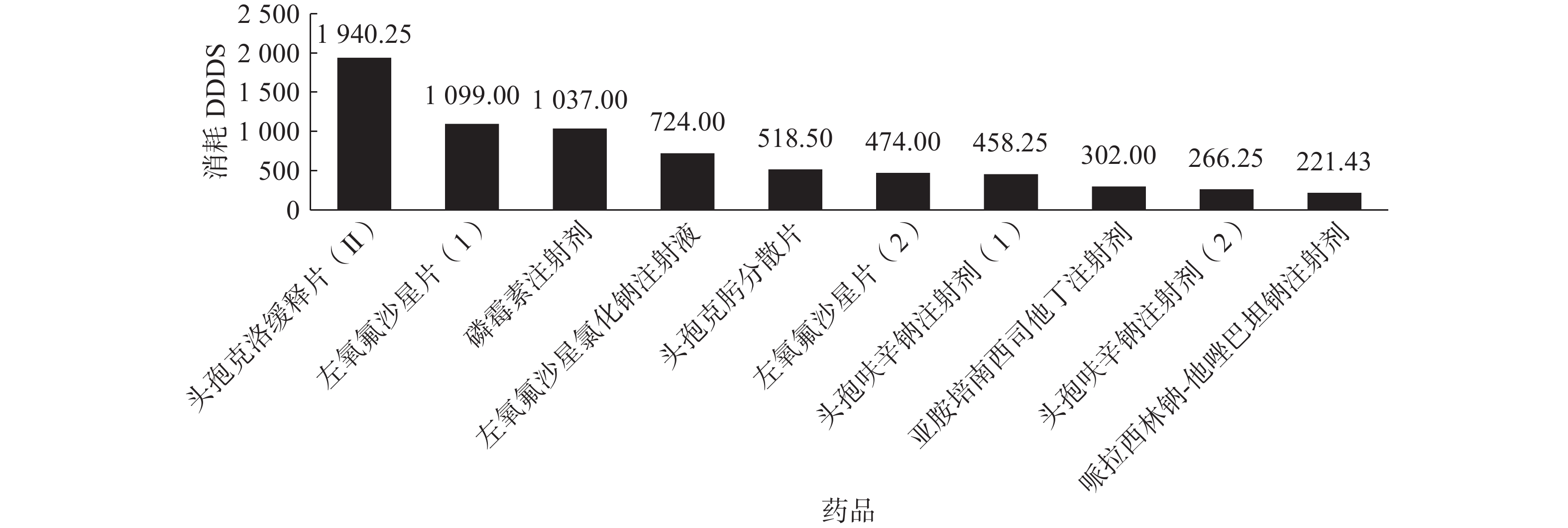
1087.50 DDDs),左氧氟沙星氯化钠注射液和亚胺培南西司他丁注射剂分别排名第三和第四,如图2所示。2022年泌尿系统碎石术预防使用抗菌药物消耗DDDs排名第一位的是头孢克洛缓释片(Ⅱ)(1940.25 DDDs),左氧氟沙星氯化钠注射液和亚胺培南西司他丁注射剂分别排名第四和第八,如图3所示。与2019年相比,2022年消耗DDDs排名第一位的抗菌药物由第三代头孢菌素变为第二代头孢菌素;左氧氟沙星氯化钠注射液排名下降一个位次,亚胺培南西司他丁注射剂排名下降明显,下降四个位次。 -
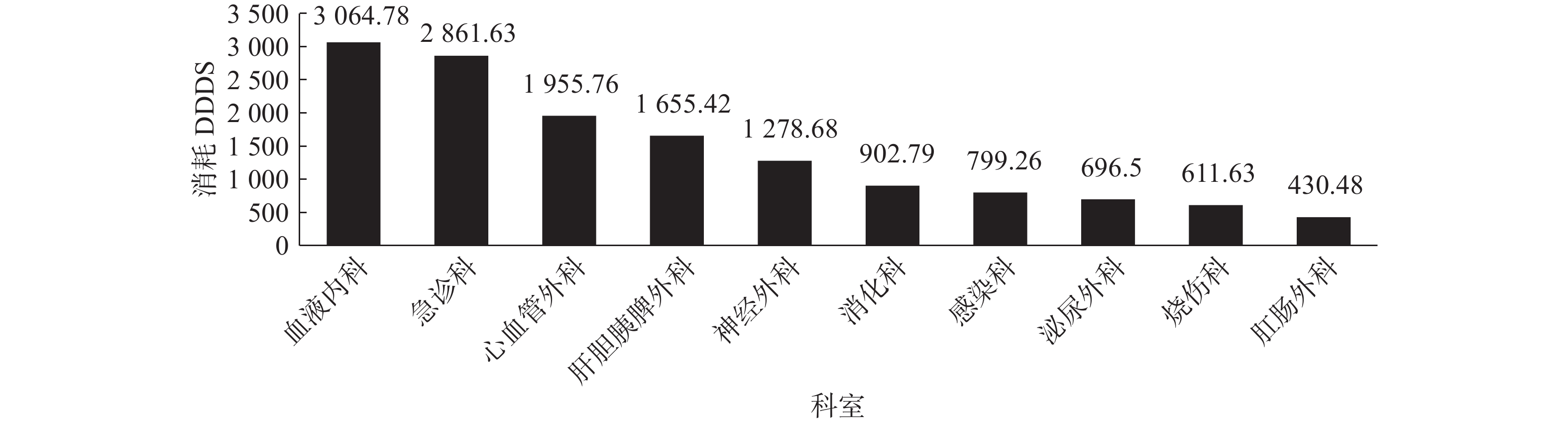
2019年全院碳青霉烯类抗菌药物消耗DDDs排名第一位科室是血液内科(
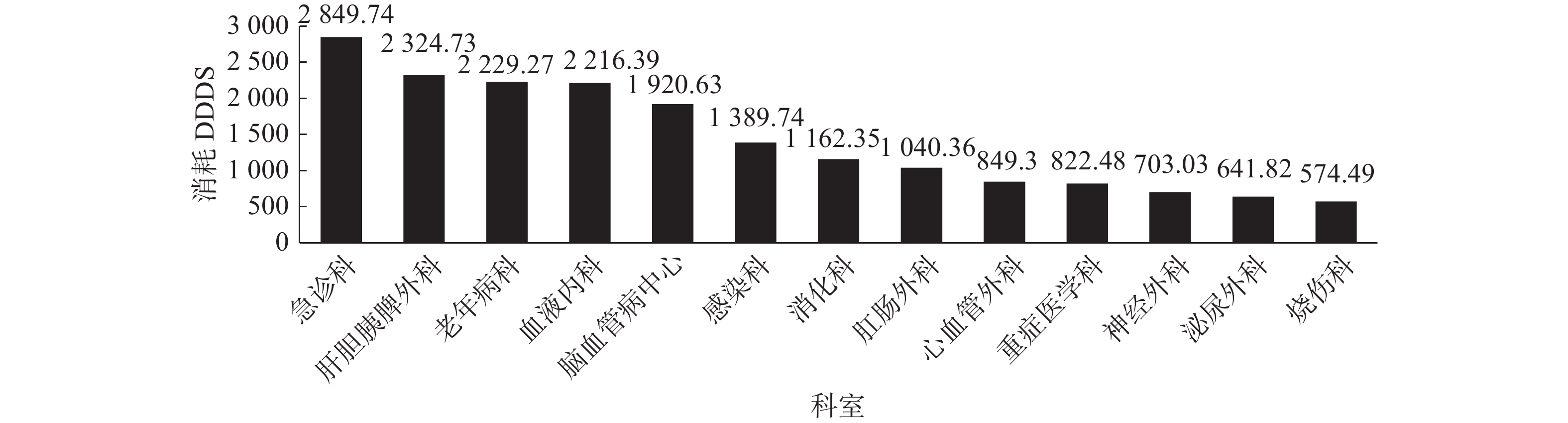
3064.78 DDDs),泌尿外科排名第八,碳青霉烯类抗菌药物消耗696.5 DDDs,如图4所示;2022年全院碳青霉烯类抗菌药物消耗DDDs排名第一位科室是急诊科,泌尿外科排名第十二,碳青霉烯类抗菌药物消耗641.82 DDDs,如图5所示。与2019年相比,碳青霉烯类抗菌药物消耗DDDs科室排名,泌尿外科下降四个位次。 -
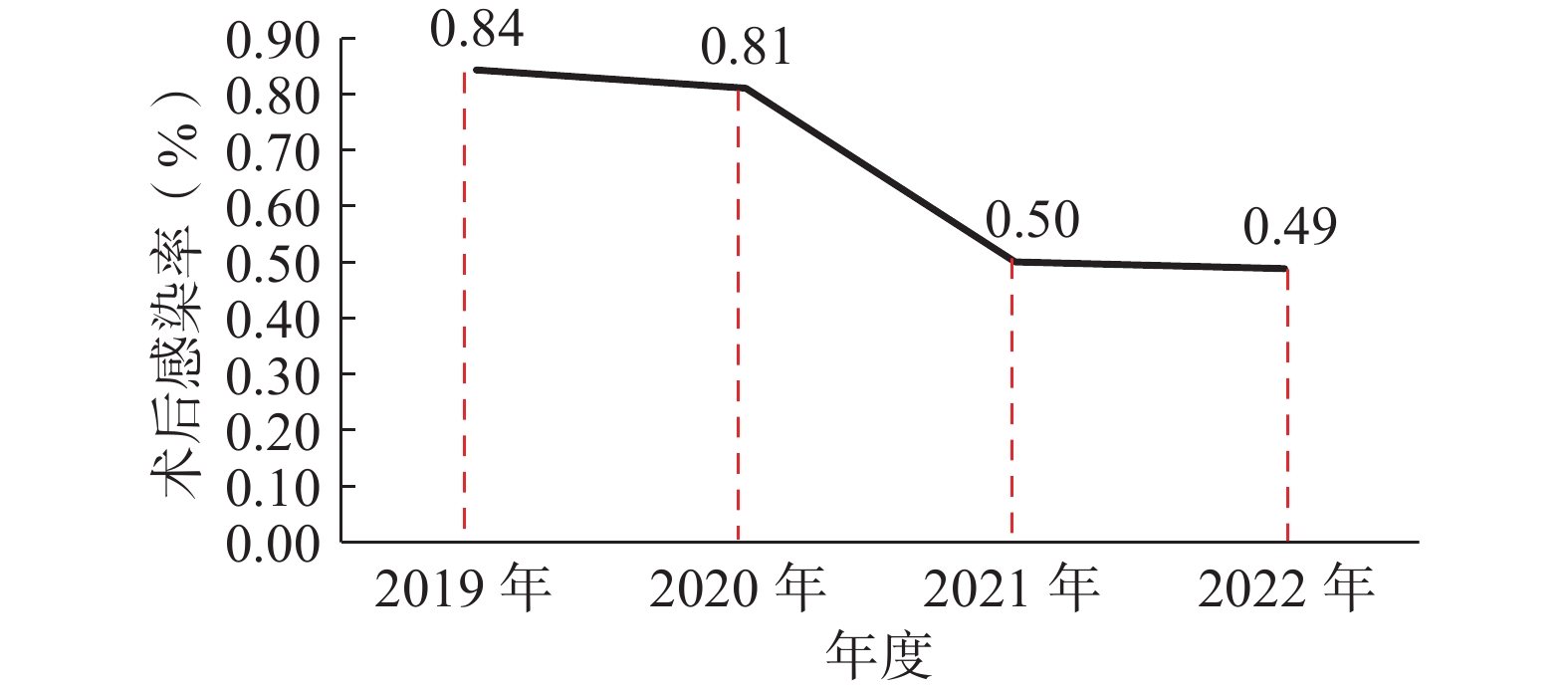
自2019年泌尿系统碎石术后感染的发生率呈逐年下降趋势,由2019年0.84%下降为0.49%,如图6所示。
-
目前国内外有越来越多的关于泌尿系统碎石术预防使用抗菌药物的指南共识,为尿路结石患者围手术期感染控制提供了很好的指导。但由于影响泌尿系统碎石术感染的因素较多[7-8],尿路感染的评价方法不同于常规感染,预防感染控制不佳会导致重症感染等原因,在临床实际工作中泌尿系统碎石术预防使用抗菌药物存在多种不合理问题,如选药品种起点较高、预防用药时间长和联合用药不适宜。其中较为突出的问题是选药品种起点较高,经点评发现有的病历甚至选用碳青霉烯类作为泌尿系统碎石术预防感染的抗菌药物,这一点在邵燕等[9]的报道中也有发现。关于泌尿系统碎石术预防感染的抗菌药物选择,国内一般推荐第一、二代头孢菌素或氟喹诺酮类[10], 国际上推荐的品种较多,有氟喹诺酮类,一、二代头孢菌素,氨基糖苷类+甲硝唑或克林霉素,阿莫西林/克拉维酸,氨苄西林/舒巴坦等[11-12]。碳青霉烯类往往会选作为尿路感染的治疗性抗菌药物[13-15] 。
针对泌尿外科抗菌药物使用强度过高, 泌尿系统碎石术预防使用碳青霉烯类情况较为普遍的问题,对该科抗菌药物的管控除了开展抗菌药物科学化管理,加强全院抗菌药物点评和通报,增补完善抗菌药物处方前置审核规则,临床药师深入临床进行培训与会诊以及通过信息化手段加强合理用药工作创新的全院举措外。针对泌尿系统碎石术抗菌药物预防使用,临床药师开展了《泌尿相关的抗菌药物使用及强度分享》专题讲座,对经皮肾镜碎石术、输尿管结石行输尿管镜碎石术、肾结石行输尿管软镜碎石术治疗临床路径涉及的抗菌药物进行评价和反馈。另科室积极配合整改,在入院之前通过降低尿路结石手术患者高危组尿路的细菌负荷后,再收入院开展碎石术,降低了围手术期感染的风险,避免了围手术期预防使用高级别的抗菌药物。
通过以上由面及点的科学化管理,2022年泌尿外科抗菌药物使用强度出现大幅降低,趋于目标值。泌尿系统碎石术预防使用碳青霉烯类的现象明显减少,主要体现在该科室碎石术预防使用抗菌药物消耗DDDs排名中亚胺培南西司他丁注射剂排名明显下降,以及全院碳青霉烯类抗菌药物消耗DDDs排名中泌尿外科名次明显下降。该科室使用碳青霉烯类抗菌药物不合理现象明显减少,与此同时泌尿系统碎石术后感染的发生率呈逐年下降趋势,说明以上院科两级的管控措施效果显著。
鉴于泌尿外科抗菌药物使用强度距离目标值还有一定差距,下一步除继续加强全院抗菌药物科学化管理外,临床药师需协助临床医生根据HALF分类方法,将拟进行碎石术患者进行分组后,再进行有针对性的术前准备和个体化的抗菌药物使用。最后希望通过全面的抗菌药物管控和精细化、个体化的用药指导,泌尿外科的抗菌药物使用强度达到目标值,泌尿系统碎石术抗菌药物预防使用更加合理。
Reasonable management and control practice of prophylactic use of antibiotics for urinary system lithotripsy
-
摘要:
目的 合理管控泌尿系统碎石术抗菌药物预防使用,并分析管控措施的成效。 方法 通过开展抗菌药物科学化管理,加强抗菌药物专项点评和合理用药信息通报,增补完善抗菌药物处方前置审核规则,临床药师深入临床进行培训与会诊,加强合理用药工作创新以及泌尿外科针对碎石术预防使用抗菌药物积极整改的多项措施,分析2019−2022年泌尿外科抗菌药物相关指标数据的变化。 结果 积极的合理管控后,泌尿外科抗菌药物使用强度逐年下降;住院患者抗菌药物使用率由2019年的94.27%下降为2022年的77.47%;各项微生物送检率于2022年都达标;泌尿系统碎石术预防使用抗菌药物消耗DDDs品种排名中亚胺培南西司他丁注射剂由2019年的第四位下降为2022年的第八位;碳青霉烯类抗菌药物消耗DDDs全院科室排名中泌尿外科由2019年的第八位下降为2022年的第十二位;与此同时泌尿系统碎石术后感染的发生率呈逐年下降趋势,由2019年的0.84%下降为2022年的0.49%。 结论 积极的管控措施可促进泌尿系统碎石术抗菌药物预防使用趋于合理。 Abstract:Objective To analyze the effectiveness of reasonable control measures for prophylactic use of antibiotics for urinary system lithotripsy. Methods By antimicrobial stewardship, strengthening special comments on antibiotics and information notification on rational use of antibiotics, adding and improving the pre-review rules for antibiotics prescriptions, conducting in-depth clinical training and consultation by clinical pharmacists, strengthening innovation in rational use of drugs, and taking various measures to actively improve rational use of prophylactic antibiotics of lithotripsy in urology department, the changes of indexes related to antibiotics in urology department from 2019 to 2022 were analyzed. Results After active and reasonable control, Antibiotics Use Density in urology department decreased year by year. The utilization rate of antibiotics in inpatients decreased from 94.27% in 2019 to 77.47% in 2022. Various rate of microbial inspection reached the standard in 2022; The imipenem and cilastatin sodium for injection ranking of prophylactic use of antibiotics consumption DDDs for urinary system lithotripsy decreased from the 4th place in 2019 to the 8th place in 2022. The ranking of the urology department on carbapenem consumption DDDs in the whole hospital decreased from the 8th place in 2019 to the 12th place in 2022. At the same time, the incidence of urinary tract lithotripsy postoperative infection showed a decreasing trend year by year, from 0.84% in 2019 to 0.49% in 2022. Conclusion Positive control measures can promote the rational use of prophylactic antibiotics for urinary system lithotripsy. -
结直肠癌(CC)发生率占所有肿瘤发生率的第3位,病死率仅次于肺癌,属于下消化系统恶性肿瘤[1]。目前,结肠癌的治疗主要采用多学科的综合治疗模式[2]。包括5-氟尿嘧啶、奥沙利铂与贝伐珠单抗等的组合[3-5]。然而,这些常规的化疗方案可能造成患者不耐受以及骨髓等的抑制。因此,寻找新的有效的药物对于现今结肠癌治疗具有重要意义。
紫杉醇(PTX)是一种广谱抗肿瘤活性的化疗药物,来源于太平洋紫杉树皮(红豆杉)[6,7]。临床试验结果表明,PTX在几种癌症治疗中有较好的活性,包括:乳腺癌、皮肤恶性肿瘤、非小细胞肺癌以及卵巢癌等[8,9]。然而,由于结肠癌中过表达的P糖蛋白(P-gp)引起了多重耐药性(MDR),导致PTX对结肠癌临床治疗效果不甚理想[10]。此外,PTX生物半衰期短,其一代药物Taxol以聚氧乙烯蓖麻油为表面活性剂,具有引起患者过敏反应的风险,从而限制了PTX临床疗效的发挥[11]。因此,迫切需要对PTX进行结构改进与剂型设计,改善其药物递送效率,提高生物利用度[12]。
脂肪酸作为生物膜和生物信号分子的重要成分,参与了细胞能量产生、代谢的过程。由于肿瘤细胞增殖快速,需要大量的细胞合成物质和能量的供应,因此,患有恶性肿瘤的患者其脂肪酸合成也较快。其中,肿瘤细胞因为迅速繁殖对含有16个碳原子的棕榈酸(PA)为主的脂肪酸需求量大,因此利用PA进行修饰有利于药物被肿瘤细胞摄取[13,14]。再者,研究发现,由PA修饰的紫杉醇,能降低其对P-gp的亲和力,避免了PTX进入肿瘤细胞后的外排,提高紫杉醇对于结肠癌治疗的有效性[15]。
此外,作为一种成熟的药物载体,脂质体(Lip)在体内可被降解、无毒性和免疫原性,能够增强药物在体内的稳定性,从而可以减少给药剂量、降低毒副作用,并且其表面具有可修饰性[16],例如,采用聚乙二醇磷脂(PEG-DSPE)修饰的脂质体因其空间位阻效应可延长其在体内的循环时间[17]。同时结合肿瘤组织的增强通透性和滞留效应(EPR),使药物通过被动靶向递送到靶部位[18]。
结合以上背景,本研究首先通过棕榈酸酯与紫杉醇共价键结合构建紫杉醇棕榈酸酯(PTX-PA),并建立基于高效液相(HPLC)的定量分析方法,旨在降低其对P-gp的亲和力,避免PTX进入肿瘤细胞后被外排,从而改善紫杉醇毒性较大、生物半衰期短、成药性差等问题,提高紫杉醇对于结肠癌治疗的有效性。其次,我们将PTX-PA包载进PEG修饰的脂质体构建紫杉醇棕榈酸酯的脂质体(PTX-PA/Lip),以实现其长循环,增加PTX的疗效、降低其毒副作用。最后,采用工艺筛选与单因素处方优化的方法制备最佳PTX-PA/Lip,为PTX-PA的制剂学研究奠定基础[19]。
1. 仪器与材料
1.1 仪器
高效液相色谱仪(安捷伦科技有限公司,美国);十万分之一电子天平(MS105DU,梅特勒托利多公司,瑞士);超滤管(30 kD,密理博公司,美国);低温高速离心机(Eppendorf-200,艾本德公司,德国);高压均质机(NanoGenizer,美国);Zeta-sizer Nano粒度仪(Nano-ZS,马尔文公司,英国)。
1.2 试剂与材料
紫杉醇购自江苏红豆杉生物科技股份有限公司,纯度≥98%;棕榈酸购自中国医药集团上海化学试剂公司,纯度≥99%;蛋黄卵磷脂(PC98-T)、胆固醇、DSPE-PEG 2000均购自上海艾韦特医药科技有限公司;1-(3-二甲氨基丙基)-3-乙基碳二亚胺(EDC)、4-二甲氨基吡啶(DMAP)、乙酸乙酯、二氯甲烷、无水乙醇、石油醚均购自中国医药集团上海化学试剂公司,分析纯;乙酸乙酯、PC-98T蛋黄卵磷脂(上海艾韦特医药科技有限公司);胆固醇(上海艾韦特医药科技有限公司);二氯甲烷、DSPE-PEG 2000(上海艾韦特医药科技有限公司);无水乙醇、石油醚购自中国医药集团上海化学试剂公司;甲醇购自美国默克公司,色谱纯。
2. 方法
2.1 PTX-PA的制备与纯化
PTX-PA前药由PTX与PA发生酯化反应合成,其合成过程如下[20,21]:精密称取PTX 0.85 g,加入无水二氯甲烷 30 ml。依次加入精密称取的EDC 0.19 g、DMAP 0.15 g和PA 0.31 g,在氮气保护下室温搅拌反应12 h。反应结束后,用5%柠檬酸水溶液、饱和食盐水洗涤3遍,旋蒸除去有机溶剂,即得PTX-PA粗品。采用石油醚和乙酸乙酯通过柱层析法对PTX-PA进行分离、纯化。洗脱完成后,将产物旋蒸去除有机溶剂,得到的白色固体即为PTX-PA,样品经核磁共振氢谱、碳谱确定为PTX-PA,样品纯度98.5%。
2.2 基于HPLC定量检测的方法学建立[22]
2.2.1 最大吸收波长测定与色谱条件设定
精密取适量的PTX-PA粉末,采用甲醇溶解,定容,通过全波长(190~400 nm)扫描测定其紫外最大吸收波长λmax。
本实验采用Agilent Eclipse plus C18色谱柱(4.6 mm×250 mm,5 μm),流动相采用甲醇/水(95∶5,V/V),进样量20 μl,流速1.0 ml/min。
2.2.2 样品溶液配制
空白溶液的配制:精密量取不含药的空白脂质体1 ml加入适量的甲醇溶液,超声,用甲醇定容至25 ml,0.45 μm的微孔滤膜过滤,滤液即为空白溶液。
对照品溶液的配制:精密称取PTX-PA 粉末50 mg,用甲醇溶解并定容至50 ml,过滤,即得PTX-PA对照品储备溶液。
供试品溶液的配制:精密量取1 ml PTX-PA/Lip,加入适量甲醇溶解、超声破乳、定容至25 ml,过滤,滤液即为供试品溶液。
2.2.3 专属性考察
分别取适量空白溶液、对照品溶液和供试品溶液,用流动相稀释至适当的浓度后,按照“色谱条件”中建立的高相液相参数进行进样分析。
2.2.4 线性关系考察
精密量取适量PTX-PA对照品储备液依次稀释为浓度1、5、10、25、50、100 μg/ml的PTX-PA系列浓度。按照“色谱条件”中的高效液相参数进行进样分析(n=5),并记录不同浓度的PTX-PA的色谱峰面积。以浓度(C)为X轴、峰面积(A)为Y轴进行回归。
2.2.5 精密度考察
日内精密度考察:精密吸取3种不同浓度(5、25、100 μg/ml)的 PTX-PA对照品溶液,对同一浓度溶液连续进样5次,每次10 µl,按照“2.2.1”项下色谱条件进行分析,记录各个浓度吸收峰面积。
日间精密度考察:精密吸取3种不同浓度(5、25、100 μg/ml)的 PTX-PA对照品溶液,对同一浓度溶液连续进样5 d,每天1次,每次10 µl,按照“2.2.1”项下色谱条件进行分析,记录第0、1、2、3、4天的吸收峰面积,计算样品浓度,考察仪器的日间精密度。
2.2.6 重复性与稳定性
空白脂质体超声破乳,配制成3种不同浓度(1、10、100 μg/ml),连续进样5次,每次10 µl,记录各吸收峰面积,考察重复性。精密吸取浓度为50 μg/ml的 PTX-PA供试品溶液,于0、2、4、6、8、12、24 h进样测定,每次进样10 µl,记录各紫外吸收峰面积,考察样品的稳定性。
2.2.7 加样回收率考察
空白脂质体超声破乳,分别加入浓度为1 mg/ml的PTX-PA溶液0.5、2.5、5 ml,采用流动相稀释定容至100 ml,分别进样,并结合PTX-PA的理论浓度(5、25、50 μg/ml)进行加样回收率的计算与分析。
2.3 紫杉醇棕榈酸酯脂质体PTX-PA/Lip的制备
2.3.1 PTX-PA/Lip的制备方法的选择
(1) 薄膜分散法
精密称取PTX-PA 20 mg、蛋黄卵磷脂350 mg、胆固醇5 mg和DSPE-PEG2000 25 mg,加入适量的二氯甲烷使其充分溶解。然后旋蒸除去有机溶剂,使圆底烧瓶底部形成一层均匀透明的薄膜,再加入预热至同等温度的重蒸水10 ml,震荡、水化,得PTX-PA/Lip粗品。将得到的粗品经探头超声(1 min)、过滤处理后,即得PTX-PA/Lip纳米给药系统[19]。
(2) 高压均质法
将薄膜分散法制得的PTX-PA/Lip粗品置于高压均质机中,经3次均质处理后(均质压力12 000 psi),即得PTX-PA/Lip纳米给药系统[23,24]。
(3)挤出法
将薄膜分散法制得的PTX-PA/Lip粗品置于挤出器中,使分别经过孔径为0.2、0.1、0.05 μm的聚碳酸酯膜,即得PTX-PA/Lip纳米给药系统[25-27]。
2.3.2 处方工艺筛选
(1)磷脂种类的选择
采用薄膜分散法考察不同磷脂制备的PTX-PA/Lip,包括:氢化磷脂(HSPC)、蛋黄卵磷脂(PC98-T)、蛋黄磷脂(EPCS)、二棕榈酸磷脂酰胆碱(DPPC),以形态、粒径、包封率为指标进行评价。
(2)磷脂和药物/胆固醇比例的考察
分别以磷脂和药物的质量比(5∶1、10∶1、20∶1、30∶1、40∶1)/PC98-T和胆固醇的质量比(4∶0.05、4∶0.1、4∶0.2、4∶0.3、4∶0.4、4∶0.5)为自变量制备PTX-PA/Lip脂质体,考察不同处方的粒径、粒径分布、包封率,确定处方中磷脂与药物/胆固醇的质量比。
(3)药物和DSPE-PEG2000比例的考察
以PTX-PA和DSPE-PEG2000的质量比(1∶0.5、1∶1、1∶1.5、1∶2、1∶2.5)为自变量,考察其用量对制剂的外观澄明度、纳米粒子大小等是否产生影响。
(4)薄膜蒸发法的温度考察
将旋转蒸发仪温度分别设置为35、40、45、50、55 ℃,考察薄膜蒸发过程中温度对PTX-PA/Lip形态、粒径、包封率等的影响。
(5)探头超声时间的考察
以探头超声PTX-PA/Lip粗品的时间为自变量,考察不同超声时间(30、60、90、180、240 s)对PTX-PA/Lip纳米制剂形态、纳米粒子大小的影响。
2.4 统计学分析
数据采用IBM SPSS Statistics 27.0进行统计分析,采用单因素方差分析ANOVA进行显著性检验与评价。
3. 结果与讨论
3.1 基于PTX-PA的HPLC定量检测方法学建立
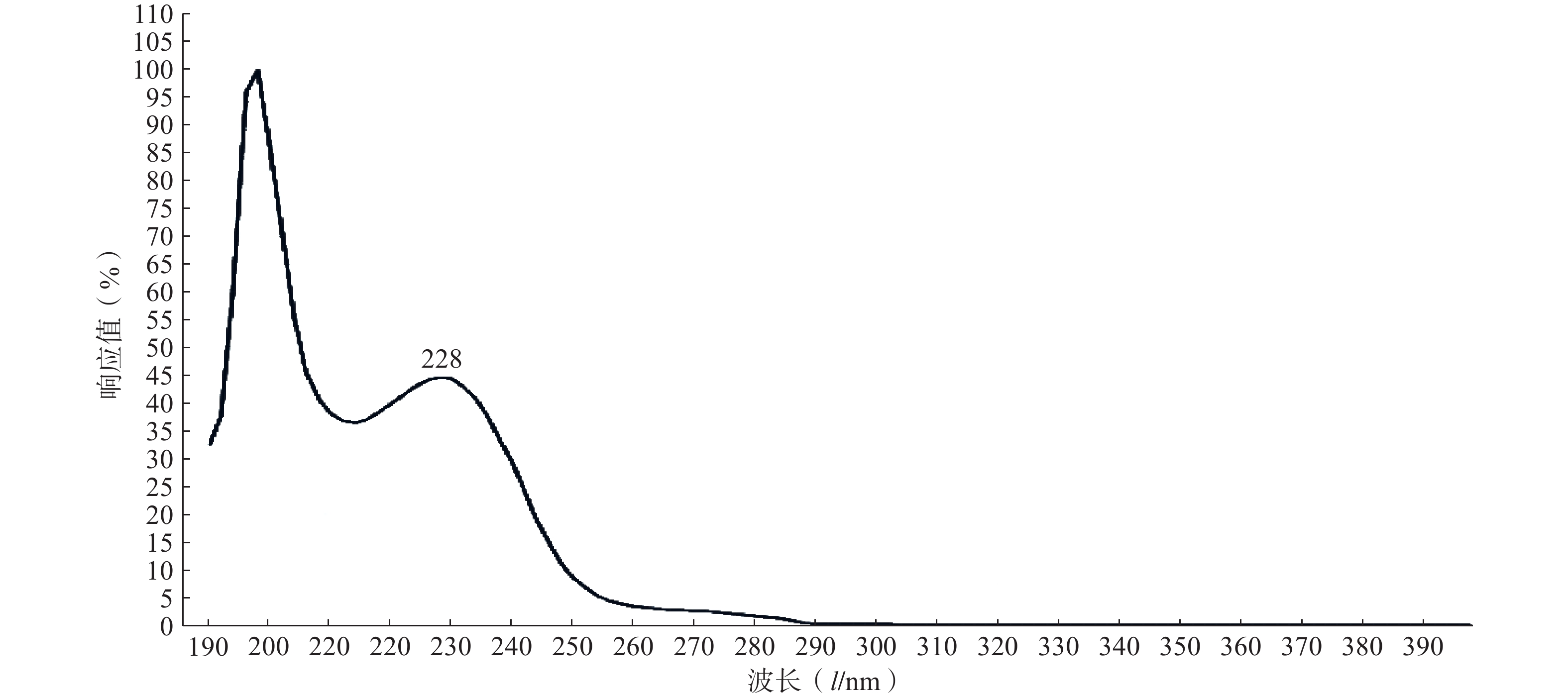
3.1.1 最大吸收波长的选择
实验结果如图1所示,选用PTX-PA的最大吸收波长为228 nm为测定波长。
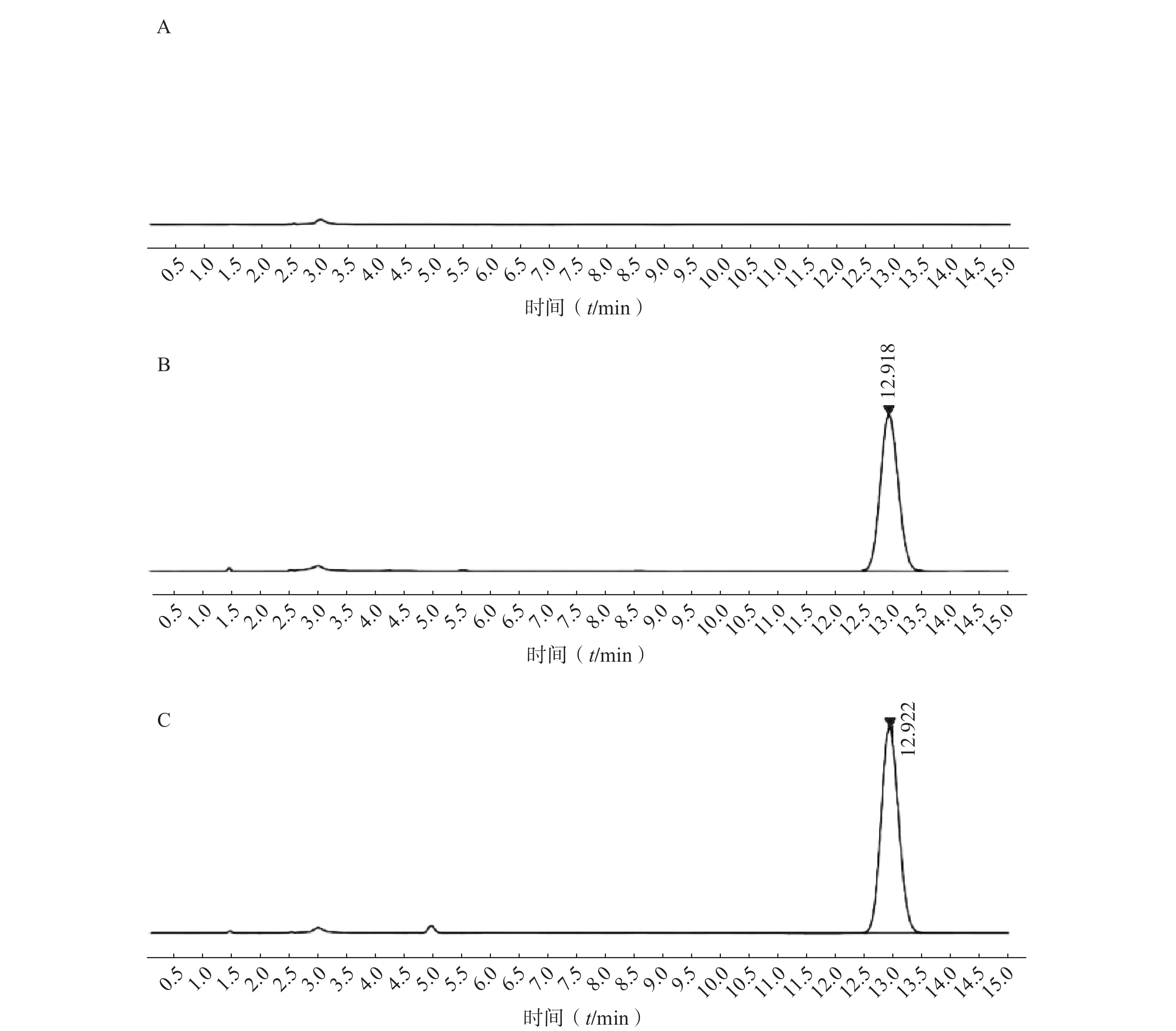
3.1.2 专属性考察
如图2所示,本章所建立的色谱条件对PTX-PA检测具有专属性,溶剂以及样品中的辅料对PTX-PA的检测不产生干扰。
3.1.3 线性关系考察
按照2.2.4方法进行回归,得PTX-PA的吸收峰面积-浓度在1~100 μg/ml的浓度范围内为线性方程:A=15.14 C+10.81(r=0.999 8)。
3.1.4 精密度考察
按照2.2.5方法进行精密度考察,结果如表1所示,日内与日间精密度各时间点峰面积的RSD均小于3%,表明仪器的日内与日间精密度符合测定要求。
表 1 PTX-PA的精密度考察结果(n=5)理论浓度(μg/ml) 实测浓度(μg/ml) RSD(%) 日内 5.00 4.98±0.13 2.65 25.00 25.30±0.55 2.18 100.00 99.66±1.11 1.11 日间 5.00 4.99±0.11 2.31 25.00 25.50±0.57 2.23 100.00 100.65±1.38 1.37 3.1.5 重复性与稳定性
按照2.2.6方法进行研究,精密吸取3种不同浓度的 PTX-PA溶液,连续进样5次并记录各吸收峰面积。各浓度峰面积RSD均<3%,表明仪器符合检测检测要求。此外,稳定性结果表明,样品溶液峰面积的RSD为0.81%,表明制备的PTX-PA溶液在24 h内稳定。
3.1.6 加样回收率
按照2.2.7方法计算加样回收率,结果如表2所示:低、中、高3个浓度的加样回收率均在95%~105%之间,且RSD分别为2.39%、1.80%、2.34%,表明本实验建立的高效液相色谱定量方法可用于PTX-PA的含量测定。
表 2 PTX-PA的加样回收率测试结果(n=5)理论浓度(μg/ml) 检测浓度(μg/ml) 回收率(%) RSD(%) 5 5.02±0.12 100.4 2.39 25 24.98±0.45 99.92 1.80 50 50.01±1.17 100.02 2.34 3.2 紫杉醇棕榈酸酯脂质体的制备及处方优化
3.2.1 PTX-PA/Lip制备方法的选择
采用不同方法制备的PTX-PA/Lip表征结果如表3所示,按照2.4方法进行统计学分析,3种制备方法的包封率无显著性差异,但采用薄膜分散法制备的PTX-PA/Lip粒径与PDI更小。因此,本研究优选薄膜分散法来构建PTX-PA/Lip。
表 3 3种常规制备方法对PTX-PA/Lip粒径、粒径分布、包封率的影响制备方法 粒径(l/nm) PDI 包封率(%) 薄膜分散法 76.76±3.39 0.104±0.02 79.38±2.00 高压均值法 125.11±5.32 0.139±0.03 78.87±2.00 挤出法 128.87±4.92 0.239±0.05 81.38±1.11 3.2.2 处方工艺筛选
(1)磷脂种类的选择
按照2.3.2(1)制备的PTX-PA/Lip表征结果如表4所示,以PC98-T为膜材制备的纳米给药系统粒径小、外观澄明、粒径分布均匀、包封率较高,因此选择PC98-T作为本研究中的磷脂。
表 4 磷脂种类对脂质体的外观形态、颗粒大小、药物包封率的影响磷脂种类 外观 粒径(l/nm) PDI 包封率(%) PC98-T 半透明 76.76±3.39 0.104±0.02 79.38±2.00 HSPC 有沉淀 177.86±5.39 0.532±0.08 59.06±1.32 EPCS 半透明 135.12±5.65 0.108±0.03 73.23±1.15 DPPC 有沉淀 158.26±4.11 0.669±0.05 53.27±2.68 (2)磷脂和药物比例的考察
按照2.3.2(2)项下确定处方中药物和磷脂的用量,其结果如表5所示,磷脂PC98-T和药物的质量比大于10时,制备的PTX-PA/Lip外观澄明度、粒子大小、粒径分散系数等参数无显著性差别。随着磷脂浓度不断增加,药物的包封率不断增加,当PC98-T和PTX-PA的质量比为20∶1时,脂质体对药物的包封率最高,后期考虑到经济成本,将PC98-T和PTX-PA的质量比定为20∶1。
表 5 磷脂和药物质量比对脂质体的外观澄明度、颗粒大小、对药物包封率的影响磷脂∶药物 外观 粒径(l/nm) PDI 包封率(%) 5∶1 略透明 134.62±2.95 0.364±0.04 58.15±1.73 10∶1 有沉淀 90.29±4.66 0.151±0.04 71.56±1.60 20∶1 半透明 84.58±1.33 0.11±0.02 83.50±0.92 30∶1 半透明 86.06±2.71 0.09±0.05 73.44±4.44 40∶1 有沉淀 88.86±1.91 0.199±0.05 68.37±11.08 (3)磷脂和胆固醇比例的考察
按照2.3.2(2)方法研究,结果如表6所示,随着胆固醇用量增多,制剂变浑浊,粒径增大,载药量显著降低。因此,胆固醇不加入本制剂的处方中。
表 6 磷脂和胆固醇质量比对脂质体外观澄明度、颗粒大小、对药物包封率的影响磷脂∶胆固醇 外观 粒径(l/nm) PDI 包封率(%) 4∶0.05 半透明 115.37±4.48 0.200±0.07 71.57±1.28 4∶0.1 半透明 160.16±3.15 0.251±0.01 61.08±3.13 4∶0.2 半透明 182.75±2.43 0.217±0.04 54.97±0.95 4∶0.3 乳白色 241.90±12.09 0.697±0.12 54.11±1.64 4∶0.4 乳白色 255.33±8.27 0.700±0.138 48.84±0.78 (4)药物和DSPE-PEG2000比例的考察
按照2.3.2(3)方法研究,其结果如表7所示,DSPE-PEG2000对包封率没有显著性影响,但当DSPE-PEG2000含量不断增加时,纳米粒子的颗粒大小先降低,当药物与DSPE-PEG2000质量比小于1∶1.5时,粒径无显著性变化,因此,药物与DSPE-PEG2000的质量比选择1∶1.5。
表 7 PTX-PA和DSPE-PEG2000的质量比对脂质体外观、粒径、药物包封率的影响药物∶DSPE-
PEG2000外观 粒径(l/nm) PDI 包封率(%) 2∶1 半透明 82.86±2.15 0.107±0.01 90.48±0.49 1∶1 半透明 78.16±2.05 0.351±0.38 90.41±0.34 1∶1.5 半透明 72.23±2.60 0.110±0.02 89.66±1.25 1∶2 半透明 74.64±1.81 0.140±0.04 90.90±2.93 1∶2.5 半透明 75.38±2.10 0.097±0.04 89.48±0.67 (5)薄膜蒸发法的温度考察
按照2.3.2(4),采用不同温度制备纳米制剂表征结果如表8所示,在筛选的5个温度中,当温度为45 ℃时,脂质体粒径最小、粒径分散性好、包封率最高,因此,本研究选用45 ℃作为薄膜蒸发温度。
表 8 温度对PTX-PA/Lip外观、粒径、包封率的影响温度(T/ ℃) 外观 粒径(l/nm) PDI 包封率(%) 35 略透明 159.42±2.42 0.545±0.08 54.94±1.85 40 半透明 105.93±6.13 0.269±0.03 73.98±1.60 45 半透明 76.97±2.50 0.105±0.049 91.13±1.45 50 半透明 91.93±2.60 0.181±0.05 80.27±2.13 55 半透明 112.23±6.37 0.233±0.06 74.15±2.12 (6)探头超声时间的考察
按照2.3.2(5)方法进行研究,结果如表9所示:处理时间较短时,纳米粒径较大,颗粒大小分布不均匀;随着超声处理的延长,粒径减小,包封率也提高;超声时间过长,脂质体结构破坏,导致药物泄露、包封率降低。因此将探头超声处理时间定为90 s。
表 9 超声处理对脂质体的外观澄明度、颗粒大小、对药物包封率的影响超声时间(t/s) 外观 粒径(l/nm) PDI 包封率(%) 30 沉淀 278.09±4.73 0.857±0.10 42.83±2.76 60 半透明 113.21±11.16 0.485±0.04 54.96±2.41 90 半透明 78.13±2.78 0.055±0.02 92.74±0.77 180 半透明 123.17±8.39 0.430±0.08 76.29±1.76 240 沉淀 261.85±4.94 0.915±0.20 50.42±2.74 3.3 紫杉醇棕榈酸酯脂质体PTX-PA/Lip的理化性质表征
综上研究,采用的最优处方和制备工艺如下:精密称取PTX-PA 20 mg、PC98-T 400 mg、DSPE-PEG2000 30 mg,加入适量二氯甲烷溶解,接着45 ℃旋蒸去除有机溶剂,再向圆底烧瓶底部薄膜中加入10 ml重蒸水(预热至同等温度),震荡、水化,得PTX-PA/Lip粗品,最后粗品探头超声(90 s)、过滤(0.22 μm),得最终样品PTX-PA/Lip纳米给药系统。
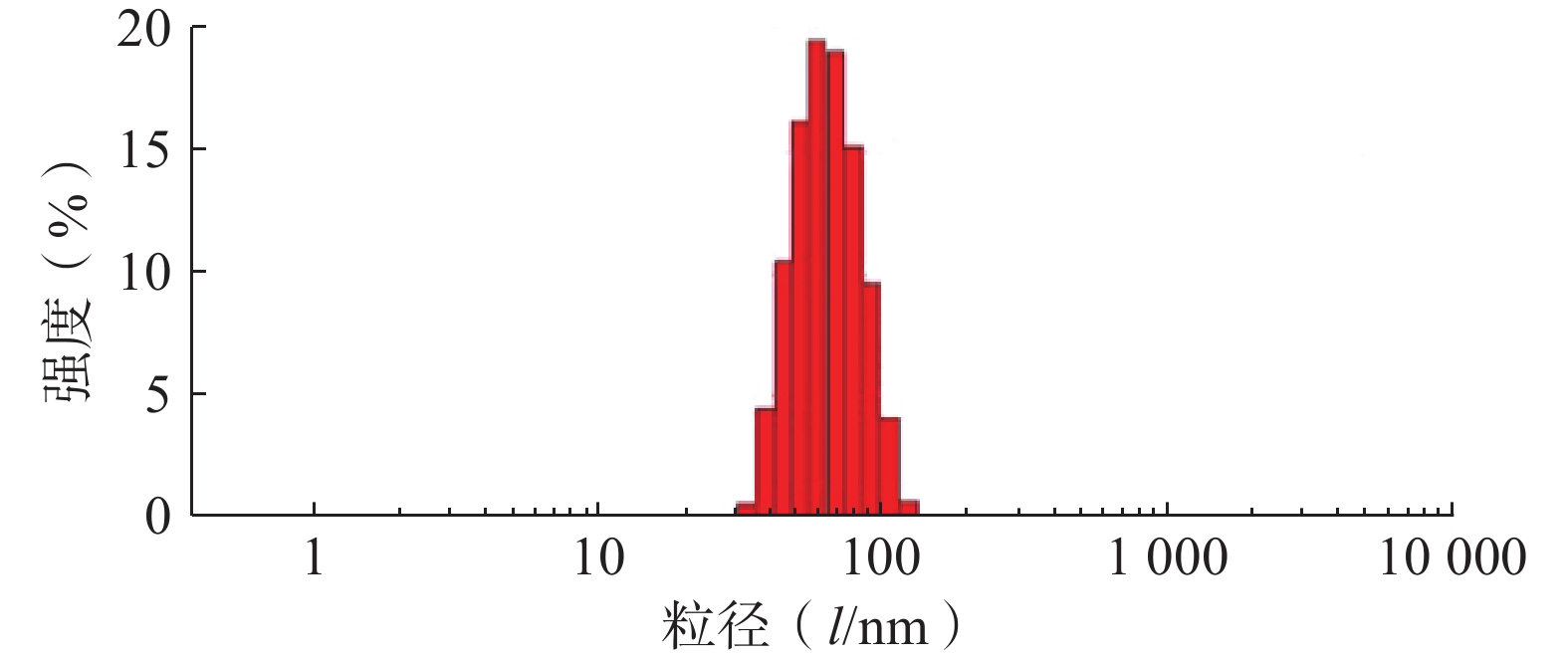
采用Zeta-sizer Nano粒度仪测定最优PTX-PA/Lip的粒径、PDI与zeta电位。结果如图3所示,制备的PTX-PA/Lip脂质体粒径大小为(62.75±1.81) nm,PDI为(0.076±0.020),Zeta电位为(−15.9±0.21) mV,表明制备的PTX-PA/Lip纳米给药系统粒径较小、分布均匀、具有良好的分散性。
4. 总结
本实验合成紫杉醇前药——紫杉醇棕榈酸酯PTX-PA,建立PTX-PA的HPLC定量测定方法,经一系列方法学验证,表明其符合PTX-PA定量分析要求,为后续试验奠定了基础。本实验采用薄膜分散法制备PTX-PA脂质体,工艺简便,技术成熟,并通过单因素筛选对PTX-PA脂质体进行处方优化。本文基于纳米技术成功制备出棕榈酸修饰的紫杉醇脂质体,增强了紫杉醇在靶细胞的递送,为PTX-PA后续的药效学研究奠定基础。
-
表 1 2019年和2022年泌尿外科抗菌药物指标详情
项目 2019 2022 目标值 住院抗菌药物使用率(%) 94.27 77.47 60 住院抗菌药物使用强度(DDDs/百人天) 125.79 67.48 40 微生物送检率(%) 39 52.74 30 微生物送检率(特殊类)(%) 91.69 93.66 80 微生物送检率(限制类)(%) 42.71 60.91 50 注:微生物送检率指接受抗菌药物治疗的住院患者微生物送检率;微生物送检率(特殊类)指接受特殊使用级抗菌药物治疗的住院患者微生物送检率;微生物送检率(限制类)指接受限制使用级抗菌药物治疗的住院患者微生物送检率。 -
[1] SKOLARIKOS A, JUNG H, NEISIUS A, et al. EAU Guidelines on urolithiasis [J]. European Association of Urology Guidelines 2023 edition, 2023: 1-120. https://d56bochluxqnz.cloudfront.net/documents/ full-guideline/ EAU-Guidelines-on-Urolithiasis-2023.pdf. [2] GERAGHTY R M, DAVIS N F, TZELVES L, et al. Best practice in interventional management of urolithiasis: an update from the European association of urology guidelines panel for urolithiasis 2022[J]. Eur Urol Focus, 2023, 9(1):199-208. doi: 10.1016/j.euf.2022.06.014 [3] 泌尿外科手术部位感染预防中国专家共识编写组. 泌尿外科手术部位感染预防中国专家共识(2019版)[J]. 中华泌尿外科杂志, 2019, 40(6):401-404. doi: 10.3760/cma.j.issn.1000-6702.2019.06.001 [4] 上尿路结石围手术期感染控制及抗菌药物应用专家意见编写组. 上尿路结石患者围手术期感染控制及抗菌药物应用专家意见(2023版)[J]. 中华泌尿外科杂志, 2023, 44(7):481-485. [5] BONKAT G, BARTOLETTI R, BRURUYÈRE F, et al. EAU Guidelines on Urological Infections[J]. European Association of Urology Guidelines 2023 edition, 2023: 1-84. [6] 乔庐东, 陈山, 马小军, 等. 上尿路结石患者围手术期抗菌药物应用的专家意见[J]. 中华泌尿外科杂志, 2017, 38(9):641-643. [7] CHEN D, JIANG C H, LIANG X F, et al. Early and rapid prediction of postoperative infections following percutaneous nephrolithotomy in patients with complex kidney stones[J]. BJU Int, 2019, 123(6):1041-1047. doi: 10.1111/bju.14484 [8] ZHOU G M, ZHOU Y, CHEN R, et al. The influencing factors of infectious complications after percutaneous nephrolithotomy: a systematic review and meta-analysis[J]. Urolithiasis, 2022, 51(1):17. doi: 10.1007/s00240-022-01376-5 [9] 邵燕, 刘群, 张东萍, 等. 我院特殊诊疗操作中预防性使用抗菌药物调查分析[J]. 中国药房, 2017, 28(26):3624-3627. doi: 10.6039/j.issn.1001-0408.2017.26.07 [10] 国卫办医发[2015]43号附件. 抗菌药物临床应用指导原则(2015年版). (2015-08-27)[2023-07-01]. https://www.gov.cn/xinwen/2015-08/27/content_2920799.htm. [11] WOLF J S Jr, BENNETT C J, DMOCHOWSKI R R, et al. Best practice policy statement on urologic surgery antimicrobial prophylaxis[J]. J Urol, 2008, 179(4):1379-1390. doi: 10.1016/j.juro.2008.01.068 [12] NABER KG. SCHAEFFER AJ. HEYNS CF, et a1. EAU-ICUD Urogenital infections [M]. First edition. The Netherlands: European Association of Urology-International Consultation on Urological Diseases, 2010: 645-710. [13] PORTSMOUTH S, VAN VEENHUYZEN D, ECHOLS R, et al. Cefiderocol versus imipenem-cilastatin for the treatment of complicated urinary tract infections caused by Gram-negative uropathogens: a phase 2, randomised, double-blind, non-inferiority trial[J]. Lancet Infect Dis, 2018, 18(12):1319-1328. doi: 10.1016/S1473-3099(18)30554-1 [14] TAN X M, PAN Q W, MO C G, et al. Carbapenems vs alternative antibiotics for the treatment of complicated urinary tract infection: a systematic review and network meta-analysis[J]. Medicine, 2020, 99(2):e18769. doi: 10.1097/MD.0000000000018769 [15] 黄茹润. 碳青霉烯类抗菌药物治疗复杂性尿路感染疗效和安全性的Meta分析[D]. 大理: 大理大学, 2021. -





 下载:
下载:
 下载:
下载: