-
雀梅藤Sageretia thea(Osbeck)Johnst又名雀梅刺、对角刺、碎米子等,为鼠李科雀梅藤属植物,主要分布地区包括云南、安徽、江苏等[1-2]。根、茎、叶均可入药,其性甘、淡、平,具有降气化痰、祛风利湿等功效[3]。民间常用雀梅藤药材煎汤或浸酒内服治疗乳腺肿瘤、淋巴结肿大和水肿等疾病,具有较好效果[4]。现代药理研究表明,雀梅藤具有抗结直肠癌、抗炎、抗氧化、抗病毒、抗菌和肝保护等活性[5-6],但尚未见雀梅藤对乳腺癌等其他肿瘤影响的报道。该研究通过多种体外实验观察雀梅藤对乳腺癌细胞增殖及凋亡的影响,并初步探索其作用机制,以证实民间应用该药材治疗乳腺肿瘤的合理性,为进一步的药物开发奠定基础。
-
CCK8 试剂盒(大连美仑生物技术有限公司);Spark酶标仪(瑞士Tecan公司);二氧化碳培养箱(Thermo Fisher);96孔培养板(泰坦);电子分析天平(塞多利斯 BSA2245-CW);细胞计数仪(Corning 6749);倒置相差显微镜(奥林巴斯 IX73)。
-
雀梅藤药材购自昆明井田药业有限公司,生产许可证号:滇20160155。经海军军医大学药学系生药学教研室辛海量教授鉴定为鼠李科雀梅藤属植物雀梅藤Sageretia thea(Osbeck)Johnst.的茎。取雀梅藤干燥药材660 g,粉碎后用8倍量75%乙醇回流提取3次,每次1.5 h。合并提取液,过滤后回收溶剂,得乙醇提取物。乙醇提取物用水溶解混悬,加入等体积的石油醚萃取3次,收集萃取液,通过旋转蒸发得到石油醚萃取部位。进一步采用真空冷冻干燥机在−80 ℃下冻干,分别称重,获得乙醇和石油醚提取物质量为57 g和0.91 g,提取得率分别为8.63%和0.13%。
-
称取20 mg雀梅藤石油醚提取物溶于1 ml的DMSO溶剂中,然后用培养液稀释成不同药物浓度,药物最高剂量下的DMSO浓度不超过0.3%。同时,对照组培养液中添加0.3%的DMSO作为阴性对照。
-
三阴性人乳腺癌细胞株MDA-MB-231、BT549购自中国科学院上海细胞库;人脐静脉血管内皮细胞株购自上海赋望实业有限公司。
-
分别取对数生长期的人三阴性乳腺癌细胞株MDA-MB-231和BT549及人脐静脉血管内皮细胞株(HUVEC)并计数,以每孔5×103个的细胞密度接种到96孔板,在37 ℃的细胞培养箱中过夜培养至细胞贴壁。实验分为对照组和给药组,对照组以正常培养基培养,给药组以不同浓度含药培养基孵育细胞24 h。随后按试剂盒说明书进行操作,每孔加入10%的CCK8试剂,在培养箱中孵育2 h后,用酶标仪在450 nm处检测各孔的吸光度(OD)值。对照组细胞活力换算为100%,其余各给药组按以下公式计算:细胞增殖抑制率(%)=[(对照组A值−实验组A值)/(对照组A值−空白组A值)]×100%。
-
取上述对数生长期的人三阴性乳腺癌细胞株,以每孔500个细胞的密度均匀接种在12孔板内,过夜,使细胞贴壁,随后加入雀梅藤提取物孵育24 h。吸弃培养基,用含10%的胎牛血清培养基继续培养,当培养皿中出现肉眼可见的克隆形成时,终止培养。吸弃上清液,用PBS小心浸洗,然后甲醇固定。去除固定液,加入适量的结晶紫染色液进行染色,采用PBS多次轻轻洗去周边染色液,干燥后拍照,随后用Image J软件进行统计分析。
-
将两种乳腺癌细胞接种于96孔板,放置培养箱中过夜,随后加入提取物孵育24 h。吸弃培养基,用PBS温和洗涤细胞一次,每孔加入100 μl的Calcein AM/PI染色工作液,放入37 ℃培养箱中避光孵育15 min后,用高内涵系统采集图像。
-
取对数生长期乳腺癌细胞株,以每孔40万个细胞接种于6孔板,培养箱中过夜,待细胞贴壁后,用含不同浓度提取物的培养基处理24 h,消化,离心收集细胞,以预冷的70%乙醇混悬固定过夜。离心,去除乙醇,用PBS清洗一次,加入500 μl的碘化丙啶染色工作液,避光染色30 min后用流式细胞仪分析细胞周期。
-
将对数生长期的三阴性乳腺癌细胞株以每孔40万个接种于6孔板中,过夜,待细胞贴壁后,用含不同浓度提取物的培养基孵育24 h。消化,离心收集细胞,用100 μl的1×结合缓冲液混悬后加入FITC Annexin V 和PI各5 μl,轻微振荡,室温下避光孵育15 min,流式细胞仪分析凋亡率。
-
将上述对数生长期的人三阴性乳腺癌细胞株以每孔20万个接种于6孔板,过夜,待细胞贴壁后,用含不同浓度提取物的培养基孵育24 h,吸弃培养基,每孔加入1 ml稀释过的DAPI染液孵育细胞10 min,PBS清洗2遍后采用Cytation 5拍照。
-
将对数生长期的人三阴性乳腺癌细胞株以每孔20万个接种于6孔板,过夜,待细胞贴壁后,用含不同浓度提取物的培养基孵育细胞24 h。吸弃培养液,PBS洗涤细胞之后每孔加入1 ml的JC-1染液,在37 ℃培养箱中孵育20 min。吸除上清液,用缓冲液洗涤细胞3次后加入2 ml细胞培养液,高内涵系统拍照。
-
取上述对数生长期细胞株,以每孔20万个的细胞密度接种于6孔板,过夜,待细胞贴壁后,用含不同浓度提取物的培养基孵育24 h。吸弃培养基,每孔加入1 ml含DCFH-DA的新鲜培养基孵育细胞20~30 min,DAPI复染,采用高内涵系统拍照。
-
使用Graphpad Prism 8.0.1分析软件对所获得的实验数据进行统计学分析,组间比较采用单因素方差分析,两组比较采用t检验,以P<0.05为差异有统计学意义。
-
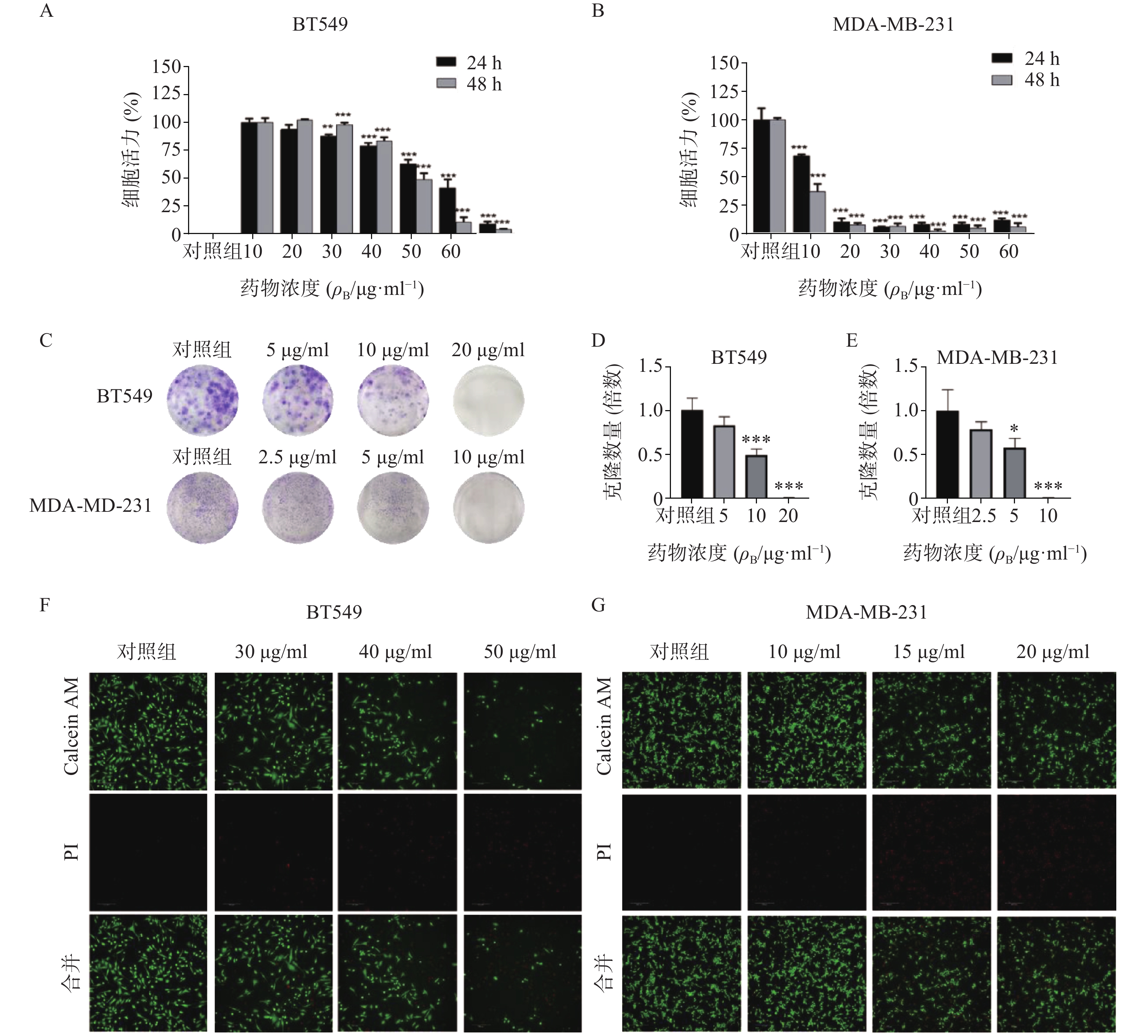
通过细胞活力分析发现,雀梅藤石油醚提取部位对多种癌细胞均有明显细胞毒性,其中对乳腺癌细胞株抑制作用最强,而且明显强于乙醇提取物。结合临床应用,实验选择两种人三阴性乳腺癌系(BT549和MDA-MB-231)进一步研究(见图1)。CCK8结果表明(图1A-B),雀梅藤石油醚提取物以剂量和时间依赖的方式抑制乳腺癌细胞活力,作用24 h和48 h的IC50值分别为45.40、12.23 μg/ml和38.87、7.60 μg/ml。平板克隆实验结果显示(图1C-E),随着雀梅藤石油醚提取物剂量的增加,两种乳腺癌细胞生长均被显著抑制。浓度分别在10 μg/ml和20 μg/ml时,MDA-MA-231和BT549细胞株的生长被完全抑制。Calcein AM/PI活死细胞染色显示(图1F-G),随着药物剂量增加,活细胞(绿色)数量较对照组显著减少,而死亡细胞(红色)数量则显著增加,与对照组比较有极显著差异。
-
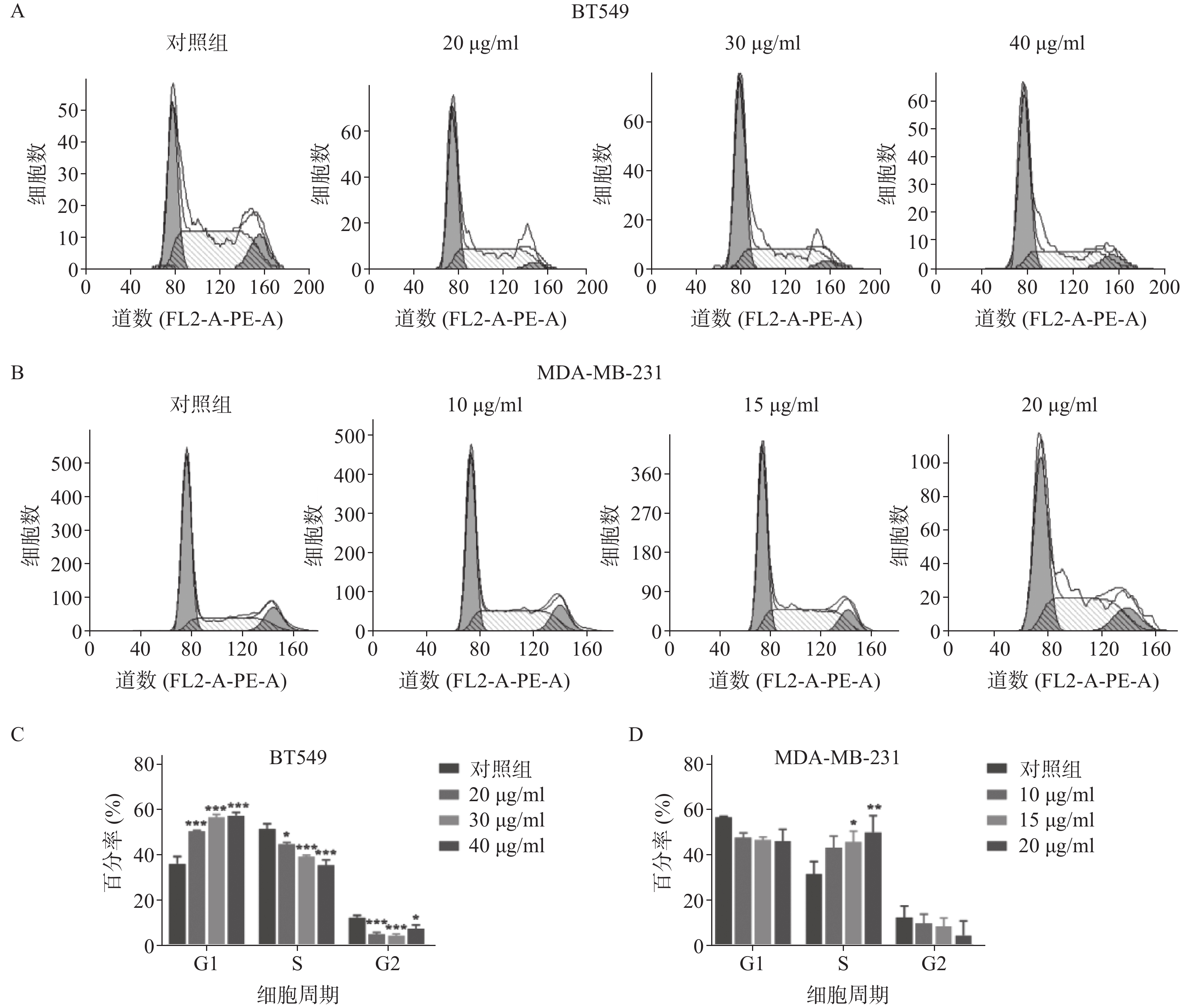
雀梅藤石油醚提取物孵育乳腺癌细胞24 h后,采用流式细胞仪测定细胞的增殖周期情况(见图2)。结果显示,药物明显阻滞两种乳腺癌细胞株的细胞周期,但对两种细胞阻滞周期不同,BT549细胞阻滞在G1期(图2A和2C,给药组G1期细胞比率较对照组显著升高),MDA-MA-231细胞阻滞在S期(图2B和2D,给药组S期细胞比率较对照组显著升高),提示石油醚提取物对两种细胞株的细胞周期阻滞可能存在不同机制。
-
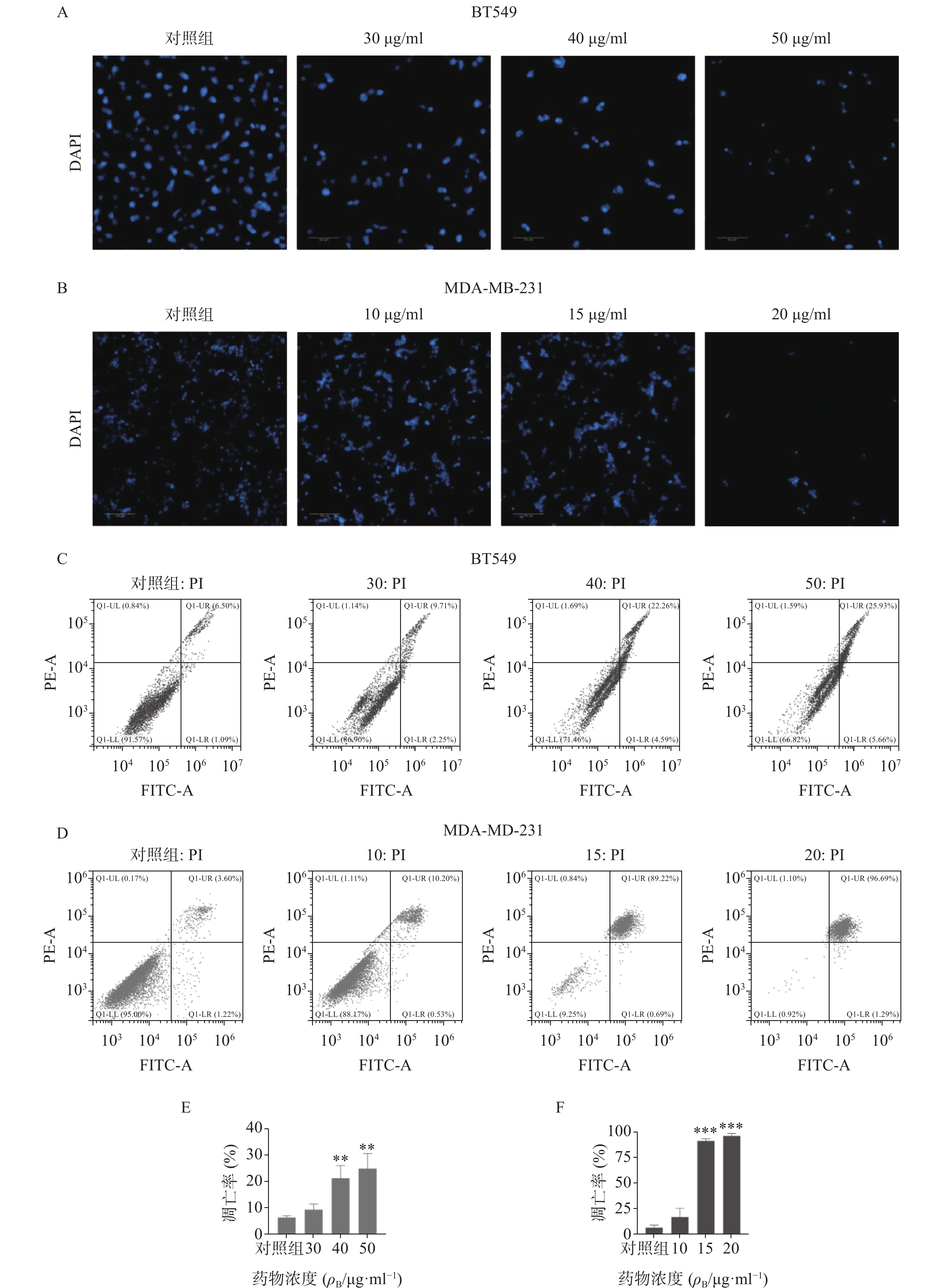
采用DAPI染色方法对细胞核形态进行分析(见图3)。如图3A-B所示,正常对照组乳腺癌细胞核呈均匀的圆形浅蓝色,药物处理后细胞核质固缩或碎裂成凋亡小体,且呈剂量依赖性。流式细胞仪凋亡定量分析显示(图3C-F),石油醚提取物显著增加两种乳腺癌细胞的凋亡率,与对照组比较有显著性差异,其中尤以MDA-MA-231细胞株明显,20 μg/ml浓度下几乎诱导细胞全部凋亡。
-
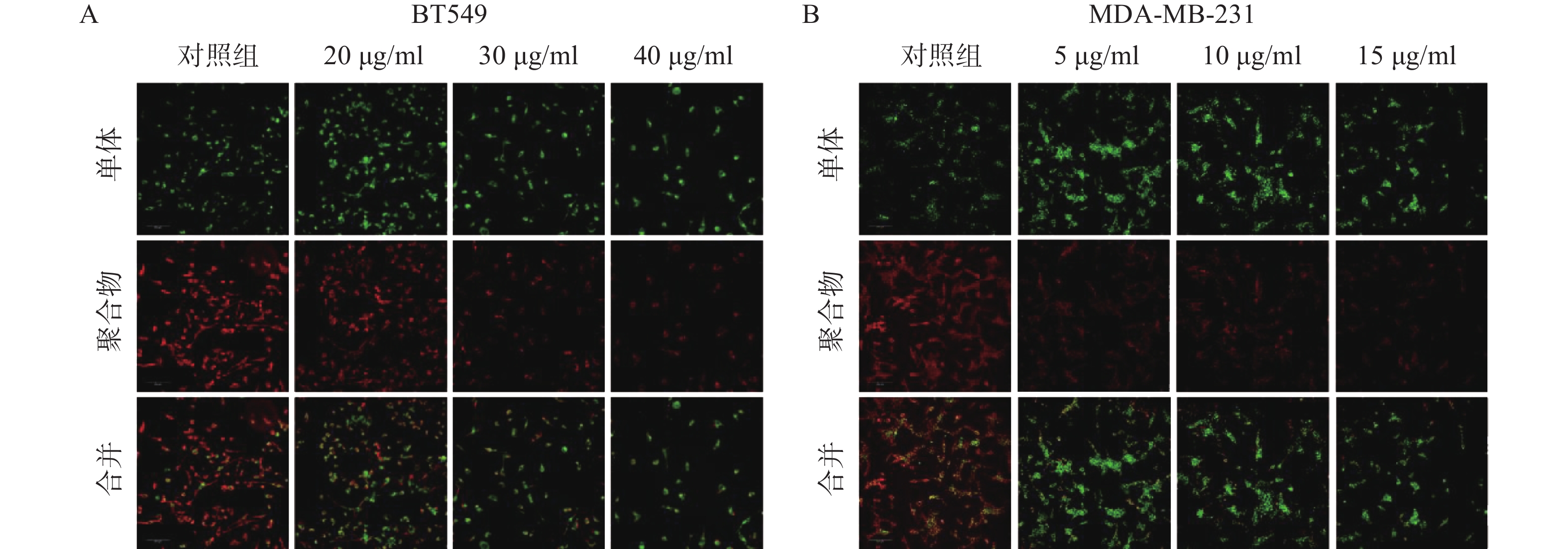
线粒体通路是肿瘤细胞最常见的凋亡途径,最典型的特征是线粒体膜电位(MMP)水平显著下降。因此,研究采用JC-1免疫荧光染色检测线粒体膜电位水平。结果如图4所示,给药组红色荧光随剂量增加明显减弱,绿色荧光则明显增强,说明给药组线粒体膜电位显著下降。实验结果提示,雀梅藤石油醚提取物可能通过损伤线粒体而促进了乳腺癌细胞凋亡。
-
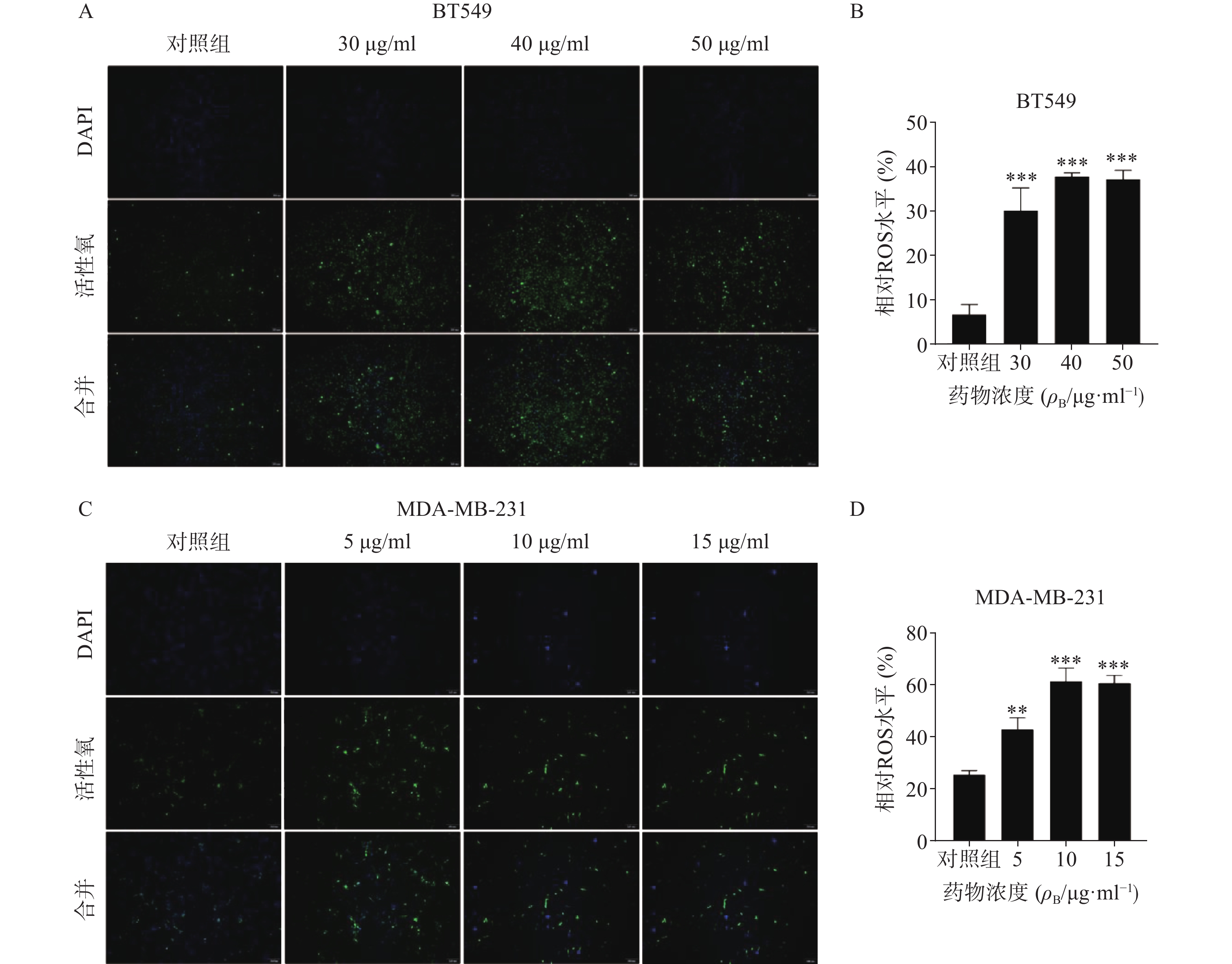
ROS升高是激活线粒体通路诱导肿瘤细胞凋亡的重要原因之一,因此进一步检测了药物处理24 h后ROS含量变化(图5)。结果代表ROS水平的绿色荧光在对照组仅有少量表达,而在给药组则显著增加,经统计学处理有显著性差异,其中尤以BT549细胞株明显,提示药物可能通过促进ROS生成而诱导了乳腺癌细胞凋亡。
-
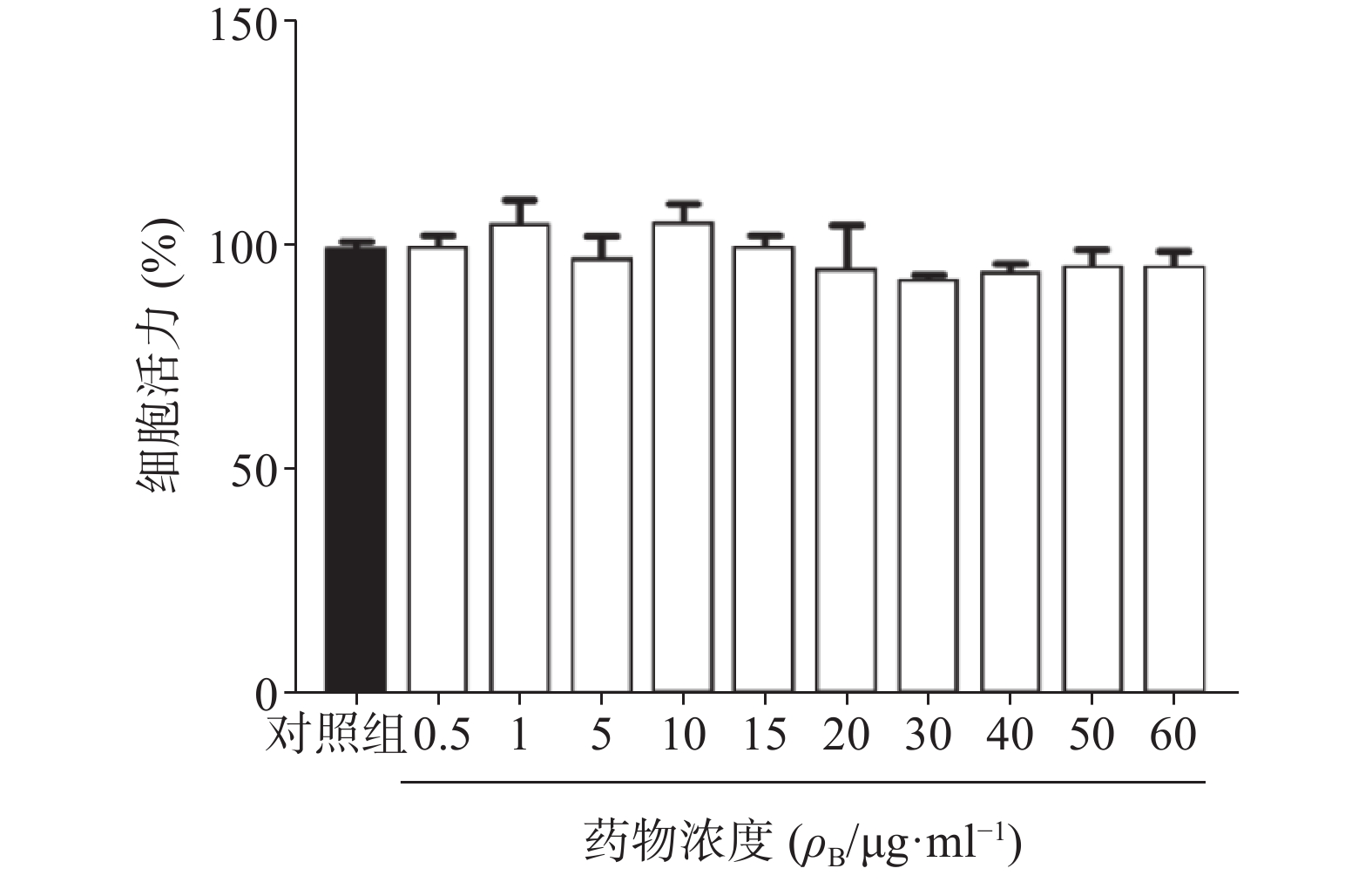
为了确定雀梅藤提取物是否对正常细胞产生毒性,进一步采用同样剂量对人正常脐静脉血管内皮细胞(HUVEC)进行CCK8细胞活力分析。结果提取物孵育24 h后,即使在60 μg/ml的最高浓度下亦未观察到内皮细胞活力受到影响,与对照组比较无明显差异(图6),提示雀梅藤石油醚提取物对正常细胞并不产生毒性,具有较好的安全性。
-
雀梅藤为云南等地民间常用中药,临床观察发现其对乳腺瘤生长有明显抑制作用[7],且毒性较小[4, 8]。研究前期对雀梅藤的乙醇、石油醚、乙酸乙酯、二氯甲烷、正丁醇等5个部位提取物进行了多种肿瘤细胞活性筛选,结果显示,对多数癌细胞,如乳腺癌、结肠癌、肝癌等,都具有明显杀伤作用,其中以石油醚部位提取物对癌细胞作用最为显著。进一步实验发现,雀梅藤石油醚提取物时间和剂量依赖地抑制乳腺癌细胞活力,显著减少细胞克隆形成率,阻滞细胞周期在G1/S期,明显增加癌细胞凋亡率,但并不影响正常血管内皮细胞活力,提示其细胞毒性具有明显的选择性。
引起细胞凋亡的途径包括线粒体通路、死亡受体通路和内质网应激通路,其中线粒体通路是药物诱导肿瘤细胞凋亡的最常见途径[9],因此研究人员进一步观察了雀梅藤石油醚提取物是否通过损伤线粒体诱导乳腺癌细胞凋亡。结果通过JC-1染色发现,两种乳腺癌细胞的线粒体膜电位均显著降低,提示雀梅藤提取物诱导了细胞线粒体途径的凋亡。
ROS的主要来源之一是线粒体内膜的呼吸链底物端,ROS升高会引起线粒体内膜损伤,造成细胞毒性,从而促进肿瘤细胞凋亡[10]。研究人员用荧光探针方法检测雀梅藤石油醚提取物孵育BT549和MDA-MB-231细胞后的ROS水平,结果发现代表ROS的绿色荧光逐渐增强,表明石油醚提取物显著升高了线粒体内ROS水平。这些结果提示,石油醚提取物可能通过升高线粒体内ROS水平,造成ROS累积,损伤了线粒体,导致线粒体内容物如细胞色素c等流出到细胞质,进而激活caspase级联瀑布反应,从而诱导了细胞凋亡[9,11]。
虽然雀梅藤提取物在体外研究中表现出较好的抗乳腺癌细胞生长作用,但是凋亡信号转导通路和作用靶点尚不明确,线粒体中蛋白表达的变化犹未可知,因此具体作用机制尚需进一步研究。此外,已有研究人员从雀梅藤药材中鉴定出43种化学成分,可分为有机酸类、黄酮类及其他类,有机酸类包括儿茶素及其衍生物等,黄酮类包括异槲皮素等[12]。但是雀梅藤提取物中究竟何种成分发挥主要抗癌作用仍需进一步证实。
Induction of apoptosis in triple-negative breast cancer cells by petroleum ether extract of Sageretia thea
-
摘要:
目的 探讨雀梅藤石油醚提取物对乳腺癌细胞增殖和凋亡的影响。 方法 石油醚提取物孵育乳腺癌细胞不同时间后,CCK8法检测细胞活力,平板克隆形成法检测细胞增殖,DAPI染色法观察细胞核形态变化,免疫荧光检测线粒体膜电位和活性氧变化,流式细胞术检测细胞周期和凋亡,CCK8法观察对人正常血管内皮细胞毒性。 结果 雀梅藤石油醚提取物孵育BT549和MDA-MB-231人三阴性乳腺癌细胞株24 h后的IC50分别为45.40 μg/ml和12.23 μg/ml,时间和剂量依赖地抑制乳腺癌细胞活力和克隆形成,诱导细胞凋亡,阻滞细胞周期于G1/S期,降低线粒体膜电位,升高活性氧;对人正常血管内皮细胞无明显毒性作用。 结论 雀梅藤石油醚提取物可能通过升高活性氧,引起线粒体膜电位坍塌,激活线粒体通路诱导细胞凋亡,从而抑制乳腺癌细胞生长,支持其民间抗乳腺肿瘤的应用。 Abstract:Objective To investigate the effect of the petroleum ether extract of Sageretia thea on the proliferation and apoptosis of breast cancer cells. Methods After breast cancer cells were incubated with the petroleum ether extract for different times, cell viability was analyzed by CCK8 assay, cell proliferation was detected by plate cloning test, nuclear morphology was observed by DAPI staining, mitochondrial membrane potential(MMP)and reactive oxygen species(ROS)were determined by immunofluorescence, and the cell cycle and apoptosis were detected by flow cytometry. After incubating with the extract for 24 h, the CCK8 assay was used to observe the toxicity to normal human vascular endothelial cells. Results The IC50 of BT549 and MDA-MB-231 breast cancer cell lines treated with the petroleum ether extract for 24 h were 45.40 μg/ml and 12.23 μg/ml, respectively. The extract time and dose dependently inhibited breast cancer cell viability and clonal formation, induced cell apoptosis and cycle arrest in G1/S phase, decreased MMP and increased ROS levels. There was no toxic effect on normal endothelial cells. Conclusion The petroleum ether extract of Sageretia thea may induce apoptosis by increasing ROS to cause MMP collapse, followed by activating mitochondrial pathway, thereby hindering the growth of breast cancer cells. These results could support the application of Sageretia thea to anti-breast tumor in the folk. -
Key words:
- Sageretia thea /
- Breast cancer /
- Proliferation /
- Apoptosis /
- Mitochondrion /
- ROS
-
盐酸普萘洛尔(propranolol hydrochloride,PPL)是治疗婴幼儿血管瘤的一线和首选药物[1]。口服盐酸普萘洛尔疗效确切,但其存在首过效应强、生物利用度低、半衰期短等问题,且不良反应发生率高[2]。普通盐酸普萘洛尔外用制剂只对浅表型血管瘤有效,对深部型和复合型血管瘤的治疗仍需结合口服给药。诸多研究表明,立方液晶(cubosomes,Cubs)可显著提高经皮给药制剂的皮肤渗透性,且能提高其在皮肤尤其是皮肤真皮层的药物滞留量,有望能提高盐酸普萘洛尔外用制剂对深部型和复合型血管瘤的疗效[3~5]。因此,课题组拟基于立方液晶载药技术将盐酸普萘洛尔制备成一种纳米经皮给药制剂,以期能降低或避免口服给药带来的高不良反应发生率,提高盐酸普萘洛尔的治疗效果和患者依从性。前期实验中,课题组筛选了盐酸普萘洛尔立方液晶纳米粒(PPL-Cubs)的制备方法,并通过单因素考察结合星点设计效应面法优化了其最佳处方和制备工艺,结果制得的PPL-Cubs包封率低(约50%),远低于药典规定的80%。立方液晶为多层囊泡结构,类似于多囊脂质体,其可能与脂质体同样存在对水溶性化合物包封率较低的问题。鉴于前期研究表明,盐酸普萘洛尔在不同pH磷酸盐缓冲液下的溶解度存在极大差异,因此,本研究拟在立方液晶常规制备的基础上,引入“pH梯度法”的载药思路,制备PPL-Cubs,以期提高其包封率。
1. 仪器与试药
1.1 仪器
岛津LC-20AD型高效液相色谱仪(日本岛津公司);DV215CD型分析天平(美国奥豪斯公司);AL204型电子天平[梅特勒-托利多仪器(上海)有限公司];DF-101B集热式恒温加热磁力搅拌器(郑州长城科工贸有限公司);高压均质机(意大利NIRO-SAVI S.P.A.公司);NICOMP 380 ZLS激光粒度测定仪(美国PSS粒度仪公司);超滤离心管(100KD,Millipore)。
1.2 试药
盐酸普萘洛尔(含量99.9%,常州亚邦制药有限公司);单油酸甘油酯(法国GATTEFOSSé公司);泊洛沙姆407(德国BASF公司);甲醇、乙腈为色谱纯,水为超纯水,其余试剂为分析纯。
2. 方法与结果
2.1 包封率的测定
取PPL-Cubs适量,装入超滤离心管中,于4000 r/min离心10 min,收集离心液,采用课题组前期建立的盐酸普萘洛尔含量测定方法测定离心液中游离药物浓度C游离;取未透析的PPL-Cubs,测定药物浓度C总;根据公式EE(%)=[(C总−C游离)/ C总]×100%计算PPL-Cubs的包封率。
2.2 PPL-Cubs的制备
2.2.1 注入法
精密称取单油酸甘油酯9 g和泊洛沙姆407 1.5 g,加入10 ml无水乙醇,20 ℃水浴下搅拌溶解,为A相;精密称取盐酸普萘洛尔3.5 g,加入86 g纯化水,20 ℃水浴下搅拌溶解,为B相。于20 ℃水浴及600 r/min搅拌速度下,将A相缓慢地滴加至B相中,待磁力搅拌1 h后加入适量纯化水使总质量为100 g,再在800 bar压力下高压均质7次,得PPL-Cubs。
2.2.2 pH梯度法
精密称取单油酸甘油酯适量,40 ℃水浴加热使融化,为A相;精密称取泊洛沙姆407适量,加入适量纯化水,40 ℃水浴加热使溶解,并用1%磷酸溶液调节pH至酸性,为B相;于40 ℃水浴及600 r/min搅拌速度下,将A相缓慢滴加到B相中,待磁力搅拌30 min后,得空白立方液晶纳米粒粗品;取空白立方液晶纳米粒粗品,高压均质数次,得空白立方液晶纳米粒(B-Cubs)。取盐酸普萘洛尔溶解于适量纯化水中,得盐酸普萘洛尔水溶液;将盐酸普萘洛尔水溶液加入一定比例的B-Cubs中,搅拌均匀,并用氢氧化钠溶液调节pH至一定值,于一定温度下持续搅拌一定时间,再放置至室温,即得PPL-Cubs。
2.3 B-Cubs的制备工艺优化
前期试验结果表明,磁力搅拌速度、时间、温度、内水相pH值对B-Cubs的粒径基本无影响,高压均质压力及均质次数是影响其粒径的主要因素,故拟进一步优化高压均质压力和均质次数。
2.3.1 高压均质压力的考察
按照“2.2.2”项下方法,取空白立方液晶纳米粒粗品,分别在400、600、800、900、1000 bar下高压均质7次,测定制得B-Cubs的粒径及多分散指数(见表1)。结果表明,随高压均质压力的提高,制得B-Cubs的粒径和多分散指数均逐渐减小,当均质压力≥900 bar时,B-Cubs的粒径和多分散指数变化较小,故确定高压均质压力为900 bar。
表 1 高压均质压力的考察(n=3)压力(bar) 粒径(nm) 多分散指数 400 169.1±3.5 0.189±0.056 600 129.9±3.2 0.172±0.062 800 110.9±2.7 0.126±0.041 900 97.9±2.1 0.073±0.016 1000 96.4±1.9 0.057±0.009 2.3.2 高压均质次数的考察
按照“2.2.2”项下方法,取空白立方液晶纳米粒粗品,分别在900 bar下高压均质3、5、7、9次,测定制得B-Cubs的粒径及多分散指数(见表2)。结果表明,随高压均质次数的增加,制得B-Cubs的粒径和多分散指数均逐渐减小,当均质次数≥7次时,B-Cubs的粒径和多分散指数变化较小,故确定高压均质次数为7次。
表 2 高压均质次数的考察(n=3)次数(次) 粒径(nm) 多分散指数 3 160.4±4.6 0.173±0.052 5 129.2±3.8 0.140±0.037 7 97.9±2.1 0.073±0.016 9 93.3±1.7 0.067±0.011 2.4 B-Cubs的处方优化
2.4.1 单油酸甘油酯用量的考察
基于优化的B-Cubs最佳制备工艺,按照“2.2.2”项下方法,固定泊洛沙姆407用量为5%,内水相pH为3.0,考察单油酸甘油酯用量(15%、20%、25%、30%、35%)对制得B-Cubs粒径及多分散指数的影响(见表3)。结果表明,随单油酸甘油酯用量的增加,制得的B-Cubs粒径呈先减小后增大趋势,多分散指数则不断降低,当单油酸甘油酯用量为25%时,制得的B-Cubs具有最小的粒径和较适宜的多分散指数,故确定单油酸甘油酯用量为25%。
表 3 单油酸甘油酯用量的考察(n=3)用量(%) 粒径(nm) 多分散指数 15 137.8±3.4 0.160±0.033 20 119.2±2.9 0.147±0.032 25 97.9±2.1 0.073±0.016 30 118.3±3.5 0.024±0.015 35 150.8±5.4 0.026±0.011 2.4.2 泊洛沙姆407用量的考察
基于优化的B-Cubs最佳制备工艺,按照“2.2.2”项下方法,固定单油酸甘油酯用量为25%,内水相pH为3.0,考察泊洛沙姆407用量(3%、4%、5%、6%、7%)对制得B-Cubs粒径及多分散指数的影响(见表4)。结果表明,制得的B-Cubs粒径随泊洛沙姆407用量的增加逐渐降低,多分散指数变化无明显规律,但均较小(<0.1);当泊洛沙姆407用量≥5%时,粒径变化幅度降低,故确定泊洛沙姆407用量为5%。
表 4 泊洛沙姆407用量的考察(n=3)用量(%) 粒径(nm) 多分散指数 3 143.6±3.5 0.064±0.019 4 116.7±3.2 0.055±0.015 5 97.9±2.1 0.073±0.016 6 91.3±1.9 0.052±0.015 7 83.2±1.8 0.062±0.021 2.5 PPL-Cubs的包封率影响因素考察
2.5.1 外水相pH值的考察
根据前期盐酸普萘洛尔在不同pH的PBS中溶解度测定结果可知(见表5),盐酸普萘洛尔在pH≥8.5时溶解度显著下降。按照“2.2.2”项下方法,制备内水相pH为3.0的B-Cubs,并按载体/药物比(以单油酸甘油酯/盐酸普萘洛尔计)为6∶1的比例与B-Cubs和盐酸普萘洛尔水溶液进行混合,以10%氢氧化钠溶液分别调节外水相pH至7.5、8.0、8.5、9.0,于20 ℃水浴(载药温度)下600 r/min磁力搅拌15 min(载药时间),制得PPL-Cubs中药物浓度为1%,测定对包封率等参数影响(见表6)。结果表明,PPL-Cubs的包封率随外水相pH值的提高逐渐增加,当外水相pH值≥8.5时,包封率增加趋势渐小;外水相pH值对PPL-Cubs的粒径和多分散指数无明显影响。
表 5 盐酸普萘洛尔在不同pH PBS中的溶解度(n=3)pH 溶解度(mg/ml) 4.5 53.50±4.22 5.5 51.70±2.34 6.5 52.60±1.53 7.5 49.80±2.14 8.5 8.50±1.15 9.5 1.41±0.33 10.5 0.87±0.08 表 6 外水相pH值的考察(n=3)pH EE(%) 粒径(nm) 多分散指数 7.5 71.29±2.58 96.8±2.6 0.063±0.012 8.0 86.24±1.05 97.5±2.3 0.054±0.006 8.5 92.55±1.27 96.3±1.9 0.045±0.005 9.0 94.58±1.57 97.6±1.7 0.051±0.006 2.5.2 内水相pH值的考察
按照“2.5.1”项下方法,固定外水相pH为8.5时,分别考察内水相pH(3.0、4.0、5.0、6.0)对制得PPL-Cubs包封率等参数的影响(见表7)。结果表明,不同内水相pH的B-Cubs对制得的PPL-Cubs包封率无明显差异,对PPL-Cubs的粒径和多分散指数亦无明显影响。
表 7 内水相pH值的考察(n=3)pH EE(%) 粒径(nm) 多分散指数 3.0 92.55±1.27 96.3±1.9 0.045±0.005 4.0 91.85±1.05 97.5±2.3 0.054±0.006 5.0 91.62±1.27 96.3±1.9 0.045±0.005 6.0 89.33±1.57 97.6±1.7 0.051±0.006 2.5.3 载体/药物的考察
按照“2.5.1”项下方法,固定外水相pH为8.5时,分别考察载体/药物(5∶1、6∶1、7∶1、8∶1)对制得PPL-Cubs包封率等参数的影响(见表8)。结果表明,当载体/药物≥6时,PPL-Cubs的包封率不再增加;载体/药物比值对PPL-Cubs的粒径和多分散指数无明显影响。
表 8 载体/药物的考察(n=3)载体/药物 EE(%) 粒径(nm) 多分散指数 5∶1 90.93±1.52 98.5±2.7 0.076±0.015 6∶1 92.55±1.27 96.3±1.9 0.045±0.005 7∶1 92.06±2.37 97.5±2.1 0.077±0.015 8∶1 92.41±2.58 98.1±2.4 0.102±0.025 2.5.4 载药温度的考察
按照“2.5.1”项下方法,固定外水相pH为8.5时,分别考察载药温度(20、30、40、50 ℃)对制得PPL-Cubs包封率等参数的影响(见表9)。结果表明,载药温度对PPL-Cubs的包封率、粒径和多分散指数无明显影响。
表 9 载药温度的考察(n=3)载药温度(℃) EE(%) 粒径(nm) 多分散指数 20 92.55±1.27 96.3±1.9 0.045±0.005 30 91.05±1.95 96.9±2.3 0.068±0.021 40 91.38±2.08 97.1±2.6 0.066±0.012 50 90.55±1.75 97.2±2.1 0.053±0.018 2.5.5 载药时间的考察
按照“2.5.1”项下方法,固定外水相pH为8.5时,分别考察载药时间(15、30、45、60 min)对制得PPL-Cubs包封率等参数的影响(见表10)。结果表明,载药时间对PPL-Cubs的粒径和多分散指数无明显影响。
表 10 载药时间的考察(n=3)载药时间(min) EE(%) 粒径(nm) 多分散指数 15 92.55±1.27 96.3±1.9 0.045±0.005 30 92.09±1.54 97.2±2.4 0.071±0.013 45 92.01±2.01 97.5±1.6 0.065±0.024 60 91.86±1.86 98.1±1.9 0.075±0.026 2.5.6 B-Cubs粒径和多分散指数的考察
通过调整高压均质压力,制备不同粒径B-Cubs。按照“2.5.1”项下方法,固定外水相pH为8.5,分别考察B-Cubs粒径和多分散指数对制得PPL-Cubs包封率等参数的影响(见表11)。结果表明,B-Cubs的粒径和多分散指数不影响所制得PPL-Cubs的包封率,但B-Cubs的粒径和多分散指数基本决定了制得PPL-Cubs的粒径和多分散指数。
表 11 B-Cubs粒径和多分散指数的考察(n=3)载体 EE(%) PPL-Cubs 粒径(nm) 多分散指数 粒径(nm) 多分散指数 97.9±2.1 0.073±0.016 92.55±1.27 96.3±1.9 0.045±0.005 129.2±3.8 0.140±0.037 91.87±1.96 128.5±2.1 0.123±0.021 160.4±4.6 0.173±0.052 91.85±2.13 158.2±2.8 0.152±0.037 210.5±5.9 0.182±0.057 91.25±2.53 209.2±2.9 0.174±0.045 2.5.7 PPL-Cubs药物浓度的考察
按照“2.5.1”项下方法,固定外水相pH为8.5,分别考察药物浓度(0.1%、0.5%、1.0%、2.0%、3.0%)对制得PPL-Cubs包封率等参数的影响(见表12)。结果表明,随着PPL-Cubs中药物浓度的提高,包封率呈逐渐增加趋势,当药物浓度≥1%时,包封率增加趋势变慢。
表 12 PPL-Cubs中药物浓度的考察(n=3)浓度 EE(%) 粒径(nm) 多分散指数 0.1 51.83±3.17 97.2±2.4 0.057±0.013 0.5 81.87±2.12 96.3±2.1 0.062±0.012 1.0 92.55±1.27 96.3±1.9 0.045±0.005 2.0 94.42±1.37 96.3±1.9 0.045±0.005 3.0 95.87±1.28 97.8±2.5 0.042±0.007 2.6 pH梯度法制备PPL-Cubs的最优处方及制备工艺
精密称取单油酸甘油酯25.0 g,40 ℃水浴加热使融化,为A相;精密称取泊洛沙姆407 5.0 g,加入70 g纯化水,40 ℃水浴加热使溶解,并用1%磷酸溶液调节pH至3.0,为B相;于40 ℃水浴及600 r/min搅拌速度下,将A相缓慢滴加到B相中,待磁力搅拌30 min后,再在900 bar下高压均质7次,得B-Cubs。取盐酸普萘洛尔1 g,溶解于适量纯化水中,得盐酸普萘洛尔水溶液;将盐酸普萘洛尔水溶液加入24 g B-Cubs中,搅拌均匀,用10%氢氧化钠溶液调节pH至8.5,于20 ℃水浴持续搅拌15 min,再放置至室温,即得PPL-Cubs
3. 讨论
立方液晶纳米粒常用的制备方法包括注入法、熔融-分散法、热处理法、喷雾干燥法等[6]。试验前期以粒径、包封率等为评价指标筛选了最佳制备方法为注入法,并优化了其最佳处方制备工艺,结果制得的载药立方液晶纳米粒包封率较低(约50%)[7]。立方液晶是两亲性脂质分子分散在过量水中形成的含双连续水区和闭合脂质双分子层的蜂窝状液晶结构;水溶性分子被包封于立方液晶水道中,脂溶性分子被包封于脂质双层膜中,两亲性分子则贯穿其中。盐酸普萘洛尔在酸性环境下具有较高的溶解性,常规方法制得的盐酸普萘洛尔立方液晶纳米粒pH约为3.5,如何让其具有进入立方液晶载体内相的“动力”是提高载药立方液晶纳米粒包封率的关键。因此,本研究引入“pH梯度法”,通过创造高溶解度内环境(低pH值内水相)和低溶解度外环境(高pH值外水相),给盐酸普萘洛尔提供进入立方液晶载体内相的“动力”。离子化的盐酸普萘洛尔在调节pH的过程中逐渐变为分子形态的普萘洛尔而进入脂质区,脂质区的普萘洛尔分子接触内水相酸性环境而被离子化,内水相中离子化的盐酸普萘洛尔无法再通过脂质区而被捕获于内水相。结果表明,pH梯度法显著提高了PPL-Cubs的包封率,包封率达到90%。
-
-
[1] 沈丕安. 中华本草[M]. 上海: 上海科学普及出版社, 2017. [2] 马雯芳. 瑶药倒丁风化学成分及质量控制研究[D]. 成都: 成都中医药大学, 2014. [3] 苗明三, 孙玉信, 王晓田. 中药大辞典[M]. 太原: 山西科学技术出版社, 2017. [4] 张美义, 篮振水, 周俊, 等. 云南民间抗肿瘤植物雀梅藤的化学和药理研究[J]. 云南植物研究, 1980, 2(1):62-66. [5] KIM H N, PARK G H, PARK S B, et al. Extracts from Sageretia thea reduce cell viability through inducing cyclin D1 proteasomal degradation and HO-1 expression in human colorectal cancer cells[J]. BMC Complement Altern Med, 2019, 19(1):43. doi: 10.1186/s12906-019-2453-4 [6] 丁永丽, 邓杨林, 陈新利, 等. 雀梅藤药用研究进展[J]. 中药材, 2020, 43(7):1755-1760. [7] 万嘉锺. 雀梅藤治疗甲状腺囊肿、乳腺瘤20例疗效观察[J]. 云南中医学院学报, 1982, 5(1):14-15. [8] 王茂三, 龚维桂, 范华芬, 等. 雀梅藤护肝作用研究[J]. 浙江药学, 1985, 2(5):11-14. [9] AN P, LU D, ZHANG L J, et al. Synergistic antitumor effects of compound-composed optimal formula from Aidi injection on hepatocellular carcinoma and colorectal cancer[J]. Phytomedicine, 2022, 103:154231. doi: 10.1016/j.phymed.2022.154231 [10] 郭晓萌, 魏婷, 张焱. 黑参皂苷的提取纯化及其对MGC-803细胞凋亡的影响[J]. 食品研究与开发, 2023, 44(4):49-57. [11] DENG Y Q, GAO M, LU D, et al. Compound-composed Chinese medicine of Huachansu triggers apoptosis of gastric cancer cells through increase of reactive oxygen species levels and suppression of proteasome activities[J]. Phytomedicine, 2024, 123:155169. doi: 10.1016/j.phymed.2023.155169 [12] 蒙雪雁, 王成海. 基于液质联用技术分析雀梅藤化学成分[J]. 中南农业科技, 2023, 44(3):37-41,55. -





 下载:
下载:
 下载:
下载: