-
糖皮质激素(glucocorticoid, GC)是一种在临床上广泛应用于治疗类风湿性关节炎、胃肠道疾病及自身免疫疾病的药物[1]。然而,研究显示,有超过50%的患者在长期接受GC的治疗过程中会发生骨质疏松症[2]。目前,糖皮质激素诱导的骨质疏松(glucocorticoid-induced osteoporosis, GIOP)已成为病理性骨丢失的第三大常见病症,仅次于老年性骨质疏松症和绝经后骨质疏松症。与此同时,GIOP由于其高致残率和高发病率给社会和家庭生活造成了极大的负担,因此,如何预防和治疗GIOP成为医学上关注的热点。
啤酒花(Humulus lupulus L.)为桑科葎草属多年生草质蔓生藤本植物,其雌性带花果穗不仅是酿造啤酒的添加原料,也是全球广泛应用的药物品种,并在欧洲广泛用于缓解更年期潮热及绝经后骨质疏松症[3]。黄腐酚(xanthohumol, XN)为啤酒花中的代表性成分,具有抗氧化、抗肿瘤、抗菌等活性[4]。课题组前期研究发现,啤酒花提取物及黄腐酚可显著改善去卵巢小鼠的骨丢失,防治绝经后骨质疏松症。此外,两者还可显著调节成骨细胞与破骨细胞的活性,维持骨稳态[5-6]。然而,目前对于啤酒花及黄腐酚抗GIOP的作用机制尚不明确。故笔者拟以地塞米松(DEX)诱导的骨质疏松小鼠及其损伤的成骨细胞为模型,采用Micro-CT及体外活性检测等方法,对啤酒花及黄腐酚抗GIOP的作用进行探究。
-
啤酒花(PJH-01),产地新疆,购自河北安国中药材市场,经海军军医大学药学院生药学教研室辛海量副教授鉴定,密封存放于干燥阴凉处。称取啤酒花药材粉末70 g,加入料液比为1∶15的75%乙醇,回流提取3次,减压浓缩干燥成浸膏,HPLC测定得浸膏中黄腐酚含量为0.55%[5]。使用前配制成相应浓度的提取液。
其他试剂及购买厂家:黄腐酚(纯度≥98%,上海历鼎);地塞米松(大连美仑);阿仑膦酸钠(上海国药);I型胶原C端肽(CTX-I)及骨钙素(BGP)Elisa试剂盒(南京建成);碱性磷酸酶(ALP)及抗酒石酸酸性磷酸酶(TRAP)试剂盒(南京建成);胎牛血清(Gibco,美国);α-MEM培养基等细胞培养试剂(天津灏洋);骨形成蛋白2(BMP-2)及成骨特异性转录因子(Runx-2)抗体(Abcam,英国);Micro-CT(eXplore Locus SP,GE,美国)。
-
3月龄ICR小鼠,体重(20 ± 2)g,购自上海斯莱克实验动物有限公司[实验动物质量合格证号:2013001831722;实验动物使用许可证号:SYXK(沪)2017-0004]。小鼠饲养于海军军医大学药学院实验动物中心清洁级动物房,室温(24 ± 0.5)℃,每日12 h光照/12 h黑暗,自由饮食饮水,适应1周后开始动物实验。
-
取自新生24 h Wistar大鼠(上海斯莱克实验动物有限公司)。所有动物实验均符合实验动物伦理学要求。
-
将56只大鼠按体重以随机区组设计分为7组(n=8):空白对照组(CON),DEX模型组(MOD, 2.5 mg/kg),阿仑膦酸钠阳性对照组(ALN, 1 mg/kg),啤酒花提取物低剂量组(HLE-L, 1 g/kg),啤酒花提取物高剂量组(HLE-H, 3 g/kg),黄腐酚低剂量组(XN-L, 30 mg/kg),黄腐酚高剂量组(XN-H, 90 mg/kg)。除空白组外,所有组别小鼠腹腔注射DEX注射液,空白对照组小鼠注射同体积的生理盐水,每周3次;与此同时,予相应药物灌胃,空白对照组和模型组小鼠灌胃相同体积生理盐水。每周灌胃给药6次,连续给药12周。每周称量体重,按体重0.1 ml/10 g调整给药体积。末次给药后,小鼠禁食、不禁水过夜,摘除眼球取血,静置离心取血清,储存于−80 ℃冰箱中用于生化指标检测,剥离小鼠后肢右侧股骨用于Mirco-CT测定。
-
取组织固定液中的小鼠右侧股骨,剔除其表面附着的结缔组织,用高分辨率Micro-CT对股骨远端进行扫描。计算骨密度(BMD)、骨表面积/骨体积(BS/BV)、相对骨体积(BV/TV)、骨小梁数目(Tb.N.)及骨小梁分离度(Tb.Sp.)。
-
按照试剂盒说明书步骤,对小鼠血清中ALP、TRAP及CTX-I水平进行检测。
-
采用二次消化法从新生大鼠颅盖骨分离得到原代成骨细胞[7],用含10%胎牛血清的α-MEM培养液进行培养,取3~4代成骨细胞进行增殖、分化以及Western blot分析。
-
取3~4代成骨细胞计算其数目,配制成细胞浓度为1×104 个/ml细胞悬液接种于96孔板。24 h后分别更换为含药培养液(DEX: 10 μmol/L;HLE: 100、20 μg/ml;XN: 5、1 μmol/L),除空白组外均给予DEX损伤。给药48 h后采用MTT法检测成骨细胞的增殖情况。
取3~4代成骨细胞计算其数目,配制成细胞浓度为5×104 个/ml细胞悬液接种于24孔板。24 h后分别更换为含药培养液(给药浓度同上)。培养过程中每3 d更换1次含药培养液。第8天裂解细胞,收集细胞裂解液,于4 ℃、13 800×g 离心5 min。用对硝基苯磷酸二钠法测定细胞 ALP活性[8]。
-
将3~4代的成骨细胞裂解,提取细胞总蛋白,根据BCA试剂盒进行蛋白定量。采用ELISA试剂盒对成骨细胞BGP含量进行检测,采用Westernblot技术[9]对BMP-2及Runx-2水平进行检测。
-
实验结果以(
$\bar x \pm s$ )表示。采用SPSS 22.0软件进行数据分析,选用单因素方差分析(One-Way ANOVA)进行组间变量的比较分析。检验水准(α)为 0.05。 -
模型组小鼠股骨的骨组织形态与空白组相比,出现明显空洞,见图1;药物治疗后,HLE及XN显著改善DEX小鼠的骨组织形态及骨微结构,防止骨质空洞。
模型组小鼠BMD、BS/TV、BV/TV及Tb.N.水平较空白组显著降低,Tb.Sp.水平显著升高(图2)。药物治疗后,HLE及XN显著逆转了DEX小鼠BMD及骨小梁参数的异常,防治骨质疏松。
-
小鼠注射DEX后,其血清ALP水平显著降低,TRAP及CTX-I水平显著升高。药物治疗后,HLE及XN可显著提高小鼠血清ALP水平,并降低TRAP及CTX-I的高表达,调节骨代谢,且药物高剂量组治疗效果更佳(图3)。
-
如图4A-B所示,DEX损伤成骨细胞后,其增殖能力及ALP活性显著降低。药物治疗后,HLE及XN可显著促进DEX损伤成骨细胞的增殖,提高ALP活性,促进成骨细胞的分化。
在骨形成相关蛋白的表达方面,HLE及XN可显著促进DEX损伤成骨细胞中BGP及BMP-2的表达,XN还可显著促进成骨细胞Runx-2的表达(图4C-E),促进成骨细胞骨形成。
-
DEX作为临床上常用的一种合成糖皮质激素,在抗炎抗免疫反应方面均具有良好的疗效。与其他糖皮质激素类似,长期使用DEX会引起严重的不良反应,尤其是对骨骼的影响,可大大增加骨质疏松及生理性骨折的发病风险[10]。本研究中,小鼠注射DEX后,其股骨的骨微结构显著破坏,骨质明显空洞,骨密度及骨小梁参数显著降低,且血清骨生化指标异常,提示小鼠处于典型的骨质疏松状态。药物治疗后,啤酒花提取物及黄腐酚均可显著改善GIOP小鼠的骨微结构破坏,增强骨密度,改善骨小梁参数,防治骨质疏松。ALP和TRAP分别为评价骨形成与骨吸收的常用指标,而CTX-I为成熟胶原降解的标志物,其活性水平与骨密度呈显著的负相关[11]。本研究中,啤酒花提取物及黄腐酚可显著提高ALP含量,抑制TRAP及CTX-I的高表达,表明两者可通过调节骨代谢的平衡防治骨丢失。
在GIOP细胞层面的发病机制中,GC对成骨细胞的影响占主导地位[12]。在成骨细胞活性检测中,MTT值及ALP活性分别代表成骨细胞的增殖及分化水平。其中,ALP合成于骨基质成熟阶段,利于骨基质矿化[13]。本研究中,DEX损伤成骨细胞后,其MTT值及ALP活性均显著下降,表示糖皮质激素抑制了成骨细胞的增殖及分化。药物治疗后,啤酒花提取物及黄腐酚可显著提高损伤成骨细胞的MTT值及ALP活性,有效促进了细胞的增殖与分化,提高成骨细胞活性。BGP、BMP-2及Runx-2均为典型的骨形成相关蛋白,其中BGP是由非增殖期的成骨细胞特异合成并分泌的非胶原蛋白[14],BMP-2是参与成骨细胞分化阶段的主要蛋白[15],而Runx-2是早期成骨细胞分化的调节因子,三者在骨骼形态发生阶段均起着关键作用[16]。本研究发现,啤酒花提取物及黄腐酚可显著促进DEX损伤成骨细胞中BGP、BMP-2及Runx-2的表达,进一步证实了其可通过促进成骨细胞的骨形成对抗GIOP。以上研究为深入探讨啤酒花及其活性成分黄腐酚抗骨质疏松的作用机制以及相关药物的研发奠定了基础。
Effects of Humulus lupulus L. and its active ingredient xanthohumol on preventing glucocorticoid-induced osteoporosis
-
摘要:
目的 研究对啤酒花及其活性成分黄腐酚抗糖皮质激素性骨质疏松(GIOP)作用。 方法 腹腔注射地塞米松(DEX)造模,并结合Micro-CT及Elisa试剂盒检测等方法,对小鼠股骨的骨微结构、骨密度及血清骨生化指标进行评价。同时,采用DEX损伤成骨细胞,对其增殖、分化水平及骨形成相关蛋白的表达进行评价。 结果 啤酒花提取物及黄腐酚可显著改善GIOP小鼠的骨微结构破坏,增强骨密度,改善骨小梁参数。在成骨细胞水平上,啤酒花及黄腐酚既可促进DEX损伤成骨细胞的增殖、分化,又可提高骨钙素(BGP)、骨形成蛋白2(BMP-2)以及成骨特异性转录因子(Runx-2)的表达水平,促进骨形成。 结论 该研究首次明确了啤酒花及黄腐酚具有抗GIOP作用,为抗骨质疏松药物的开发提供了新资源。 -
关键词:
- 啤酒花 /
- 黄腐酚 /
- 糖皮质激素性骨质疏松 /
- 地塞米松 /
- 成骨细胞
Abstract:Objective To explore the effects of Humulus lupulus L. extract (HLE) and xanthohumol (XN) on preventing glucocorticoid-induced osteoporosis (GIOP). Methods The GIOP model was established by intraperitoneal injection of dexamethasone (DEX). Bone microstructure, bone mineral density and serum biochemical indexes were evaluated by Micro-CT and ELISA kits. The levels of cells proliferation and ALP activity, and the expression of bone formation related proteins were assayed with primary osteoblasts injured by DEX. Results HLE and XN significantly alleviated the bone microstructure damage, enhanced the bone mineral density, and improved the trabecular parameters in GIOP mice. In vitro experiments showed that HLE and XN can prevent bone loss not only by improving cell proliferation and ALP activity, but also through increasing the expression of bone γ-glutamic acid-containing proteins (BGP), bone morphogenetic protein 2 (BMP-2) and runt-related transcription factor 2 (Runx-2). Conclusion This study confirmed that HLE and XN had anti-GIOP effects for the first time. It provides a new resource for the development of anti-osteoporosis medications. -
Key words:
- Humulus lupulus L. /
- xanthohumol /
- glucocorticoid-induced osteoporosis /
- dexamethasone /
- osteoblast
-
骨质疏松症(OP)是一种由骨吸收和骨形成之间的关系失衡造成,以低骨量和骨组织微结构破坏为特征,导致骨质脆性增加和易于骨折的全身性骨代谢疾病。其中,成骨细胞是骨形成的功能细胞,在维持骨稳态中起到关键作用[1]。目前,高氧化应激相关的骨丢失已成为骨质疏松研究领域的热点。有研究表明,细胞保护酶是机体对抗氧化应激状态下活性氧(ROS)损伤的主要机制,其活性主要由转录因子Nrf2和FoxO调控,而二者所介导的氧化应激通路同样被证实具有调节成骨细胞氧化还原平衡以及促进骨形成分化的功能[2]。与此同时,β-淀粉样蛋白(amyloid β-protein,Aβ)的沉积可使机体ROS生成增多,进而抑制成骨细胞的增殖、成骨基质的产生及矿化[3]。由此可见,Aβ沉积偶联的氧化损伤是破坏成骨细胞骨形成,进而引发骨丢失的一大诱因。
啤酒花(Hops, Humulus lupulus L.)为桑科葎草属多年生草质蔓生藤本植物,其雌性球穗花序不仅作为啤酒酿造的添加原料,也是全球广泛应用的植物药,在欧洲广泛用于缓解更年期潮热及绝经后骨质疏松症[4]。我们前期研究发现啤酒花能够促进成骨细胞骨矿化结节的形成,降低活性氧水平,并显著改善APP/PS1转基因小鼠的骨丢失[5-6],但其对外源性Aβ损伤成骨细胞的氧化应激水平及骨形成的影响尚不明确。此外,我们首次确认了氧化应激和Aβ沉积之间的双向关联,及其在老年性骨质疏松症发病中的重要作用[7-8]。故本文拟以Aβ损伤的成骨细胞为模型,以Nrf2和FoxO1两条经典氧化应激相关通路为核心,对啤酒花的抗氧化能力及对骨形成干预作用进行探究。
1. 材料与方法
1.1 药材及试剂
啤酒花药材购于昌吉市山水啤酒花有限公司(产地:新疆昌吉;批号:PJH-01),经海军军医大学药学系生药学教研室辛海量副教授鉴定为啤酒花 Humulus lupulus L.的雌性球穗花序。称取啤酒花药材粉末70 g,加入料液比为1∶15的75%乙醇,回流提取3次,减压浓缩干燥成浸膏,HPLC测定得浸膏中主要成分黄腐酚含量为0.55%[9],使用前配制成相应浓度(生药量/ml)的提取液。
其他试剂及厂家:Aβ1-42寡聚体(上海吉尔);N-乙酰-L-半胱氨酸(NAC,上海碧云天);胎牛血清(Gibco,美国);α-MEM培养基等细胞培养试剂(天津灏洋);碱性磷酸酶(ALP)染色试剂盒(南京建成);I型胶原酶(COL-I)、骨桥蛋白(OPN)、核因子-E2-相关因子(Nrf2)、血红素加氧酶-1(HO-1)、NAD(P)H:醌氧化还原酶(NQO1)、细胞叉头框蛋白O1(FoxO1)、超氧化物歧化酶(SOD-2)抗体(Abcam,英国)。
1.2 实验动物及原代成骨细胞分离培养
新生24 h Wistar大鼠,购自上海斯莱克实验动物有限公司[合格证号:2013001831722;许可证号:SYXK(沪)2017-0004]。所有动物实验均符合实验动物伦理学要求。采用二次消化法从新生大鼠颅盖骨分离得到原代成骨细胞,用含10%胎牛血清的α-MEM培养液进行培养,取3~4代成骨细胞进行后续实验分析。
1.3 成骨细胞增殖及碱性磷酸酶检测
取3~4代成骨细胞计算其数目,配制成细胞浓度为1×104个/ml细胞悬液接种于96孔板,根据前期实验结果[9]设置分组:空白对照组,模型组(40 μmol/L Aβ),阳性对照组(NAC, 2.5 mmol/L),啤酒花提取物低剂量组(HLE, 4 μg/ml)、中剂量组(HLE, 20 μg/ml)、高剂量组(HLE, 100 μg/ml),每组设置4个复孔。24 h后按照上述分组更换为含药培养液。给药48 h后采用MTT法检测成骨细胞的增殖情况。
取3~4代成骨细胞计算其数目,配制成细胞浓度为5×104个/ml细胞悬液接种于24孔板。24 h后分别更换为含药培养液(给药浓度同上)。培养过程中每3 d更换1次含药培养液。第8天裂解细胞,收集细胞裂解液,于4 ℃、13 800×g 离心5 min。用对硝基苯磷酸二钠法测定细胞ALP活性[10]。参照ALP染色试剂盒说明书对成骨细胞进行染色。
1.4 成骨细胞凋亡检测
取3~4代成骨细胞计算其数目,配制成细胞浓度为2×105个/ml细胞悬液接种于6孔板。24 h后分别更换为含药培养液(给药浓度同上)。给药48 h后收集各孔中培养基上清液,加入200 μl 0.25%胰蛋白酶消化30 s,离心并重悬,参照凋亡检测试剂盒装载探针,室温避光孵育5 min后,用流式细胞仪进行凋亡率检测。
1.5 蛋白质印迹检测
取3~4代成骨细胞接种于6孔板,24 h后分别更换为含药培养液(给药浓度同上)。给药48 h后进行细胞裂解,提取细胞总蛋白,根据BCA试剂盒进行蛋白定量。蛋白变性后进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳分离,转膜、封闭后,分别加入COL-I、OPN、Nrf2、HO-1、NQO1、FoxO1及SOD-2抗体,4 ℃孵育过夜。用洗膜缓冲液(Tris-buffered saline/Tween-20,TBST)洗膜3×10 min,加入二抗,室温孵育30 min。用TBST再次洗膜3×10 min,采用ECL试剂进行检测。采用Tanon Image软件对蛋白印迹进行半定量分析。
1.6 免疫荧光检测
取3~4代成骨细胞配制成浓度为2×104个/ml细胞悬液接种于无菌激光共聚焦皿中。24 h后分别更换为含药培养液(Aβ, 40 μmol/L HLE, 100 μg/ml)。给药48 h后用4%的多聚甲醛固定细胞30 min,PBS浸洗后用0.5% Triton X-100(PBS配制)通透20 min,并用5% BSA封闭液室温封闭1 h。先后加入FoxO1抗体及荧光二抗(TRITC标记山羊抗兔抗体)进行孵育,加入DAPI染液避光孵育10 min进行染核。最后洗去多余的DAPI染液,加入少量PBS使细胞保持湿润,并置于荧光显微镜下观察采集图像。
1.7 统计学分析
实验结果以均值±标准差(
$ \bar x$ ±s)表示。采用SPSS 22.0软件进行数据分析,选用单因素方差分析(One-Way ANOVA)进行组间变量的比较分析。2. 结果
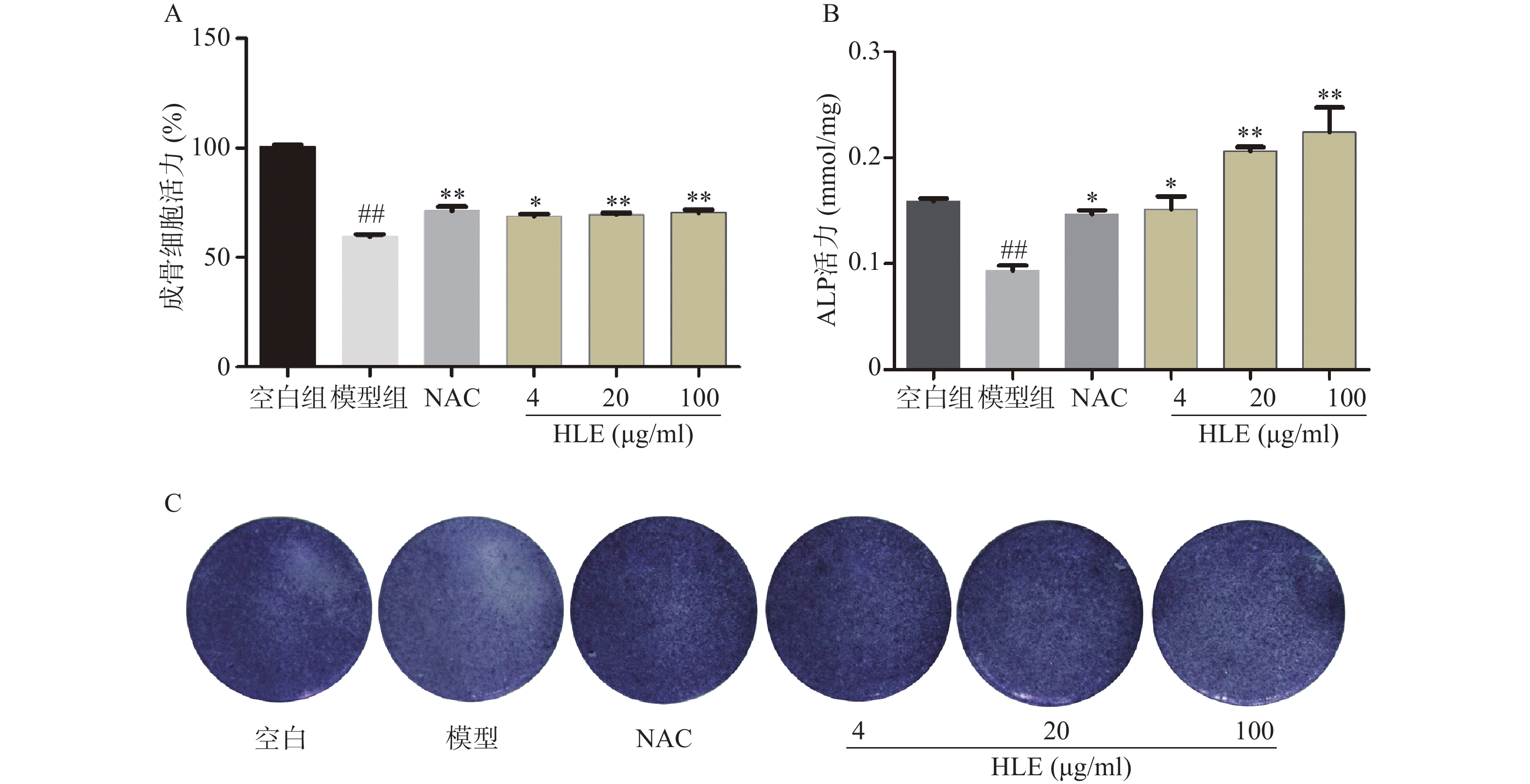
2.1 啤酒花提取物促进Aβ损伤成骨细胞增殖,提高ALP活性
如图1A所示,与空白组相比,Aβ损伤成骨细胞后,其增殖能力显著降低。药物治疗后,低、中、高剂量的啤酒花提取物均可显著促进Aβ损伤成骨细胞的增殖。另一方面,与空白组比,Aβ显著降低了成骨细胞的ALP活性,而啤酒花提取物显著逆转了Aβ损伤成骨细胞的ALP活性,促进成骨细胞的分化(图1B-C)。
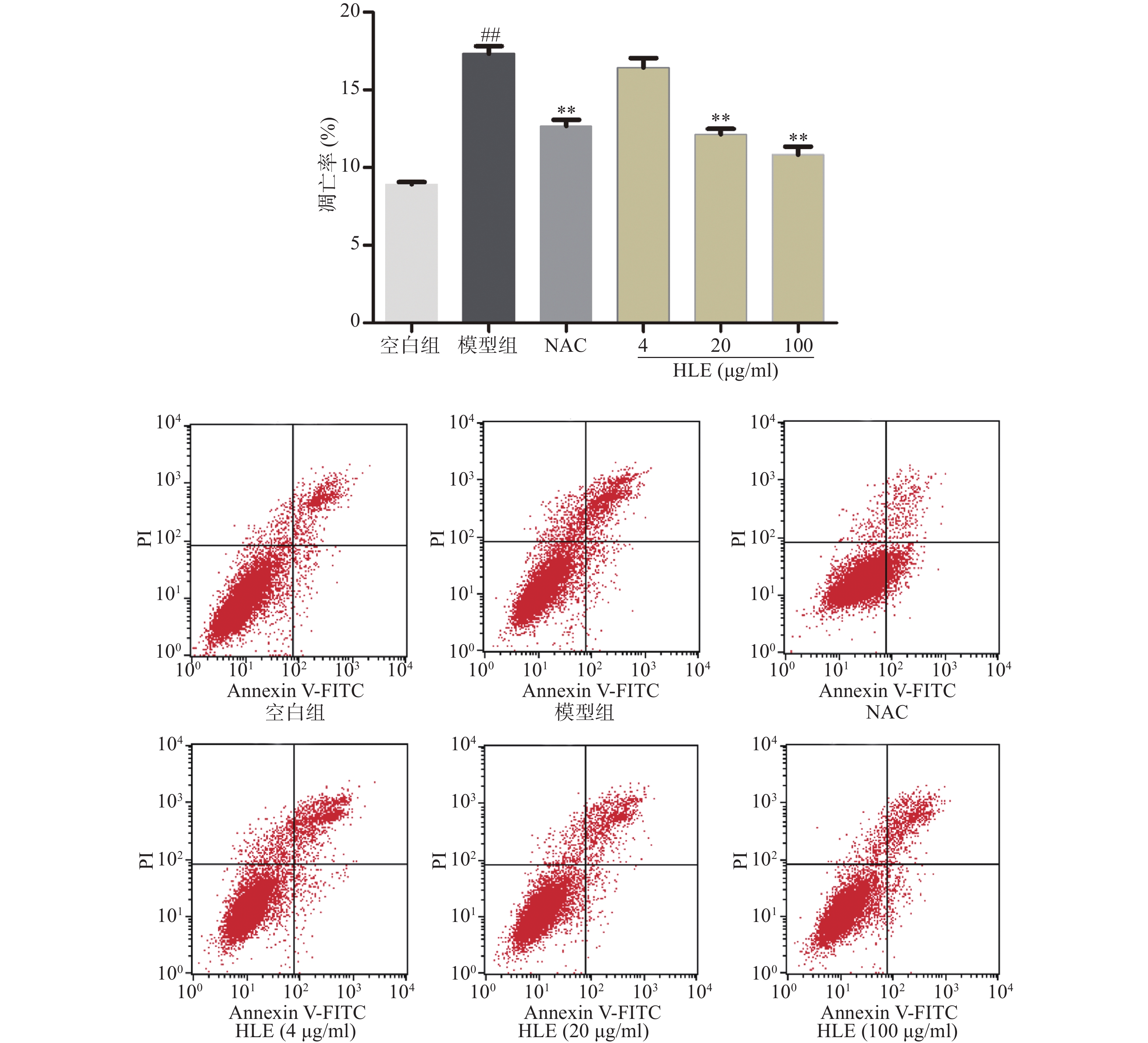
2.2 啤酒花提取物抑制Aβ损伤成骨细胞凋亡
如图2所示,与空白组相比,Aβ损伤提高了成骨细胞的凋亡率,而啤酒花提取物(20,100 μg/ml)可显著抑制Aβ损伤成骨细胞的凋亡。提示啤酒花提取物对Aβ诱导的成骨细胞具有较强的抗凋亡作用。
2.3 啤酒花提取物促进Aβ损伤成骨细胞中骨形成相关蛋白表达
如图3所示,Aβ损伤成骨细胞后,细胞中骨形成相关蛋白COL-I和OPN的表达显著降低。给予啤酒花提取物(20,100 μg/ml)干预后,COL-I及OPN的表达显著增加,提示啤酒花可显著促进Aβ损伤成骨细胞的骨形成。
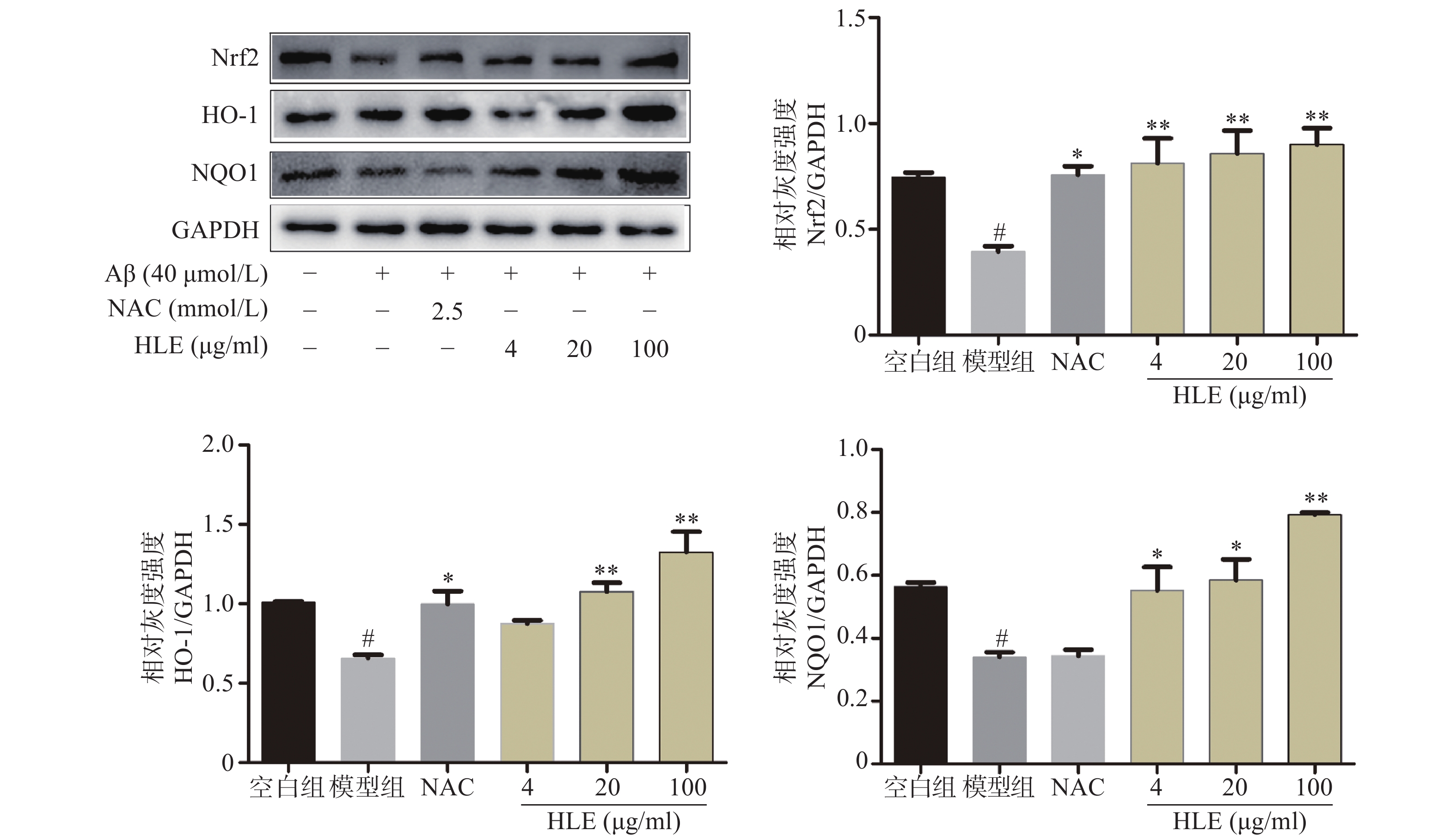
2.4 啤酒花提取物调节Nrf2氧化应激通路
采用Western blot分析Aβ和啤酒花提取物对成骨细胞中Nrf2及其下游抗氧化酶HO-1和NQO1的影响。结果显示,Aβ显著抑制了成骨细胞中Nrf2及其下游蛋白HO-1和NQO1的表达;而低、中、高剂量的啤酒花提取物均可显著促进Aβ损伤成骨细胞中Nrf2、HO-1及NQO1的表达(图4),提示其能够通过介导Nrf2信号通路发挥抗氧化作用。
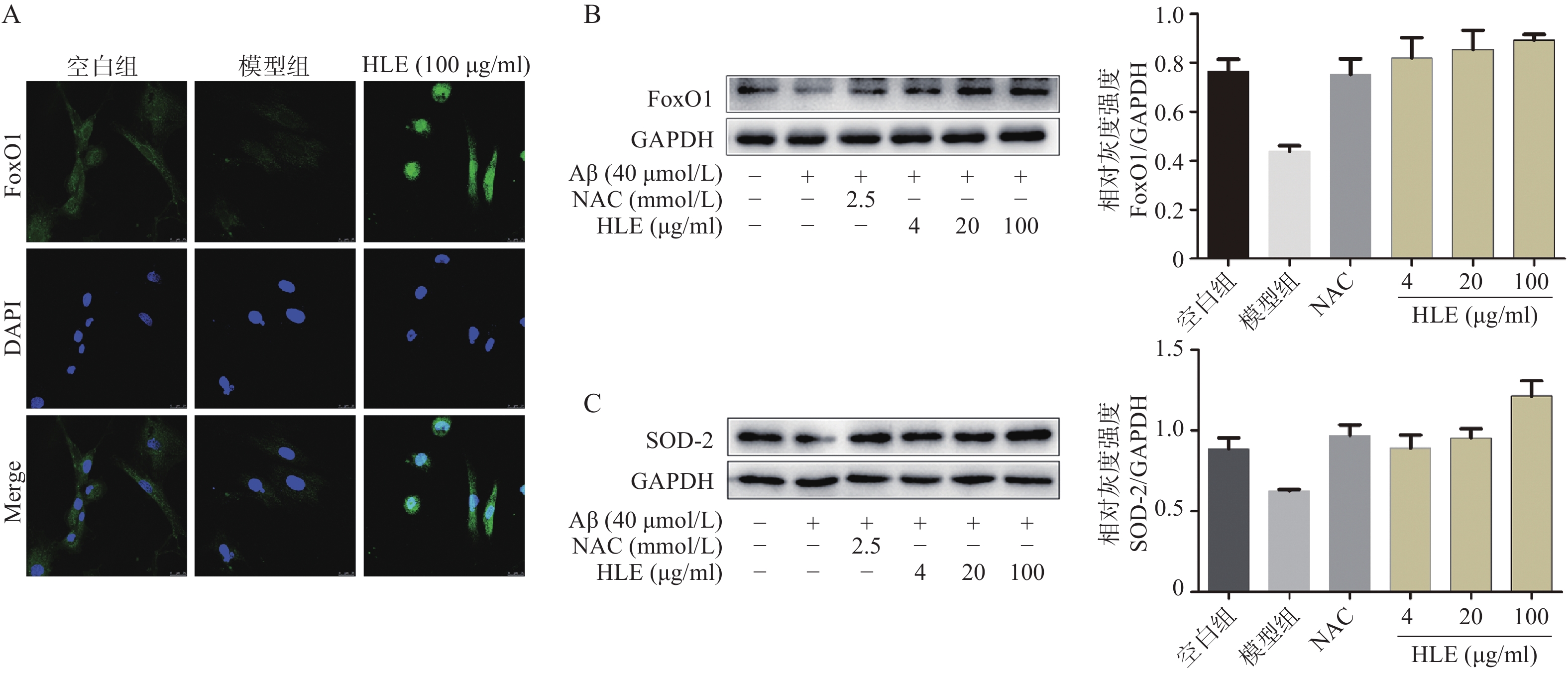
2.5 啤酒花提取物调节FoxO1抗氧化通路
采用免疫荧光及Western blot分析Aβ和啤酒花提取物对成骨细胞中FoxO1信号通路的影响。结果显示,与空白组相比,Aβ显著降低了成骨细胞中的FoxO1含量,而啤酒花提取物(100 μg/ml)可显著下调FoxO1的表达,且使其更多聚集在细胞核内(图5A)。此外,啤酒花提取物(4、20、100 μg/ml)还可显著促进Aβ损伤成骨细胞中FoxO1及其下游蛋白SOD-2的表达,提示啤酒花能够通过介导FoxO1信号通路发挥抗氧化作用。
3. 讨论
成骨细胞是骨形成的主要功能细胞,在骨形成过程中经历增殖、分化、矿化和凋亡四个阶段。其中,成骨细胞的增殖水平反映骨形成的强弱,其分泌的ALP是成骨细胞分化阶段的关键酶[11],可介导骨组织矿化。在骨形成相关蛋白中,COL-I是骨细胞外基质的主要成分之一,约占骨总蛋白的80%[12],而OPN是一种骨基质糖蛋白,能够促进成骨细胞的黏附和分化[13],二者均为成骨细胞分化成熟的标志。此外,Aβ沉积会引起机体的氧化损伤,在骨代谢中可降低骨髓间充质干细胞向成骨细胞的分化,破坏成骨细胞的活性和功能,抑制骨形成[14]。我们前期研究同样发现过量的Aβ在聚集过程中会产生大量的活性氧,使机体处于高氧化应激状态,反过来又刺激Aβ产生和聚集,形成Aβ与氧化损伤相偶联[15]。该机制在老年性骨质疏松症发病中处于特别重要的位置,并受到学界关注[16]。本研究中,啤酒花提取物可显著逆转Aβ损伤所致的成骨细胞增殖水平下降、ALP活性降低,以及COL-I和OPN的低表达,表明其可显著促进成骨细胞的成熟分化;并抑制Aβ损伤成骨细胞的凋亡,表明其可显著改善Aβ沉积所致成骨细胞的活性损伤,促进骨形成,在维持骨稳态中发挥重要作用。
Nrf-2信号通路是典型的抗氧化通路,能够拮抗各种原因引起的氧化应激。激活Nrf2信号通路不仅能够抑制氧化损伤成骨细胞的凋亡,促进骨形成[17],而且能够拮抗Aβ诱导的细胞损伤[18-19]。应激状态下,Nrf-2转移入核内,与基因中的抗氧化反应元件结合,启动下游Ⅱ相代谢酶基因的表达和转录,以增加细胞对氧化应激的抵抗作用,使细胞免于凋亡[20]。FoxO1为调节成骨细胞氧化还原平衡和成骨功能的主要转录因子,其入核可激活下游SOD-2抗氧化酶,调控细胞内的氧化还原平衡,并促进成骨细胞的增殖与分化,在骨代谢中同样发挥着重要作用[20]。本研究结果表明,啤酒花可激活Aβ损伤成骨细胞的Nrf-2和FoxO1信号通路,促进该氧化应激信号通路中相关蛋白的表达,增加成骨细胞对氧化应激的抵抗作用,使其免于凋亡,进而促进成骨细胞增殖与分化。提示啤酒花具有通过抗氧化而调控骨代谢、维持骨稳态之应用潜力。
-
[1] CAIN D W, CIDLOWSKI J A. Immune regulation by glucocorticoids[J]. Nat Rev Immunol,2017,17(4):233-247. doi: 10.1038/nri.2017.1 [2] IOANNIDIS G, PALLAN S, PAPAIOANNOU A, et al. Glucocorticoids predict 10-year fragility fracture risk in a population-based ambulatory cohort of men and women: Canadian Multicentre Osteoporosis Study (CaMos)[J]. Arch Osteoporos,2014,9:169. doi: 10.1007/s11657-013-0169-5 [3] AGHAMIRI V, MIRGHAFOURVAND M, MOHAMMAD-ALIZADEH-CHARANDABI S, et al. The effect of Hops (Humulus lupulus L.) on early menopausal symptoms and hot flashes: a randomized placebo-controlled trial[J]. Complement Ther Clin Pract,2016,23:130-135. doi: 10.1016/j.ctcp.2015.05.001 [4] LIU M, HANSEN P E, WANG G Z, et al. Pharmacological profile of xanthohumol, a prenylated flavonoid from hops (Humulus lupulus)[J]. Molecules,2015,20(1):754-779. doi: 10.3390/molecules20010754 [5] XIA T S, LIN L Y, ZHANG Q Y, et al. Humulus lupulus L. extract prevents ovariectomy-induced osteoporosis in mice and regulates activities of osteoblasts and osteoclasts[J]. Chin J Integr Med,2021,27(1):31-38. doi: 10.1007/s11655-019-2700-z [6] 林柳悦, 夏天爽, 蒋益萍, 等. 啤酒花活性成分黄腐酚抗骨质疏松作用研究[J]. 药学实践杂志, 2018, 36(3):219-223. doi: 10.3969/j.issn.1006-0111.2018.03.006 [7] GU G, HENTUNEN T A, NARS M, et al. Estrogen protects primary osteocytes against glucocorticoid-induced apoptosis[J]. Apoptosis,2005,10(3):583-595. doi: 10.1007/s10495-005-1893-0 [8] 张乃丹. 基于分子对接策略的熟地黄防治糖尿病性骨质疏松症有效成分及其作用机制研究[D]. 上海: 第二军医大学, 2016. [9] 夏天爽, 林柳悦, 蒋益萍, 等. 苦味酸类成分蛇麻酮和葎草酮对大鼠成骨细胞和破骨细胞的干预作用[J]. 第二军医大学学报, 2019, 40(1):25-30. [10] CAMOZZI V, BETTERLE C, FRIGO A C, et al. Vertebral fractures assessed with dual-energy X-ray absorptiometry in patients with Addison's disease on glucocorticoid and mineralocorticoid replacement therapy[J]. Endocrine,2018,59(2):319-329. doi: 10.1007/s12020-017-1380-8 [11] 张萌萌. 中国老年学学会骨质疏松委员会骨代谢生化指标临床应用专家共识[J]. 中国骨质疏松杂志, 2014, 20(11):1263-1272. [12] BERENDSEN A D, OLSEN B R. Osteoblast-adipocyte lineage plasticity in tissue development, maintenance and pathology[J]. Cell Mol Life Sci,2014,71(3):493-497. doi: 10.1007/s00018-013-1440-z [13] XIA T S, DONG X, LIN L Y, et al. Metabolomics profiling provides valuable insights into the underlying mechanisms of Morinda officinalis on protecting glucocorticoid-induced osteoporosis[J]. J Pharm Biomed Anal,2019,166:336-346. doi: 10.1016/j.jpba.2019.01.019 [14] 阙文君, 冯正平. 骨转换生化标志物的研究进展[J]. 中国骨质疏松杂志, 2014, 20(5):575-579. doi: 10.3969/j.issn.1006-7108.2014.05.025 [15] NGUYEN H T, ONO M, OIDA Y, et al. Bone marrow cells inhibit BMP-2-induced osteoblast activity in the marrow environment[J]. J Bone Miner Res,2019,34(2):327-332. doi: 10.1002/jbmr.3598 [16] XIA T S, DONG X, JIANG Y P, et al. Metabolomics profiling reveals rehmanniae Radix preparata extract protects against glucocorticoid-induced osteoporosis mainly via intervening steroid hormone biosynthesis[J]. Molecules,2019,24(2):E253. doi: 10.3390/molecules24020253 期刊类型引用(4)
1. 徐卫凡,徐武牧,丁卢颖,蒋益萍,夏天爽,辛海量. 巴戟天丸防治D-半乳糖损伤成骨细胞骨丢失的作用及机制研究. 药学实践与服务. 2023(03): 155-159 .  本站查看
本站查看2. 欧泽洁,孔凡玉,周月南,杨朝霞,庞雪莉. 基于超临界CO_2萃取和旋转锥体柱法的啤酒花提取物香气特征比较. 食品安全质量检测学报. 2023(12): 46-53 .  百度学术
百度学术3. 赖立勇,徐圣焱,夏天爽,蒋益萍,辛海量. 基于抗氧化机制的中药及其化学成分在骨质疏松中的应用. 海军军医大学学报. 2022(08): 943-950 .  百度学术
百度学术4. 郝建秦,张晶晶,薛洁,张磊,王德良. 啤酒花中多酚类化合物指纹图谱及化学计量学分析. 中外酒业. 2022(09): 1-7 .  百度学术
百度学术其他类型引用(2)
-






 下载:
下载:


 下载:
下载:









