-
在我国成人死因中,脑卒中位列第一,全球第二[1-2]。在所有的脑卒中患者中,有78%的患者是缺血性脑卒中,其他为出血性脑卒中[3]。脑卒中的治疗药物很少,目前FDA唯一批准的药物只有组织纤溶酶原激活剂。但是,由于其治疗窗口狭窄、有禁忌证和并发症风险,组织纤溶酶原激活剂仅适用于3%~5%的脑卒中患者[2]。因而,寻求新的治疗靶点和手段显得十分重要。
烟酰胺磷酸核糖转移酶(Nampt)又被称作内脏脂肪素,也是一种脂肪因子。它还有一个名称是PBEF,是合成哺乳动物细胞内烟酰胺腺嘌呤二核苷酸(NAD+)的关键限速酶[4]。最近的研究证明了Nampt可以作为缺血性脑卒中治疗新靶点[2-3,5-7]。Nampt治疗缺血性脑卒中的作用机制包括急性期的脑保护以及慢性期的促血管修复和神经再生作用。这些作用机制通过体内体外试验在神经细胞、内皮祖细胞和神经干细胞得到证实。NAD+在细胞能量维持中起着关键作用[8],而Nampt可以通过补救合成途径促进哺乳动物中NAD+生物合成,影响ATP的产生,对抗缺血性脑卒中后的供能不足,维持细胞内能量稳态,抑制神经细胞死亡[3]。
Nampt既可存在于细胞内,也可以分泌到细胞外[9]。从细胞分泌出来后可以存在于血液中,与高血压、糖尿病等多种疾病相关[10,11]。在缺血性脑卒中发生后,外周血液的Nampt会显著性升高[12-13]。局部脑组织内Nampt对缺血性脑卒中的保护作用已经十分明确,而脑外组织来源的Nampt对缺血性脑卒中的作用研究较少。已知肝脏细胞可以分泌Nampt,并且肝脏被认为是血液Nampt的主要组织来源之一[3,14-15]。本研究主要通过Cre/loxP重组酶系统特异性敲除肝脏Nampt基因的表达,利用大脑中动脉阻塞(MCAO)缺血性脑卒中模型,研究肝脏来源的Nampt是否参与缺血性脑卒中的保护,为进一步明确Nampt作为缺血性脑卒中治疗新靶点的重要意义,为探究外周器官参与缺血性脑卒中损伤及修复的新机制打下基础。
-
NamptloxP/loxP小鼠(南京医科大学王强教授实验室赠予)和Albumin-Cre小鼠(上海南方模式生物科技发展有限公司)。动物自由饮水、进食;环境温度控制在(25±1) ℃,相对湿度40%~60%,昼夜均为12 h。所有动物实验均符合实验动物伦理学要求。
-
PCR仪(TaKaRa),M200 PRO多功能酶标仪(瑞士Tecan公司),SC12型水平电泳槽(北京凯元信瑞仪器有限公司),FR-980A生物电泳图像分析系统(上海复日科技有限公司),红外激光扫描成像系统(LI-COR),蛋白电泳、转膜系统(上海天能科技有限公司),高通量组织研磨仪(上海万柏生物科技有限公司),颅骨钻(广州坤图生物科技有限公司),CHR多功能手术仪(武汉春光医疗美容仪器有限公司)。
-
小鼠鉴定引物(上海生工生物工程股份有限公司)序列如表1所示。
表 1 基因型鉴定引物
序号 引物序列(5’-3’) 鉴定基因型 条带位置 引物1 野生型上游引物:
TGCAAACATCACATGCACAC
通用型下游引物:
TTGGCCCCTTACCATAACTG
突变型上游引物:
GAAGCAGAAGCTTAGGAAGATGGNamptloxP/loxPAlb-Cre 150 bp
351 bp
390 bpNamptloxP/loxP 351 bp 引物2 下游引物:
TTCCAGGCTATTCTGTTCCAG
上游引物:
TCTGGCTCTGTGTACTGCTGANamptloxP/loxP 300 bp 鼠尾基因组DNA提取试剂盒(康为世纪生物科技有限公司),多聚甲醛(博光生物科技有限公司),GAPDH抗体和BCA蛋白浓度试剂盒(上海碧云天生物技术有限公司),PBEF抗体(F-8)(Santa Cruz Biotechnology),Premix TaqTM (TaKaRa),硝酸纤维素转移膜(Whatman),IRDye®800CW Donkey anti-Mouse IgG二抗(LI-COR),血浆Visfatin 检测试剂盒(Phoenix Pharmaceuticals, Inc),2,3,5-氯化三苯基四氮唑(BBI Life Science),异戊巴比妥(BIOSZUNE LIFE SCIENCES DEP),水合氯醛(国药集团化学试剂有限公司)。
-
白蛋白(Alb)仅在肝脏中表达。目前,Alb基因启动子作为肝脏特异性启动子被广泛用于制备肝脏特异性基因敲除小鼠模型[16]。NamptloxP/loxPAlb-Cre及其同窝对照NamptloxP/loxP小鼠由NamptloxP/loxP和Alb-Cre两种小鼠杂交获得。培育过程如图1:①将NamptloxP/loxP 小鼠与Alb-Cre小鼠交配,筛选获得NamptloxP/WTAlb-Cre,②NamptloxP/WTAlb-Cre与NamptloxP/loxP小鼠交配,得到NamptloxP/loxPAlb-Cre,③最后将NamptloxP/loxPAlb-Cre与NamptloxP/loxP交配,得到用于实验的NamptloxP/loxPAlb-Cre(即liver-specific Nampt knockout mice,以下简称LNKO)及其同窝对照NamptloxP/loxP小鼠(以下简称WT),用引物1对其子代进行基因型鉴定。实验中①②③交配使用的NamptloxP/loxP 小鼠全部用NamptloxP/loxP与NamptloxP/loxP小鼠交配所得,用引物2对其子代进行基因型鉴定。
-
剪取5周龄小鼠尾巴约0.5 cm。置于1.5 ml离心管中,剪碎后,按照鼠尾基因组DNA提取试剂盒(康为世纪生物科技有限公司)说明书进行提取。
-
扩增小鼠DNA,扩增程序如图2,扩增体系20 μl:Premix TaqTM 10 μl,引物1 μl (5 μm),DNA溶液2 μl,ddH2O体积为7 μl,混合均匀后放入PCR仪进行扩增。NamptloxP/loxPAlb-Cre与NamptloxP/loxP交配得到的子代用引物1和扩增程序图2A进行鉴定,NamptloxP/loxP 与NamptloxP/loxP交配得到的子代,理论上都为NamptloxP/loxP,用引物2和扩增程序图2B进行鉴定。
-
配制2%的琼脂糖凝胶(琼脂糖凝胶未凝固前每10 ml加入1 μl的gelRed试剂),在水平100 V电泳槽中电泳30 min。
-
最后用生物电泳图像分析系统,在312 nm紫外线下拍摄成像。
-
用1%异戊巴比妥腹腔麻醉小鼠(100 mg/kg),心脏取血后,取出小鼠的肝脏、脑,用高通量组织研磨仪对组织进行匀浆,在4 ℃,12 000×g的条件下,离心20 min后取上清液,用BCA法进行蛋白定量,通过蛋白免疫印迹法检测Nampt蛋白。
-
用4%水合氯醛腹腔麻醉小鼠(400 mg/kg),将小鼠固定在鼠板上,剔除左眼周围的毛发后,酒精棉球消毒,用镊子揪起左耳外耳道和左眼外眦之间的皮,平行于下层肌肉表面做1 cm切口,分离头骨外周肌肉,用颅骨钻在颞骨前下紧邻颧弓前上缘的部位打磨使颞骨变薄,用镊子去除部分头骨,在手术显微镜下找到大脑中动脉,并用电凝器凝断位于嗅束至大脑下静脉之间的主干,再缝合伤口。术后将小鼠置于保温毯上,待清醒后放回动物笼内饲养。
-
神经行为学损伤评分采用5分法[17]。0分:正常,无神经功能缺损;1分:瘫痪侧前爪不能完全伸展,轻度神经功能缺损;2分:行走时,小鼠向瘫痪侧转圈,中度神经功能缺损;3分:行走时,小鼠身体向瘫痪侧倾倒,重度神经功能缺损;4分:不能自发行走,有意识丧失。
-
MCAO造模24 h后将小鼠麻醉,断头取出脑,放入−20 ℃冷冻15~20 min,再用刀片将全脑冠状切出6片1 mm厚的脑片,去掉尾部带有嗅球、小脑和低位脑干的部分。脑片用37 ℃预热的2% TTC染色,37 ℃避光染色30 min,正常组织为红色,梗死组织为白色。4%多聚甲醛固定1 h后,用滤纸吸干液体再取出脑片,用扫描仪扫描脑片,用Image J计算梗死面积,以测量梗死脑组织体积占总测量脑片体积的百分比作为衡量脑梗死的指标。每片切片的脑梗死体积=(该切片双面梗死面积之和÷2)×层厚,相对脑梗死体积(%)=(全部切片梗死体积之和÷全部切片体积之和)×100%。
-
小鼠心脏取血得到血浆后,用ELISA法测定Nampt的含量。测定步骤按照血浆Visfatin 检测试剂盒说明书进行。
-
采用GraphPad Prism 8.0软件对数据进行统计分析,实验数据用(
$ \stackrel{-}{x} $ ±s)表示,通过独立样本t检验分析组间差异的显著性,以P<0.05为具有统计学差异。 -
核酸电泳条带为150 bp+351 bp+390 bp的为NamptloxP/loxPAlb-Cre,即LNKO小鼠,核酸电泳条带为351 bp的为NamptloxP/loxP,即WT小鼠。小鼠基因型鉴定结果如图3所示,从左到右,泳道1为DNA Maker,泳道2和3为WT小鼠(351 bp),泳道4和5为LNKO小鼠(150 bp+351 bp+390 bp)。
-
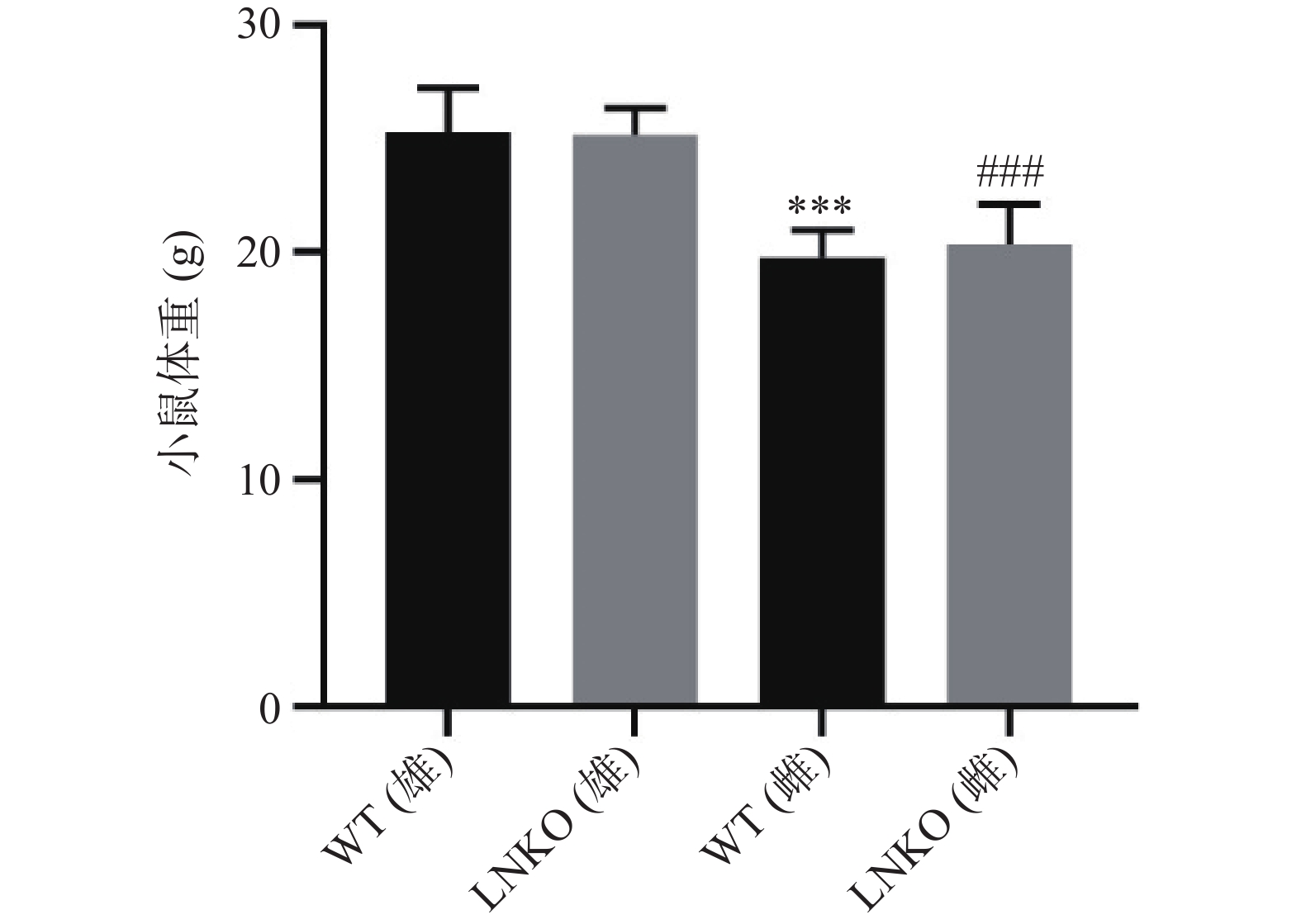
比较各组小鼠12周龄的体重。如图4所示,WT雄性小鼠的体重为(25.31±1.91) g,LNKO雄性小鼠的体重为(25.19±1.17) g,WT雌性小鼠的体重为(19.79±1.19) g,LNKO雌性小鼠的体重为(20.36±1.79) g。同一性别中,LNKO和WT小鼠体重比较没有显著性差异。WT小鼠中,雄鼠比雌鼠平均重5.52 g(P<0.001)。LNKO小鼠中,雄鼠比雌鼠平均重4.83 g (P<0.001)。以上结果说明特异性敲除肝脏Nampt基因表达,对小鼠的体重无影响。
-
为进一步验证成功培育肝脏特异性Nampt基因敲除小鼠,提取各组小鼠的肝脏和脑组织蛋白,通过蛋白免疫印迹验证两种组织中Nampt蛋白的表达。如图5A所示,同一性别肝脏组织中,LNKO小鼠Nampt蛋白表达水平都显著性低于其对照WT小鼠,其中LNKO雄性小鼠Nampt蛋白表达水平比WT雄性小鼠降低了67.1%;LNKO雌性小鼠Nampt蛋白表达水平比WT雌性小鼠降低了81.3%。如图5B所示,在脑组织中,LNKO小鼠Nampt蛋白表达水平与其对照小鼠相比无显著性差异。蛋白免疫印迹结果进一步证明,肝脏特异性Nampt基因敲除小鼠被成功构建。
-
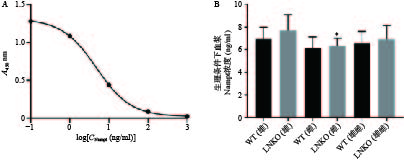
根据血浆Visfatin检测试剂盒的数据处理方法,测量Nampt蛋白的标准品(浓度依次为0.1、1、10、100、1000 ng/ml)在450 nm处的吸光度(A)值,对数据进行四参数Logistic曲线拟合得到图6A,R2=1,曲线拟合效果很好。
根据拟合曲线方程和样品的吸光度值,计算各组小鼠血浆Nampt蛋白浓度。如图6B所示,同一性别对应的LNKO与WT小鼠血浆Nampt蛋白浓度无显著性差异,LNKO与WT小鼠的血浆Nampt蛋白浓度也无显著性差异。只有LNKO雄性组的血浆Nampt蛋白平均浓度比LNKO雌性组略升高0.91 ng/ml(P<0.05)。
-
MCAO造模43只小鼠,成功造模38只,其中WT雄性小鼠11只,LNKO雄性小鼠8只,WT雌性小鼠11只,LNKO雌性小鼠8只,造模成功率为88.37%。
-
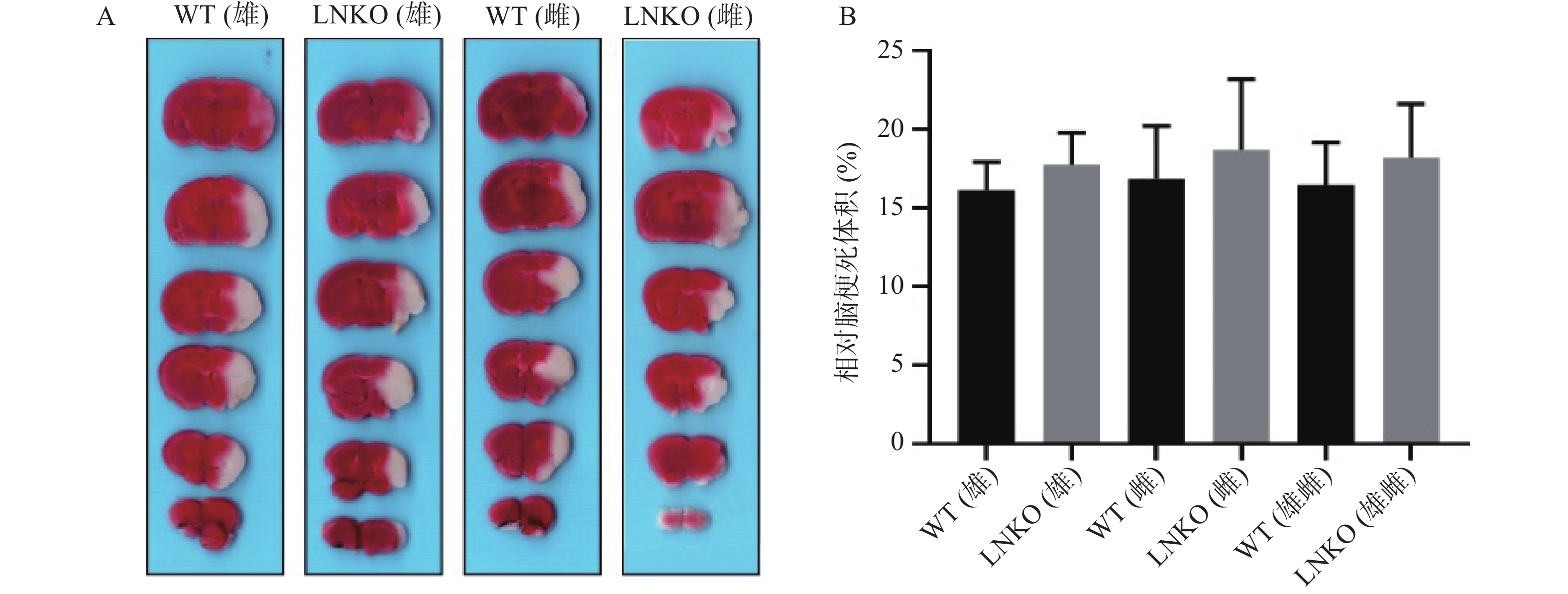
图7A显示各组典型脑片TTC染色,白色是梗死区。图7B代表统计后各组相对脑梗死体积。MCAO造模24 h后,相对脑梗死体积数据如下:WT雄性组为(16.14±1.78)%,LNKO雄性组为(17.71±2.08)%,WT雌性组为(16.85±3.36)%,LNKO雌性组为(18.68±4.50)%。各组在MCAO 造模24 h后的相对脑梗死体积无显著性差异。
-
神经行为学损伤评分数据如表2所示。造模24 h后,各组小鼠以轻度神经功能损伤为主,瘫痪侧前肢不能完全伸展;每组都存在部分发生中度神经功能损伤,行走时向瘫痪侧转圈。各组在MCAO造模24 h后神经行为学评分无显著性差异,而且各组神经行为学评分高低与相对脑梗死体积一致。
表 2 各组小鼠MCAO造模24 h后神经行为学损伤评分 (n≥8)
组别 神经行为学损伤评分(分) WT雄性组 1.20±0.42 LNKO雄性组 1.50±0.71 WT雌性组 1.32±0.56 LNKO雌性组 1.63±0.69 WT组 1.26±0.49 LNKO组 1.56±0.68 WT: 肝脏特异性Nampt基因敲除小鼠同窝对照;LNKO: 肝脏特异性Nampt基因敲除小鼠。 -
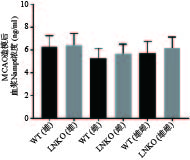
MCAO造模24 h后,各组血浆Nampt蛋白平均浓度:WT雄性组为(6.26±0.98) ng/ml,LNKO雄性组为(6.44±1.03) ng/ml,WT雌性组为(5.28±0.86) ng/ml,LNKO雌性组为(5.70±0.80) ng/ml。如图8所示,LNKO及其同窝对照WT小鼠在MCAO造模24 h后血浆Nampt蛋白表达无显著性差异。
-
本研究利用Cre/loxP重组酶系统成功构建肝脏特异性Nampt基因敲除小鼠,并证实肝脏来源Nampt对缺血性脑卒中没有明显保护作用。
Cre/loxP重组酶系统介导的基因打靶方法是目前应用最为广泛的基因条件性敲除方法。 loxP序列中的特殊回文结构可以被Cre酶特异性识别结合并催化两个loxP序列之间的片段发生同源重组,进而实现对该片段的基因敲除。我们通过基因鉴定和肝脏Nampt蛋白免疫印迹从基因和蛋白两个层面对该动物模型进行验证,结果都表明小鼠肝脏Nampt基因被特异性敲除。以同窝对照为阴性对照,监测两组小鼠的一般状况,发现其体重、活动状态等无显著差异。有研究曾比较10、55、110周雌性肝脏特异性Nampt基因敲除小鼠与对照小鼠体重,两者无显著性差异,这与本研究结果一致[16]。
Nampt是一种脂肪细胞因子,可由脂肪组织大量分泌。除此以外,其他如肝细胞,白细胞,单核细胞,B细胞,心肌细胞和各种神经细胞也可分泌Nampt,目前认为脂肪、肝脏和白细胞是血液Nampt来源的主要器官[3],但是血液中Nampt的各组织分泌的贡献率并不是十分清楚。本研究首次显示特异性敲除小鼠肝脏Nampt基因的表达并不能显著影响生理情况下血浆Nampt蛋白浓度,这是基于肝脏特异性Nampt基因敲除小鼠的一个在体研究结果,不同于前期的相关研究。前期研究报道了肝脏HepG2细胞[15]、大鼠来源肝细胞[14-15]和原代人的肝细胞[15]可以大量分泌Nampt蛋白,这些结论主要基于的都是体外的细胞实验,没有研究整体的动物和人。本研究结果说明生理状态下肝脏Nampt的分泌水平可能相对较低,对血液Nampt的贡献率不如脂肪组织。肝脏特异性Nampt基因敲除导致的Nampt分泌减少在生理状态下可能仍然能够被脂肪等组织很好地代偿,因而血浆Nampt水平不改变。在这点上,脂肪特异性Nampt基因敲除对血液Nampt水平的影响更大。Yoon等[18]发现雌性脂肪特异性Nampt基因敲除鼠的血浆Nampt水平显著低于雌性对照鼠。此外,研究结果说明肝脏特异性敲除Nampt基因表达后,性别因素并不显著影响肝脏对血液Nampt的贡献率,这与脂肪特异性Nampt基因敲除小鼠有所不同[18]。
但是肝脏特异性Nampt基因敲除是否影响外周血Nampt水平还可能与病理状态和禁食因素等有关。有研究报道与健康对照组相比,肝硬化患者的血液Nampt水平显著升高[19],提示病理状态时肝脏对血液Nampt的贡献会发生改变。另一方面, 血液Nampt水平受禁食因素影响,所以检测结果和动物进食状态有关。有研究发现禁食会升高Nampt血液水平[18]。本研究在未禁食下检测,肝脏特异性Nampt基因敲除不改变血液Nampt水平。但在禁食状态下,各组织对血液Nampt贡献情况很可能会发生改变,从而引起血液Nampt水平变化。本研究所反映的仅是在非禁食的生理状态下以及脑缺血后的肝脏特异性Nampt基因敲除小鼠的外周血Nampt水平,在其他条件下肝脏特异性Nampt基因敲除是否对血液Nampt水平有影响有待进一步研究。
本研究的一个重要目的是确认肝脏来源Nampt是否参与脑缺血损伤及修复。在缺血性脑卒中时,机体除了调动脑内细胞的Nampt发挥保护作用,肝脏来源的Nampt是否也参与了机体的内在防御修复作用仍属未知。本研究采用电凝法制备脑卒中模型和肝脏特异性Nampt基因敲除动物开展研究。电凝法手术在直视下操作,手术中出血量少,造模成功率高,导致的脑缺血效果稳定,可模拟永久性脑梗死。造模后小鼠出现轻度到中度神经功能损伤,脑片TTC染色出现白色梗死区域,说明电凝法可成功制备MCAO模型。肝脏特异性Nampt基因敲除小鼠肝脏Nampt蛋白表达下降,而脑内Nampt蛋白表达不受影响,非常适合本课题的研究目的。研究结果显示,同一性别,与野生型相比,肝脏特异性Nampt基因敲除并不影响脑卒中的相对梗死体积和神经行为学评分,说明肝脏来源Nampt不主要参与脑缺血损伤及修复。这一结果的原因可能与肝脏来源Nampt对血液Nampt的贡献率不大有关。血液Nampt的水平是外周Nampt发挥脑生物学功能的基础。在正常条件下,本研究已证实肝脏来源Nampt对血液Nampt的贡献率不大。在脑卒中条件下,卒中后24 h肝脏特异性Nampt基因敲除组和对照组小鼠血液Nampt水平无显著性差异,也说明肝脏来源Nampt对卒中后血液Nampt变化的贡献率不大。
本研究显示,肝脏特异性Nampt基因敲除后,雄性小鼠比雌性小鼠血浆中Nampt表达水平略高,但是后续这两种性别小鼠在缺血后脑梗死面积并没有显著性差异。在生理状态下,LNKO雄性比LNKO雌性血液Nampt水平表达略高。脑卒中24 h后,LNKO雄性小鼠比LNKO雌性小鼠血液Nampt水平有升高趋势,但无统计学差异。这两个血液水平的结果是比较一致的。同样,从脑梗死结果来看,虽然LNKO雌性小鼠的脑梗死体积和LNKO雄性小鼠相比无统计学差异,但是有升高趋势。从行为学评分来看,LNKO雌性小鼠的神经功能学损伤评分相比LNKO雄性小鼠也有升高趋势。这两个结果与血液水平也是总体一致的。
血液水平Nampt改变仅仅是影响脑梗死严重程度的一个因素,组织水平Nampt改变也会影响脑梗死程度。不仅如此,动物的个体差异,手术操作的差异,也会影响脑梗死程度。因此,在现有的动物例数下,两种性别的小鼠在缺血后脑梗死面积并没有统计学差异。后续可以考虑进一步扩大例数,确认两种性别小鼠在脑梗死程度上是否存在差别,并同时观察脑组织Nampt水平是否在两种性别小鼠脑缺血模型上有差别,以明确不同性别小鼠外周来源Nampt和脑组织Nampt对卒中的影响是否存在差异。
Nampt是防治脑卒中的内源性靶点[3],是兼具有多种重要功能的脂肪因子。已知Nampt 可被分泌入血,血液Nampt具有酶活性,有生物学功能[12]。外周来源Nampt很可能是机体维持生理稳态,在病理状态下加强防御、促进修复的重要内源性调控因子。因此,确认Nampt的血液来源和探究血液Nampt的潜在生物学功能具有重要意义。本研究首次确认了肝脏来源Nampt对生理状态血液Nampt的贡献情况和对脑缺血损伤的作用,为后续研究打下了重要基础。当然,本研究也存在不足,比如仅观测卒中后24 h的情况,未观察多个时间点的卒中情况,以及卒中慢性恢复期的情况。血液Nampt的另一个主要来源是脂肪,脂肪来源Nampt对血液Nampt的贡献情况已有报道[18],但对脑缺血损伤的作用尚未见报道。这些都有待进一步研究探索。
Effects of liver-specific Nampt knockout on ischemic stroke
-
摘要:
目的 烟酰胺磷酸核糖转移酶(nicotinamide phosphoribosyltransferase,Nampt)是缺血性脑卒中的治疗新靶点。本研究旨在阐明肝脏来源的Nampt是否对缺血性脑卒中具有保护作用。 方法 运用Cre/loxP系统制备肝脏特异性Nampt基因敲除小鼠。将NamptloxP/loxP小鼠与肝脏特异性表达Cre重组酶小鼠(Alb-Cre)进行杂交,采用聚合酶链反应方法鉴定子代基因型。测定基因敲除小鼠和同窝对照小鼠的体重。蛋白免疫印迹法检测小鼠肝脏和脑中Nampt蛋白的表达。采用电凝法对肝脏特异性Nampt基因敲除小鼠和对照小鼠制备大脑中动脉阻塞(middle cerebral artery occlusion,MCAO)脑卒中模型,造模24 h后对各组小鼠进行神经功能损伤评分,TTC染色测定脑梗死体积,ELISA法检测各组小鼠血浆Nampt水平。 结果 成功构建肝脏特异性Nampt基因敲除小鼠,其基因型为NamptloxP/loxP Alb-Cre。肝脏特异性Nampt基因敲除组肝脏Nampt蛋白表达与对照组相比下降74.2%。脑Nampt蛋白的表达在敲除组与对照组之间无显著性差异。肝脏特异性Nampt基因敲除对小鼠的体重无影响。正常生理条件下,同性别肝脏特异性Nampt基因敲除小鼠与对照小鼠血浆Nampt水平无明显差异。MCAO造模24 h后,肝脏特异性Nampt基因敲除组与对照组神经行为学损伤评分、脑梗死体积和血浆Nampt浓度也无显著性差异。 结论 成功构建肝脏特异性Nampt基因敲除小鼠;肝脏来源Nampt对缺血性脑卒中没有明显保护作用。 -
关键词:
- 烟酰胺磷酸核糖转移酶 /
- 特异性敲除 /
- 肝脏 /
- 脑卒中
Abstract:Objective Nicotinamide phosphoribosyltransferase (Nampt) is a new therapeutic target for ischemic stroke. The aim of this study was to investigate protective effect of liver-derived Nampt on ischemic stroke. Methods Liver-specific Nampt knockout mice were generated using the Cre/loxP system. NamptloxP/loxP mice were crossed with liver-specific Cre recombinase expression mice (Alb-Cre), and the progeny genotypes were identified by polymerase chain reaction. Body weight of knockout mice and control mice were measured. Nampt in liver and brain was determined by Western blot assay. Middle cerebral artery occlusion (MCAO), a classical ischemic stroke model, was generated in liver-specific Nampt knockout mice and control mice by electrocoagulation. After 24 h of modeling, neurological deficit scores of each group were evaluated and TTC staining was performed to determine the cerebral infarction volume. The level of plasma Nampt in each group was determined by ELISA. Results Liver-specific Nampt knockout mice with the genotype of NamptloxP/loxPAlb-Cre were successfully constructed. The hepatic Nampt expression in knockout mice was significantly decreased by 74.2% compared to control mice, while there was no significant difference in the expression of brain Nampt protein between the knockout group and the control group. Specific knockout of liver Nampt gene expression had no effect on the body weight of mice. Under normal physiological conditions, there was no significant difference in plasma Nampt levels between liver-specific Nampt knockout mice and control mice of the same gender. 24 h after MCAO modeling, there were no significant differences in neurological deficit scores, cerebral infarct volume and plasma Nampt concentration between liver-specific Nampt knockout group and control group. Conclusion Liver-specific Nampt knockout mice are successfully constructed. Liver-derived Nampt has no significant protective effects on ischemic stroke. -
Key words:
- Nampt /
- specific knockout /
- liver /
- stroke
-
类风湿关节炎(RA) 是一种以滑膜关节病变为主的慢性全身性、进行性自身免疫性疾病。疾病最早开始表现是滑膜炎,继而引发骨损伤及侵蚀,直至骨关节畸形及功能障碍[1-2],RA动物模型中广泛使用的是佐剂性关节炎模型和胶原诱导的关节炎模型。佐剂性关节炎又称弗氏佐剂性关节炎,是建立免疫性关节炎动物模型的基本方法[3]。RA发病机制还不明确,目前缺乏理想的治疗方案。临床上治疗RA主要是非甾体类抗炎药、抗风湿药物及糖皮质激素等[4],但往往因为药物的不良反应、价格等因素,难以坚持长期服药。
茵连痛风颗粒是上海中医药大学附属岳阳中西医结合医院院内制剂,由菌陈、连钱草、伸筋草组成,具有清热利湿、通络的功效。其处方是依据沪上著名夏氏外科传人夏涵教授数年临床经验方制成,用于治疗痛风性关节炎,临床具有显著疗效[5]。本实验通过弗氏完全佐剂诱导大鼠关节炎模型,观察茵连痛风颗粒对佐剂性关节炎的影响,为茵连痛风颗粒的临床应用提供科学依据。
1. 材料
1.1 药物与试剂
茵连痛风颗粒(上海中医药大学附属岳阳中西医结合医院药剂科自制,沪药制字:Z05050342,批号:1811001);塞来昔布胶囊(辉瑞制药有限公司,批号:AN8171);弗氏完全佐剂(Sigma 公司); IL-10、IL-4、前动力蛋白(PK1、2)酶联免疫分析试剂盒均购自上海威奥生物科技有限公司。
1.2 动物
SD 大鼠,雄性,体重(160±10)g,[上海斯莱克实验动物有限责任公司,实验动物生产许可证号:SCXK(沪)2017-0005]。
1.3 仪器
酶标仪(型号:DENLEY DRAGON Wellscan MK3,公司:Thermo);离心机(型号:TGL-168,公司:上海安亭科学仪器厂);数字显示隔水式电热恒温培养箱(型号:PYX-DHS,公司:上海跃进医疗器械厂);自制刻度软尺。
2. 方法
2.1 分组给药和模型建立
将48只SD雄性大鼠适应性饲养1周后,随机分为6组,每组8只。分别为正常组,模型组,塞来昔布阳性组(0.017 g/kg),茵连痛风颗粒高剂量组(15.4 g/kg),茵连痛风颗粒中剂量组(7.7 g/kg),茵连痛风颗粒低剂量组(3.8 g/kg)。除正常组外,其余各组大鼠右后足皮内注射弗氏完全佐剂 0.1 ml/足。注射弗氏完全佐剂后第8天,按照如上剂量灌胃给予相应浓度的受试药品,正常组和模型组给予等体积蒸馏水,每天给药1次,连续给药28 d。
模型鉴定:造模后各组大鼠的皮肤肿胀,皮肤温度及踝关节肿胀度与正常组之间是否有统计学差异,是模型成功与否的判定标准。
2.2 实验方法
2.2.1 大鼠一般情况和关节炎症状评分
分别在大鼠给药后7、14、28 d记录大鼠四肢关节病变程度,采用关节炎指数(AI)评分分级法评价大鼠病变程度。关节炎指数分为 5级(0~4分):0分,关节无红肿;l分,单个趾关节明显红肿;2分,发红并(或)肿胀关节>l个;3分,整个足及跖关节明显红肿;4分,严重的关节肿胀或畸形。根据未注射佐剂的余下肢体的病变程度累计积分,计算出AI(各个关节的积分累计起来,即为每只大鼠的 AI)。
2.2.2 茵连痛风颗粒对大鼠踝关节肿胀度影响
分别于造模前、给药后1 d、以及每间隔8 d,用刻度软尺测量大鼠右后踝关节周长,并观察各组动物关节病变情况。按照下列公式计算踝关节肿胀率:踝关节肿胀率=(致炎后踝关节周长-致炎前踝关节周长) /致炎前踝关节周长×100% 。
2.2.3 对大鼠甲醛致痛的影响[6]
末次给药后2 h,于大鼠左足趾皮下注射50 μl 2.5%甲醛,观察1~10 min(第I时相)和10~30 min(第II时相)的行为反应。评分标准:第I时相抬足1次,计1分;第II时相舔足、咬足或抖足1次,计2分。计算30 min内的总得分。
2.2.4 血清炎症指标检测和病理组织观察
末次给药后禁食、禁水12 h,大鼠注射10%水合氯醛(0.3 ml/100 g)进行麻醉,腹主动脉取血,离心取血清,用ELISA 法检测血清中IL-10、IL-4、PK1、PK2含量; 各组大鼠取左侧足掌肉垫,福马林固定,乙醇梯度脱水,石蜡包埋、切片和HE染色,病理组织学观察。
2.3 统计学分析
采用 SPSS 21.0 统计软件进行分析,实验数据以(
$ \bar x \pm s $ )表示,组间比较采用单因素方差分析。3. 结果
3.1 茵连痛风颗粒对大鼠一般情况及关节炎指数的影响
造模前各组大鼠毛色光亮,动作敏捷,精神状态和饮食均良好。模型组大鼠在造模后,自主活动减少、足底局部出现红肿,后期整只爪和关节均有不同程度肿胀,最初表现为足部肿胀,而后肿胀向上到达踝关节,肿胀部位皮肤发红,温度升高。随着时间延长,大鼠食欲减退,毛色暗黄,且运动功能逐渐减退。给予茵连痛风颗粒高、中、低剂量组及塞来昔布阳性组大鼠精神状态有所好转,关节肿胀度、食欲等有不同程度的缓解。表1结果表明,与模型组比较,给药7、14、28 d后,茵连痛风颗粒高、中剂量组和阳性组大鼠关节炎指数显著降低(P<0.01)。
表 1 茵连痛风颗粒对大鼠关节炎指数的影响 ($ \bar x \pm s $ ,n=8)组别 剂量(g/kg) 给药后关节炎指数 第7天 第14天 第28天 正常组 — 0.00±0.00 0.00±0.00 0.00±0.00 模型组 — 6.37±0.52## 9.63±0.74## 8.38±0.92## 阳性组 0.017 5.63±0.51** 6.50±0.93** 4.38±0.52** 高剂量组 15.4 5.50±0.53** 7.13±0.0.83** 4.13±0.64** 中剂量组 7.7 5.75±0.46** 8.13±0.0.83** 5.63±0.52** 低剂量组 3.8 5.88±0.35* 9.13±0.81 8.13±0.74 *P<0.05,**P<0.01,与模型组比较;##P<0.01,与正常组比较。 3.2 茵连痛风颗粒对大鼠踝关节肿胀度影响
表2结果显示,与同期正常组比较,模型组在给药第9天时肿胀率达峰值, 17d开始,肿胀逐日减轻,给药第9天开始,阳性组和茵连痛风颗粒高剂量组足肿胀与模型组比较,肿胀明显减轻,有显著统计学差异(P<0.01);在给药第25、28天,茵连痛风颗粒中剂组与模型组有显著性差异(P<0.05),茵连痛风颗粒低剂组无明显差异。结果显示了茵连痛风颗粒对佐剂性关节炎大鼠原发足踝关节肿胀有剂量依赖性抑制作用。
表 2 茵连痛风颗粒对大鼠踝关节肿胀率的影响 ($ \bar x \pm s $ ,n=8)组 别
踝关节周长(l/cm)给药后踝关节肿胀率(%) 第1天 第9天 第17天 第25天 第28天 正常组 2.24±0.05 2.77±0.71 3.36±1.87 3.56±4.70 3.94±6.89 4.31±7.95 模型组 2.26±0.06 28.75±6.36## 30.09±8.24## 26.51±10.43## 25.44±12.90## 23.31±13.26## 阳性组 2.27±0.08 27.00 ±0.00 22.63±1.77** 20.61±1.45** 19.33±4.31** 18.45±4.67** 高剂量 2.22±0.05 27.54 ±1.03 23.85±1.56** 20.01±0.04** 18.14±1.52** 17.85±2.40** 中剂量 2.24±0.06 28.24 ±0.67 28.68±0.92 25.19±0.88 22.26±1.52* 21.85±2.40* 低剂量 2.28±0.07 29.48 ±0.21 29.49±2.23 26.05±0.99 25.01±0.32 24.10±0.28 *P<0.05,**P<0.01,与模型组比较; ##P<0.01,与正常组比较。 3.3 茵连痛风颗粒对大鼠甲醛致痛的影响
与模型组比较,在I时相和II时相,阳性组和茵连痛风颗粒高、中、低剂量组可显著降低甲醛致痛分值(P<0.01),表明茵连痛风颗粒具有很好的镇痛作用(表3)。
表 3 茵连痛风颗粒对大鼠甲醛致痛的影响 ($ \bar x \pm s $ ,n=8)组 别 剂量 (g/kg) 甲醛致痛分值 1~10 min(Ⅰ时相) 10~30 min(Ⅱ时相) 正常组 — 2.38±0.52 1.38±0.52 模型组 — 33.63±1.41## 14.88±1.64## 阳性组 0.017 11.38±1.06** 3.50±0.93** 高剂量组 15.4 12.13±0.99** 3.25±1.04** 中剂量组 7.7 16.00±1.60** 5.25±0.89** 低剂量组 3.8 19.38±1.19** 6.50±1.20** **P<0.01;与模型组比较; ##P<0.01,与正常组比较。 3.4 茵连痛风颗粒对IL-4、IL-10、PK1、PK2的影响
模型组大鼠IL-10,IL-4与正常组相比显著降低(P<0.01),炎性反应较明显;茵连痛风颗粒各组和阳性组均能升高IL-10,IL-4水平。同时,模型组大鼠 PK1、PK2水平与正常组相比显著升高(P<0.01),阳性组和茵连痛风颗粒各组均能降低两者水平,与模型组比较有显著差异 (P<0.01),其中,茵连痛风颗粒高剂量组更明显(表4)。
表 4 茵连痛风颗粒对大鼠血清IL-4、IL-10、PK1、PK2的影响 ($ \bar x \pm s $ ,n=8)组别 剂量 (g/kg)
IL-4
IL-10
PK1
PK2正常组 — 79.49±4.38 97.07±2.97 491.76±8.56 926.24±25.38 模型组 — 59.89±3.45## 20.99±2.78## 706.31±67.83## 1455.40±147.81## 阳性组 0.017 139.69±13.78** 98.94±6.72** 567.10±20.58** 1099.60±63.63** 高剂量组 15.4 101.45±7.05** 90.36±5.43** 365.49±27.65** 656.07±194.68** 中剂量组 7.7 95.60±4.52** 82.75±8.49** 433.91±22.29** 866.73±21.57** 低剂量组 3.8 72.50±3.09** 78.15±5.47** 529.20±12.79** 1015.51±18.36** **P<0.01,与模型组比较; ##P<0.01,与正常组比较。 3.5 病理观察
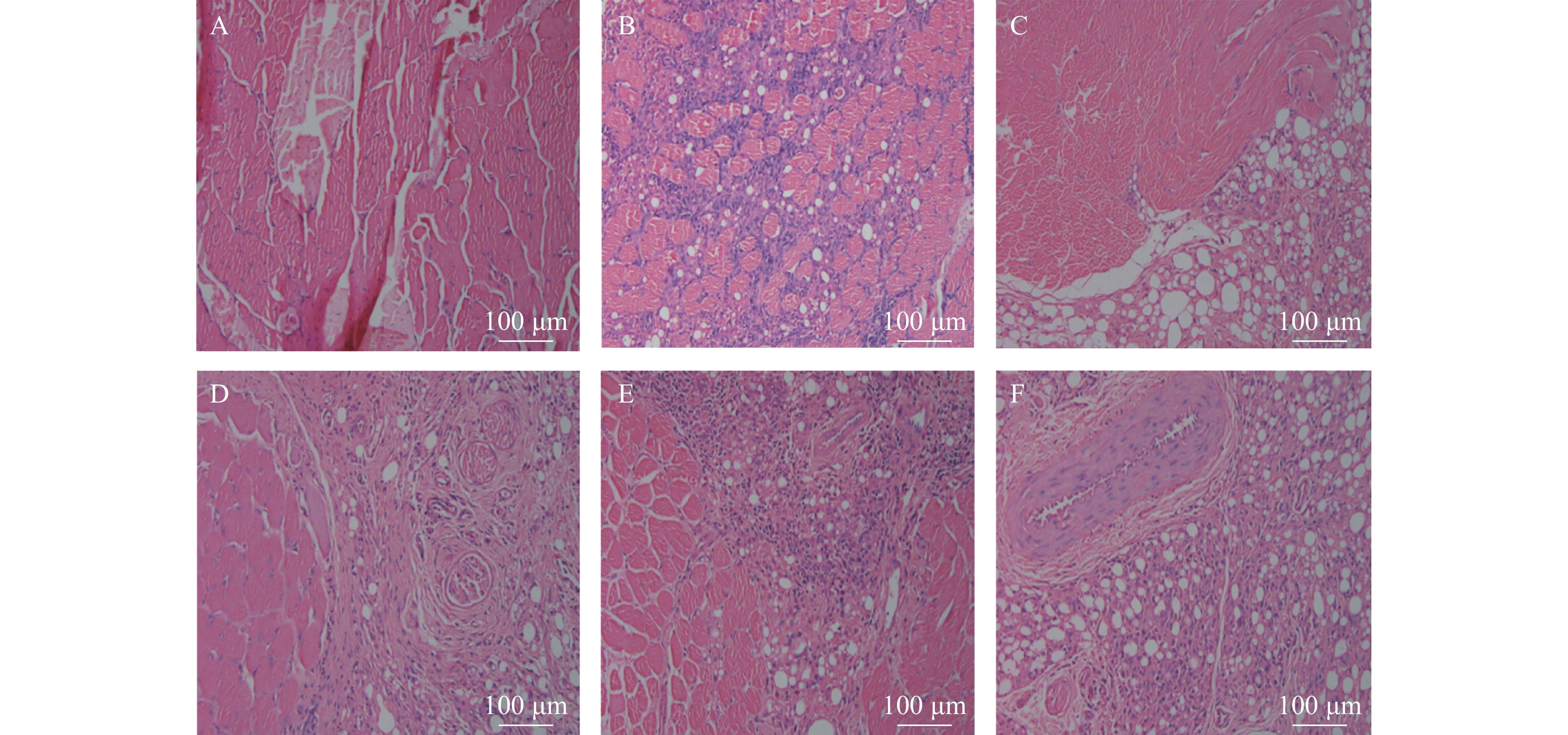
由图1可见,正常对照组足趾肉垫无炎症细胞浸润,而模型组可见大量淋巴细胞浸润。塞来昔布组可见淋巴细胞浸润程度的大幅度降低,而茵连痛风颗粒高、中、低剂量组均可降低淋巴细胞浸润,而以茵连痛风颗粒高剂量组最为显著。
4. 讨论
类风湿关节炎在中医归属“痹症”范畴,治疗以祛风除湿、散寒通络、扶正固本、清热解毒为主[7]。茵连痛风颗粒有茵陈、连钱草、伸筋草三味药材组成。茵陈作为君药,具有清利湿热、芳香舒脾、透表畅气之效;臣药连钱草,取其消石之功,防止痛风性尿路结石的产生,具有利湿通淋、清热解毒、散瘀消肿之功效;佐药伸筋草具有祛风除湿、舒筋活血之效,为治痹痛拘挛及伤损瘀肿之要药,配伍茵陈可以增强该复方利湿通络的作用。该方配伍符合中医理论对类风湿性关节炎的认识[8]。
弗氏佐剂关节炎动物模型是经典的类风湿关节炎模型,与类风湿性关节炎模型的病因、病症更接近。它能较为真实地反映类风湿关节炎的病理进程,与痛风性关节炎同属中医 “痹证”“白虎历节风”范畴,而且制备方法简便、易重复。常用于关节炎药物的药效评估[9]。IL-4、IL-10细胞因子在类风湿性关节炎患者中,起到十分重要的作用。这类细胞因子与滑膜炎性反应、增生及关节变形有着密切的关系。PK信号通路是近年新发现的调节通路,包括两种结构上关联的小分子肽PK1和PK2及相应的G蛋白偶联受体PK(PKR1和PKR2),PKs及其受体PKRs广泛分布在许多人体组织中。在免疫细胞中参与炎症发生和疼痛传递的重要环节,如PK2参与免疫调节,诱导骨髓细胞分化为单核细胞系和巨噬细胞系,并通过激活单核细胞、巨噬细胞和树突状细胞上的 PKRs,释放IL-1、IL-6、TNF-a等炎性细胞因子,触发和维持炎性疼痛,调节免疫炎症反应[10-11]。研究发现在前动力蛋白信号通路中加入PKRs激动剂可以显著降低IL-10和IL-4生成[12]。损伤组织中释放的PKs是免疫-炎症反应的一种自分泌或旁分泌的调节剂,能够刺激神经元中PKRs而增强伤害性感受器的敏感性,说明PKs信号通路在调节伤害性感受阈方面发挥重要功能,因此阻断PKs信号通路是目前治疗炎性疼痛的新策略[11]。然而,关于PK信号通路在中药镇痛方面的研究报道较少,其干预中药镇痛的具体机制有待进一步研究证实。本实验结果显示,茵连痛风颗粒可明显减轻RA大鼠足踝关节肿胀,按照人和大鼠之间的体表面积换算成大鼠的给药中剂量,并设置高、中、低3个剂量组。以高剂量组改善最为明显,并呈现剂量依赖性。同时,病理结果显示,茵连痛风颗粒高中低剂量组均可降低淋巴细胞浸润,以茵连痛风颗粒高剂量组最为显著。其作用机制可能是通过PK信号通路抑制PK1、PK2分泌,以及促进细胞因子IL-4、IL-10等分泌达到抗类风湿性关节炎的作用。为茵连痛风颗粒作用机制的阐明打下了基础。这些研究结果表明,茵连痛风颗粒对佐剂关节炎具有明显抑制作用,暗示其对类风湿关节炎的治疗前景,作用机制有待进一步研究。
-
表 1 基因型鉴定引物
序号 引物序列(5’-3’) 鉴定基因型 条带位置 引物1 野生型上游引物:
TGCAAACATCACATGCACAC
通用型下游引物:
TTGGCCCCTTACCATAACTG
突变型上游引物:
GAAGCAGAAGCTTAGGAAGATGGNamptloxP/loxPAlb-Cre 150 bp
351 bp
390 bpNamptloxP/loxP 351 bp 引物2 下游引物:
TTCCAGGCTATTCTGTTCCAG
上游引物:
TCTGGCTCTGTGTACTGCTGANamptloxP/loxP 300 bp 表 2 各组小鼠MCAO造模24 h后神经行为学损伤评分 (n≥8)
组别 神经行为学损伤评分(分) WT雄性组 1.20±0.42 LNKO雄性组 1.50±0.71 WT雌性组 1.32±0.56 LNKO雌性组 1.63±0.69 WT组 1.26±0.49 LNKO组 1.56±0.68 WT: 肝脏特异性Nampt基因敲除小鼠同窝对照;LNKO: 肝脏特异性Nampt基因敲除小鼠。 -
[1] CAMPBELL B C V, KHATRI P. Stroke[J]. Lancet,2020,396(10244):129-142. doi: 10.1016/S0140-6736(20)31179-X [2] WANG S N, MIAO C Y. Targeting NAMPT as a therapeutic strategy against stroke[J]. Stroke Vasc Neurol,2019,4(2):83-89. doi: 10.1136/svn-2018-000199 [3] WANG P, MIAO C Y. NAMPT as a therapeutic target against stroke[J]. Trends Pharmacol Sci,2015,36(12):891-905. doi: 10.1016/j.tips.2015.08.012 [4] REVOLLO J R, GRIMM A A, IMAI S. The NAD biosynthesis pathway mediated by nicotinamide phosphoribosyltransferase regulates Sir2 activity in mammalian cells[J]. J Biol Chem,2004,279(49):50754-50763. doi: 10.1074/jbc.M408388200 [5] CHEN F, WENG Z, XIA Q, et al. Intracerebroventricular delivery of recombinant NAMPT deters inflammation and protects against cerebral ischemia[J]. Transl Stroke Res,2019,10(6):719-728. doi: 10.1007/s12975-019-00692-0 [6] ZHU T, XIE W J, WANG L, et al. Notoginsenoside R1 activates the NAMPT-NAD+-SIRT1 cascade to promote postischemic angiogenesis by modulating Notch signaling[J]. Biomed Pharmacother,2021,140:111693. doi: 10.1016/j.biopha.2021.111693 [7] WANG X, LI H, DING S. Pre-B-cell colony-enhancing factor protects against apoptotic neuronal death and mitochondrial damage in ischemia[J]. Sci Rep,2016,6:32416. doi: 10.1038/srep32416 [8] HOUTKOOPER R H, CANTÓ C, WANDERS R J, et al. The secret life of NAD+: an old metabolite controlling new metabolic signaling pathways[J]. Endocr Rev,2010,31(2):194-223. doi: 10.1210/er.2009-0026 [9] LIU J, CHE X, YOU J, et al. Intracellular Nampt impairs esophageal squamous cell carcinoma neo-adjuvant chemotherapy response independent of eNampt[J]. Am J Transl Res,2021,13(3):1411-1421. [10] DAKROUB A, NASSER S A, YOUNIS N, et al. Visfatin: a possible role in cardiovasculo-metabolic disorders[J]. Cells,2020,9(11):2444. doi: 10.3390/cells9112444 [11] ZHOU L, ZHANG S, BOLOR-ERDENE E, et al. NAMPT/SIRT1 attenuate ang II-induced vascular remodeling and vulnerability to hypertension by inhibiting the ROS/MAPK pathway[J]. Oxidative Med Cell Longev,2020,2020:1974265. [12] ZHAO Y, LIU X Z, TIAN W W, et al. Extracellular visfatin has nicotinamide phosphoribosyltransferase enzymatic activity and is neuroprotective against ischemic injury[J]. CNS Neurosci Ther,2014,20(6):539-547. doi: 10.1111/cns.12273 [13] LU L F, YANG S S, WANG C P, et al. Elevated visfatin/pre-B-cell colony-enhancing factor plasma concentration in ischemic stroke[J]. J Stroke Cerebrovasc Dis,2009,18(5):354-359. doi: 10.1016/j.jstrokecerebrovasdis.2009.01.003 [14] ŠKOP V, KONTROVÁ K, ZÍDEK V, et al. Autocrine effects of visfatin on hepatocyte sensitivity to insulin action[J]. Physiol Res,2010:615-618. doi: 10.33549/physiolres.931845 [15] GARTEN A, PETZOLD S, BARNIKOL-OETTLER A, et al. Nicotinamide phosphoribosyltransferase (NAMPT/PBEF/visfatin) is constitutively released from human hepatocytes[J]. Biochem Biophys Res Commun,2010,391(1):376-381. doi: 10.1016/j.bbrc.2009.11.066 [16] DALL M, TRAMMELL S A J, ASPING M, et al. Mitochondrial function in liver cells is resistant to perturbations in NAD+ salvage capacity[J]. J Biol Chem,2019,294(36):13304-13326. doi: 10.1074/jbc.RA118.006756 [17] LONGA E Z, WEINSTEIN P R, CARLSON S, et al. Reversible middle cerebral artery occlusion without craniectomy in rats[J]. Stroke,1989,20(1):84-91. doi: 10.1161/01.STR.20.1.84 [18] YOON M J, YOSHIDA M, JOHNSON S, et al. SIRT1-mediated eNAMPT secretion from adipose tissue regulates hypothalamic NAD+ and function in mice[J]. Cell Metab,2015,21(5):706-717. doi: 10.1016/j.cmet.2015.04.002 [19] MOSCHEN A R, GERNER R, SCHROLL A, et al. A key role for Pre-B cell colony-enhancing factor in experimental hepatitis[J]. Hepatology,2011,54(2):675-686. doi: 10.1002/hep.24416 -







 下载:
下载:




 下载:
下载: