-
烟酰胺腺嘌呤二核苷酸(NAD+)是一种重要的代谢产物,其参与许多生化过程,如能量代谢、基因表达调控、DNA修复等[1, 2]。人体皮肤、血液、肝脏、肌肉和大脑中的NAD+浓度会随着年龄的增长而降低,因此,增强NAD+可能在缓解相关的细胞功能和整体健康受损方面发挥关键作用[3]。烟酰胺单核苷酸(NMN)是NAD+生物合成的前体。体内外研究表明,补充NMN可以提高NAD+水平[4]。NMN可以缓解各种心脑血管疾病的发展,包括中风[5]、心力衰竭[6]和心肌缺血等[7]。此外,NMN还与改善线粒体功能和潜在的抗衰老益处有关[8]。几项临床试验探索了NMN补充剂的有效性和安全性(标识号:NCT04228640[9],NCT04823260[10],UMIN000036321[11])[8],证明了其对心血管保护的潜力。然而,NMN的研究仍然缺乏大规模可靠的人体试验数据,特别是关于其治疗高血压等特定疾病的疗效问题。虽然早期研究显示了一些有希望的结果,但需要更广泛的基础研究和临床试验来证实其在不同患者群体中的疗效和安全性。
高血压是一系列健康问题的重要危险因素,包括心脏、肾脏疾病以及中风等脑血管疾病[12],影响着全世界数百万人[13]。高血压的危险在于,随着时间的推移会导致靶器官损伤,发生如动脉粥样硬化、肾功能衰竭、心力衰竭和中风等疾病。高血压的发生与衰老和肥胖等因素有关,而这两者都源自于NAD+缺乏。因此,NAD+已成为高血压的潜在治疗靶点。
目前关于NMN对高血压的影响研究相对有限。只有一项临床前实验表明NMN可以降低血管紧张素II(Ang II)诱导的高血压小鼠的血压[14]。另有一项临床研究表明,补充NMN可以降低高血压患者的血压(标识号:NCT04903210[14])。然而,目前的证据不足以将NMN开发为抗高血压药物,特别是其缺乏较为全面的临床前药效评价。因此需要更严格的研究来确定NMN是否能作为高血压治疗药物。自发性高血压大鼠(SHR)是一种遗传性高血压模型动物,常用于评估抗高血压药物[15-17]。双肾双夹(2K2C)大鼠是一种实验性易卒中肾血管性高血压模型动物,这些大鼠在术后2周内100%发生高血压[15, 16],也常用于评估抗高血压药物。本次研究中,我们采用单次胃瘘给药和长期药物饲料喂养方式给予受试大鼠NMN治疗,观察NMN对原发性和继发性高血压大鼠模型的血压和器官损伤的影响。此外,我们还观察了终身给药NMN对2K2C大鼠模型死亡率和寿命的影响[15]。
-
Sprague-Dawley(SD)雄性大鼠(160~180 g)购于上海必凯科翼生物科技有限公司。2K2C大鼠由SD大鼠双侧肾动脉嵌套0.2 mm内径的U型银夹制作而成。雄性SHR(250~290 g)购于北京维通利华实验动物技术有限公司。
所有大鼠均饲养于独立通气笼盒(IVC)系统中,饲养温度为24±2°C,相对湿度为40%~60%,照明时间为8:00~20:00,自由饮食和饮水(特定情况除外)。本实验研究严格遵守实验动物福利等伦理原则。
-
NMN(批号2021046B)由尚科生物医药(上海)有限公司提供,氯沙坦钾(Losartan)(批号LOSB-4-06210326)由浙江美诺华药业股份有限公司提供,戊巴比妥钠购于德国Merck公司,注射用青霉素钠购于山东鲁抗医药股份有限公司,肝素钠(批号H3v60)购于上海博光生物科技有限公司,EVG弹力纤维染色试剂盒购于北京索莱宝科技有限公司。
U型银夹(0.2 mm内径)、血压与心率分析系统(型号MPA-HBBS)购于上海奥尔科特生物科技有限公司,聚乙烯导管购于法国Biotrol公司。
-
NMN单次给药治疗研究:包括SHR和2K2C大鼠两种模型,在各自模型实验中,大鼠均被随机分配为对照组(蒸馏水)和NMN给药组(200 mg/kg),并通过胃瘘导管给药。
NMN长期给药(4周)治疗研究:包括SHR和2K2C大鼠两种模型,在各自模型实验中,大鼠均被随机分配为对照组(普通饲料)和NMN给药组[药物饲料,等效NMN剂量200 mg/(kg·d)]。
生存时间观察研究:采用2K2C大鼠模型,实验包括假手术组(正常SD大鼠,普通饲料)和2K2C造模组,2K2C造模组大鼠再被随机分为模型组(普通饲料)、氯沙坦给药组[药物饲料,等效剂量20 mg/(kg·d)]和NMN给药组[药物饲料,等效剂量200 mg/(kg·d)]。
-
2K2C模型是通过在正常SD大鼠的两个肾动脉上放置0.2 mm尺寸的银夹后造成的高血压模型,参考本教研室文献及方案[16,17]。简言之,SD大鼠用2%戊巴比妥钠(40 mg/kg)麻醉,腹部切口,轻轻翻转肾脏,游离出肾动脉后放上内径为0.2 mm的U形银夹。在另一侧肾脏重复相同步骤。小心复位肾脏和周围组织。假手术的大鼠进行相同的操作至游离血管步骤,但不放置U形银夹。以上步骤完成后,滴加青霉素,缝合。然后将大鼠放在电热毯上,苏醒后送回IVC系统笼。
-
用2%戊巴比妥钠(40 mg/kg)麻醉大鼠,腹部区域脱毛并消毒,自剑突下沿腹部中间切口2 cm,使用无菌棉签将胃轻轻拉出,于近幽门段并且避开血管作荷包预缝合,预留区域内戳出小孔,迅速将胃瘘导管缠有胶布端插入胃内,拉紧预缝合线固定导管,经背部皮下牵引至颈后穿出并固定。随后,将胃瘘导管以大鼠马甲方式固定于背部防止动物清醒后抓咬。手术完成后,动物于电热毯上保温至复苏。
-
参考本教研室文献及方案[15, 16],用2%戊巴比妥钠(40 mg/kg)麻醉大鼠,左侧腹股沟区域脱毛并消毒,并沿股动脉方向切开皮肤,暴露股动脉。游离出一段股动脉,插入特制的PE测压导管,导管前端依次穿行过股动脉、髂总动脉并最后进入腹主动脉,此时测得血压为腹主动脉血压,导管的另一端沿皮下穿行至颈部背侧皮肤后穿出,用自制马甲固定,缝合伤口。术后,大鼠饲养于测量系统笼里适应环境,自由饮食和饮水。24 h后,测压导管连接压力传感器,经MPA-HBBS数据分析系统处理后将压力信号转化为血压波形显示在电脑屏幕上。同时以0.3 ml/h的速率连续输注25 U/ml肝素钠,以防止测压过程中凝血。
NMN单次给药实验中,大鼠股动脉插管手术后次日上午9:00开启测量系统,连续记录血压和心率信号。12:00,通过胃管给予相应的药物(NMN或蒸馏水)。连续记录24 h血压和心率变化(取给药前1 h的数据作为基础血压和心率)。NMN长期给药实验中,NMN给药组和对照组的大鼠同样使用上述方法进行血压和心率测量,并连续记录2 h。
-
在完成血压和心率测量后,大鼠再次麻醉并迅速打开胸腔,用4 ℃预冷的生理盐水对大鼠进行心脏灌注。取出脑、肝脏、心脏、肾脏和主动脉(从左锁骨下动脉分支到横膈膜段),测量器官重量,以及主动脉长度、左心室壁厚度、肾皮质和髓质厚度。随后,将脑、心脏、主动脉、和肾脏用4%多聚甲醛固定,并进行病理形态学分析,包括EVG、苏木素-伊红(HE)和Masson染色[18]。
-
所有实验数据均以“均值±标准误(mean±SEM)”表示。使用GraphPad Prism 10软件进行统计分析。使用非配对Student-t检验进行组间比较,生存曲线使用Log-rank检验分析。以P<0.05为具有统计学差异。
-
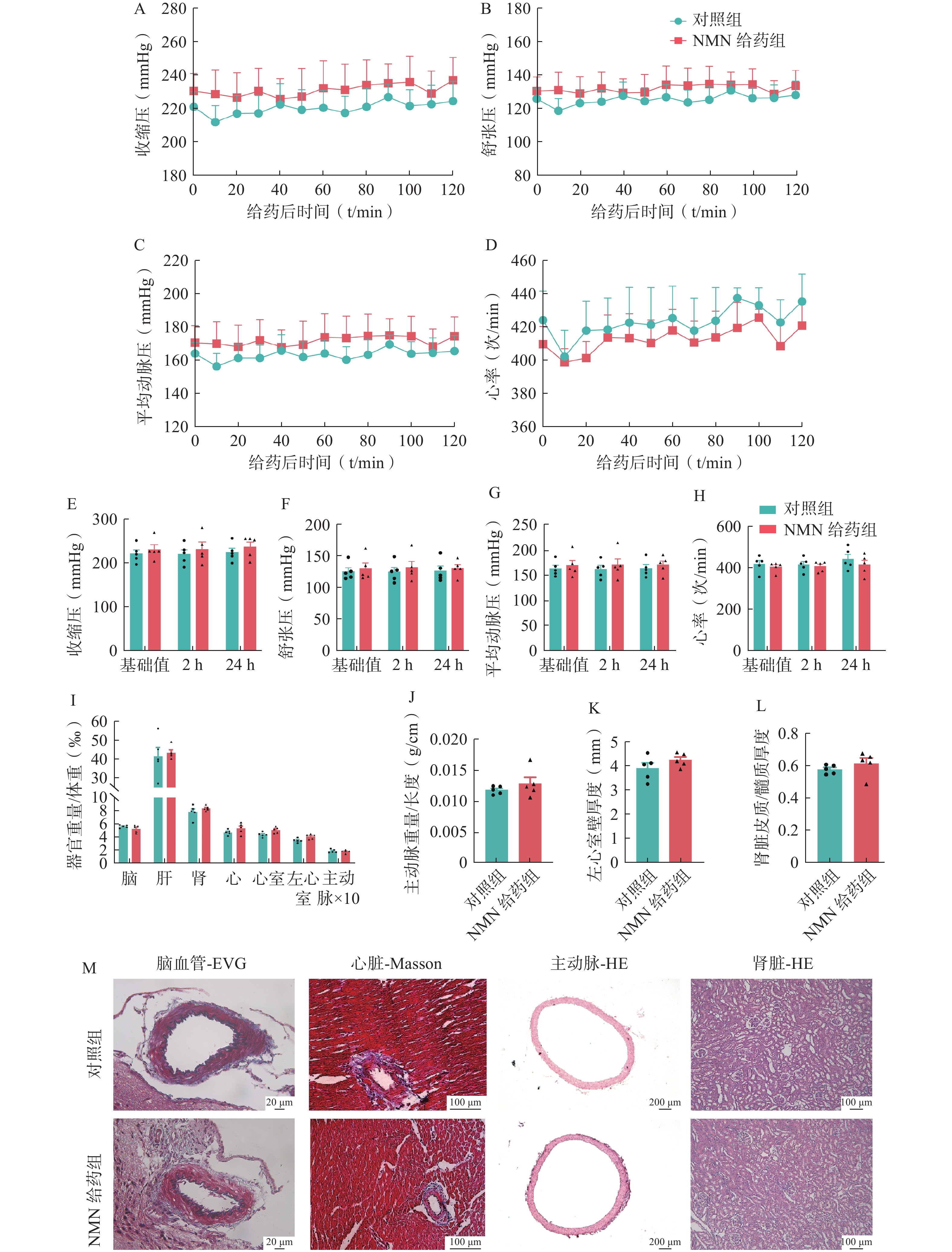
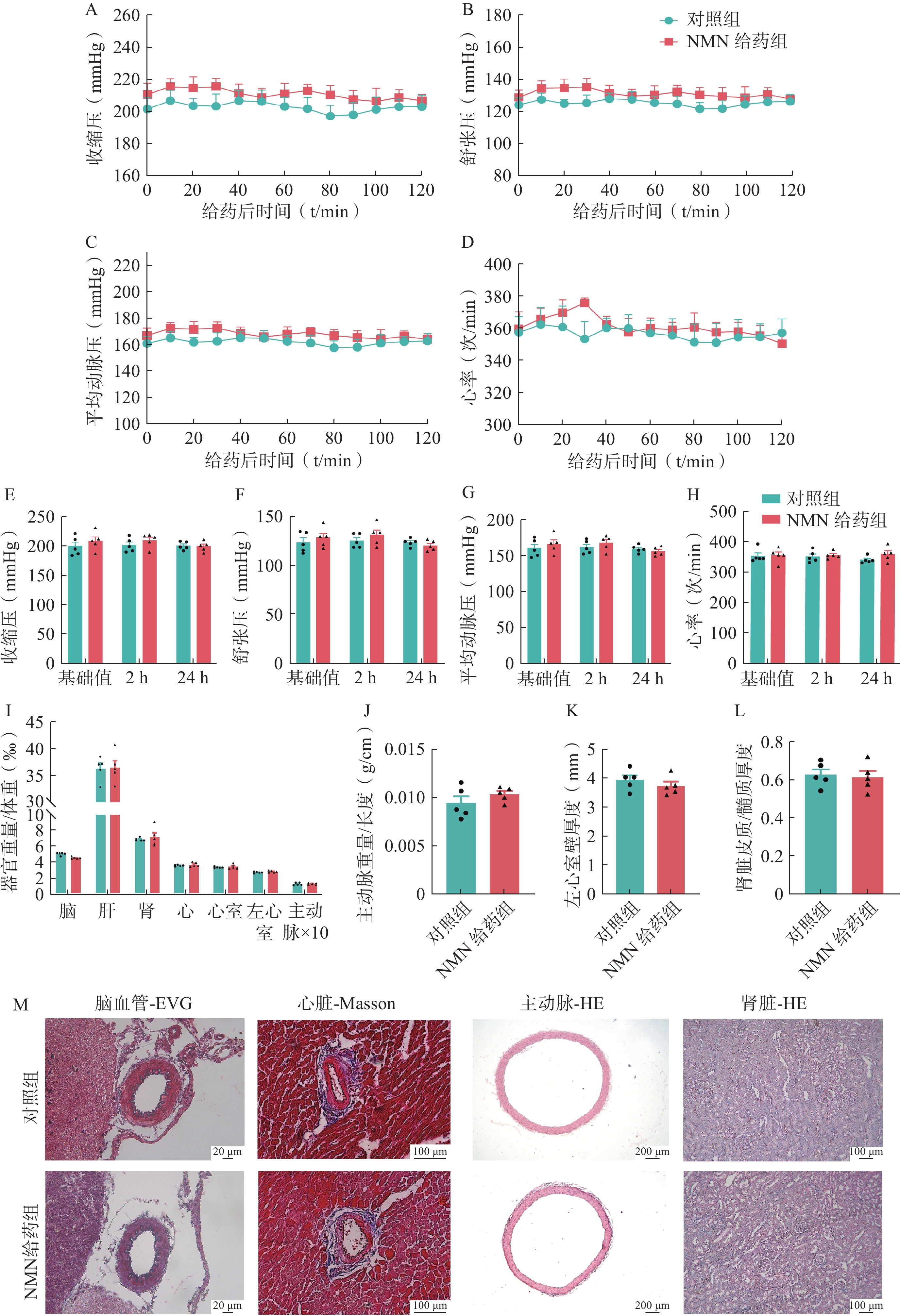
SHR是一种原发性高血压大鼠模型,单次给予200 mg/kg NMN后,2 h内,NMN给药组和溶剂对照组的收缩压、舒张压、平均动脉压或心率没有显著差异(图1:A-D)。对NMN给药后2 h和24 h内的区间血压进行测量分析,两组的收缩压、舒张压、平均动脉压或心率均值也没有显著差异(图1:E-H)。
高血压还可导致心室肥大、主动脉增厚、肾脏皮质萎缩等靶器官损伤。进一步比较两组大鼠的器官损伤程度,与溶剂对照组相比,NMN给药组的脑、肝、肾、心脏、心室、左心室和主动脉的器官相对重量没有显著变化(图1:I)。同时,两组在主动脉重量与长度比、左心室壁厚度和肾皮质与髓质厚度比方面也没有显著差异(图1:J-L)。
对脑血管进行EVG染色,两组大鼠的弹力纤维均清晰、完整,没有发生显著的病理损伤;对心脏进行Masson染色,也没有发现NMN可以改善血管周围的胶原纤维分布;对主动脉和肾脏进行HE染色,同样没有发现NMN减轻主动脉厚度或改善肾小球萎缩等病变(图1:M)。这些结果表明,在SHR模型中,单次给药NMN对血压或器官保护方面没有治疗作用。
-
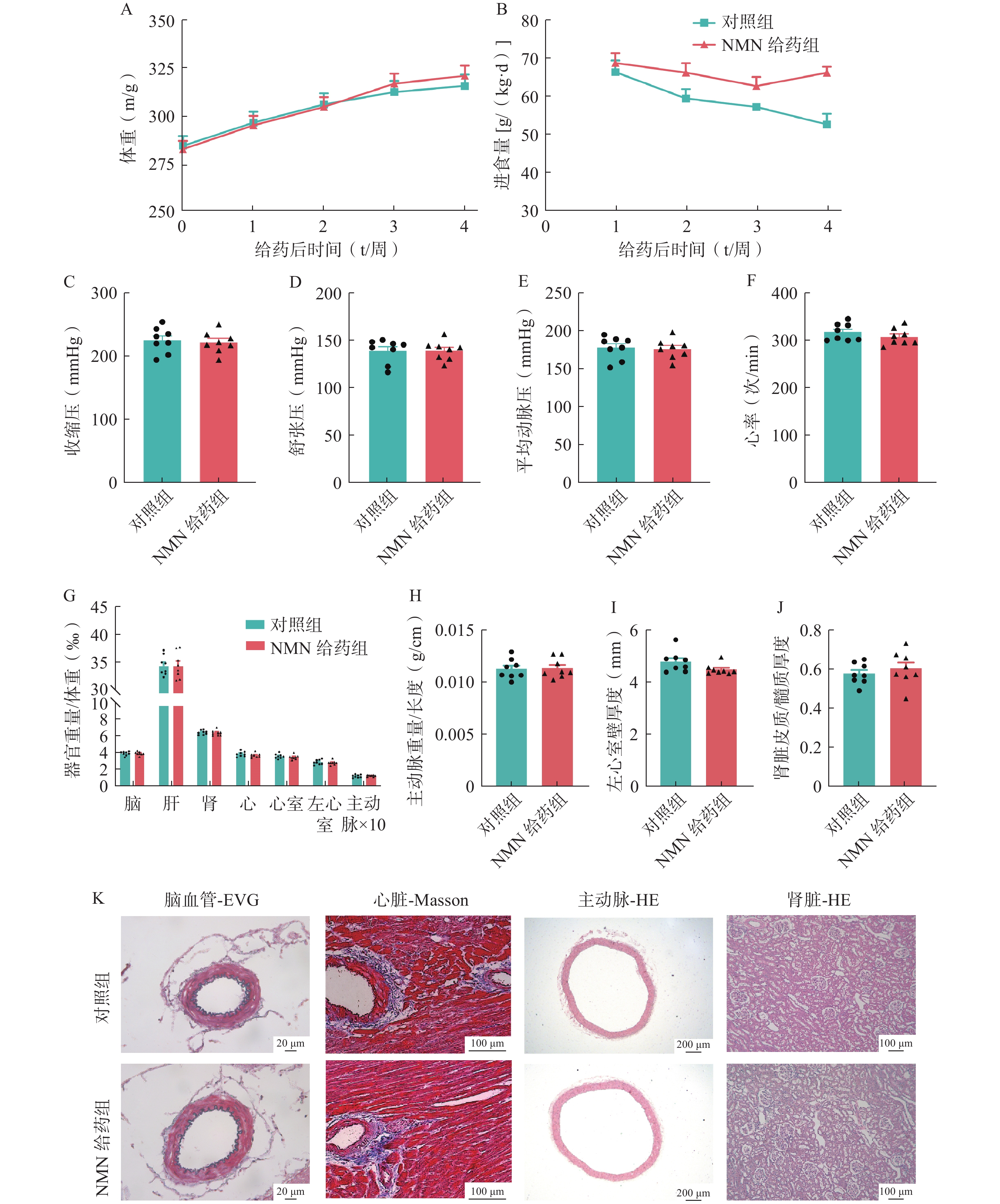
高血压是一种慢性疾病,进一步在SHR模型上长期给予NMN药物饲料喂养4周,等效剂量为200 mg/(kg·d),以评估其对血压和器官损伤的影响。与对照组相比,长期NMN药物饲料治疗组的大鼠体重没有显著变化,但第4周时,NMN给药组大鼠的进食量显著增加(图2:A-B)。NMN药物饲料喂养4周后,对照组和NMN给药组的收缩压、舒张压、平均动脉压或心率均没有显著差异(图2:C-F)。
比较两组大鼠的器官损伤程度,与NMN单次给药治疗的结果相似,NMN药物饲料治疗4周依然没有显著的靶器官保护作用(图2:G-K)。这些结果表明,在SHR模型中,NMN长期给药也没有降低血压或器官保护作用。
-
2K2C大鼠模型是继发性高血压的实验室模型,通过2K2C手术造模后,大鼠血压明显升高[16],进一步研究了在2K2C大鼠模型中单次给药200 mg/kg NMN的治疗效果。与SHR模型中观察到的结果一致,与对照组相比,单次给药NMN后2 h或24 h内对血压和心率没有影响(图3:A-H)。2K2C大鼠单次服用NMN后,脑、心脏、肾脏和主动脉等组织的形态学评估和病理染色也没有显示出任何器官保护作用(图3:I-M)。这些结果表明,在2K2C模型中,单次给药NMN对血压或器官保护方面也没有显著影响。
-
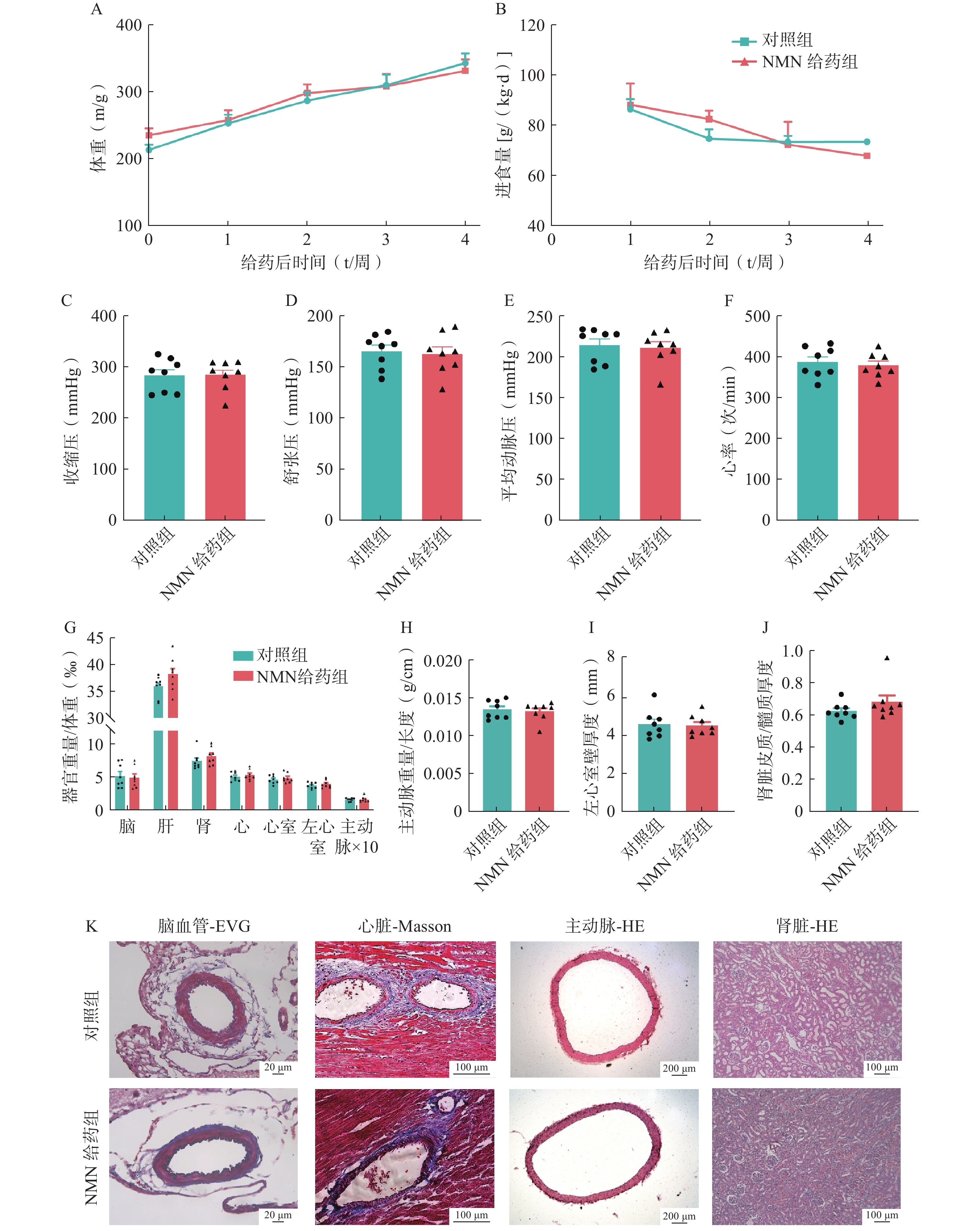
在2K2C模型中长期给予NMN 200 mg/(kg·d),与对照组相比,长期NMN治疗组的体重没有显著变化,尽管第4周的进食量明显减少(图4:A-B)。连续给予NMN 4周后,测量两组大鼠的收缩压、舒张压、平均动脉压或心率,没有观察到显著差异(图4:C-F)。形态学评估,包括脑、肝、肾、心脏、心室、左心室和主动脉的相对器官重量;主动脉重量与长度比;左心室壁厚度、和肾皮质与髓质厚度比;结合EVG、Masson和HE染色,两组之间没有显著差异(图4:G-K)。这些结果表明,在2K2C模型中,长期给药NMN对血压或器官保护也没有显著影响。
-
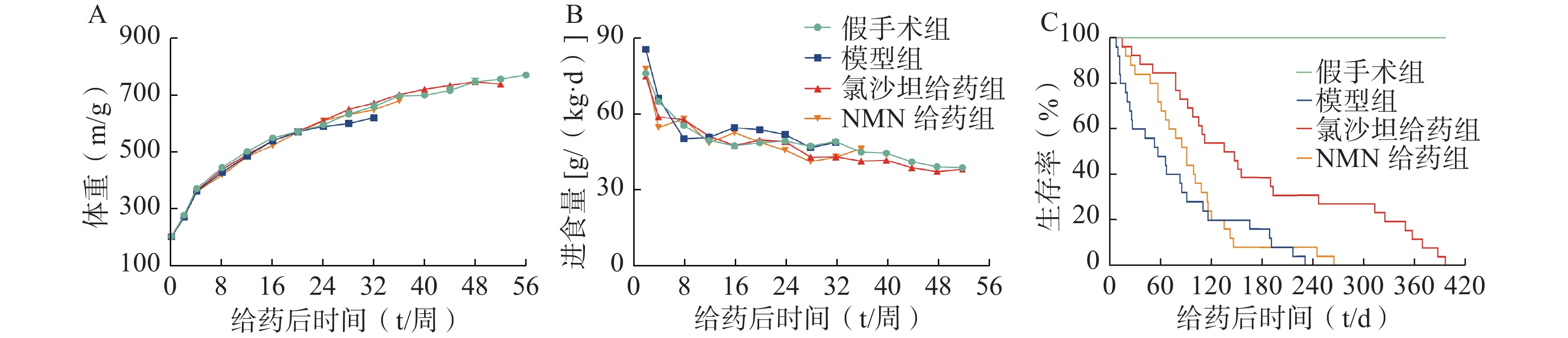
NMN在多种病理生理过程中起着重要作用[10]。进一步考察终身服用NMN是否可以延长2K2C高血压大鼠的存活时间。治疗期间,各组大鼠的体重或进食量没有显著差异(图5:A-B)。与假手术组相比,2K2C模型大鼠的存活时间显著减少,经氯沙坦治疗后,2K2C大鼠的存活时间显著延长。而NMN治疗的2K2C大鼠生存曲线与模型组没有显著差异(图5C)。以上结果表明,在2K2C模型中,NMN没有延长高血压大鼠存活时间的作用。
-
本研究使用两种成熟的高血压大鼠模型:SHR和2K2C大鼠模型,探讨了NMN对高血压的可能影响。研究结果表明,在上述模型中,单次或长期NMN治疗均未显示出显著的抗高血压和保护器官损伤作用,也没有延长生存时间的作用。
高血压对健康存在重大威胁,会导致严重的并发症,如心脏疾病、中风和慢性肾病等。抗高血压治疗在高血压的管理中至关重要。氯沙坦是一种经典的抗高血压药物,能够特异性拮抗血管紧张素II的AT1型受体,并在2K2C和易卒中自发性高血压大鼠(SHR-SP)模型中被证明存在降低血压,减轻器官损伤,延长存活时间的作用[15, 19]。因此,我们选择氯沙坦作为阳性对照药物,它显著延长了高血压大鼠的存活时间。相比之下,NMN并没有延长高血压大鼠的存活时间。此外,在2K2C大鼠和SHR模型中,无论是单次治疗还是长期治疗,NMN对高血压和器官损伤都没有影响。
在最近的一项研究中,在AngⅡ诱导的高血压小鼠模型中证明了NMN有抗高血压和器官保护作用[14]。有几个因素可能导致我们的发现与该团队的发现之间存在差异,如动物模型、给药方案、NMN给药时间和血压测量方法的变化,特别是所用模型之间的差异,SHR和2K2C大鼠模型更广泛地用于评估抗高血压药物的效果。我们使用了与该团队近似的药物剂量进行单次和长期给药来评估NMN药效,但该团队只研究了长期给药。此外,实验动物的血压测量方法可能是观察到结果差异的重要原因。在本研究中,我们采用更为准确的清醒自由活动大鼠血压测定方法,而该团队采用了非侵入性尾套法。总的来说,我们直接评估了NMN对SHR和2K2C大鼠经典高血压模型中高血压和器官损伤的影响,发现NMN对高血压大鼠的血压和器官损伤没有治疗作用。
同时,氯沙坦的降血压作用已多次被我们证实,例如,在2K2C模型上,长期给药氯沙坦4周,收缩压降低约40 mmHg[15],并且氯沙坦的降压作用被国内外广泛证明。因此研究NMN治疗对血压的影响实验中,不设氯沙坦阳性药对照组。而前期我们未证明过氯沙坦对大鼠寿命的影响,因此选择氯沙坦作为阳性对照药物,发现它显著延长了高血压大鼠的存活时间。
关于文中NMN剂量的选择,目前,NMN在各种人群中通常用作营养保健品,剂量范围为50~150 mg/d[20]。小鼠常用NMN剂量为300 mg/kg,对应大鼠剂量约为200 mg/kg,对应人(70 kg)剂量为33 mg/kg;临床试验剂量最大一般设为900 mg/d[21],因此,上述剂量已是较大剂量,若再尝试加大剂量没有实际应用价值,故未设计再高剂量组。
综上,本研究评估了单次和长期NMN治疗对SHR和2K2C大鼠模型中高血压和器官损伤的影响。结果表明,NMN对高血压大鼠的血压、器官损伤和寿命均没有影响,这些发现为NMN的未来临床研究提供了有价值的见解和参考。
The effects of nicotinamide mononucleotide on hypertensive rats
-
摘要:
目的 探讨烟酰胺单核苷酸(NMN)口服给药对高血压大鼠是否具有治疗作用。 方法 采用两种大鼠高血压模型:自发性高血压大鼠(SHR)和双肾双夹(2K2C)易卒中肾血管性高血压大鼠,分别单次、长期或终身给予NMN。通过观察高血压大鼠的血压变化、靶器官损伤程度和生存时间,评估NMN的降血压作用。 结果 NMN没有降低高血压大鼠的血压水平、减轻器官损伤以及延长存活时间的作用。 结论 NMN口服给药对高血压大鼠没有降压作用,为未来NMN的临床研究提供有价值的见解。 Abstract:Objective To exploring the effects of nicotinamide mononucleotide (NMN) on hypertensive rats. Methods Two rat hypertension models including hypertensive rats(SHR)and two-kidney two-clip (2K2C) rats were used to be given single, long-term or lifelong administration of NMN respectively. NMN’s effects were assessed comprehensively by monitoring survival time, blood pressure levels, and the extent of organ damage in hypertensive model rats. Results It was revealed that NMN did not exhibit protective effects in terms of lowering blood pressure levels, reducing organ damage or increasing survival time in hypertensive rats. Conclusion This study suggested that NMN did not demonstrate antihypertensive effects in rat hypertension models and may provide valuable insights for future clinical observation on NMN. -
Key words:
- NMN /
- hypertension /
- rat hypertension models /
- organ damage /
- lifespan
-
抑郁症是一种使人衰弱的精神障碍,其特征是持续情绪低落,对几乎所有活动都失去兴趣或愉悦感,并与疲劳、睡眠障碍、焦虑和神经认知障碍症状有关[1],是全球残疾的第三大原因。抑郁症患者工作低下、具有较高的自杀倾向,严重影响患者的生活,造成沉重的社会经济负担[2]。由于疫情的影响,社会心理健康问题正在急剧增加[3,4]。目前,临床上使用的大多数抗抑郁药都具有耐药性,并伴有各种不良反应。因此,寻找安全性更高、不良反应更少的抑郁症治疗方法具有重要意义。既往研究表明,炎症反应在抑郁症中起着至关重要的作用[5]。抑郁症患者血液及额叶皮层中的促炎细胞因子增加[6,7]。抗炎治疗可以产生抗抑郁作用,而抗抑郁药可以减弱抑郁症中促炎细胞因子的表达[8,9]。因此,抑制神经炎症是治疗抑郁症的重要方向。
百合知母汤是中国东汉张仲景医典《金匮要略》中记载的一种经典中药方剂,用于治疗“百合病”[10]。中医“百合病”被认为与现代抑郁症的表现具有较高的相似性[11]。目前,百合知母汤在中医临床上被广泛用于治疗抑郁症[12]。药理学研究表明,百合知母汤在动物模型中具有显著的抗抑郁作用[13]。然而,百合知母汤治疗抑郁症的作用机制并未完全明了。前期研究发现百合知母汤能够通过抑制CUMS抑郁模型小鼠的神经炎症,降低海马IL-1β、 IL-6和TNF-α等促炎细胞因子的表达,来发挥抗抑郁作用[14]。鉴于NLRP1炎症小体在炎症反应过程中的重要的作用[15],且最近研究发现NLRP1炎症小体在抑郁症的发展过程中扮演重用角色[16]。该研究基于NLRP1炎症小体的活化,对百合知母汤的抗抑郁作用进行进一步的探索。
1. 材料和方法
1.1 百合知母汤的制备
取百合药材400 g、知母药材200 g,浸泡0.5 h后,加10倍量水,煎煮两次,每次2 h,煎液过滤后,将两次滤液混合并浓缩至600 ml。
1.2 实验试剂
Muramyl dipeptide(MDP)购自Sigma-Aldrich公司;IL-1β、IL-6、TNF-α、5-HT、NE、DA试剂盒和ELISA试剂盒均购自美国R&D公司;BSA购自美国Sigma-Aldric公司;去离子水采用Milli-Q纯水机制备(Millipore公司);NLRP1、ASC、caspase-1、BDNF、TrkB、ERK、AKT、mTOR、β-actin等抗体均购自 Cell Signaling公司; BCA蛋白测定试剂盒与RIPA裂解液购自碧云天公司。
1.3 实验动物
雄性C57BL/6J小鼠8周龄,体质量22 g~25 g,购自浙江维通利华实验动物技术有限公司,生产许可证: SCXK(浙)[2019-0001]。所有小鼠均在标准条件下饲养(12 h光/暗循环,温度:22 ℃~24 ℃,湿度:55%±10%),在整个实验过程小鼠自由摄取食物和水。实验前对所有小鼠进行适应性喂养1周。该研究经上海交通大学医学院附属仁济医院伦理委员会审批通过,实验操作严格按照动物福利和伦理原则进行。
1.4 CUMS模型建立
CUMS造模过程参考前期研究,通过给予小鼠不同刺激构建抑郁症模型小鼠,主要过程如下:①禁食24 h;②禁水 24 h;③空瓶刺激 1 h;④昼夜照明 24 h;⑤笼子倾斜45◦ ,24 h;⑥潮湿垫料24 h;⑦摇笼30 min;⑧夹尾1 min;⑨冰水游泳5 min。小鼠每天接受不同的应激,持续5周。
1.5 动物分组及给药
根据前期研究[14],百合知母汤给药采用6 g生药量/kg(相当于百合4 g,知母2 g)和12 g生药量/kg(相当于百合8 g,知母4 g)两个剂量。将30只雄性C57BL/6J小鼠随机分为5组(n=6):对照组、模型组、百合知母汤低剂量组(百合知母汤,6 g/kg,i.g.)、百合知母汤高剂量组(百合知母汤,12 g/kg,i.g.)、百合知母汤+MDP组(百合知母汤,12 g/kg,i.g.;MDP,脑立体定位注射)。除对照组外,各组小鼠接受CUMS刺激,持续5周,对照组被放置在不受干扰的笼子里。从第6周开始,给药组按剂量通过灌胃给予百合知母汤浓缩液,1次/d,持续4周。模型组小鼠给予等量的蒸馏水。为考察NLRP1在百合知母汤抗抑郁过程中的重要作用,设立百合知母汤+MDP组,给药前接受脑立体定位注射NLRP1激活剂MDP,过程如下:经异氟烷麻醉的小鼠俯卧位固定于脑立体定位仪上,将眼中线靠后 2~3 cm 处用 75% 乙醇消毒、剪皮露出头骨,用注射器针头将头骨表层骨膜轻挑剥离,前后囟在同一水平,暴露前囟(冠状缝)。选择小鼠双侧海马CA1 区为注射位置,进针 1.6 mm 至海马区,注射MDP,剂量5 mg/kg,结束后使用可吸收缝合线进行无菌缝合。
1.6 行为学考察
1.6.1 蔗糖偏好实验
每只小鼠置于单独的笼子里孤养,放置2瓶含有1%蔗糖溶液,进行24 h的适应。然后其中一瓶蔗糖溶液用蒸馏水代替,进行另一次24 h的适应。随后禁水、禁食 24 h。最后,放置2个预先称重的含有1%蔗糖溶液或蒸馏水的瓶子。3 h后,记录蔗糖溶液消耗量和水消耗量,计算蔗糖偏好指数。
1.6.2 悬尾实验
用胶带固定每只小鼠的尾部,头部向下,离台面50 cm。在实验过程中,将小鼠隔开以避免互相干扰。记录6 min内小鼠的累计不动时间。
1.6.3 强迫游泳实验
在室温下,将每只小鼠分别放入直径12 cm的塑料桶中,桶中装满25 cm深的水。在正式实验前24 h,进行15 min的预游泳适应训练。记录5 min内小鼠的累计漂浮不动时间。
1.6.4 旷场实验
将小鼠单独放置在敞箱装置中,给予6 min的自由探索时间,使其适应,然后记录其4 min内穿越的格子数。
1.7 神经递质和炎症因子水平的测定
各组小鼠用10%(w/v)水合氯醛深度麻醉。迅速取脑,置于冰上。分离海马,液氮预冷冻,于−80 ℃下储存,分析用。检测时,取海马,加入磷酸盐缓冲液(PBS:137 nmol/L NaCl、2.7 nmol/L KCl、10 nmol/L Na2HPO4、1.8 nmol/L KH2PO4),于冰上匀浆,4 ℃下以
12000 r/min,离心10 min,收集上清液。使用ELISA试剂盒检测小鼠海马中的炎症因子水平。IL-1β、IL-6、TNF-α、5-HT、NE 和DA的水平,操作均按照说明书进行。1.8 免疫荧光染色
迅速取小鼠大脑放置冰上,分离海马,用液氮预冷冻,并在−80 ℃下储存。使用冷冻切片机将海马组织切成5 μm的切片。切片用PBS缓冲液洗涤2次。然后用含0.5% Triton X-100的PBS 缓冲液透化,并用0.5% BSA固定,加入一抗,4℃,孵育过夜。加入荧光素标记的二抗孵育(室温,1 h)。通过荧光显微镜对切片成像。
1.9 Western blot法检测蛋白的表达水平
取小鼠海马组织,加入含1%蛋白酶抑制剂的RIPA裂解液,于冰上研磨,在4℃下,
12000 r/min,离心10 min。收集上清液,用BCA蛋白浓度测定试剂盒测定蛋白浓度后,用10%十二烷基硫酸钠/聚丙烯酰胺凝胶电泳(SDS-PAGE)分离总蛋白,分离后转移到聚偏氟乙烯(PVDF)膜上,用5%牛血清白蛋白(BSA)在室温下封闭2 h,随后孵上一抗,4 ℃,孵育过夜。过夜后用TBST洗涤3次,每次洗涤10 min。然后与辣根过氧化物酶标记的二抗孵育1 h,TBST洗涤3次,每次10 min。最后使用ECL显影液进行显影。1.10 统计分析
使用GraphPad Prism 8.0(GraphPad Software,USA)进行统计分析。数据以平均值±标准差(SD)表示。使用单向方差分析和Tukey HSD检验评估各组之间的差异。P<0.05的显著性水平被认为是统计学显著性的指示。
2. 结果
2.1 百合知母汤对CUMS小鼠行为学影响
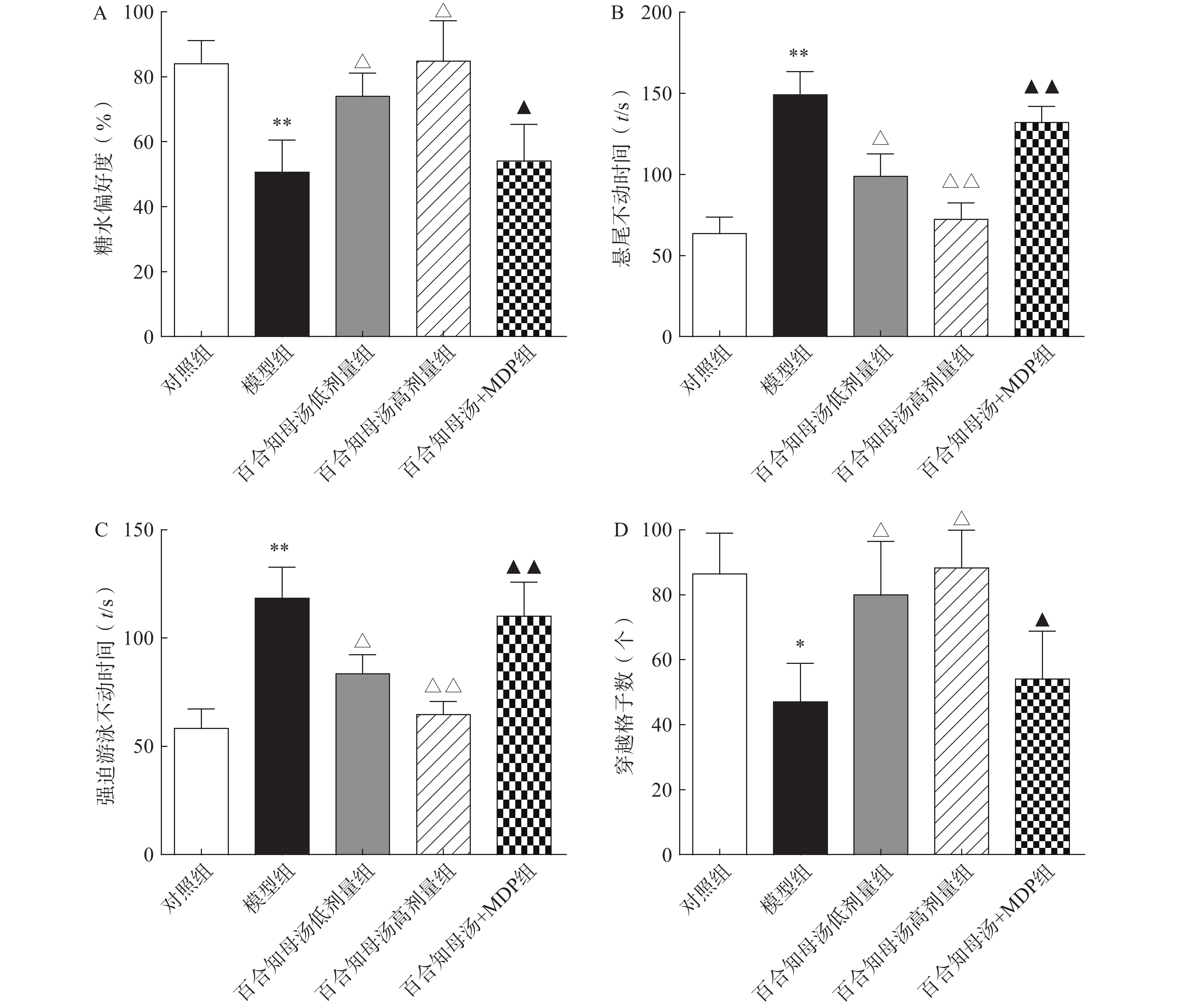
为了评估百合知母汤的药理作用,首先进行糖水消耗实验、悬尾实验、强迫游泳实验和旷场实验,观察百合知母汤对CUMS小鼠行为学的影响。如图1所示,与对照组相比,CUMS模型组在糖水消耗实验中的蔗糖消耗百分比和旷场实验中的格子穿越数显著减少(P<0.01,P<0.05),而悬尾实验和强迫游泳实验的不动时间显著增加(P<0.01)。而百合知母汤能显著提高这些参数(P<0.05,P<0.01),并呈明显的剂量依赖性。表明百合知母汤能改善抑郁小鼠的行为学特征。值得注意的是,NLRP1炎症小体激活剂MDP能够显著的逆转百合知母汤对抑郁症小鼠行为学的作用(P<0.05,P<0.01),提示百合知母汤通过抑制NLRP1炎症小体活化来发挥抗抑郁作用。
2.2 百合知母汤对CUMS小鼠神经递质变化的影响
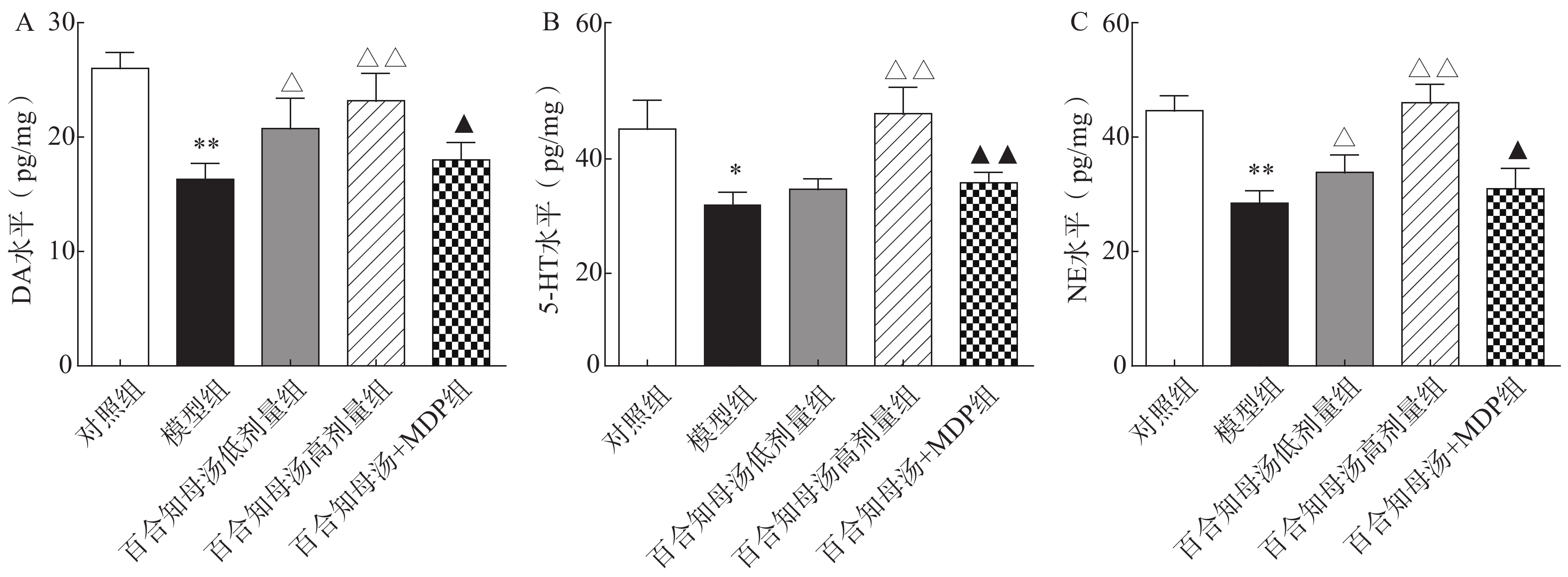
中枢神经系统单胺类神经递质水平降低与抑郁症的产生具有密切关系。图2结果表明,CUMS模型组的DA、5-HT、NE水平与对照组相比显著降低(P<0.05,P<0.01),而CUMS+BZD6组和CUMS+BZD12组上述神经递质的含量明显高于模型组(P<0.05,P<0.01)。NLRP1激活能够显著的逆转百合知母汤对上述神经递质的影响(P<0.05,P<0.01)。
2.3 百合知母汤对抑郁症相关炎症因子的影响
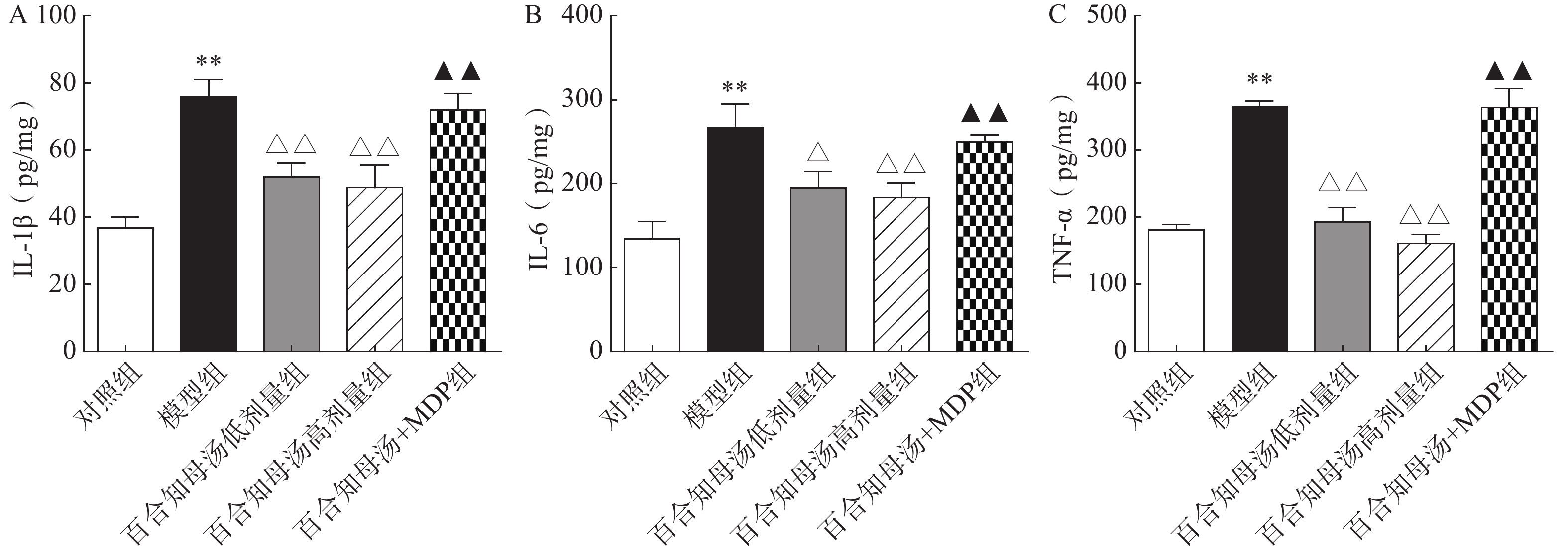
越来越多的研究表明炎症在抑郁症的病因中起着关键作用。因此,用ELISA法测定了几种关键的促炎细胞因子。如图3所示,与对照组相比,CUMS模型组小鼠海马中的IL-1β、IL-6和TNF-α水平显著升高(P<0.01),而百合知母汤显著抑制了由CUMS引起的这些炎症因子的升高(P<0.05,P<0.01),NLRP1激活剂MDP能够显著的逆转百合知母汤对上述神经递质的影响(P<0.01)。
2.4 百合知母汤对小鼠海马NLRP1炎症小体的影响
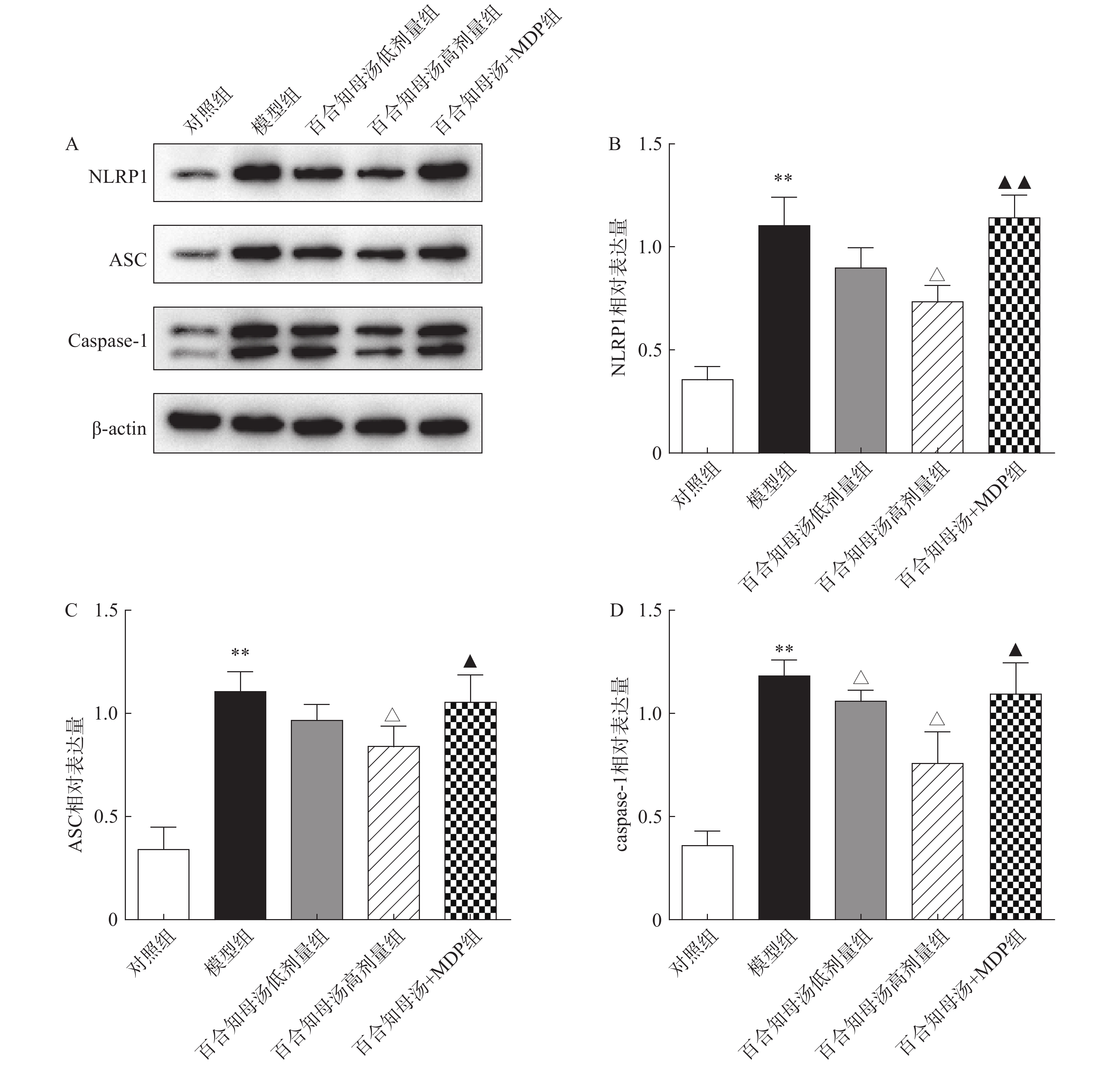
NLRP1炎症小体在神经炎症相关疾病中扮演重用角色,NLRP1炎症小体的活化能促进各种炎症因子的产生[17]。因此,采用Western blot检测NLRP1炎症小体的活化。图4结果显示,CUSM刺激显著增加了NLRP1、ASC和caspase-1的蛋白表达(P<0.01),表明NLRP1炎症小体在CUSM抑郁模型中被激活。而百合知母汤显著抑制了由CUMS引起NLRP1、ASC和caspase-1表达升高(P<0.05)。表明百合知母汤能抑制NLRP1炎症小体的激活。值得注意的是,NLRP1激活剂MDP能够显著逆转百合知母汤对上述蛋白表达的抑制作用(P<0.05,P<0.01),进一步表明百合知母汤通过抑制NLRP1炎症小体活化来发挥抗神经炎症的作用。
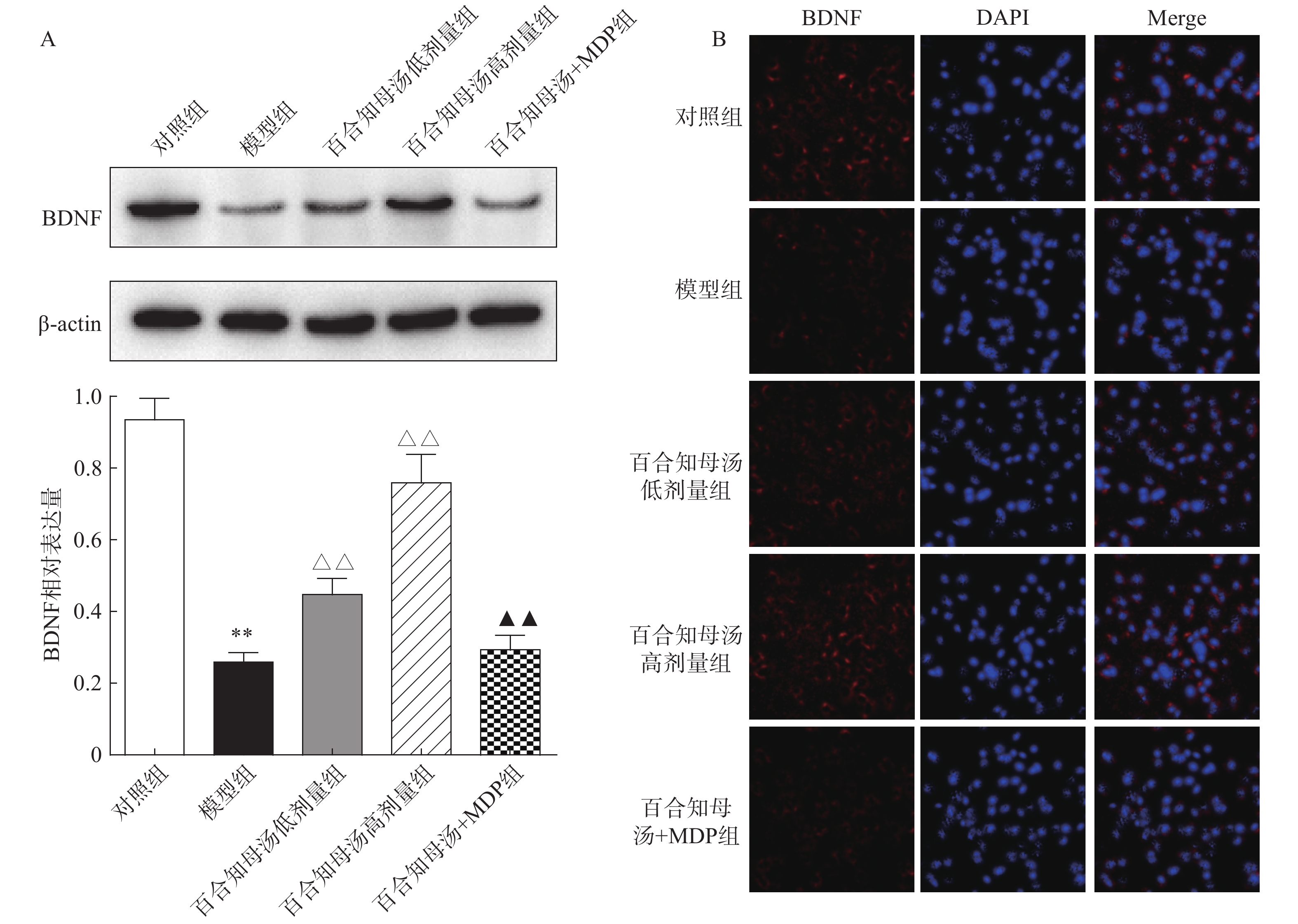
2.5 百合知母汤对小鼠海马BDNF表达的影响
由于BDNF与抑郁症的发生发展密切相关[18],通过Western blot检测BDNF在不同组小鼠海马中的表达(图5A)。与对照组相比,CUMS模型组小鼠海马表达BDNF水平显著降低(P<0.01),而百合知母汤以量效依赖方式显著上调BDNF表达水平(P<0.01)。MDP能够显著阻断百合知母汤对BDNF表达水平的作用(P<0.01)。
随后,用免疫荧光对小鼠海马的BDNF表达进行检测(图5B)。结果发现,与对照组相比,CUMS模型组小鼠海马表达BDNF水平显著降低,而百合知母汤治疗组BDNF表达水平显著上调。NLRP1激活剂MDP能够显著的逆转百合知母汤对BDNF表达水平表达的上调作用。
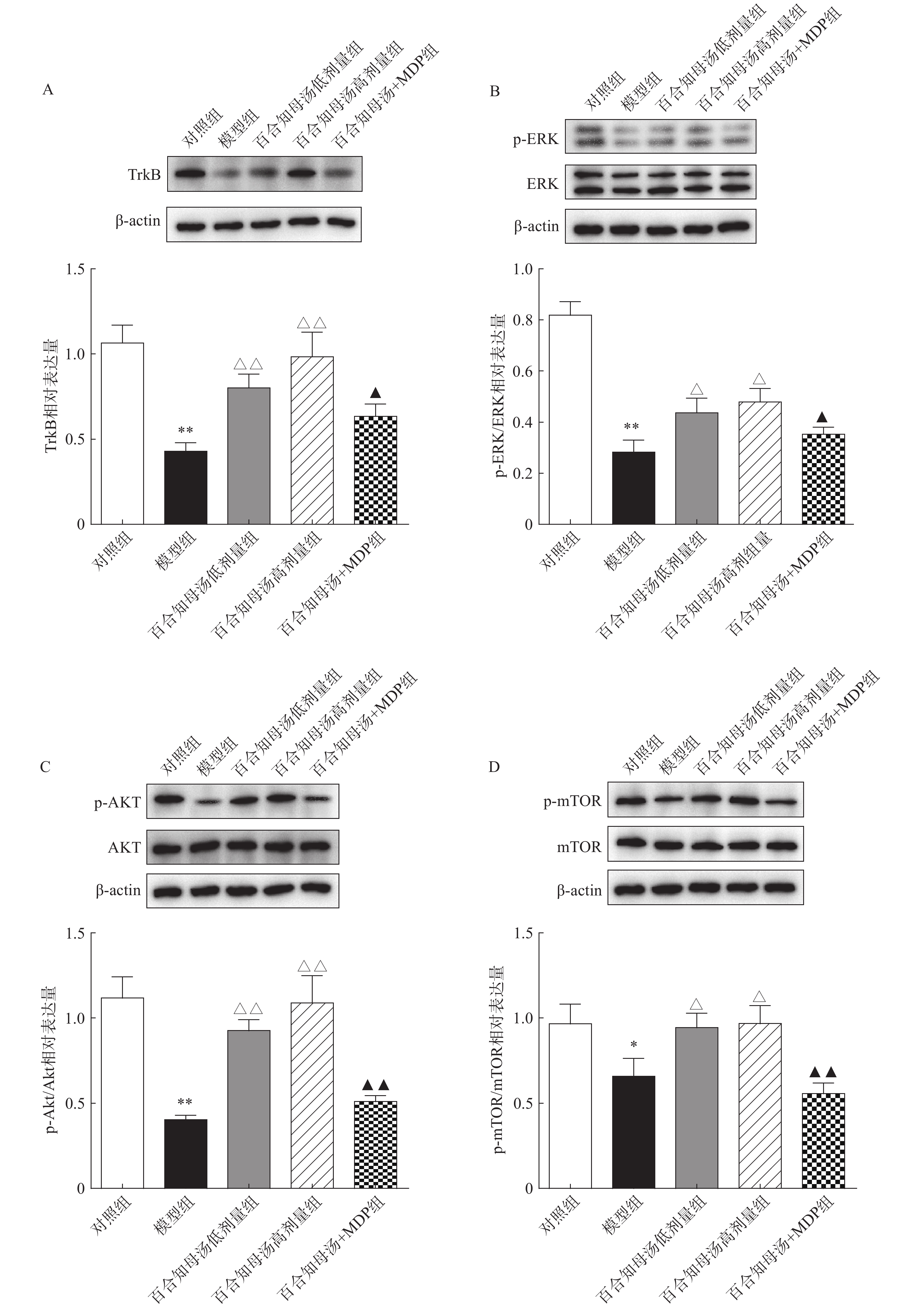
2.6 百合知母汤对小鼠海马TrkB和下游ERK/AKT/mTOR通路相关蛋白表达的影响
BDNF能够与TrkB结合,从而激活AKT/mTOR级联反应,最终通过调节突触蛋白合成和细胞骨架发育来增强树突的复杂性[19]。因此,继续探讨百合知母汤对TrkB及下游ERK/AKT/mTOR通路关键蛋白表达的影响。百合知母汤对小鼠海马TrkB表达的影响如图6A所示。与对照组相比CUMS模型组小鼠海马TrkB的表达显著降低(P<0.01),百合知母汤给药组小鼠海马TrkB的表达水平显著升高(P<0.01)。而MDP能够逆转百合知母汤对TrkB表达水平的上调作用(P<0.05)。
如图6B-D所示,与对照组相比,CUMS组小鼠海马ERK、AKT和mTOR的磷酸化水平显著降低,而百合知母汤给药可显著促进抑郁小鼠ERK、AKT和mTOR的磷酸化水平(P<0.05,P<0.01)。NLRP1激活剂MDP能够显著的逆转百合知母汤对上述蛋白磷酸化水平的促进作用(P<0.05,P<0.01)。
3. 讨论
神经炎症是一种对组织损伤的先天免疫反应,在许多中枢神经系统疾病中发挥着重要作用,被认为与抑郁症的发生发展息息相关[20, 21]。大量证据表明,海马体的神经炎症对抑郁和焦虑障碍的发展至关重要。神经性疼痛诱导的抑郁样行为的发作与海马TNF及其受体TNFR1水平的增加相关[22]。敲减海马中IL-1β可以减轻LPS诱导的小鼠焦虑和抑郁样行为[23]。而给予IL-1受体拮抗剂可以改善神经性疼痛对抑郁样行为的影响[24]。以上研究结果表明,海马神经炎症在抑郁症的病理过程中起着重要作用。
炎症小体是先天免疫反应的关键成分,据报道与炎症相关神经系统疾病的机制有关[25]。NLRP1炎症小体由受体蛋白NLRP1、衔接蛋白ASC和效应蛋白caspase-1组成,在神经炎症相关疾病中起重要作用。NLRP1可被多种刺激激活,包括炭疽杆菌致死毒素、弓形虫、胞壁酰二肽、宿主细胞内ATP耗竭等[21]。NLRP1炎症小体的激活导致Caspase-1的直接成熟,随后诱导促炎细胞因子(如IL-1β和IL-18)的产生,从而触发神经炎症反应[26]。据报道,NLRP1炎症小体驱动的炎症途径与许多神经系统疾病有关,如脑损伤、神经退行性疾病、伤害感受和癫痫[27]。
百合知母汤抗抑郁作用及其机制既往已有研究[13,14],然而基于NLRP1炎症小体的活化对其抗抑郁机制的研究未见报道。该研究旨在通过探讨百合知母汤对NLRP1炎症小体的活化作用来阐释百合知母汤抗抑郁的作用机制。结果显示,百合知母汤抑制了CUMS抑郁症小鼠海马NLRP1、ASC和Caspase-1的表达升高。表明百合知母汤能够抑制NLRP1炎症小体的活化。为了证实百合知母汤通过NLRP1/Caspase-1通路发挥抗抑郁作用,采用NLRP1激活剂MDP注射抑郁症小鼠。结果发现,MDP逆转了百合知母汤对CUMS小鼠的抑郁样行为和神经炎症的改善作用。因此,百合知母汤可能通过抑制NLRP1炎症小体的活化,以调节抑郁症小鼠的神经炎症反应,来发挥抗抑郁作用。
BDNF属于神经营养因子家族,在神经的生成、发展和功能维持中起着至关重要的作用[28]。大量研究表明,BDNF与抑郁症的病理生理学和抗抑郁疗效有关[29]。研究发现,抑郁症动物和患者以及抑郁症受试者的尸检样本中,大脑BDNF水平降低[28, 30]。此外,给予LPS或促炎细胞因子可显著降低海马和大脑皮层的BDNF水平[31]。这表明炎症会影响BDNF的表达。抗抑郁药物治疗可以有效改善抑郁症引起的BDNF含量的降低,进一步促进神经发生,增强神经可塑性,并起到抗抑郁的作用[32]。研究发现,BDNF的释放以及与TrkB的结合能够触发多种下游信号级联,包括RAS/MAPK通路和PI3K/AKT通路,这些信号通路与抑郁症的发生发展密切相关[33]。慢性应激可抑制ERK信号的传递,抗抑郁治疗则可逆转这种抑制[34],表明ERK信号阻断会导致抑郁和焦虑行为。这与抑郁症患者的尸检报告一致[35]。此外,慢性应激还会导致内侧前额叶皮层锥体神经元的树突形态发生变化,具体表现为树突回缩和树突棘丢失[36]。而抗抑郁治疗可以通过AKT/mTOR途径逆转这一现象,并有效改善小鼠的抑郁样症状[37]。上述研究表明,BDNF与TrkB结合,进而通过ERK和AKT/mTOR信号通路引发的信号级联反应可能是抗抑郁药物发挥治疗作用的关键分子机制。本研究结果显示,百合知母汤能显著促进抑郁症小鼠海马BDNF和TrkB的表达水平,表明百合知母汤能上调BDNF/TrkB信号通路。同时,百合知母汤能显著促进RK、AKT和mTOR的磷酸化水平。表明百合知母汤能同时激活下游的ERK/AKT/mTOR信号通路。而采用NLRP1激活剂MDP活化NLRP1炎症小体后,百合知母汤对BDNF/TrkB信号通路和ERK/AKT/mTOR信号通路上调作用被显著逆转,表明百合知母汤通过抑制NLRP1炎症小体活化,激活BDNF/TrkB信号通路和ERK/AKT/mTOR信号通路。
综上所述,百合知母汤通过抑制NLRP1炎症小体活化,抑制CUMS抑郁症小鼠海马的神经炎症反应,进而激活BDNF/TrkB信号通路和ERK/AKT/mTOR信号通路来改善CUMS小鼠的抑郁样行为。
-
-
[1] COVARRUBIAS A J, PERRONE R, GROZIO A, et al. NAD+ metabolism and its roles in cellular processes during ageing[J]. Nat Rev Mol Cell Biol, 2021, 22(2):119-141. doi: 10.1038/s41580-020-00313-x [2] WANG P, MIAO C Y. NAMPT as a therapeutic target against stroke[J]. Trends Pharmacol Sci, 2015, 36(12):891-905. doi: 10.1016/j.tips.2015.08.012 [3] YOSHINO J, BAUR J A, IMAI S I. NAD+ intermediates: the biology and therapeutic potential of NMN and NR[J]. Cell Metab, 2018, 27(3):513-528. doi: 10.1016/j.cmet.2017.11.002 [4] YOSHINO J, MILLS K F, YOON M J, et al. Nicotinamide mononucleotide, a key NAD(+)intermediate, treats the pathophysiology of diet- and age-induced diabetes in mice[J]. Cell Metab, 2011, 14(4):528-536. doi: 10.1016/j.cmet.2011.08.014 [5] WANG S N, MIAO C Y. Targeting NAMPT as a therapeutic strategy against stroke[J]. Stroke Vasc Neurol, 2019, 4(2):83-89. doi: 10.1136/svn-2018-000199 [6] YAGI M, DO Y, HIRAI H, et al. Improving lysosomal ferroptosis with NMN administration protects against heart failure[J]. Life Sci Alliance, 2023, 6(12):e202302116. doi: 10.26508/lsa.202302116 [7] DENG H Y, DING D, MA Y, et al. Nicotinamide mononucleotide: research process in cardiovascular diseases[J]. Int J Mol Sci, 2024, 25(17):9526. doi: 10.3390/ijms25179526 [8] SONG Q, ZHOU X F, XU K X, et al. The safety and antiaging effects of nicotinamide mononucleotide in human clinical trials: an update[J]. Adv Nutr, 2023, 14(6):1416-1435. doi: 10.1016/j.advnut.2023.08.008 [9] HUANG H. A multicentre, randomised, double blind, parallel design, placebo controlled study to evaluate the efficacy and safety of uthever(NMN supplement), an orally administered supplementation in middle aged and older adults[J]. Front Aging, 2022, 3:851698. doi: 10.3389/fragi.2022.851698 [10] YI L, MAIER A B, TAO R S, et al. The efficacy and safety of β-nicotinamide mononucleotide(NMN)supplementation in healthy middle-aged adults: a randomized, multicenter, double-blind, placebo-controlled, parallel-group, dose-dependent clinical trial[J]. Geroscience, 2023, 45(1):29-43. doi: 10.1007/s11357-022-00705-1 [11] IGARASHI M, NAKAGAWA-NAGAHAMA Y, MIURA M, et al. Chronic nicotinamide mononucleotide supplementation elevates blood nicotinamide adenine dinucleotide levels and alters muscle function in healthy older men[J]. NPJ Aging, 2022, 8(1):5. [12] XU T Y, WANG P, TIAN J S, et al. Pharmacological characterization of MT-1207, a novel multitarget antihypertensive agent[J]. Acta Pharmacol Sin, 2021, 42(6):885-897. doi: 10.1038/s41401-021-00636-1 [13] RAPSOMANIKI E, TIMMIS A, GEORGE J, et al. Blood pressure and incidence of twelve cardiovascular diseases: lifetime risks, healthy life-years lost, and age-specific associations in 1·25 million people[J]. Lancet, 2014, 383(9932):1899-1911. doi: 10.1016/S0140-6736(14)60685-1 [14] QIU Y M, XU S Y, CHEN X, et al. NAD+ exhaustion by CD38 upregulation contributes to blood pressure elevation and vascular damage in hypertension[J]. Signal Transduct Target Ther, 2023, 8(1):353. doi: 10.1038/s41392-023-01577-3 [15] TIAN J S, WEI Y C, WANG P, et al. Pharmacological effects of MT-1207 in bilateral renal artery stenosis hypertension and its hypotensive targets validation[J]. Biomed Pharmacother, 2024, 178:117234. doi: 10.1016/j.biopha.2024.117234 [16] LING Q S, ZHANG S L, TIAN J S, et al. Allisartan isoproxil reduces mortality of stroke-prone rats and protects against cerebrovascular, cardiac, and aortic damage[J]. Acta Pharmacol Sin, 2021, 42(6):871-884. doi: 10.1038/s41401-021-00684-7 [17] WU M Y, MA X J, YANG C, et al. Effects of allisartan, a new AT(1)receptor blocker, on blood pressure and end-organ damage in hypertensive animals[J]. Acta Pharmacol Sin, 2009, 30(3):307-313. doi: 10.1038/aps.2009.11 [18] OTALI D, FREDENBURGH J, OELSCHLAGER D K, et al. A standard tissue as a control for histochemical and immunohistochemical staining[J]. Biotech Histochem, 2016, 91(5):309-326. doi: 10.1080/10520295.2016.1179342 [19] SHIMAMURA T, IWASAKI T, HAYASAKI-KAJIWARA Y, et al. Effects of losartan and benazepril on abnormal circadian blood pressure rhythm and target organ damage in SHRSP[J]. Clin Exp Hypertens, 2002, 24(3):187-205. doi: 10.1081/CEH-120003200 [20] SOMA M, LALM S K. The role of nicotinamide mononucleotide (NMN) in anti-aging, longevity, and its potential for treating chronic conditions[J]. Molecular Biology Reports, 2022, 49(10):9737-9748. doi: 10.1007/s11033-022-07459-1 [21] Yi L, Maier A B, Tao R, et al. The efficacy and safety of β-nicotinamide mononucleotide (NMN) supplementation in healthy middle-aged adults: A randomized, multicenter, double-blind, placebo-controlled, parallel-group, dose-dependent clinical trial[J]. Geroscience, 2023, 45(1):29-43. doi: 10.1007/s11357-022-00705-1 -





 下载:
下载:
 下载:
下载: