-
人体表面及内部生活着数量巨大、种类多样的微生物,其中绝大部分是由细菌菌群组成的。肠道微生物和中枢神经系统之间存在相互作用,肠道微生物的异常可以通过“菌-肠-脑”轴参与到机体认知和社会行为等的复杂调控中,且已有多项研究发现肠道菌失调与抑郁症的发生密切相关[1],会通过多种不同的方式和途径加速或诱导抑郁症的发生。口服药物治疗是目前常用的方式,可在一定程度上减缓病人症状,但是目前部分抗抑郁药物仍具有一定的局限性[2]。现已有研究发现,益生菌可以通过多重机制来控制抑郁样行为[3],这为我们探索抗抑郁药物的研发提供了一个新的方向。本综述将从抑郁症、肠道菌代谢产物、作用分子水平出发探讨抑郁症的机制,在对现有益生菌生物制剂治疗抑郁症的研究发现的基础上,对肠道菌这一新靶点进行展望,为寻找抗抑郁药物研发的方向提供帮助。
-
目前抑郁症确切的病理生理机制仍不清楚,多集中在单胺神经递质紊乱、肾上腺轴功能障碍、缺乏神经营养因子和促炎细胞因子过度等方面,随着肠道菌在抑郁症中的调控机制逐渐被揭示,肠道菌对相关致抑郁小分子的作用也逐渐被证实。
-
据报道,细胞炎性因子在正常大脑以及大脑发育过程中十分重要,促炎因子可以直接或通过强效激活下丘脑-垂体-肾上腺轴(HPA轴)来诱导或加速抑郁症的发病[4]。HPA轴功能异常是抑郁病理生理机制的重要组成部分之一。目前有关抑郁症发病机制中作用的促炎性细胞因子有TNF-α、IL-1和IL-6 等,另外新的分子和机制也逐渐被发现。动物研究发现,动物在注入促炎性细胞因子后出现了一系列与抑郁症表现非常相似的行为学变化[5]。
-
脑源性神经营养因子假说是抑郁症发病机制假说之一, BDNF是神经生长的重要调节因子, 当BDNF水平受到影响减少时会对抑郁症的发生起到促进作用[6],有研究表明BDNF可以参与神经突触可塑性调控,与情绪障碍有很大的联系。
-
神经递质是神经细胞交流的信使, 在个体心理和行为中发挥着重要作用, 抑郁症与神经递质异常有直接关系[7]。抑郁症假说之一表明抑郁是由于脑内单胺类神经递质缺乏引起的,另外有研究发现,其他的神经递质也有可能对抑郁症产生影响[8]。
-
HPA轴是指下丘脑-垂体-肾上腺轴,糖皮质激素就是这条轴上的介质之一。研究发现糖皮质激素对维持机体正常生理状态十分重要,参与中枢神经系统的调节,可对抑郁的产生起到重要影响[9]。HPA轴的异常是导致神经行为异常的原因之一。
-
某些针对抑郁患者或抑郁大鼠的研究发现,正常与抑郁状态下其肠道菌群的丰度存在显著差异,即抑郁状态会导致肠道菌丰度的改变[10-15],大多导致拟杆菌门丰度增高而厚壁菌门丰度降低[10-13]。反之,肠道菌的紊乱对抑郁症的发生起到诱导或加速作用这一点也在多项研究中得到肯定[16]。
-
在门水平上,Liu 等[10]通过对抑郁症患者和健康者进行比对发现两种状态下的肠道群的显著不同,拟杆菌门 Bacteroidetes增高,而厚壁菌门 Firmicutes 降低。除此之外,Chen 等[11]的实验也发现,抑郁症患者肠道菌在拟杆菌门Bacteroidetes、变形菌门 Proteobacteria 、厚壁菌门Firmicutes、放线菌门 Actinobacteria 这4个门中存在显著差异。
在正常与抑郁模型大鼠肠道菌中,差异同样显著存在。Yu 等[12]的实验研究表明了这一点,他们用16S rRNA基因测序法,对由慢性多变压力刺激建立的抑郁大鼠模型进行基因测定,发现与正常大鼠相比,抑郁大鼠模型肠道中厚壁菌门Firmicutes含量是减少的,而拟杆菌门Bacteroidetes含量是增多的。同样证实这一点的还有刘佳琳[13],她通过对慢性不可预知温和应激实验所造的抑郁模型大鼠进行的实验,发现与正常大鼠相比,抑郁模型大鼠盲肠内容物中拟杆菌门Bacteroidetes和变形菌门Proteobacteria相对丰度升高,厚壁菌门Firmicutes的相对丰度降低。
-
在科、属水平上,Jiang等[14]采用测定16S RNA这一细菌身份证片段基因的方法测定 30 例抑郁症患者肠道微生物的变化,发现氨基酸球菌属Acidaminococcus在抑郁症患者中表达上调。而荣晗等 [15]通过选取30岁以上的复发性抑郁症患者做肠道菌群丰度和种类及基因功能测定研究,也证实了氨基酸球菌属表达上调。
在大鼠抑郁模型中,Yu 等[12]实验结果表明,抑郁状态大鼠肠道中的分节丝状菌Candidatus Arthromitu 、颤杆菌克属 Oscillibacter 明显增加,Marvinbryantia、棒状杆菌属 Corynebacterium 、冷杆菌属 Psychrobacter、Christensenella Lactobacillus、Peptostreptococcaceae incertae se-dis、Anaerovorax、Clostridiales incertae sedis 和粪球菌属 Coprococcus 明显降低。刘佳琳[13]探究的抑郁模型大鼠显示,寡源杆菌属 Oligella 、另枝菌属 Alistipes 和脱硫弧菌属Desulfovibrio相对丰度显著增高而乳杆菌属 Lactobacillus 和罗姆布茨菌属Romboutsia 相对丰度显著降低。
-
有研究显示肠道微生物可以调控HPA轴、细胞因子和单胺类神经递质等,Messaoudi等[16]将含有双歧杆菌及乳杆菌的配方物质及空白安慰剂随机分配给重度抑郁症患者口服后,通过严格的评价标准,试验组患者的精神压力、抑郁、焦虑、敌对症状评分均有显著改善,这表明通过补充益生菌可以改善抑郁行为。综合目前对抑郁症的肠道微生物多样性研究报道可以看出,拟杆菌门和厚壁菌门是抑郁症的代表微生物,拟杆菌门与抑郁症正相关,而厚壁菌门与抑郁症负相关。拟杆菌门与厚壁菌门比例的改变会导致抑郁症的发生发展。这些方面均提示肠道菌群可能与抑郁症的发病存在相关性。
-
肠道菌代谢产物,如短链脂肪酸、吲哚等,被认为通过以下几种机制调节抑郁行为:对中央受体的直接作用;激活神经、免疫或内分泌途径的外周受体;组蛋白去乙酰化或DNA甲基化的表观遗传调控。通过代谢产物了解这些机制,有利于加深我们对抑郁症病因的理解,从而利用这些生物活性分子开发新策略进行有益的精神治疗。
-
SCFAs是由肠道菌群厌氧发酵不可消化的碳水化合物产生,极易在大肠中被吸收。已有研究表明SCFAs参与消化、免疫和中枢系统功能,通过控制3个最丰富的SCFAs(丙酸、乙酸和丁酸盐)可以缓解小鼠的抑郁症状[17]。研究发现,抑郁症(MDD)病人体内出现了丙酸、乙酸和丁酸盐的减少[18],而生活质量较高的人群拥有更多能够产生丁酸盐的肠道菌,如栖粪杆菌属 Faecalibacterium和粪肠球菌属 Coprococcus spp.,其中,栖粪杆菌属是肠道中最丰富的微生物属之一,对包括MDD在内的多种疾病具有重要的免疫功能和临床意义[19]。SCFAs能够结合并激活G蛋白偶联受体,使其在体内多个器官中广泛表达,推测SCFAs可能通过直接刺激神经通路或通过神经-内分泌和免疫激活的间接中枢作用来调控抑郁行为。
组蛋白去乙酰化酶活性的改变是抑郁的特征之一,例如,丁酸盐的全身给药诱导小鼠海马和额叶皮质的组蛋白乙酰化[20]以及反复注射丁酸钠通过海马组蛋白H3和H4的乙酰化介导抗抑郁作用[21]。色氨酸代谢改变是抑郁症的特征,其中,丙酸盐通过增加色氨酸羟化酶(TPH)促使色氨酸向5-羟色胺的转化[22]。
-
研究表明,色氨酸经宿主(TDO和IDO)和肠道菌酶(色氨酸酶等)代谢后产生具有既定情绪调节特性的神经活性分子,包括5-HT、犬尿氨酸和吲哚。只有不到5%的色氨酸被色氨酸羟化酶沿着甲氧基吲哚途径转化为5-HT,其余95%通过犬尿氨酸途径由TDO和IDO酶代谢。色氨酸代谢紊乱(即色氨酸从5-HT转移到犬尿氨酸代谢合成)可能是典型抑郁症表现在情绪、认知和睡眠障碍的部分原因[23]。在被定植色氨酸代谢细菌的动物体内发现了色氨酸减少和海马体5-HT浓度增加,并伴有类似焦虑行为的减少[24]。
吲哚通过增加与上皮细胞结构和功能有关的基因表达来增强肠上皮屏障功能,并且通过影响孢子形成、质粒稳定性与耐药性、生物膜形成和毒力在微生物群落中发挥重要作用。另外,吲哚进一步代谢经氧化和偶联的产物——氧化吲哚和2,3-吲哚醌,同样是具有神经活性的信号分子,能够调节运动功能和情绪行为。2,3-吲哚醌是一种内源性单胺氧化酶(MAO)B抑制剂和苯二氮䓬受体拮抗剂,在小鼠和大鼠中都具有抗焦虑的特性[25]。
-
其他肠道菌产生的代谢物质,如乳酸、胆汁酸、神经递质、胆碱代谢物、维生素等也会对抑郁产生一定影响。
乳酸是乳酸菌(乳酸乳球菌、格氏乳杆菌、罗伊氏乳杆菌等)、双歧杆菌和变形杆菌在哺乳动物寄主过程中对膳食纤维发酵产生的有机酸[26],可以被几种细菌转化为SCFAs,对整个菌池有贡献。其调节情绪行为的一个潜在机制是通过直接激活受体GPR81,在海马体、新大脑皮层和小脑表达[27]。
胆汁酸是由胆固醇衍生的类固醇酸,在肝脏合成后分泌到小肠,并在回肠吸收。胆酸(CA)和鹅去氧胆酸(CDCA)这两种主要的胆汁酸在人体和大鼠的肠道中通过肠道菌群进一步结构修饰,转化为二级和三级胆汁酸[28]。胆汁酸具有局部去污性,能够乳化亲脂分子,进而促进营养物质的消化和吸收。此外,胆汁酸可能通过破坏紧密连接的表达,导致肠和中央上皮细胞的通透性,从而导致严重的抑制[29]。有研究表明,胆汁酸的作用在一定程度上可能取决于其物理和化学性质,而这些性质又取决于微生物介导的化合物修饰[30]。另一个可能会影响胆汁酸行为结果的因素是受体介导的响应。此外,一些胆汁酸,如碎石胆酸,可刺激中枢PXR和维生素D受体(VDR),具有良好的抗抑郁作用[31]。
-
如今人们面临的各方面压力越来越大,抑郁症的发病率呈明显的上升趋势,已经成为一个严重的社会和医疗问题。但它发病机制十分繁杂,在治疗上有相当大的阻力。大量关于肠道菌的基础研究已经证实了肠道微生物的结构和多样性紊乱后会诱导或者加速抑郁症的发生,无论是临床统计观察还是实验动物模型检测,都证实了这一点,改善肠道微生物的状态能预防和治疗抑郁症,这一点也同样被研究佐证。
目前已有多项实验研究发现益生菌[32]以及中药复方提取物[33]等可以通过恢复抑郁状态下紊乱的肠道微生物结构来改善抑郁状态,这一点对抑郁症的治疗产生了极大的应用价值。但是基于肠道菌而进行抑郁症疾病药物研发的探究目前仍是处于初级阶段,对于抑郁症相关性高的肠道菌进行调控,是否会与其他肠道菌群产生反应而造成反作用或毒副作用影响机体健康,对于实验结果的普遍性和有效性能否做到更广泛的临床验证,对于直接补充肠道菌代谢产物是否比直接针对肠道菌群进行改造更有效,这些都是需要考虑的,因此,对于后续存在的问题有待继续挖掘和深入探索。
Advances in antidepressant therapy related to gut microbiota
-
摘要:
目的 介绍肠道菌群与抑郁症的病理机制以及相关治疗的研究进展,为后续以肠道菌为靶点的抗抑郁药物的研发提供帮助。 方法 查阅近年来肠道菌群与抑郁症方面的33篇中英文文献进行分类总结,从肠道菌群的门、科、属水平的角度探讨了抑郁状态下肠道菌群多样性的变化,从分子水平上阐述了肠道菌与抑郁症发病机制之间的关系,总结现有相关研究,进一步探索以肠道菌群为靶点进行药物研发治疗的可行性。 结果 肠道菌紊乱与抑郁症之间相互作用,现有益生菌等生物制剂可通过改善肠道菌群病理状态下的紊乱对抑郁症治疗起到缓解作用。 结论 肠道菌群失调与抑郁的发生密切相关,以肠道菌为靶点的相关药物研发治疗,可能成为治疗抑郁症的新途径。 Abstract:Objective This paper introduces the research progress on the pathogenesis of depression related to gut microbiota and provides the resources for the subsequent development of antidepressant drugs targeting gut microbiota. Methods 33 literatures on gut microbiota and depression in recent years were reviewed. The changes of gut microbiota diversity under depression were discussed from the perspectives of phylum, family and genus. The relationship between gut microbiota and the pathogenesis of depression was expounded at the molecular level, and the existing relevant studies were summarized. The feasibility of drug development targeting gut microbiota was explored. Results There is a relationship between gut microbiota disorder and depression. Existing biological agents such as probiotics can alleviate depression by adjusting the disorder of gut microbiota. Conclusion The imbalance of gut microbiota is closely related to the occurrence of depression, and the development of drugs targeting gut microbiota may become a new way to treat depression. -
Key words:
- depression /
- gut microbiota /
- microbiome-gut-brain axis
-
神经炎症是外周血液系统和中枢神经系统中免疫细胞活化和浸润、神经胶质细胞活化和炎性介质产生的过程[1]。脊髓中产生的炎性神经胶质介质调节突触传递,诱导和维持慢性疼痛,并提供神经炎症和慢性疼痛之间的联系[2]。炎症疼痛是一种常见的慢性疾病,以往研究提示,前动力蛋白(prokineticin,PK)系统参与组织损伤和神经损伤后的外周和中枢敏化,其在炎症疼痛中的作用已经被证实[3]。本文针对近年发表的有关PK系统参与炎症疼痛的研究文献,回顾性分析该镇痛靶点所发挥的镇痛机制。
1. PK系统及其生理功能
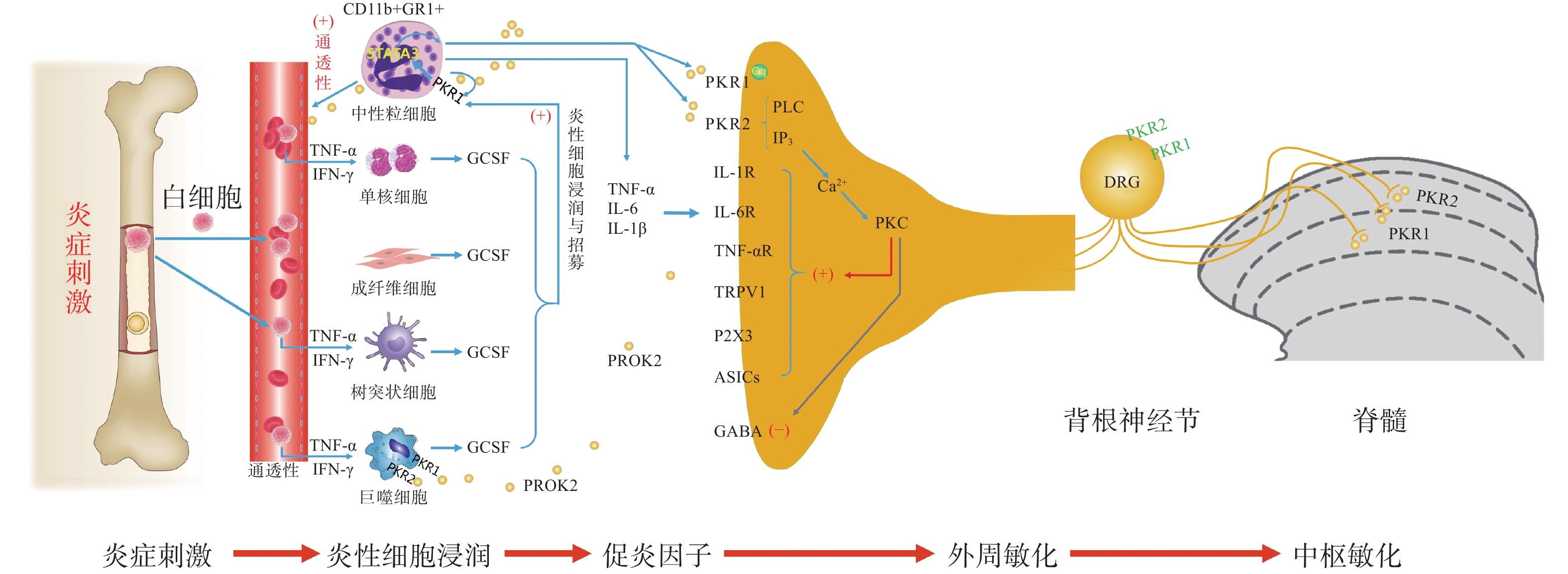
PK信号通路是近年来新发现的介导疼痛发生和维持的重要调节通路,包括两种结构上关联的小分子肽PK1和PK2,以及相应的G蛋白偶联受体PKR1和PKR2[4],PKs及其受体广泛分布在许多人体组织中,例如卵巢、睾丸、肾上腺、胎盘、子宫、大脑、肠道、心脏、骨髓和外周血。虽然PKR1和PKR2在多种组织中共同表达,但PKR1主要表达于外周组织,包括生殖系统[5]的内分泌腺和器官、胃肠道、脾脏、胰腺、肺、心脏和血细胞[6]。PKR2主要在脊髓背角神经元和星形胶质细胞中表达,PKR1主要存在于星形胶质细胞和外周神经元的末端,主要分布于背角的表层(图1)。PK2对这两种受体的亲和力均略高于PK1,而PK1在DRG(背根神经节)和脊髓中不表达,更多地参与血管生成[7],PK1是强有力的血管生成因子,被认为在内分泌腺、心血管、肾脏、肿瘤等血管新生中发挥重要作用。
PKs在神经系统、免疫系统、生殖系统、心血管系统等多部位发挥广泛的生理作用[8],此外PK2可通过降低对化学和机械刺激的疼痛阈值,PKRs的拮抗剂可以用来缓解关节炎炎症和急慢性疼痛[9-10]。PKs通过激活单核细胞、巨噬细胞和树突状细胞上的PKRs,释放炎性细胞因子,触发和维持炎性疼痛(图1),调节免疫炎症反应,而在外周,PK2 /PKR2参与心脏和肾脏新生血管的形成,PKR1的缺失会引起心脏和肾脏的结构和功能变化[11-12]。因此,PKs系统在体内发挥着广泛的生理作用,也是众多疾病的潜在治疗靶点。
2. PK系统与躯体痛觉敏化
PK系统在调节与伤害相关的伤害性事件方面起着关键作用,因为它可以调节炎症反应,并同时作用于中枢和外周神经系统。PKRs的激活可以引起痛觉感受,参与痛觉感受器对不同刺激的敏感性。PK系统(PKs和PKRs)是在免疫细胞中参与炎症发生和疼痛传递的重要环节,如PK2参与免疫调节,诱导骨髓细胞分化为单核细胞系和巨噬细胞系,并通过激活单核细胞、巨噬细胞和树突状细胞上的PKRs,释放IL-1β、IL-6、TNF-α等炎性细胞因子,触发和维持炎性疼痛,调节免疫炎症反应[13]。
2.1 外周敏化
PK2在炎症细胞中呈强上调,并在病理状态下维持炎症循环。在纳摩尔范围内,PKs结合并激活受体PKR1和PKR2,使PK2在粒细胞、树突状细胞和巨噬细胞中表达,尤其在局部炎症后表达增加。此外,PK2在免疫细胞和神经胶质细胞中被强烈上调,并在炎症组织中,维持促炎循环。在中性粒细胞依赖性炎症和超痛觉过敏中起关键作用[14]。第一个关于PK的促痛作用的证据来自于对啮齿动物全身注射Bv8/PK2,激活其位于痛觉传入通路的PKRs受体而引起机械和热刺激痛觉过敏[15-16]。在完全弗氏佐剂(CFA)诱导的慢性炎症动物模型中,炎症与浸润炎症组织的粒细胞中PK2的过表达呈高度正相关,而PK2的上调则与炎症相关的痛觉过敏也有关,PKR1拮抗剂PC1能够有效消除CFA引起的痛觉过敏,PC1能明显抑制疼痛、水肿和外渗[17]。PK2在人和动物炎症组织中过表达,主要在浸润的中性粒细胞中作为主要的前感受介质之一,通过激活初级传入神经元上的PKRs受体(图1),增强伤害性信号向中枢神经系统传递。PK2反过来调节血管生成和血管通透性,激活巨噬细胞,并通过PKRs调节毛细血管内皮细胞和白细胞的免疫反应,使得炎症反应循环。
PKR1和PKR2基因的缺失大大降低了炎症诱导的热敏感性和机械敏感性[18-19],但是只有PKR1基因的缺失才会降低PK2的上调,这表明这两种受体虽然都介导疼痛的感受和传递,但只有PKR1参与了炎症过程中Bv8/PK2表达水平的增强。外周局部给予PKRs拮抗剂(PC1或PC7)后疼痛明显减轻,与Bv8/PK2对血管通透性的影响效果一致。在CFA诱导的大鼠或小鼠炎症模型中,在它们健康的爪子中很难检测到的PK2 mRNA,而在炎症皮肤中显著增加,且与浸润细胞(粒细胞和巨噬细胞)相关,并与疼痛和其他炎症在时间上相关。粒细胞释放PK2直接作用于痛觉受器,调节急性炎症性疼痛,进而发挥趋化作用,诱导促炎性巨噬细胞表型,并使Th1(T淋巴细胞1)/Th2(T淋巴细胞2)失衡向Th1倾斜[20-21],抑制Th1介导的免疫反应发挥抗炎作用。
PK2通过激活初级传入神经元上的PKR1和PKR2参与调节痛觉感知(图1),PKRs根据细胞定位可能与G蛋白结合,并激活不同的细胞内信号通路。在单核细胞/巨噬细胞/小胶质细胞谱系中,以及在DRG及脊髓中,PKRs是Gq偶联受体,通过激活磷脂酶C-β (PLC)和形成IP3,促进细胞内Ca2+的动员,诱发蛋白激酶C (PKC) -ε易位到质膜,外周高度表达的PKRs能够对TRPV1(瞬时感受器电位香草素亚型1)和TRPA1 (瞬时感受器电位锚蛋白亚型1)的促进性激活有助于外周敏化[22],尤其是PKR1定位于表达TRPV1和TRPA1的伤害性感觉纤维,在外周DRG水平这些共定位表达,为通过激活PKC-ε的痛觉敏化的协同作用提供了解剖学基础。在大鼠初级感觉神经元中,PK2还通过PKC信号通路增强了门控离子通道电流、抑制GABA激活电流、敏化嘌呤核苷酸P2受体(P2X)[23]。对PK2反应的DRG神经元中50%也表达参与疼痛处理的神经介质,如降钙素基因相关肽(CGRP)和P物质,且在这些神经元暴露于PKs时释放这些神经肽,提示PKs不仅仅参与调节中枢疼痛机制[24]。
2.2 中枢敏化
脊髓PK2主要存在于小鼠脊髓星形胶质细胞中[25],最大密度的PKRs位于背角[26],这表明这些受体可能参与了伤害性信号的中枢传递。非神经元细胞如星形胶质细胞、小胶质细胞等都有PKR1表达,此外,PKR1受体在人和啮齿类单核/巨噬细胞上也比PKR2更为丰富。免疫组化定位显示,PKR1与进入背角和外皮层的伤害感受器末端有关,PKR2存在于沿着浅背角的神经元胞体中,也有可能是投射神经元。PK2诱导脊髓背角和活化的星形胶质细胞中PKRs的激活,有助于中枢敏化和维持慢性痛、神经性疼痛,而且PK2作用于单核细胞、巨噬细胞和树突状细胞上的PKRs,还能诱导炎症因子和致痛因子的释放[27]。在慢些压迫性损伤(CCI)模型中发现,PK2在脊髓星形胶质细胞和初级感觉神经元中表达上调[26]。同时,PK2可抑制下丘脑、导水管周围灰质(PAG)脑区中脑啡肽 (ENK)阳性神经元的动作电位放电,表明PK2能够抑制这类细胞释放阿片样物质。通过配体和受体在神经元和星形胶质细胞中的不同分布,PK2既可以诱导星形胶质细胞激活,发挥星形胶质细胞分泌生长因子的功能,也可以促进脊髓神经元的兴奋性突触传递,增强中枢敏化。PK2小分子拮抗剂改善持续疼痛超敏反应的能力以及在“神经元-神经胶质”和“神经元-免疫细胞”相互作用中分子变化,表明了PK2信号在这种行为中的重要性(图1)。阻断PK受体的药物可能为治疗慢性疼痛状态提供一种新形式[28]。在啮齿动物中注射PK2可激活位于疼痛传递主要部位的PKRs受体诱导对机械和热刺激的痛觉过敏[15]。痛觉过敏的初始阶段是由对伤害感受器的局部作用引起的,痛觉过敏的第二阶段是由于中枢作用引起的[24],表明PKs /PKRs在中枢与周围部位的作用存在差异。在敲除PK2基因的小鼠中进行研究表明,PKs在疼痛感知中具有直接作用,与正常野生型小鼠相比,基因敲除的小鼠对温度和化学刺激的伤害感受降低[18-19]。
损伤部位异常增加的IL-6、IL-1β反过来促进PK2的释放,进一步促进外周免疫细胞的过度激活,加速外周敏化的形成和维持。在DRG和脊髓中,PKR通过Gq激活后增加细胞内钙和诱发蛋白激酶C (PKC) -ε易位到质膜,PK2能够敏化表达TRPV1和TRPA1的痛觉感受器,从外周组织、DRG和脊髓等部位发挥多途径的抑制PK系统的激活而发挥镇痛效应。
综上所述,PKs在疼痛的发生和维持中发挥了重要作用,其在调节与伤害相关的伤害性事件方面起着关键作用,在未来的研究中,有望以PKs信号通路为靶点研究出新的治疗药物。
-
[1] KELLY J R, BORRE Y, O' BRIEN C, et al. Transferring the blues: Depression-associated gut microbiota induces neurobehavioural changes in the rat[J]. J Psychiatr Res,2016,82:109-118. doi: 10.1016/j.jpsychires.2016.07.019 [2] 查伟, 李树生, 徐柯, 等. 柴桂温胆定志汤联合帕罗西汀治疗抑郁症疗效和安全性评价[J]. 中国药业, 2019, 28(13):53-55. doi: 10.3969/j.issn.1006-4931.2019.13.016 [3] GILBERT K, ARSENEAULT-BRÉARD J, FLORES MONACO F, et al. Attenuation of post-myocardial infarction depression in rats by n-3 fatty acids or probiotics starting after the onset of reperfusion[J]. Br J Nutr,2013,109(1):50-56. doi: 10.1017/S0007114512003807 [4] ZHUANG F, ZHOU X, GAO X, et al. Cytokines and glucocorticoid receptors are associated with the antidepressant-like effect of alarin[J]. Peptides,2016,76:115-129. doi: 10.1016/j.peptides.2016.01.002 [5] 汪崇泽, 盛国红. 免疫炎症途径与抑郁症的研究进展[J]. 精神医学杂志, 2015, 28(5):397-400. doi: 10.3969/j.issn.2095-9346.2015.05.025 [6] AAN HET ROT M, MATHEW S J, CHARNEY D S. Neurobiological mechanisms in major depressive disorder[J]. CMAJ,2009,180(3):305-313. doi: 10.1503/cmaj.080697 [7] HAMON M, BLIER P. Monoamine neurocircuitry in depression and strategies for new treatments[J]. Prog Neuropsychopharmacol Biol Psychiatry,2013,45:54-63. doi: 10.1016/j.pnpbp.2013.04.009 [8] PYTKA K, DZIUBINA A, MŁYNIEC K, et al. The role of glutamatergic, GABA-ergic, and cholinergic receptors in depression and antidepressant-like effect[J]. Pharmacol Rep,2016,68(2):443-450. doi: 10.1016/j.pharep.2015.10.006 [9] MORAITIS A G, BLOCK T, NGUYEN D, et al. The role of glucocorticoid receptors in metabolic syndrome and psychiatric illness[J]. J Steroid Biochem Mol Biol, 2017, 165(pt a): 114-120. [10] LIU Y X, ZHANG L, WANG X Q, et al. Similar fecal microbiota signatures in patients with diarrhea-predominant irritable bowel syndrome and patients with depression[J]. Clinical Gastroenterology and Hepatology,2016,14(11):1602-1611.e5. doi: 10.1016/j.cgh.2016.05.033 [11] CHEN Z, LI J, GUI S, et al. Comparative metaproteomics analysis shows altered fecal microbiota signatures in patients with major depressive disorder[J]. Neuroreport,2018,29(5):417-425. doi: 10.1097/WNR.0000000000000985 [12] YU M, JIA H, ZHOU C, et al. Variations in gut microbiota and fecal metabolic phenotype associated with depression by 16S rRNA gene sequencing and LC/MS-based metabolomics[J]. J Pharm Biomed Anal,2017,138:231-239. doi: 10.1016/j.jpba.2017.02.008 [13] 刘佳琳. 肠道菌群介导的栀子豉汤抗抑郁作用及配伍机制研究[D]. 上海: 海军军医大学, 2019. [14] JIANG H, LING Z, LING Z, et al. Altered fecal microbiota composition in patients with major depressive disorder[J]. Brain Behav Immun,2015,48:186-194. doi: 10.1016/j.bbi.2015.03.016 [15] RONG HAN. A case-control study on the abundance, species and gene functional pathway of gut microbiota in patients with depression[J]. China Med Abstr Intern Med,2017,34(3):191-192. [16] MESSAOUDI M, LALONDE R, VIOLLE N, et al. Assessment of psychotropic-like properties of a probiotic formulation (Lactobacillus helveticus R0052 and Bifidobacterium longum R0175) in rats and human subjects[J]. Br J Nutr,2011,105(5):755-764. doi: 10.1017/S0007114510004319 [17] VAN DE WOUW M, BOEHME M, LYTE J M, et al. Short-chain fatty acids: microbial metabolites that alleviate stress-induced brain-gut axis alterations[J]. J Physiol,2018,596(20):4923-4944. doi: 10.1113/JP276431 [18] CHEN J J, ZHOU C J, LIU Z, et al. Divergent urinary metabolic phenotypes between major depressive disorder and bipolar disorder identified by a combined GC–MS and NMR spectroscopic metabonomic approach[J]. J Proteome Res,2015,14(8):3382-3389. doi: 10.1021/acs.jproteome.5b00434 [19] CORRÊA-OLIVEIRA R, FACHI J L, VIEIRA A, et al. Regulation of immune cell function by short-chain fatty acids[J]. Clin Trans Immunol,2016,5(4):e73. doi: 10.1038/cti.2016.17 [20] SCHROEDER F A, LIN C L, CRUSIO W E, et al. Antidepressant-like effects of the histone deacetylase inhibitor, sodium butyrate, in the mouse[J]. Biological psychiatry,2007,62(1):55-64. doi: 10.1016/j.biopsych.2006.06.036 [21] YAMAWAKI Y, YOSHIOKA N, NOZAKI K, et al. Sodium butyrate abolishes lipopolysaccharide-induced depression-like behaviors and hippocampal microglial activation in mice[J]. Brain Res,2018,1680:13-38. doi: 10.1016/j.brainres.2017.12.004 [22] NANKOVA B B, AGARWAL R, MACFABE D F, et al. Enteric bacterial metabolites propionic and butyric acid modulate gene expression, including CREB-dependent catecholaminergic neurotransmission, in PC12 cells - possible relevance to autism spectrum disorders[J]. PLoS One,2014,9(8):e103740. doi: 10.1371/journal.pone.0103740 [23] VAN DER VEEN F M, EVERS E A, DEUTZ N E, et al. Effects of acute tryptophan depletion on mood and facial emotion perception related brain activation and performance in healthy women with and without a family history of depression[J]. Neuropsychopharmacology,2007,32(1):216-224. doi: 10.1038/sj.npp.1301212 [24] CLARKE G, GRENHAM S, SCULLY P, et al. The microbiome-gut-brain axis during early life regulates the hippocampal serotonergic system in a sex-dependent manner[J]. Mol Psychiatry,2013,18(6):666-673. doi: 10.1038/mp.2012.77 [25] BHATTACHARYA S K, MITRA S K, ACHARYA S B. Anxiogenic activity of isatin, a putative biological factor, in rodents[J]. J Psychopharmacol,1991,5(3):202-206. doi: 10.1177/026988119100500304 [26] RÍOS-COVIÁN D, RUAS-MADIEDO P, MARGOLLES A, et al. Intestinal short chain fatty acids and their link with diet and human health[J]. Front Microbiol,2016,7:185. [27] LAURITZEN K H, MORLAND C, PUCHADES M, et al. Lactate receptor sites link neurotransmission, neurovascular coupling, and brain energy metabolism[J]. Cerebral Cortex,2014,24(10):2784-2795. doi: 10.1093/cercor/bht136 [28] RUSSELL D W. The enzymes, regulation, and genetics of bile acid synthesis[J]. Annu Rev Biochem,2003,72(1):137-174. doi: 10.1146/annurev.biochem.72.121801.161712 [29] QUINN M, MCMILLIN M, GALINDO C, et al. Bile acids permeabilize the blood brain barrier after bile duct ligation in rats via Rac1-dependent mechanisms[J]. Dig Liver Dis,2014,46(6):527-534. doi: 10.1016/j.dld.2014.01.159 [30] RAIMONDI F, SANTORO P, BARONE M V, et al. Bile acids modulate tight junction structure and barrier function of Caco-2 monolayers via EGFR activation[J]. Am J Physiol-Gastrointest Liver Physiol,2008,294(4):G906-G913. doi: 10.1152/ajpgi.00043.2007 [31] MOORE L B, GOODWIN B, JONES S A, et al. St. John's wort induces hepatic drug metabolism through activation of the pregnane X receptor[J]. PNAS,2000,97(13):7500-7502. doi: 10.1073/pnas.130155097 [32] 安邦, 张大维, 赵珊珊, 等. 双歧杆菌三联活菌辅助帕罗西汀治疗女性抑郁症患者效果观察及机制探讨[J]. 山东医药, 2020, 60(29):58-60. doi: 10.3969/j.issn.1002-266X.2020.29.016 [33] 吴国琳, 余国友, 范小芬, 等. 单味中药及其有效成份对肠道微生态的调节作用研究概况[J]. 中国中医药现代远程教育, 2015, 13(9):134-136. doi: 10.3969/j.issn.1672-2779.2015.09.067 -

 点击查看大图
点击查看大图
计量
- 文章访问数: 8234
- HTML全文浏览量: 2465
- PDF下载量: 35
- 被引次数: 0




 下载:
下载:

 下载:
下载:
