-
放线菌以其能产生结构新颖且有良好生物活性的先导化合物而备受关注[1],一直被认为是天然药物的重要生产者,其主要结构类型包括聚酮、生物碱、多肽和萜烯类化合物等,同时涵盖了多种多样的生物活性如抗菌、抗寄生虫、免疫调节、抗炎、抗癌等[2-4],这突显了放线菌具有不可预估的药物开发潜力。
随着研究的深入,陆地和普通环境中的资源日趋枯竭,很多微生物及其次生代谢产物被重复开发和提取分离,发现新活性分子的几率愈来愈低,开发创新药物的难度越来越大[5-6];而极地极端的生态环境造就的微生物具有产生更为特别的化学骨架和活性次生代谢产物的能力,是新型药源分子的重要来源。本文以采自北极楚克奇海域海绵共附生放线菌Streptomyces sp. LHW11-07为研究对象,从其发酵浸膏中分离鉴定了9个单体化合物1~9(图1),其中化合物1和2为该属内首次分离得到。
-
AMX-600型核磁共振仪(德国Bruker公司);Xevo G2-XS Q-TOF液质联用仪、1525/2996, 2998型高效液相色谱仪(美国Waters公司);半制备型HPLC色谱柱(Atlantis Prep T3,美国Waters公司;YMC C18,日本YMC公司);中压柱色谱仪(法国Interchim公司);恒温振荡培养箱(上海一恒科学仪器有限公司);N-1000型旋转蒸发仪(上海爱郎仪器有限公司);反相ODS硅胶和Sephadex LH-20柱色谱填料(Pharmacia公司);正相硅胶(200-300目)和TLC薄层板(烟台江友硅胶开发有限公司);分析级试剂(上海化学试剂公司);色谱级试剂(德国Merck公司);氘代试剂(美国剑桥同位素实验室公司)。
-
菌株分离于北极海域来源的海绵样本,经16S rRNA基因序列鉴定为Streptomyces sp.,编号为LHW11-07,菌种保存于上海交通大学医学院附属仁济医院药学部海洋药物研究中心。
-
培养基为ISP2:葡萄糖(4 g/L)、酵母提取物(4 g/L)、麦芽糖提取物(10 g/L)以及海盐(25 g/L),加水溶解后调节pH为7.2~7.4,分装后高压灭菌20 min (121 ℃),冷却备用。
挑取Streptomyces sp. LHW11-07单菌落至1级种子培养基里(100 ml ISP2培养基至250 ml三角瓶),置于30 ℃,220 r/min的恒温摇床培养3 d,得1级种子液;将1级种子液按5%接种量接到2级种子培养基里(150 ml ISP2培养基至500 ml三角瓶),置于30 ℃,220 r/min的恒温摇床培养3 d,得2级种子液;将2级种子液按5%接种量接到大发酵培养基里(700 ml ISP2培养基至2 L三角瓶),置于30 ℃,220 r/min的恒温摇床培养7 d,共得到发酵液50 L。
-
菌株培养7 d后,用等体积的乙酸乙酯萃取3次,合并乙酸乙酯提取液,减压浓缩得粗浸膏9.8 g。粗浸膏先经凝胶柱分离,二氯甲烷:甲醇(1∶1)的混合溶剂进行洗脱,得到组份Fr.1~Fr.7。
组份Fr.4经正相中压柱色谱分离(二氯甲烷:甲醇100:0~0:100),得到组份Fr.4a~Fr.4j。组份Fr.4d再经反相中压柱色谱分离(10%~100%乙腈水),得到组份Fr.4d1~Fr.4d8,Fr.4d2和Fr.4d3用反相半制备HPLC纯化(35%甲醇水,YMC C18),分别得到化合物1 (12 mg, tR=26 min)和2 (47.6 mg, tR=30 min);Fr.4d6用反相半制备HPLC纯化(49%甲醇水,YMC C18),得到化合物3 (8.4 mg, tR=23 min)和4 (2.0 mg, tR=30 min);组份Fr.4g再经凝胶柱纯化,洗脱剂为正己烷:二氯甲烷:甲醇(4∶5∶1),得到组份Fr.4g1~Fr.4g11,其中Fr.4g3用反相半制备HPLC纯化(25%乙腈水,YMC C18),得到化合物5 (1.2 mg, tR=18 min)。
组份Fr.7经反相中压柱色谱分离(10%~100%乙腈水),得到组份Fr.7A~Fr.7D。组份Fr.7A用反相半制备HPLC纯化(20%乙腈水,YMC C18),得到化合物6 (18 mg, tR=19 min)和7 (3.4 mg, tR=25 min);组份Fr.7B经正相中压柱分离(石油醚:丙酮100:0~0:100),得到组份Fr.7B1~Fr.7B9,Fr.7B4用反相半制备HPLC纯化(88%乙腈水,Atlantis Prep T3),得到化合物8 (12 mg, tR=23 min)和9 (8.4 mg, tR=26 min)。
-
化合物1:淡黄色固体,ESI-MS显示准分子离子峰m/z 372 [M+Na]+。1H-NMR (600 MHz, DMSO)显示在低场区有吲哚环的特征信号δH 7.00 (1H, s, H-2),7.49 (1H, d, J=8.0 Hz, H-4),7.02 (1H, t, J=7.6 Hz, H-5),7.05 (1H, t, J=7.6 Hz, H-6),7.32 (1H, d, J=8.0 Hz, H-7);4个活泼氢质子信号δH 10.89 (1H, d, J=2.6 Hz, NH-1),7.83 (1H, d, J=3.0 Hz, NH-10),7.62 (1H, d, J=3.0 Hz, NH-13),9.20 (1H, s, OH-19);4个芳香质子信号δH 6.53 (2H, d, J=8.4 Hz, H-17, H-21),6.59 (2H, d, J=8.4 Hz, H-18, H-20),提示分子中有1个对位二取代的苯环;在高场区有两组亚甲基质子信号δH 2.80 (1H, dd, J=14.5, 4.5 Hz, H-8),2.43 (1H, ov, H-8),δH 1.83 (1H, dd, J=13.4, 6.9 Hz, H-15),2.47 (1H, ov, H-15),两个次甲基质子信号δH 4.01 (1H, m, H-9),3.95 (1H, m, H-12)。13C-NMR (150 MHz, DMSO)结合DEPT谱表明其有20个碳信号,2个酮羰基碳δC 166.7,166.2,14个芳香碳,2个亚甲基碳δC 30.0,40.0和2个次甲基碳δC 55.9,55.2。对其碳信号进行归属:δC 118.7 (C-2)、108.9 (C-3)、127.5 (C-3a)、118.4 (C-4)、120.8 (C-5)、124.3 (C-6)、111.3 (C-7)、136.0 (C-7a)、30.0 (C-8)、55.9 (C-9)、166.7 (C-11)、55.2 (C-12)、166.2 (C-14)、40.1 (C-15)、126.4 (C-16)、130.7 (C-17, C-21)、114.9 (C-18, C-20)、156.0 (C-19)。以上数据与文献[7]对比基本一致,故确定为cyclo-(L-Tyr-L-Trp)。
化合物2:淡黄色固体,ESI-MS显示准分子离子峰m/z 274 [M+H]+。1H-NMR (600 MHz, DMSO)发现其与化合物1一样有吲哚环的特征信号δH 7.09 (1H, s, H-2),7.52 (1H, d, J = 7.9 Hz, H-4),6.99 (1H, t, J = 7.8 Hz, H-5),7.02 (1H, t, J = 7.8 Hz, H-6),7.30 (1H, d, J = 7.8 Hz, H-7);3个活泼氨基质子信号δH 10.87 (1H, s, NH-1),δH 8.30 (1H, m, NH-10),7.85 (1H, d, J = 2.9 Hz, NH-13);两组亚甲基质子信号δH 3.21 (1H, m, H-8),3.13 (1H, m, H-8),δH 3.65 (1H, m, H-15),3.05 (1H, m, H-15),两个次甲基质子信号δH 4.87 (1H, m, H-9),4.00 (1H, m, H-12)。13C-NMR (150 MHz, DMSO)结合DEPT谱表明其有14个碳信号,2个酮羰基碳δC 167.2,165.7,8个芳香碳,2个亚甲基碳δC 63.0,30.3和2个次甲基碳δC 57.3,55.5。对其碳信号进行归属:δC 127.6 (C-2)、111.2 (C-3)、136.0 (C-3a)、118.6 (C-4)、120.8 (C-5)、124.0 (C-6)、118.3 (C-7)、109.0 (C-7a)、30.3 (C-8)、57.3 (C-9)、167.2 (C-11)、55.5 (C-12)、165.7 (C-14)、63.0 (C-15)。以上数据与文献[8]对比基本一致,故确定为cyclo-(L-Trp-L-Ser)。
化合物3:白色固体,ESI-MS显示准分子离子峰m/z 261 [M+H]+。1H-NMR (600 MHz, DMSO)提示有2个活泼氢质子信号δH 7.87 (1H, s, NH-8),9.22 (1H, s, OH-4’);1组对位二取代的苯环芳香质子信号δH 7.04 (2H, d, J = 8.2 Hz, H-2’, H-6’),6.63 (2H, d, J = 8.2 Hz, H-3’, H-5’);2个次甲基质子信号δH 4.24 (1H, t, J = 8.2 Hz, H-6),4.03 (1H, dd, J = 9.9, 2.9 Hz, H-9);4组亚甲基质子信号δH 3.42 (1H, m, H-3),3.24 (1H, m, H-3),1.73 (2H, m, H2-4),2.00 (1H, m, H-5),1.41 (1H, m, H-5),2.93 (2H, m, H2-10)。13C-NMR (150 MHz, DMSO)结合DEPT谱表明其有14个碳信号,2个酮羰基碳δC 168.9,165.1,6个芳香碳,2个次甲基碳δC 58.4,56.0以及4个亚甲基碳δC 44.6,34.7,27.8,21.9。对其碳信号进行归属:δC 165.1 (C-1)、44.6 (C-3)、21.9 (C-4)、27.8 (C-5)、58.4 (C-6)、168.9 (C-7)、56.0 (C-9)、34.7 (C-10)、127.0 (C-1’)、130.8 (C-2’, C-6’)、114.8 (C-3’, C-5’)、155.9 (C-4’)。以上数据与文献[9]对比基本一致,故确定为cyclo-(D-Tyr-D-Pro)。
化合物4:白色固体,ESI-MS显示准分子离子峰m/z 311 [M+H]+。1H-NMR (600 MHz, DMSO)显示3个活泼氢质子信号δH 9.30 (1H, s, OH-11),7.84 (2H, t, J = 2.9 Hz, NH-1, NH-4);9个芳香区质子信号:4个归为1组对位二取代苯环δH 6.85 (2H, d, J = 8.5 Hz, H-9, H-13),6.65 (2H, t, J = 8.5 Hz, H-10, H-12),5个归为1组单取代苯环δH 7.20 (1H, t, J = 7.6 Hz, H-18),7.04 (2H, d, J = 6.9 Hz, H-16, H-20),7.28 (2H, t, J = 7.6 Hz, H-17, H-19);2组亚甲基质子信号δH 2.58 (1H, dd, J = 13.6, 5.0 Hz, H-7),2.20 (1H, d, J = 6.5 Hz, H-7),2.19 (2H, dd, J = 13.6, 6.5 Hz, H2-14),2个次甲基质子信号δH 3.95 (1H, m, H-3),3.90 (1H, m, H-6)。13C-NMR (150 MHz, DMSO)结合DEPT谱显示其有18个碳信号,2个酮羰基碳δC 166.2,166.2,12个芳香碳,2个亚甲基碳δC 40.1,38.5和2个次甲基碳δC 55.7,55.4。对其碳信号进行归属:δC 166.2 (C-2)、55.7 (C-3)、166.3 (C-5)、55.4 (C-6)、40.1 (C-7)、126.5 (C-8)、130.8 (C-9, C-13)、115.0 (C-10, C-12)、156.1 (C-11)、38.5 (C-14)、136.7 (C-15)、129.7 (C-16, C-20)、128.2 (C-17, C-19)、126.4 (C-18)。以上数据与文献[10]对比基本一致,故确定为cyclo-(L-Tyr-L-Phe)。
化合物5:白色固体,ESI-MS显示准分子离子峰m/z 277 [M+H]+。1H-NMR (600 MHz, DMSO)显示3个活泼氢质子信号δH 9.22 (1H, s, OH-4’),8.02 (2H, dd, J = 5.6, 2.5 Hz, NH-1, NH-4);4个芳香质子信号δH 6.90 (2H, d, J = 8.2 Hz, H-2’, H-6’),6.64 (2H, d, J = 8.2 Hz, H-3’, H-5’),提示分子中有1个对位二取代苯环;3个次甲基质子信号δH 4.06 (1H, q, J = 3.3 Hz, H-3),3.44 (1H, m, H-6),1.43 (1H, ov, H-8),2个亚甲基质子信号δH 1.43 (1H, m, H-7),1.23 (1H, m, H-7),2.69 (1H, q, J = 13.6, 4.8 Hz, H-11),3.01 (1H, q, J = 13.7, 3.7 Hz, H-11)以及2个末端甲基质子信号δH 0.63 (6H, ov, H3-9, H3-10)。13C-NMR (150 MHz, DMSO)结合DEPT谱显示其有15个碳信号,2个酮羰基碳δC 166.2,167.4,6个芳香碳,2个亚甲基碳δC 43.7,37.7,3个次甲基碳δC 55.7,52.3,21.4以及2个甲基碳δC 22.9,22.8。对其碳信号进行归属:δC 166.2 (C-2)、55.7 (C-3)、167.4 (C-5)、52.3 (C-6)、43.7 (C-7)、21.4 (C-8)、22.9 (C-9)、22.8 (C-10)、37.7 (C-11)、125.8 (C-1’)、131.2 (C-2’, C-6’)、114.8 (C-3’, C-5’)、156.4 (C-4’)。以上数据与文献[11]对比基本一致,故确定为cyclo-(L-Tyr-L-Leu)。
化合物6:白色固体,ESI-MS显示准分子离子峰m/z 259 [M+Na]+。1H-NMR (600 MHz, DMSO)显示有2个活泼氢质子信号δH 5.05 (1H, d, J = 4.5 Hz, OH-4)和4.39 (1H, q, J = 4.0 Hz, OH-13),3个甲基质子信号δH 0.88 (3H, d, J = 6.8 Hz, H3-12),0.98 (3H, s, H3-14)和δH 1.05 (3H, s, H3-15),5对亚甲基质子信号δH 2.14 (1H, m, H-3),1.23 (1H, m, H-3),1.74 (1H, m, H-9),1.60 (1H, m, H-9),1.44 (3H, m, H2-10, H-11),1.32 (1H, d, J = 10.4 Hz, H-11),3.95 (2H, m, H2-13),3个次甲基质子信号δH 1.68 (1H, m, H-2),4.57 (1H, m, H-4),1.77(1H, m, H-8)。13C-NMR (150 MHz, DMSO)结合DEPT谱共显示有15个碳信号,包括4个季碳δC 52.1,150.1,136.7,39.8;3个次甲基碳δC 35.2,69.8,46.4;5个亚甲基碳δC 42.4,23.8,28.7,36.4,57.1以及3个甲基碳δC 13.7,29.1,24.4。对其碳信号进行归属:δC 52.1 (C-1)、35.2 (C-2)、42.4 (C-3)、68.9 (C-4)、150.1 (C-5)、136.7 (C-6)、39.8 (C-7)、46.4 (C-8)、23.8 (C-9)、28.7 (C-10)、36.4 (C-11)、13.7 (C-12)、57.1 (C-13)、29.1 (C-14)、24.4 (C-15)。以上数据与文献[12]对比基本一致,故确定为albaflavenol B。
化合物7:白色结晶固体,ESI-MS显示准分子离子峰m/z 268 [M+H]+。1H-NMR (600 MHz, DMSO)可看出其有13个氢信号,包括5个活泼氢质子信号δH 3.56 (2H, m, NH2),5.49 (1H, s, OH-5’),5.36 (1H, t, J = 4.9 Hz, OH-2’)和5.23 (1H, s, OH-3’),4个连氧次甲基质子信号δH 4.56 (1H, s, H-2’),4.14 (1H, s, H-3’),3.96 (1H, m, H-4’)和5.90 (1H, d, J = 5.8 Hz, H-1’),1组亚甲基信号δH 3.66 (2H, m, H2-5’)以及2个低场区的烯氢质子信号δH 8.37 (1H, s, H-8)和8.21 (1H, s, H-2)。13C-NMR (150 MHz, DMSO)显示其共有10个碳信号,结合DEPT谱可推测有3个芳香季碳δC 149.9,119.8,154.3,2个连氮的芳香次甲基碳δC 151.7,138.6,4个次甲基碳δC 87.8,73.5,70.5,85.7,1个亚甲基碳δC 61.5。对其碳信号进行归属:δC 151.7 (C-2)、149.9 (C-4)、119.8 (C-5)、154.3 (C-6)、138.6 (C-8)、87.8 (C-1’)、73.5 (C-2’)、70.5 (C-3’)、85.7 (C-4’)、61.5 (C-5’)。以上数据与文献[13]对比基本吻合,故确定为β-adenosine。
化合物8:绿色无定型固体,ESI-MS显示准分子离子峰m/z 297 [M+H]+。1H-NMR (600 MHz, MeOD)显示有12个氢信号,包括1个活泼氢质子信号δH 8.37 (1H, s, H-11),1个甲氧基质子信号δH 3.79 (3H, s),1个甲基质子信号δH 1.25 (3H, d, J = 6.4 Hz, H3-13),3个低场区的芳香氢质子信号δH 8.31 (1H, d, J = 7.8 Hz, H-4),6.92 (1H, t, J = 8.0 Hz, H-5)和7.65 (1H, d, J = 8.0 Hz, H-6),以及2个次甲基质子信号δH 4.74 (1H, d, J = 3.2 Hz, H-8)和4.40 (1H, m, H-12),后与文献[14]对比发现其有4个活泼氢质子信号没有显示出来,而根据相关化学位移可确定其是同一个已知化合物。13C-NMR (150 MHz, MeOD)显示有13个碳信号,结合DEPT谱可推测有6个芳香碳δC 123.4,119.4,126.2,128.2,152.5,115.6,2个羰基碳δC 171.8,172.4,而δC 162.1为醛基碳,2个次甲基碳δC 59.4,68.4,1个甲基碳δC 20.5,以及1个甲氧基碳δC 52.9。对其碳信号进行归属:δC 115.6 (C-1)、152.5 (C-2)、128.2 (C-3)、126.2 (C-4)、119.4 (C-5)、123.4 (C-6)、171.8 (C-7)、59.4 (C-8)、172.4 (C-9)、52.9 (C-10)、162.1 (C-11)、68.4 (C-12)、20.5 (C-13)。以上数据与文献[14]对比基本吻合,故确定为N-formylantimyic acid methyl ester。
化合物9:白色粉末状固体,ESI-MS显示准分子离子峰m/z 499 [M+H]+。1H-NMR (600 MHz, DMSO)显示有19个氢信号:δH 8.20 (1H, s, H-11),6.82 (1H, s, H-10),6.32 (1H, dd, J = 10.5, 1.3 Hz, H-3),5.01 (1H, m, H-7),2.99 (1H, dd, J = 2.5, 15.8 Hz, H-8),2.80 (1H, dd, J = 10.3, 15.6 Hz, H-8),2.58 (1H, m, H-4),1.66 (1H, m, H-5),1.65 (3H, s, 2-Me),1.27 (1H, m, H-6),1.25 (1H, m, H-5),1.06 (3H, d, J = 6.5 Hz, 4-Me)和0.95 (3H, d, J = 5.9 Hz, 6-Me)。而13C-NMR (150 MHz, DMSO)结合DEPT谱显示只有14个碳信号:δC 166.0 (C-1),126.8 (C-2),147.4 (C-3),30.7 (C-4),37.6 (C-5),35.1 (C-6),74.5 (C-7),24.0 (C-8),149.4 (C-9),122.9 (C-10),151.3 (C-11),12.7 (2-Me),21.1 (4-Me)和16.2 (6-Me),说明这个化合物可能是一个具有对称结构的二聚体,通过与文献[15]中化合物conglobatin A对比后发现两者波谱数据完全吻合,故最终确定为conglobatin A。
-
自上世纪发现青霉素以来,微生物中活性次生代谢产物一直是药物先导化合物的重要来源之一,据统计1940年—2019年间,科学家从微生物中开发出293种治疗不同疾病的临床药物[16]。但随着研究的深入,很多微生物及其次生代谢产物存在被重复开发和提取分离的问题,加之多重耐药性的产生,迫使人们需要开拓新的制造药物的微生物来源[5-6],而其中极地微生物资源是珍贵而特殊的。来自极地海洋等特殊生态环境的生物往往具有比陆地生物更为丰富的代谢途径和功能基因簇,增加了产生结构新颖且功能独特的次生代谢物的可能性。极地生物以微生物和一些能适应极端条件的海洋生物为主,然而与已报道的大量极地微生物相比,鲜有微生物活性天然产物相关研究报道,因此,极地微生物极具研究价值[17-18]。
笔者以一株采自北极海域海绵共附生放线菌Streptomyces sp. LHW11-07为研究对象,从其发酵浸膏中分离得到9个单体化合物1~9,包括环二肽化合物1~5,倍半萜化合物6,核苷类化合物7,以及两个其他结构类型化合物8和9,其中化合物1和2是首次分离于Streptomyces放线菌,而这些化合物的生物活性还有待进一步探究;本研究进一步丰富了该属放线菌的化学多样性,同时,为高值化开发利用极地微生物这一国家战略资源提供了物质基础和理论依据。
据文献报道,化合物1对所测试的病原性细菌和真菌均具有一定的对抗作用[19],化合物2测试了4种肿瘤细胞均无明显的细胞毒性[20],化合物3对海胆Strongylocentrotus intermedius胚胎具有细胞毒活性[9],化合物5具有抗炎活性并对H1N1和RSV病毒有一定的杀伤作用[21],化合物7作为一种内源性嘌呤核苷,具有降低血压、抑制血小板聚焦、舒张血管、减慢心律等生理活性[22],而化合物9可抑制癌细胞株的增殖,在体外对Trypanosoma brucei brucei GUTat 3.1表现出抗锥虫体活性等[23]。
Study on the secondary metabolites from a polar marine sponge associated actinomyces Streptomyces sp. LHW11-07
-
摘要:
目的 对极地海绵共附生放线菌Streptomyces sp. LHW11-07进行次生代谢产物的研究,以期得到结构新颖且具有良好生物活性的小分子化合物。 方法 综合运用凝胶柱色谱、硅胶柱色谱、反相中压柱色谱和高效液相色谱等分离手段对Streptomyces sp. LHW11-07发酵产物进行分离和纯化,采用质谱、一维、二维核磁共振等现代波谱方法并结合相关文献调研鉴定它们的结构。 结果 从该菌的发酵产物中共分离得到9个单体化合物,分别为cyclo-(L-Tyr-L-Trp) ( 1 )、cyclo-(L-Trp-L-Ser) ( 2 )、cyclo-(D-Tyr-D-Pro) ( 3 )、cyclo-(L-Tyr-L-Phe) ( 4 )、cyclo-(L-Tyr-L-Leu) ( 5 )、albaflavenol B ( 6 )、β-adenosine ( 7 )、N-formylantimyic acid methyl ester ( 8 )和conglobatin A ( 9 )。 结论 化合物 1 和 2 是首次分离于Streptomyces属放线菌。 Abstract:Objective In order to obtain small molecule compounds with novel structure and good biological activity, the secondary metabolites of polar sponge-symbiotic Streptomyces sp. LHW11-07 were studied. Methods The fermentation product of Streptomyces sp. LHW11-07 was isolated and purified by gel column chromatography, silica gel column chromatography, reversed-phase medium pressure column chromatography and high performance liquid chromatography. The structures of the monomeric compound were identified by modern spectroscopic methods such as mass spectrometry, nuclear magnetic resonance and related literature reports. Results A total of nine compounds were isolated from the fermentation of this strain, which were cyclo-(L-Tyr-L-Trp) ( 1 ), cyclo-(L-Trp-L-Ser) ( 2 ), cyclo-(D-Tyr-D-Pro) ( 3 ), cyclo-(L-Tyr-L-Phe) ( 4 ), cyclo-(L-Tyr-L-Leu) ( 5 ), albaflavenol B ( 6 ), β-adenosine ( 7 ), N-formylantimyic acid methyl ester ( 8 ) and conglobatin A ( 9 ). Conclusion Compounds 1 and 2 were isolated from Streptomyces sp. for the first time. -
Key words:
- polar region /
- sponge /
- actinomyces /
- secondary metabolite
-
高原是指海拔高于2 500 m能够引起机体产生明显生物学效应的地区[1]。高原低氧环境会影响机体的生理功能与药物疗效的发挥[2]。高原地区高血压患病率显著高于平原地区,高血压是高原地区最常见的慢性疾病和心血管疾病的严重危险因素。临床上最常使用钙通道阻滞剂类降压药(CCB)[3],硝苯地平是治疗高血压的一线用药,通过阻断血管平滑肌细胞上的钙通道从而扩张血管降低血压,同时阻断心肌细胞L型钙通道从而减慢心率[4]。本课题组前期研究表明,急进高原后大鼠体内硝苯地平的药动学参数会发生显著变化[5]。由于高原低氧环境导致药物的药动学参数改变,体内血药浓度可能达不到有效治疗浓度,从而影响硝苯地平降压效果,但目前有关硝苯地平对高原高血压人群的疗效研究尚未见报道。本研究首次报道高原低氧环境下硝苯地平控释片对高血压患者降压作用的临床疗效及安全性评价,从而为高原高血压人群提供有效治疗方案,为临床合理用药提供参考。
1. 材料与方法
1.1 病例选择
研究对象为2020年2月至2021年2月于中国人民解放军联勤保障部队第九四〇医院及玉树八一医院诊治的共84例高血压患者。本研究经第九四〇医院伦理委员会批准,审批编号为2019KYLL068。
1.1.1 诊断与入选标准
①符合《中国高血压防治指南》中关于高血压的诊断标准[6],即非同日3次所测量的诊室血压:收缩压(SBP)≥140 mmHg和(或)舒张压(DBP)≥90 mmHg的患者;②高原高血压患者为久居高原1年及以上者,平原高血压患者为久居平原1年及以上者,两组患者近1个月内未服用降压药物;③入院后连续每日晨起服用硝苯地平控释片30 mg,连续6 d达到稳态血药浓度者;④年龄40~85岁。
1.1.2 排除标准
①继发性高血压或临床诊断为病危者;②伴发有严重心脑血管疾病者。③肝功能异常者,丙氨酸氨基转移酶(ALT)或天冬氨酸氨基转移酶(AST)超过上限1.5倍者;④肾功能异常者或存在影响肾功能的急性因素者。
1.2 药品
硝苯地平控释片,规格:30 mg/片,批号:IX20200382,批准文号:国药准字J20180025,德国Bayer AG公司生产。
1.3 分组与治疗方法
将42例第九四〇医院高血压住院患者(海拔1 500 m)设为平原高血压组,42例八一医院高血压住院患者(海拔3 800 m)设为高原高血压组。两组患者均给予硝苯地平控释片每日晨起口服30 mg,连续6 d。
1.4 观察指标与疗效判定
根据我国总结和规定的降压药临床研究指导原则:将血压作为药效评价的主要指标,将记录的平原与高原组血压值,按照疗效标准等级:显效、有效、无效进行评价。考察相同剂量下,高原低氧环境对硝苯地平降压疗效的影响。监测平原高血压组和高原高血压组患者按照每日晨起口服30 mg硝苯地平控释片连续6 d的血压值,包括每天清晨、服药前及临睡前3个时段的SBP和DBP。具体操作为:在患者平躺情况下,对每个时间段的每次血压均测定3次,计算出平均值。疗效判定按文献[7-8]的方法对3个时间段的血压进行评价,分为显效、有效和无效。显效:SBP下降幅度≥10 mmHg并降至正常或SBP未达正常但下降幅度≥20 mmHg;有效:SBP下降1~10 mmHg并降至正常或SBP未降至正常但下降10~19 mmHg;无效:未达到上述标准。对总有效率(总有效率=显效率+有效率)进行统计学比较,以判定疗效。
此外,临床研究显示,较快的心率会显著增加高血压患者心血管事件和病死率[9-11]。依据专家建议,高血压患者应首先控制血压达标,在降压治疗的同时注重心率管理[12]。硝苯地平控释片具有反射性刺激交感神经激活的作用,可能导致心率加快引起心悸等不良反应。根据国内外指南和专家共识,在测定血压时一并测得心率,详细记录清晨、服药前、临睡前的心率。
1.5 统计学处理
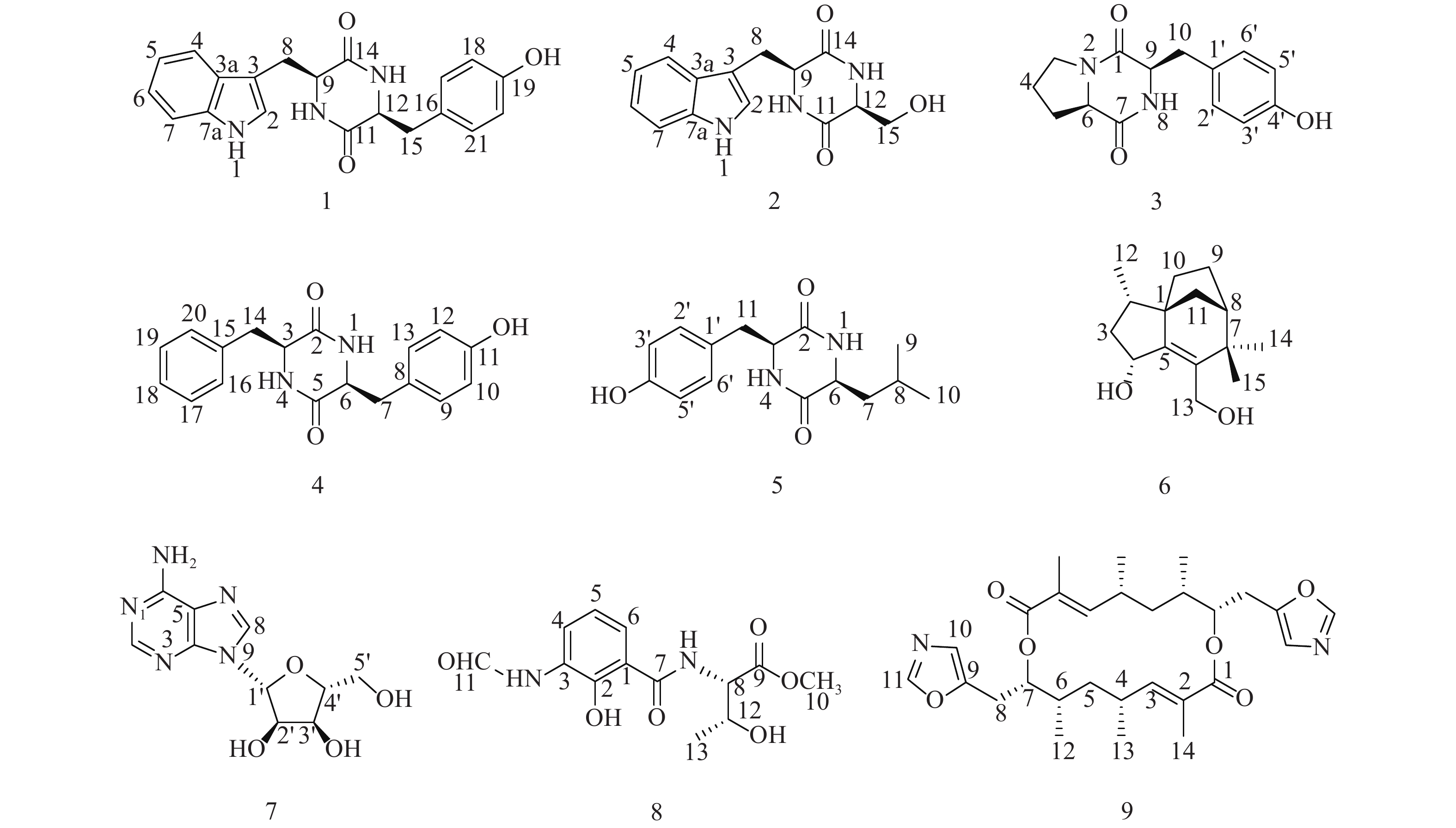
用SPSS Statistics 21进行统计分析。计量资料用
$ \bar x \pm s $ 表示,组间比较用独立样本t检验,组内比较用卡方检验;计数资料用率表示,比较用卡方检验。2. 结果
2.1 一般资料
调查内容包括一般人口学资料、身高、体重、BMI、ALT、AST、Cr等。平原高血压组及高原高血压组的AST、ALT、Cr值均符合纳入排除标准,患者伴发疾病及合并用药较少。两组患者的一般资料比较,差异均无统计学意义(P>0.05),组间具有可比性,见表1。
表 1 平原高血压组和高原高血压组患者的一般资料比较($ \bar x \pm s $ ,n=42)项目 平原高血压组 高原高血压组 性别(男/女) 30/12 22/20 年龄 61.24±8.02 60.19±9.28 身高(l/cm) 168.79±9.09 168.31±6.45 体重(m/kg) 69.30±10.64 67.29±7.36 BMI (kg/m2) 24.23±2.45 23.80±2.54 AST(U/L) 21.31±8.87 25.14±9.77 ALT(U/L) 27.14±16.90 28.38±15.37 Cr(μmol/L) 74.93±17.33 76.17±19.79 2.2 高原及平原高血压人群血压值统计
依据临床血压监测指导原则,测定了3个不同时间段的血压值,分别为清晨、用药前及临睡前的血压。治疗前,高原高血压组的清晨DBP、服药前及临睡前的SBP和DBP均显著高于平原高血压组,且高原组舒张压升高更为显著。连续用药6 d后,平原高血压组的清晨、服药前及临睡前SBP均显著低于治疗前(P<0.01)。高原高血压组治疗前后的各时间段SBP和DBP均显著高于平原高血压组,差异均有统计学意义(P<0.05),但高原组治疗后与治疗前相比无显著性差异,且血压未降至正常,可见高原高血压组服用硝苯地平在6 d内的降血压疗效比平原高血压组差,详见表2。
表 2 平原高血压组和高原高血压组不同时段血压值比较(mmHg,$ \bar x \pm s $ ,n=42)组别 检测时间 SBP DBP 清晨 服药前 临睡前 清晨 服药前 临睡前 平原高血压组 治疗前 151.14±15.70 146.90±10.45 148.93±12.39 89.43±13.11 87.48±10.30 89.62±11.60 治疗后 138.86±14.66## 137.93±14.44# 137.95±17.82# 86.90±12.52 86.05±14.06 85.05±12.70 高原高血压组 治疗前 154.55±12.29 153.38±11.66** 154.60±11.98* 104.67±17.18*** 106.86±15.09*** 106.64±14.18*** 治疗后 148.93±19.76* 148.55±19.28** 149.10±20.00** 100.07±16.11*** 102.19±16.60*** 101.86±15.89*** *P<0.05, **P<0.01, ***P<0.001,与平原高血压组比较;#P<0.05,##P<0.01,与治疗前比较。 采用配对样本t检验判断硝苯地平治疗前后对平原高血压组和高原高血压组患者血压的影响,表3结果显示,平原高血压组治疗前后的清晨、服药前及临睡前SBP、临睡前DBP有统计学差异,高原高血压组治疗前后各时间段的SBP和DBP无统计学差异。
表 3 平原高血压组和高原高血压组患者治疗前后血压下降值比较(mmHg,$ \bar x \pm s $ ,n=42)组别 SBP下降值 DBP下降值 清晨 服药前 临睡前 清晨 服药前 临睡前 平原高血压组 12.29±17.10*** 8.98±15.40** 10.98±17.70*** 2.52±10.56 1.43±12.36 4.57±10.43** 高原高血压组 5.62±16.72 4.83±19.17 5.50±19.58 4.59±16.94 4.67±17.91 4.78±17.59 **P<0.01, ***P<0.001,与治疗前清晨、服药前、临睡前比较。 2.3 平原高血压组和高原高血压组患者的临床疗效评价
专家建议将研究结束时给药间隔末(谷值时)血压与基线血压的差值作为主要疗效指标[8],本研究中选用服药前时间段的治疗前后血压之差进行疗效评价。高原高血压组和平原高血压组的总有效率分别为47.62%(20例/42例)和76.19%(32例/42例),高原高血压组硝苯地平控释片降压总有效率显著低于平原高血压组(P<0.05),见表4。
表 4 平原高血压组和高原高血压组患者的临床疗效比较[例(%),n=42]组别 显效 有效 无效 总有效率 平原高血压组 24(57.14) 8(19.05) 10(23.81) 32(76.19) 高原高血压组 13(30.95) 7(16.67) 22(52.38) 20(47.62)* *P<0.05,与平原高血压组比较。 两组患者均按照医嘱连续服药,获得81例患者不同时段心率数据。其中,平原高血压组41例,高原高血压组40例。高原高血压组各时间段的心率均显著高于平原高血压组,证实高原低氧环境会导致心率显著上升。连续用药6 d后,平原高血压组的清晨及服药前心率显著低于治疗前(P<0.05),高原高血压组心率有所下降,但无显著性差异(P>0.05),见表5。提示应在降压治疗的同时关注心率管理,以预防心血管事件的发生。
表 5 平原高血压组与高原组患者心率指标比较($ \bar x \pm s $ )组别 治疗前 治疗后 清晨 服药前 临睡前 清晨 服药前 临睡前 平原高血压组 109.51±17.46 110.37±17.90 109.85±17.62 100.46±21.13# 101.46±21.88# 101.39±21.42 高原高血压组 119.03±13.96** 119.70±14.64* 119.43±14.05** 113.65±20.22** 113.18±19.56* 114.55±19.55** *P<0.05,**P<0.01,与平原高血压组比较;#P<0.05,与治疗前比较。 2.4 安全性评价
在试验过程中,平原高血压组5例患者发生心动过速、心悸的症状,高原高血压组6例患者发生心动过速、心悸的症状。两组患者的药物不良反应发生率分别为11.90%和14.29%,差异无统计学意义(P>0.05)。
3. 讨论
本研究结果表明,高原高血压组的血压和心率值均显著高于平原高血压组,且高原高血压组血压控制不良、心率管理不佳,高原高血压患者服用与平原高血压患者同剂量的硝苯地平控释片未能有效地控制短期内血压。高原地区硝苯地平用药剂量应高于平原剂量,因此有必要建议《中国高血压防治指南》可增加一项高原地区高血压人群用药剂量。以增加药物在机体内的血药浓度,从而长期有效控制血压,与此同时需做好高血压患者服药前后血压的监测及患者安全用药教育,减少药物不良反应的发生,从而提高高原地区用药的合理性、安全性及有效性。
高原合理用药展望,目前,高原地区的合理用药指导有待提高,原因有以下几点:①地域偏远、文化差异及经济欠发达导致高原地区医护人员的合理用药意识存在局限性。此外,高原地区高血压的患病率高于全国平均水平,但患者的知晓率、治疗率和控制率明显偏低[13]。②高血压是心血管系统中最常见的慢性疾病,可诱发许多并发症,高血压严重危害高原地区人群的生命健康,降低血压可随之降低心血管疾病并发率,改善预后[14-15],但高原地区患者服药的依从性差,不能长期遵医嘱服药,导致血压控制不佳,增加心血管疾病患病风险。③高原低氧环境会改变药物药动学参数从而影响药物疗效,但高原地区人体的药动学研究少有报道。从事高原合理用药研究的相关人员较少,高原人群的特殊用药至今未列入研究的议事日程。高原低氧环境导致药动学改变从而导致药效的差异是个体化合理用药中必须考虑的问题。综上,针对高原地区沿用平原临床用药方案的问题亟需解决,应着重研究高原与平原地区合理用药的临床疗效差异,发布高原地区合理用药指南,培养和提高高原地区医护人员合理用药意识,提高患者对疾病的知晓率、治疗率和控制率,提高患者用药依从性。
-
[1] ABDELMOHSEN U R, BAYER K, HENTSCHEL U. Diversity, abundance and natural products of marine sponge-associated actinomycetes[J]. Nat Prod Rep,2014,31(3):381-399. doi: 10.1039/C3NP70111E [2] PIMENTEL-ELARDO S M, KOZYTSKA S, BUGNI T S, et al. Anti-parasitic compounds from Streptomyces sp. strains isolated from Mediterranean sponges[J]. Mar Drugs,2010,8(2):373-380. doi: 10.3390/md8020373 [3] MAYER A M, HAMANN M T. Marine pharmacology in 2001: 2002: marine compounds with anthelmintic, antibacterial, anticoagulant, antidiabetic, antifungal, anti-inflammatory, antimalarial, antiplatelet, antiprotozoal, antituberculosis, and antiviral activities; affecting the cardiovascular, immune and nervous systems and other miscellaneous mechanisms of action[J]. Comp Biochem Physiol C Toxicol Pharmacol,2005,140(3-4):265-286. doi: 10.1016/j.cca.2005.04.004 [4] ABDELMOHSEN U R, SZESNY M, OTHMAN E M, et al. Antioxidant and anti-protease activities of diazepinomicin from the sponge-associated Micromonospora strain RV115[J]. Mar Drugs,2012,10(10):2208-2221. [5] ROTHSCHILD L J, MANCINELLI R L. Life in extreme environments[J]. Nature,2001,409(6823):1092-1101. doi: 10.1038/35059215 [6] WILSON Z E, BRIMBLE M A. Molecules derived from the extremes of life[J]. Nat Prod Rep,2009,26(1):44-71. doi: 10.1039/B800164M [7] LIU J, YU H L, LI S M. Expanding tryptophan-containing cyclodipeptide synthase spectrum by identification of nine members from Streptomyces strains[J]. Appl Microbiol Biotechnol,2018,102(10):4435-4444. doi: 10.1007/s00253-018-8908-6 [8] HAN W R, CAI J, ZHONG W M, et al. Protein tyrosine phosphatase 1B (PTP1B) inhibitors from the deep-sea fungus Penicillium chrysogenum SCSIO 07007[J]. Bioorg Chem,2020,96:103646. doi: 10.1016/j.bioorg.2020.103646 [9] SOBOLEVSKAYA M P, DENISENKO V A, FOTSO S, et al. Biologically active metabolites of the actinobacterium Streptomyces sp. GW 33/1593[J]. Russ Chem Bull,2008,57(3):665-668. doi: 10.1007/s11172-008-0105-9 [10] WEI H X, FANG X W, XIE X S, et al. Secondary metabolites of a soil-derived Streptomyces kunmingensis[J]. Chem Nat Compd,2017,53(4):794-796. doi: 10.1007/s10600-017-2125-x [11] SONG M M, XIE Y H, CHEN W H, et al. Diketopiperazine and enterotoxin analogues from the mangrove derived-soil Streptomyces sp. SCSIO 41400 and their biological evaluation[J]. Nat Prod Res,2022,36(5):1197-1204. doi: 10.1080/14786419.2020.1864632 [12] RAJU R, GROMYKO O, FEDORENKO V, et al. Albaflavenol B, a new sesquiterpene isolated from the terrestrial actinomycete, Streptomyces sp[J]. J Antibiot (Tokyo),2015,68(4):286-288. doi: 10.1038/ja.2014.138 [13] MOHAMED N M, AHMED M A M, KHAN S I, et al. Anti-inflammatory and cytotoxic specialised metabolites from the leaves of Glandularia × hybrida[J]. Phytochemistry,2022,195:113054. doi: 10.1016/j.phytochem.2021.113054 [14] ISHIBASHI M, TAMAI Y, TOUME K, et al. Griseoviridin and cyclic hydroxamates found in a screening program for Wnt signal inhibitor[J]. HETEROCYCLES,2012,86(2):1517. doi: 10.3987/COM-12-S(N)64 [15] WESTLEY J W, LIU C M, EVANS R H, et al. Conglobatin, a novel macrolide dilactone from Streptomyces conglobatus ATCC 31005[J]. J Antibiot (Tokyo),1979,32(9):874-877. doi: 10.7164/antibiotics.32.874 [16] 鞠建华, 杨镇业, 李青连, 等. 微生物药物研究开发现状与思考[J]. 山东大学学报(医学版), 2021, 59(9):43-50,63. [17] LIU J T, LU X L, LIU X Y, et al. Bioactive natural products from the Antarctic and Arctic organisms[J]. Mini Rev Med Chem,2013,13(4):617-626. doi: 10.2174/1389557511313040013 [18] FRIEDMANN E I. Extreme environments and exobiology[J]. Plant Biosyst,1993,127(3):369-376. [19] KUMAR S N, MOHANDAS C, NAMBISAN B. Purification, structural elucidation and bioactivity of tryptophan containing diketopiperazines, from Comamonas testosteroni associated with a rhabditid entomopathogenic nematode against major human-pathogenic bacteria[J]. Peptides,2014,53:48-58. doi: 10.1016/j.peptides.2013.09.019 [20] WANG F Z, HUANG Z, SHI X F, et al. Cytotoxic indole diketopiperazines from the deep sea-derived fungus Acrostalagmus luteoalbus SCSIO F457[J]. Bioorg Med Chem Lett,2012,22(23):7265-7267. doi: 10.1016/j.bmcl.2012.08.115 [21] ZHAO L, LI W, DAI S J, et al. Alkaloids bearing rare skeletons from Forsythia suspensa with anti-inflammatory and anti-viral activities in vitro[J]. Phytochemistry,2021,186:112739. doi: 10.1016/j.phytochem.2021.112739 [22] 赵京林, 杨跃进. 腺苷与心脏保护的研究进展[J]. 中国心血管病研究杂志, 2004(8):658-661. [23] LACEY H J, BOOTH T J, VUONG D, et al. Conglobatins B-E: cytotoxic analogues of the C2-symmetric macrodiolide conglobatin[J]. J Antibiot (Tokyo),2020,73(11):756-765. doi: 10.1038/s41429-020-0332-3 -





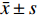

 下载:
下载:



 下载:
下载:


