-
对各种药品生产相关的数据进行统计分析,可以有效地对药品质量进行宏观控制。能力六合图是质量控制图中的一种,“六合图”包含单值控制图、极差控制图、最后25个观测值、能力直方图、正态概率图及能力图。Minitab软件能力分析的“六合图”,能对数据进行自动分析、对过程稳定性和过程能力进行综合评估[1],通过判定一个过程的过程能力绩效,起到对生产过程的改进与提高作用。此方法快速准确,是制药行业实施新版GMP时进行产品质量回顾的有效工具,也是提升质量管理水平的较好途径。
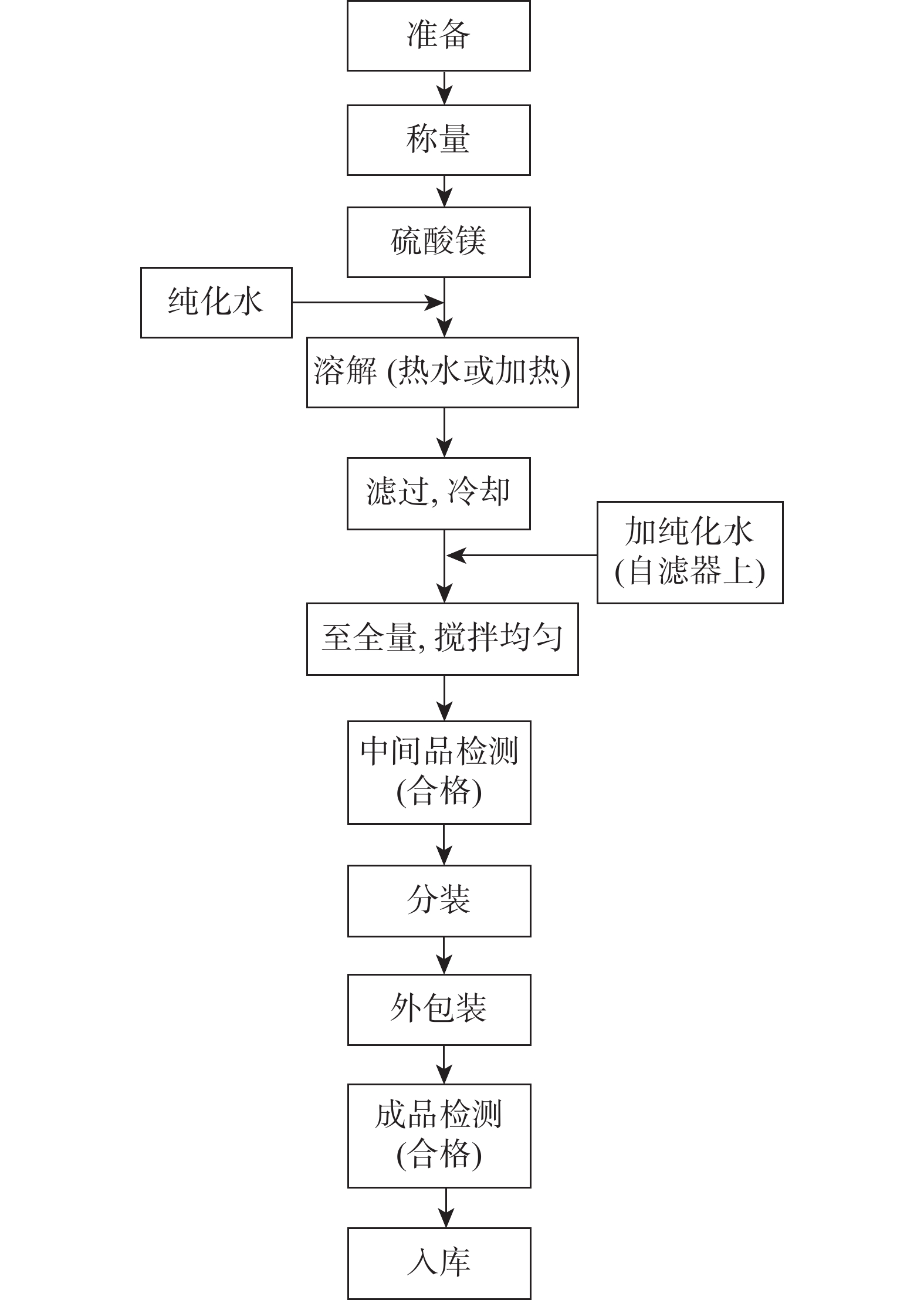
硫酸镁口服溶液为我院院内制剂,临床上主要用于利胆、导泻。硫酸镁口服溶液生产工艺流程图见图1。通过能力六合图分析27批次硫酸镁口服溶液中硫酸镁含量的质量数据,判断在生产过程中对硫酸镁含量是否达到控制状态、硫酸镁口服溶液的生产工艺是否处于稳定状态。
-
查阅我院2015年2月至2020年1月生产的硫酸镁口服溶液的工艺规程、主要生产设备的标准操作规程、检验操作规程和记录等文件,确定药品是在同一生产工艺及同一检验环境下完成,生产记录和检验结果真实可靠。统计2015年2月至2020年1月我院生产的连续27批次硫酸镁口服溶液的检验结果,分析项目包括:性状、鉴别、装量、微生物限度、硫酸镁含量[2-3]。
-
根据《中国人民解放军医疗机构制剂规范》(2015年版)中硫酸镁口服溶液的质量标准,对27批次的硫酸镁口服溶液进行质量考察。硫酸镁口服溶液质量标准见表1。其中,性状、鉴别、装量和微生物限度等检查项目依据标准直接进行判定,硫酸镁含量使用Minitab软件的六合图功能进行分析[4]。
表 1 硫酸镁口服溶液质量标准
项目名称 标准 性状 无色、澄清液体,味苦、咸 镁盐、硫酸盐 阳性、阳性 装量 ≥97%的标示量 微生物限度 菌数≤100 cfu/ml,不得检出大肠杆菌 硫酸镁含量 标示量的95.0%~105.0% -
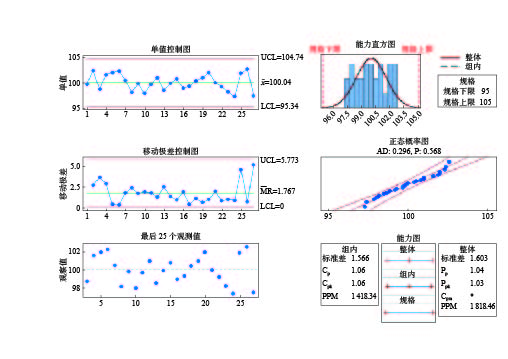
2015年2月至2020年1月生产的27批次硫酸镁口服溶液的性状、鉴别、装量、微生物限度均合格,各批次硫酸镁含量结果汇总见表2。打开Minitab软件,输入数据,硫酸镁口服溶液中硫酸镁含量的能力六合图见图2。
表 2 27批次硫酸镁口服溶液含量的检验结果(2015年2月至2020年1月)
序号 批号 含量
(%)序号 批号 含量
(%)序号 批号 含量
(%)1 150203 99.7 10 161219 97.9 19 180507 101.0 2 150616 102.4 11 170316 99.7 20 181129 102.0 3 150824 98.7 12 170515 101.0 21 190226 100.0 4 151030 101.6 13 170629 98.5 22 190506 99.2 5 151224 102.0 14 170925 99.9 23 190624 98.2 6 160411 102.3 15 171113 100.8 24 190628 97.3 7 160614 100.5 16 180119 98.9 25 191101 101.9 8 160808 98.1 17 180307 99.3 26 200106 102.6 9 161017 99.8 18 180402 100.4 27 200111 97.4 -
Minitab软件依据统计理论的小概率事件原理,对控制图有8项检验标准[4-5]:①超出上下控制界限;②连续9点落在中心线同一侧;③连续6点递增或递减;④连续14点上下交错;⑤连续3点中有2个点距离中心线(同侧)大于2个标准差;⑥连续5点中有4个点距离中心线(同侧)大于1个标准差;⑦连续15点在距离中心线(任意一侧)1个标准差之内;⑧连续8点距离中心线(任一侧)大于1个标准差。以上8项检验标准的意义在于:①是公认的、用于检测失控情况的必要检验;②可以标识过程居中或变异中的偏移,可创建一个敏感度更高的控制图;③用于检测趋势;④可检测系统变异;⑤和⑥用于检测过程中的较小偏移;⑦可检测是否存在控制限过宽的现象;⑧检测混合模式。在混合模式中,这些点趋于避开中心线,而落在控制限附近。
为了使硫酸镁含量的控制图敏感度更高,我们选择对其进行8项检验。由图2知,硫酸镁含量的移动极差控制图、单值控制图上所有的点在控制限内随机分布,进行8项检验亦无异常值,说明该组数据处于控制状态,即硫酸镁口服溶液中硫酸镁含量处于受控状态。
-
由图2知,硫酸镁含量的最后25个观测值显示数据波动在正常范围内,能力直方图显示工艺过程受控,正态概率图显示数据分布密集且呈正态分布(P>0.05)。
-
能力图用于计算工序能力指数(Cpk)。传统统计控制理论将工序能力分为5级[6]:①Cpk≥1.67,工序能力过剩;②1.33<Cpk<1.67,一般加工工序能力富裕,可维持现状;③1<Cpk≤1.33,工序能力尚可,但有缺陷发生;④0.67<Cpk≤1,工序能力不足;⑤Cpk≤0.67,工序能力严重不足,需采取紧急措施。
硫酸镁含量的能力六合图显示Cpk为1.06,工序能力尚可,但提示有缺陷发生。在该能力指数下,单值图的上下控制线分别为95.34和104.74,几乎和规格线95、105重叠,因此,该控制限起不到控制的作用,只能用于分析用。
-
应用Minitab软件制作的硫酸镁含量的能力六合图显示,在硫酸镁口服溶液生产过程中对硫酸镁成分达到控制状态,硫酸镁口服溶液的生产工艺处于受控状态,但能力图同时也提示了该品种的工艺过程有潜在缺陷发生。
-
由于该产品的数据收集时间跨度长,潜在异常原因分析难度大,如果仅依靠经验判断,难以提出有针对性的预防措施。基于风险管理理念,我们需要系统地识别、查找潜在风险来源,做好质量风险的前瞻性管理。在本制剂室现有的风险管理程序下,我们采用失败模式和效应分析(FMEA)为本次风险管理工具[7],对风险的严重程度(S)、发生概率(O)以及风险被检测的可能性(D)评分,评分实行5分制[8-10],建立的风险评估表见表3。风险指数(RPN)=严重程度(S)×发生概率(O)×风险被检测的可能性(D),风险指数下的风险级别见表4。采用头脑风暴法列出可能发生硫酸镁含量偏差的因素,最后确定潜在的失效模式与潜在风险因素,并对风险进行分析分级,结果见表5。
表 3 风险评估表
严重程度(S) 发生概率(O) 可检测性(D) 评分 严重危害:直接影响产品质量,导致产品不可使用 极高:每批次发生或每年发生3批次以上 不能或极小 5 高:影响产品质量,导致产品质量不可控 高:每年发生1批次 可能性较低 4 中等:间接影响产品质量,导致产品质量可控但不稳定 中等:每3年发生1批次 中等可能性 3 低:较小影响产品质量,导致产品质量可控,较少出现不稳定 低:每5年发生1批次 可能性较大 2 微小:不影响产品质量 微小:几乎不发生 可能性非常大或几乎肯定能 1 表 4 风险级别表
风险指数 风险级别 评估 ≤25 低 可接受 26≤RPN≤59 中 考虑改进措施 ≥60 高 不可接受,需要整改 表 5 硫酸镁含量偏差风险因素分级结果
风险项目 失效模式 严重程度(S) 发生几率(O) 可检测性(D) RPN 风险等级 失败影响 评分 失败原因 评分 现有控制措施 评分 人员 配制、检验岗位人员岗位职责不熟悉、操作失误 不能准确称量投药量、准确测定含量 5 岗位职责不明确、管理规程指导性差、操作规程不切实际、人员培训未到位 3 岗位职责、管理规程、操作规程等文件齐全;定期进行各项操作培训,每年度进行各项考核。 2 30 中 原辅料 原辅料质量不合格 原辅料硫酸镁含量不合格或杂质超标,导致产品质量不可控 5 未按照入库规程进行原辅料入库;原辅料库环境不符合要求 1 原辅料入库实行双人验收,且药检人员对原辅料进行抽检。原辅料库每天监测温湿度并有防虫防霉措施 2 10 低 设备 天平未定期及时校准 硫酸镁含量可控但不稳定 3 设备管理人员因各种原因未及时进行天平校准 3 设备管理人员职责规定必须及时校验设备;天平侧部贴有校准结果和时效 1 9 低 方法 含量测定方法未验证 含量测定结果不准确,导致产品质量不可控 4 相关法规变更、检测方法变更、首次使用未验证 3 制订了相关岗位职责和操作规程 2 24 低 根据硫酸镁含量偏差风险因素分级结果,人员是硫酸镁口服溶液中硫酸镁含量偏差风险控制的关键。对此,我们进行如下改进措施:重新审核岗位职责、管理规程及操作规程等文件,由岗位人员、管理人员共同参与修订,增强文件的可操作性;人员培训时:理论培训需结合实际案例进行,同时注重现场操作的讲解且讲解结束后需进行全员实际技能操作,培训考核以笔试和实际操作相结合,并不定期进行考核,随时保证岗位人员的操作水平和理论知识水平。
-
医院制剂的很多品种为小批量、经常性生产品种,结合医院制剂的国家政策、制剂本身、医药市场等因素影响,原有的经常性生产品种也可能因为政策变化导致大幅减产[11]。在对医院制剂进行质量分析时,存在医院制剂年生产批次少,难以进行趋势分析的问题。因此,我们采用在年度产品批次少于10批时,对这些批次的生产数据进行罗列,避免因人员更替等原因导致数据丢失,同时可确保产品年度质量回顾工作的开展。但该阶段只确认年度该产品所有质量数据未超出标准范围,不进行趋势分析。当10≤批次<25时,采用单值-移动极差控制图(I-MR控制图)对数据进行分析[12-13],此时,对比第一阶段单纯的罗列数据,控制图可以直接反映单值、控制限、规格限、移动极差的分布,以及数据是否存在异常波动,可反映生产过程的大概趋势及稳定程度,判断过程是否受控。当数据足够多,即能收集25批次以上数据时,用Minitab软件中六合图对数据进行分析,除了可以有效观测到第二阶段情况外,还可考察样本正态分布情况,观察数据波动情况,以及从能力图中获得Cpk和工序性能指数(Ppk)等相关数据,为科学的评价工艺、流程的稳定性和可靠性提供数据支持。
常规控制图按用途可分为分析用控制图和控制用控制图。前者用来控制生产过程中有关质量特性值的变化情况,判断工序是否处于受控状态,后者主要用于发现生产过程是否有异常情况出现,以防不合格品产生。实际工作中,当数据积累足够多时,若与产品生产相关的各项因素没有发生变更,且控制图性能良好,绘制出的控制图就可用于生产过程的控制。在本文中,我们所绘制的控制图因控制限与规格线几乎重叠,且过程能力指数较低,只能用于分析用而不能转化成控制用控制图。
我们通过将能力六合图应用于医院制剂硫酸镁口服溶液的质量分析,发现虽然硫酸镁口服溶液的生产工艺处于受控状态,但存在潜在缺陷。基于风险管理理念,采用FMEA进行风险的前瞻性管理,并针对风险等级提出改进措施。但风险管理是一个持续、动态的过程,该改进措施能否有效控制风险还需进行一段时间的验证。只有风险得到有效控制,风险管理能力不断提高,才能使硫酸镁口服溶液的生产工艺更稳定,质量更优异。
Application of capability sixpack in quality analysis of hospital preparation magnesium sulfate oral solution
-
摘要:
目的 应用能力六合图对医院制剂硫酸镁口服溶液进行质量分析。 方法 运用Minitab软件中能力分析的“六合图”功能,以硫酸镁口服溶液的硫酸镁含量为指标,判断生产过程中硫酸镁含量是否达到控制状态,硫酸镁口服溶液的生产工艺是否稳定。 结果 硫酸镁含量及硫酸镁口服溶液的生产工艺处于受控状态,但存在潜在缺点。基于风险管理理念,应用失败模式和效应分析(FMEA)进行了潜在风险的前瞻性管理。 结论 应用能力六合图于医院制剂硫酸镁口服溶液的质量分析,有助于我们发现生产工艺受控状态下的潜在风险,有利于制剂生产过程的改进以及制剂质量的保证。 Abstract:Objective To analyze the quality of the hospital preparation magnesium sulfate oral solution by using capability sixpack. Methods By using the capability sixpack of Minitab, the content of magnesium sulfate in the magnesium sulfate oral solution was used as an indicator to determine whether the magnesium sulfate composition reached a controlled state during the production process and whether the production process of magnesium sulfate oral solution was stable. Results The content of magnesium sulfate and the production process of magnesium sulfate oral solution was under control, but there were potential disadvantages. Based on the concept of risk management philosophy, The failure model and effect analysis (FMEA) were applied to the prospective management of potential risks. Conclusion The application of the capability sixpack in the quality analysis of the hospital preparation of magnesium sulfate oral solution is helpful for us to discover the potential risks under the controlled state of the production process, which is beneficial to the improvement of the preparation production process and the assurance of the quality of the preparation. -
表 1 硫酸镁口服溶液质量标准
项目名称 标准 性状 无色、澄清液体,味苦、咸 镁盐、硫酸盐 阳性、阳性 装量 ≥97%的标示量 微生物限度 菌数≤100 cfu/ml,不得检出大肠杆菌 硫酸镁含量 标示量的95.0%~105.0% 表 2 27批次硫酸镁口服溶液含量的检验结果(2015年2月至2020年1月)
序号 批号 含量
(%)序号 批号 含量
(%)序号 批号 含量
(%)1 150203 99.7 10 161219 97.9 19 180507 101.0 2 150616 102.4 11 170316 99.7 20 181129 102.0 3 150824 98.7 12 170515 101.0 21 190226 100.0 4 151030 101.6 13 170629 98.5 22 190506 99.2 5 151224 102.0 14 170925 99.9 23 190624 98.2 6 160411 102.3 15 171113 100.8 24 190628 97.3 7 160614 100.5 16 180119 98.9 25 191101 101.9 8 160808 98.1 17 180307 99.3 26 200106 102.6 9 161017 99.8 18 180402 100.4 27 200111 97.4 表 3 风险评估表
严重程度(S) 发生概率(O) 可检测性(D) 评分 严重危害:直接影响产品质量,导致产品不可使用 极高:每批次发生或每年发生3批次以上 不能或极小 5 高:影响产品质量,导致产品质量不可控 高:每年发生1批次 可能性较低 4 中等:间接影响产品质量,导致产品质量可控但不稳定 中等:每3年发生1批次 中等可能性 3 低:较小影响产品质量,导致产品质量可控,较少出现不稳定 低:每5年发生1批次 可能性较大 2 微小:不影响产品质量 微小:几乎不发生 可能性非常大或几乎肯定能 1 表 4 风险级别表
风险指数 风险级别 评估 ≤25 低 可接受 26≤RPN≤59 中 考虑改进措施 ≥60 高 不可接受,需要整改 表 5 硫酸镁含量偏差风险因素分级结果
风险项目 失效模式 严重程度(S) 发生几率(O) 可检测性(D) RPN 风险等级 失败影响 评分 失败原因 评分 现有控制措施 评分 人员 配制、检验岗位人员岗位职责不熟悉、操作失误 不能准确称量投药量、准确测定含量 5 岗位职责不明确、管理规程指导性差、操作规程不切实际、人员培训未到位 3 岗位职责、管理规程、操作规程等文件齐全;定期进行各项操作培训,每年度进行各项考核。 2 30 中 原辅料 原辅料质量不合格 原辅料硫酸镁含量不合格或杂质超标,导致产品质量不可控 5 未按照入库规程进行原辅料入库;原辅料库环境不符合要求 1 原辅料入库实行双人验收,且药检人员对原辅料进行抽检。原辅料库每天监测温湿度并有防虫防霉措施 2 10 低 设备 天平未定期及时校准 硫酸镁含量可控但不稳定 3 设备管理人员因各种原因未及时进行天平校准 3 设备管理人员职责规定必须及时校验设备;天平侧部贴有校准结果和时效 1 9 低 方法 含量测定方法未验证 含量测定结果不准确,导致产品质量不可控 4 相关法规变更、检测方法变更、首次使用未验证 3 制订了相关岗位职责和操作规程 2 24 低 -
[1] 季哲, 衣明永. 运用能力六合图优化生产过程绩效[J]. 世界最新医学信息文摘, 2019, 19(19):194. [2] 中国人民解放军总后勤部卫生部. 中国人民解放军医疗机构制剂规范(2002年版)[M]. 北京: 人民军医出版社, 2003: 13. [3] 中央军委后勤保障部卫生局. 中国人民解放军医疗机构制剂规范[M]. 北京: 人民军医出版社, 2016: 334. [4] GITLOWA H S, OPPENHEIM A J, OPPENHEIM R, et al. 质量管理[M]. 张杰, 译. 北京: 机械工业出版社, 2008:95-111. [5] 王春涛, 唐静, 陈伟. Minitab软件在药品生产质量控制中的应用[J]. 中国执业药师, 2012, 9(11):42-46. [6] 贾新章, 李京苑. 统计过程控制与评价—Cpk、SPC和PPM技术[M]. 北京: 电子工业出版社, 2004: 37-39. [7] 翟铁伟. 药品生产中的关键工艺参数确认和控制方法探讨[J]. 化工与医药工程, 2019, 40(3):35-38. [8] 李宵, 任炳楠, 崔赛, 等. 失效模式和效应分析在医院冷链药品风险管理中的应用[J]. 中国医院药学杂志, 2019, 39(21):2216-2221. [9] 乔晓芳, 杨胜亚, 王志超. 药品生产质量风险管理现状分析及改进措施[J]. 化工与医药工程, 2019, 40(2):53-58. [10] 樊蓉, 袁偲偲, 张海莲. 基于失效模式和效应分析的高锰酸钾外用制剂用药错误风险点研究[J]. 药物不良反应杂志, 2019, 21(2):123-128. doi: 10.3760/cma.j.issn.1008-5734.2019.02.009 [11] 陶春, 宋洪涛. 新医改形势下医院制剂的发展思路[J]. 药学实践杂志, 2016, 34(6):574-576. doi: 10.3969/j.issn.1006-0111.2016.06.023 [12] 曹玲, 吴莉, 王玉, 等. 药品检验中常用的统计学方法及其应用[J]. 中南药学, 2019, 17(9):1508-1513. [13] 中华人民共和国国家质量监督检验检疫总局, 中国国家标准化管理委员会. 实验室质量控制 利用统计质量保证和控制图技术 评价分析测量系统的性能: GB/T 27407—2010[S]. 北京: 中国标准出版社, 2011:8. 期刊类型引用(0)
其他类型引用(1)
-





 下载:
下载: