-
市售复方酮康唑乳膏包含酮康唑、硫酸新霉素和丙酸氯倍他索,是治疗浅部真菌感染的常用药物。其中,酮康唑是最常用的抗真菌药物,具有价格低、抗菌谱广、抗真菌活性强等优势。但细菌对硫酸新霉素易产生耐药性,可导致患者反复感染,难以根治,且丙酸氯倍他索不适合12岁以下儿童使用,副作用较多,可产生红斑、灼热、瘙痒等刺激症状,长期大面积用药可导致高血糖等[1-5]。针对上述问题,为改善市售产品的有效性和安全性,本课题组将硫酸新霉素替换为抗菌作用更强的莫匹罗星,将丙酸氯倍他索替换为副作用较少的糠酸莫米松,再结合酮康唑,制备新型复方酮康唑软膏,以提高患者的用药依从性[6-8]。
本研究采用反相高效液相色谱法同时测定复方酮康唑软膏中酮康唑、莫匹罗星和糠酸莫米松3种药效成分的含量,该方法目前未见有文献报道。本法简便,灵敏,分离度好,准确性高,可以为该制剂的质量标准研究提供依据。
-
AL204型电子天平(梅特勒-托利多仪器有限公司);TU-1901型紫外可见分光光度计(北京普析通用仪器有限责任公司);Agilent 1200型高效液相色谱仪(美国Agilent公司);Starter 2C型实验室pH计(奥豪斯仪器有限公司);KQ-800KDE型超声波清洗器(昆山市超声仪器有限公司)。
-
酮康唑对照品(批号:100294-201203,含量99.4%)、莫匹罗星对照品(批号:130568-200501,含量94.2%)、糠酸莫米松对照品(批号:100930-201201,含量99.9%)均购自中国食品药品检定研究院;酮康唑原料药(批号:20130405)、莫匹罗星原料药(批号:20130301)、糠酸莫米松原料药(批号:20130228)均购自武汉鑫佳公司;聚乙二醇400和聚乙二醇3350(中国医药对外贸易公司)。
-
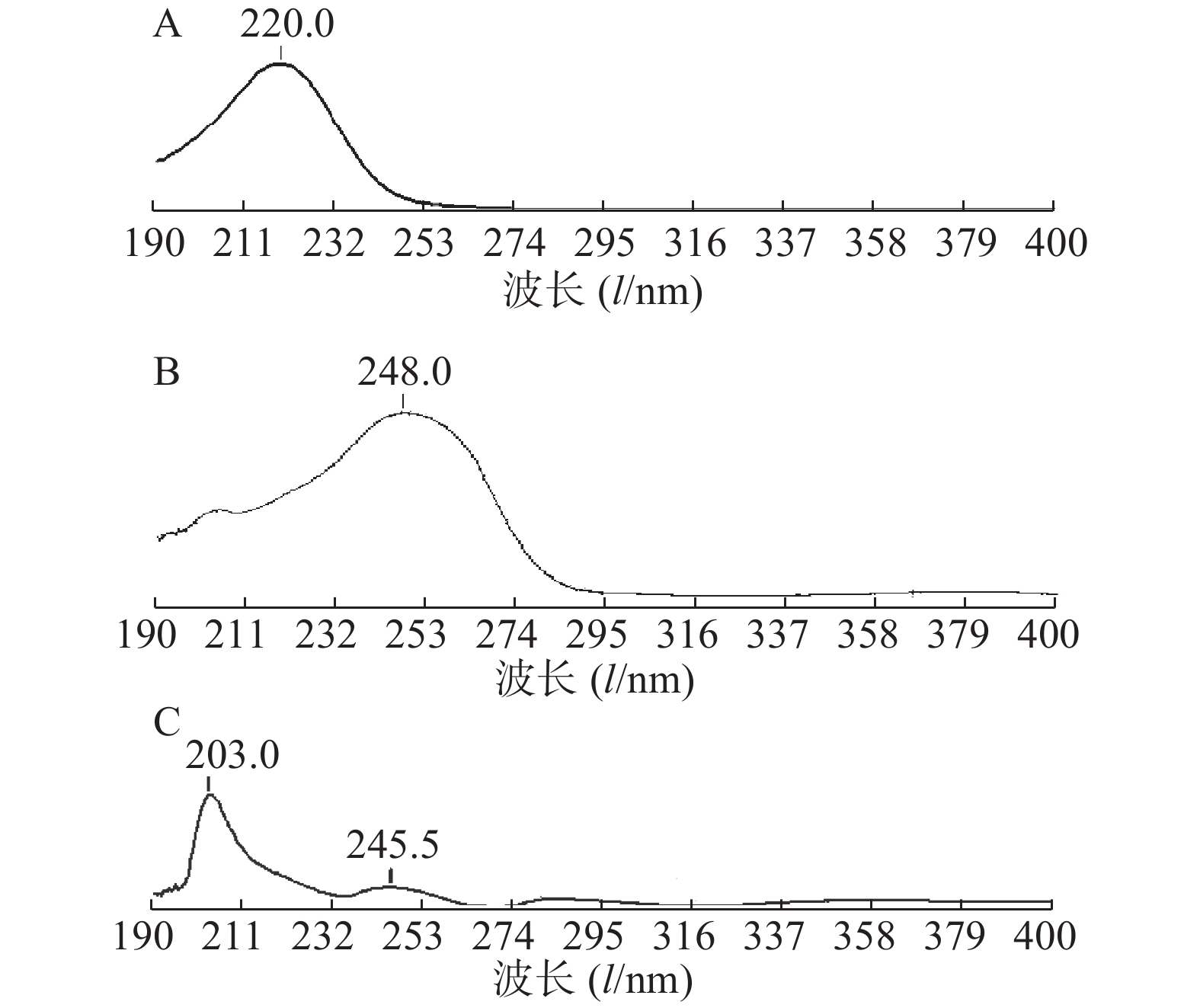
分别取酮康唑、莫匹罗星和糠酸莫米松适量,精密称定,加流动相制备成适宜浓度的溶液,以相应的溶剂为空白溶液,在190~400 nm波长范围内进行紫外扫描,结果见图1。
由图1可见,莫匹罗星在220 nm处具有最大吸收波长,糠酸莫米松在248 nm处具有最大吸收波长,酮康唑在203 nm和245.5 nm具有最大吸收波长,三者在220 nm与248 nm之间均有吸收,因在供试品中酮康唑和莫匹罗星的浓度均是糠酸莫米松的20倍,糠酸莫米松在220 nm处响应值较小,为保证3种药物能同时测定,确定酮康唑、莫匹罗星和糠酸莫米松的检测波长为248 nm。
-
色谱柱:Intersil ODS-3柱(250 mm×4.6 mm,5 µm),流动相为甲醇-pH5.5磷酸盐缓冲液(65∶35),柱温45 ℃,流速1.0 ml/min,检测波长248 nm,进样量10 µl。理论塔板数以各组分峰计,均不低于5000,各色谱峰的分离度良好。
-
酮康唑对照品溶液:取酮康唑20 mg,精密称定,置10 ml量瓶中,加入适量65%甲醇,超声使其完全溶解,加65%甲醇稀释至刻度,摇匀,得到酮康唑的标准储备液,4 ℃低温避光保存。精密吸取酮康唑的标准储备液1 ml,置于10 ml量瓶中,加65%甲醇稀释至刻度,摇匀,即得。
莫匹罗星对照品溶液:取莫匹罗星20 mg,精密称定,置10 ml量瓶中,加入适量65%甲醇,超声使其完全溶解,加65%甲醇稀释至刻度,摇匀,得到莫匹罗星的标准储备液,4 ℃低温避光保存。精密吸取莫匹罗星的标准储备液1 ml,置于10 ml量瓶中,加65%甲醇稀释至刻度,摇匀,即得。
糠酸莫米松对照品溶液:取糠酸莫米松10 mg,精密称定,置100 ml量瓶中,加入适量65%甲醇,超声使其完全溶解,加65%甲醇稀释至刻度,摇匀,得到糠酸莫米松的标准储备液,4 ℃低温避光保存。精密吸取糠酸莫米松的标准储备液1 ml,置于10 ml量瓶中,加65%甲醇稀释至刻度,摇匀,即得。
混合对照品溶液:取酮康唑、莫匹罗星和糠酸莫米松的标准储备液各1 ml,置10 ml量瓶中,加65%甲醇稀释至刻度,摇匀,即得。
-
取复方酮康唑软膏0.5 g,精密称定,置于50 ml的容量瓶中,加65%甲醇适量,超声溶解,加65%甲醇稀释至刻度,摇匀,即得供试品溶液。
-
取空白软膏基质0.5 g,精密称定,置于50 ml的容量瓶中,加65%甲醇适量,超声溶解,加65%甲醇稀释至刻度,摇匀,即得阴性对照溶液。
-
取上述对照品溶液、供试品溶液和阴性对照溶液,用0.22 μm微孔滤膜过滤,弃去初滤液,续滤液分别按照上述色谱条件进样,记录色谱图及相关参数。莫匹罗星的保留时间为5.075 min,理论塔板数为9196,对称因子0.81;糠酸莫米松的保留时间为18.413 min,理论塔板数为11859,对称因子0.88;酮康唑的保留时间为23.318 min,理论塔板数为12291,对称因子0.89,空白基质对莫匹罗星、糠酸莫米松和酮康唑的测定无干扰,方法专属性好。对照品溶液、供试品溶液及阴性对照溶液色谱见图2。
-
分别精密吸取酮康唑、莫匹罗星和糠酸莫米松标准储备液各0.2、0.4、0.8、1.0、1.2、1.4、1.6、2 ml,置10 ml量瓶中,用65%甲醇稀释至刻度,摇匀,0.22 μm微孔滤膜过滤,弃去初滤液,续滤液按上述色谱条件分别进样10 µl,记录色谱图峰面积。以峰面积A对浓度C (µg/ml)进行线性回归,结果见表1。
表 1 复方酮康唑软膏中主药的线性方程
药名 线性方程 r 线性范围(µg/ml) 莫匹罗星 A=2.295C+10.20 0.9995 40.0~400.0 糠酸莫米松 A=28.240C+1.871 0.9995 2.0~20.0 酮康唑 A=12.280C+27.94 0.9995 40.0~400.0 -
分别精密量取同一批复方酮康唑软膏6份,每份约0.5 g,按“2.3.2”项下操作,测定,计算酮康唑、莫匹罗星和糠酸莫米松含量。结果见表2,结果表明该方法重复性良好。
表 2 复方酮康唑软膏中三种主药的重复性试验结果
药物 含量(µg/ml) 测得量(µg/ml) 平均含量(µg/ml) RSD(%) 莫匹罗星 200.00 203.60 204.30 1.51 200.00 204.90 200.00 201.70 200.00 208.80 200.00 206.40 200.00 200.40 糠酸莫米松 10.00 10.10 9.99 1.23 10.00 9.91 10.00 10.06 10.00 10.10 10.00 9.99 10.00 9.79 酮康唑 200.00 203.30 203.60 0.65 200.00 203.90 200.00 202.60 200.00 204.90 200.00 205.00 200.00 201.60 -
取供试品溶液,室温放置,分别于0、2、4、6、8、12、24 h进样10 µl测定,计算不同时间点莫匹罗星、糠酸莫米松和酮康唑的含量,结果见表3。
表 3 复方酮康唑软膏中三种主药的稳定性试验结果
主药 时间(t/h) RSD
(%)0 2 4 6 8 12 24 莫匹罗星 100.00 99.94 100.00 99.94 99.81 99.12 98.49 0.68 糠酸莫米松 100.00 99.69 100.49 100.38 100.38 99.65 98.37 0.74 酮康唑 100.00 99.90 100.06 100.02 100.04 99.64 100.00 0.15 -
分别精密称取莫匹罗星8、10、12 mg,糠酸莫米松0.4、0.5、0.6 mg,酮康唑8、10、12 mg(相当于标示量的80%、100%、120%),精密称定,分别置于0.5 g的空白基质中,加适量流动相溶液,超声10 min使溶解,置于50 ml量瓶中,加流动相溶液稀释至刻度,摇匀,得低、中、高不同浓度的溶液,每个浓度各3份。用0.22 µm微孔滤膜过滤,弃去初滤液,续滤液按上述色谱条件分别进样,记录色谱图峰面积。根据回归方程计算出相应浓度和含量,并计算回收率、平均回收率及RSD。结果见表4。
表 4 复方酮康唑软膏中三种主药回收率试验结果(n=3)
药名 加入量(µg/ml) 测得量(µg/ml) 回收率(%) 平均回收率(%) RSD
(%)莫匹罗星 160.00 154.40 96.50 97.50 0.59 160.00 156.59 97.87 160.00 155.87 97.42 200.00 195.76 97.88 200.00 193.35 96.67 200.00 194.55 97.28 240.00 235.70 98.21 240.00 234.92 97.88 240.00 234.74 97.81 糠酸莫米松 8.00 7.73 96.62 97.99 0.79 8.00 7.84 98.00 8.00 7.83 97.91 10.00 9.88 98.80 10.00 9.71 97.10 10.00 9.78 97.80 12.00 11.88 99.00 12.00 11.85 98.75 12.00 11.75 97.92 酮康唑 160.00 153.63 96.02 97.62 0.74 160.00 156.39 97.74 160.00 155.84 97.40 200.00 195.72 97.86 200.00 194.06 97.03 200.00 195.44 97.72 240.00 236.46 98.52 240.00 235.60 98.17 240.00 235.38 98.08 -
取3批样品,依法测定,结果见表5。
表 5 3批次样品含量测定结果(n=3,%)
样品批号 酮康唑 莫匹罗星 糠酸莫米松 20190411 99.03 99.20 101.4 20190415 106.3 99.76 101.6 20190408 100.6 100.7 100.7 -
本研究根据软膏剂的特性,选择了提取效率较高,操作简便的超声提取法进行样品前处理,对溶剂种类、溶剂体积、提取时间进行考察,最终选择65%甲醇50 ml,超声提取10 min,该提取方法可有效的除去样品中的杂质,让测定的专属性更高。
-
对于流动相的选择,本实验尝试以甲醇-0.6%醋酸铵溶液作为流动相[9-12],结果基线非常不稳定,这可能是由于醋酸铵的紫外吸收所造成。以甲醇-水、乙腈-水,甲醇-磷酸二氢钠溶液和甲醇-乙腈-水等作为流动相[13-15],使用磷酸二氢钠溶液分离效果及峰形较好,有机相甲醇的比例应控制在一定范围,甲醇低于50%则酮康唑峰保留时间过长;流动相的酸度对酮康唑(弱碱性)和莫匹罗星(弱酸性)[16]的峰形及保留时间亦有影响,用磷酸将磷酸二氢钠的pH值调节到4.5、5.0、5.5和6.0。结果表明,当流动相的pH值为5.5时,莫匹罗星、糠酸莫米松和酮康唑的三组峰值均具有较好的分离度,并且无前延和拖尾现象。对于检测波长的选择,酮康唑、莫匹罗星和糠酸莫米松在220 nm与248 nm均有吸收,因在供试品中酮康唑和莫匹罗星的浓度均是糠酸莫米松的20倍,为了让这三种药物能同时测定,提高检测的灵敏度,确定最佳检测波长为248 nm。对于色谱柱的选择,本研究考察了岛津、安捷伦和沃特世等品牌的色谱柱,最终选择了岛津Intersil ODS-3柱,三种待测成分在该柱上分离度好,峰形佳,所以确定为最佳色谱柱。
-
3个批次的复方酮康唑软膏均为实验室自制,从测定结果可以看出,不同批次的样品中酮康唑、莫匹罗星和糠酸莫米松的含量有一定波动,这提示我们在进行中试放大生产时,要充分考虑各因素的影响,保证制剂中主要成分的含量稳定,同时对软膏剂的长期稳定性也需要进行考察。
Determination of three constituents in compound ketoconazole ointment by RP-HPLC
-
摘要:
目的 建立同时测定复方酮康唑软膏中酮康唑、莫匹罗星和糠酸莫米松含量的方法。 方法 采用反相高效液相色谱法,色谱柱为Intersil ODS-3(250 mm×4.6 mm,5 μm),流动相为甲醇-pH5.5磷酸盐缓冲液(65∶35),柱温45 ℃,流速1.0 ml/min,检测波长248 nm。 结果 方法学验证表明,酮康唑、莫匹罗星和糠酸莫米松3种成分线性关系良好(r≥0.9995),日内日间精密度均小于3.0%,回收率在90%~108%之间,稳定性和重复性的RSD均小于3.0%,符合方法学要求。按照新建立的方法测定了3个批次样品中三组分的含量,结果符合要求。 结论 该方法简便可靠,可为复方酮康唑软膏的质量控制提供依据,也为其质量标准研究奠定了基础。 Abstract:Objective To establish a RP-HPLC method for determination of ketoconazole, mupirocin and mometasone furoate in compound ketoconazole ointment. Methods RP-HPLC was conducted on a Intersil ODS-3 column (250 mm×4.6 mm, 5 μm), with methanol-PBS with pH 5.5 (65:35) as the mobile phase and the column temperature was 45 ℃. The flow rate was 1.0 ml/min, and the detection wavelength was 248 nm. Results The methodological verification showed that ketoconazole, mupirocin and mometasone furoate had a good linearity (r≥0.9995). The inter/intra-day precisions were less than 3.0%, The recovery rates were between 90% and 108%. The stability and repeatability of RSD were also less than 3.0%, which met the requirements of method validation. The contents of the three components in three batches were determined by the new method. Conclusion The method is simple and reliable. It can provide a basis for the quality control of compound ketoconazole ointment and lay a foundation for its quality standard research. -
Key words:
- RP-HPLC /
- ketoconazole /
- mupirocin /
- mometasone furoate
-
肝纤维化(HF)是一种创伤愈合反应,其特征是细胞外基质(ECM)在肝内的过度沉积,导致肝功能丧失和肝脏结构破坏[1]。在正常肝脏中,肝星状细胞(HSC)是位于肝脏窦状隙的DISE腔内,负责储存维生素A。当肝脏受到损伤刺激时,HSC从静止状态转化为具有增殖、类维生素A消失、趋化性、收缩性、纤维生成等特性的肌成纤维细胞(MFs),参与肝纤维化进程[2-4]。
核糖体蛋白S5(RPS5)是核糖体40S小亚基的组成成分,是核糖体生物发生所必需的。越来越多的证据表明,一些核糖体蛋白除了参与蛋白质加工合成之外,还具有许多核糖体外功能[5-6]。例如,RPS5基因对于胚胎干细胞的分化和类胚体的形成至关重要[7];RPS5的β-发夹结构能够与HCV IRES相互作用,并介导HCV的翻译过程[8];RPS5在结肠癌中异常表达,并可能在癌变过程中作为检查点发挥重要作用[9]。此外,RPS5还参与小鼠红白血病细胞分化,其表达下调会影响细胞周期蛋白依赖激酶-2、-4和-6的蛋白水平,并延迟体外红细胞成熟,引起G1/G0细胞周期停滞[10-11]。
本课题组前期研究发现,在肝纤维化过程中,RPS5在静息和激活的HSC内存在差异表达[12-13]。体外实验证实RPS5参与HSC活化,体内研究表明,RPS5基因敲减可加重肝纤维化,RPS5过表达则减轻肝纤维化[13]。但是,我们并没有研究特异性敲减HSC内RPS5的表达对肝纤维化的影响[14-17]。为此,我们构建了GFa2(GFAP启动子)-驱动shRPS5腺病毒,并研究其靶向敲减HSC的RPS5表达对肝纤维化进展的影响。
1. 材料和方法
1.1 材料
1.1.1 实验试剂
高糖DMEM培养基(Gibco);Western及IP细胞裂解液液(Beyotime);BCA蛋白定量试剂盒(Thermo Fisher Scientific);RPS5抗体(Santa Cruz)、ALB、GAPDH抗体(Cell Signaling Technology)、GFAP、α-SMA、胶原蛋白 I抗体(Abcam);山羊(多克隆)抗兔 IgG(H+L)、山羊(多克隆)抗小鼠 IgG(H+L)(LI-COR Biosciences);Odyssey成像系统(LI-COR Biotechnology);SYBR Premix Ex TaqTM PCR 试剂盒(Takara)。
1.1.2 实验动物
雄性Sprague-Dawley大鼠,清洁级,重约200 g,购于上海SLAC实验动物有限公司。
1.2 方法
1.2.1 原代HSC和肝细胞提取
原代HSC和肝细胞从雄性SD大鼠分离,通过蛋白酶-胶原酶消化,单步Nycodenz梯度纯化[13]。分离的HSC和肝细胞在含有10%胎牛血清(FBS)DMEM培养基,5% CO2、37 ℃培养箱中培养。每隔1天更换1次培养基。通过GFAP免疫染色评估,HSC的纯度为90%~95%。本实验于分离后第3天在转分化的HSC上进行。HSC以感染复数(MOI)50感染腺病毒48 h。
1.2.2 构建重组腺病毒
根据AdEasy™ Adenoviral Vector System(AgilentStratagene, USA)的说明制备质粒 pShuttle-GFa2-shRPS5。将GFAP基因启动子(GFa2)、shRPS5序列和必需元件克隆到无启动子穿梭载体pShuttle中,穿梭载体pShuttle-GFa2驱动shRPS5的表达。重组AdGFa2-shRPS5和AdGFa2-shNC腺病毒在293细胞中扩增,通过氯化铯梯度超速离心纯化。使293细胞通过噬斑测定病毒原液的滴度。shRPS5和shNC序列见表1。
表 1 shRPS5和shNC序列名称 序列 shRPS5 5′-GCTCATGACTGTACGAATTCTCGAGAATTCGTACAGTCAT GAGC-3′ shNC 5′-GCGCGCTTTGTAGGATTCGCTCGAGCGAATCCTACAAA GCGCGC-3′ 1.2.3 蛋白印迹法(Western-blot)
将HSC细胞中的培养基吸弃,用PBS洗涤1次,加入Western及IP细胞裂解液冰上裂解20 min。通过BCA法测量蛋白浓度后将蛋白样品在95 ℃下加热5 min。制胶上样,将20 μg样品进行10% SDS-PAGE电泳,结束后将蛋白质转移到NC膜上。5%脱脂奶粉封闭1 h。分别加入RPS5、ALB、GAPDH、GFAP、α-SMA和I型胶原的单克隆抗体4 ℃孵育过夜,用PBST洗膜3次,每次10 min。山羊(多克隆)抗兔IgG(H+L)或山羊(多克隆)抗小鼠IgG(H+L)室温孵育2 h,PBST洗膜3次,每次10 min。Odyssey红外扫描成像系统对NC膜扫描,观察相关蛋白的表达情况。
1.2.4 实时PCR
用Trizol试剂盒提取总RNA。用SYBR Premix Ex TaqTM PCR试剂盒,合成cDNA,定量PCR检测基因mRNA表达。以管家基因β-肌动蛋白(β-actin)作为内部对照,并将基因特异性mRNA表达与β-actin表达进行归一化。引物序列见表2。
表 2 实时qPCR引物序列名称 正向引物序列 反向引物序列 β-actin 5′-CCAT TGAACACGGCATTGTC-3′ 5′-TCATAGATGGGCACAC AGTG-3′ RPS5 5′-AAATGTGCAGGTGTTGACCA-3′ 5′-CACGCTCCTCCTGAAGAATC-3′ α-SMA 5′-CCGAGATCTCACCGACTACC-3′ 5′-TCCA GAGCGACATAGCACAG-3′ collagen I 5′-CCGTGACCTCAAGATG TGCC-3′ 5′-GCTCATACCTTCGCTT CCAA-3′ 1.2.5 动物肝纤维化模型
用二甲基亚硝胺(DMN)和胆管结扎术(BDL)的方法建立大鼠肝纤维化模型[13],尾静脉注射腺病毒(4×109pfu)特异性敲减肝内HSC的RPS5水平。
1.2.6 组织标本采集及指标的检测
肝组织切片HE染色分析病理改变情况;羟脯氨酸(羟脯氨酸检测试剂盒)含量测定、切片天狼星红和 Masson染色评价胶原沉积情况;免疫组织化学染色检测α-SMA和RPS5的表达情况。
1.2.7 统计分析
数据分析通过SPSS 21统计软件进行,采用t检验分析,实验结果用均数±标准差(
$\bar x $ ±s)表示。与对照组比较,P<0.05 则认为差异具有统计学意义。2. 结果
2.1 AdGFa2-shRPS5对RPS5表达的抑制作用
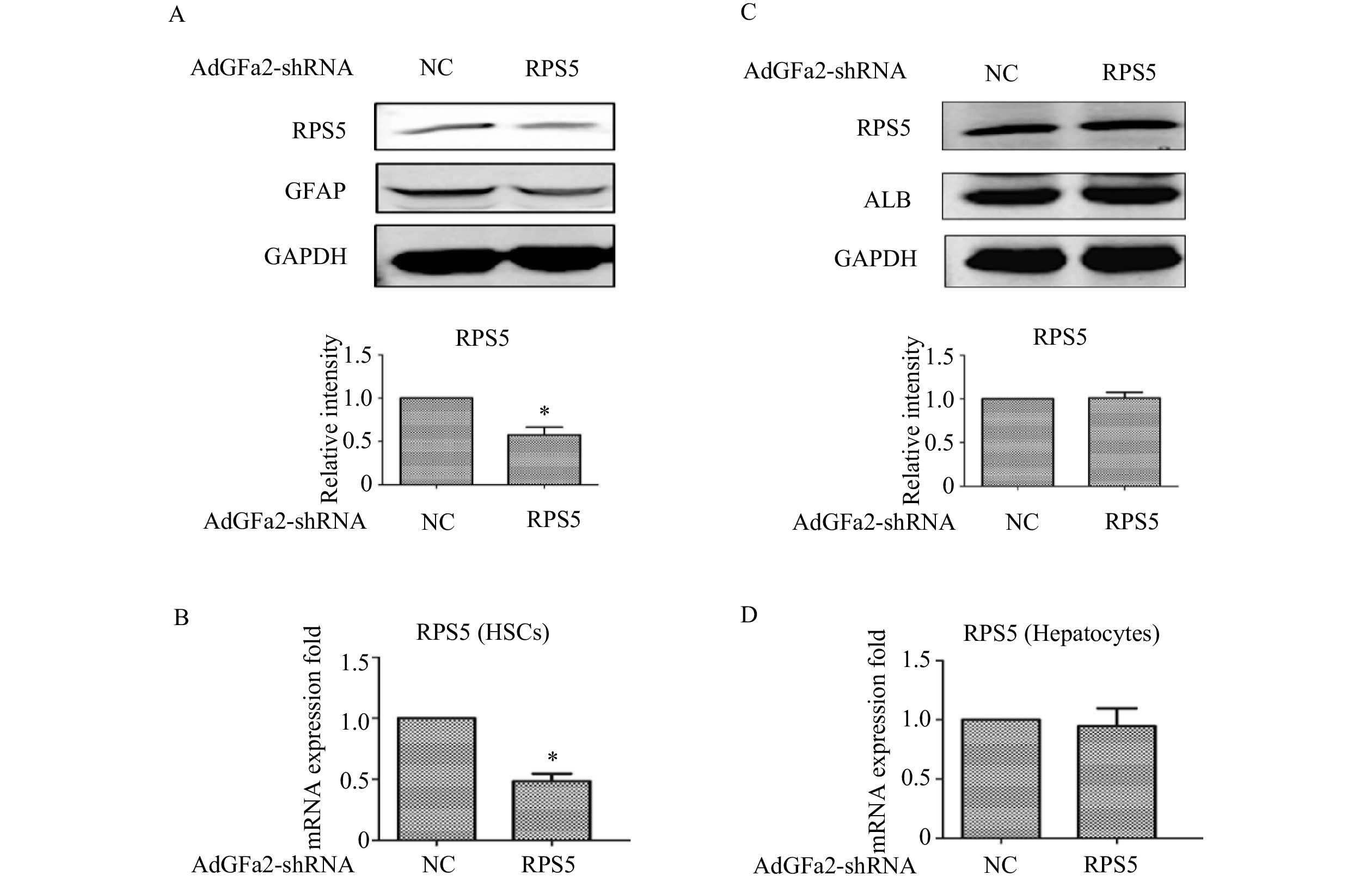
为了确定AdGFa2-shRPS5对RPS5表达的影响及对HSC的特异性,我们分别用AdGFa2-shRPS5和AdGFa2 shNC转染大鼠的原代HSC和肝细胞48 h,蛋白印迹法和实时PCR测定RPS5的表达情况。结果显示,RPS5 mRNA和蛋白质水平仅在原代HSC中降低(图1A、1B),在肝细胞中没有明显变化(图1C、1D)。
2.2 AdGFa2-shRPS5对HSC活化的影响
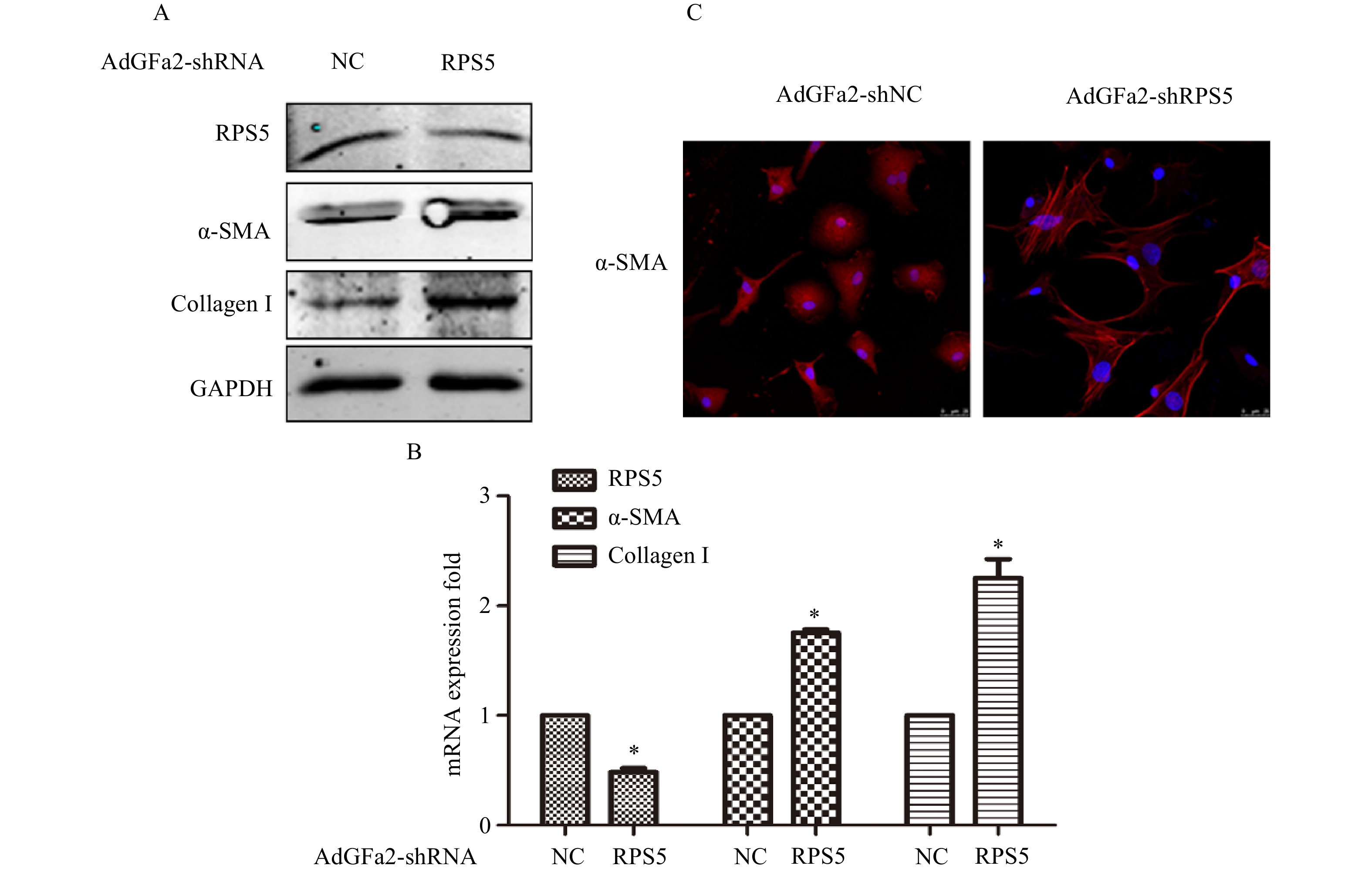
AdGFa2-shRPS5转染原代培养的HSC,蛋白印迹法和实时PCR分析α-SMA和I型胶原表达变化。结果表明,AdGFa2-shRPS5感染HSC后,α-SMA和I型胶原mRNA和蛋白质的表达显著增加(图2A、2B)。免疫荧光结果显示,转染AdGFa2-shRPS5的HSC形态明显改变,细胞更加扁平而延展(图2C)。以上结果表明RPS5敲减促进了HSC的活化。
2.3 AdGFa2-shRPS5对BDL诱导的肝纤维化的影响
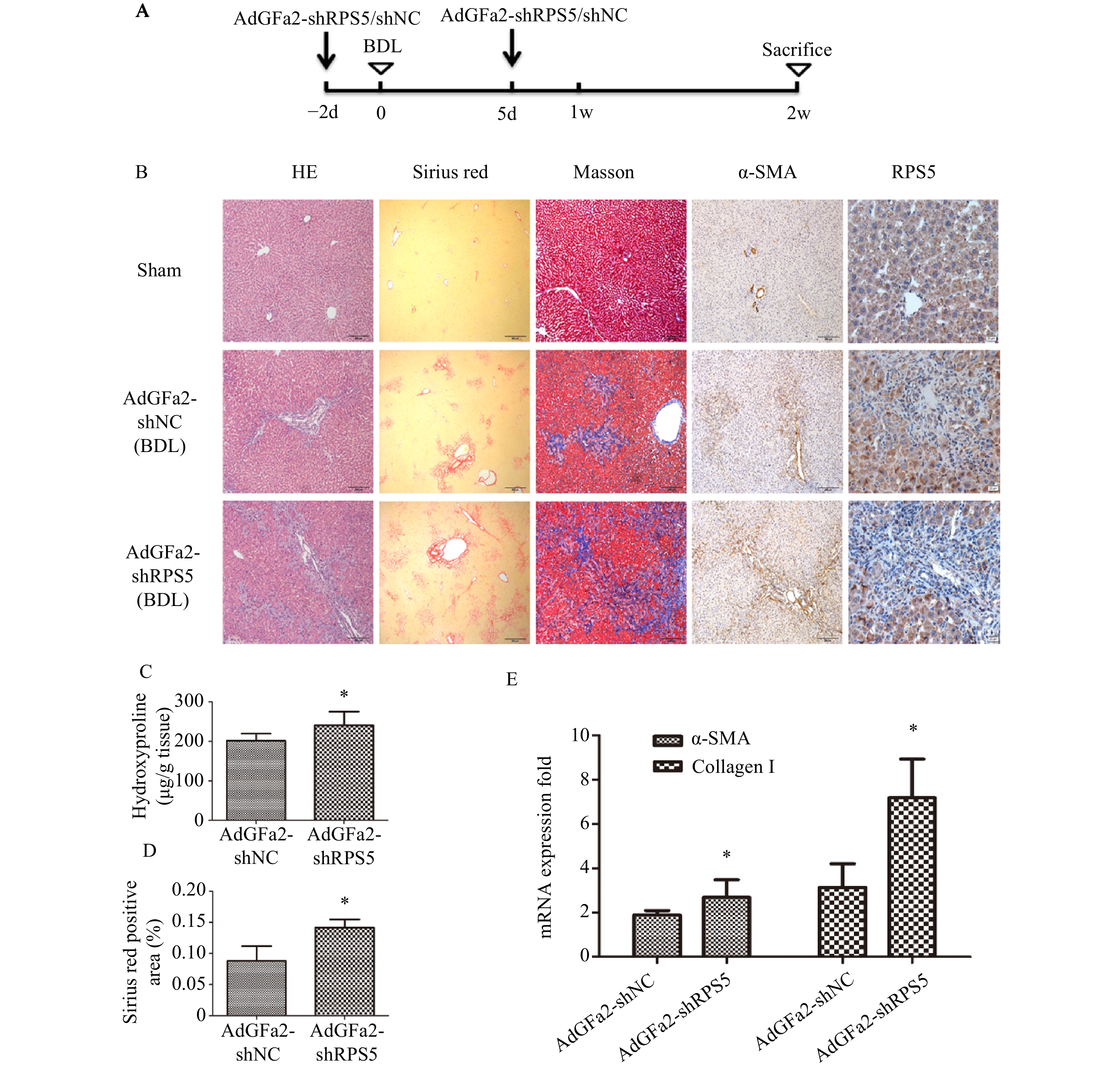
为了考察AdGFa2-shRPS5体内对肝纤维化的影响,我们构建了BDL肝纤维化模型。BDL手术前2 d和手术后5 d由尾静脉注射AdGFa2-shRPS5,2周后处死所有大鼠(图3A),评价肝纤维化情况。免疫组织化学染色结果所示,与AdGFa2-shNC组相比,AdGFa2-shRPS5降低了小鼠体内RPS5的表达,促进HSC的活化,α-SMA表达相应增加,表明肝纤维化程度加重。HE染色结果表明,在AdGFa2-shRPS5组中,反应性胆管周围有更广泛的胆管增生和有害的肝实质塌陷,α-SMA阳性表达增加。此外,天狼星红和Masson染色结果显示AdGFa2-shRPS5增加了胶原沉积(图3B)。天狼星染色半定量分析表明,AdGFa2-shRPS5处理的BDL大鼠纤维化面积增加了161%(P<0.05,图3C)。羟脯氨酸含量AdGFa2-shRPS5组明显高于AdGFa2 shNC组(P<0.05,图3D)。并且α-SMA和I型胶原mRNA的表达也与其蛋白质水平结果表达相一致(图3E)。
2.4 AdGFa2-shRPS5对DMN诱导的肝纤维化的影响
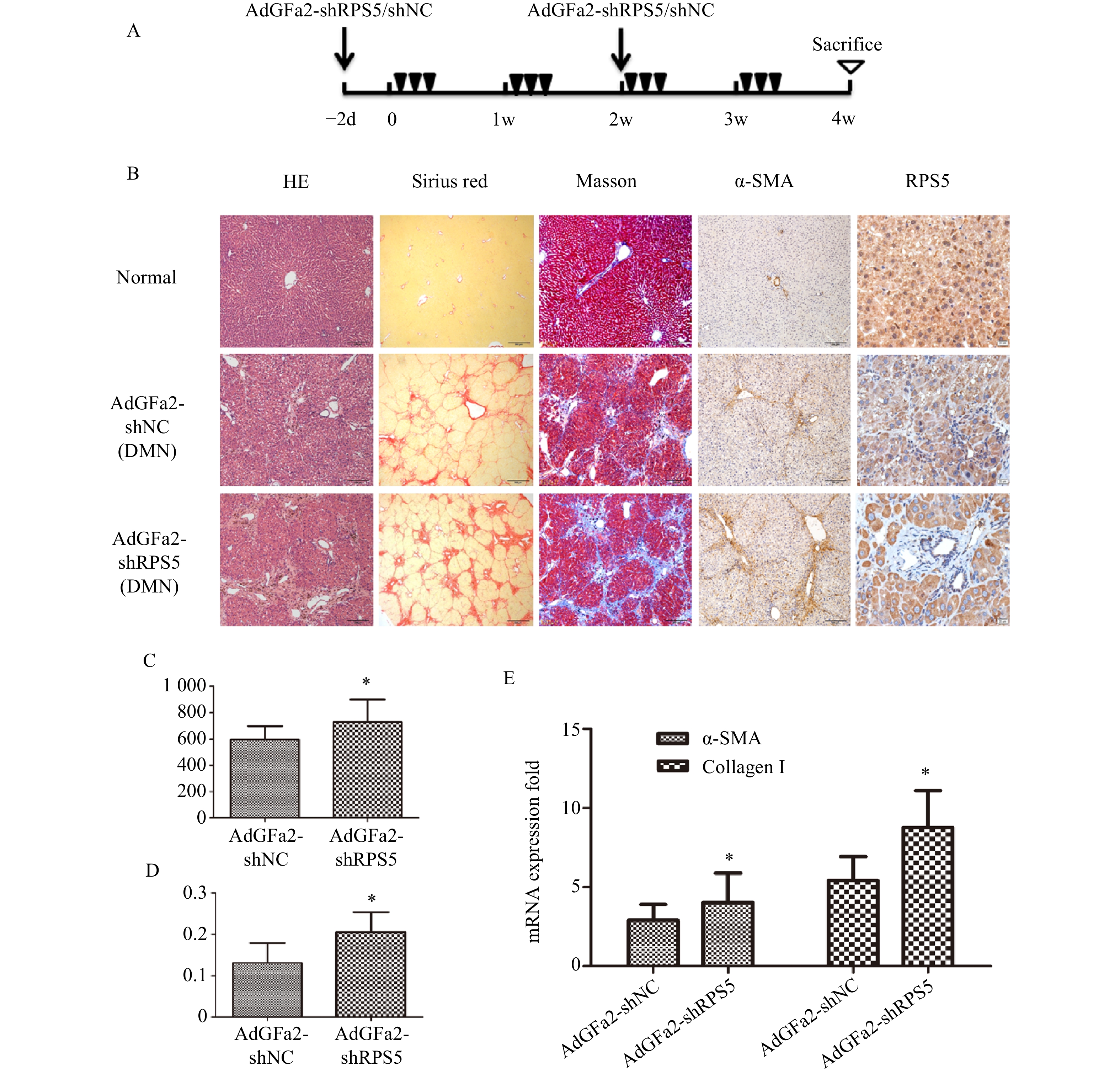
为了进一步证实AdGFa2-shRPS5对肝纤维化的作用,腹腔注射DMN制备纤维化模型。分别在第一次DMN注射前2天和后2周通过尾静脉向大鼠注射AdGFa2-shRPS5,在4周后处死所有大鼠(图4A)。AdGFa2-shRPS5抑制大鼠体内RPS5的表达,α-SMA在肝脏中的表达增加(图4B)。与BDL模型一致,HE、天狼星红、Masson、α-SMA染色及α-SMA RT-PCR分析证实(图4B,4E),AdGFa2-shRPS5也促进了DMN诱导的肝纤维化的发展。在DMN模型中,AdGFa2-shRPS5组的羟脯氨酸含量高于AdGFa2 shNC组(P<0.05,图4C)。天狼星红染色的半定量分析结果显示,AdGFa2-shRPS5使纤维化面积显著增加约157%(P<0.05,图4D)。综上结果证实特异性敲减HSC内的RPS5加剧了纤维化的进展。
3. 讨论
肝纤维化是一个动态过程,其特征是慢性肝损伤导致ECM的过度沉积,当肝损伤发生时,HSC活化以获得成纤维能力,因此HSC是肝纤维化的主要生成细胞。文献表明,在转分化的HSC和人类肝硬化肝脏中RPS5显著降低[13]。RPS5的过表达使得体内肝纤维化得到改善,而RPS5的敲减促进了肝纤维化[13]。但究竟是哪一种细胞在这一过程中起主要作用仍值得进一步研究。因此,有必要仅针对肝脏中一个或有限细胞群进行研究。胶质纤维酸性蛋白GFAP是成熟星形胶质细胞中的主要中间丝状蛋白,但也在肝脏的HSCs中表达。因此,使用GFAP启动子GFa2来驱动RPS5敲减可能是靶向HSC的方法。在此研究中,我们使用GFAP启动子驱动shRNA系统来研究RPS5靶向HSCs对大鼠肝纤维化进展的影响。
本研究构建重组腺病毒AdGFa2-shRPS5,并证实AdGFa2-shRPS5可以特异性地将HSCs中RPS5的表达降低约50%,对肝细胞没有明显作用。研究证明RPS5的敲减促进HSCs的活化。体内研究结果表明,两种慢性肝损伤动物模型中纤维化的发展随着RPS5的特异性敲减而加重,并伴有显著的细胞外基质沉积。综上结果表明,RPS5的下调有助于HSC的激活,从而促进体内肝纤维化,表明RPS5可能是HSC激活的分子开关。
RPS5是核糖体40S小亚基的组成成分,是核糖体生物发生所必需的,并且具有许多核糖体外功能,如促进细胞的凋亡、DNA修复、细胞增殖和分化[5-6,10-11]。文献证实RPS5可抑制LPS诱导的巨噬细胞中的IL-6和NO释放,表明RPS5也参与炎症过程[18]。本研究结果表明,RPS5在调节HSC活化中起着重要作用,揭示了RPS5的新功能。由于GFa2启动子的活性较弱,我们没有研究过表达HSC中的RPS5对体内肝纤维化的影响。
本研究为敲减HSC中的RPS5对肝纤维化有促进作用提供了证据。使用AdGFa2-shRPS5的一个关键优势是靶向HSC,并且对正常肝细胞没有影响。结果表明,RPS5对肝纤维化的发生发展至关重要,可能是治疗肝纤维化的一个有前景的靶点。
-
表 1 复方酮康唑软膏中主药的线性方程
药名 线性方程 r 线性范围(µg/ml) 莫匹罗星 A=2.295C+10.20 0.9995 40.0~400.0 糠酸莫米松 A=28.240C+1.871 0.9995 2.0~20.0 酮康唑 A=12.280C+27.94 0.9995 40.0~400.0 表 2 复方酮康唑软膏中三种主药的重复性试验结果
药物 含量(µg/ml) 测得量(µg/ml) 平均含量(µg/ml) RSD(%) 莫匹罗星 200.00 203.60 204.30 1.51 200.00 204.90 200.00 201.70 200.00 208.80 200.00 206.40 200.00 200.40 糠酸莫米松 10.00 10.10 9.99 1.23 10.00 9.91 10.00 10.06 10.00 10.10 10.00 9.99 10.00 9.79 酮康唑 200.00 203.30 203.60 0.65 200.00 203.90 200.00 202.60 200.00 204.90 200.00 205.00 200.00 201.60 表 3 复方酮康唑软膏中三种主药的稳定性试验结果
主药 时间(t/h) RSD
(%)0 2 4 6 8 12 24 莫匹罗星 100.00 99.94 100.00 99.94 99.81 99.12 98.49 0.68 糠酸莫米松 100.00 99.69 100.49 100.38 100.38 99.65 98.37 0.74 酮康唑 100.00 99.90 100.06 100.02 100.04 99.64 100.00 0.15 表 4 复方酮康唑软膏中三种主药回收率试验结果(n=3)
药名 加入量(µg/ml) 测得量(µg/ml) 回收率(%) 平均回收率(%) RSD
(%)莫匹罗星 160.00 154.40 96.50 97.50 0.59 160.00 156.59 97.87 160.00 155.87 97.42 200.00 195.76 97.88 200.00 193.35 96.67 200.00 194.55 97.28 240.00 235.70 98.21 240.00 234.92 97.88 240.00 234.74 97.81 糠酸莫米松 8.00 7.73 96.62 97.99 0.79 8.00 7.84 98.00 8.00 7.83 97.91 10.00 9.88 98.80 10.00 9.71 97.10 10.00 9.78 97.80 12.00 11.88 99.00 12.00 11.85 98.75 12.00 11.75 97.92 酮康唑 160.00 153.63 96.02 97.62 0.74 160.00 156.39 97.74 160.00 155.84 97.40 200.00 195.72 97.86 200.00 194.06 97.03 200.00 195.44 97.72 240.00 236.46 98.52 240.00 235.60 98.17 240.00 235.38 98.08 表 5 3批次样品含量测定结果(n=3,%)
样品批号 酮康唑 莫匹罗星 糠酸莫米松 20190411 99.03 99.20 101.4 20190415 106.3 99.76 101.6 20190408 100.6 100.7 100.7 -
[1] 万芳友, 李爱华. 反相高效液相色谱法同时测定复方酮康唑搽剂中三种组分的含量[J]. 药物分析杂志, 2013, 33(7):1263-1266. [2] AMRUTIYA N, MADAN M, BAJAJ A. Development and validation of RP-HPLC method for simultaneous estimation of prednicarbate, mupirocin and ketoconazole in topical dosage forms[J]. J Anal Chem,2010,65(11):1148-1154. doi: 10.1134/S1061934810110109 [3] 王爱平, 李若瑜. 2%酮康唑乳膏在皮肤科疾病中的应用[J]. 中国真菌学杂志, 2010, 5(3):179-183. [4] 陆雪华, 陆艳萍, 覃美玲, 等. 复方酮康唑莫匹罗星联合治疗真菌性皮肤溃疡疗效观察[J]. 基层医学论坛, 2018, 22(2):158-160. [5] 中国中西医结合学会皮肤性病学分会环境与职业性皮肤病学组. 糠酸莫米松乳膏临床应用专家共识[J]. 中国中西医结合皮肤性病学杂志, 2017, 16(1):88-90. [6] 孟甄, 金建玲, 刘玉庆, 等. 细菌耐药性的诱导与消除[J]. 中国药理学通报, 2003, 19(9):1047-1051. [7] 谢阳, 万苗坚. 皮肤科常用糖皮质激素类药物的类型及适应证[J]. 中国医学文摘(皮肤科学), 2015, 32(3):283-288. [8] 刘淮, 刘景桢. 外用糖皮质激素的适应症与副作用[J]. 皮肤病与性病, 2016, 38(1):19-20. [9] 李文仕. RP-HPLC法测定复方中风康复片中盐酸麻黄碱的含量[J]. 中国药事, 2012, 26(5):494-496. [10] 颜苗, 张金娇, 李焕德, 等. RP-HPLC法同时测定甘草酸制剂中18α-、18β-甘草酸的含量[J]. 药物分析杂志, 2012, 32(2):301-304, 309. [11] ABDELWAHAB N S, ALI N W, ABDELKAWY M, et al. Validated RP-HPLC and TLC-densitometric methods for analysis of ternary mixture of cetylpyridinium chloride, chlorocresol and lidocaine in oral antiseptic formulation[J]. J Chromatogr Sci,2016,54(3):318-325. [12] WAN F Y, LI A H. Determination of three constituents in compound ketoconazole liniment by RP-HPLC[J]. Chin J Pharm Anal,2013,33(7):1263-1266. [13] SHEHNAZ H, HAIDER A, SAEED ARAYNE M, et al. Carboxyterfenadine antacid interaction monitoring by UV spectrophotometry and RP-HPLC techniques[J]. Arab J Chem,2014,7(5):839-845. doi: 10.1016/j.arabjc.2013.01.011 [14] VENISHETTY V K, PARIKH N, SISTLA R, et al. Application of validated RP-HPLC method for simultaneous determination of docetaxel and ketoconazole in solid lipid nanoparticles[J]. J Chromatogr Sci,2011,49(2):136-141. doi: 10.1093/chrsci/49.2.136 [15] AHMMED S M, MUKHERJEE P K, BAHADUR S, et al. CYP450 mediated inhibition potential of Swertia chirata: an herb from Indian traditional medicine[J]. J Ethnopharmacol,2016,178:34-39. doi: 10.1016/j.jep.2015.11.046 [16] STAUB I, FLORES L, GOSMANN G, et al. Photostability studies of ketoconazole: isolation and structural elucidation of the main photodegradation products[J]. Lat Am J Pharm,2010,29(7):1100-1106. -





 下载:
下载:

 下载:
下载:



