-
对照品系指国家药品标准中用于鉴别、检查、含量测定、杂质和有关物质检查等的标准物质[1]。《中国药典》中并没有明确规定对照品溶液的存放有效期,但《中国药典》和《药品生产质量管理规范》(GMP)均要求使用单位应对对照品溶液的稳定性和使用效期进行验证,通过研究结果来确定内控效期[1-7]。本实验结合日常检验工作的使用率、制剂中间品和成品抽检的周期,挑选5种制剂(维生素E珍珠乳膏、新面醑、复方替硝唑溶液、磺胺嘧啶鱼肝油滴鼻剂和地塞米松磷酸钠滴鼻液),涉及8种常用的对照品(维生素E、甲硝唑、氯霉素、水杨酸、替硝唑、醋酸氯己定、磺胺嘧啶和地塞米松磷酸酯),按照相应的质量标准方法进行测定[8-14],考察各对照品储备液在2~10 ℃冰箱中的稳定性,为存放效期提供必要依据,从而规定对照品储存的内控时间[15-18]。
-
Agilent 1260 型高效液相色谱仪(包括脱气机、四元泵、自动进样系统、G7114A紫外检测器、Chemstation工作站,美国Agilent公司);Agilent 1200 型高效液相色谱仪(包括脱气机、四元泵、自动进样系统、G1314B紫外检测器、Chemstation工作站,美国Agilent公司);PHS-3C型精密 pH计(上海雷磁仪器厂);ME235S电子天平(德国赛多利斯);EX225DZH电子天平(美国奥豪斯)。
-
对照品维生素E(批号10062-0007,纯度99.2%)、甲硝唑(批号100191-201808,纯度100.0%)、氯霉素(批号130555-201203,纯度99.8%)、水杨酸(批号100106-201104,纯度99.9%)、替硝唑(批号100336-201704,纯度100.0%)、醋酸氯己定(批号100183-201003,纯度96.2%)、磺胺嘧啶(批号100026-201404,纯度99.7%)、地塞米松磷酸酯(批号101116-201102,纯度98.6%)购自中国食品药品检定研究院;甲醇、乙腈为色谱纯(霍尼韦尔,美国);磷酸、磷酸二氢钾、盐酸、醋酸铵、三乙胺为分析纯;水为纯化水。
-
色谱柱:Hypersil BDS C18(250 mm×4.6 mm,5 μm),流动相为甲醇,流速为1.5 ml/min,检测波长为284 nm,进样量为10 μl。
-
色谱柱:Hypersil BDS C18(250 mm×4.6 mm,5 μm),流动相为甲醇-0.04%磷酸溶液(V∶V=47∶53),流速为1.0 ml/min,检测波长为284 nm,进样量为10 μl。
-
色谱柱:Hypersil BDS C18(250 mm×4.6 mm,5 μm),以甲醇为流动相A,以甲醇-0.05 mol/L磷酸二氢钾溶液(pH3.5)(V∶V=20∶80)为流动相B,梯度洗脱(0~8 min,0%~55% A;8~15 min,55% A;15~15. 1 min,55%~0% A;15. 1~20 min,0% A),流速为1.0 ml/min,检测波长为280 nm,进样量为10 μl。
-
色谱柱:Hypersil BDS C18(250 mm×4.6 mm,5 μm),流动相为乙腈-0.3%醋酸铵溶液(V∶V=20∶80),流速为1.0 ml/min,检测波长为260 nm,进样量为10 μl。
-
色谱柱:Hypersil BDS C18(150 mm×4.6 mm,5 μm),流动相为0.75%三乙胺溶液(磷酸调pH 至3.0)-甲醇-乙腈(V∶V∶V = 55∶40∶5),流速为1.0 ml/min,检测波长为242 nm,进样量为10 μl。
-
精密称取维生素E对照品约10 mg,置50 ml量瓶中,加甲醇溶解并稀释至刻度,摇匀,制成每1 ml中约含维生素E 0.2 mg的对照品溶液。
-
精密称取甲硝唑、氯霉素对照品各约10 mg,分别置10 ml量瓶中,加流动相溶解并稀释至刻度,摇匀;另精密称取水杨酸对照品约12.5 mg,置100 ml量瓶中,加流动相溶解并稀释至刻度,摇匀;精密量取上述甲硝唑、氯霉素对照品稀释液各5 ml、水杨酸对照品稀释液10 ml,置于同一25 ml量瓶中,加流动相稀释至刻度,摇匀,制成每1 ml中约含甲硝唑、氯霉素和水杨酸分别为0.2 mg、0.2 mg和0.05 mg的混合对照品溶液。
-
精密称取替硝唑对照品约10 mg、醋酸氯己定对照品约10 mg置于同一50 ml量瓶中,加水溶解并稀释成每1 ml中约含替硝唑、醋酸氯己定各0.2 mg的混合对照品溶液。
-
精密称取磺胺嘧啶对照品约12.5 mg,置25 ml量瓶中,加稀盐酸1 ml溶解后,用流动相稀释至刻度,摇匀。精密量取2 ml,置10 ml量瓶中,用流动相稀释至刻度,摇匀,制成每1 ml中约含磺胺嘧啶0.1 mg的对照品溶液。
-
精密称取地塞米松磷酸酯对照品约15 mg,置50 ml量瓶中,加水溶解并稀释至刻度,摇匀;精密量取稀释液3 ml,置25 ml量瓶中,加流动相稀释至刻度,摇匀,制成每1 ml 约含地塞米松磷酸酯0.036 mg的溶液。
上述对照品溶液均置于具塞的量瓶中,且用封口膜封口,取用后立即冷藏(2~10 ℃)保存,分析前需放至室温。
-
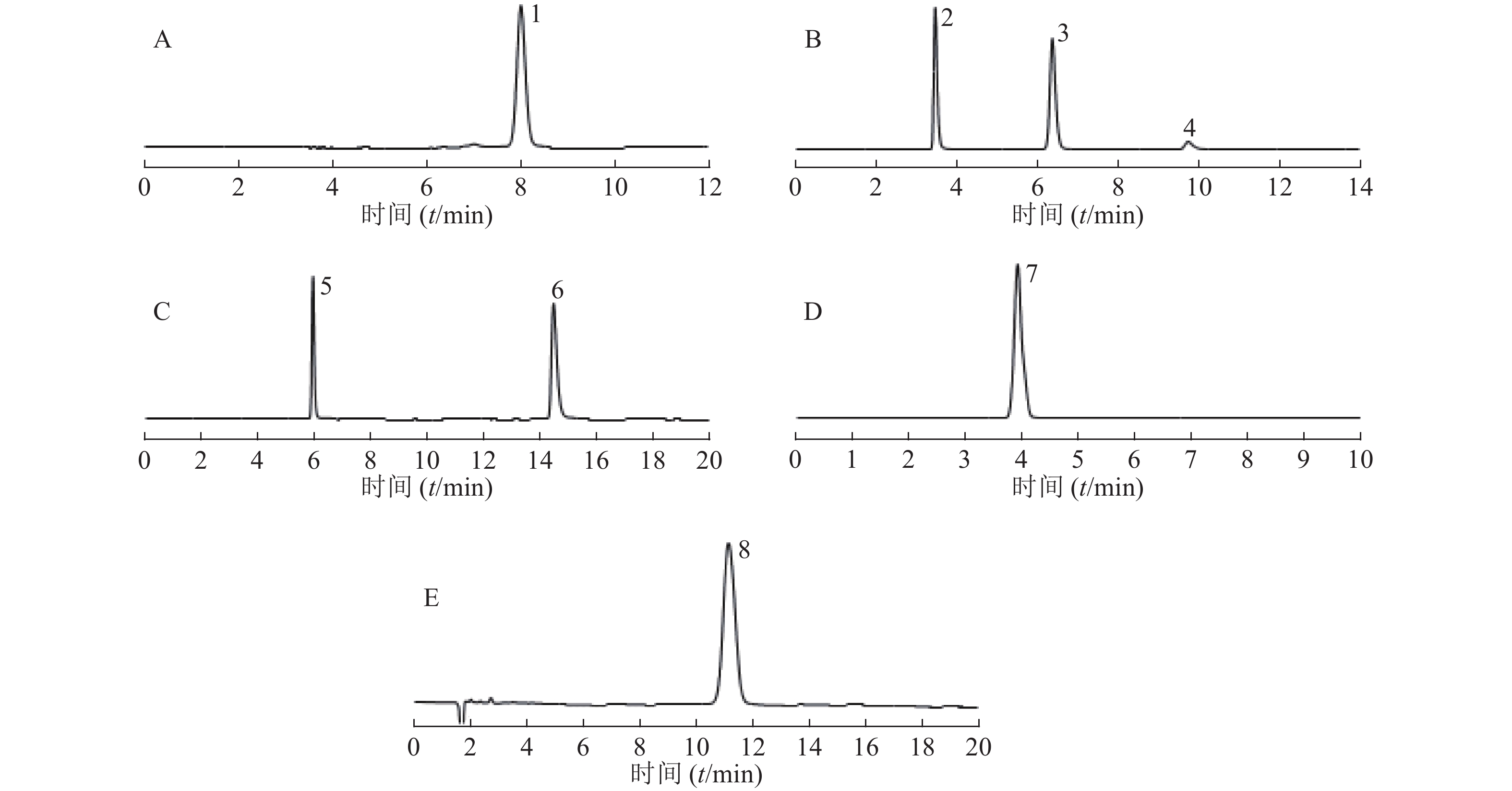
按“2.1”项下色谱条件进样测定,记录色谱图,详见图1。各色谱条件下,各主成分峰分离度均大于1.5,理论板数满足相应制剂标准要求,且各出峰情况与文献一致[8-14]。
-
将上述3种对照品溶液在保存0、1、4、7、10、14、21、28、35 d时,与当天新鲜配制的相应对照品溶液按照相应色谱条件分别进样,分别计算平均峰面积,以当天新鲜配制的对照品溶液计算对照品储存溶液的含量值。
-
每个测试时间点的结果都是用新鲜配制的对照品溶液的平均响应值,来重新计算用于研究效期的对照品溶液的标示量,基于下述公式进行计算:
$$ \mathrm{X}\mathrm{\%}=\frac{{\mathrm{A}}_{\mathrm{T}}\times {\mathrm{C}}_{\mathrm{N}}}{{\mathrm{A}}_{\mathrm{N}}\times {\mathrm{C}}_{\mathrm{T}}}\times 100\mathrm{\%} $$ 式中,AN和CN表示新鲜配制对照品的峰面积和浓度;AT和CT表示对照品储存溶液的峰面积和浓度。
-
各对照品溶液均未出现浑浊、沉淀等异常现象;测试用对照品溶液与新鲜配制的对照品溶液外观一致;色谱图中均未出现显著的杂质峰;每个分析测试点,要求对照品储存溶液的标示量与零点的差异不得超过2.0%。
-
上述各类对照品溶液在2~10 ℃冰箱内密封储存35 d,测试用对照品溶液外观与新配制对照品溶液一致,未出现浑浊、沉淀等现象;色谱中均未出现显著的杂质峰,每个分析测试点,对照品溶液的含量变化如图2所示,维生素E储存35 d、甲硝唑、氯霉素和水杨酸混合对照品储存7 d、替硝唑和醋酸氯己定混合对照品储存35 d、磺胺嘧啶储存35 d、地塞米松磷酸酯储存35 d,含量符合要求。结合含量标准要求,在2~10 ℃冰箱中,维生素E对照品、替硝唑和醋酸氯己定混合对照品、磺胺嘧啶对照品、地塞米松磷酸酯对照品溶液的效期可定为35 d,甲硝唑、氯霉素和水杨酸混合对照品溶液定为7 d。
-
对照品溶液是药品检验的重要部分,对照品储存在冰箱中需要以封口膜封口,减少溶剂的挥发;从冰箱中取出时,需超声半分钟或放至室温,摇匀后再取下封口膜取样,避免直接打开引起瓶内挥发的溶剂流失,影响测定结果。
考察结果中发现甲硝唑、氯霉素和水杨酸混合对照品溶液稳定性较差,各组分储存期分别为35、21和7 d。采用三组分单独配制储存进行考察,结果发现甲硝唑、氯霉素、水杨酸溶液的储存时间分别为35、35和10 d,同比混合对照品溶液中,氯霉素稳定性增加,但对水杨酸稳定性改善不明显,因此推测氯霉素的不稳定性是受其他成分的影响,水杨酸的不稳定性是其固有属性。
通过对照品储存溶液稳定性的考察,可为实验室对照品溶液内控管理提供数据参考,有助于减少对照品的损耗,节约药品检验成本[2,19]。对于某些说明书中附有“本品具有引湿性,建议打开包装后一次使用完毕”的对照品,可于首次打开后精密称定多份置于适宜的容量瓶内备用,从而降低检验成本,如中国食品药品检定研究院在售对照品地塞米松磷酸酯[25]为200 mg/支(单价为390元),即可采用首次开封后,按需求单剂量分装的方式储存。
实际生产过程中,环节多而繁琐,常常中间品和成品抽检时间跨度长,增加了对照品的消耗。《中国药典》四部[1]规定,标准物质溶液应临用前配制,否则应证明其适用性。各类制剂质量标准建立的过程中,一般考察为对照品室温和4 ℃条件下24 h内的稳定性,这个时间远远不能满足中间品和成品的时间跨度。文中对5种制剂涉及的8种对照品储存液适用性进行考察,验证其稳定性,为内控效期的制定提供了依据,基本能够保证对照品储备液的效期能够涵盖中间品和成品检验时间的跨度,完成一批检品的检验。
The investigation of the stability of 8 commonly used reference solutions by HPLC
-
摘要:
目的 考察8种常用对照品溶液稳定性,以此确定内控效期。 方法 配制对照品储存溶液,密封保存于2~10 ℃冰箱中,于0、1、4、7、10、14、21、28、35 d采用高效液相色谱法测定各对照品储存溶液与新配制的对照品溶液含量,计算含量变化值。 结果 各对照品溶液在考察期内,外观与新配制对照品溶液一致;色谱中均未出现显著的杂质峰。甲硝唑、氯霉素和水杨酸混合对照品储存7 d,维生素E对照品、替硝唑和醋酸氯己定混合对照品、磺胺嘧啶对照品、地塞米松磷酸酯对照品储存35 d,含量均符合要求。 结论 在2~10 ℃冰箱中,维生素E对照品、替硝唑和醋酸氯己定混合对照品、磺胺嘧啶对照品、地塞米松磷酸酯对照品溶液的效期可定为35 d,甲硝唑、氯霉素和水杨酸混合对照品溶液定为7 d。 Abstract:Objective To investigate the stability of 8 commonly used reference solutions and determine the validity period of internal control. Methods The storage solutions of reference substances were prepared and stored in the refrigerator at 2 to 10 ℃. The content of the storage solutions and the newly prepared reference solutions were determined by HPLC on days 0, 1, 4, 7, 10, 14, 21, 28 and 35, and their change values of the content were calculated. Results During the inspection period, the appearance of each reference solution was consistent with the newly prepared reference solution. There was no significant impurity peak in the chromatography. For mixed references of metronidazole, chloramphenicol and salicylic acid stored for 7 days, vitamin E, mixed references of tinidazole and chlorhexidine acetate, sulfadiazine, dexamethasone phosphate for 35 days, their contents met the requirements. Conclusion Stored in the refrigerator at 2 to 10 ℃, the effective time period of vitamin E reference solution, mixed references solution of tinidazole and chlorhexidine acetate, sulfadiazine reference, dexamethasone phosphate reference solution can be 35 days, and the mixed references solution of metronidazole, chloramphenicol and salicylic acid defined can be 7 days. -
Key words:
- vitamin E /
- new surface Xu /
- compound tinidazole solution /
- sulfadiazine /
- dexamethasone phosphate /
- substance stability /
- HPLC
-
对照品系指国家药品标准中用于鉴别、检查、含量测定、杂质和有关物质检查等的标准物质[1]。《中国药典》中并没有明确规定对照品溶液的存放有效期,但《中国药典》和《药品生产质量管理规范》(GMP)均要求使用单位应对对照品溶液的稳定性和使用效期进行验证,通过研究结果来确定内控效期[1-7]。本实验结合日常检验工作的使用率、制剂中间品和成品抽检的周期,挑选5种制剂(维生素E珍珠乳膏、新面醑、复方替硝唑溶液、磺胺嘧啶鱼肝油滴鼻剂和地塞米松磷酸钠滴鼻液),涉及8种常用的对照品(维生素E、甲硝唑、氯霉素、水杨酸、替硝唑、醋酸氯己定、磺胺嘧啶和地塞米松磷酸酯),按照相应的质量标准方法进行测定[8-14],考察各对照品储备液在2~10 ℃冰箱中的稳定性,为存放效期提供必要依据,从而规定对照品储存的内控时间[15-18]。
1. 仪器与试剂
1.1 仪器
Agilent 1260 型高效液相色谱仪(包括脱气机、四元泵、自动进样系统、G7114A紫外检测器、Chemstation工作站,美国Agilent公司);Agilent 1200 型高效液相色谱仪(包括脱气机、四元泵、自动进样系统、G1314B紫外检测器、Chemstation工作站,美国Agilent公司);PHS-3C型精密 pH计(上海雷磁仪器厂);ME235S电子天平(德国赛多利斯);EX225DZH电子天平(美国奥豪斯)。
1.2 试药
对照品维生素E(批号10062-0007,纯度99.2%)、甲硝唑(批号100191-201808,纯度100.0%)、氯霉素(批号130555-201203,纯度99.8%)、水杨酸(批号100106-201104,纯度99.9%)、替硝唑(批号100336-201704,纯度100.0%)、醋酸氯己定(批号100183-201003,纯度96.2%)、磺胺嘧啶(批号100026-201404,纯度99.7%)、地塞米松磷酸酯(批号101116-201102,纯度98.6%)购自中国食品药品检定研究院;甲醇、乙腈为色谱纯(霍尼韦尔,美国);磷酸、磷酸二氢钾、盐酸、醋酸铵、三乙胺为分析纯;水为纯化水。
2. 方法与结果
2.1 色谱条件
2.1.1 维生素E珍珠乳膏(维生素E)色谱条件[8-9]
色谱柱:Hypersil BDS C18(250 mm×4.6 mm,5 μm),流动相为甲醇,流速为1.5 ml/min,检测波长为284 nm,进样量为10 μl。
2.1.2 新面醑(甲硝唑、氯霉素、水杨酸)色谱条件[10-11]
色谱柱:Hypersil BDS C18(250 mm×4.6 mm,5 μm),流动相为甲醇-0.04%磷酸溶液(V∶V=47∶53),流速为1.0 ml/min,检测波长为284 nm,进样量为10 μl。
2.1.3 复方替硝唑溶液(替硝唑、醋酸氯己定)色谱条件[12]
色谱柱:Hypersil BDS C18(250 mm×4.6 mm,5 μm),以甲醇为流动相A,以甲醇-0.05 mol/L磷酸二氢钾溶液(pH3.5)(V∶V=20∶80)为流动相B,梯度洗脱(0~8 min,0%~55% A;8~15 min,55% A;15~15. 1 min,55%~0% A;15. 1~20 min,0% A),流速为1.0 ml/min,检测波长为280 nm,进样量为10 μl。
2.1.4 磺胺嘧啶鱼肝油滴鼻剂(磺胺嘧啶)色谱条件[13]
色谱柱:Hypersil BDS C18(250 mm×4.6 mm,5 μm),流动相为乙腈-0.3%醋酸铵溶液(V∶V=20∶80),流速为1.0 ml/min,检测波长为260 nm,进样量为10 μl。
2.1.5 地塞米松磷酸钠滴鼻液(地塞米松)色谱条件[14]
色谱柱:Hypersil BDS C18(150 mm×4.6 mm,5 μm),流动相为0.75%三乙胺溶液(磷酸调pH 至3.0)-甲醇-乙腈(V∶V∶V = 55∶40∶5),流速为1.0 ml/min,检测波长为242 nm,进样量为10 μl。
2.2 对照品溶液的制备
2.2.1 维生素E对照品溶液
精密称取维生素E对照品约10 mg,置50 ml量瓶中,加甲醇溶解并稀释至刻度,摇匀,制成每1 ml中约含维生素E 0.2 mg的对照品溶液。
2.2.2 甲硝唑、氯霉素、水杨酸混合对照品溶液
精密称取甲硝唑、氯霉素对照品各约10 mg,分别置10 ml量瓶中,加流动相溶解并稀释至刻度,摇匀;另精密称取水杨酸对照品约12.5 mg,置100 ml量瓶中,加流动相溶解并稀释至刻度,摇匀;精密量取上述甲硝唑、氯霉素对照品稀释液各5 ml、水杨酸对照品稀释液10 ml,置于同一25 ml量瓶中,加流动相稀释至刻度,摇匀,制成每1 ml中约含甲硝唑、氯霉素和水杨酸分别为0.2 mg、0.2 mg和0.05 mg的混合对照品溶液。
2.2.3 替硝唑、醋酸氯己定混合对照品溶液
精密称取替硝唑对照品约10 mg、醋酸氯己定对照品约10 mg置于同一50 ml量瓶中,加水溶解并稀释成每1 ml中约含替硝唑、醋酸氯己定各0.2 mg的混合对照品溶液。
2.2.4 磺胺嘧啶对照品溶液
精密称取磺胺嘧啶对照品约12.5 mg,置25 ml量瓶中,加稀盐酸1 ml溶解后,用流动相稀释至刻度,摇匀。精密量取2 ml,置10 ml量瓶中,用流动相稀释至刻度,摇匀,制成每1 ml中约含磺胺嘧啶0.1 mg的对照品溶液。
2.2.5 地塞米松磷酸酯对照品溶液
精密称取地塞米松磷酸酯对照品约15 mg,置50 ml量瓶中,加水溶解并稀释至刻度,摇匀;精密量取稀释液3 ml,置25 ml量瓶中,加流动相稀释至刻度,摇匀,制成每1 ml 约含地塞米松磷酸酯0.036 mg的溶液。
上述对照品溶液均置于具塞的量瓶中,且用封口膜封口,取用后立即冷藏(2~10 ℃)保存,分析前需放至室温。
2.3 系统适用性试验
按“2.1”项下色谱条件进样测定,记录色谱图,详见图1。各色谱条件下,各主成分峰分离度均大于1.5,理论板数满足相应制剂标准要求,且各出峰情况与文献一致[8-14]。
2.4 对照品溶液稳定性考察
2.4.1 试验方法[15-24]
将上述3种对照品溶液在保存0、1、4、7、10、14、21、28、35 d时,与当天新鲜配制的相应对照品溶液按照相应色谱条件分别进样,分别计算平均峰面积,以当天新鲜配制的对照品溶液计算对照品储存溶液的含量值。
2.4.2 结果计算[2,20-23]
每个测试时间点的结果都是用新鲜配制的对照品溶液的平均响应值,来重新计算用于研究效期的对照品溶液的标示量,基于下述公式进行计算:
$$ \mathrm{X}\mathrm{\%}=\frac{{\mathrm{A}}_{\mathrm{T}}\times {\mathrm{C}}_{\mathrm{N}}}{{\mathrm{A}}_{\mathrm{N}}\times {\mathrm{C}}_{\mathrm{T}}}\times 100\mathrm{\%} $$ 式中,AN和CN表示新鲜配制对照品的峰面积和浓度;AT和CT表示对照品储存溶液的峰面积和浓度。
2.4.3 判断标准[2]
各对照品溶液均未出现浑浊、沉淀等异常现象;测试用对照品溶液与新鲜配制的对照品溶液外观一致;色谱图中均未出现显著的杂质峰;每个分析测试点,要求对照品储存溶液的标示量与零点的差异不得超过2.0%。
2.4.4 结果
上述各类对照品溶液在2~10 ℃冰箱内密封储存35 d,测试用对照品溶液外观与新配制对照品溶液一致,未出现浑浊、沉淀等现象;色谱中均未出现显著的杂质峰,每个分析测试点,对照品溶液的含量变化如图2所示,维生素E储存35 d、甲硝唑、氯霉素和水杨酸混合对照品储存7 d、替硝唑和醋酸氯己定混合对照品储存35 d、磺胺嘧啶储存35 d、地塞米松磷酸酯储存35 d,含量符合要求。结合含量标准要求,在2~10 ℃冰箱中,维生素E对照品、替硝唑和醋酸氯己定混合对照品、磺胺嘧啶对照品、地塞米松磷酸酯对照品溶液的效期可定为35 d,甲硝唑、氯霉素和水杨酸混合对照品溶液定为7 d。
3. 讨论
对照品溶液是药品检验的重要部分,对照品储存在冰箱中需要以封口膜封口,减少溶剂的挥发;从冰箱中取出时,需超声半分钟或放至室温,摇匀后再取下封口膜取样,避免直接打开引起瓶内挥发的溶剂流失,影响测定结果。
考察结果中发现甲硝唑、氯霉素和水杨酸混合对照品溶液稳定性较差,各组分储存期分别为35、21和7 d。采用三组分单独配制储存进行考察,结果发现甲硝唑、氯霉素、水杨酸溶液的储存时间分别为35、35和10 d,同比混合对照品溶液中,氯霉素稳定性增加,但对水杨酸稳定性改善不明显,因此推测氯霉素的不稳定性是受其他成分的影响,水杨酸的不稳定性是其固有属性。
通过对照品储存溶液稳定性的考察,可为实验室对照品溶液内控管理提供数据参考,有助于减少对照品的损耗,节约药品检验成本[2,19]。对于某些说明书中附有“本品具有引湿性,建议打开包装后一次使用完毕”的对照品,可于首次打开后精密称定多份置于适宜的容量瓶内备用,从而降低检验成本,如中国食品药品检定研究院在售对照品地塞米松磷酸酯[25]为200 mg/支(单价为390元),即可采用首次开封后,按需求单剂量分装的方式储存。
实际生产过程中,环节多而繁琐,常常中间品和成品抽检时间跨度长,增加了对照品的消耗。《中国药典》四部[1]规定,标准物质溶液应临用前配制,否则应证明其适用性。各类制剂质量标准建立的过程中,一般考察为对照品室温和4 ℃条件下24 h内的稳定性,这个时间远远不能满足中间品和成品的时间跨度。文中对5种制剂涉及的8种对照品储存液适用性进行考察,验证其稳定性,为内控效期的制定提供了依据,基本能够保证对照品储备液的效期能够涵盖中间品和成品检验时间的跨度,完成一批检品的检验。
-
-
[1] 国家药典委员会. 中华人民共和国药典2020年版四部[S]. 北京: 中国医药科技出版社, 2020: 34-35. [2] 国家食品药品监督管理局药品认证管理中心. 药品GMP指南—质量控制实验室与物料系统[S]. 北京: 中国医药科技出版社, 2011: 87-98. [3] 何国强. 制药工艺验证实施手册[M]. 北京: 化学工业出版社, 2012: 230-256. [4] 肖丽华, 马玲云, 马双成, 等. 国家药品标准物质稳定性核查探讨[J]. 中国药师, 2012, 15(4):553-554. doi: 10.3969/j.issn.1008-049X.2012.04.044 [5] The International Standard Organization. ISO guide 31: 2015 reference materials-contents of certificates, labels and accompanying documentation[S]. 2015. [6] The United States Pharmacopeial Convention. USP reference standards catalog[EB/OL].[2020-09-05]. https://www.usp.org/reference-standards/reference-standards-catalog. [7] World Health Organization. WHO technical report series No.943 annex 3 general guidelines for the establishment maintenance and distribution of chemical reference substances[S]. 2007. [8] 蔡素芬, 黄久遂, 徐晓. HPLC法测定维生素E乳中维生素E的含量[J]. 今日药学, 2014, 24(10):729-731. [9] 何玉川, 张亚茹. 高效液相色谱法测定维生素E乳中维生素E的含量[J]. 中国当代医药, 2013, 20(21):64-65. doi: 10.3969/j.issn.1674-4721.2013.21.030 [10] 刘徽, 蔡琳, 廖海燕. HPLC法测定新面醑中甲硝唑、氯霉素、水杨酸含量[J]. 西南国防医药, 2018, 28(3):222-224. doi: 10.3969/j.issn.1004-0188.2018.03.008 [11] 杜建红, 钟元高, 何德云, 等. 高效液相色谱法同时测定新面醑中甲硝唑、氯霉素、水杨酸三组分含量[J]. 世界最新医学信息文摘, 2018, 18(72):270-271, 275. [12] 高磊, 贾燕花, 王晓青, 等. RP-HPLC同时测定复方替硝唑溶液中替硝唑和醋酸氯己定的含量[J]. 河北医药, 2015, 37(2):290-291. [13] 中国人民解放军中央军委后勤保障部卫生局. 磺胺嘧啶鱼肝油滴鼻剂(总JBF705013-2018)[S]. [14] 中国人民解放军中央军委后勤保障部卫生局. 地塞米松磷酸钠滴鼻液(总JBF705001-2016)[S]. [15] 陈亚飞, 肖新月, 何平, 等. 标准物质稳定性考察规范解读和有效期管理方式的研究[J]. 中国药事, 2018, 32(3):317-322. [16] 金建平. 药品检测实验室标准物质的管理、使用和期间核查[J]. 海峡药学, 2013, 25(2):270-272. doi: 10.3969/j.issn.1006-3765.2013.02.156 [17] 杨文慧, 路盛. 实验室质量控制中标准物质管理及期间核查方法探讨[J]. 中国卫生检验杂志, 2012, 22(8):1990-1991. [18] 高艾英, 韩德娟. 实验室常用标准溶液稳定性的因素评定[J]. 现代食品, 2019(3):153-154, 158. [19] 解联合, 刘敏红, 刘平, 等. 标准溶液的校正[J]. 中国卫生检验杂志, 2003, 13(1):116-117. doi: 10.3969/j.issn.1004-8685.2003.01.071 [20] 杨金颖, 纪京辉. 高效液相色谱法考察五种常用对照品溶液的稳定性[J]. 山西医药杂志, 2018, 47(7):814-815. doi: 10.3969/j.issn.0253-9926.2018.07.033 [21] 聂黎行, 张烨, 戴忠, 等. 桂皮醛在常用溶剂中稳定性考察—对中国药典2015年版桂皮醛含量测定方法的探讨[J]. 药物分析杂志, 2016, 36(9):1679-1683. [22] 邓凯, 梁雅甜. 水杨酸对照品溶液稳定性研究[J]. 轻工科技, 2015, 31(10):30-31. [23] 常艳, 马双成, 胡昌勤. 美洛西林标准物质短期稳定性研究[J]. 药物分析杂志, 2013, 33(4):684-688. [24] 陈永艳, 吕佳, 邢方潇, 等. 饮用水检测中抗生素类标准物质稳定性研究[J]. 中国抗生素杂志, 2019, 44(6):758-763. doi: 10.3969/j.issn.1001-8689.2019.06.019 [25] 中国食品药品检定研究院. 国家药品标准物质使用说明书[EB/OL].[2020-09-05]. http://aoc.nifdc.org.cn/sell/uploadft/154684100582878288779436885788. -





 下载:
下载:
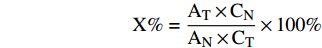

 下载:
下载:


