-
肝纤维化(hepatic fibrosis,HF)是以肝内细胞外基质(extracellular matrix protein,ECM)过度沉积和纤维瘢痕形成为特征的慢性肝病,在世界范围内具有较高的发病率和病死率,持续发展导致肝硬化、肝癌的发生[1]。肝纤维化发病机制复杂,病毒性肝炎、自身免疫性肝炎、非酒精性脂肪性肝病、胆汁淤积性肝病等均可能导致慢性肝炎症,并最终导致肝纤维化[2]。然而,除肝移植外,目前尚无有效治疗肝纤维化的方法,针对肝纤维化早期识别和治疗对于预防相关负面后果至关重要。鉴于肝脏是人体最大的器官和主要代谢枢纽,探讨肝纤维化的代谢特征有望发现新的标志物和治疗靶点。
二氢丹参酮Ⅰ(dihydrotanshinone I,DHI)是中药丹参中的亲脂性成分,被认为是一种潜在的治疗肝纤维化的药物,其肝脏保护作用、抗癌作用、抗流感活性、抗炎作用等生物学功能已多次报道[3-5]。在本课题组前期扶正化瘀方抗肝纤维化机制研究中发现DHI是扶正化瘀胶囊的重要药效物质基础,也在细胞活性实验中证明其能显著抑制细胞活性发挥抗肝纤维化作用[6]。然而,DHI对肝纤维化治疗作用的体内药效及机制尚不明确。本研究利用肝脏代谢组学方法研究肝纤维化密切相关的生物标志物,探索肝纤维化相关病理过程,同时采用DHI进行干预,研究其对肝纤维化的治疗作用及作用机制,为肝纤维化早期诊断、有效治疗提供科学依据。
-
METTLER AE240 型电子天平(瑞士梅特勒公司);FRESCO17台式冷冻离心机 (Thermo Fisher,美国);DZG-6020真空干燥箱 (上海益恒实验仪器公司);Agilent 1290 Infinity 液相色谱仪、Agilent 6538 Q-TOF/MS 质谱仪、Micro17高速离心机(Thermo Fisher Scientific,美国);HSS T3柱(2.1 mm×100 mm,2.5μm)(Waters,美国)。
-
DHI(纯度 98%,上海一飞生物科技有限公司);硫代乙酰胺(thioacetamide,TAA,东京化成工业株式会社);甲醇、乙腈(均为色谱纯,德国Merck公司),甲酸(色谱纯,ROE scientific INC,美国);水为实验室制备的超纯水,其他试剂均为分析纯。
-
SD大鼠,雄性,质量(200~250 g),共28只,购自中国科学院上海实验动物中心,合格证号:SCXK(沪)2012-0002。饲养于海军军医大学实验动物中心,遵循动物实验的标准操作规范。饲养条件:温度(22±2)℃,相对湿度40%~60%,12 h昼夜交替循环的条件下笼养。
-
将28只雄性SD大鼠随机分为4组:正常组、肝纤维化模型组、DHI低剂量组和DHI高剂量组,每组7只。24 h适应性饲养后,除正常组外,模型组及不同用药剂量干预组每周3次腹腔注射200 mg/kg TAA,持续给TAA造模8周;同时,自第5周起,按照给药剂量持续给药4周:正常组、模型组,每日给予生理盐水10 ml/kg;DHI低剂量组,每日给予DHI15 mg/kg;DHI高剂量组,每日给予30 mg/kg。
-
最后一次给药24 h后,采用脊椎脱臼法处死大鼠。快速切除肝脏后,用0 ℃生理盐水冲洗并立即放于液氮中快速冷冻,储存于−80 ℃冰箱直至分析。
-
将冻存的肝脏组织置于室温自然解冻,取约100 mg肝脏样本于匀浆管中,加入800μl甲醇,在60 Hz下充分匀浆至没有纤维颗粒,4 ℃离心15 min(14 500×g)后取上清液置于1.5 ml的离心管中,氮气吹干。在上述氮气吹干的样品残渣中加入300 μl含内标甲醇涡旋30 s(内标为L-2-氯苯丙氨酸,浓度为5 μg/ml),每个样品取10μl混匀作为质量控制样品。
-
色谱条件:Agilent 1290 Infinity UHPLC,色谱柱:Waters XSelect HSS T3 column色谱柱,柱温:30 ℃;进样量:3 μl;流动相A:含0.1 %甲酸的水,流动相B:含0.1 %甲酸的乙腈。流速:0.4 ml/min;梯度洗脱条件:0~2 min,2 %B,2~17 min,2 %~98 % B,17~19 min,98 %B。质谱条件:Agilent 6530 Accurate-Mass QTOF/MS,离子源:电喷雾(ESI)离子源,正、负离子检测模式;干燥气温度:350 ℃,干燥气体流量:11 L/min;碎裂电压:120 V;毛细管电压:4 000 V(ESI+)/3 500 V(ESI-);质谱扫描范围:50~1 500 m/z。
-
将采集的质谱数据转换为mzData格式文件,然后通过R软件XCMS程序将质谱数据转化为含有保留时间、质核比、峰强度的数据矩阵。保留频数超过80%的质核比数据,并对所有峰面积以内标峰面积和肝组织质量进行归一化处理。
-
将上述获得的二维矩阵列表导入SIMCA 14.1软件中进行多元统计分析,采用正交偏最小二乘判别分析研究各组间差异,并得到变量VIP值。正常组和模型组组间比较采用独立样本t检验,采用VIP>1,且选择差异具有显著性(P<0.05)的变量作为潜在的差异代谢物,然后检索数据库(HMDB、METLIN、KEGG数据库),筛选出潜在的差异代谢物。
-
使用SPSS 21.0统计软件进行数据统计分析,组间数据采用单因素方差分析(ANOVA),两组样本分析采用独立样本t检验,分析数据差异的统计学意义,以P<0.05为差异有统计学意义。
-
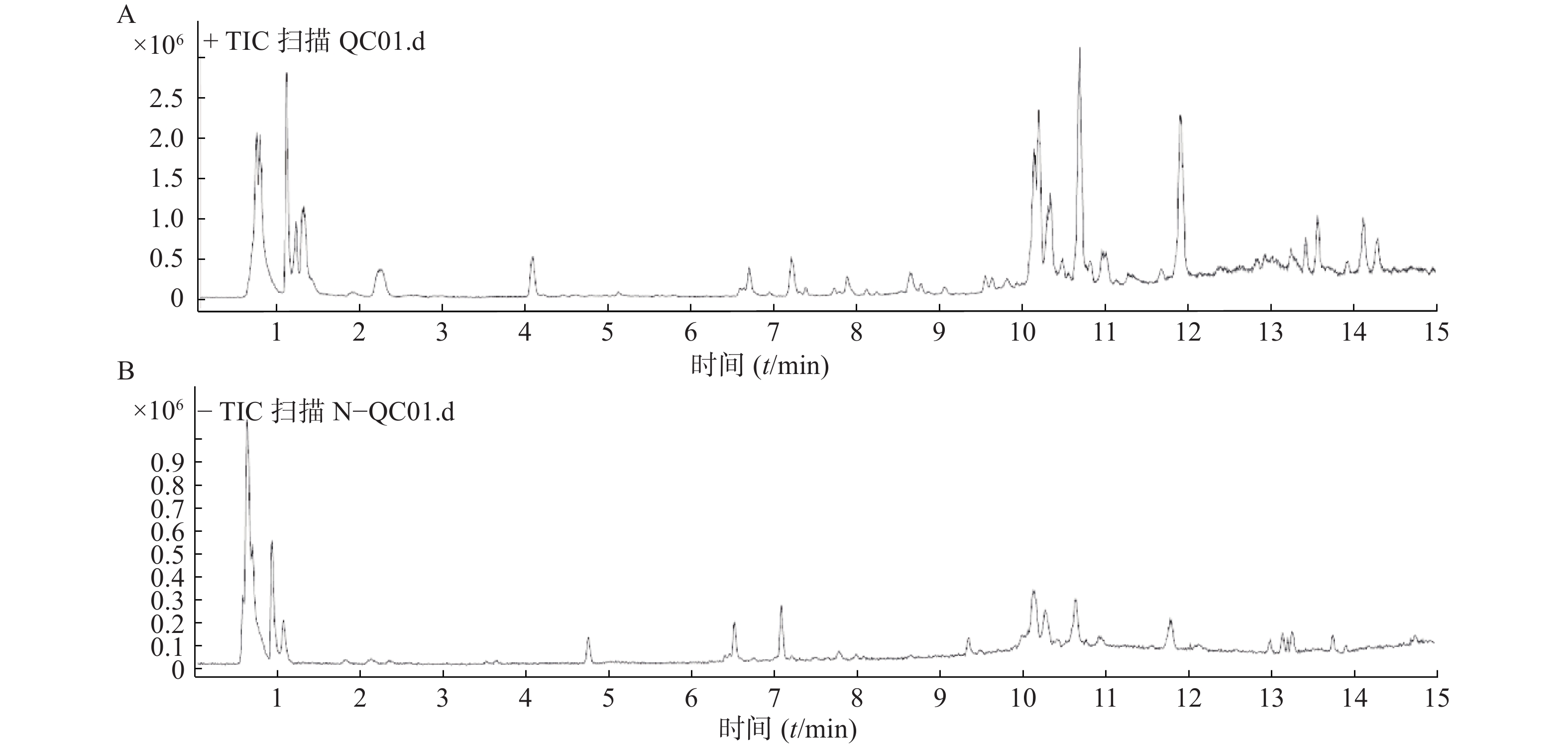
本研究采用UPLC-Q-TOF/MS在正、负两种模式下对肝组织进行代谢组学分析,两种模式下典型的总离子流图见图1。代谢组学数据的稳定性、重现性对研究的可靠性非常重要,为考察实验的系统稳定性,本研究从每个肝组织样品中取10 μl混匀后作为质量控制样品。在样品序列一开始连续进样10针QC样品,并按每7个样品再进样一针,共进样14次。正、负离子模式下,QC样品均显示良好的聚集状况,证明该分析系统稳定可靠。
-
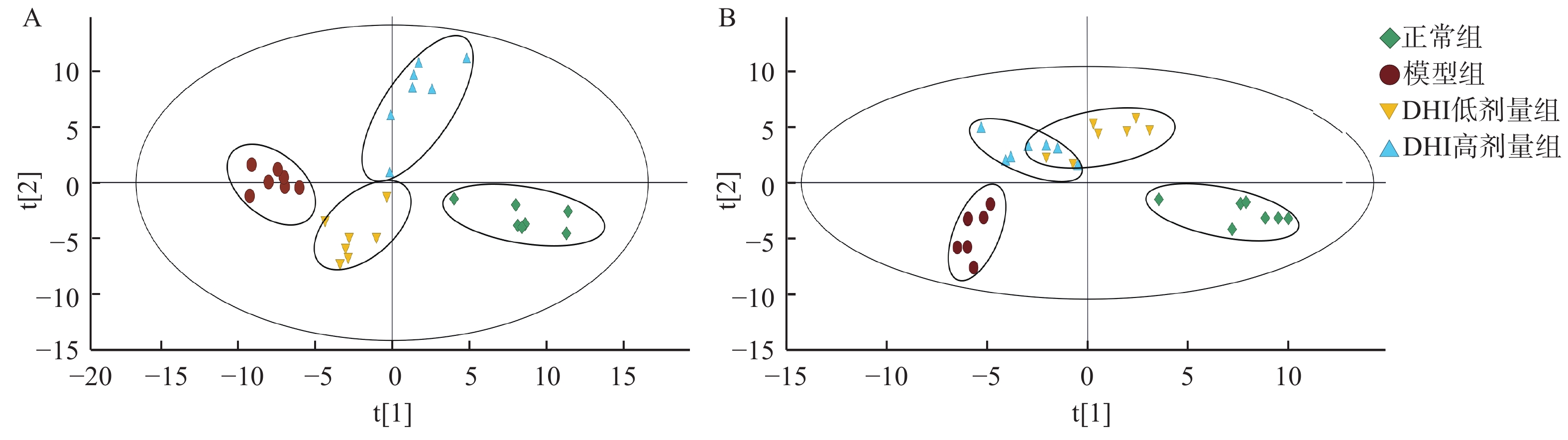
经过数据处理后,LC-MS数据集在正离子模式下得到368个离子,在负离子模式下得到249个离子。根据OPLS-DA方法对数据进行分析,OPLS-DA是一种多因变量对多自变量的回归建模方法,最大特点是可以去除自变量和分类变量无关的分类变异,根据得分图可以揭示数据离散程度,发现异常值[7]。在得分图上具有相似的代谢物组成的样本,处在比较相似的位置,样本间距越远代表代谢物差异越大,样本间生理状态相差越大。将正常组、模型组、DHI低剂量组和DHI高剂量组的LC-MS数据导入到SIMCA进行分析,其得分如图2A、2B所示,正常组与模型组样本各自聚为一类,并且完全分离,说明肝纤维化大鼠模型的肝组织代谢轮廓发生显著改变,代谢物的种类或水平发生了明显变化。DHI给药组(DHI低剂量组、DHI高剂量组)能够与模型组明显区分,并向正常组靠近,表明DHI给药组可恢复部分代谢物至正常水平。
-
OPLS-DA可用于寻找导致聚类间显著差异的变量,筛选正常组和肝纤维化大鼠模型组间潜在的差异代谢物。基于OPLS-DA模式下VIP>1筛选两组间的差异代谢物,进行t检验后,筛出模型组和正常组间差异具有显著性的变量(P<0.05)。基于VIP和t检验以及HMDB和KEGG等数据库比对,筛选出38个与TAA诱导肝纤维化大鼠模型相关的较为重要的差异代谢物作为潜在生物标志物(表1)。通过KEGG、HMDB等数据库查询,我们发现这些代谢物主要涉及谷胱甘肽代谢、褪黑素代谢、氨基酸代谢、脂质代谢、三羧酸循环等途径。
表 1 TAA诱导肝纤维化相关的差异代谢物及其代谢通路
编号 代谢物 精确分子量 加合离子 分子式 调节趋势 相关通路 1 丁二酸 118.026 6 M-H C4H6O4 ↓* TCA循环 2 柠檬酸 130.026 6 M+NH4 C5H6O4 ↑** 脂肪酸代谢 3 戊二酸 130.026 6 M+FA-H C5H6O4 ↓*** / 4 L-天冬氨酸 133.037 5 M-H C4H7NO4 ↑* 丙氨酸、天冬氨酸和谷氨酸代谢 5 丝氨酸甘氨酸 162.064 1 M+H-H2O C5H10N2O4 ↑* 二肽 6 左旋肉碱 162.113 0 M+H C7H16NO3 ↓** 肉碱合成 7 2-甲基-3-苯基丙酸 164.083 7 M+H-H2O C10H12O2 ↑*** / 8 顺乌头酸 174.016 4 M-H C6H6O6 ↓** 三羧酸循环 9 半胱氨酰甘氨酸 178.041 2 M+H C5H10N2O3S ↓*** 谷胱甘肽代谢 10 缬氨冬酰胺 231.121 9 M+NH4 C9H17N3O4 ↓* 二肽 11 尿苷 244.069 5 M-H C9H12N2O6 ↓** 嘧啶代谢 12 甘油磷酸甘油 246.050 5 M-H C6H15O8P ↓** 脂质代谢 13 环状6-羟基褪黑素 246.100 4 M+Na C13H14N2O3 ↓** 褪黑素代谢 14 7,8-二氢蝶呤 255.096 8 M+H C9H13N5O4 ↓* 蝶呤生物合成 15 谷氨酰胺天冬酰胺 261.096 1 M+Na C9H15N3O6 ↑*** 二肽 16 γ-谷氨酰鸟氨酸 261.132 5 M+NH4 C10H19N3O5 ↑*** 二肽 17 3-羟基异戊酰肉碱 261.1576 M+NH4 C12H23NO5 ↓*** 脂肪酸代谢 18 天冬氨酰谷氨酸 262.080 1 M+FA-H C9H14N2O7 ↓*** 二肽 19 N-乙酰5-羟色胺硫酸盐 298.062 3 M-H20-H C12H14N2O5S ↓*** 褪黑素代谢 20 视黄酯 302.224 6 M-H C20H30O2 ↓* 脂肪酸代谢 21 谷胱甘肽 307.083 8 M+H C10H17N3O6S ↓** 谷胱甘肽代谢 22 吲哚酚葡萄糖醛酸苷 309.084 9 M+H C14H15NO7 ↓** 脂质代谢 23 3'-AMP 347.063 1 M+H C10H14N5O7P ↓* 胆酸生物合成 24 苯酰甘氨酸 397.355 6 M+Na C24H47NO3 ↑* 脂肪酸代谢 25 花生四烯酰肉碱 448.342 1 M+H C27H46NO4 ↓** 脂质代谢 26 花生四烯基肉碱 455.397 5 M+H-H2O C27H53NO4 ↑** 脂肪酸代谢 27 溶血磷脂酰乙醇胺(0∶0/18∶2(9Z,12Z)) 477.285 5 M+H C23H44NO7P ↓* 甘油磷脂代谢 28 溶血磷脂酰乙醇胺(18∶2(9Z,12Z)/0∶0) 477.285 5 M-H C23H44NO7P ↓* 甘油磷脂代谢 29 溶血磷脂酰乙醇胺(0∶0/20∶5(5Z,8Z,11Z,14Z,17Z)) 499.269 9 M+FA-H C25H42NO7P ↓* 甘油磷脂代谢 30 牛磺熊去氧胆酸 499.296 8 M-H C26H45NO6S ↓* 脂质代谢 31 溶血磷脂酰乙醇胺(20∶4(8Z,11Z,14Z,17Z)/0∶0) 501.285 5 M+H C25H44NO7P ↓* 甘油磷脂代谢 32 二酰甘油(16∶1n7/0∶0/18∶3n3) 588.475 4 M+H-H2O C37H64O5 ↑*** 脂质代谢 33 二酰甘油(14∶0/0∶0/22∶5n3) 614.491 0 M+H C39H66O5 ↑*** 脂质代谢 34 磷脂神经酰胺(d18∶1/16∶0) 617.478 4 M+H-H2O C34H68NO6P ↑*** 鞘脂代谢 35 鞘糖脂(d18∶1/12∶0) 643.502 3 M+H C36H69NO8 ↑*** 磷脂代谢 36 磷脂酰乙醇胺(16∶0/P-16∶0) 675.520 3 M+H-H2O C37H74NO7P ↑** 磷脂代谢 37 磷脂酰乙醇胺(18∶0/15∶0) 705.530 9 M+H-H2O C38H76NO8P ↑*** 磷脂代谢 38 心磷脂(i-13∶0/i-22∶0/i-12∶0/i-13∶0) 1 296.909 6 M+H-H2O C69H134O17P2 ↓* 磷脂代谢 *P<0.05、**P<0.01、***P<0.001,模型组与正常组比较 -
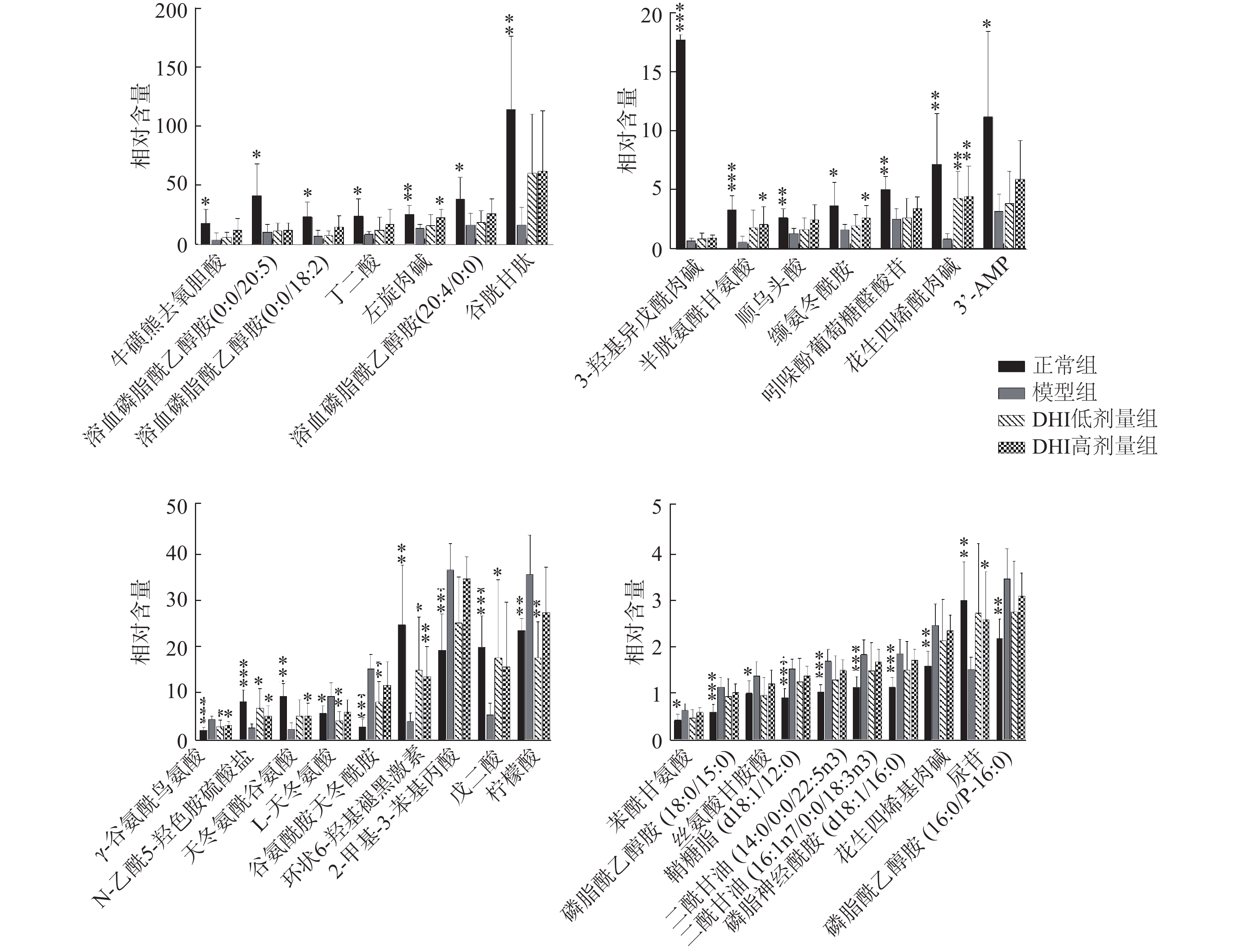
以肝纤维化相关的差异代谢物的相对含量作为检测指标可以评价DHI对肝纤维化的治疗作用,比较发现33种代谢物的含量发生明显逆转(图3),同时,有14种代谢物的含量回调与DHI的剂量成正相关性,即高剂量组比低剂量组回调更多(图3A、3B)。
-
肝纤维化是一种发病机制复杂,可导致肝硬化、肝衰竭甚至肝癌等严重肝脏疾病的慢性流行肝病,然而目前并没有药物可以治疗肝纤维化,中药及其活性成分由于其多靶点、多通路等特点被认为是肝纤维化治疗的潜在药物。代谢组学可以对生物体内小分子代谢产物进行动态分析,通过分析阐述代谢物与生理病理变化间的联系,对肝纤维化的机制进一步阐述,也能通过肝纤维化相关差异代谢物的含量相对变化分析药物对肝纤维化模型的药效作用。本研究用肝脏代谢组学方法分析了与TAA诱导的肝纤维化模型密切相关的38种代谢物,主要涉及谷胱甘肽代谢、褪黑素代谢、氨基酸代谢、脂质代谢、三羧酸循环等途径,DHI能够通过调节部分代谢通路发挥预防和治疗肝纤维化作用。
-
肝纤维化的产生伴随着肝细胞死亡和肝星状细胞(HSCs)的活化,HSCs约占正常人肝脏中非实质细胞的1/3和总驻留细胞的15%,HSCs从静态到激活会使得ECM过剩表达而导致纤维化,而氧化应激在HSCs激活和ECM形成中发挥重要的促进作用[1, 8]。谷胱甘肽(GSH)是人体内含量最丰富的抗氧化剂,也是体内氧化防御体系的主要组成成分之一[9]。GSH可以在谷胱甘肽过氧化物酶和谷胱甘肽-S-转移酶以及谷胱甘肽还原酶的作用下与其氧化态相互转换,清除部分有机过氧化物,调节体内的氧化还原稳态,缓解氧化应激对组织造成的损伤[10-11]。有研究表明,在对乙酰氨基酚、四氯化碳、重金属砷等诱导下,大鼠肝组织中GSH含量下降[12]。本研究中,TAA诱导的肝纤维化大鼠模型肝组织中GSH显著下降,这与谷胱甘肽在其他肝损模型中下调的趋势一致。经过DHI干预后GSH回调,且高剂量DHI比低剂量组回调比例更大,这说明DHI可能调整体内谷胱甘肽代谢通路,通过提高体内谷胱甘肽含量恢复肝组织抗氧化功能,缓解氧化应激对肝脏的进一步损伤,从而起到抗肝纤维化作用。
-
肝纤维化过程中,抑制HSC的激活和增殖是预防和治疗肝纤维的重要途径。血小板衍生生长因子(PDGF)可以激活JAK2/STAT3信号通路,致使HSC增殖,并抑制HSC凋亡[13]。已有研究证明,褪黑素通过抑制JAK2/STAT3相关信号通路或抗氧化机制来抑制HSC的激活和增殖从而发挥肝脏保护作用[14-15]。在本研究中,环6-羟基褪黑素及N-乙酰血清素硫酸盐均为褪黑素代谢产物,在模型组中含量显著增加,说明褪黑素被大量代谢,肝脏保护作用被抑制。经过DHI的干预后两种褪黑素代谢产物均回调,这提示DHI可能通过调整褪黑素代谢,回调褪黑素及其代谢产物的机体内含量发挥抗肝纤维化活性。
-
肝脏是机体物质代谢的中枢器官,在氨基酸的新陈代谢和蛋白质的合成与分解中发挥重要作用。天冬氨酸是一种酸性氨基酸。天冬氨酸在哺乳动物中一般被认为是一种营养上非必需的氨基酸。然而,越来越多的文献表明,天冬氨酸在包括肝脏生理学在内的许多生物和生理过程中起着重要作用,如合成精氨酸以维持巨噬细胞应对免疫挑战,同时,也有证据表明天冬氨酸可以减轻肝损伤、增强肝脏功能[16]。本研究发现TAA诱导大鼠肝纤维化后,与正常组比较,模型组中丙氨酸、天冬氨酸和谷氨酸代谢通路被干扰,L-天冬氨酸含量显著变化,经过DHI的干预后回调,这提示DHI可能调整丙氨酸、天冬氨酸和谷氨酸代谢通路,改变体内天冬氨酸含量发挥肝保护作用。
-
脂质不仅是细胞膜的组成成分,而且参与信号转导。磷脂酰胆碱、鞘脂、溶血性磷脂酰胆碱是血清脂蛋白和细胞膜的重要组成成分。溶血磷脂酰乙醇胺是磷脂酶A1水解磷脂酰乙醇胺(PE)失去一分子脂肪酸生成的产物,作为一种溶血卵磷脂,在肝脏中与卵磷脂一起在线粒体间进行转移[17]。有研究证明,PE通过N-甲基转移酶生成PC的通路约占PC产生量的30%,磷脂酰胆碱为肝脏重要营养来源,可以拮抗肝脏受病毒、药物、酒精及其他有毒物质的侵害,防止肝纤维化[9]。肝脏是脂质生成和脂肪酸氧化等脂类代谢的主要场所,肝纤维化时可以引起脂质合成、转运及分解代谢的普遍紊乱,而脂质代谢异常又会加重肝损害,引起肝脏的脂毒性[18]。在本研究中,4种LysoPE在模型组中均发生下降,另外一些磷脂代谢相关物质,如GlcCer(d18:1/12:0)、PE(16:0/P-16:0)、PE(18:0/15:0)、CL(i-13:0/i-22:0/i-12:0/i-13:0)和脂质代谢相关物质如二酰甘油(DG)、甘油磷酸甘油、牛磺酸熊去氧胆酸等在正常组与模型组大鼠中也存在显著差异,说明TAA诱导的大鼠肝纤维化模型脂质代谢的紊乱。经过DHI干预治疗后,代谢物水平不同程度得到回调,表明DHI可通过干预多个脂质代谢通路发挥其抗肝纤维化活性。
-
三羧酸循环是糖、脂肪、氨基酸三大营养素的最终代谢通路,在能量代谢、提供生物合成的前体中起重要作用。琥珀酸既是三羧酸循环的的重要中间产物,也是一种重要的细胞外信号分子,在信号传递、炎症反应、肝纤维化的发生发展中发挥着重要作用[19]。在本研究中,肝纤维化模型组大鼠琥珀酸的代谢变化趋势均与正常大鼠相反,而给予DHI后趋近正常,说明DHI能够改善肝纤维化大鼠的能量代谢。
-
本研究建立了LC-MS代谢组学分析的方法,通过OPLS-DA筛选出与肝纤维化密切相关的38种差异代谢产物,主要涉及谷胱甘肽代谢、褪黑素代谢、氨基酸代谢、脂质代谢、三羧酸循环等途径。基于38种差异代谢物在正常组、模型组及DHI给药组之间相对含量的差异,对DHI预防治疗大鼠肝纤维化模型的药效进行了评价,结果表明DHI能够回调34种潜在差异代谢物的相对含量,调节部分失衡代谢通路,发挥抗肝纤维化作用。本研究为肝纤维化的新标志物和治疗靶点的发现以及DHI作为抗肝纤维化潜在药物的进一步开发应用提供实验依据。
Metabolomics study of dihydrotanshinone Ⅰ on hepatic fibrosis with LC-MS technology
-
摘要:
目的 利用肝脏代谢组学方法监测肝纤维化相关的代谢变化,评价二氢丹参酮Ⅰ治疗肝纤维化的药效及作用机制。 方法 将28只雄性SD大鼠随机分为4组:正常组、肝纤维化模型组和二氢丹参酮Ⅰ低剂量组、二氢丹参酮Ⅰ高剂量组。采用硫代乙酰胺诱导肝纤维化模型,给予4周治疗后,取大鼠肝脏进行液相色谱-质谱分析,结合OPLS-DA模式识别方法筛选模型组和正常组之间的差异代谢物,并以此评价二氢丹参酮Ⅰ对肝纤维化的治疗作用。 结果 通过肝脏代谢组学分析鉴定了38种肝纤维化相关的生物标志物,涉及谷胱甘肽代谢、褪黑素代谢、氨基酸代谢、脂质代谢、三羧酸循环等代谢通路,同时数据显示二氢丹参酮Ⅰ的干预对肝纤维化有改善作用。 结论 二氢丹参酮Ⅰ能够通过调节失衡的谷胱甘肽代谢、褪黑素代谢、氨基酸代谢、脂质代谢、三羧酸循环等途径而发挥预防和治疗肝纤维化作用。 Abstract:Objective To evaluate therapeutic effects of dihydrotanshinone Ⅰ on hepatic fibrosis based on liver metabolomics method. Methods 28 rats were randomly divided into four groups including control group, hepatic fibrosis model group and dihydrotanshinone Ⅰ low dose group and dihydrotanshinone Ⅰ high dose group. The dihydrotanshinone Ⅰ treated groups received dihydrotanshinone Ⅰ for 28 days. The rat liver samples were collected and analyzed by liquid chromatography-mass spectrometer (LC-MS). The OPLS-DA pattern recognition analysis of metabolomics differences among the groups and therapeutic effects of dihydrotanshinone Ⅰ on hepatic fibrosis were evaluated. Results 38 metabolites were identified through liver metabolomics analysis. The possible mechanism of hepatic fibrosis was mainly involved glutathione metabolism, melatonin metabolism, amino acid metabolism, lipid metabolism and TCA cycle. The hepatic fibrosis induced by TAA was reversed by dihydrotanshinone Ⅰ. Conclusion Dihydrotanshinone Ⅰ provided satisfactory therapeutical effects on hepatic fibrosis through partially regulating the perturbed glutathione metabolism, melatonin metabolism, amino acid metabolism, lipid metabolism, TCA cycle. -
Key words:
- hepatic fibrosis /
- dihydrotanshinone I /
- LC-MS /
- metabolomics
-
延胡索为罂粟科植物延胡索(Corydalis yanhusuo W.T.Wang)的干燥块茎,主产地为浙江、安徽、江苏等地,中医药应用历史悠久。其具有活血、行气、止痛之功效,用于胸胁,脘腹疼痛,胸痹心痛,经闭痛经,产后淤阻,跌扑肿痛[1]。现代科学研究发现延胡索主要含有生物碱、有机酸、甾体、挥发油、糖类、氨基酸等活性成分[2-3],具有镇痛、镇静催眠、抗溃疡、抗菌、抗炎、抗肿瘤、扩张冠状动脉,增加冠脉血流量,抑制血小板聚集,抗心律失常,改善心肌供氧,增加心输出量等药理作用[4]。含延胡索的中药处方及延胡索乙素制剂广泛应用于胃痛、伤痛、心绞痛、痛经等多种痛症。延胡索临床应用常以炮制品入药,目前常用的炮制方法主要有炒制、醋制、酒制等[5],其中又以醋制为主,醋制可以提高主要活性成分延胡索乙素的含量[6-7],《中国药典》(2015年版)收载醋制延胡索为醋炙和醋煮,醋蒸法始载于明代卢之颐的《本草乘雅半偈》,但药典及其他炮制规范等地方标准也无收载。本实验是在《安徽省中药饮片炮制规范》(2019年版)修订课题的基础上完成,实验数据及操作过程,符合中药标准制定规范要求。
1. 仪器与试药
1.1 仪器
超声波清洗仪(德国Elma公司);分析天平(METTLER TOLEDO公司);多功能振荡器(山东申仪电子科技有限公司);高温箱型电炉、数显鼓风干燥箱(上海博讯实业有限公司);普利菲尔超纯水机(上海富诗特仪器设备有限公司);赛默飞U3000系列液相色谱仪(赛默飞世尔科技有限公司)。
1.2 试药
本实验共收集10批延胡索药材,经海军军医大学药学系中药鉴定学教研室张成中老师鉴定为罂粟科植物延胡索的干燥块茎。延胡索乙素(中国食品药品检定研究院,批号:110726-201516,纯度:99.8%);食用醋(江苏恒顺醋业股份有限公司);自制超纯水;色谱级甲醇、氨水(国药集团)。
2. 方法与结果
2.1 炮制工艺
取净制、切制后的延胡索,大小分档,加醋拌匀、润透,置蒸制容器内,用蒸汽加热蒸透、内无硬心,取出,干燥。炮制操作主药与辅料按延胡索与米醋的质量比为100∶20(kg/kg)制备醋蒸延胡索。
2.2 性状鉴别
取10批醋蒸延胡索分别编号为CYHS-01-01~10,观察其大小、形状、色泽、质地、气、味等总结其共性特征。本品呈不规则的圆形厚片,表面黄褐色,有不规则网状皱纹。质硬而脆,断面黄褐色,角质样,有蜡样光泽。微具醋香气,味苦。
2.3 薄层鉴别
取醋蒸延胡索粉末1 g,参照《中国药典》(一部)2015年版延胡索薄层鉴别项下制备供试品溶液。另取延胡索对照药材l g,同法制成对照药材溶液。再取延胡索乙素对照品,加甲醇制成每l ml含0.5 mg 的溶液,制成对照品溶液。吸取上述3种溶液各2~3μl分别点于用1%氢氧化钠溶液制备的同一硅胶G 薄层板上,以甲苯-丙酮(9∶2)为展开剂,展开,取出,晾干,置碘缸中显色约3 min后取出,待板上吸附的碘挥尽后,置紫外光灯(365 nm)下检视。从色谱图上可以看出,供试品色谱中,在与对照药材及对照品色谱相应的位置上,显相同颜色的斑点和荧光斑点(图1)。
2.4 水分测定
参照《中国药典》(四部)2015年版0832水分测定法第二法共测定10批次醋蒸延胡索饮片,水分最低值11.87%,最高值15.74%(表1),根据数据及公式μ=
$ \bar x $ + ts/$\sqrt{n} $ +MU[注:$\bar x $ 是样本的平均数;t是置信水平为99%的学生t检测值(单尾);s是样本的标准偏差;n是样本的批数;MU是不确定度评估(MU=0.1270×$\bar x $ )]计算,限度应为15.61%,参照《中国药典》(一部)2015年版延胡索项下,拟定水分限度不得超过15.0%。表 1 10批醋蒸延胡索水分测定结果(%)序号 含水量A 含水量B 平均值 相对偏差 CYHS-01-01 13.62 13.45 13.54 0.63 CYHS-01-02 12.12 12.35 12.24 0.94 CYHS-01-03 12.39 12.62 12.51 0.92 CYHS-01-04 12.15 12.04 12.10 0.45 CYHS-01-05 12.50 12.15 12.33 1.42 CYHS-01-06 14.09 13.86 13.98 0.82 CYHS-01-07 11.97 11.76 11.87 0.88 CYHS-01-08 16.09 15.38 15.74 2.26 CYHS-01-09 12.40 12.06 12.23 1.39 CYHS-01-10 13.07 12.72 12.90 1.36 2.5 总灰分测定
参照《中国药典》(四部)2015年版2302灰分测定法共测定10批次醋制延胡索饮片,总灰分最低值2.77%,最高值3.80%(表2),根据数据参照《中国药典》(一部)2015年版延胡索项下,根据公式μ=
$\bar x $ +ts/$\sqrt{n} $ +MU计算,限度应为:3.53%,参考《中国药典》(一部)2015年版延胡索项下总灰分限度,拟定不得超过4.0%。表 2 10批醋蒸延胡索总灰分测定结果(%)序号 灰分A 灰分B 平均值 相对偏差 CYHS-01-01 3.15 3.04 3.10 1.78 CYHS-01-02 2.76 2.80 2.78 0.72 CYHS-01-03 2.89 2.93 2.91 0.69 CYHS-01-04 3.78 3.82 3.80 0.53 CYHS-01-05 2.88 2.95 2.92 1.20 CYHS-01-06 2.74 2.79 2.77 0.90 CYHS-01-07 3.24 3.20 3.22 0.62 CYHS-01-08 3.20 3.23 3.22 0.47 CYHS-01-09 3.25 3.29 3.27 0.61 CYHS-01-10 3.22 3.19 3.21 0.47 2.6 浸出物测定
按照《中国药典》(四部)2015年版2201醇溶性浸出物测定法热浸法,用稀乙醇作溶剂,共测定10批次醋延胡索浸出物, 10批醋延胡索的浸出物在11.68%~18.20%之间(表3)。以统计学方法分析测试数据, 基于测试数据, 设定浸出物限度的公式如下:μ=
$\bar x $ −ts/$\sqrt{n}$ −MU(其中,$\bar x $ 是样本的平均数;t是置信水平为99%的学生t检测值(单尾)t0.01,9=2.821;s是样本的标准偏差;n是样本的批数;MU是不确定度评估MU=0.1413×$\bar x $ )。浸出物测定限度为:10.41%。拟定醇溶性浸出物测定法,参照《中国药典》2015年版(四部)2201测定,用稀乙醇作溶剂,浸出物不得少于11.0%。表 3 10批醋蒸延胡索浸出物测定结果(%)序号 浸出物A 浸出物B 平均值 相对偏差 CYHS-01-01 13.69 13.48 13.59 0.77 CYHS-01-02 18.51 18.20 18.36 0.84 CYHS-01-03 14.06 14.15 14.11 0.32 CYHS-01-04 13.87 13.67 13.77 0.73 CYHS-01-05 14.39 14.05 14.22 1.20 CYHS-01-06 16.46 16.21 16.34 0.77 CYHS-01-07 14.66 14.50 14.58 0.55 CYHS-01-08 11.43 11.68 11.56 1.08 CYHS-01-09 13.68 13.79 13.74 0.40 CYHS-01-10 11.78 11.92 11.85 0.59 2.7 含量测定
2.7.1 色谱条件与系统适用性试验
以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.1%磷酸溶液(三乙胺调pH至6.0)(55∶45)为流动相;检测波长为280 mn。理论板数按延胡索乙素峰计算应不低于3 000。
2.7.2 对照品溶液的制备
取P2O5减压干燥12 h后延胡索乙素对照品适量,精密称定,加甲醇制成每1 ml含46 μg的溶液,即得。
2.7.3 供试品溶液的制备
取醋蒸延胡索粉末(过三号筛)约0.5 g,精密称定,置平底烧瓶中,精密加入浓氨试液-甲醇(1∶20)混合溶液50 ml,称定重量,浸渍1 h后加热回流1 h,放冷,再称定重量,用浓氨试液-甲醇(1∶20)混合溶液补足减失的重量,摇匀,滤过。精密量取续滤液25 ml,蒸干,残渣加甲醇溶解,转移至5 ml量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得。
2.7.4 测定法
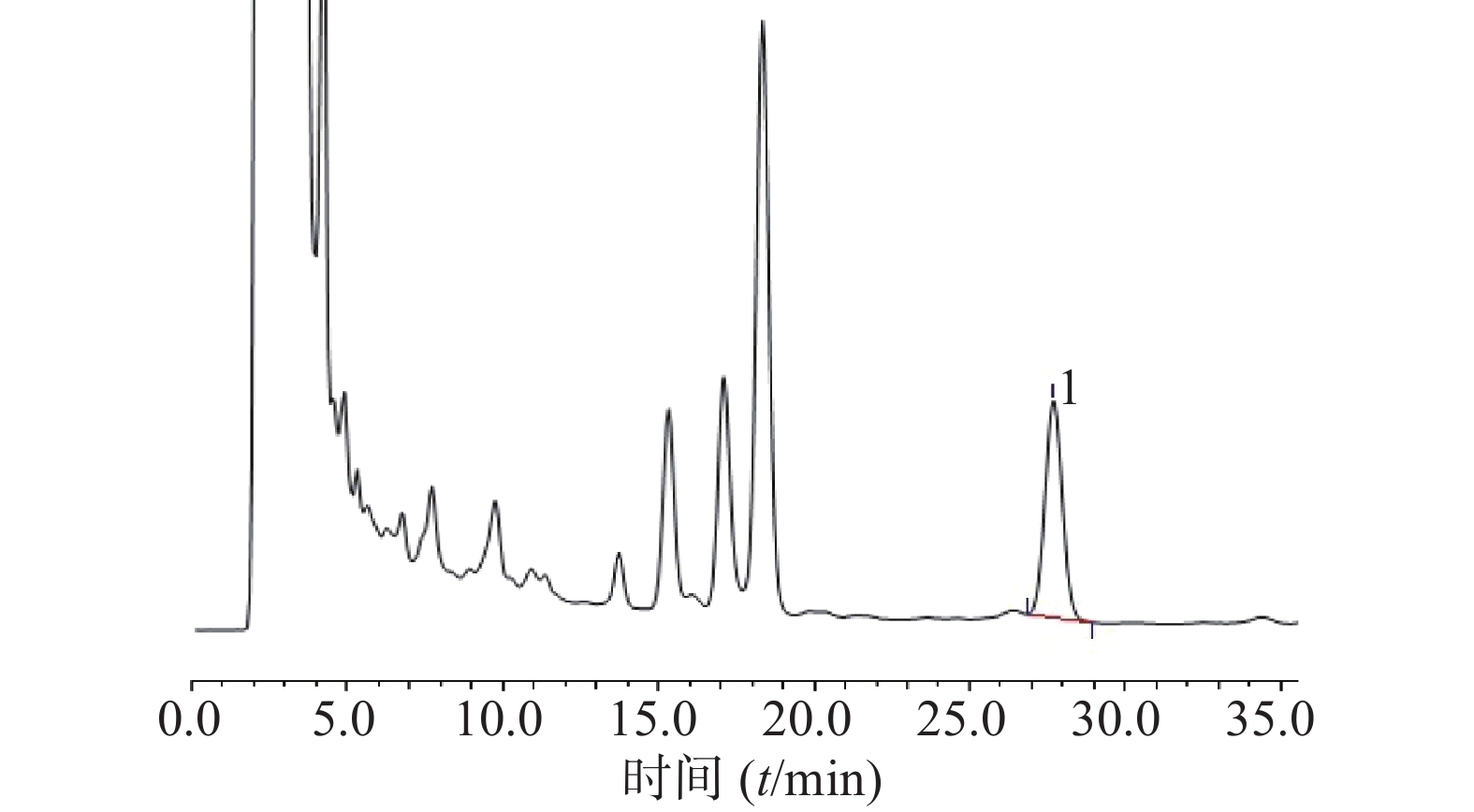
分别精密吸取延胡索乙素对照品溶液与醋蒸延胡索供试品溶液各10μl,注入液相色谱仪,测定,即得(图2、图3)。
2.7.5 线性范围考察
精密称取纯度为99.8%的延胡索乙素对照品适量置50 ml容量瓶中,加甲醇稀释至刻度,摇匀,得对照品溶液储备液,分别精密量取一定量的对照品储备液稀释成浓度分别为0.0101、0.0202、0.0404、0.0809、0.1213、0.1618 mg/ml的对照品溶液,注入液相色谱仪,测定含量,以浓度为纵坐标、峰面积为横坐标得标准曲线Y=931.64X+5.1405 (r=0.99995)。
2.7.6 重复性试验
取CYHS-01-010样品约0.5 g,精密称定,按供试品溶液制备方法处理,测定含量,平行取样测定6次,计算每次测定延胡索乙素的含量为0.097%,RSD为2.4%,符合要求。
2.7.7 精密度试验
精密称取延胡索乙素对照品溶液10 μl注入液相色谱仪,测定峰面积,平行测定8次,计算RSD为1.1%,符合要求。
2.7.8 稳定性试验
取CYHS-01-010样品约0.5 g,精密称定,按供试品溶液制备方法处理,分别在0、2、4、6、8、12、24 h测定含量,计算每次测定延胡索乙素的RSD为1.8%,符合规定。
2.7.9 加样回收率试验
取CYHS-01-010样品约0.25 g,精密称定,精密加入含延胡素乙素0.202 2 mg的对照品溶液,按供试品溶液制备方法处理,得相关溶液,进液相色谱仪处理,计算含量及加样回收率,理论要求加样回收率85%~110%(CYHS-01-010含量为0.097%),RSD<5%(表4)。
表 4 加样回收率试验结果编号 取样量(m/g) 加样量(m/mg) 回收率(%) RSD(%) 1 0.2418 0.2022 100.4 3.3 2 0.2417 0.2022 106.7 3 0.2427 0.2022 104.6 4 0.2462 0.2022 105.7 5 0.2453 0.2022 100.0 6 0.2440 0.2022 98.5 2.7.10 样品含量测定
测定10批样品,根据数据计算,结果参照《中国药典》(一部)2015年版延胡索项下制订,拟定含量限度为:不得少于0.050%(10批检品含量差别不大,最大值与最小值差别接近1倍),见表5。根据公式μ=
$\bar x $ -ts/$\sqrt{n} $ -MU计算,限度应不得少于0.060%,醋蒸为醋制延胡索的一个炮制规格,结合《中国药典》(2015年版)一部延胡索项下的含量限度,设定按干燥品计算,延胡索乙素(C21H25NO4)不少于 0.050%。表 5 10批醋蒸延胡索含量测定结果样品 含量(%) 平均值(%) CYHS-01-01 0.064 0.077 CYHS-01-02 0.068 CYHS-01-03 0.055 CYHS-01-04 0.058 CYHS-01-05 0.072 CYHS-01-06 0.092 CYHS-01-07 0.068 CYHS-01-08 0.100 CYHS-01-09 0.098 CYHS-01-10 0.098 2.8 标准其他项目
辛、苦、温,归肝、脾经。具有活血,行气,止痛之功。性味与归经、功能与主治、用法与用量、储藏等项目参照现行版《中国药典》(一部)2015年版延胡索项下制定。
3. 讨论
蒸法炮制药材早在2000多年前的医药文献《五十二病方》中就有“陈藿,蒸而取其汁”记载,汉代张仲景的《伤寒论》中有“乌梅...蒸之”,至明代缪希雍《炮炙大法》中已有近百味药材的蒸制记载。蒸法的广泛应用使其成为中药炮制最常用的炮制工艺之一。中药延胡索的炮制在宋代出现了醋炒、醋煮、盐炒等工艺,及至明清时又出现了醋纸煨、酒煮等工艺,延胡索醋蒸始载于明代《本草乘雅半偈》“醋润,蒸之,从巳至亥,俟冷取出,焙干,研细用”。现在主要炮制方法为醋炙、醋煮、酒炙、醋蒸等,醋蒸延胡索临床上虽广泛应用,但尚缺法定质量标准。
延胡索经过醋炙后,饮片中延胡索乙素的含量较醋炙前变化较小,但醋炙后延胡索煎剂中延胡索乙素的含量变化较大,溶出会显著增加,表明延胡索醋制后大量生物碱和醋酸反应生成生物碱盐,可提高煎出量,继而提高延胡索止痛作用[8-9]。江国荣等将延胡索生品分别经醋炙、醋煮、醋烘、酒炙后,测定生物碱的含量,发现延胡索经不同炮制后生物碱含量均有所升高,说明临床上可以根据治疗需要,对延胡索采用醋烘、醋炙、酒炙等炮制方法来提高有效成分的含量[10]。李春等采用正交试验法优化延胡索醋蒸炮制工艺,以延胡索粗粉为原料,加醋量30%,闷润2 h,蒸制2 h后,延胡索乙素的含量明显提高[11]。郑军献等对新采集的延胡索进行加工炮制,发现通过不同炮制方法制备延胡索药材,水煮法、蒸制法、烘干法在外形、性状基本一致,但延胡索乙素及成品折干率相差较大,蒸制延胡索乙素含量比水煮高出16.35%,成品折干率比煮法高出3.52%,说明蒸制法优于水煮法。蒸制时间10 min,延胡索乙素含量达到最高,当蒸制时间延长时,其含量反而降低[12]。龙全江等研究发现,经煮制加工的延胡索药材样品中3 种生物碱的含量总体低于蒸制加工所得的延胡索药材,其结果为延胡索药材蒸制炮制工艺的确定提供了物质基础和研究依据 [13]。
在现有文献的基础上,经实验研究分析,醋蒸延胡索具备现行版《中国药典》一部收载的醋炙延胡索质量要求,且延胡索乙素的含量明显高于药典中醋炙延胡索的要求,延胡索乙素可以作用于中枢神经系统,止痛、镇静,降低成瘾性、保护大脑的作用;也可以作用于心血管系统,抗心律失常、改善血流动力学、降低血脂[14]。延胡索乙素含量的增加符合醋制增强行气、止痛之功的炮制目的。因此制定醋蒸延胡索质量标准要求应为:性状为不规则的圆形厚片,表面黄褐色,有不规则网状皱纹。质硬而脆,断面黄褐色,角质样,有蜡样光泽,微具醋香气,味苦;水分不超过15%;总灰分不超过5%;以稀乙醇作溶剂,浸出物不少于11.0%;延胡索乙素(C21H25NO4)含量,按干燥品计算不少于 0. 050%。
-
表 1 TAA诱导肝纤维化相关的差异代谢物及其代谢通路
编号 代谢物 精确分子量 加合离子 分子式 调节趋势 相关通路 1 丁二酸 118.026 6 M-H C4H6O4 ↓* TCA循环 2 柠檬酸 130.026 6 M+NH4 C5H6O4 ↑** 脂肪酸代谢 3 戊二酸 130.026 6 M+FA-H C5H6O4 ↓*** / 4 L-天冬氨酸 133.037 5 M-H C4H7NO4 ↑* 丙氨酸、天冬氨酸和谷氨酸代谢 5 丝氨酸甘氨酸 162.064 1 M+H-H2O C5H10N2O4 ↑* 二肽 6 左旋肉碱 162.113 0 M+H C7H16NO3 ↓** 肉碱合成 7 2-甲基-3-苯基丙酸 164.083 7 M+H-H2O C10H12O2 ↑*** / 8 顺乌头酸 174.016 4 M-H C6H6O6 ↓** 三羧酸循环 9 半胱氨酰甘氨酸 178.041 2 M+H C5H10N2O3S ↓*** 谷胱甘肽代谢 10 缬氨冬酰胺 231.121 9 M+NH4 C9H17N3O4 ↓* 二肽 11 尿苷 244.069 5 M-H C9H12N2O6 ↓** 嘧啶代谢 12 甘油磷酸甘油 246.050 5 M-H C6H15O8P ↓** 脂质代谢 13 环状6-羟基褪黑素 246.100 4 M+Na C13H14N2O3 ↓** 褪黑素代谢 14 7,8-二氢蝶呤 255.096 8 M+H C9H13N5O4 ↓* 蝶呤生物合成 15 谷氨酰胺天冬酰胺 261.096 1 M+Na C9H15N3O6 ↑*** 二肽 16 γ-谷氨酰鸟氨酸 261.132 5 M+NH4 C10H19N3O5 ↑*** 二肽 17 3-羟基异戊酰肉碱 261.1576 M+NH4 C12H23NO5 ↓*** 脂肪酸代谢 18 天冬氨酰谷氨酸 262.080 1 M+FA-H C9H14N2O7 ↓*** 二肽 19 N-乙酰5-羟色胺硫酸盐 298.062 3 M-H20-H C12H14N2O5S ↓*** 褪黑素代谢 20 视黄酯 302.224 6 M-H C20H30O2 ↓* 脂肪酸代谢 21 谷胱甘肽 307.083 8 M+H C10H17N3O6S ↓** 谷胱甘肽代谢 22 吲哚酚葡萄糖醛酸苷 309.084 9 M+H C14H15NO7 ↓** 脂质代谢 23 3'-AMP 347.063 1 M+H C10H14N5O7P ↓* 胆酸生物合成 24 苯酰甘氨酸 397.355 6 M+Na C24H47NO3 ↑* 脂肪酸代谢 25 花生四烯酰肉碱 448.342 1 M+H C27H46NO4 ↓** 脂质代谢 26 花生四烯基肉碱 455.397 5 M+H-H2O C27H53NO4 ↑** 脂肪酸代谢 27 溶血磷脂酰乙醇胺(0∶0/18∶2(9Z,12Z)) 477.285 5 M+H C23H44NO7P ↓* 甘油磷脂代谢 28 溶血磷脂酰乙醇胺(18∶2(9Z,12Z)/0∶0) 477.285 5 M-H C23H44NO7P ↓* 甘油磷脂代谢 29 溶血磷脂酰乙醇胺(0∶0/20∶5(5Z,8Z,11Z,14Z,17Z)) 499.269 9 M+FA-H C25H42NO7P ↓* 甘油磷脂代谢 30 牛磺熊去氧胆酸 499.296 8 M-H C26H45NO6S ↓* 脂质代谢 31 溶血磷脂酰乙醇胺(20∶4(8Z,11Z,14Z,17Z)/0∶0) 501.285 5 M+H C25H44NO7P ↓* 甘油磷脂代谢 32 二酰甘油(16∶1n7/0∶0/18∶3n3) 588.475 4 M+H-H2O C37H64O5 ↑*** 脂质代谢 33 二酰甘油(14∶0/0∶0/22∶5n3) 614.491 0 M+H C39H66O5 ↑*** 脂质代谢 34 磷脂神经酰胺(d18∶1/16∶0) 617.478 4 M+H-H2O C34H68NO6P ↑*** 鞘脂代谢 35 鞘糖脂(d18∶1/12∶0) 643.502 3 M+H C36H69NO8 ↑*** 磷脂代谢 36 磷脂酰乙醇胺(16∶0/P-16∶0) 675.520 3 M+H-H2O C37H74NO7P ↑** 磷脂代谢 37 磷脂酰乙醇胺(18∶0/15∶0) 705.530 9 M+H-H2O C38H76NO8P ↑*** 磷脂代谢 38 心磷脂(i-13∶0/i-22∶0/i-12∶0/i-13∶0) 1 296.909 6 M+H-H2O C69H134O17P2 ↓* 磷脂代谢 *P<0.05、**P<0.01、***P<0.001,模型组与正常组比较 -
[1] Tsochatzis EA, Bosch J, Burroughs A K. Liver cirrhosis[J]. Lancet,2014,383(9930):1749-1761. doi: 10.1016/S0140-6736(14)60121-5 [2] CHANG M L, YANG S S. Metabolic signature of hepatic fibrosis: from individual pathways to systems biology[J]. Cells,2019,8(11):E1423. doi: 10.3390/cells8111423 [3] GE M X, LIU H, ZHANG Y X, et al. The anti-hepatic fibrosis effects of dihydrotanshinone I are mediated by disrupting the yes-associated protein and transcriptional enhancer factor D2 complex and stimulating autophagy[J]. Br J Pharmacol,2017,174(10):1147-1160. doi: 10.1111/bph.13766 [4] WANG F, MA J, WANG K S, et al. Blockade of TNF-α-induced NF-κB signaling pathway and anti-cancer therapeutic response of dihydrotanshinone I[J]. Int Immunopharmacol,2015,28(1):764-772. doi: 10.1016/j.intimp.2015.08.003 [5] WEI Y D, XU M J, REN Y, et al. The cardioprotection of dihydrotanshinone I against myocardial ischemia-reperfusion injury via inhibition of arachidonic acid ω-hydroxylase[J]. Can J Physiol Pharmacol,2016,94(12):1267-1275. doi: 10.1139/cjpp-2016-0036 [6] 邢心睿. 扶正化瘀方抗肝纤维化的网络多靶标作用机制研究[D]. 上海: 海军军医大学, 2019. [7] 李俊南, 侯艳, 孙凤宇, 等. OPLS方法的原理及其在代谢组学数据判别分析中的应用[J]. 中国卫生统计, 2014, 31(5):765-769. [8] LUANGMONKONG T, SURIGUGA S, MUTSAERS H A M, et al. Targeting oxidative stress for the treatment of liver fibrosis[J]. Rev Physiol Biochem Pharmacol,2018,175:71-102. [9] HOU Y Y, WANG Y, WANG H H, et al. Induction of glutathione synthesis in human hepatocytes by acute and chronic arsenic exposure: differential roles of mitogen-activated protein kinases[J]. Toxicology,2014,325:96-106. doi: 10.1016/j.tox.2014.09.002 [10] TRAVERSO N, RICCIARELLI R, NITTI M, et al. Role of glutathione in cancer progression and chemoresistance[J]. Oxid Med Cell Longev,2013,2013:972913. [11] 高兰, 龙世棋, 陈博鑫, 等. 还原型谷胱甘肽靶向氧化应激对肝癌干细胞的作用[J]. 临床与实验病理学杂志, 2020, 36(8):887-892. [12] 刘仁伟, 刘冰. 黄芩苷胶囊联合胸腺法新治疗慢性乙型肝炎的临床研究[J]. 现代药物与临床, 2018, 33(12):3312-3316. [13] 岳彩飞, 洪汝涛, 徐德祥, 等. 褪黑素对PDGF诱导的肝星状细胞中JAK2/STAT3信号通路的影响[J]. 中国药理学通报, 2020, 36(3):403-407. doi: 10.3969/j.issn.1001-1978.2020.03.020 [14] LIN X, KONG L N, HUANG C, et al. Hesperetin derivative-7 inhibits PDGF-BB-induced hepatic stellate cell activation and proliferation by targeting Wnt/β-catenin pathway[J]. Int Immunopharmacol,2015,25(2):311-320. doi: 10.1016/j.intimp.2015.02.009 [15] LEBDA M A, SADEK K M, ABOUZED T K, et al. Melatonin mitigates thioacetamide-induced hepatic fibrosis via antioxidant activity and modulation of proinflammatory cytokines and fibrogenic genes[J]. Life Sci,2018,192:136-143. doi: 10.1016/j.lfs.2017.11.036 [16] LENG W B, LIU Y L, SHI H F, et al. Aspartate alleviates liver injury and regulates mRNA expressions of TLR4 and NOD signaling-related genes in weaned pigs after lipopolysaccharide challenge[J]. J Nutr Biochem,2014,25(6):592-599. doi: 10.1016/j.jnutbio.2014.01.010 [17] 仰贤莉, 李光伟, 康璐, 等. 扶正化瘀方抗大鼠肝纤维化疗效的代谢组学研究[J]. 中成药, 2016, 38(11):2342-2346. [18] WU T, ZHENG X J, YANG M, et al. Serum lipid alterations identified in chronic hepatitis B, hepatitis B virus-associated cirrhosis and carcinoma patients[J]. Sci Rep,2017,7:42710. doi: 10.1038/srep42710 [19] LI Y H, WOO S H, CHOI D H, et al. Succinate causes α-SMA production through GPR91 activation in hepatic stellate cells[J]. Biochem Biophys Res Commun,2015,463(4):853-858. doi: 10.1016/j.bbrc.2015.06.023 -





 下载:
下载:

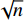


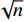

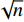



 下载:
下载: