-
清肠栓是由上海市名中医马贵同教授创制的医院制剂。该方基于溃疡性结肠炎“湿热瘀互结肠道”的关键病机,以清热化湿、活血止血立法,在锡类散、青黛散治疗黏膜溃疡的基础上优化筛选而来[1-2]。主要由三七和青黛全粉入药,五倍子和马齿苋经提取后浸膏粉入药,再加入冰片、羊毛脂,以半合成脂肪酸酯为基质制备而成的中药栓剂。
冰片为一种传统中药,清香宣散,具有开窍醒神,清热败毒的功效。现代药理学研究表明,冰片具有镇静安神、醒脑、促透、抗菌、抗炎等作用[3]。冰片常被用于肛肠外科,可避免药物的首过效应,提高药物有效性。冰片能开放并透过血脑屏障,有助于其他药物通过血脑屏障,促进疗效[4]。
冰片具有挥发性,龙脑常被作为其主要的质量控制指标,含量测定方法主要包括气相色谱法、衍生化高效液相色谱法、薄层色谱法等[5]。2020年版《中国药典》中,采用气相色谱法测定,冰片含龙脑成分不得少于55.0%,樟脑不得超过0.50%[6]。 目前,已有文献对清肠栓中三七皂苷、人参皂苷、没食子酸、靛蓝和靛玉红进行含量测定[7-8],故本实验采用气相色谱法对清肠栓中冰片含量进行测定,并计算龙脑、异龙脑的相对含量,为进一步提高清肠栓的质量控制提供有效依据。
-
7820A型气相色谱仪、氢火焰离子化检测(FID)(美Agilent 公司);225D-1CN型电子分析天平、BSA124S型电子分析天平(赛多利斯科学仪器有限公司,精度:十万分之一);S450H型超声波清洗器(德国Elma)。
-
清肠栓为院内制剂室提供(批号:210420-210425、211018、211020、211022、211025、190107、190114、190121、190304、190311、190318、190408、190415、190422、190506、190513和200302);樟脑对照品(上海诗丹德标准技术服务有限公司,批号:2814,纯度:95.0%);龙脑对照品(中国食品药品检定研究院,批号:110881-201709,纯度:99.6%);异龙脑对照品(中国食品药品检定研究院,批号:111512-201904,纯度:98.4%);水为超纯水(实验室自制);乙酸乙酯(上海凌峰化学试剂有限公司,分析纯)。
-
采用Agilent7890A型气相色谱仪FID检测器;DIKMA DM-Wax聚乙二醇20000(PEG-20M)毛细管色谱柱(30 m×0.25 mm×0.25 µm);进样口温度为250 ℃;检测器(FID)温度为250 ℃;柱温140 ℃;空气流速为450 ml/min,氢气燃气流速为50 ml/min;尾吹气为25 ml/min;分流比为20:1,进样量为1 µl。理论板数按龙脑峰计算应不低于2 000。
-
称取樟脑对照品适量,精密称定,加乙酸乙酯溶解,制成每1 ml含樟脑0.1 mg的对照品溶液。另取龙脑、异龙脑对照品适量,精密称定,加乙酸乙酯溶解,制成每1 ml含龙脑0.3 mg、异龙脑0.2 mg的混合对照品溶液。
-
取清肠栓(批号:200302)样品10粒,研细,取约60 mg,精密称定,置10 ml量瓶中,加乙酸乙酯8 ml,超声(频率37 kHz,功率800 w)处理30 min,放冷,加乙酸乙酯至刻度,摇匀,滤过,取续滤液,即得。
-
按清肠栓制剂处方比例,配制缺冰片的阴性样品,再按供试品溶液制备方法制备,即得。
-
精密吸取樟脑对照品溶液、龙脑和异龙脑对照品溶液、供试品溶液、阴性对照溶液各1 µl,按“2.1”项色谱条件下方法分别进样测定,结果樟脑、异龙脑和龙脑对照品的理论板数分别为88 684、107 331、108 387,远大于规定的2 000。供试品溶液色谱图中,未检出与樟脑对照品溶液保留时间相同的色谱峰,阴性对照溶液色谱图中在与龙脑、异龙脑相同保留时间处无干扰峰,表明该方法专属性良好。色谱图见图1。
-
分别精密称取龙脑对照品14.92 mg、异龙脑对照品10.25 mg、樟脑对照品4.83 mg,置同一10 ml量瓶中,加乙酸乙酯溶解并稀释至刻度,摇匀,制成每1 ml含龙脑1.492 mg、异龙脑1.025 mg、樟脑0.483 mg的混合对照品溶液,作为贮备液。
精密吸取5份贮备液各1 ml,加乙酸乙酯分别稀释50倍、20倍、5倍、2倍、1倍;分别精密吸取5个不同浓度的龙脑、异龙脑、樟脑混合对照品溶液,分别进样1 µl,按按“2.1 色谱条件”项下的方法测定,以进样浓度(X)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线,求得回归方程分别为:Y1=283.4X1+1.320(r=1.000,n=5);Y2=283.5X2+0.8597(r=1.000,n=5);Y3=276.9X3+0.5444(r=1.000,n=5)。线性范围分别为 0.0299~1.497µg、 0.0205~1.025µg、 0.0097~0.4830µg。
-
精密吸取“2.2”项下对照品溶液,按“2.1 ”项的方法测定,重复进样6次,测定峰面积。结果龙脑、异龙脑、樟脑峰面积RSD分别为0.3%、0.4%、0.6%(n=6),表明仪器精密度良好。
-
精密吸取同一供试品溶液(批号:200302),室温下分别放置0、4、8、12、16、20、24 h,按“2.1 色谱条件”项下的方法测定,记录峰面积。结果樟脑未检出,龙脑与异龙脑峰面积的RSD分别为1.6%和1.5%,表明供试品溶液在室温下放置24h稳定。
-
精密称取清肠栓样品粉末60 mg(批号:200302),精密称定,平行称取6份,按“2.3供试品溶液的制备”项下制备供试品溶液,按“2.1”项方法测定,结果均未检出樟脑,龙脑和异龙脑平均含量的RSD分别为0.8%和1.1%(n=6),表明该方法的重复性良好。
-
称取清肠栓样品粉末30 mg(批号:200302),精密称定,平行称取6份,分别精密加入龙脑、异龙脑、樟脑对照品溶液,按“2.3” 项方法制备供试品溶液,按“2.1”项方法测定,记录峰面积,并计算加样回收率。结果见表1。
表 1 龙脑回收率试验(n=6)
成分 原有量(mg) 加入量
(mg)测得量
(mg)回收率
(%)平均回收率
(%)RSD
(%)龙脑 0.47 0.50 0.97 100.8 101.0 0.51 0.48 0.50 0.98 101.6 0.47 0.50 0.97 101.2 0.47 0.50 0.97 100.8 0.47 0.50 0.97 100.2 0.47 0.50 0.97 101.4 异龙脑 0.28 0.29 0.58 102.8 102.5 1.66 0.28 0.29 0.59 104.5 0.28 0.29 0.58 104.2 0.28 0.29 0.57 100.4 0.28 0.29 0.58 102.1 0.28 0.29 0.57 100.8 樟脑 0.00 0.13 0.12 97.06 99.69 3.77 0.00 0.13 0.12 93.91 0.00 0.13 0.13 102.6 0.00 0.13 0.13 99.43 0.00 0.13 0.13 104.2 0.00 0.13 0.13 101.0 -
取清肠栓制剂2019、2021年共20个批次的样品,按“2.3”项方法制备供试品溶液,再按“2.1”项方法测定,20个批次均未检出樟脑。样品中龙脑和异龙脑含量见表2(表中1~10为2019年样品,11~20为2021年样品)。
表 2 清肠栓样品含量实验
样品序号 龙脑(mg/g) 异龙脑(mg/g) 冰片(mg/g) 1 14.23 8.509 22.74 2 14.19 8.564 22.76 3 14.38 8.665 23.05 4 14.26 8.569 22.83 5 14.28 8.511 22.79 6 14.21 8.571 22.78 7 14.24 8.446 22.68 8 14.41 8.632 23.04 9 14.13 8.329 22.46 10 13.89 8.401 22.29 11 18.76 11.35 30.11 12 18.60 11.20 29.80 13 18.93 11.39 30.32 14 19.03 11.37 30.40 15 18.65 11.26 29.91 16 18.82 11.38 30.19 17 18.89 11.35 30.24 18 18.74 11.28 30.02 19 18.94 11.35 30.29 20 18.88 11.39 30.27 -
乙酸乙酯对冰片具有较好的溶解性,并且样品中其他干扰成分的溶出较少,故选择其作为提取溶剂。本实验考察了不同提取时间(15 min、30 min、45 min)对样品提取效果的影响,观察比较不同条件处理后供试品溶液色谱情况,根据含量结果选择提取时间为30 min。最终以乙酸乙酯为提取溶剂,超声处理30 min作为供试品制备时的提取方式。
-
柱温的选择:由于2020年版《中国药典》中冰片含量测定选择的注温为140 ℃,而查阅文献,部分实验者选择的柱温为160 ℃[9],因此,我们分别选择140 ℃和160 ℃进行试验,根据出峰时间及峰形比较,最终选择140 ℃作为实验条件。色谱柱的选择:实验研究使用的两种色谱柱分别为DIKMA DM-Wax(PEG-20M)毛细管色谱柱(30 m×0.25 mm,0.25 µm);Agilent HP-INNOWAX(PEG-20M)毛细管色谱柱(30 m×0.25 mm,0.25 µm),比较两种色谱柱的塔板数,实验显示色谱峰分离度良好,说明色谱柱对样品的测定结果影响较小,此方法具有普遍性,故最终选择本实验室常用的DIKMA DM-Wax色谱柱。樟脑检出限和定量限确定:检测限及定量限采用信噪比法确认,当信噪比(S/N)为3∶1时,樟脑检出限为1.4 μg/g;当信噪比(S/N)为10∶1时,其定量限为4.6 μg/g。
-
2020年版《中国药典》中,冰片的描述为冰片(合成龙脑),其中对樟脑的检测要求为不得超过0.50%。本次实验,通过查阅文献,参考其它含冰片制剂中对樟脑残留的检测方法[10],对清肠栓样品进行樟脑含量测定,发现成品栓剂中均未检测到樟脑,证明我院制剂室所用冰片符合药典的相关规定。
2020年版《中国药典》是以龙脑作为冰片的含量测定指标,但通过查阅文献可知,近年对冰片的含量测定中,多以龙脑与异龙脑总量来计算冰片的含量,[11-14]。考虑到本次实验是完善清肠栓的内控标准,提高制剂的稳定性,故本实验以龙脑和异龙脑的总量来计算冰片的含量。
综上所述,本方法为冰片中龙脑、异龙脑的含量测定和樟脑限度检查制定提供参考,操作简单、重复性良好、结果准确,可用于清肠栓中冰片的质量控制。
Determination of camphor residue and borneol content in Qingchang Suppository by GC
-
摘要:
目的 建立清肠栓中樟脑残留物和冰片含量的气相测定方法。 方法 采用气相色谱法,色谱柱为Agilent毛细管柱(30 m×0.25 mm×0.25 µm),柱温为140 ℃,进样口温度250 ℃,检测器(FID)温度为250 ℃。 结果 樟脑、龙脑和异龙脑在0.0299~1.497µg(r=1.000)、0.0205~1.025µg(r=1.000)、0.0097~0.4830 µg(r=1.000)范围内呈现良好的线性关系。精密度、稳定性、重复性试验结果的RSD均小于2%,平均加样回收率分别为99.7%、101.0%、102.5%。 结论 该方法准确、可靠、简便快速,可用于清肠栓中龙脑含量的测定。 Abstract:Objective To establish a gas chromatography for simultaneous determination of camphor residue and borneolum content in Qingchang Suppository. Methods Gas chromatograph method was used. The chromatographic column was Agilent capillary column(30 m×0.25 mm×0.25 µm). The column temperature was 140 ℃. The sample injection temperature was 250 ℃. The FID detector temperature was 250 ℃. Results Camphor, borneol and isoborneol content showed good linear in the extent of 0.0299~1.497(r=1.000), 0.0205~1.025(r=1.000), 0.0097~0.4830 µg (r=1.000). RSDs of precision, stability and repeatability test results were less than 2%. The recovery was 99.7%, 101.0%, 102.5%. Conclusion This method is simple and quick with accurate result, which could be used for the content determination of Borneol in Qingchang Suppository. -
Key words:
- GC /
- Qingchang Suppository /
- Camphor /
- Borneol /
- Isoborneol /
- Content determination
-
目前全球尚无预防和治疗新冠肺炎(COVID-19)确认的特效药物。有学者试图遴选已有的抗病毒药物,以期尽快开发“老药新用”的治疗方案。国家卫生健康委员会陆续发布了7版试行《新型冠状病毒肺炎诊疗方案》,其中,广谱抗病毒药物利巴韦林被作为可试用的临床治疗药物。
利巴韦林(ribavirin)常用剂型有注射剂、片剂、口服液、气雾剂等,国外临床上多以雾化剂用于成人和儿童的呼吸道合胞病毒性肺炎的治疗[1]。体外研究表明[2],利巴韦林可增强干扰素的体外活性,在治疗SARS-CoV感染者中,诊断后立即使用利巴韦林时治疗效果较好[3]。利巴韦林对DNA和RNA病毒均具有抑制作用,通常以雾化剂用于成人和儿童的呼吸道合胞病毒性肺炎的治疗。美国食品药品管理局(FDA)于1986年首次批准利巴韦林吸入溶液气雾剂(Virazole®,USP)[4],于1992年上市,而说明书中明确规定用于严重下呼吸道感染的住院患儿,且全程气雾治疗3~7 d,可见其应用的严格限制。根据国内多家临床中心的试验数据表明,与利巴韦林颗粒剂相比,国内的利巴韦林气雾剂(信韦林)达到同等的治疗效果时,虽然用药剂量大幅下降,但不良反应率无明显差异[5-8],表明利巴韦林吸入溶液气雾剂(Virazole®,USP)和利巴韦林气雾剂(信韦林)可能存在不良反应较大的缺陷,临床应用受到一定的限制。
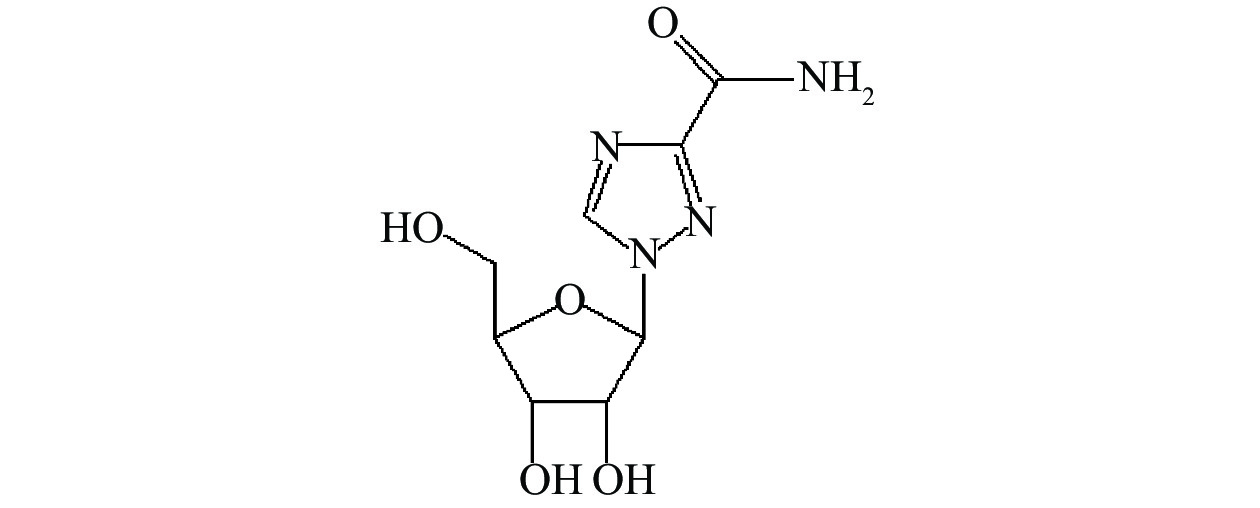
脂质体定量吸入粉雾剂(DPI)是肺部给药系统的研究热点之一。脂质体由于类似细胞结构而具有被动靶向性,作为药物载体常用于肺部给药,有利于抗病毒药物直接递送并作用于肺部细胞,抑制病毒的繁殖,特定粒径的脂质体粉雾剂可使药物不同程度地的分布于人体上、下呼吸道,从而发挥更好的临床治疗效果[9-10]。利巴韦林水溶性较好,亲脂性较差,如图1的结构式所示,不易被细胞渗透吸收,采用脂质体包裹,并制成粉雾剂给药至呼吸道或肺泡组织,可实现肺部沉积增强的作用效果,同时降低不良反应。本文根据临床急需及利巴韦林的药物理化性质,结合吸入制剂肺部给药方面的治疗优势,设计研制了一种利巴韦林脂质体吸入粉雾剂。以此开展设计研究,尝试开发抗病毒药物新型给药系统,以期为扩大利巴韦林临床使用范围,也为制剂学基础研究提供参考。
1. 仪器与材料
1.1 仪器
高效液相色谱仪(Agilent 1200);ME104E电子天平(METTLER TOLEDO);EYELA N-1000旋转蒸发仪(日本东京理化器械株式会社);Niro NS2006L高压匀质机(意大利GEA Niro Soavi公司);Nano NS90粒度检测仪(英国马尔文仪器有限公司);Hitachi S-3400N扫描电子显微镜(日本日立公司)。
1.2 材料
利巴韦林原料药(纯度>98%,西安康诺化工有限公司);利巴韦林对照品(629-200202,中国食品药品检定研究院);大豆卵磷脂(SPC)、脱氧胆酸钠(SDC)(北京化学试剂公司);N,N-二甲基甲酰胺、无水乙醇、磷酸氢二钠、磷酸二氢钠(分析纯,北京化学试剂公司);蒸馏水。
2. 方法与结果
2.1 利巴韦林脂质体冻干粉含量测定方法
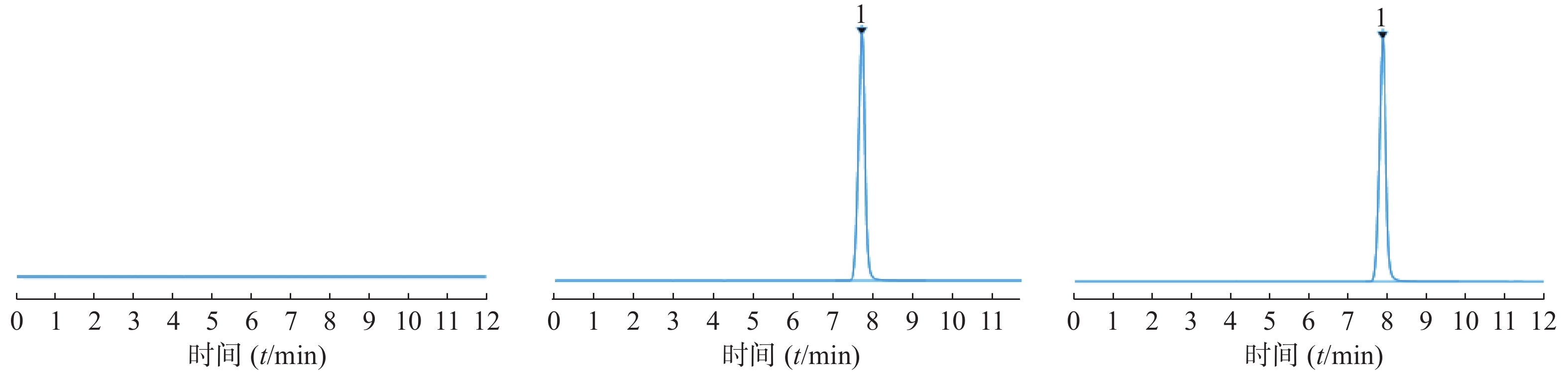
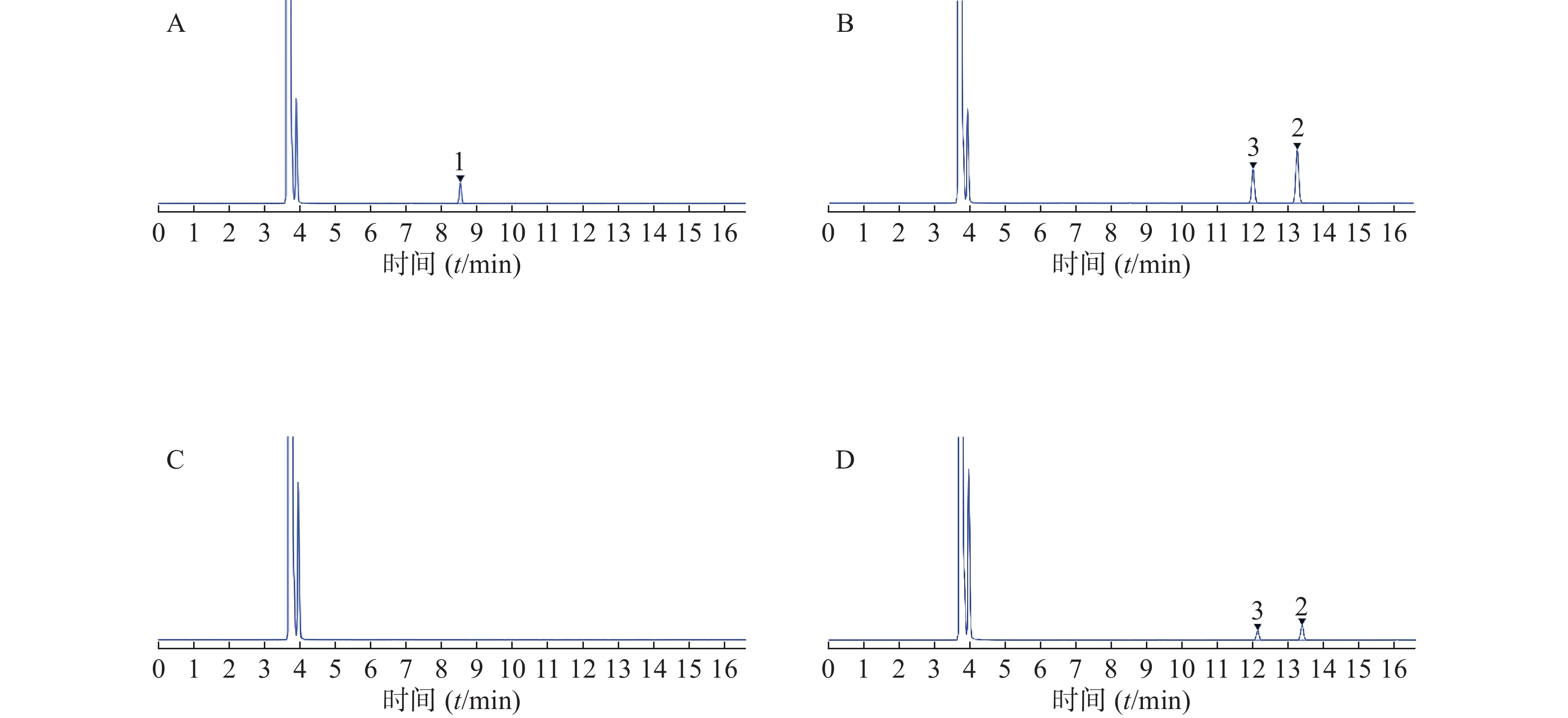
参照美国药典第40版中“利巴韦林”含量测定方法[11],采用高效液相色谱法测定。色谱条件:色谱柱为Carbomix H-NP5(7.8 mm×100 mm,5 μm);流动相硫酸溶液调整pH至2.5±0.1;流速:0.6 ml/min;柱温:60 ℃;检测波长UV 207 nm;进样量10 μl,取利巴韦林对照品适量,流动相溶解稀释至浓度为0.025 mg/ml,过滤,进样检测。取利巴韦林脂质体冻干粉适量,加入无水乙醇少量破乳,呈透明溶液后流动相稀释,制成浓度0.025 mg/ml供试品溶液;同样方式处理阴性样品溶液。在该色谱条件下得到图2的色谱图,图中利巴韦林峰型较佳,出峰时间适宜,阴性对照无干扰。
2.2 利巴韦林脂质体粉雾剂的制备
取大豆卵磷脂(5 mmol/L),脱氧胆酸钠(5 mmol/L),为制备具有高稳定性的双分子膜,在处方中加入适量维生素E置于250 ml的茄形瓶中,加入无水乙醇溶解,超声,至呈透明黄色溶液;将此溶液置旋转蒸发仪上旋转蒸发除去溶剂成膜;另取利巴韦林原料药溶解于磷酸盐缓冲液中(20 mg/ml),溶解完全后匀速加入至茄形瓶内,并于40 ℃水浴温度水化薄膜,直到完全水化呈近均一透明的乳白色溶液;高压均质机下将上述溶液均质,即得到粒径100~200 nm的利巴韦林脂质体溶液。加入冻干保护剂乳糖, 溶解摇匀后置西林瓶中,启动冷冻干燥程序,即得疏松利巴韦林脂质体冻干粉。
2.3 外观形态
取载药脂质体经处理后于透射电镜下观察,呈类圆形球状物,直径约200 nm,见图3。
2.4 流动性、松密度
将粉末通过下孔径为5 mm 的玻璃漏斗,从10 cm的高度缓慢、均匀地落入平板上,形成圆锥体。测量圆锥体的高度(h)和基底的半径(r),按公式计算休止角(θ,tanθ=h/r)。粉末休止角为37~40°,流动性较好。取量筒,自由落体方式装入脂质体冻干粉,记录质量与体积,计算松密度约0.25 g/ml。
2.5 包封率、冻干粉含量测定
取利巴韦林脂质体冻干粉适量,纯化水溶解得脂质体复溶物,取复溶物适量加入无水乙醇少量破乳,呈透明溶液后用流动相稀释,制成0.025 mg/ml供试品溶液,按“2.1”项下色谱条件检测冻干粉含量。
经过前期实验对比,本研究采用Sephadex G-50柱层析法测定包封率。分别精密量取1 ml脂质体和冻干粉复溶物上柱,用纯化水洗脱,流速0.5 d/s,从洗脱液由澄清变乳白色开始收集至洗脱液再次变澄清(约15 ml),置50 ml容量瓶中,以乙醇定容至刻度,振摇破乳;10 μl进样分析,记录色谱图,计算包封药物含量(W包);另各取1 ml脂质体溶液及冻干粉复溶物置50 ml容量瓶中,乙醇稀释至刻度,振摇破乳,10μl进样分析,记录色谱图,计算总药量(W总)。以包封率=(W包/W总)×100%,计算结果见表1。
表 1 利巴韦林脂质体冻干粉含量与包封率项目 样品 No.1 No.2 No.3 平均值 含量(mg/g) 脂质体冻干粉末 9.4 8.6 9.3 9.1 包封率 /% 冻干前脂质体溶液 64.23 63.83 66.34 64.80 脂质体冻干粉复溶液 63.43 61.65 64.10 63.06 结果表明,按照初步拟定方法制得的脂质体包封率约63%,冻干前后数据无明显差别,复溶效果较好,载药量较高,但包封率较低,处方工艺需要进一步优化。
2.6 复溶液粒径、聚合物分散指数与电位测定
取本品复溶液适量,纯化水再次稀释100倍,于马尔文粒径仪检测,如表2所示,本品冻干前后溶液粒径约160 nm,聚合物分散指数(PDI)、电位均较好,表明稳定性较好。
表 2 利巴韦林脂质体冻干复溶液粒径、PDI与电位样品 No.1 No.2 No.3 平均值 粒径/PDI 电位 粒径/PDI 电位 粒径/PDI 电位 粒径 电位 冻干前溶液 148.3 nm/0.57 −45.4 mv 163.7 nm/0.63 −41.8 mv 172.6 nm/0.39 −40.5 mv 161.5 nm −42.6 mv 冻干复溶液 147.8 nm/0.58 −42.5 mv 161.8 nm/0.65 −38.6 mv 181.7 nm/0.41 −39.1 mv 163.8 nm −40.1 mv 2.7 冻干粉溶解性
脂质体具有优良的两亲性,冻干保护剂亦有很好的亲水性。取本品冻干粉5 g置10 ml容量瓶中,加水10 ml,轻轻振摇即刻溶解完成,形成均一的乳白色胶束溶液,说明本品溶解性较好。
3. 讨论
病毒通过侵入人体呼吸道黏膜上皮细胞而感染,并在细胞内进行复制与表达,再释放至细胞外感染宿主其他细胞,最终导致机体产生过度免疫反应。与一些在下呼吸道的细胞内进行复制繁殖的高致病性病毒类似,COVID-19导致下呼吸道症状较为明显。故若将抗病毒药物递送至下呼吸道,直达病灶,并进入被感染的机体上皮细胞内,可能更好地发挥抑制或清除病毒的作用。通常肺吸入给药后可直接将药物运送至肺组织,在局部起效,与全身给药治疗肺部疾病相比较,可明显减少药物用量,降低药物在其他部位分布与吸收造成的不良反应,加之粉雾剂具备给药剂量准确、无需抛射剂、方便、易用及肺部靶标部位药物沉积量高等优势,是肺部疾病治疗药物较为理想的给药途径。
将利巴韦林通过脂质体包裹技术实现粉雾剂肺部细胞靶向治疗,相比普通口服与常规气雾剂可减少用药剂量和降低不良反应,理论上具有一定的可行性。因而,对轻、中度COVID-19感染患者也许是一种潜在的抗病毒药物治疗方式。
经对利巴韦林脂质体粉雾剂的初步制剂技术探究,结果证明制备的制剂满足粉雾剂的基本要求。由于粉雾剂具有无需抛射剂、药物相对稳定的优势[12],而且给药装置易于携带,操作简单、给药剂量相对准确等优点,故适合开发研制成利巴韦林脂质体吸入粉雾剂。此外,制备的利巴韦林脂质体冻干粉还可开发为溶液气雾剂,故在药剂开发方面也有较好前景。然而,本实验尚为初步研究,仍需要对制剂处方工艺进一步优化,以进一步提高包封率与改善整体粒径分布等性能。如要进入临床试用,还需对给药装置筛选、体内外药物沉积、药效学等进行深入考察,以满足临床使用的基本要求。
-
表 1 龙脑回收率试验(n=6)
成分 原有量(mg) 加入量
(mg)测得量
(mg)回收率
(%)平均回收率
(%)RSD
(%)龙脑 0.47 0.50 0.97 100.8 101.0 0.51 0.48 0.50 0.98 101.6 0.47 0.50 0.97 101.2 0.47 0.50 0.97 100.8 0.47 0.50 0.97 100.2 0.47 0.50 0.97 101.4 异龙脑 0.28 0.29 0.58 102.8 102.5 1.66 0.28 0.29 0.59 104.5 0.28 0.29 0.58 104.2 0.28 0.29 0.57 100.4 0.28 0.29 0.58 102.1 0.28 0.29 0.57 100.8 樟脑 0.00 0.13 0.12 97.06 99.69 3.77 0.00 0.13 0.12 93.91 0.00 0.13 0.13 102.6 0.00 0.13 0.13 99.43 0.00 0.13 0.13 104.2 0.00 0.13 0.13 101.0 表 2 清肠栓样品含量实验
样品序号 龙脑(mg/g) 异龙脑(mg/g) 冰片(mg/g) 1 14.23 8.509 22.74 2 14.19 8.564 22.76 3 14.38 8.665 23.05 4 14.26 8.569 22.83 5 14.28 8.511 22.79 6 14.21 8.571 22.78 7 14.24 8.446 22.68 8 14.41 8.632 23.04 9 14.13 8.329 22.46 10 13.89 8.401 22.29 11 18.76 11.35 30.11 12 18.60 11.20 29.80 13 18.93 11.39 30.32 14 19.03 11.37 30.40 15 18.65 11.26 29.91 16 18.82 11.38 30.19 17 18.89 11.35 30.24 18 18.74 11.28 30.02 19 18.94 11.35 30.29 20 18.88 11.39 30.27 -
[1] 谢建群, 张涛, 施斌, 等. 清肠栓治疗溃疡性结肠炎的临床和实验研究述评[J]. 上海中医药大学学报, 2008, 22(1): 70-72. doi: 10.3969/j.issn.1008-861X.2008.01.022 [2] 李超男, 龚雨萍. 清肠栓治疗溃疡性结肠炎的临床和实验研究进展[J]. 临床医药文献电子杂志, 2018, 5(9): 181-183, 185. doi: 10.3877/j.issn.2095-8242.2018.09.100 [3] 吴谕锋, 朱泽宇, 陈靖南, 等. 冰片药理作用及冰片酯的研究进展[J]. 药学研究, 2020, 39(4): 217-224. doi: 10.13506/j.cnki.jpr.2020.04.007 [4] 滕毅, 杨海玲. 冰片在药代动力学方面的研究进展[J]. 中国临床药理学与治疗学, 2015, 20(4): 469-475. [5] 汪汝沛, 戚进, 余伯阳. 冰片含量测定方法研究进展[J]. 药学进展, 2010, 34(8): 359-364. doi: 10.3969/j.issn.1001-5094.2010.08.004 [6] 国家药典委员会. 中华人民共和国药典(一部)[S]. 中国医药科技出版社, 2020: 152-153. [7] 韩柱, 崔波, 陆菁, 等. 清肠栓质量标准研究[J]. 中成药, 2016, 38(8): 1749-1753. [8] 于天源, 周昕, 徐俐伟. 清肠栓中没食子酸、靛蓝和靛玉红含量测定[J]. 河南中医, 2019, 39(3): 453-458. doi: 10.16367/j.issn.1003-5028.2019.03.0114 [9] 刘斌, 李祥兰, 王晓晓, 等. 气相色谱法同时测定复方丹参片中樟脑残留量及冰片含量[J]. 中国药业, 2019, 28(16): 32-34. doi: 10.3969/j.issn.1006-4931.2019.16.010 [10] 王艳伟, 李桂本, 代雪平. 气相色谱法测定活血消痛酊中樟脑、薄荷脑、龙脑和异龙脑的含量[J]. 西北药学杂志, 2019, 34(5): 612-614. doi: 10.3969/j.issn.1004-2407.2019.05.010 [11] 庞静, 王学涛, 王健, 等. GC法测定牛黄上清丸中冰片的含量[J]. 食品与药品, 2019, 21(3): 187-190. doi: 10.3969/j.issn.1672-979X.2019.03.005 [12] 王伟, 刘星雨, 金辉辉, 等. GC同时测定麝香通心滴丸中龙脑、异龙脑和麝香酮的含量[J]. 中国现代应用药学, 2020, 37(11): 1328-1332. doi: 10.13748/j.cnki.issn1007-7693.2020.11.009 [13] 郭玉岩, 李春成, 王力勋, 等. GC法测定复方洋金花软膏中冰片的含量[J]. 化学工程师, 2020, 34(6): 27-30. doi: 10.16247/j.cnki.23-1171/tq.20200627 [14] 范斌, 柏冬, 刘泓, 等. 气相色谱法测定艾奇康胶囊中龙脑的含量[J]. 中国实验方剂学杂志, 2009, 15(6): 15-17. doi: 10.3969/j.issn.1005-9903.2009.06.006 -





 下载:
下载:

 下载:
下载:


