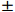-
中风是人类死亡的主要原因之一,全世界范围内中风的发病率、死亡率和致残率均较高。缺血性脑卒中(IS)是常见的一种中风,也是导致人类死亡和残疾的最常见因素[1]。目前溶栓是IS的首选治疗方法,其中药物溶栓最为有效,但往往具有黄金治疗时间,可能约3~8%的患者才有资格使用药物溶栓治疗[2-3]。因此,需要针对IS开发新的药物以提高溶栓治疗的疗效。咪达唑仑是一种有效的短效苯二氮卓类药物,具有抗焦虑、镇静和催眠作用[4]。YU等[5]研究表明咪达唑仑通过抗凋亡机制减少细胞毒性和凋亡,从而保护缺血环境下的神经元,具有治疗中风的潜在能力,但其具体机制仍需探索。线粒体是细胞的能量来源,在决定细胞死亡中起着关键作用,PTEN诱导假定激酶1(PINK1)/E3泛素连接酶(PARKIN)信号通路在线粒体吞噬和线粒体运动中起关键作用,已有研究显示PINK1/PARKIN介导的线粒体自噬在中风后的神经元和组织损伤中起主要作用,能够防止IS后神经元凋亡[6-7]。动脉阻塞法建立IS动物模型是最接近模拟人类IS的模型之一[8-10]。本研究通过动脉阻塞法建立IS大鼠,探讨咪达唑仑是否通过调节PINK1/PARKIN信号通路影响IS大鼠神经元损伤,从而为咪达唑仑治疗脑中风提供理论依据。
-
健康无特定病原体级成年雄性SD大鼠(6周龄,200~230 g)在室温和光照/黑暗(12 h/12 h)交替循环的条件下喂养,并自由获得食物和水。大鼠由郑州大学(河南省实验动物中心)提供,许可证号:SCXK(豫)2022−0001,本研究实验符合《中华人民共和国实验动物指南》规定,并获得动物伦理委员会批准。
-
咪达唑仑注射液(国药准字H20031037,批号20211120)。
-
美国Selleck Chemicals公司提供自噬抑制剂(3-MA);上海天能科技有限公司提供ECL化学发光试剂盒;Abcam公司提供PINK1、ARKIN、微管相关蛋白1轻链3(LC3)及P62一抗;上海生物工程有限公司提供线粒体提取试剂盒、TUNEL试剂盒;北京Solarbio公司提供苏木精-伊红(HE)染色液;美国Bioteke公司提供二辛可宁酸(BCA)蛋白定量试剂盒。
-
美国Bio-Rad公司提供凝胶电泳、转移装置;日本JEOL电子公司提供透射电子显微镜(1400PLUS型)。
-
大鼠适应性喂养一周后,通过中动脉阻塞法建立IS大鼠模型[11]:将麻醉的大鼠置于立体定位框架中,颈部正中央做一切口,手术分离右侧颈总动脉、颈内动脉和颈外动脉,结扎颈外动脉,然后将线栓穿过颈外动脉残端插入颈内动脉,在离插入点约18至22 mm处闭塞大脑中动脉,固定2 h后,抽出线栓并缝合伤口。当大鼠出现自主向左旋转的行为,记为IS大鼠造模成功,术后死亡大鼠给予相应补充。将造模成功的大鼠随机分为IS组、药物低剂量(药物-L)、药物中剂量(药物-M)、药物高剂量(药物-H)组、药物-H+3-MA组,并以仅进行分离血管的正常大鼠为假手术组,其中药物-L组、药物-M组、药物-H组根据参考文献[12]和前期预实验结果分别以30、60、90 mg/kg咪达唑仑进行腹腔注射给药干预,同时给予生理盐水干预;药物-H+3-MA组在给予90 mg/kg咪达唑仑腹腔注射给药的同时,以30 mg/kg 3-MA灌胃给药干预[13];其余各组分别以等体积的生理盐水腹腔注射、灌胃干预,每日一次,连续两周。
-
以有经验的测试者根据Longa方法采用双盲设计评估神经功能缺损评分,神经功能缺损评分中无神经功能缺损症状,活动正常,记为0分;大鼠左前肢不能完全伸直,记为1分;大鼠爬行时转向对侧,记为2分;自发的向左转圈或行走,记为3分;大鼠无法行走,失去知觉,记为4分。
-
神经功能评分结束后,随机取5只大鼠麻醉,用0.9%生理盐水经心脏灌注,然后用4%多聚甲醛灌注,直到四肢僵硬,立即取出大脑,并在4 ℃下经固定剂固定部分脑组织24 h。将脑组织包埋在石蜡中,并切成连续的冠状切片,然后将切片脱蜡、再水合并用苏木精伊红染色,于显微镜下观察并拍照。
-
取1.2.3中脑组织石蜡片,脱蜡后按照试剂盒要求检测TUNEL阳性细胞,并计算凋亡率,其中棕黄色或棕褐色颗粒为阳性细胞。
-
取部分脑组织皮质区,并以戊二醛、四氧化锇固定,经浸透、包埋、聚合后制备超薄切片,透射电镜下观察皮质区自噬小体的变化。
-
利用线粒体分离试剂盒提取剩余8只大鼠脑组织线粒体,在含有蛋白酶抑制剂和磷酸酶抑制剂的RIPA缓冲液中,在玻璃匀浆器中将脑组织匀浆并定量,将蛋白质经过常规十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分离、电转移、抗体反应(PINK1、PARKIN、LC3及P62一抗)后,利用增强化学发光(ECL)试剂盒进行可视化,用荧光成像仪拍摄图像,随后用Image J软件定量分析。
-
采用SPSS 27.0软件分析数据,计量资料以均数
$ \pm $ 标准差($ \bar{x} \pm s $ )表示,P<0.05时,差异有统计学意义。单因素方差分析用于多组间比较,以snk-q检验进一步两两比较。 -
与假手术组相比,IS组神经功能评分显著增加(P<0.001);但经药物-L组、药物-M组、药物-H组干预后,神经功能评分逐渐降低,呈剂量依赖性(P<0.001);与药物-H组相比,药物-H+3-MA组神经功能评分显著增加(P<0.001),见图1。
-
假手术组脑组织皮质区结构完整,未见细胞变性,神经元形态饱满,数量较多;而IS组皮质区结构间隙较大,结构疏松,神经元数量明显减少;药物-L组、药物-M组、药物-H组病理状况有所改善,神经元形态逐渐改善,数量逐渐增加;但药物-H+3-MA组较药物-H组皮质区结构呈筛网状,神经元存在坏死现象,见图2。
-
与假手术组相比,IS组神经元凋亡率显著增加(P<0.001);但经药物-L组、药物-M组、药物-H组干预后,神经元凋亡率逐渐降低,呈剂量依赖性(P<0.001);与药物-H组相比,药物-H+3-MA组神经元凋亡率显著增加(P<0.001),见图3、表1。
表 1 各组大鼠细胞凋亡变化比较(
$ \bar{x} \pm s $ ,n=5)组别 凋亡率(%) 假手术组 6.22±0.63 IS组 21.28±2.13*** 药物-L组 16.11±1.63### 药物-M组 11.32±1.14### 药物-H组 8.02±0.81### 药物-H+3-MA组 17.11±1.72△△△ ***P<0.001,与假手术组比较; ###P<0.001,与IS组比较;△△△P<0.001,与药物-H组比较。 -
与假手术组相比,IS组脑组织皮质区自噬小体的数目增加;经药物-L组、药物-M组、药物-H组干预后,皮质区自噬小体的数目也呈现增加趋势,以药物-H组最为显著;但药物-H+3-MA组较药物-H组自噬小体的数目逐渐减少,见图4。
-
与假手术组相比,IS组脑组织线粒体PINK1、ARKIN、LC3及P62蛋白显著增加(P<0.001);与IS组相比,药物-L组、药物-M组、药物-H组PINK1、PARKIN、LC3蛋白表达增加,P62蛋白显著降低,呈剂量依赖性(P<0.01或P<0.001);与药物-H组相比,药物-H+3-MA组PINK1、PARKIN、LC3蛋白表达降低,P62蛋白显著增加(P<0.001),见图5、表2。
表 2 脑组织线粒体中PINK1、PARKIN、LC3及P62表达比较(
$ \bar{x} \pm s $ ,n=8)组别 PINK1/β-actin PARKIN/β-actin LC3/β-actin P62/β-actin 假手术组 0.29±0.03 0.41±0.05 0.38±0.04 0.64±0.07 IS组 0.55±0.06*** 0.69±0.07*** 0.62±0.07*** 1.85±0.19*** 药物-L组 0.72±0.08## 0.96±0.10### 0.83±0.09## 1.34±0.14### 药物-M组 0.92±0.10### 1.39±0.14### 1.24±0.13### 1.06±0.11### 药物-H组 1.34±0.15### 1.67±0.17### 1.67±0.17### 0.72±0.08### 药物-H+3-MA组 0.66±0.07△△△ 0.88±0.09△△△ 0.75±0.08△△△ 1.42±0.15△△△ ***P<0.001,与假手术组比较; ##P<0.01,###P<0.001,与IS组比较;△△△P<0.001,与药物-H组比较。 -
咪达唑仑是一种γ-氨基丁酸A苯二氮卓类受体激动剂,是诱导镇静的常用麻醉剂,咪达唑仑处理可维持树突结构,并且不影响麻醉期间的神经元发育,研究表明咪达唑仑可以保护大脑中动脉闭塞诱导的神经元变性和神经细胞凋亡[14]。本研究发现IS大鼠神经功能评分、神经元凋亡率显著增加,HE结果显示皮质区病理损伤严重,皮质区结构疏松、间隙较大,提示IS大鼠的构建伴随着严重的神经元损伤,与杨秋怡等[15]结果相吻合。但经不同剂量的咪达唑仑治疗后,病理损伤得到改善,神经功能评分、神经元凋亡率显著降低,呈剂量依赖性,提示咪达唑仑尤其是高剂量咪达唑仑可保护IS大鼠神经元损伤,但其机制仍未阐明。
自噬是一种基因程序化的过程,选择性自噬最典型的类型是线粒体自噬,即针对受损的线粒体进行降解,促进线粒体的更新,防止功能障碍的细胞器积累[16-17]。在自噬过程中,LC3羧基端经剪切后形成LC3I,LC3I泛素化后形成LC3II,在自噬体膜表面附着,LC3II与LC3I比值是判断自噬体形成的标志。LC3与P62结合形成自噬小体,P62会随溶酶体的降解而降解,P62与自噬强弱呈反比[10]。PINK1-PARKIN介导的线粒体自噬在线粒体质量控制中起关键作用,并与多种疾病相关,包括神经退行性疾病、心血管疾病以及脑缺血损伤[18-19]。在脑缺血再灌注大鼠中,活血荣络方在一定程度上通过激活PINK1/Parkin介导的自噬抑制神经元损伤,保护大鼠受损脑组织[20]。本研究结果发现IS大鼠自噬小体较多,线粒体中PINK1、PARKIN、LC3及P62蛋白显著增加,提示IS大鼠脑组织中自噬体增加,但并未得到及时降解;经咪达唑仑干预后,IS大鼠自噬小体逐渐增多,线粒体中PINK1、PARKIN、LC3蛋白显著增加,P62蛋白表达降低,提示咪达唑仑可通过激活PINK1/PARKIN信号通路激活线粒体自噬,并加快自噬体降解,减轻IS大鼠神经元损伤。为进一步验证实验结论,以自噬抑制剂3-MA进行回复验证,结果发现3-MA逆转了咪达唑仑对IS大鼠神经元损伤的保护作用,表明咪达唑仑改善IS大鼠神经元损伤,与激活PINK1/PARKIN信号通路有关。
综上所述,咪达唑仑通过激活PINK1/PARKIN信号通路诱导IS大鼠线粒体自噬,降低神经元凋亡,改善IS大鼠神经元损伤,为咪达唑仑治疗脑中风提供理论依据。
Effect of midazolam on neuronal damage in ischemic stroke rats by regulating the PINK1/PARKIN signaling pathway
-
摘要:
目的 探讨咪达唑仑对缺血性脑卒中(IS)大鼠神经元损伤的影响及其与PTEN诱导假定激酶1(PINK1)/E3泛素连接酶(PARKIN)信号通路的调节作用。 方法 通过动脉阻塞法建立IS大鼠模型,将造模成功的大鼠随机分为IS组、药物低、中、高剂量(药物-L、M、H,30、60、90 mg/kg咪达唑仑)组、药物-H+自噬抑制剂-3-MA组(90 mg/kg咪达唑仑+30 mg/kg 3-MA),并以仅分离血管的大鼠为假手术组,各组均进行相应剂量药物或生理盐水干预,随后进行神经功能评分、脑组织病理学、神经元凋亡、超微结构以及线粒体中PINK1、PARKIN、微管相关蛋白1轻链3(LC3)及P62蛋白表达检测。 结果 与IS组相比,药物-L组、药物-M组、药物-H组病理损伤得到改善,自噬小体呈现增加趋势,PINK1、PARKIN、LC3蛋白表达增加,神经功能评分、神经元凋亡率、P62蛋白显著降低,呈剂量依赖性(P<0.01或P<0.001);与药物-H组相比,药物-H+3-MA组病理损伤加重,自噬小体减少,PINK1、PARKIN、LC3蛋白表达降低,神经功能评分、神经元凋亡率、P62蛋白显著增加(P<0.001)。 结论 咪达唑仑通过激活PINK1/PARKIN信号通路诱导IS大鼠线粒体自噬,降低神经元凋亡,改善IS大鼠神经元损伤。 Abstract:Objective To investigate the effect of midazolam on neuronal damage in ischemic stroke (IS) rats and its regulatory effect on PTEN-induced putative kinase 1 (PINK1)/E3 ubiquitin ligase (PARKIN) signaling pathway. Methods An IS rat model was established using arterial occlusion method. The rats with successful model were randomly divided into IS group, drug-low, medium, high-dose (drug-L, M, H, 30, 60, 90 mg/kg midazolam) groups, drug-H+autophagy inhibitor 3-MA group (90 mg/kg midazolam+30 mg/kg 3-MA), and rats with only isolated blood vessels were used as sham surgery groups. Each group received corresponding doses of drugs or physiological saline intervention, and the neurological function scoring, brain histopathology, neuronal apoptosis, ultrastructure, and expression of PINK1, PARKIN, microtubule-associated protein 1 light chain 3 (LC3), and P62 protein in mitochondria were detected. Results Compared with the IS group, the pathological damage of the drug-L group, drug-M group, and drug-H group was improved, and autophagosomes showed an increasing trend, the expression of PINK1, PARKIN, and LC3 proteins increased, the neurological function score, neuronal apoptosis rate, and P62 protein obviously decreased in a dose-dependent manner (P<0.01 or P<0.001); compared with the drug-H group, the pathological damage in the drug-H+3-MA group increased and autophagosomes decreased, the expression of PINK1, PARKIN, and LC3 proteins decreased, the neurological function score, neuronal apoptosis rate, and P62 protein obviously increased (P<0.001). Conclusion Midazolam induced mitochondrial autophagy in IS rats by activating the PINK1/PARKIN signaling pathway, neuronal apoptosis was reduced and neuronal damage were improved in IS rats. -
Key words:
- KER WORDS Midazolam /
- PINK1/PARKIN signaling pathway /
- Ischemic stroke /
- Neuron /
- Autophagy /
- Apoptosis
-
0. 前言
RRx-001化学名称为2-溴-1-(3, 3-二硝基氮杂环丁烷-1-基)乙烷-1-酮,结构如图1所示。RRx-001是由EpicentRx公司研发、具有首创潜质的小分子药物,经过美国食品药品监督管理局(FDA)批准,RRx-001作为孤儿药进入临床试验用于治疗小细胞癌、神经内分泌癌和胶质母细胞瘤的患者。另外,RRx-001作为放疗增敏剂也已进入临床试验。RRx-001不仅可作为单药用于临床,还可与化疗、放疗、靶向药物及其他免疫疗法联合使用[1, 2]。RRx-001具有较短的半衰期,体内代谢较快[3],临床试验采用口服给药或静脉给药[4]。作为一种新型抗肿瘤药物,RRx-001因其结构中包含的α-溴乙酰基片段,可通过双分子亲核取代反应机制与游离的巯基如还原性谷胱甘肽和血红蛋白β链上Cys93等发生选择性化学反应[5]。 RRx-001最常见的副作用是静脉输液相关疼痛,因此临床试验研究时将RRx-001与患者血液混合后给药,并且控制较慢的输注速度 [6, 7]。本文综述了RRx-001的作用机制研究最新进展,总结了近年来RRx-001临床试验的研究结果,为RRx-001进一步结构优化和临床应用研究提供了事实依据和指导方向。
1. RRx-001的作用机制研究新进展
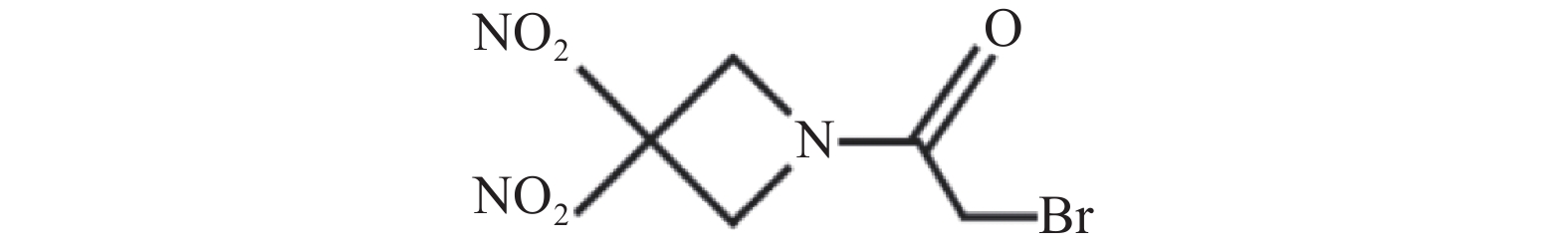
早期研究表明,RRx-001是一种NO拮抗剂,不仅可作为NO供体,而且能作为“红细胞吞噬免疫治疗剂”,可增加红细胞对肿瘤血管的依附性[8]。血红蛋白β链上的Cys93与RRx-001结合位后,释放出NO并入血。在缺氧条件下,RRx-001能增强脱氧血红蛋白亚硝酸盐还原酶的活性,使NO的生成大大增加[9]。RRx-001能选择性并不可逆地与血红蛋白β链上的Cys93结合[10],增加红细胞对内皮的黏附能力,提高红细胞膜磷脂酰丝氨酸表达量,并且可使红细胞优先定位到实体瘤 [11]。与RRx-001结合后的红细胞优先粘附在肿瘤血管内皮后,肿瘤便以“特洛伊木马”的方式内化和分解代谢,释放具有氧化还原活性的RRx-001和红细胞代谢物(图2)[12]。
此外,RRx-001是一种Myc蛋白抑制剂,通过抑制Myc可下调PD-L1的表达从而抑制免疫逃逸。研究表明,RRx-001还可作为Nrf2诱导剂发挥放化疗保护作用,Nrf2是bZip转录因子,属于调控蛋白,Nrf2能通过细胞氧化还原状态的改变而被激活,并通过上调抗氧化剂、异种生物代谢和其他细胞保护酶来恢复细胞内稳态[13]。RRx-001能促进Nrf2在人克隆结肠腺癌细胞(Caco-2细胞)核内的积累,导致血清HO-1的表达显著增加[14]。但RRx-001对Nrf2的调控具有“双刃剑”作用,Nrf2长期激活亦有促癌作用,可以诱导氧化应激,使老年人或慢性病患者OS水平升高[15]。抑制G6PD活性可能是RRx-001发挥抗肿瘤作用的另一个重要机制,研究发现,RRx-001能以浓度依赖的方式抑制G6PD [16]。作为一种有效的G6PD抑制剂,RRx-001已处于临床试验用于小细胞肺癌患者的治疗。并且,RRx-001与JQ1的联合治疗显著降低了皮下肿瘤组织中KEAP1的表达水平,通过调控KEAP1-Nrf2-G6PD轴,抑制小细胞肺癌细胞的氧化还原代谢[17]。
迄今为止,RRx-001的作用机制尚未明确。近年来研究表明,RRx-001除可能通过以上作用机制发挥抗肿瘤活性以外,还可能作为CD47小分子调节剂发挥抗肿瘤免疫活性。并且也可作为NLRP3抑制剂起到抗炎作用,进一步拓展其在抗肿瘤和抗炎药物开发的应用。
1.1 RRx-001通过调控CD47信号通路发挥抗肿瘤免疫活性
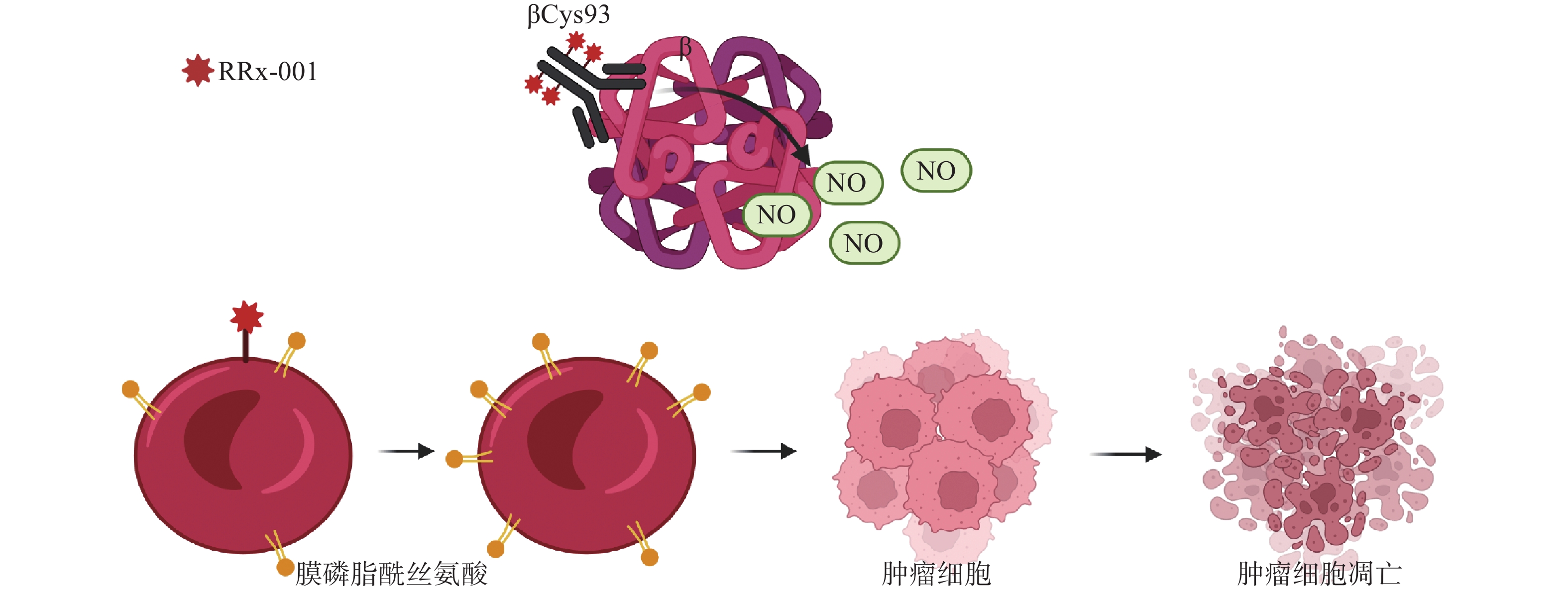
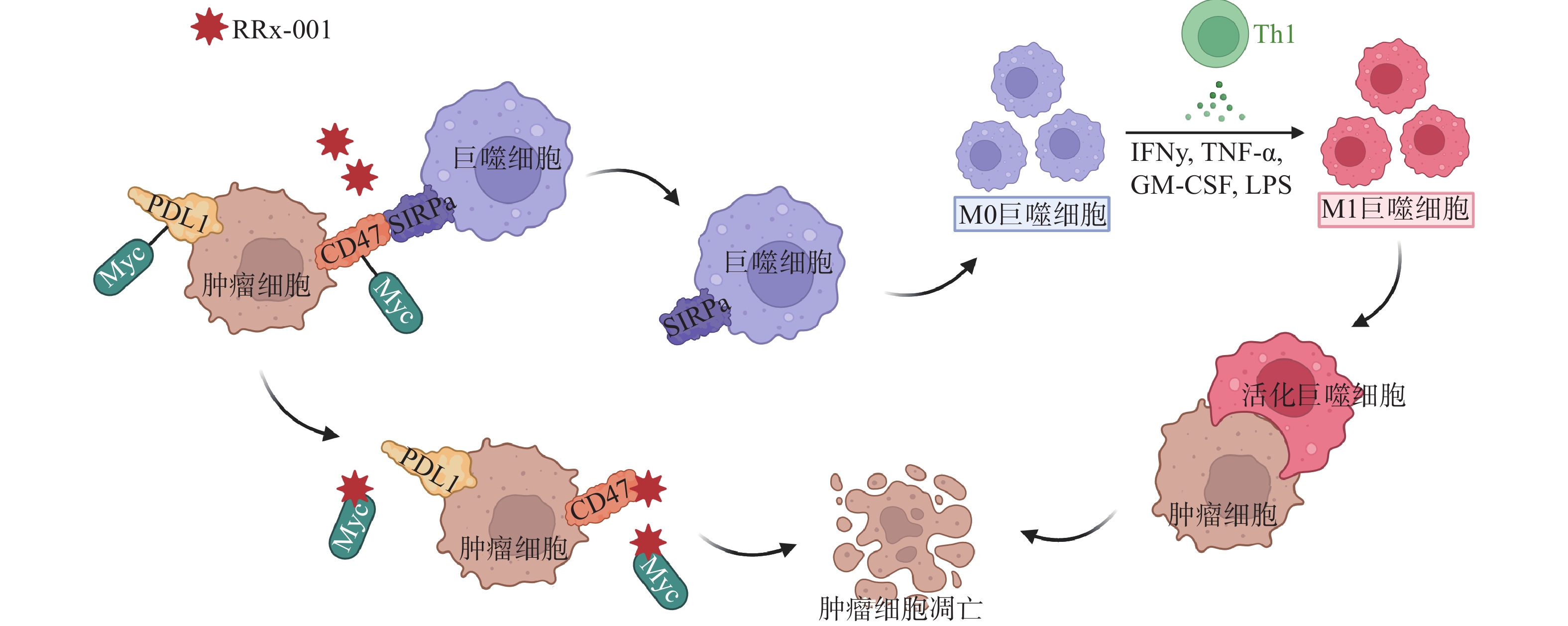
CD47是肿瘤细胞上一种广泛表达的细胞表面蛋白,能传递抗吞噬的信号从而阻止巨噬细胞介导的对肿瘤细胞的吞噬[18]。通过下调CD47的表达,可恢复巨噬细胞的作用,使巨噬细胞向M1巨噬细胞分化,刺激颗粒细胞瘤(GCT)的吞噬作用从而可达到杀灭肿瘤细胞的作用[19]。RRx-001是首个进入临床的CD47小分子调节剂,降低了肿瘤细胞和单核/巨噬细胞上CD47的表达水平,恢复了CD47-SIRPα相互作用导致的吞噬抑制功能(图3)。体内研究证实,肿瘤微环境中浸润巨噬细胞的存在是RRx-001具有抗肿瘤活性的必要条件[20]。研究表明,作为CD47小分子调节剂,RRx-001还可以与pH响应型纳米药物以及T型钙通道抑制剂联用,将药物输送到肺肿瘤中对肿瘤细胞起到杀伤作用[21]。
1.2 RRx-001通过抑制NLRP3信号通路产生抗炎作用
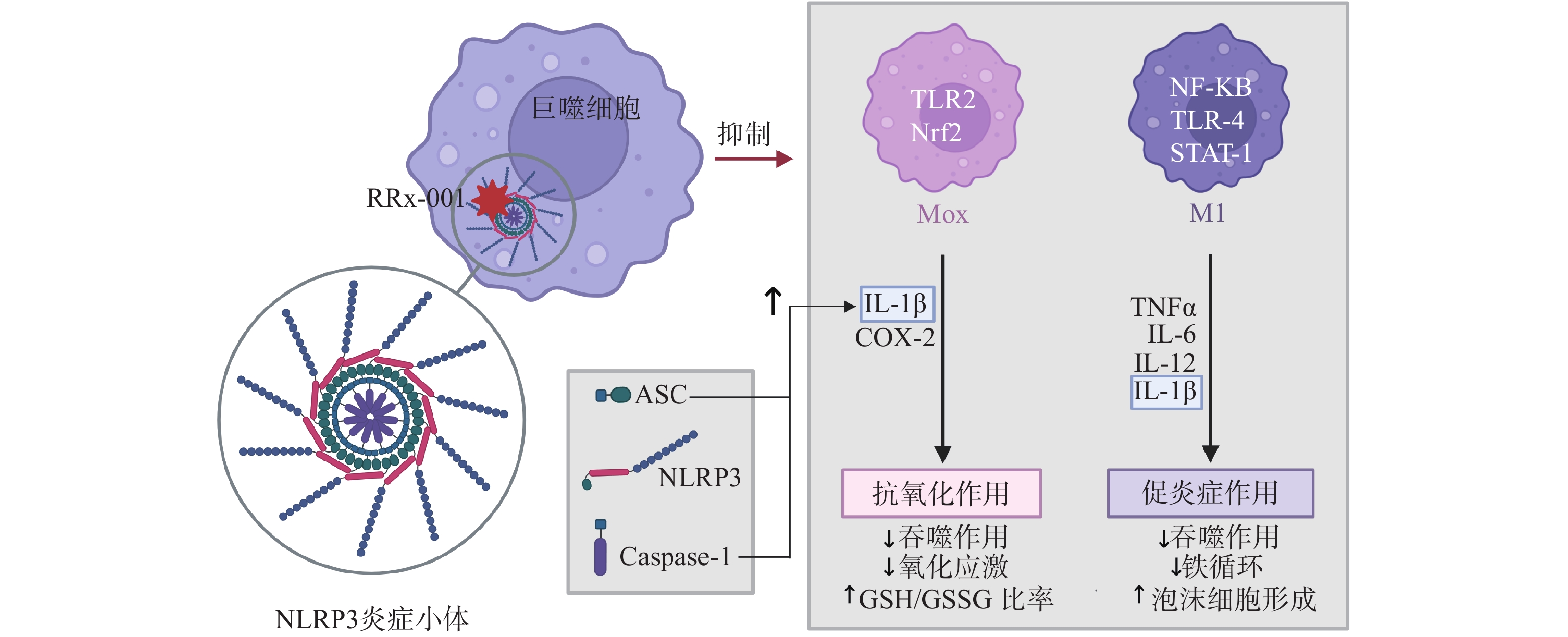
NLRP3炎症小体是固有免疫的主要组成成分之一,在机体免疫反应和炎症性疾病发生发展过程中起到了非常重要的作用,炎症小体激活的失调导致一些自身炎症性疾病如代谢综合征、2型糖尿病、阿尔兹海默病、心血管疾病、癌症等,这些疾病与较高水平的IL-1β和IL-18分泌有关[20]。RRx-001是NLRP3炎症小体的双重抑制剂,能选择性与NLRP3中心结构域的半胱氨酸结合[15],并且与NLRP3的结合能以级联的方式抑制巨噬细胞的极化,减少IL-1β的释放,阻滞增强的免疫反应和自身免疫的发生(图4)[14]。RRx-001还能剂量依赖性抑制ASC的聚合,直接抑制NEK7、NLRP3和ASC间的相互作用以及NEK7和NLRP3之间的相互作用,进而抑制NLRP3炎症小体的组装过程。[22]
2. RRx-001的临床研究进展
RRx-001的临床研究主要是以肿瘤为适应症,进展最快的已进入Ⅲ期临床试验,研究较多的为小细胞肺癌和非小细胞肺癌,其他如结直肠癌、脑转移癌等研究亦有所涉及。除肿瘤外,因发现RRx-001可作为NLRP3抑制剂,一些炎症相关和神经保护的临床试验研究也正在开展,在今年热点COVID-9领域中的研究也证明了RRx-001对于新冠肺炎导致的急性呼吸道症状可能具有治疗作用[23-25]。综述[26]总结了RRx-001的3个主要临床试验:ROCKET、G-FORCE和QUADRUPLE THREAT,本文在此基础上,对RRx-001的临床试验进行了深入系统总结(表1)。
表 1 RRx-001部分临床试验序号 名称 临床试验 临床阶段 试验时间 给药剂量 适应证 1 剂量依赖性试验 NCT01359982 Ⅰ期 2011.10至2013.03 推荐剂量16.7 mg/m2 肿瘤 2 PRIMETIME NCT02518958 Ⅰ期 2015.01至2015.11 剂量递增,最大剂量16 mg 晚期转移性癌症 3 G-FORCE-1 NCT02871843 Ⅰ期 2016.07至2018.05 推荐剂量4 mg 高级别胶质母细胞瘤 4 BRAINSTORM NCT02215512 Ⅰ/Ⅱ期 2015.02至2017.02 推荐剂量10 mg/m2 脑转移瘤全颅放疗 5 ROCKET NCT02096354 Ⅱ期 2014.06起 4 mg 三/四线转移性结直肠癌 6 QUADRUPLE THREAT NCT02489903 Ⅱ期 2015.06起 4 mg+自体静脉血12 ml 小细胞肺癌,EFGR突变的非小细胞肺癌,
高级别神经内分泌肿瘤,卵巢肿瘤7 PREVLAR NCT03515538 Ⅱ期 2018.07至2019.08 4 mg 口腔黏膜炎 8 REPLATINUM NCT03699956 Ⅲ期 2019.03起 4 mg 三线小细胞肺癌 2.1 剂量依赖性临床试验
剂量依赖性临床试验是一项较早开展,首次进入人体的开放式I期临床试验。研究评估了RRx-001的安全性、耐受性、剂量推荐和毒性反应情况。研究于2011-2013年共招募25例患者,给药剂量递增前有两周观察期,3名患者的起始剂量为10 mg/m2,剂量递增依次为 16.7、24.6、33、55 mg/m2和 83 mg/m2,每个剂量组中至少入组3名患者。治疗持续到病情进展或出现剂量依赖毒性反应或其他不良事件出现,每个治疗日都进行标准的血液检查和化学检查,同时观测治疗效果。从研究结果可以看出,RRx-001总体具有良好的耐受性,不良反应多为1~2级,主要不良反应为输液相关手臂疼痛,因而推荐每周16.7 mg/m²的剂量为Ⅱ期临床试验剂量[27]。
2.2 PRIMETIME
PRIMETIME是一项针对于晚期转移性癌症的I期先导性研究,研究采用了3+3的形式确定每个剂量水平的联合用药安全性。研究选用的给药方法是对于入选的晚期癌症患者每周使用一次递增剂量的RRx-001,同时与每隔一周3 mg/kg的纳武利尤单抗联合使用,RRx-001的最高剂量为16 mg,每6周评估一次治疗效果。由于样本量较小,研究结果暂无统计学意义,现有数据表明RRx-001参与的治疗总体耐受性良好,肿瘤相关巨噬细胞密度可能与RRx-001相关联。但是,RRx-001给药期间观察到假性进展即肿瘤先随着免疫细胞的渗透而增大,后因肿瘤细胞的清除退化趋于稳定。此项临床试验研究初步提供了RRx-001有效性的证据,以及进一步的临床研究方案依据[28]。
2.3 G-FORCE-1
G-FORCE-1是一项非随机、开放式,分为两部分的I期临床试验,研究放疗时RRx-001和替莫唑胺剂量递增或固定剂量带来的临床治疗效果。临床试验包括6组患者,所有患者均接受了总剂量60 G,30次照射。前4组患者照射期间接受每日75 mg/m2剂量的替莫唑胺和每周递增剂量的RRx-001,依次为0.5、1、2、4 mg,最多治疗6次。替莫唑胺的剂量由放疗结束6周后开始,起始剂量变为150 mg/m2,28 d为一个周期,连续治疗5个周期,如无2级以上不良反应则增加到200 mg/m2,连续治疗6个周期。第5和第6组患者则是在照射期间接受每日75 mg/m2剂量的替莫唑胺和每周固定剂量的RRx-001(4 mg),放疗结束6周后,第5组患者开始接受100 mg/m2替莫唑胺和0.5 mg RRx-001,第6组患者接受100 mg/m2替莫唑胺和4 mg RRx-001,治疗结束的标准均为病情进展或完成6个周期的治疗。结果表明,在放疗和替莫唑胺治疗方案中添加RRx-001可以增加其治疗耐受性,提高受试者生活质量。并且,降低了毒性如血液学毒性的减少、部分骨髓保护作用[29]。
2.4 BRAINSTORM
BRAINSTORM是一项单臂、多机构、开放式I/Ⅱ期临床试验,旨在研究RRx-001对于脑转移瘤患者全颅放疗的安全性和有效性。在此研究中,患者在全颅放疗前两周,每周两次,以及放疗前的第2天和第4天静脉给药RRx-001,并且在放疗疗程进行的第1、4、8、11天接受RRx-001治疗,剂量升级梯度为10、17、33、55 mg/m²。治疗期间使用磁共振对患者炉内病灶进行评估,对最佳颅内总反应率和总生存期进行计算评估。研究表明,RRx-001和全颅放疗之间具有潜在协同作用,RRx-001治疗总体耐受良好。尽管接受RRx-001治疗的患者颅内疾病控制率和仅接受全颅放疗的患者相比无统计学改善,并且总生存期也没有明显改变。但是,没有出现患者死于神经系统疾病,这一定程度上肯定了RRx-001对于脑的保护作用[30]。
2.5 ROCKET
ROCKET是一项旨在比较RRx-001 和伊立替康联合使用与瑞格菲尼单药在既往接受伊立替康治疗的三、四线结肠直肠癌患者中的安全性和有效性。34例患者以2∶1的比例接受RRx-001治疗,即RRx-001治疗组的患者先用4 mg的RRx-001作为“入门药”治疗两个月,若被认为临床适用则给予180 mg/m2的伊立替康。另一组则是患者接受160 mg瑞格菲尼,若被认为临床适用则再给予180 mg/m2的伊立替康。治疗后每周观察患者病情进展情况并计算患者的无进展生存期和总生存期。研究表明,在三、四线晚期结直肠癌的治疗中,先使用RRx-001,然后再给予伊立替康治疗可能是一种有效的治疗方案,这种方法比瑞格菲尼单药带来更好的疗效,显著改善无进展生存期和总生存期,并且毒性更低。但此研究规模较小,需要进一步扩大样本量确认RRx-001的有效性[31]。ROCKET实验后,动物实验又验证了RRx-001与瑞格菲尼联用的可能性,实验结果证明联合用药可以提升抗肿瘤活性并且减小副作用[32]。
2.6 QUADRUPLE THREAT
QUADRUPLE THREAT是一项探索性、开放式Ⅱ期临床试验,评估了既往治疗过的小细胞肺癌、EGFR突变的非小细胞肺癌、恶性程度较高神经内分泌肿瘤和卵巢癌患者使用RRx-001后再进行铂类化疗的安全性和可行性。此项研究中患者接受每周一次4 mg的RRx-001混合自身12 ml自体静脉血共同输注,这是为了减少剂量增加后导致的凝血和溶血风险。在RRx-001治疗的过程中通过影像检查评估患者的肿瘤进展状况,若出现肿瘤进展或临床恶化则使用6个周期化疗药物治疗,如给予100 mg/m2的依托泊苷或60 mg/m2的顺铂。研究结果证明,RRx-001的耐受性良好并与既往治疗过的小细胞肺癌患者中对依托泊苷和其他铂类药物的后续反应相关。临床目前的标准治疗并不有效,对于接受临床三线及以上治疗的患者,RRx-001给此类患者的后续治疗提供了可能性[33]。动物实验将RRx-001的疗效和安全性与铂类药物进行对比,结果证明RRx-001的疗效明显高于其他铂类药物略低于顺铂,但毒性明显低于顺铂,与临床结果一致[3]。
2.7 PREVLAR
PREVLAR是一项随机、无盲、开放式Ⅱa期临床试验,旨在研究RRx-001对头颈部癌症患者化放疗导致口腔黏膜炎的治疗方案安全性和有效性。在此研究中53名患者被分为4组,在以顺铂为基础的化放疗外,1~3组在开始化放疗两周前地塞米松处理后接受每周两次4 mg的RRx-001,第4组则不接受RRx-001的干预。1~3组在开始化放疗后进行不同处理,第2组在疗程的第2和第5周再接受两次4 mg的RRx-001,第3组则在疗程的前6周每周接受一次4 mg的RRx-001,第1组疗程内不接受RRx-001的干预。化放疗开始后每周对口腔黏膜炎进行两次评估,直至溃疡性口腔黏膜炎消除,此为观察结束终点。研究结果表明,接受RRx-001治疗后溃疡性口腔黏膜炎的病程缩短,严重程度和症状有明显减轻,因而体现出放疗保护作用。研究还指出RRx-001似乎不能降低放疗期间罹患溃疡性口腔黏膜炎的绝对风险,但可显著缩短其持续时间。并且,RRx-001治疗方案未见明显不良反应,耐受性良好。此研究使RRx-001获得FDA快速通道资格,可作为放疗保护剂预防或改善严重的口腔黏膜炎[15, 34]。
2.8 REPLATINUM
REPLATINUM是一项随机、开放式Ⅲ期临床试验,旨在分析RRx-001和铂类药物联合治疗与仅用铂类药物治疗三线小细胞肺癌的疗效差异。研究将患者1∶1随机分配到两组中,一组接受3周为一个周期、每周一次4 mg的RRx-001和第1~3天的依托泊苷100 mg/m2以及另一种铂类药物如顺铂60 mg/m2或卡铂治疗,若病情好转则交替使用连续两周每周一次4 mg的RRx-001和减量单药铂类药物维持治疗。另一组则仅接受21天为周期的第1~3天的依托泊苷100 mg/m2以及另一种铂类药物如顺铂60 mg/m2或卡铂治疗。治疗一个周期后通过CT评估,此后每两个治疗周期评估一次,安全性评估则贯穿整个治疗过程。目前此研究正在进行中,研究结果将揭示RRx-001对于铂类药物化疗的敏感性,以及和铂类药物交替使用的可行性和安全性[35]。
3. 展望
RRx-001作为一种首创小分子药物,主要作用机制除了NO拮抗剂、Myc抑制剂、G6PD抑制剂以及对于红细胞的作用以外,作用机制研究的热点是作为NLRP3抑制剂、Nrf2诱导剂、CD47抑制剂。目前,RRx-001已经进入了III期临床试验阶段,在此之前,I和Ⅱ期临床试验已经证实其在小细胞肺癌、结直肠癌、头颈部癌、脑转移和神经胶质瘤以及肺部炎症等的治疗效果以及放化疗的增敏和保护作用。尽管RRx-001还没有获批上市,现有临床试验一定程度上证实了RRx-001作为单药使用时以及与其他药物联用时的有效性和安全性,但仍需进一步扩大临床样本开展更大规模的临床试验证实。但是,基于现有临床数据,RRx-001有望成为治疗晚期癌症患者或是恶性程度较高癌症患者的治疗药物。
-
表 1 各组大鼠细胞凋亡变化比较(
$ \bar{x} \pm s $ ,n=5)组别 凋亡率(%) 假手术组 6.22±0.63 IS组 21.28±2.13*** 药物-L组 16.11±1.63### 药物-M组 11.32±1.14### 药物-H组 8.02±0.81### 药物-H+3-MA组 17.11±1.72△△△ ***P<0.001,与假手术组比较; ###P<0.001,与IS组比较;△△△P<0.001,与药物-H组比较。 表 2 脑组织线粒体中PINK1、PARKIN、LC3及P62表达比较(
$ \bar{x} \pm s $ ,n=8)组别 PINK1/β-actin PARKIN/β-actin LC3/β-actin P62/β-actin 假手术组 0.29±0.03 0.41±0.05 0.38±0.04 0.64±0.07 IS组 0.55±0.06*** 0.69±0.07*** 0.62±0.07*** 1.85±0.19*** 药物-L组 0.72±0.08## 0.96±0.10### 0.83±0.09## 1.34±0.14### 药物-M组 0.92±0.10### 1.39±0.14### 1.24±0.13### 1.06±0.11### 药物-H组 1.34±0.15### 1.67±0.17### 1.67±0.17### 0.72±0.08### 药物-H+3-MA组 0.66±0.07△△△ 0.88±0.09△△△ 0.75±0.08△△△ 1.42±0.15△△△ ***P<0.001,与假手术组比较; ##P<0.01,###P<0.001,与IS组比较;△△△P<0.001,与药物-H组比较。 -
[1] ZHAO B, YUAN Q, HOU J B, et al. Inhibition of HDAC3 ameliorates cerebral ischemia reperfusion injury in diabetic mice in vivo and in vitro[J]. J Diabetes Res, 2019, 2019:8520856. [2] XIAO L, DAI Z W, TANG W J, et al. Astragaloside IV alleviates cerebral ischemia-reperfusion injury through NLRP3 inflammasome-mediated pyroptosis inhibition via activating Nrf2[J]. Oxid Med Cell Longev, 2021, 2021(1):9925561. [3] SO P W, EKONOMOU A, GALLEY K, et al. Intraperitoneal delivery of acetate-encapsulated liposomal nanoparticles for neuroprotection of the penumbra in a rat model of ischemic stroke[J]. Int J Nanomedicine, 2019, 14:1979-1991. doi: 10.2147/IJN.S193965 [4] MANSO M A, GUITTET C, VANDENHENDE F, et al. Efficacy of oral midazolam for minimal and moderate sedation in pediatric patients: a systematic review[J]. Paediatr Anaesth, 2019, 29(11):1094-1106. doi: 10.1111/pan.13747 [5] YU H, WANG X Z, KANG F X, et al. Neuroprotective effects of midazolam on focal cerebral ischemia in rats through anti-apoptotic mechanisms[J]. Int J Mol Med, 2019, 43(1):443-451. [6] GUAN R Q, ZOU W, DAI X H, et al. Mitophagy, a potential therapeutic target for stroke[J]. J Biomed Sci, 2018, 25(1):87. doi: 10.1186/s12929-018-0487-4 [7] SUN E, ZHANG J, DENG Y, et al. Docosahexaenoic acid alleviates brain damage by promoting mitophagy in mice with ischaemic stroke[J]. Oxid Med Cell Longev, 2022, 2022:3119649. [8] GUO P P, JIN Z, WU H S, et al. Effects of irisin on the dysfunction of blood-brain barrier in rats after focal cerebral ischemia/reperfusion[J]. Brain Behav, 2019, 9(10):e01425. [9] 杨涛, 刘勇, 曹兴华, 等. 三七总皂苷对短暂性前脑缺血大鼠海马区神经元的修复作用实验研究[J]. 陕西医学杂志, 2023, 52(7):803-808. doi: 10.3969/j.issn.1000-7377.2023.07.006 [10] 周丽娜, 辛欢, 杨敏, 等. 丹参酚酸A对脑缺血大鼠神经功能及热休克蛋白基因表达的影响[J]. 陕西中医, 2022, 8(11):1521-1526. [11] 李亚琴, 任维, 罗钢, 等. 蛭龙活血通瘀胶囊对缺血性脑卒中模型大鼠的作用及对脑皮层神经元线粒体的影响[J]. 中药药理与临床, 2021, 37(5):119-124. [12] 刘建, 叶玉军, 刘树民, 等. 基于p38MAPK信号通路分析咪达唑仑对腰椎间盘突出症模型大鼠疼痛的影响[J]. 中国骨伤, 2023, 9(1):55-60. [13] 陆晓华, 金桂芳, 余河汉, 等. 基于PINK1/Parkin信号通路研究细叶远志皂苷对AD模型小鼠脑组织线粒体自噬的影响[J]. 中国药房, 2021, 7(22):2748-2754. doi: 10.6039/j.issn.1001-0408.2021.22.11 [14] LIU J Y, GUO F, WU H L, et al. Midazolam anesthesia protects neuronal cells from oxidative stress-induced death via activation of the JNK-ERK pathway[J]. Mol Med Rep, 2017, 15(1):169-179. doi: 10.3892/mmr.2016.6031 [15] 杨秋怡, 王琪, 马博. 柔肝通络汤上调血管内皮生长因子及其受体表达对缺血性脑卒中大鼠脑皮质血管再生、神经元损伤的影响[J]. 广州中医药大学学报, 2022, 39(12):2870-2876. [16] PALIKARAS K, LIONAKI E, TAVERNARAKIS N. Mechanisms of mitophagy in cellular homeostasis, physiology and pathology[J]. Nat Cell Biol, 2018, 20(9):1013-1022. doi: 10.1038/s41556-018-0176-2 [17] 王谢, 谢道俊, 杜世超, 等. 肝豆灵片对肝豆状核变性认知障碍模型小鼠海马神经元自噬的作用机制[J]. 陕西中医, 2023, 44(7):833-838. doi: 10.3969/j.issn.1000-7369.2023.07.002 [18] WEN H X, LI L X, ZHAN L X, et al. Hypoxic postconditioning promotes mitophagy against transient global cerebral ischemia via PINK1/Parkin-induced mitochondrial ubiquitination in adult rats[J]. Cell Death Dis, 2021, 12(7):630. doi: 10.1038/s41419-021-03900-8 [19] WU M, LU G, LAO Y Z, et al. Garciesculenxanthone B induces PINK1-Parkin-mediated mitophagy and prevents ischemia-reperfusion brain injury in mice[J]. Acta Pharmacol Sin, 2021, 42(2):199-208. doi: 10.1038/s41401-020-0480-9 [20] 颜思阳, 杨仁义, 刘利娟, 等. 活血荣络方对脑缺血再灌注损伤大鼠PINK1/Parkin信号通路的影响[J]. 中国中医药信息杂志, 2023, 30(2):87-92. -





 下载:
下载:


 下载:
下载: