-
METRNL(Meteorin-like)是一个新发现的分泌蛋白,为神经营养调节因子Meteorin的同源蛋白。2014年,本实验室首次报道METRNL是一个新的脂肪因子,由于其在皮下白色脂肪组织中表达很丰富,故也称为Subfatin[1]。10年来,我们对METRNL的功能进行了多方面的探索,并不断扩展METRNL的研究工具与平台。我们的研究已发现,该蛋白参与调节机体多种病理生理过程,比如:脂肪细胞METRNL可促进白色脂肪分化、脂质代谢并抑制脂肪炎症,从而抵抗高脂饮食诱导的胰岛素抵抗[2];肠上皮细胞METRNL参与调节肠道抗菌肽的平衡[3],且肠道METRNL缺乏会加重溃疡性结肠炎[4];此外,METRNL促进小鼠皮肤创伤愈合[5],并能对抗D-半乳糖诱导的衰老小鼠的认知功能障碍[6]。最近,我们新报道了血液METRNL的主要分泌来源是血管内皮细胞,并发现内皮细胞METRNL对维持血管内皮正常功能和对抗动脉粥样硬化具有重要作用[7]。在这些研究中,我们构建METRNL基因的全身性和各种组织特异性的敲除小鼠,以及多种双基因敲除小鼠,并在体外细胞实验中充分利用METRNL重组蛋白探索相关治疗学意义。除了本实验室,全球其他多个实验室也展开了对METRNL的功能探索,并发现METRNL在能量代谢[8-9]、炎症[10-11]、心脏疾病[12-13]等多种病理生理过程中发挥积极作用。
尽管目前有很多关于METRNL的研究结果提示,该蛋白具有非常好的临床治疗潜力,但有关整体METRNL治疗学探索不多,尤其是长期治疗研究几乎没有。主要原因之一是市场METRNL重组蛋白价格昂贵,而且我们前期研究结果发现:对C57BL/6J 小鼠单次静脉注射1.75 µg METRNL重组蛋白后,血清METRNL在15 min后急剧升高(226 ng/ml),接着在4 h内迅速下降约90%。虽然在注射后24 h仍明显高于基础水平,但此时血中METRNL浓度已下降约97%[2]。因此,以重组蛋白给药方式在动物整体水平研究METRNL的治疗学作用,尤其是长期治疗学作用将产生巨大经济成本。另一方面,对于一些已经体现METRNL治疗潜力的疾病(如动脉粥样硬化),疾病发展缓慢,短期给予METRNL重组蛋白很难起到治疗作用。
因此,本研究旨在构建一株长期稳定高表达METRNL的小鼠作为METRNL的治疗学研究工具,并对该小鼠高表达METRNL的情况进行验证。
-
鼠尾DNA提取试剂盒(CW2094S)购自北京康伟试剂生物科技有限公司;5 × PrimeScript RT Master Mix(Takara 公司);小鼠Tubulin抗体( AT819,碧云天公司);通用型RNA提取试剂盒Ⅱ(AG21022,艾瑞克生物科技);Human Meteorin-like/METRNL DuoSet ELISA试剂盒(DY7867-05,R&D system公司);山羊抗兔 IgG(ab175471)、山羊抗小鼠 IgG(ab216772)、抗METRNL抗体(ab235775)购自Abcam公司。
LightCycler96实时荧光定量PCR仪(Roche公司);TP600PCR仪(Takara公司);5200S化学发光分析系统(Tanon公司)。
-
人METRNL基因条件性过表达(R26-LSL-METRNL+/-)小鼠为实验室前期构建所得。SPF级8周龄 C57BL/6J 小鼠和Dppa-Cre小鼠购自上海南方模式生物技术有限公司。
所有实验小鼠均饲养在独立通气笼盒(IVC)系统中,温度(24±2)℃,相对湿度为40%~60%,饲养期间笼盒内保持清洁,小鼠在笼内自由活动、进食及饮水,动物房内照明系统为自动控制(12 h照明、12 h黑暗)。动物实验标准均依照国家《实验动物护理使用卫生指南》,并经过海军军医大学医学研究伦理委员会批准指导。
-
将剪刀消毒后剪取小鼠尾尖约3 mm,剪碎,按照DNA提取试剂盒的说明书方法提取DNA之后,对目的基因进行PCR扩增,各引物序列见表1。
表 1 PCR扩增实验中的引物序列
基因名称 上游引物(5’→3’) 下游引物(5’→3’) R26-WT TCAGATTCTTTTATAGGGGACACA TAAAGGCCACTCAATGCTCACTAA R26-L-METRNL AAAGTCCCGGAAAGGAGCTG GAGGCTCCATCCAGCAAGTT R26-Stop GGGCAACGTGCTGGTTATTG ACTTGCCCCTTGCTCCATAC 内参基因 TGGGTTGGGTGTCTGTTTCATTGT GATCCACCTGTCTCTGCCTTCC Dppa-Cre TGGGTTGGGTGTCTGTTTCATTGT GACCTTGCATTCCTTTGGCGAGAG 将PCR产物进行1.2% 琼脂糖凝胶电泳,上样量为每孔6 μl,电泳条件为100 V,30 min,结束后进行拍照、分析。
-
将小鼠称重后,腹腔注射1%戊巴比妥钠溶液(100 mg/kg),待小鼠处于深度麻醉后,打开其胸腔,自上下腔静脉汇合处缓慢抽取血液,并转移至1.5 ml EP管静置于室温。迅速剪取小鼠心、肝、脾、肺、肾、脑、白色脂肪和肌肉组织,放入组织冻存管扔进液氮速冻,待取材结束后及时转入−80 ℃超低温冰箱储存。血液于室温静置2 h后离心:4 ℃,3000×g,15 min,分离血清,储存至−80 ℃超低温冰箱。
-
使用RNA提取试剂盒提取组织RNA,将得到的RNA进行浓度测定与吸光度测定后进行逆转录,得到cDNA用于实时荧光定量PCR实验,各引物序列见表2。
表 2 实时荧光定量PCR实验中的引物序列
基因名称 上游引物(5′→3′) 下游引物(5′→3′) 人 METRNL ACCAGCGACTTCGTAATTCAC CAGCTCCACGTCATGGGTG 小鼠 Gapdh GTATGACTCCACTCACGGCAAA GGTCTCGCTCCTGGAAGATG -
取适量组织至2 ml高速离心管,加入蛋白裂解液后,使用高通量匀浆仪匀浆240 s。取出高速离心管,离心:12000 × g,20 min。将上清液转移至另一干净1.5 ml EP管中,进行蛋白浓度测定,剩余样品加入5 × 蛋白上样缓冲液,97 ℃变性10 min得到蛋白样品。
使用10% SDS-PAGE凝胶进行电泳,电泳条件为:150 V,60 min。使用PVDF膜进行转膜,转膜条件为100 V,60 min。
转膜结束后,使用快速封闭液封闭15 min,之后使用1×TBST缓冲液洗膜,5 min × 3次。加入一抗(1∶1000稀释)4 ℃孵育过夜。次日去除一抗孵育液,使用1 × TBST缓冲液洗膜,5 min × 3次。加入二抗孵育液(1∶2 000稀释)常温孵育1 h,用1 × TBST缓冲液洗去二抗,5 min × 4次,结束后即可进行扫膜。
-
使用酶联免疫吸附实验试剂盒(DY7867-05)测定小鼠血清中的METRNL水平,具体操作按照试剂盒说明书进行。
-
实验数据使用GraphPad Prism 8.0进行统计分析。两组间的比较使用双尾t检验,P<0.05视为差异有统计学意义。
-
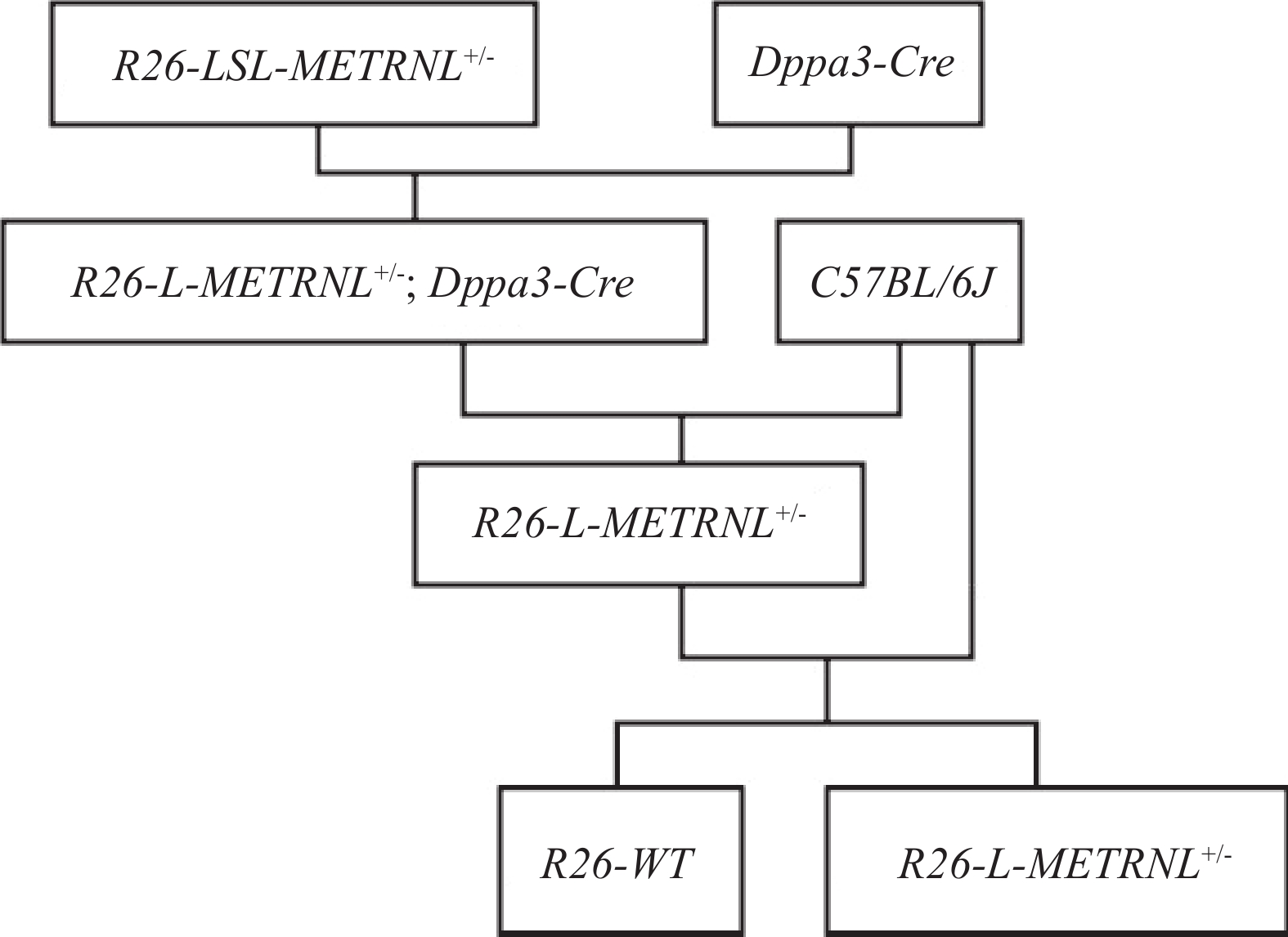
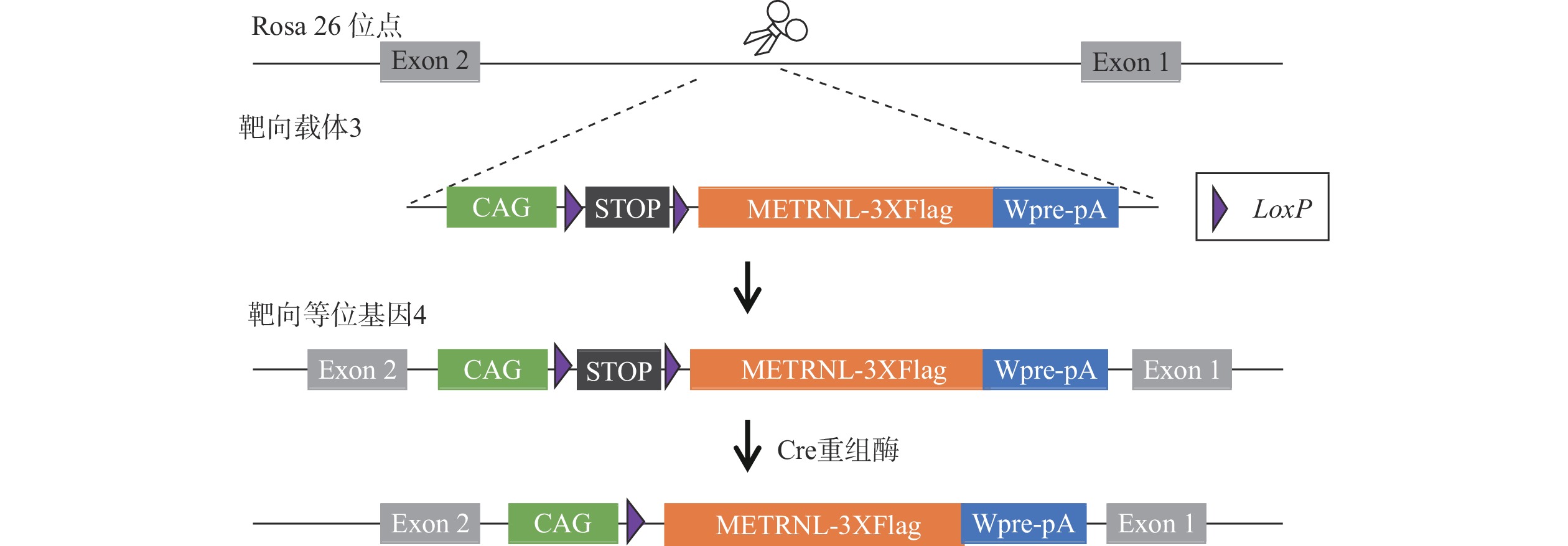
本研究基于前期构建好的人METRNL基因条件性过表达小鼠(简称为R26-LSL-METRNL+/-小鼠)和Cre-LoxP技术,最终获得全身过表达人METRNL基因小鼠(简称为R26-L-METRNL+/-小鼠),具体构建策略如图1所示。
R26-LSL-METRNL+/-小鼠是前期通过CRISPR/Cas9基因编辑技术构建而成,即在其中一个Rosa26基因位点定点插入了CAG-LoxP-Stop-LoxP-METRNL-3XFlag-Wpre-pA表达框,且该表达框的终止密码子Stop两侧插有同向LoxP位点,可基于Cre-loxP系统在Cre酶的作用下,将LoxP位点之间的序列切除,只留下一个LoxP位点,最终达到人METRNL基因过表达的目的。在该小鼠的名称“R26-LSL-METRNL+/-”中,“+”表示有外源基因表达框的插入,“-”表示无外源基因表达框插入。
Dppa3-Cre小鼠是由Dppa3基因启动子介导Cre重组酶在全身表达的工具鼠,将R26-LSL-METRNL+/-小鼠和Dppa3-Cre小鼠杂交,可获得R26-L-METRNL+/-小鼠,具体繁殖方法如图2所示。其中,野生对照小鼠简写为R26-WT,表示在Rosa26位点没有外源人METRNL基因表达框的插入。
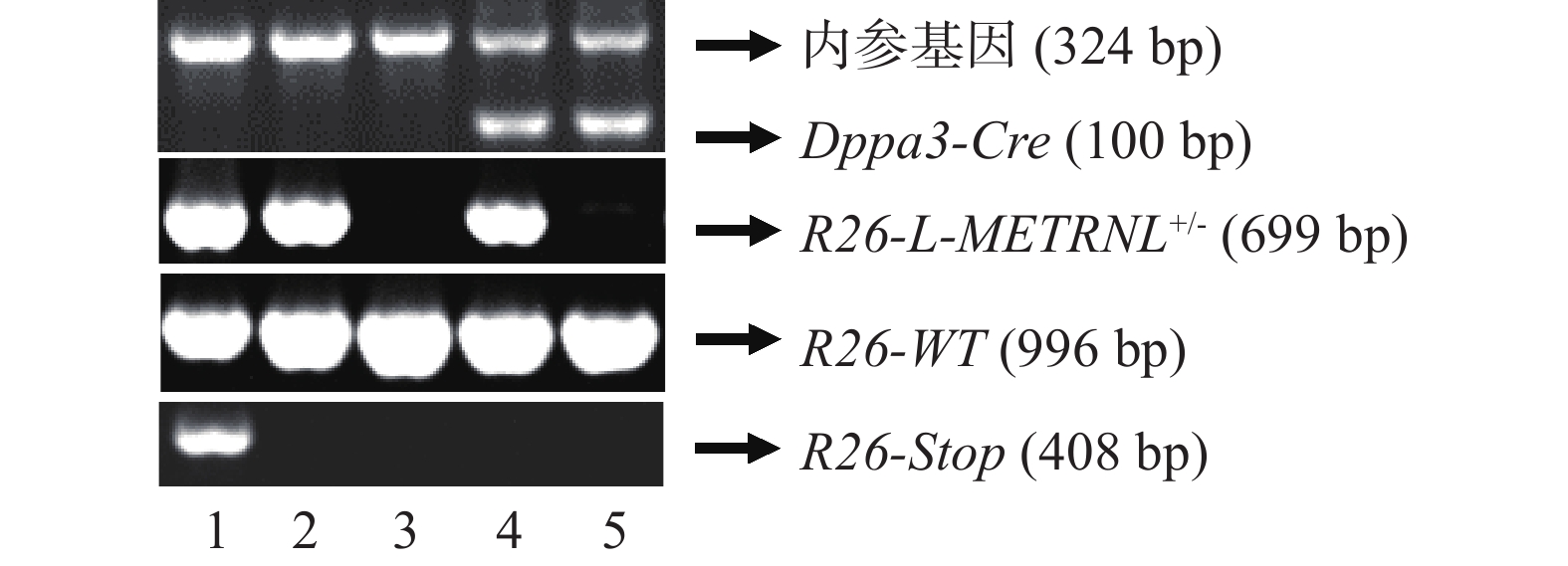
在繁殖过程中进行基因型鉴定时,需确认外源人METRNL基因表达框、终止密码子Stop和Dppa-Cre基因的存在情况。采用相应基因上下游引物分别进行鼠尾基因型鉴定,外源性表达框阳性条带为699 bp,对应野生型序列条带为996 bp,终止密码子Stop阳性条带为408 bp,Cre基因阳性条带为100 bp。如图3所示,泳道1为R26-LSL-METRNL+/-小鼠,泳道2为R26-L-METRNL+/-小鼠,泳道3为R26-WT小鼠,泳道4为R26-L-METRNL+/-Cre小鼠,泳道5为R26-WT;Cre小鼠。
-
为验证R26-L-METRNL+/-小鼠是否存在人METRNL基因过表达,本研究首先利用实时荧光定量PCR技术检测了该小鼠各组织中人METRNL mRNA的表达情况。如图4所示,以 R26-WT 小鼠白色脂肪的人 METRNL mRNA表达量为1,肝、脾、肺、肾、白色脂肪和脑组织的相对表达量分别为94 008.6、618.1、88 537.3、68 897.9、32 386.3和24 816.5。该结果说明,R26-L-METRNL+/-小鼠在组织mRNA水平上实现了人METRNL基因过表达。
-
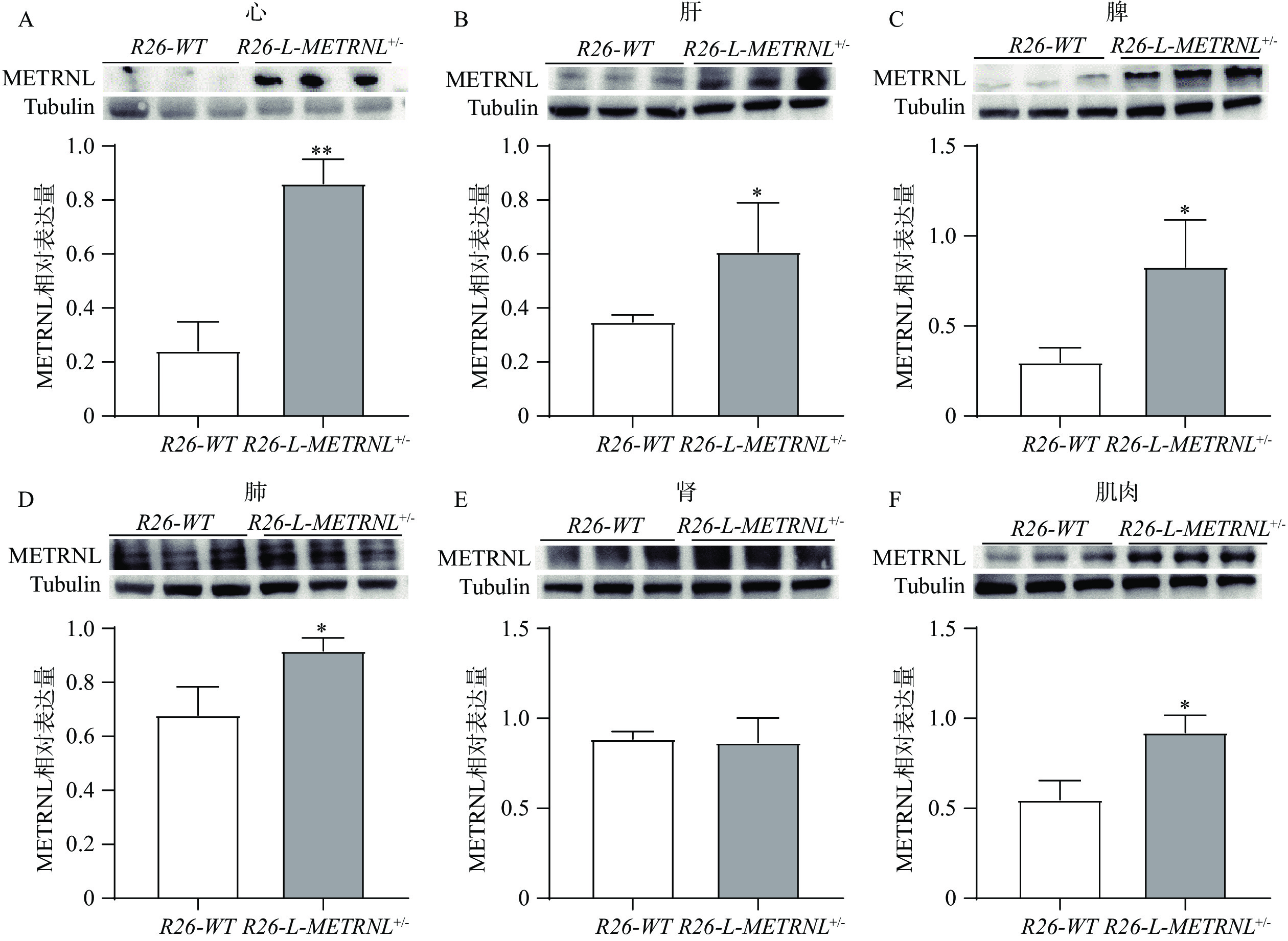
接着,本研究提取各组织的蛋白,使用蛋白免疫印迹实验方法验证R26-L-METRNL+/-小鼠各组织中人METRNL蛋白表达情况。在该实验中,所用METRNL抗体可同时抗人和小鼠的METRNL蛋白。如图5所示,METRNL蛋白在R26-L-METRNL+/-小鼠的心、肝、脾、肺和肌肉组织中的含量明显高于R26-WT小鼠,而在肾组织中METRNL抗体的结合效果不佳,且并未发现两组小鼠肾METRNL蛋白存在明显差异。该结果提示,R26-L-METRNL+/-小鼠在组织蛋白水平上实现了人METRNL基因过表达。
-
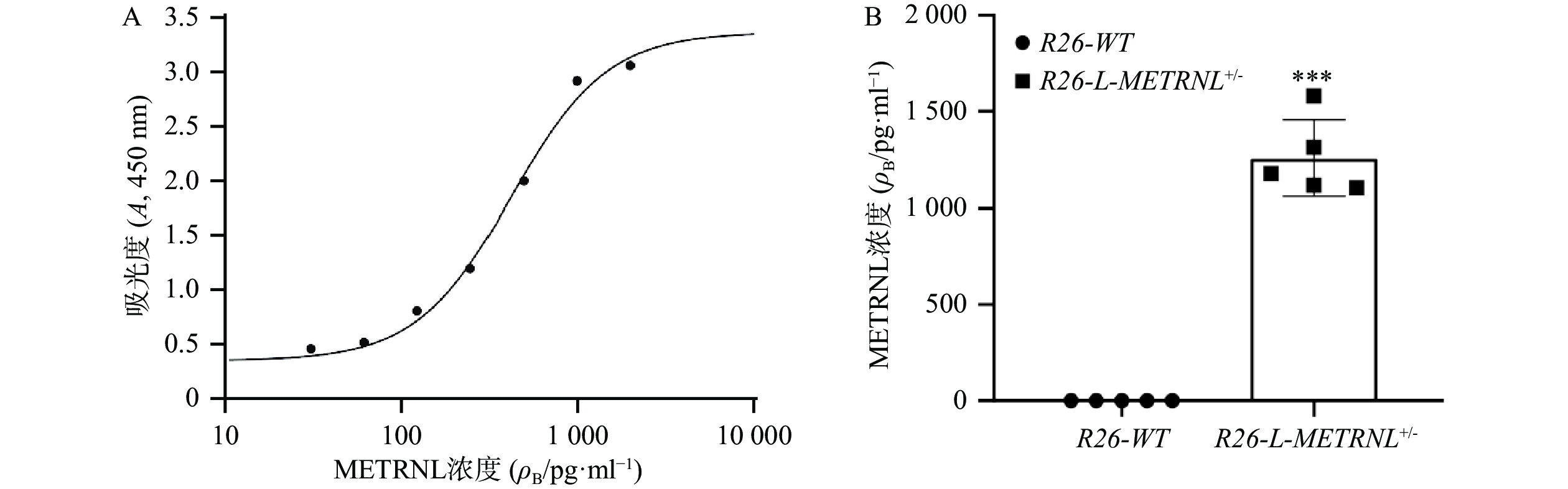
由于METRNL为分泌性蛋白,本研究最后使用ELISA方法测定R26-L-METRNL+/-小鼠及其对照小鼠血清中人METRNL蛋白水平。如图6所示,可成功检测到R26-L-METRNL+/-小鼠血液中的人METRNL,浓度在1 100.3~1 579.3 pg/ml,而在R26-WT小鼠血液中检测不到人METRNL。该结果说明,R26-L-METRNL+/-小鼠的血液中存在大量人METRNL蛋白,提示R26-L-METRNL+/-小鼠实现了人METRNL基因过表达。
-
本研究利用Dppa-Cre小鼠和实验室前期构建的R26-LSL-METRNL+/-小鼠进行杂交繁殖,最终获得R26-L-METRNL+/-小鼠。该小鼠与R26-LSL-METRNL+/-小鼠都在Rosa26基因位点含有外源性基因表达框,不同的是在R26-L-METRNL+/-小鼠外源表达框中的终止密码子Stop被Cre酶成功切除,因此R26-L-METRNL+/-小鼠可实现全身细胞过表达人METRNL。
本研究从mRNA水平、组织蛋白水平和血清蛋白水平考察了R26-L-METRNL+/-小鼠过表达METRNL的情况。由于该小鼠插入的外源METRNL基因是人METRNL基因,因此在进行实时荧光定量PCR实验时,使用的是人METRNL引物和小鼠Gapdh引物。类似地,在ELISA实验中,使用的是检测人METRNL的试剂盒。由于没有特异性抗人的METRNL抗体,因此在蛋白免疫印迹实验中使用的是可同时抗人和小鼠的METRNL抗体,而内参使用的是抗鼠的Tubulin抗体。本研究结果显示,R26-L-METRNL+/-小鼠的各组织存在人METRNL mRNA高表达,虽然各组织的表达量有所波动,但都比R26-L-WT小鼠的表达量高几千倍甚至是数十万倍。蛋白免疫印迹实验结果显示,在R26-L-METRNL+/-小鼠的心、肝、脾、肺、肌肉组织存在明显升高的METRNL蛋白水平,但该实验中检测的METRNL蛋白量升高倍数不多,可能与使用的METRNL抗体可以同时抗人和小鼠的METRNL有关。另外,我们也注意到两组小鼠肾组织的METRNL蛋白水平并没有明显差异,并且两组条带都非常微弱,为确证实验结果,我们进行了重复实验,得出相同结果。经过分析可能是因为该METRNL抗体对肾组织蛋白的亲和力不是很高,导致检测出的蛋白绝对量都太低而使两组之间很难出现差异。在血清水平,本研究结果提示R26-L-METRNL+/-小鼠的血液中存在大量人METRNL蛋白,而R26-L-WT小鼠血中检测不到该蛋白,说明R26-L-METRNL+/-小鼠成功过表达人METRNL,并可以成功分泌至血液中。同时,该实验提示,本研究所使用的人METRNL ELISA试剂盒特异性比较好,可以清晰区别人和鼠来源的METRNL蛋白。
在小鼠培育过程当中,尚未发现R26-L-METRNL+/-小鼠和同窝对照WT小鼠在体重、形态等方面有何差异。根据图2中R26-L-METRNL+/-小鼠的培育方式,采用R26-L-METRNL+/-小鼠与C57BL/6J 小鼠杂交进行扩大繁殖和保种,基于孟德尔遗传定律,后代鼠中R26-L-METRNL+/-小鼠理论得率为50%,但实际中,我们发现该小鼠的得率仅为15%左右,远低于理论值。这一现象非常有趣,因为此前本实验室构建过多种基因工程动物模型,均没有发现类似偏离孟德尔遗传定律的现象,而这一现象是否与METRNL蛋白的全身性过表达有关,值得我们进一步研究。
Construction and validation of a mouse model with systemic overexpression of human METRNL gene
-
摘要:
目的 构建全身过表达人METRNL基因的小鼠模型(R26-L-METRNL+/-小鼠)。 方法 基于Cre-loxP系统利用Dppa3-Cre小鼠和实验室前期构建的人METRNL基因条件性过表达(R26-LSL-METRNL+/-)小鼠进行交配繁殖,得到目标R26-L-METRNL+/-小鼠。将该目标小鼠进行基因型鉴定,收集其血液及心、肝、脾、肺、肾、脑、白色脂肪和肌肉组织,利用实时荧光定量PCR技术、蛋白免疫印迹实验和血清酶联免疫吸附实验,考察人METRNL基因在小鼠的表达情况。 结果 R26-L-METRNL+/- 小鼠的人METRNL在组织mRNA水平、组织蛋白水平和血液蛋白浓度方面都有显著表达,远高于野生对照组小鼠。 结论 R26-L-METRNL+/-小鼠模型构建成功。 Abstract:Objective To generate mice with whole-body overexpression of human METRNL gene. Methods Based on Cre-loxP system, Dppa3-Cre mice were mated with Rosa26-LSL-METRNL knock-in mice(R26-LSL-METRNL+/-)to generate R26-L-METRNL+/- mice. The genotypes of the offsprings were identified, and tissues of the blood, heart, liver, spleen, lung, kidney, brain, white adipose and muscle were collected. The expression of human METRNL gene in mice was investigated by quantitative real-time PCR, western blot and enzyme linked immunosorbent assay. Results Compared with wild type control mice, human METRNL in R26-L-METRNL+/- mice significantly expressed at both mRNA and protein levels in tissues, with abundant METRNL protein in blood. Conclusion The mouse model overexpressing human METRNL gene(R26-L-METRNL+/- mouse)was successfully constructed. -
Key words:
- METRNL /
- systemic overexpression /
- mouse
-
肌间沟臂丛阻滞(interscalene brachial plexus block, ISB)是肩关节镜手术的常用麻醉方式[1],但膈神经麻痹(hemidiaphragmatic paresis,HDP)的发生率高,对术前合并呼吸系统疾病的患者不利[2]。此外,肌间沟臂丛阻滞还会导致术后长时间的上肢感觉及运动障碍,降低患者满意度及舒适度[3]。Kim等[4]与Kang等[5]于近期报道臂丛上干阻滞(superior trunk block,ST)应用于肩关节镜手术可以有效减少HDP的发生,同时对肌力的影响更小。周阳洋等[6]报道低浓度低剂量(0.375% 10 ml)罗哌卡因行臂丛上干阻滞,完全的HDP发生率为0,还能提供良好的术后镇痛,保留患肢部分肌力,提高患者舒适度,但部分HDP发生率较高(87.2%)。为进一步探究降低部分HDP发生率的可能性,本研究采用更低浓度(0.25%)的罗哌卡因比较肌间沟与臂丛上干阻滞用于肩关节镜手术的临床效果。
1. 资料与方法
1.1 一般资料
本研究获得海军军医大学第二附属医院伦理委员会批准(CZEC2020-10),所有患者及家属均签署知情同意书。选择2020年8月至12月于本院择期行肩关节镜下肩袖修补术的患者46例,男22例,女24例,年龄26~70岁,BMI (24.5±2.5)kg/m2,ASA I~Ⅱ级。排除标准:①神经阻滞禁忌证;②长期服用镇痛药物;③不能理解疼痛评分;④不能配合完成握力检查及膈肌移动度检查。采用随机数字法(n=46)分成2组:超声引导下肌间沟臂丛神经阻滞组(ISB组)和臂丛上干阻滞组(ST组)。
1.2 方法
1.2.1 麻醉监测
患者入室后监测心电图、脉氧饱和度,桡动脉穿刺监测有创动脉压。
1.2.2 阻滞药物的制备
ISB 组与ST组所用的药液均配制成浓度为 0.25% 10 ml罗哌卡因。取5 ml 0.75%罗哌卡因,加入0.9%氯化钠注射液10 ml,配制成浓度为0.25%的15 ml溶液,取10 ml 备用。
1.2.3 盐酸右美托咪定配制
取用 2 ml 盐酸右美托咪定注射液(规格 2 ml:200 µg)加入 48 ml 0.9% 氯化钠注射液,配制成50 ml 浓度为 4 µg/ml 的 总溶液。
1.2.4 神经阻滞
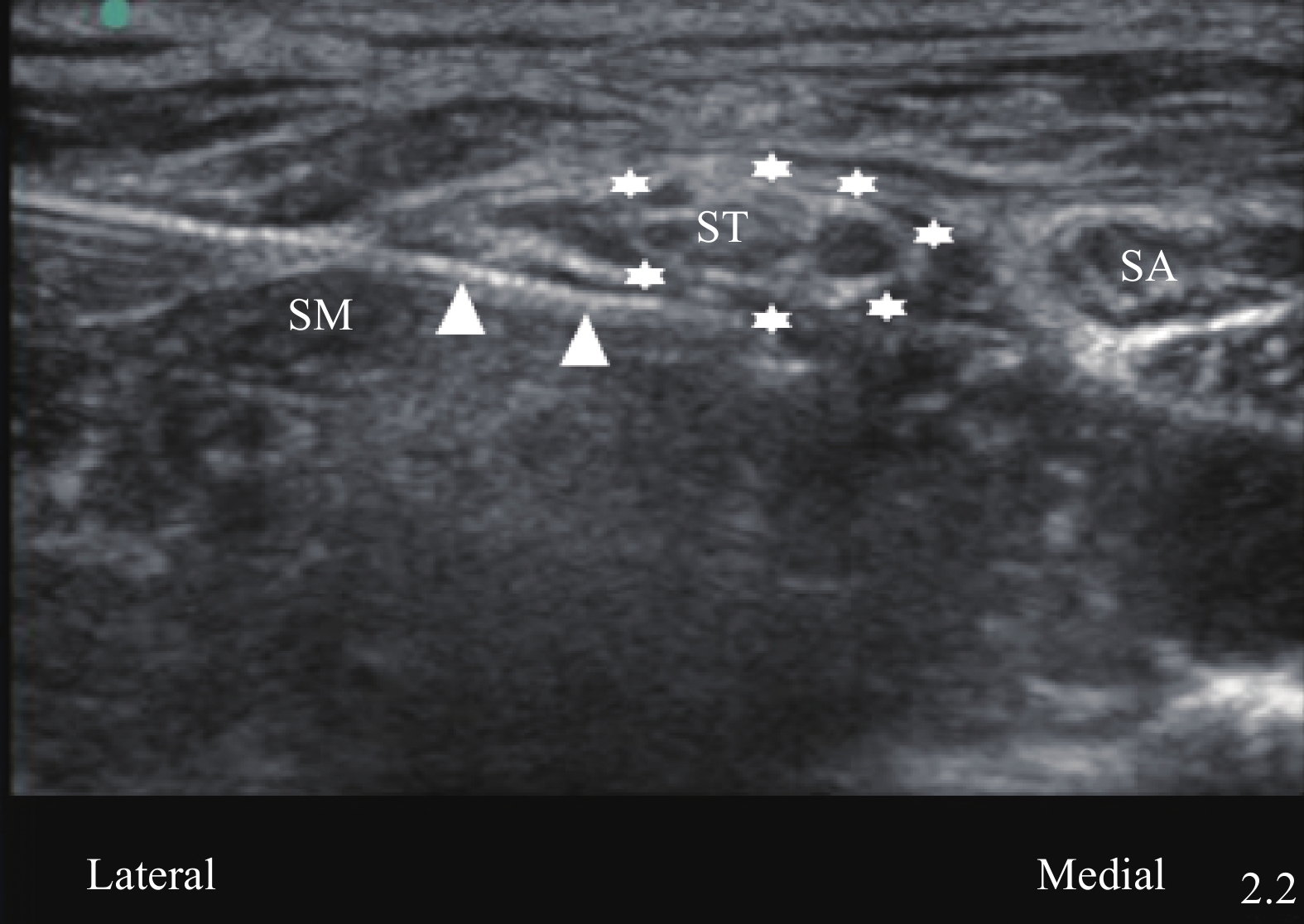
患者取平卧位,测量平静状态膈肌移动度,握力计测患侧手的握力。嘱患者头向健侧转 30°,使用高频线性探头进行定位扫查,对于ISB组,根据横突结节形状定位 C5、C6、C7 神经,找到“红绿灯征象”[7]后,平面内进针由外侧向内侧,穿过中斜角肌,采用一点法,针尖到达C5、C6外侧时回抽无血并注药,单次注射10 ml。对于ST组,在准确识别神经根的基础上探头缓慢向尾侧滑行,直至看到C5、C6汇合成臂丛上干,肩胛上神经即将分出,将该部位作为目标靶点。同样采用平面内进针,由外向内,超声引导下将针尖移至上干深面,旋转针尖使其开口朝向上干,包绕式注射5 ml 0.25% 罗哌卡因。注射完成后,将针尖移至上干浅面,阻滞针尖旋转180°,使其开口斜面继续朝向上干,包绕式注射剩余局麻药,见图1。
1.2.5 监护麻醉(MAC)
针刺拟手术区域,确认阻滞效果后,嘱患者摆侧卧位,予鼻导管吸氧及右美托咪定负荷剂量0.5~0.8 μg/kg(20 min内泵完)镇静,余以0.2~0.5 µg/(kg·h)微泵维持,直至手术结束前15 min停止泵注。
1.3 观察指标
1.3.1 膈肌移动度
测量患者阻滞前以及阻滞后30 min、3 h膈肌移动度。采用低频探头(X-Porte,Sonosite),通过肝窗或脾窗测量右侧或左侧膈肌移动度。测量平静呼吸及最大深吸气时的膈肌移动幅度,测量3遍,取平均值。膈肌麻痹(HDP)的程度是通过测量膈肌移动度的减少(以百分比差值计算)来定义。完全麻痹定义平静呼吸状态,移动度减少75%~100%,部分膈肌麻痹是指平均呼吸状态移动度减少25%~75%和轻度膈肌麻痹是指下降幅度小于25%[5]。
1.3.2 握力检查
患侧手全力抓持握力器,测量3次取均值。分别为阻滞前以及阻滞后30 min、3 h的平均握力。
1.3.3 术后疼痛
采用疼痛数字评分法(NRS)评估患者疼痛程度,记录神经阻滞后0~6 h,6~12 h及12~24 h时间段内患者静息状态下NRS最高评分以及阻滞时长(从阻滞开始起,直至出现痛觉恢复的时间)。
1.4 并发症
记录阻滞不全、霍纳(HONOR)综合征、声嘶、术后恶心呕吐的发生情况。
2. 结果
2.1 一般情况
本试验共纳入51例患者,共剔除5例。其中4例是因为ISB组阻滞效果欠佳,重新追加注射麻药,ST组1例是因对患者实施双侧臂丛上干阻滞。两组患者一般情况无统计学差异(P>0.05),见表1。
表 1 两组患者一般资料比较组别 例数
(例)年龄
(岁,
$\bar x $±s)性别
(例,
男/女)BMI
(kg/m2 ,
$\bar x $±s)阻滞侧
(例,
右/左)手术时间
(t/min,
$\bar x $±s)ISB组 23 58.3±10.3 11/12 24.6±2.4 13/10 81.9±8.6 ST组 23 61.1±6.6 9/14 23.8±2.5 11/12 83.7±12.5 2.2 膈肌移动度
ISB组患者平静呼吸状态下膈肌移动度为(2.02±0.42)cm,阻滞后30 min下降为(1.50±0.29)cm,阻滞后3 h膈肌移动度为(0.98±0.20)cm。最大深呼吸时膈肌移动度则分别为(5.30±0.70)cm、(3.53±1.04)cm和(1.86±0.58)cm。
ST组平静呼吸状态膈肌移动度为(1.91±0.21)cm,阻滞后30 min为(1.63±0.22)cm,阻滞后3 h膈肌移动度为(1.43±0.18)cm。最大深呼吸时膈肌移动度则分别为(5.17±0.48) cm、(3.51±0.95)cm和(2.29±0.55)cm。阻滞后30 min,ISB组与ST组膈肌移动度下降幅度差异无统计学意义(P>0.05),阻滞后3 h,两组之间膈肌移动度下降幅度差异显著(P<0.05)。阻滞后膈肌移动度,见表2。
表 2 两组患者阻滞侧膈肌移动度(cm,$\bar x $ ±s)时间 组别 平静呼吸 最大深呼吸 阻滞前 ISB组 2.02±0.42 5.30±0.70 ST组 1.91±0.21 5.17±0.48 阻滞后30 min ISB组 1.50±0.29 3.53±1.04 ST组 1.63±0.22 3.51±0.95 阻滞后3 h ISB组 0.98±0.20 1.86±0.58 ST组 1.43±0.18* 2.29±0.55* *P < 0.05,与ISB组比较。 根据膈肌麻痹定义,两组患者轻度麻痹、部分麻痹、完全麻痹的例数,见表3。
表 3 两组膈肌移动度下降例数及百分比[例(%)]时间 组别 平静呼吸 轻度麻痹 部分麻痹 完全麻痹 阻滞后30 min ISB组 9(39.1) 12(52.2) 2(8.7) ST组 17(73.9) 6(26.1) 0(0.0) 阻滞后3 h ISB组 4(17.4) 15(65.2) 4(17.4) ST组 14(60.9) 9(39.1)* 0(0.0)* *P<0.05,与ISB组比较。 2.3 握力检查
神经阻滞前,ISB组与ST组患者握力无明显差异(P=0.721),阻滞后30 min,ISB组与ST组握力下降幅度差异显著(P<0.001),阻滞后3 h,两组差异同样显著(P<0.001),ST组对握力的保留明显优于ISB组,见表4。
表 4 两组患者握力检查对比及下降幅度(kg,$\bar x $ ±s)时间 组别 握力 P 下降幅度(%) 阻滞前 ISB组 30.94±7.64 0.721 — ST组 30.23±5.58 — 阻滞后30 min ISB组 15.20±6.15 <0.001 52.17 ST组 24.01±4.91 20.59 阻滞后3 h ISB组 6.14±2.27 <0.001 80.11 ST组 14.35±3.33 52.38 注:“—”表示未获得数据。 2.4 术后疼痛评分及阻滞时长
2.4.1 两组患者各时间段的NRS最高评分
两组患者在阻滞后3~6 h,6~12 h及12~24 h 3个时间段内,NRS最高评分均具有显著差异(P<0.05),见表5。
表 5 两组患者各时间段的NRS最高评分(分,$\bar x $ ±s)组别 阻滞后时间段 PACU~3 h 3~6 h 6~12 h 12~24 h ISB组 0 0.57±1.16 2.74±1.25 3.39±1.27 ST组 0 0 1.74±0.86 1.83±1.07 P值 — 0.024 0.003 <0.001 注:“—”表示未获得数据。PACU表示麻醉后监护室。 2.4.2 阻滞时长
阻滞时长是指从神经阻滞完成直至患者痛觉恢复的时间,ISB组与ST组的平均时长分别是(8.3±1.97)h和(10.9±1.26)h,存在显著差异(P<0.01)。ISB组最长阻滞时长为11.6 h,最短为4.2 h,5名患者在6 h内恢复痛觉。ST组最长阻滞时间为13.6 h,最短为8.5 h 。
2.5 不良反应及并发症
所有入组患者均无霍纳(HONOR)综合征、声嘶、局麻药过敏及中毒的情况。
3. 讨论
肩关节镜手术虽属微创手术,但术后疼痛剧烈[8]。良好的术后镇痛可以加速患者康复,从而推进ERAS进程。近些年,围绕肩关节镜手术的神经阻滞报道很多,全世界学者都努力寻找麻醉的平衡点,镇痛完全,又能有效降低膈肌麻痹的发生率[9]。
肌间沟臂丛阻滞是肩关节围术期镇痛最常用的麻醉方式。但因解剖的关系在C5、C6和(或)C7处注射局麻药常会扩散至位于前斜角肌表面的膈神经,不可避免地导致膈肌麻痹。尽管降低局麻药浓度和(或)剂量可以减少HDP的发生,但迄今为止报道用最低容量5 ml 0.75%罗哌卡因行肌间沟臂丛阻滞,HDP的发生率仍达到33%[10]。Laurent等[11]提出臂丛上干阻滞的概念,Kim也报道了采用15 ml 0.375%布比卡因行上干阻滞+监护麻醉,HDP的发生率仅为4.8%[4]。我们课题组先前报道10 ml 0.375% 罗哌卡因环形包绕上干注射,完全HDP发生率为0.0%,但部分HDP发生率仍高达87.2%。为进一步降低HDP,减少对膈肌影响,因此,本研究选择10 ml 0.25% 罗哌卡因,进一步探讨低浓度低剂量局麻药在肩关节镜围术期的临床有效性。
结果显示,采用10 ml 0.25% 罗哌卡因,阻滞后30 min,ISB组与ST组对膈肌影响无明显差异(平静时P值=0.100;最大吸气时P值=0.955),考虑可能与低浓度罗哌卡因对运动神经阻滞起效慢相关,所以较短时间内两组差异性不明显。在阻滞后3 h,两组膈肌移动度下降具有显著差异(P<0.05)。此外,本研究ISB组采用的注药方式为临床上常用的一点法,由外向内进针,穿过中斜角肌,到达C5、C6外侧时注药,10 ml 0.25% 罗哌卡因可能无法完全包绕C5、C6神经根,导致阻滞不全或镇痛时间减少。肌间沟注药部位,膈神经常可于前斜角肌表面扫查到,采用类似于臂丛上干包绕式注药方式,局麻药注射至C5内侧时,药液常直接扩散至膈神经,导致其被阻滞。尽管本研究采用迄今为止满足外科手术麻醉最低药量,但ISB组平静呼吸时完全HDP的发生率仍有17.4%,而ST组则为0.0%,主要考虑臂丛上干阻滞距离膈神经更远,膈肌麻痹发生率更低。
术后疼痛方面,ST组明显优于ISB组。Kang[5]的研究认为,臂丛上干阻滞提供与肌间沟臂丛阻滞相似的镇痛效果。但本研究发现,无论是各时间段静息痛NRS最高评分,还是阻滞时长方面,ST组均明显优于ISB组,具有显著差异,这可能归因于解剖因素与给药方式。这类手术阻滞的目的是完全阻滞C5、C6神经根(无须阻滞C5分出的肩胛背神经)。在肌间沟水平,C5、C6常位于前、中斜角肌之间,神经周围的筋膜很薄,使得C5、C6边界难以辨别,会增加神经内注射风险,而且会有部分药液扩散至C7甚至C8,导致目标神经阻滞药量减少。本研究剔除的4例阻滞不全患者,可能与上述因素有关。
在握力方面,ST组明显优于ISB组,这与先前的两项RCT结果相符[4-5]。罗哌卡因本身具有运动感觉分离的效应,浓度高低决定了运动阻滞的程度,低浓度的使用使得运动功能的保留更为显著[3]。我们课题组也尝试采用更低浓度罗哌卡因(0.15%~0.2%)或者剂量(5~10 ml)行神经阻滞,握力的保留虽然更好,但有一定比例患者阻滞不全或者达到外科麻醉需求时间过长。
综上所述,10 ml 0.25%罗哌卡因臂丛上干阻滞较肌间沟臂丛阻滞具有更长的阻滞时间,更低的HDP发生率,更优的术后镇痛效果,更好的握力保留。
-
表 1 PCR扩增实验中的引物序列
基因名称 上游引物(5’→3’) 下游引物(5’→3’) R26-WT TCAGATTCTTTTATAGGGGACACA TAAAGGCCACTCAATGCTCACTAA R26-L-METRNL AAAGTCCCGGAAAGGAGCTG GAGGCTCCATCCAGCAAGTT R26-Stop GGGCAACGTGCTGGTTATTG ACTTGCCCCTTGCTCCATAC 内参基因 TGGGTTGGGTGTCTGTTTCATTGT GATCCACCTGTCTCTGCCTTCC Dppa-Cre TGGGTTGGGTGTCTGTTTCATTGT GACCTTGCATTCCTTTGGCGAGAG 表 2 实时荧光定量PCR实验中的引物序列
基因名称 上游引物(5′→3′) 下游引物(5′→3′) 人 METRNL ACCAGCGACTTCGTAATTCAC CAGCTCCACGTCATGGGTG 小鼠 Gapdh GTATGACTCCACTCACGGCAAA GGTCTCGCTCCTGGAAGATG -
[1] LI Z Y, ZHENG S L, WANG P, et al. Subfatin is a novel adipokine and unlike Meteorin in adipose and brain expression[J]. CNS Neurosci Ther, 2014, 20(4):344-354. doi: 10.1111/cns.12219 [2] LI Z Y, SONG J, ZHENG S L, et al. Adipocyte metrnl antagonizes insulin resistance through PPARγ signaling[J]. Diabetes, 2015, 64(12):4011-4022. doi: 10.2337/db15-0274 [3] LI Z Y, FAN M B, ZHANG S L, et al. Intestinal Metrnl released into the gut lumen acts as a local regulator for gut antimicrobial peptides[J]. Acta Pharmacol Sin, 2016, 37(11):1458-1466. doi: 10.1038/aps.2016.70 [4] ZHANG S L, LI Z Y, WANG D S, et al. Aggravated ulcerative colitis caused by intestinal Metrnl deficiency is associated with reduced autophagy in epithelial cells[J]. Acta Pharmacol Sin, 2020, 41(6):763-770. doi: 10.1038/s41401-019-0343-4 [5] XU T Y, QING S L, ZHAO J X, et al. Metrnl deficiency retards skin wound healing in mice by inhibiting AKT/eNOS signaling and angiogenesis[J]. Acta Pharmacol Sin, 2023, 44(9):1790-1800. doi: 10.1038/s41401-023-01090-x [6] HONG C, WANG Z, ZHENG S L, et al. Metrnl regulates cognitive dysfunction and hippocampal BDNF levels in D-galactose-induced aging mice[J]. Acta Pharmacol Sin, 2023, 44(4):741-751. doi: 10.1038/s41401-022-01009-y [7] ZHENG S L, LI Z Y, SONG J, et al. Endothelial METRNL determines circulating METRNL level and maintains endothelial function against atherosclerosis[J]. Acta Pharm Sin B, 2023, 13(4):1568-1587. doi: 10.1016/j.apsb.2022.12.008 [8] AMANO Y, NONAKA Y, TAKEDA R, et al. Effects of electrical stimulation-induced resistance exercise training on white and brown adipose tissues and plasma meteorin-like concentration in rats[J]. Physiol Rep, 2020, 8(16):e14540. [9] RAO R R, LONG J Z, WHITE J P, et al. Meteorin-like is a hormone that regulates immune-adipose interactions to increase beige fat thermogenesis[J]. Cell, 2014, 157(6):1279-1291. doi: 10.1016/j.cell.2014.03.065 [10] USHACH I, ARREVILLAGA-BONI G, HELLER G N, et al. Meteorin-like/meteorin-β is a novel immunoregulatory cytokine associated with inflammation[J]. J Immunol, 2018, 201(12):3669-3676. doi: 10.4049/jimmunol.1800435 [11] JUNG T W, LEE S H, KIM H C, et al. METRNL attenuates lipid-induced inflammation and insulin resistance via AMPK or PPARδ-dependent pathways in skeletal muscle of mice[J]. Exp Mol Med, 2018, 50(9):1-11. [12] REBOLL M R, KLEDE S, TAFT M H, et al. Meteorin-like promotes heart repair through endothelial KIT receptor tyrosine kinase[J]. Science, 2022, 376(6599):1343-1347. doi: 10.1126/science.abn3027 [13] LU Q B, DING Y, LIU Y, et al. Metrnl ameliorates diabetic cardiomyopathy via inactivation of cGAS/STING signaling dependent on LKB1/AMPK/ULK1-mediated autophagy[J]. J Adv Res, 2023, 51:161-179. doi: 10.1016/j.jare.2022.10.014 期刊类型引用(4)
1. 余万冰,张单丽,关素珍,王海燕. 基于高效液相色谱一测多评技术联合化学计量学的脂必泰胶囊质量评价. 中国药品标准. 2024(06): 545-554 .  百度学术
百度学术2. 严家文,朱琼. 来曲唑片仿制药与原研药溶出一致性评价研究. 广州化工. 2022(23): 126-129 .  百度学术
百度学术3. 胡天骄,刘雪赟. 阿戈美拉汀片溶出度测定的方法研究. 中南药学. 2020(02): 218-221 .  百度学术
百度学术4. 邢秀,李琼,张晶,孙国祥,张艳华. 多波长串联指纹图谱结合紫外全指纹溶出度测定评价复方两面针含片质量. 药物分析杂志. 2020(10): 1887-1896 .  百度学术
百度学术其他类型引用(1)
-





 下载:
下载:



 下载:
下载: