-
扶正化瘀胶囊(旧名扶正化瘀方)是针对肝纤维化“正虚血瘀”的基本病机研制而成的[1],该复方由丹参、桃仁、五味子、冬虫夏草、绞股蓝、松花粉六味药材组成[2-7],丹参在方中活血祛瘀作为君药,冬虫夏草补虚损、益精气,桃仁助丹参活血祛瘀,共为臣药,松花粉益气润燥,绞股蓝清热解毒,两者共为佐药;五味子味酸,为引经使药。从中医角度出发,丹参、冬虫夏草、桃仁、松花粉、绞股蓝、五味子这六味药材的药效物质基础主要包含脂溶性的丹参酮类和水溶性的丹酚酸类、多糖、甾醇、多种氨基酸、多种维生素、挥发油、木脂素等物质。以上六味药合用共奏活血化瘀、益精养肝之功效,适用于肝纤维化证属“瘀血阻络,肝肾不足”者[8]。其临床疗效显著,已受国家发明专利保护,获得国家中药Ⅲ类新药证书。而且2006年扶正化瘀片通过美国食品药品监督管理局审批,免于进行Ⅰ期临床,直接进入Ⅱ期临床试验,并在2013年圆满完成Ⅱ期临床实验,成为肝病领域中首个通过美国Ⅲ期临床试验的中成药[9],将来也有望成为第一个获准进入美国主流医药市场的复方中药。(标红的5处字体均用罗马字)
该复方在我国已使用多年,但由于其组分复杂,一直缺乏系统性研究,尽管目前关于该复方作用机制报道较多[10-15],然而对于整个复方的入血成分还未见报道。而且复方组成复杂,比分析单位药材的入血成分更困难,因此,明确扶正化瘀胶囊各部分的入血成分对于该复方治疗效果、作用机制的深入研究具有重要意义。
UHPLC和Q-TOF/MS的串联技术在中药复方等复杂体系研究中占有一定优势,该技术集色谱的高效分离能力和质谱的高灵敏、高分辨、强定性能力于一体,已经成为中药复方化学成分分析和鉴定的有效手段之一[16-18]。本实验采用UHPLC-QTOF/MS技术首次对扶正化瘀胶囊中的入血成分进行快速分析,并对其成分进行药材归属鉴定,进一步阐明了扶正化瘀胶囊的药效物质基础,具有重要的临床意义。
-
Agilent 1290 Infinity 液相系统,包括G4220A四元泵、G4226自动进样器G1316C柱温箱(安捷伦科技有限公司,美国);Agilent 6538 UHD and Accurate-Mass Q-TOF/MS质谱仪,配有标准电喷雾离子源(ESI)及MassHunter Qualitative Analysis Software 分析工作站(安捷伦科技有限公司,江苏);JY10001十万分之一电子天平(精密科学仪器有限公司,上海);Heal Force SMART-N 超纯水机(力康生物医疗科技控股有限公司,香港);Micro 17高速离心机(Thermo Fisher Scientific,美国);甲醇、乙腈均为色谱纯试剂(Merck,德国),甲酸为色谱级试剂(ROE scientific INC,美国),水为实验室制备的超纯水,其他试剂均为分析级。
-
丹参素、丹酚酸B、二氢丹参酮I、丹酚酸A、五味子乙素、苦杏仁苷、腺苷、五味子醇甲、绞股蓝皂苷XLIX、山奈酚对照品(一飞生物科技有限公司,纯度≥98%),批号分别为:76822-21-4、121521-90-2、87205-9-0、96574-01-5、61281-37-6。扶正化瘀胶囊(黄海制药有限责任公司,上海)购于益丰大药房,批号分别为:161220、170640、171116。
-
取丹参素、丹酚酸B、二氢丹参酮I、丹酚酸A、五味子乙素对照品适量,精密称定后,用甲醇溶解并定容成10 mg/ml的对照品储备液。吸取各对照品溶液适量,用甲醇稀释成各对照品浓度约2 mg/ml的对照品混合溶液。
-
称取扶正化瘀胶囊适量,配制成浓度为0.3 g/ml的混悬水溶液,供大鼠灌胃使用。取雄性SD大鼠6只,随机分为两组(空白组和给药组),给药前12 h禁食、不禁水,按照给药体积4 ml/kg(0.3 g/ml,临床4倍剂量)灌胃给药样品,空白组灌胃蒸馏水。给药23 min后采用眼眶取血约1.5 ml置离心管中,静置1 h后,离心(3 500 r/min,10 min)后取上清液约0.5 ml,−80 ℃冷冻保存。
-
精确吸取50 μl血清,溶于150 μl 含有内标的100%甲醇中,涡旋30 s,静置5 min,于4 ℃、1 000 r/min离心10 min,取上清液,即得血清样品。
-
色谱柱:ACQUITY UPLCHSS T3(2.1 mm×100 mm,1.8 μm,Waters Corporation,Ireland)。流动相由0.1%甲酸水溶液(A)-0.1%甲酸乙腈溶液(B)组成。梯度洗脱条件:0~3 min,2%B;3~18 min,2%~50%B;18~22 min,50%~95% B;22~25 min,95%B。平衡时间为10 min,流速为0.40 ml/min,分析所用时间为25 min。进样体积设置为3 μl,柱温箱温度为40 ℃,自动进样器的温度为4 ℃。
-
电喷雾离子源采用正、负离子模式。正离子模式条件:毛细管电压4 V;干燥气体流速11 L/min;干燥气体温度350 ℃;雾化器压力45 psig;碎片电压120 V;skimmer电压60 V。质谱采集范围从100~1 100 m/z ,参比离子为121.051和922.010 m/z。负离子模式下,除了毛细管电压为 3.5 kV,其余条件与正离子模式相同。负离子模式下的参比离子分别为 119.036 3 和 966.000 7 m/z。
-
根据国内外已有的专业数据库TCM@taiwan、TCMID(traditional Chinese medicine integrative database)和上海中科院化学专业数据库及相关研究文献,共收集了扶正化瘀胶囊六味药材中801个化学成分。利用Agilent公司研发的“Formula-Database-Generator”软件,通过各化学成分包含碳、氢、氧的个数,计算化合物精确的相对分子质量,建立化学成分的分子式和相对分子质量的数据库。
-
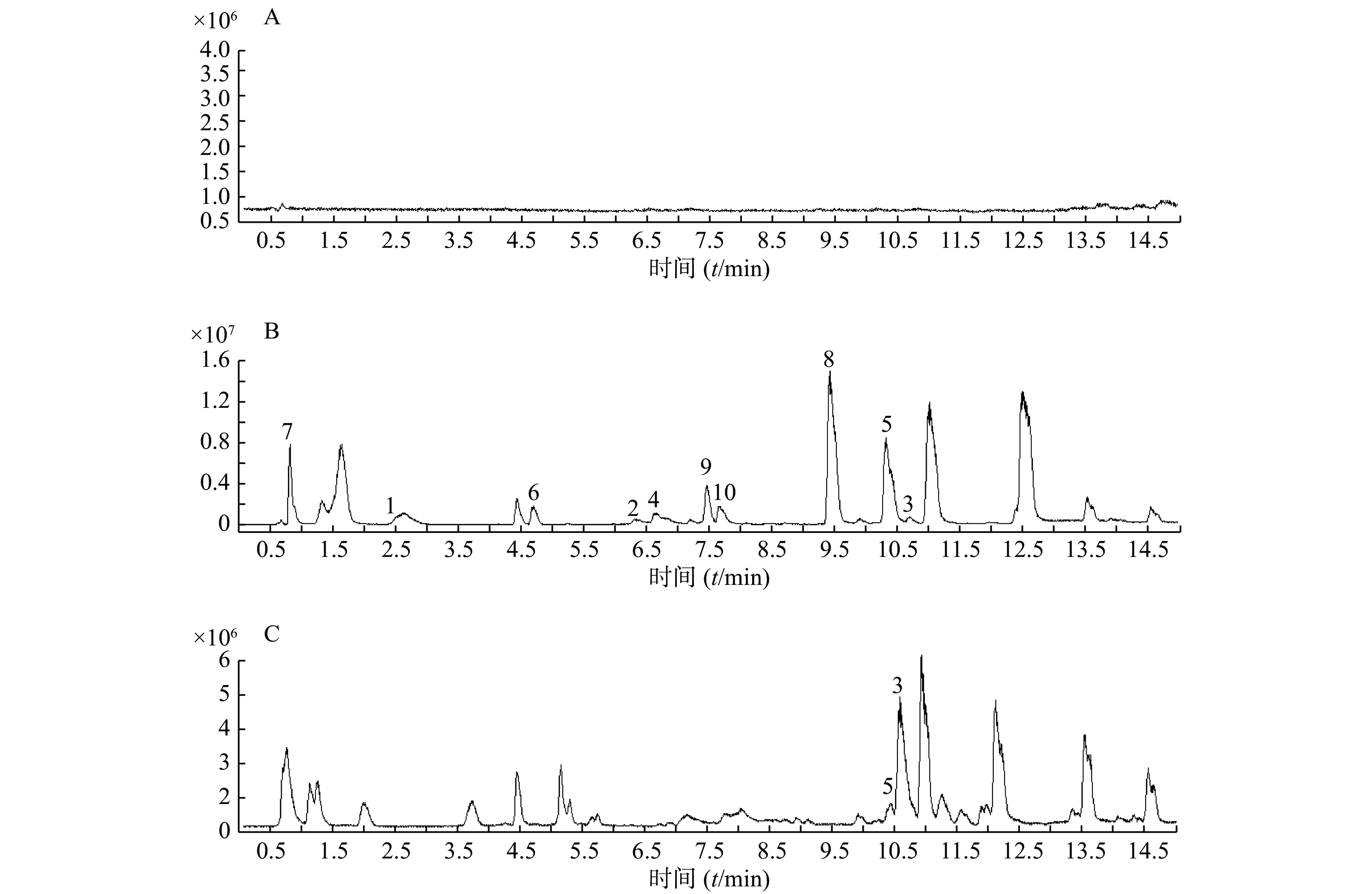
精密吸取扶正化瘀胶囊血清样品溶液和对照品混合溶液200 μl于进样小瓶,按照上述质谱和色谱测试条件进行样品分析。同时检测空白血清、混合对照品溶液和含药血清在正离子检测模式下的总离子流图,如图1所示。
-
以正离子模式下3号峰二氢丹参酮I为例,说明扶正化瘀胶囊中的色谱峰鉴别过程。TIC图中的保留时间为10.453 min(图1B),色谱峰显示的准分子离子峰为279.101,利用Qualiative Analysis软件分析工具(calculator)精确计算质量数可能的元素组成(<5 ppm),结合数据库内已知的化合物质核比,可以初步确定分子式为C18H14O3。通过计算准分子离子的核素分布情况,得出同位素分布的理论值与实际值吻合良好,确定此峰为二氢丹参酮I(图2)。
-
根据飞行时间质谱测得的精确相对分子质量,比对所建的扶正化瘀胶囊化学成分数据库,应用 Qualiative Analysis质谱分析软件计算分子组成,将理论值与实测值进行比对,结合上述对照品鉴别结果及相关文献报道[19-20],对扶正化瘀胶囊血清供试品在正、负离子模式下所得的色谱图中色谱峰进一步分析,其中,血清供试品在正离子模式下初步鉴别出43个化学成分,结果见表1。在负离子模式下初步鉴别出10个化学成分,结果见表2。其中,正、负离子模式下均有响应的有4个(表中标①)。对于化学成分的药材归属,见表1。
表 1 入血化学成分的正离子模式鉴别结果
编号 保留时间 (t/min) 化合物名称 分子式 M+X 理论分子量(m/z) 实际分子量(m/z) 误差(ppm) 归属药材 1 10.157 dihydrokaranone C15 H22 O (M+H)+ 219.174 1 219.174 3 2.01 Salvia miltiorrhiza Bge. 2 10.453 dihydrotanshinone I C18 H14 O3 (M+H)+ 279.101 0 279.101 4 0.29 Salvia miltiorrhiza Bge. 3 12.031 salvianonol C18 H20 O4 (M+H)+ 301.141 7 301.141 3 5.72 Salvia miltiorrhiza Bge. 4 10.009 isocryptotanshinone II C19 H20 O3 (M+H)+ 297.148 1 297.148 1 1.49 Salvia miltiorrhiza Bge. 5 11.078 sugiol C20 H28 O2 (M+H)+ 301.216 0 301.216 0 0.78 Salvia miltiorrhiza Bge. 6 11.636 salviol C20 H30 O2 (M+H)+ 303.231 9 303.232 2 −0.13 Salvia miltiorrhiza Bge. 7 12.762 dihydrovalepotriate C22 H32 O8 (M+H)+ 425.216 3 425.215 1 2.87 Salvia miltiorrhiza Bge. 8 7.232 4-methyl salicylaldehyde C8 H8 O2 (M+H)+ 137.059 9 137.059 8 0.05 Salvia miltiorrhiza Bge. 9 1.168 nicotinamide C6 H6 N2 O (M+H)+ 123.055 1 123.054 1 2.14 Cordyceps sinensis 10 0.642 histidine① C6 H9 N3 O2 (M+H)+ 156.075 8 156.076 8 1.52 Cordyceps sinensis 11 1.061 valine C5 H11 N O2 (M+H)+ 118.086 2 118.086 2 0.61 Cordyceps sinensis 12 1.357 adenosine C10 H13 N5 O4 (M+H)+ 268.104 2 268.104 4 −0.54 Cordyceps sinensis 13 0.765 arginine C6 H14 N4 O2 (M+H)+ 175.118 7 175.118 8 2.03 Cordyceps sinensis 14 0.634 lysine C6 H14 N2 O2 (M+H)+ 147.112 9 147.112 8 −0.45 Cordyceps sinensis 15 9.590 cis-9-octadecenoic acid C18 H34 O2 (M+NH4)+ 300.289 2 300.289 4 1.78 Cordyceps sinensis 16 9.360 octadecanoic acid C18 H36 O2 (M+NH4)+ 302.305 4 302.305 1 −0.76 Cordyceps sinensis 17 1.751 leucine C6 H13 N O2 (M+H)+ 132.102 1 132.101 3 −1.57 Cordyceps sinensis 18 1.361 pedatisectine B C5 H5 N5 (M+H)+ 136.062 2 136.061 8 1.02 Cordyceps sinensis 19 8.259 linoleic acid C18 H32 O2 (M+NH4)+ 298.274 0 298.274 1 0.9 Cordyceps sinensis 20 1.102 methionine C5 H11 N O2 S (M+H)+ 150.058 5 150.058 4 −0.61 Cordyceps sinensis 21 10.979 linoleic acid C18 H32 O2 (M+NH4)+ 298.273 9 298.274 1 2.57 Semen Persicae 22 4.726 glucose C6 H12 O6 (M+H)+ 181.070 5 181.070 8 0.95 Semen Persicae 23 9.648 GA17① C20 H26 O7 (M+Na)+ 401.158 3 401.159 2 −2.24 Semen Persicae 24 5.194 prunasin① C14 H17 N O6 (M+Na)+ 318.095 6 318.096 0 −1.94 Semen Persicae 25 9.623 gomisin R C22 H24 O7 (M+H)+ 401.158 5 401.159 1 2.71 Schisandra chinensis Fructus 26 11.168 2-(2-phenyl cyclohexyloxy) ethanol C14 H20 O2 (M+Na)+ 243.135 3 243.135 8 1.78 Schisandra chinensis Fructus 27 9.911 deangeloylgomisin F C23 H28 O8 (M+Na)+ 455.168 9 455.168 2 −0.19 Schisandra chinensis Fructus 28 12.524 schisandrin B C23 H28 O6 (M+Na)+ 423.177 5 423.177 6 1.88 Schisandra chinensis Fructus 29 8.333 gomisin Q C24 H32 O8 (M+Na)+ 471.198 1 471.198 2 1.56 Schisandra chinensis Fructus 30 9.130 (±)-gomisin m1 C22 H26 O6 (M+Na)+ 409.161 8 409.161 8 0.64 Schisandra chinensis Fructus 31 11.973 1,1alpha,4,5,6,7,7alpha,7beta-octahydro-1,1,7,7alpha-tetramethyl-2h-cyclopropa (alpha)-naphthalen-2-one C14 H22 O (M+H)+ 207.174 9 207.174 2 −2.61 Schisandra chinensis Fructus 32 6.870 1-phenyl-1,3-butanedion C10 H10 O2 (M+H)+ 163.075 5 163.075 8 −1.40 Schisandra chinensis Fructus 33 10.839 geranyl acetate C12 H20 O2 (M+H)+ 197.153 8 197.153 5 1.07 Schisandra chinensis Fructus 34 11.110 tigloylgomisin P C28 H34 O9 (M+NH4)+ 532.254 3 532.253 8 0.22 Schisandra chinensis Fructus 35 7.322 citronellyl acetate C12 H22 O2 (M+NH4)+ 216.195 3 216.195 4 2.48 Schisandra chinensis Fructus 36 0.814 gama-octalactone C8 H14 O2 (M+NH4)+ 160.133 0 160.132 9 0.27 Schisandra chinensis Fructus 37 9.607 gomisin D C28 H34 O10 (M+Na)+ 553.204 2 553.203 9 0.61 Schisandra chinensis Fructus 38 10.248 1,1α,2,4,6,7,7α,7β-octahydro-1,1,7,7α-tetra-methyl-5h-cyclopropa (α)-naphthalen-5-one C15 H22 O (M+H)+ 219.173 7 219.174 3 2.92 Schisandra chinensis Fructus 39 9.935 phenyl-2-propanone C9 H10 O (M+H)+ 135.080 2 135.080 2 1.81 Schisandra chinensis Fructus 40 11.834 prehispanolone① C20 H30 O3 (M+H)+ 319.226 3 319.225 7 2.56 Schisandra chinensis Fructus 41 9.919 psilostachyin C15 H20 O5 (M+H)+ 281.137 9 281.138 4 1.67 Schisandra chinensis Fructus 42 11.324 santlic acid C15 H22 O2 (M+H)+ 235.168 3 235.170 5 0.58 Schisandra chinensis Fructus 43 7.355 gomisin A C23 H28 O7 (M+H)+ 417.190 6 417.190 3 0.23 Schisandra chinensis Fructus 注:“①”表示正、负离子模式下都已鉴别出。 表 2 入血化学成分的负离子模式鉴别结果
编号 保留时间 (t/min) 化合物名称 分子式 M-X 理论分子量(m/z) 实际分子量(m/z) 误差(ppm) 归属药材 1 6.795 tanshindiol C C18 H16 O5 (M+COOH)− 357.098 9 357.099 7 −1.34 Salvia miltiorrhiza Bge. 2 13.681 paramiltioic acid C19 H24 O5 (M+COOH)− 377.161 6 377.161 9 −1.84 Salvia miltiorrhiza Bge. 3 0.812 histidine① C6 H9 N3 O2 (M-H)− 154.062 6 154.061 2 −2.28 Cordyceps sinensis 4 0.764 glutamic acid C5 H9 N O4 (M-H)− 146.045 7 146.044 9 1.02 Gynostemma pentaphyllum (Thunb.) Makino 5 13.632 GA17① C20 H26 O7 (M-H)− 377.161 6 377.161 9 −2.18 Semen Persicae 6 3.714 GA19 C20 H26 O6 (M+COOH)− 407.171 9 407.171 7 0.02 Semen Persicae 7 13.632 GA119 C19 H24 O5 (M+COOH)− 377.161 6 377.161 9 −2.48 Semen Persicae 8 5.209 prunasin① C14 H17 N O6 (M+COOH)− 340.102 9 340.102 3 0.40 Semen Persicae 9 11.060 prehispanolone① C20 H30 O3 (M-H)− 317.211 5 317.210 9 2.19 Schisandra chinensis Fructus 10 14.158 schisandrone C21 H24 O5 (M-H)− 355.156 4 355.156 6 −2.79 Schisandra chinensis Fructus 注:“①”表示正、负离子模式下都已鉴别出。 -
本研究首次运用UHPLC-Q-TOF/MS对扶正化瘀胶囊入血成分进行分析,该方法效率高、稳定性好、灵敏度高,能快速检测出含量较低的化学成分,优于其他方法。利用该技术快速初步鉴别出扶正化瘀胶囊血清供试品共49个化学成分,推测其可能为扶正化瘀胶囊发挥药效的物质基础。已鉴别出的化学成分主要集中在丹参、冬虫夏草,符合中药复方“君臣佐使”的配伍原则。为进一步探究其作用机制,拟进一步从 49 种入血成分筛选出抗肝纤维化的体内、外活性测试,期望筛选出具有抗肝纤维化的活性单体。该研究进一步将相应物质的色谱峰明确化,为扶正化瘀胶囊的深入研究奠定了良好基础。
Rapid identification of chemical constituents in serum and plasma of Fuzheng Huayu capsules by UHPLC-TOF/MS
-
摘要:
目的 本研究运用超高效液相色谱-高分辨飞行时间质谱(UHPLC-Q-TOF/MS)联用技术鉴别扶正化瘀胶囊入血成分。 方法 色谱分离采用ACQUITY UPLCHSS T3 (2.1 mm×100 mm,1.8 μm);流动相0.1%甲酸水溶液(A)−0.1%甲酸乙腈溶液(B),梯度洗脱条件:0~3 min,2%B;3~18 min,2%~50%B;18~22 min,50%~95%B;22~25 min,95%B。平衡时间为10 min,流速为0.4 ml/min,分析时间为25 min。质谱定性电喷雾离子源采用在正、负离子模式扫描,采集范围从100~1 100 m/z。 结果 在血清样品中一次性鉴别出49个成分,其中正、负离子模式下均有响应的有4个。 结论 本研究较全面地阐明了扶正化瘀胶囊的入血成分,丰富了扶正化瘀胶囊的科学内涵,为该复方的深入研究奠定了基础。 Abstract:Objective To identify the blood components of Fuzheng Huayu capsule by ultra performance liquid chromatography-high resolution time-of-flight mass spectrometry (UHPLC-Q-TOF/MS). Methods ACQUITY UPLCHSS T3 (2.1 mm × 100 mm, 1.8 μm) was used to chromatographic separation; mobile phase was 0.1% formic acid aqueous solution (A) −0.1% formic acid acetonitrile solution (B). The gradient elution conditions included: 0−3 min, 2% B; 3−18 min, 2%−50% B; 18−22 min, 50%−95% B; 22−25 min, 95% B. The equilibration time was 10 min, the flow rate was 0.40 ml/min, and the analysis time was 25 min. The mass spectrometry was characterized by electrospray ionization by a positive-negative ion mode scan with a range of 100-1 100 m/z. Results 49 components were identified in the serum samples at one time, of which 4 were positive and negative ion modes. Conclusion The blood components of Fuzheng Huayu capsule were clarified by this method, which enriched the scientific connotation of Fuzheng Huayu capsule, and laid the foundation for the in-depth study of the compound. -
肠道菌群是定植在人体内复杂而庞大的微生物群落,成人肠道中有多达上千种的细菌,基因数超过人类100多倍[1]。在已确定的细菌门类中,厚壁菌门和拟杆菌门占95%以上,很大程度上影响着整个菌群的功能[2]。在漫长的生物共演化过程中,这些肠道菌群与人体形成了相互依存的共生关系。肠道菌群及其代谢产物具有协助消化吸收食物、合成维生素和能量、保护肠道黏膜屏障等功能,在参与人体重要代谢、抵御外来致病菌侵袭以及调节免疫机制等方面发挥重要作用[3]。多项研究表明,大量慢性疾病的发生与体内肠道菌群结构的改变有关,包括炎性肠病、代谢性疾病、肥胖或营养不良、神经系统疾病和心血管疾病等[4-5]。
成骨细胞和破骨细胞参与骨形成和吸收的过程称为骨代谢,成人的骨代谢活动处于动态平衡状态,一旦因各种原因导致骨吸收与骨形成失衡,就会引起局部或整体骨代谢异常,引发骨质疏松症、关节病、类风湿等一系列骨代谢疾病[6]。其中,骨质疏松症是由多种原因引起,以骨量降低、骨组织微结构损坏为特征,导致骨脆性增加、骨折风险增高的常见全身性骨代谢疾病。近年来,肠道菌群调控骨代谢的研究受到广泛关注,已有较多研究发现肠道菌群与骨量减少及骨质疏松症的发病关系密切[4],肠道中的微生物可通过影响营养吸收、产生代谢产物、调控宿主内分泌及免疫系统等途径影响骨代谢。中药具有多成分、多靶点的作用机制,目前中药干预肠道菌群调控骨代谢研究亦有较多报道。本文将对肠道菌群影响骨代谢机制及中药经此途径调控骨代谢相关研究进展进行综述。
1. 肠道菌群与骨代谢关系研究
1.1 肠道菌群通过营养吸收影响骨代谢
肠道菌群可通过影响机体对营养物质的吸收来调控骨代谢。肠道菌群结构发生变化可改变肠道局部环境的pH值,影响大分子物质和矿物质的吸收。其中,乳酸杆菌和双歧杆菌浓度升高可促进钙、镁和磷等矿物质的吸收,从而增加骨矿物质密度[7]。此外,肠道菌群可通过胆汁酸代谢途径来调控骨代谢,其不仅参与原代胆汁酸的转化,而且可以使之脱羟基化产生次级胆汁酸参与代谢,从而促进维生素D的吸收,影响成骨细胞和破骨细胞的形成[8]。同时,肠道菌群可影响肠道胆汁酸库的组成,并调控结肠Foxp3调节性T细胞(Tregs)群体,进而调控肠道免疫反应影响骨代谢[9-10]。另外,有研究显示胆汁酸对于肠道中钙离子的吸收也有一定的影响[11]。可见,肠道菌群对宿主营养物质的吸收、合成具有重要作用,菌群中的有益菌可对骨骼健康产生积极影响。
1.2 肠道菌群代谢物短链脂肪酸调控骨代谢
短链脂肪酸(SCFAs) 是膳食纤维经肠道菌群发酵产生的代谢产物,主要包含乙酸、丙酸和丁酸。SCFAs的产生依赖于肠道菌群,其中梭状杆菌、双歧杆菌、乳酸菌等是产生SCFAs的主要菌群。反之,SCFAs可通过降低肠道pH值,抑制各种致病菌生长等作用,来维持肠道菌群的平衡,影响肠道菌群结构。两者或单独或协同在宿主的营养吸收、免疫、内分泌等多方面发挥重要作用[4]。
SCFAs可直接作用于骨细胞调控骨代谢。Lucas等[12] 研究发现,外源补充丙酸和丁酸可降低小鼠破骨细胞相关基因TRAF6和NFATc1表达,调节破骨细胞分化,抑制体外和体内的骨吸收而不影响骨形成,从而显著增强骨量。而Martinis等[13] 研究发现,SCFAs中的丁酸盐,可能通过诱导组蛋白乙酰化,调控miRNA表达,发挥调控骨结构、骨重吸收和成骨细胞分化间平衡的作用。总之,在肠菌代谢物直接作用于骨细胞的过程中,肠内SCFAs浓度的增加可有效抑制骨吸收,减缓骨流失。
1.3 肠道菌群调控氧化应激影响骨代谢
肠道菌群可通过调控机体氧化应激对骨代谢产生影响。益生菌能通过多种途径降低机体的氧化应激,如与金属离子Fe2+、Cu2+等发生螯合反应,产生谷胱甘肽、丁酸盐、叶酸等具有抗氧化活性的代谢产物,介导Nrf2-Keap1-ARE、NFκB、MAPK、PKC等抗氧化信号通路,调控机体抗氧化酶反应等[14]。若有害菌过度增殖,则会诱导血液中的内毒素引起明显的氧化应激反应。已有研究证实,过度的氧化应激在骨重塑过程中,会促进骨形成相关细胞如骨髓间充质干细胞、成骨细胞,并促进骨细胞的凋亡和破骨细胞的增殖及分化,导致骨形成速率相对骨吸收速率滞后,打破骨代谢的动态平衡[15]。
1.4 肠道菌群调控免疫影响骨代谢
1.4.1 肠道菌群影响炎症因子调控免疫
肠道菌群可通过影响炎症因子表达诱导机体免疫调控骨代谢。肠菌失调可直接刺激炎性细胞因子表达,导致破骨细胞过度活跃,加速骨流失,影响骨稳态。研究显示,与普通小鼠相比,无菌小鼠炎症因子、B细胞和T细胞的表达均减少,而骨小梁数目、骨密度则明显增加[16]。另有研究显示,特定种类的梭状芽孢杆菌比例增高,会促进肠道中CD4 T细胞向 Th17 细胞和 Treg 细胞的分化[17]。其中,Th17细胞数量增加可导致IL-17、TNF-α和IL-1水平上升,从而诱导 RANKL的表达,加速破骨细胞生成[18];Treg细胞则通过促炎细胞因子IL-4、IL-10、TGF-β等,间接促进破骨细胞活化加速骨吸收[19]。值得注意的是,肠菌代谢物丁酸盐可直接调节CD4 T、CD8 T和Tc17细胞的基因表达,诱导小鼠结肠Treg细胞分化,并通过为肠黏膜上皮细胞提供能量、改善肠道屏障等多角度影响宿主免疫系统[20];双歧杆菌、嗜热链球菌等多种益生菌,同样参与诱导Th17 细胞和 Treg 细胞的分化[21]。
1.4.2 肠道菌群影响肠黏膜屏障功能
肠道菌群还能通过维持肠道上皮黏膜屏障功能调控机体免疫影响骨代谢。肠黏膜屏障是由杯状细胞分泌的黏蛋白形成的黏液层,是肠道菌群的能量来源。健康的黏液层可减少肠内菌群与内层上皮细胞接触,具有抑制细菌黏附、限制免疫反应等作用[22]。研究显示,肠菌结构和代谢物的变化可直接造成黏蛋白减少,肠道通透性增加,导致肠道中有害菌及代谢物进入机体,引发免疫应答,最终刺激破骨细胞的激活,促进骨吸收[23]。另外,Wang等[24]研究发现,将老年性骨质疏松大鼠的粪菌移植到幼龄大鼠体内可诱发年轻大鼠骨质疏松。粪菌移植后,模型大鼠肠道菌群组成和结构发生改变,影响了黏蛋白表达,导致肠结构损伤、绒毛缩短、肠通透性增加,肠屏障功能严重受损;而骨钙素、CTX和P1NP显著升高,骨体积、骨体积密度、骨小梁数显著降低。通过KEGG预测发现,引起骨质流失的主要原因可能与模型大鼠RIG-I样受体信号通路显著增加有关。
可见,在肠道菌群调控免疫影响骨代谢的过程中,有害菌过度增殖或过量益生菌均可使肠菌结构发生改变,导致机体炎症因子表达上调,肠黏膜屏障功能受损,加速骨吸收。
1.5 肠道菌群通过调节内分泌影响骨代谢
1.5.1 肠道菌群与雌激素相互作用
肠道菌群可通过与雌激素代谢间的相互作用调控骨代谢。雌激素戒断会增加肠道通透性致使肠道菌群结构发生变化,降低菌群多样性;同时肠道菌群结构改变,菌群将减少β-葡萄糖醛酸酶的分泌,继而降低肠内雌激素吸收[25]。雌激素可通过与雌激素受体结合直接作用骨细胞、改变转录因子活性、降低NF-κB活性、调节自噬等多种途径影响骨代谢,是维持骨代谢平衡的重要物质[26]。Ma等[27]研究发现,切除双侧卵巢(OVX)的大鼠肠道菌群严重失调,菌群中厚壁菌门与拟杆菌门比值显著增加;其中瘤胃球菌属、梭菌属和粪球菌属与破骨性指标呈正相关,且与OVX大鼠的骨量丢失趋势一致;拟杆菌属和丁酸弧菌属则与骨量丢失呈负相关。黄俊俊等[28]在对OVX小鼠骨折愈合效果的研究中发现,补充益生菌可升高血钙及骨钙素水平,增加骨小梁数量和骨密度,促进小鼠骨折部位愈合。该实验为改善肠道菌群可正向调节雌激素缺乏所引起的骨丢失提供了有力的依据。
1.5.2 肠道菌群诱导甲状旁腺激素的合成代谢
肠道菌群可通过多种方式调控甲状旁腺激素代谢,对骨代谢产生影响。甲状旁腺激素是细胞外钙和磷酸盐水平的主要内分泌调节剂,可促进骨骼形成和骨吸收[29]。研究发现,在原发性和继发性甲状旁腺功能亢进症小鼠模型中,肠内分节丝状细菌过度增殖,是引起肠道Th17细胞增高,刺激甲状旁腺激素诱导骨吸收的主要原因[30]。Li等[31]则从肠菌代谢物丁酸盐信号通路角度展开研究,发现丁酸盐可通过诱导甲状旁腺激素的合成代谢,增加Tregs细胞的数量,并通过CD8 T细胞刺激成骨Wnt配体Wnt10b的产生,进而激活Wnt信号传导促进骨形成。
1.5.3 肠道菌群及SCFAs调控IGF-1水平
肠道菌群及其代谢物SCFAs均可通过干预宿主体内胰岛素样生长因子-1(IGF-1)水平影响骨代谢[32]。有研究显示,相较于普通小鼠,无菌小鼠的IGF-1 水平更低[33]。Yan等[34]研究发现,抗生素治疗可降低小鼠血清IGF-1,并抑制骨形成。给抗生素治疗的小鼠补充SCFAs后,IGF-1和骨量均可恢复至抗生素治疗前水平。另外,该研究表明无菌小鼠定植SPF肠道菌群的初期,会出现急性骨吸收增加导致骨量减少。定植1个月后,骨吸收消退,骨形成占据主导,测得定植小鼠肠内SCFAs浓度、血清IGF-1相较无菌小鼠均显著升高,提示菌群定植的时长也是影响骨代谢的关键因素。
1.5.4 肠道菌群调节5-羟色胺合成
肠道菌群还可通过诱导肠嗜铬细胞(EC)中5-羟色胺(5-HT)的合成调控骨代谢[35]。肠菌代谢产生的SCFAs可增加TPH1 mRNA表达并与EC细胞合成5-HT[36] 。5-HT是机体重要的激素和神经递质,其信号转导在骨骼发育和维护中起着重要的调节作用。研究发现,口服5-HT合成初始酶Tph-1抑制剂6周可升高OVX小鼠成骨细胞数量、骨形成率和血清骨钙素水平,显著改善骨质疏松症状[37]。而转录因子FOXO1可能是5-HT抑制成骨细胞增殖、降低成骨细胞与破骨细胞的比例的关键因素[38] 。
2. 中药干预肠道菌群调控骨代谢
传统中医认为骨质疏松症以肾精亏虚、骨枯髓减为本,以淤血痹阻、骨络失荣为标。病位主要在肝、肾、脾,临床治疗以温补肝肾为主,辅以健脾活血[39]。现代药理研究表明,补益类中药如淫羊藿、杜仲、黄芪等富含黄酮类、多糖等有效成分,对骨质疏松具有显著的疗效。近年研究发现,补益类中药发挥抗骨质疏松症作用的同时,可以调节机体的肠菌结构,并且可能通过干预肠道菌群结构和丰度、调节机体脂质和胆汁酸代谢、保护肠黏膜屏障功能、减少炎症因子释放、调节自噬等方面对骨质疏松的治疗发挥积极的作用。与此同时,有研究发现,黄连、葛根、马齿苋等清热药在调节肠道菌群结构,发挥解热抗炎作用的过程中,可以缓解宿主骨质疏松的症状。提示清热药可能通过调节宿主的肠道菌群发挥抗骨质疏松的作用。以下列举部分中药及复方的相关研究。
2.1 清热类中药
2.1.1 黄连
黄连主要成分黄连素是异喹啉生物碱类化合物,具有广谱抑菌作用,临床常用于治疗胃肠炎、细菌性痢疾等肠道感染。Jia等[40]研究发现,OVX-牙周炎大鼠在给予黄连素后,肠道菌群结构发生改变,肠菌代谢物丁酸盐显著增加,肠屏障功能明显好转,相关炎症因子IL-17A表达显著降低,缓解了牙周骨质流失。这一实验表明,黄连素可能通过改变肠菌结构,调节宿主免疫等方面对改善骨代谢产生积极影响。
2.1.2 葛根
葛根在传统论著中多用于表征发热、脾虚泄泻、消渴等病症。而现代药理研究发现,葛根中黄酮、萜类、有机酸等成分均具有广泛的药理活性。其中异黄酮类化合物葛根素具雌激素样作用,可用于绝经后骨质疏松的治疗。Li等[41]研究发现,葛根素可扭转OVX大鼠雌激素缺乏导致的肠菌失调,增加肠道内SCFAs含量,修复损伤的肠黏膜,降低结肠上皮通透性,减少TNF-α、IL-6、IL-1β等相关炎症因子释放,从而改善骨微环境。提示葛根素通过干预肠道菌群调节宿主免疫可能是其改善骨质疏松的途径之一。
2.1.3 马齿苋
马齿苋性寒味酸,具有清热燥湿、凉血解毒的作用,临床常用于湿热、热毒引起的痢疾。冯澜等[42]研究发现,马齿苋多糖可以调节脂多糖诱导的结肠炎小鼠肠道菌群结构,上调双歧杆菌和乳杆菌丰度, 降低肠道炎症因子释放,发挥抗炎、调节免疫的作用。另有研究发现,马齿苋可降低脂多糖诱导的溶骨小鼠的促炎症因子,抑制其破骨细胞分化,发挥抗骨质疏松的疗效[43]。提示在脂多糖诱导的炎症模型中,马齿苋可能通过干预肠道菌群调控宿主的免疫,进而影响骨代谢。
2.2 补益类中药
2.2.1 淫羊藿
淫羊藿是传统的补肝肾、强筋骨中药,现代药理学证实其有效成分淫羊藿苷可通过诱导骨形成、抑制骨吸收等途径改善骨质疏松症状[44]。Wang等[45]研究发现,淫羊藿苷可以改变OVX大鼠肠道菌群结构及粪便代谢物组成。其中乳酸菌等关键菌群丰度的上升,可显著上调机体胆汁酸、氨基酸和脂肪酸的代谢,从而提高OVX大鼠雌激素水平,产生抗骨质疏松作用。提示通过调节肠道菌群影响雌激素代谢可能是淫羊藿苷干预、防治骨质疏松的潜在途径。
2.2.2 女贞子
女贞子具有滋补肝肾的功效,临床上常配伍淫羊藿等药物治疗骨质疏松[46]。Chen等[47]研究发现,女贞子水提物可通过改变肠道菌群结构和丰度、促进肠道SCFAs生成等途径,改善OVX大鼠十二指肠绒毛形态,增加肠隐窝深度和吸收面积,从而增强肠道中钙结合蛋白D9k的表达,促进钙离子吸收,发挥抗骨质疏松作用。
2.2.3 杜仲
中药杜仲以干燥树皮入药,具有补肝肾、强筋骨、安胎的作用。现代研究表明,杜仲枝干、叶、花具有与树皮相似的化学成分和药理作用[48]。Zhao等[49]研究发现,杜仲叶醇提物可以在体外促进保加利亚乳杆菌的生长,有效抑制破骨细胞生成。在体内研究中,杜仲叶醇提物能够调节快速衰老模型小鼠的肠道菌群,具体表现在丰富肠菌多样性,调控厚壁菌门/拟杆菌门比例,增加小鼠血清及粪便中SCFAs浓度等方面,对抑制破骨细胞生成,提高骨密度,改善骨质疏松具有潜在影响。
2.2.4 黄芪
中药黄芪长于健脾补中,治疗脾、肺气虚证。现代药理学研究证实黄芪中富含皂苷、多糖等多种活性成分,具有广泛的药理活性。Liu等[50]研究发现,黄芪多糖可以显著改善地塞米松模型大鼠的肠菌结构,通过上调乳杆菌属、经黏液真杆菌属等益生菌群,下调梭状芽孢杆菌、普雷沃氏菌属等致病菌,显著降低酸性磷酸酶5和促炎细胞因子IL-2和TNF-α的生成,抑制破骨细胞生成,改善骨质疏松。
另外,有研究显示,肠道菌群可通过合成和代谢维生素B和维生素K促进成骨细胞向骨细胞转化,抑制破骨细胞生成,介导骨钙素羧化过程等发挥抗骨质疏松作用 [51-52]。因此,在研究中药干预肠道菌群结构的同时,菌群对宿主体内药物的吸收和代谢效果,可能影响到药物抗骨质疏松的疗效,同样值得关注。
2.3 中药复方
2.3.1 仙灵骨葆胶囊
仙灵骨葆胶囊具有滋补肝肾,活血通络,强筋壮骨的功效,临床常用于治疗肝肾不足,瘀血阻络所致的骨质疏松症。Tang等[53]基于LC-MS和宏基因组测序的方法,对仙灵骨葆胶囊在肠道菌群作用下的代谢、转化进行了定量分析。研究发现,仙灵骨葆胶囊可以改变OVX大鼠的肠道菌群结构,加速药物脱糖基化反应,有利于活性成分淫羊藿苷、补骨脂素和异补骨脂素等的吸收代谢;同时,仙灵骨葆胶囊可以促进拟杆菌、普氏菌和益生菌乳酸杆菌的生长,帮助调节机体脂质和胆汁酸代谢,改善骨质疏松。可见,在仙灵骨葆胶囊吸收代谢的过程中,肠道菌群发挥了重要作用;同时,仙灵骨葆胶囊可能通过干预肠道菌群对宿主的骨代谢产生潜在的作用。
2.3.2 补肾化痰方
熊孟欣[54]在结合多样性和宏基因组测序发现,补肾化痰方在改善OVX大鼠骨质疏松的同时,纠正了OVX大鼠失调的肠道菌群。研究显示,给药组肠道菌群中厚壁菌门丰度增加,拟杆菌门、变形菌门丰度减少,肠菌结构与空白组趋于一致。该变化有助于升高粪便和血清中SCFAs浓度,从而影响AMPK/m TOR/ULK1自噬信号通路调控, 促进OVX大鼠体内自噬。
2.3.3 健骨颗粒
健骨颗粒由淫羊藿、骨碎补、山茱萸等10味药组成,是临床上治疗绝经后骨质疏松的常用方剂。Sun等[55]研究发现,健骨颗粒能够改善雌激素缺乏引起的肠菌紊乱,恢复肠道菌群丰度,并通过GM-SCFAs-Treg/Th17轴,调节骨免疫相关细胞因子,有效减少骨质流失,改善OVX大鼠骨质疏松。
2.3.4 葛根芩连汤
葛根芩连汤由葛根、黄芩、黄连、甘草四味药组成,具解表清里之功效,善治急性肠炎、细菌性痢疾等,在临床上对胃肠道疾病、糖尿病及脂代谢疾病均有良好的疗效。长期糖脂代谢异常往往伴随骨代谢失调,王雅婷等[56]在对糖尿病继发骨质疏松大鼠的研究中发现,葛根芩连汤在治疗糖尿病的同时,模型大鼠的骨密度、骨钙含量、极限载荷等均有所回升。而多项研究表明,葛根芩连汤可以通过改善肠道菌群的结构、多样性,抑制致病菌,增加肠内SCFAs浓度等方面干预肠道菌群调控宿主的糖脂代谢,对糖尿病继发骨质疏松症的治疗发挥积极的作用 [57-58]。
3. 小结与展望
肠道菌群与骨代谢之间存在着密切的关联,肠菌结构改变可诱发机体骨代谢异常,导致骨量降低,造成骨质疏松症患病风险增加,是原发性骨质疏松症的重要致病机制之一。目前,对于肠道菌群调控骨代谢的研究大多停留在16S rRNA菌群种属多样性差异分析以及表型的检测,以此来预测其潜在的途径和机制。随着微生物组学测序技术的不断发展,在未来的研究中,可以通过但不限于宏基因组学、靶向代谢组学等分析手段,深入探索肠道菌群中不同门类细菌对骨代谢的影响,确定与骨骼健康密切相关的关键菌种,挖掘相关靶点和分子机制,为肠道菌群调控骨代谢提供更多理论依据。
此外,越来越多的研究证实药物-微生物组的互作机制对菌群平衡和药物疗效有重要的影响,因此,深入研究传统抗骨质疏松中药及复方与肠道菌群的互作机制,发现药物干预肠道菌群调控骨代谢的潜在靶点和通路,通过调节肠道菌群组成,优化药物对骨代谢相关疾病的治疗效果;挖掘清热药通过干预肠道菌群调控宿主脂质代谢和炎症反应发挥抗骨质疏松作用的潜力,或将为改善骨骼健康、防治骨代谢相关疾病提供新思路,为骨质疏松症治疗药物的研究提供新的方向。
-
表 1 入血化学成分的正离子模式鉴别结果
编号 保留时间 (t/min) 化合物名称 分子式 M+X 理论分子量(m/z) 实际分子量(m/z) 误差(ppm) 归属药材 1 10.157 dihydrokaranone C15 H22 O (M+H)+ 219.174 1 219.174 3 2.01 Salvia miltiorrhiza Bge. 2 10.453 dihydrotanshinone I C18 H14 O3 (M+H)+ 279.101 0 279.101 4 0.29 Salvia miltiorrhiza Bge. 3 12.031 salvianonol C18 H20 O4 (M+H)+ 301.141 7 301.141 3 5.72 Salvia miltiorrhiza Bge. 4 10.009 isocryptotanshinone II C19 H20 O3 (M+H)+ 297.148 1 297.148 1 1.49 Salvia miltiorrhiza Bge. 5 11.078 sugiol C20 H28 O2 (M+H)+ 301.216 0 301.216 0 0.78 Salvia miltiorrhiza Bge. 6 11.636 salviol C20 H30 O2 (M+H)+ 303.231 9 303.232 2 −0.13 Salvia miltiorrhiza Bge. 7 12.762 dihydrovalepotriate C22 H32 O8 (M+H)+ 425.216 3 425.215 1 2.87 Salvia miltiorrhiza Bge. 8 7.232 4-methyl salicylaldehyde C8 H8 O2 (M+H)+ 137.059 9 137.059 8 0.05 Salvia miltiorrhiza Bge. 9 1.168 nicotinamide C6 H6 N2 O (M+H)+ 123.055 1 123.054 1 2.14 Cordyceps sinensis 10 0.642 histidine① C6 H9 N3 O2 (M+H)+ 156.075 8 156.076 8 1.52 Cordyceps sinensis 11 1.061 valine C5 H11 N O2 (M+H)+ 118.086 2 118.086 2 0.61 Cordyceps sinensis 12 1.357 adenosine C10 H13 N5 O4 (M+H)+ 268.104 2 268.104 4 −0.54 Cordyceps sinensis 13 0.765 arginine C6 H14 N4 O2 (M+H)+ 175.118 7 175.118 8 2.03 Cordyceps sinensis 14 0.634 lysine C6 H14 N2 O2 (M+H)+ 147.112 9 147.112 8 −0.45 Cordyceps sinensis 15 9.590 cis-9-octadecenoic acid C18 H34 O2 (M+NH4)+ 300.289 2 300.289 4 1.78 Cordyceps sinensis 16 9.360 octadecanoic acid C18 H36 O2 (M+NH4)+ 302.305 4 302.305 1 −0.76 Cordyceps sinensis 17 1.751 leucine C6 H13 N O2 (M+H)+ 132.102 1 132.101 3 −1.57 Cordyceps sinensis 18 1.361 pedatisectine B C5 H5 N5 (M+H)+ 136.062 2 136.061 8 1.02 Cordyceps sinensis 19 8.259 linoleic acid C18 H32 O2 (M+NH4)+ 298.274 0 298.274 1 0.9 Cordyceps sinensis 20 1.102 methionine C5 H11 N O2 S (M+H)+ 150.058 5 150.058 4 −0.61 Cordyceps sinensis 21 10.979 linoleic acid C18 H32 O2 (M+NH4)+ 298.273 9 298.274 1 2.57 Semen Persicae 22 4.726 glucose C6 H12 O6 (M+H)+ 181.070 5 181.070 8 0.95 Semen Persicae 23 9.648 GA17① C20 H26 O7 (M+Na)+ 401.158 3 401.159 2 −2.24 Semen Persicae 24 5.194 prunasin① C14 H17 N O6 (M+Na)+ 318.095 6 318.096 0 −1.94 Semen Persicae 25 9.623 gomisin R C22 H24 O7 (M+H)+ 401.158 5 401.159 1 2.71 Schisandra chinensis Fructus 26 11.168 2-(2-phenyl cyclohexyloxy) ethanol C14 H20 O2 (M+Na)+ 243.135 3 243.135 8 1.78 Schisandra chinensis Fructus 27 9.911 deangeloylgomisin F C23 H28 O8 (M+Na)+ 455.168 9 455.168 2 −0.19 Schisandra chinensis Fructus 28 12.524 schisandrin B C23 H28 O6 (M+Na)+ 423.177 5 423.177 6 1.88 Schisandra chinensis Fructus 29 8.333 gomisin Q C24 H32 O8 (M+Na)+ 471.198 1 471.198 2 1.56 Schisandra chinensis Fructus 30 9.130 (±)-gomisin m1 C22 H26 O6 (M+Na)+ 409.161 8 409.161 8 0.64 Schisandra chinensis Fructus 31 11.973 1,1alpha,4,5,6,7,7alpha,7beta-octahydro-1,1,7,7alpha-tetramethyl-2h-cyclopropa (alpha)-naphthalen-2-one C14 H22 O (M+H)+ 207.174 9 207.174 2 −2.61 Schisandra chinensis Fructus 32 6.870 1-phenyl-1,3-butanedion C10 H10 O2 (M+H)+ 163.075 5 163.075 8 −1.40 Schisandra chinensis Fructus 33 10.839 geranyl acetate C12 H20 O2 (M+H)+ 197.153 8 197.153 5 1.07 Schisandra chinensis Fructus 34 11.110 tigloylgomisin P C28 H34 O9 (M+NH4)+ 532.254 3 532.253 8 0.22 Schisandra chinensis Fructus 35 7.322 citronellyl acetate C12 H22 O2 (M+NH4)+ 216.195 3 216.195 4 2.48 Schisandra chinensis Fructus 36 0.814 gama-octalactone C8 H14 O2 (M+NH4)+ 160.133 0 160.132 9 0.27 Schisandra chinensis Fructus 37 9.607 gomisin D C28 H34 O10 (M+Na)+ 553.204 2 553.203 9 0.61 Schisandra chinensis Fructus 38 10.248 1,1α,2,4,6,7,7α,7β-octahydro-1,1,7,7α-tetra-methyl-5h-cyclopropa (α)-naphthalen-5-one C15 H22 O (M+H)+ 219.173 7 219.174 3 2.92 Schisandra chinensis Fructus 39 9.935 phenyl-2-propanone C9 H10 O (M+H)+ 135.080 2 135.080 2 1.81 Schisandra chinensis Fructus 40 11.834 prehispanolone① C20 H30 O3 (M+H)+ 319.226 3 319.225 7 2.56 Schisandra chinensis Fructus 41 9.919 psilostachyin C15 H20 O5 (M+H)+ 281.137 9 281.138 4 1.67 Schisandra chinensis Fructus 42 11.324 santlic acid C15 H22 O2 (M+H)+ 235.168 3 235.170 5 0.58 Schisandra chinensis Fructus 43 7.355 gomisin A C23 H28 O7 (M+H)+ 417.190 6 417.190 3 0.23 Schisandra chinensis Fructus 注:“①”表示正、负离子模式下都已鉴别出。 表 2 入血化学成分的负离子模式鉴别结果
编号 保留时间 (t/min) 化合物名称 分子式 M-X 理论分子量(m/z) 实际分子量(m/z) 误差(ppm) 归属药材 1 6.795 tanshindiol C C18 H16 O5 (M+COOH)− 357.098 9 357.099 7 −1.34 Salvia miltiorrhiza Bge. 2 13.681 paramiltioic acid C19 H24 O5 (M+COOH)− 377.161 6 377.161 9 −1.84 Salvia miltiorrhiza Bge. 3 0.812 histidine① C6 H9 N3 O2 (M-H)− 154.062 6 154.061 2 −2.28 Cordyceps sinensis 4 0.764 glutamic acid C5 H9 N O4 (M-H)− 146.045 7 146.044 9 1.02 Gynostemma pentaphyllum (Thunb.) Makino 5 13.632 GA17① C20 H26 O7 (M-H)− 377.161 6 377.161 9 −2.18 Semen Persicae 6 3.714 GA19 C20 H26 O6 (M+COOH)− 407.171 9 407.171 7 0.02 Semen Persicae 7 13.632 GA119 C19 H24 O5 (M+COOH)− 377.161 6 377.161 9 −2.48 Semen Persicae 8 5.209 prunasin① C14 H17 N O6 (M+COOH)− 340.102 9 340.102 3 0.40 Semen Persicae 9 11.060 prehispanolone① C20 H30 O3 (M-H)− 317.211 5 317.210 9 2.19 Schisandra chinensis Fructus 10 14.158 schisandrone C21 H24 O5 (M-H)− 355.156 4 355.156 6 −2.79 Schisandra chinensis Fructus 注:“①”表示正、负离子模式下都已鉴别出。 -
[1] 刘成海, 刘平, 胡义扬, 等. 中医药抗肝纤维化临床与基础研究进展[J]. 世界科学技术(中医药现代化), 2007, 9(2):112-119. [2] JIA Y H, WANG R Q, MI H M, et al. Fuzheng Huayu recipe prevents nutritional fibrosing steatohepatitis in mice[J]. Lipids Health Dis,2012,11:45. doi: 10.1186/1476-511X-11-45 [3] LIU C H, HU Y Y, XU L M, et al. Effect of Fuzheng Huayu For Mula and its actions against liver fibrosis[J]. Chin Med,2009,4:12. doi: 10.1186/1749-8546-4-12 [4] LIU P. Fuzheng Huayu capsule in the treatment of liver fibrosis: clinical evidence and mechanism of action[J]. Chin J Integr Med,2012,18(5):398-400. doi: 10.1007/s11655-012-1030-1 [5] LIU P, LIU C, XU L M, et al. Effects of Fuzheng Huayu 319 recipe on liver fibrosis in chronic hepatitis B[J]. World J Gastroenterol,1998,4(4):348-353. doi: 10.3748/wjg.v4.i4.348 [6] 范小云, 吴青芸. 扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化60例疗效分析[J]. 中国医药指南, 2012, 10(18):272-273. doi: 10.3969/j.issn.1671-8194.2012.18.214 [7] 赵长青, 吴艺青, 徐列明. 扶正化瘀胶囊抗肝纤维化的临床疗效和作用机制[J]. 中西医结合学报, 2006, 4(5):467-472. [8] 李丽, 何清, 杨大国, 等. 扶正化瘀胶囊治疗慢性乙型肝炎肝纤维化有效性和安全性的系统评价[J]. 中国循证医学杂志, 2008, 8(10):892-897. doi: 10.3969/j.issn.1672-2531.2008.10.018 [9] ZHANG L J, SCHUPPAN D. Traditional Chinese Medicine (TCM) for fibrotic liver disease: hope and hype[J]. J Hepatol,2014,61(1):166-168. doi: 10.1016/j.jhep.2014.03.009 [10] CHEN Q L, WU F Z, WANG M, et al. Transcriptional profiling and miRNA-target network analysis identify potential biomarkers for efficacy evaluation of fuzheng-Huayu For Mula-treated hepatitis B caused liver cirrhosis[J]. Int J Mol Sci,2016,17(6):E883. doi: 10.3390/ijms17060883 [11] CHENG Q, LI N, CHEN M Q, et al. Fuzheng Huayu inhibits carbon tetrachloride-induced liver fibrosis in mice through activating hepatic NK cells[J]. J Ethnopharmacol,2013,145(1):175-181. doi: 10.1016/j.jep.2012.10.047 [12] TAO Y Y, YAN X C, ZHOU T, et al. Fuzheng Huayu recipe alleviates hepatic fibrosis via inhibiting TNF-α induced hepatocyte apoptosis[J]. BMC Complement Altern Med,2014,14:449. doi: 10.1186/1472-6882-14-449 [13] WANG R Q, MI H M, LI H, et al. Modulation of IKKβ/NF-κB and TGF-β1/Smad via Fuzheng Huayu recipe involves in prevention of nutritional steatohepatitis and fibrosis in mice[J]. Iran J Basic Med Sci,2015,18(4):404-411. [14] XIE H D, TAO Y Y, LV J, et al. Proteomic analysis of the effect of fuzheng Huayu recipe on fibrotic liver in rats[J]. Evid Based Complement Alternat Med,2013,2013:972863. [15] XING X R, CHEN S, LI L, et al. The active components of fuzheng Huayu For Mula and their potential mechanism of action in inhibiting the hepatic stellate cells viability-A network pharmacology and transcriptomics approach[J]. Front Pharmacol,2018,9:525. doi: 10.3389/fphar.2018.00525 [16] 安芸, 杨剑宏, 王臣臣, 等. UHPLC/Q-TOF-MS法分析决明子化学成分[J]. 中成药, 2017, 39(4):776-781. [17] 李军茂, 何明珍, 欧阳辉, 等. 超高效液相色谱与飞行时间质谱联用快速鉴别木芙蓉叶的化学成分[J]. 中国药学杂志, 2016, 51(14):1162-1168. [18] 吴欢, 占远, 陈海芳, 等. UHPLC-ESI-Q-TOF-MS/MS对紫花地丁中化学成分的快速表征[J]. 中国实验方剂学杂志, 2016, 22(24):70-75. [19] 陈珏蓓, 马文彪, 王月红. HPLC法测定心舒乐片中丹参酮ⅡA、羟基红花黄色素A、苦杏仁苷[J]. 中成药, 2012, 34(3):490-494. doi: 10.3969/j.issn.1001-1528.2012.03.027 [20] 官玲花. HPLC法同时测定仙灵骨葆胶囊中二氢丹参酮Ⅰ、隐丹参酮、丹参酮Ⅰ和丹参酮Ⅱ_A的含量[J]. 中国药房, 2013, 24(32):3056-3058. -





 下载:
下载:



