-
肾衰宁颗粒由太子参、黄连、制半夏、陈皮、茯苓、大黄、丹参、牛膝、红花、甘草等十味中药制成;具有补气健脾,活血化痰,祛浊的功效[1]。有文献表明,肾衰宁在治疗慢性肾脏疾病中疗效较为显著[2];在尿毒症腹膜透析患者的治疗过程中能够降低血清硫酸吲哚酯浓度[3];对于慢性肾脏病的Ⅳ期患者,在西医基础治疗的同时服用肾衰宁颗粒,可以明显改善肾功能,同时提升患者的治愈率,具有较高的临床使用价值[4]。由于中药成分复杂[5],使得如何控制中药的质量成为十分重要的问题。指纹图谱是在了解中药物质整体作用的基础上,通过光谱和色谱技术获得中药化学成分的光谱或色谱图,以鉴别中药的真伪,评价质量的一致性和产品的稳定性,其具有信息量大、特征性强、完整性和模糊性等特点[6]。指纹图谱中的质量控制技术既能保证中药的功效,又在实现中药现代化过程中起关键性作用[7]。因此,本实验以10个批次的肾衰宁颗粒为研究对象,拟建立肾衰宁颗粒的指纹图谱,对肾衰宁颗粒进行质量评价。
肾衰宁颗粒是由十味中药组成的复方制剂,其化学成分十分复杂,且许多复方治疗疾病的药物基础并不明显,因此检测成分必须是发挥药效的有效成分[8],本实验针对大黄中的大黄酚(chrysophanol)[9-10]、丹参中的丹酚酸B(salvianolic acid B)[11]、陈皮中的橙皮苷(hesperidin)[9, 12]3种指标性成分,进行HPLC法含量测定。在多成分的质量控制检测成本高而对照品紧缺的情况下,能较大程度地节约检验成本,又可较全面地控制该制剂的质量,保证临床用药的有效性和安全性,同时为肾衰宁颗粒的质量控制提供参考。
-
Agilent 1260高效液相色谱仪(美国Agilent公司),包含G1311C四元泵,G1329B自动进样器,G1316A柱温箱,G4212B-DAD二极管阵列检测器,Chemstation色谱工作站;光电分析天平(德国Sartorius公司,CPA 225D型),最大载荷220 g,分度值0.01 mg;冷冻真空浓缩仪(丹麦Labogene公司,ScanVac ScanSpeed 40型);超声波清洗器(上海科导超声仪器有限公司,SK7200H型);涡旋混匀器(海门市其林贝尔仪器制造有限公司,Vortex QL-901型)。
-
肾衰宁颗粒(德元堂制药集团,批号:51103111、51103009 346、51103010 471、51103011 593、51103105、51103018 486、41103033 563、51103110、61103102、61103101)。蜕皮激素(ecdysterone,批号:P11N6F5706)、甘草苷(liquiritin,批号:2O1027BA14)、甘草酸(glycyrrhizic acid,批号:230A6B1)、大黄酚(chrysophanol,批号:T31O6F5345)、丹酚酸B(salvianolic acid B,批号:Y14M7H14804)、橙皮苷(hesperidin,批号:K02M3C1)对照品,均由上海源叶有限公司提供。大黄素(modin,批号:110756-200110)、盐酸小檗碱(berberine hydrochloride,批号:09030522)对照品,由中国食品药品检定研究院提供。甲醇、乙腈、甲酸,均为德国Merck公司生产,色谱纯。二氯甲烷,色谱纯。水为纯净水,娃哈哈公司生产。
-
色谱柱:Waters SunFire™ C18(250 mm×4.6 mm,5 μm)。流动相A:乙腈;流动相B:0.1%甲酸溶液,梯度洗脱。流速:1 ml/min。柱温:25 ℃。进样量:10 μl。检测波长:254 nm。梯度洗脱条件见表1。
表 1 梯度洗脱条件
时间(t/min) 乙腈(%) 0.1%甲酸溶液(%) 0 5 95 1 23 77 18 25 75 19 30 70 31 75 25 60 85 15 -
精密依次称取丹酚酸B、橙皮苷、大黄素标准品10.25、10.35、10.05 mg,分别置于10 ml容量瓶中,以纯甲醇定容至刻度,摇匀,得储备液并将其分装后储存于−20 ℃的冰箱中。精密称取10.10 mg大黄酚,置于10 ml容量瓶中,加入少量二氯甲烷溶解,超声处理3 min,然后用纯甲醇稀释至刻度,摇匀,得到对照品的储备液,置于−20 ℃冰箱保存。
-
取肾衰宁颗粒适量,研磨成细粉,混合均匀,精密称取0.10 g,加适量70%甲醇溶液使其溶解,超声45 min,再用70%甲醇溶液定容至2 ml,冷却,过0.45 μm微孔滤膜后,取续滤液进样分析。
-
取肾衰宁颗粒(批号:41103033 563),按照“2.3”项制备供试品溶液,在“2.1”项色谱条件下连续进样5次,通过大黄素(7号色谱峰)作为参照峰,确定相对保留时间和相对峰面积。相对保留时间的RSD在1.0%以内,相对峰面积的RSD在2.0%以内,表明进样仪器的精密度良好。
-
取肾衰宁颗粒(批号:41103033 563),按照“2.3”项平行制备5份供试品溶液,测定在“2.1”项色谱条件下的相对保留时间和相对峰面积。相对保留时间RSD在1.0%以内,相对保留面积RSD在2.0%以内。表明该实验方法的重复性良好。
-
取肾衰宁颗粒(批号:41103033 563),并根据“2.3”项下平行制备5份供试品溶液,在“2.1”项色谱条件下,分别记录0、4、8、24、36 h的相对保留时间和相对峰面积。相对保留时间RSD在1.0%以内,相对保留面积RSD在2.0%以内。表明供试样品溶液在36 h内稳定性好。
-
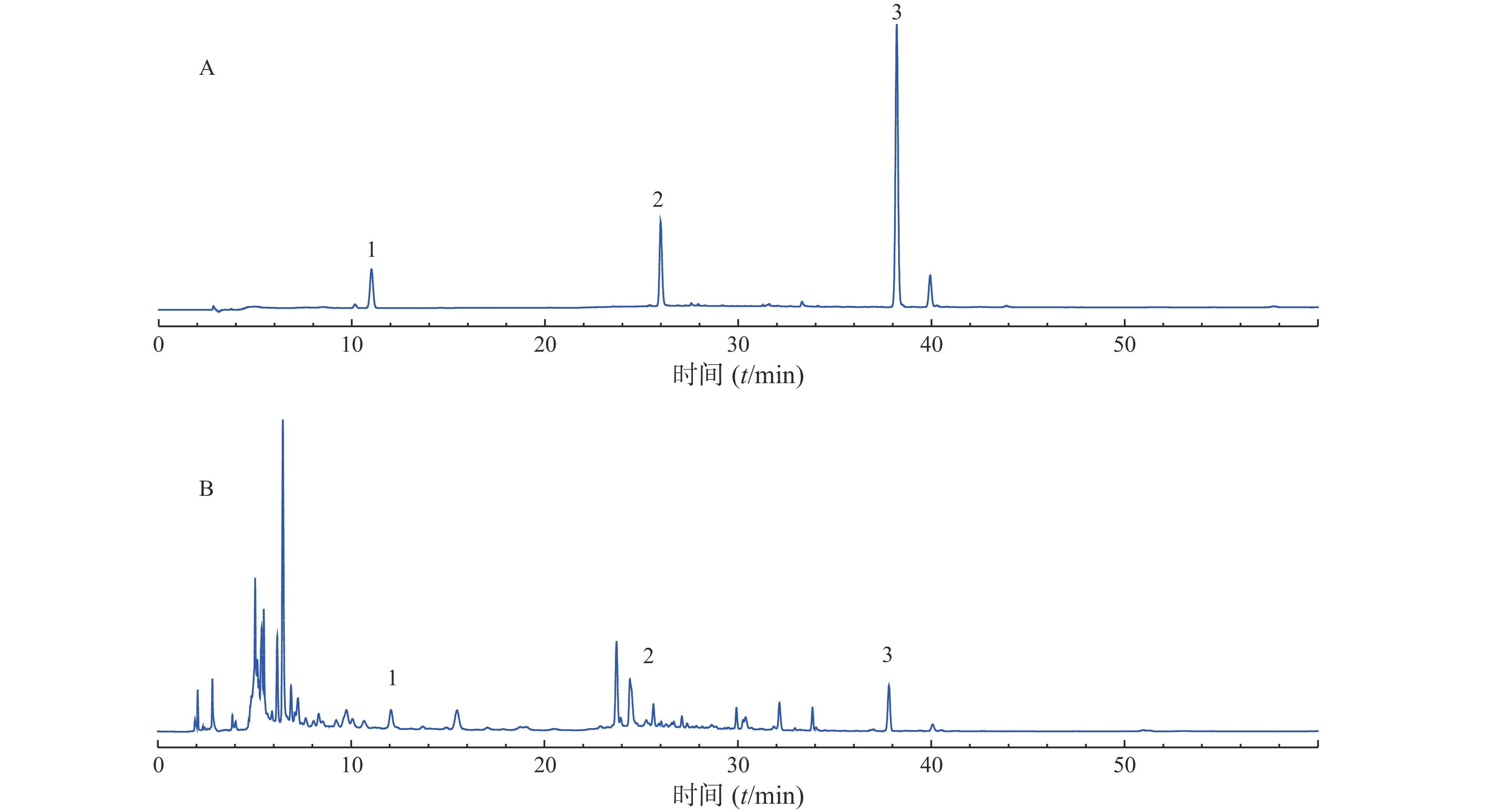
分别称取10个批次的肾衰宁粉末,按照“2.3”项制备供试品溶液,每个批次平行制备3份供试品溶液,记录图谱,见图1。利用中国药典委员会“中药色谱指纹图谱相似度评价系统2008A版”的软件,将10批次肾衰宁颗粒的图谱导入,将批号为61103102的样品溶液用作针对相似性计算校正的参考图。结果显示,1~9批制剂间指纹图谱与对照图谱之间相似度均不小于0.90,见表2,表明相似度良好。对保留时间0~60 min内的色谱峰进行分析,均有22个稳定的特征峰,确定其为肾衰宁的共有指纹峰,经过标准品比对,其中,6号峰为橙皮苷,14号峰为丹酚酸B,21号峰为大黄酚。
表 2 10批肾衰宁颗粒HPLC指纹图谱相似度
样品号 S1 S2 S3 S4 S5 S6 S7 S8 S9 S10 对照指纹图谱 S1 1.000 0.980 0.910 0.941 0.934 0.948 0.916 0.941 0.950 0.874 0.965 S2 0.980 1.000 0.934 0.934 0.932 0.945 0.951 0.946 0.978 0.867 0.973 S3 0.910 0.934 1.000 0.952 0.947 0.937 0.972 0.940 0.945 0.914 0.973 S4 0.941 0.934 0.952 1.000 0.990 0.984 0.951 0.971 0.923 0.940 0.986 S5 0.934 0.932 0.947 0.990 1.000 0.978 0.938 0.976 0.910 0.910 0.979 S6 0.948 0.945 0.937 0.984 0.978 1.000 0.954 0.987 0.931 0.923 0.986 S7 0.916 0.951 0.972 0.951 0.938 0.954 1.000 0.949 0.966 0.913 0.979 S8 0.941 0.946 0.940 0.971 0.976 0.987 0.949 1.000 0.928 0.890 0.980 S9 0.950 0.978 0.945 0.923 0.910 0.931 0.966 0.928 1.000 0.892 0.969 S10 0.874 0.867 0.914 0.940 0.910 0.923 0.913 0.890 0.892 1.000 0.937 对照指纹图谱 0.965 0.973 0.973 0.986 0.979 0.986 0.979 0.980 0.969 0.937 1.000 -
按照“2.2”项下制备标准品溶液,得到混合对照品色谱图见图2。将标准品储备液用纯甲醇稀释,丹酚酸B浓度梯度为:10、20、40、80和100 μg/ml;橙皮苷浓度梯度为:40、80、160、320和400 μg/ml;大黄酚浓度梯度为:8、16、40、100和350 μg/ml。在“2.1”项色谱条件下,分别记录3种成分的峰面积,以峰面积(Y)对浓度(X)进行线性回归,结果见表3。
表 3 各成分线性关系
对照品 回归方程 r 线性范围(μg/ml) 橙皮苷 Y=2.391 8X–2.798 3 0.999 7 40~400 丹酚酸B Y=10.689X–5.578 3 0.999 8 10~100 大黄酚 Y=58.983X+121.99 0.999 9 7~350 -
取同一对照品溶液,根据“2.1”项下色谱条件进行测定,重复进样5次,并记录峰面积。橙皮苷、丹酚酸B、大黄酚峰面积的RSD分别为0.17%、0.20%、0.15%,表明仪器精密度良好。
-
精密吸取橙皮苷、丹酚酸B、大黄酚对照品溶液适量,使用甲醇逐步稀释,至色谱图中上述3种成分的峰高分别为噪音的3倍和10倍,测得橙皮苷的检测限和定量限分别为0.18和1 μg/ml;丹酚酸B的检测限和定量限分别为0.3和1.2 μg/ml;大黄酚的检测限和定量限分别为1和5 μg/ml。
-
取同一供试品溶液(批号:41103033 563),并根据“2.1”项色谱条件在0、2、4、8、24、36 h测定。橙皮苷、丹酚酸B、大黄酚的峰面积的RSD分别为2.01%、2.22%、2.05%,结果表明:供试品在36 h内稳定。
-
取同一供试品溶液(批号:41103033 563),平行制备6份,并根据“2.1”项色谱条件进行测定,橙皮苷、丹酚酸B、大黄酚的峰面积的RSD分别为0.67%、2.00%、2.02%,表明系统重复性良好。
-
精密量取肾衰宁溶液1 ml,分别加入100%含量橙皮苷对照品(理论值为192.02 μg),100%含量丹酚酸B对照品(理论值为62.66 μg),100%含量大黄酚对照品(理论值35.22 μg),按照“2.2”项平行制备6份,并根据“2.1”的色谱条件进行测量,按照下述公式计算加样回收率,平均加样回收分别为119.20%、84.69%、84.58%。结果见表4。
表 4 加样回收率试验结果
成分 取样量(V/ml) 样品含量(m/μg) 加入量(m/μg) 测得量(m/μg) 回收率(%) 平均回收率(%) 橙皮苷 1.00 383.02 95.88 773.46 101.80 100.27 1.00 380.39 95.88 764.91 100.26 1.00 380.31 95.88 763.64 99.95 1.00 384.46 95.88 771.17 100.83 1.00 385.81 95.88 772.95 100.94 1.00 389.20 95.88 764.32 97.81 丹酚酸B 1.00 120.79 31.80 250.42 101.91 98.82 1.00 122.50 31.80 251.14 101.12 1.00 125.56 31.80 248.78 96.87 1.00 127.57 31.80 254.87 100.07 1.00 127.74 31.80 251.44 97.25 1.00 127.75 31.80 249.44 95.66 大黄酚 1.00 72.67 17.79 138.19 92.06 97.36 1.00 69.62 17.79 135.41 92.44 1.00 68.46 17.79 140.83 101.69 1.00 71.03 17.79 141.25 98.66 1.00 68.98 17.79 141.57 102.00 1.00 71.92 17.79 141.17 97.30 回收率=(实测量-样品含量)/加入量×100%。
-
取10批肾衰宁颗粒,按“2.2”项制备试液,按“2.1”项色谱条件测定,结果见表5。
表 5 10批肾衰宁样品中3种成分的测定结果
药品批号 橙皮苷(μg/ml) 丹酚酸B(μg/ml) 大黄酚(μg/ml) 61103102 66.99 42.29 44.65 51103110 83.41 39.34 42.89 51103111 94.75 41.36 44.51 51103009 346 80.57 43.21 43.44 51103011 593 83.51 42.04 42.58 51103018 486 79.94 41.94 42.96 51103010 471 90.03 41.88 44.03 41103033 563 83.48 43.01 43.94 61103101 85,92 42.93 43.85 51103105 88.04 41.76 42.94 -
在190~400 nm处全波长扫描,盐酸小檗碱、大黄素、大黄酚、丹酚酸B、蜕皮激素、甘草酸、甘草苷、橙皮苷分别在345、254、254、286、250、237、237、283 nm处有最大吸收,通过对比分析,在波长254 nm处,上述8种成分具有良好的响应,样品中相邻色谱峰的基线分离可以满足含量检测的要求。因此,选择波长254 nm作为检测波长。
-
将肾衰宁粉末直接用水溶解后进样,发现样品出峰很少,所测成分在色谱条件下没有吸收。后用50%、70%、80%的甲醇溶解样品,发现用70%甲醇溶解出峰数最多,且所测成分在此条件下均有吸收,故选择70%甲醇进行样品的前处理。
-
有文献报道,肾衰宁含量测定使用甲醇-0.1%磷酸[13]、乙腈-水-1%甲酸[14]、乙腈-05%磷酸[15]进行90 min的大梯度洗脱,发现色谱峰分不开,且特征峰较少。经过反复实验,确定乙腈-0.1%甲酸水溶液用作梯度洗脱的流动相,分离出样品中测得的特征峰,特征峰很多,峰形良好。
Research on the fingerprint and three active components assay in Shenshuaining granules by HPLC
-
摘要:
目的 通过高效液相色谱法建立肾衰宁颗粒的指纹图谱,并测定肾衰宁颗粒中3种有效成分(橙皮苷、丹酚酸B和大黄酚)的含量,为肾衰宁颗粒的质量控制提供依据。 方法 采用SunFireTM C18色谱柱,乙腈-0.1%甲酸水溶液为流动相,梯度洗脱,流速1 ml/min,检测波长254 nm,柱温25 ℃,建立肾衰宁颗粒的指纹图谱,并对3种有效成分的含量进行测定。 结果 测定10批肾衰宁颗粒的色谱图,确立的标准指纹图谱上有22个共有峰,各批次的指纹图谱与对照图谱之间相似度均不小于0.90,相似度良好。方法学验证结果表明重复性、稳定性、精密度结果均符合要求。 结论 本法操作简单、可靠,适用于肾衰宁颗粒指纹图谱的建立及含量测定,为肾衰宁颗粒的质量控制提供依据。 Abstract:Objective To establish the fingerprint spectrum and assay three active components (hesperidin, salvianolic acid B and chrysophanol) in Shenshuaining granule by HPLC method. Methods The chromatographic separation was achieved on SunFireTM C18 column with acetonitrile-0.1% formic acid aqueous solution as mobile phase. Gradient elution program was applied with flow rate of 1.0 ml/min, detection wavelength at 254 nm and the column temperature at 25 ℃. The fingerprint spectrum was established and three active components in Shenshuaining granule were assayed. Results There were 22 common peaks on the fingerprints after analyzing chromatograms from 10 batches of Shenshuaining granules. Good fingerprint similarities (≥0.9) between different batches and the control chromatogram were found. This method has great repeatability, stability and precision, which meets all the assay requirements. Conclusion A simple and reliable HPLC method was developed, which is suitable for the fingerprint establishment of Shenshuaining granules. It provides a method for the quality control of Shenshuaining granules. -
Key words:
- Shenshuaining granules /
- HPLC /
- fingerprinting /
- content determination
-
在当代社会,医院青年药师在工作和生活中存在不同程度的冲突,不规律的工作安排和沉重的工作也带来不小压力[1],而过度的心理压力将对药师的成长带来不利影响,影响药师工作质量[2]。当前国家力推医保支付模式的转变和疾病诊断相关分组(DRG)控费,大多数青年药师面临转型期的工作模式的重大改变,他们将不再简单地从事药品调剂,而是从窗口走出药房,走进病房,走近患者。然而,青年药师对自我的专业知识储备和专业技能能否适应角色转型,心存疑虑,职业压力空前增加。本课题组之前的调查研究发现[3],随着药学本科教育的逐渐普及,本科及以上学历的药学毕业生在医院药师队伍中所占比例显著提高,但与之相伴的是青年药师职业满意度不高。这可能与周而复始的药品调剂工作所带来的职业倦怠和社会认同较低等因素有关。而新情况新形势下社会对执业需求的提高,势必给青年药师形成更大压力,使其感到前所未有的职业挑战,导致职业倦怠显现,创新能力和自我成就感弱化[4]。青年药师从业时间不长,作为这一职业人群的新生代,若长时间处于压力中,会对其职业发展产生不利影响。本研究聚焦于青年药师,通过问卷调查青年药师在医改新形势下的职业压力现状,对导致青年药师职业压力的因素进行统计分析,探讨相应干预对策,以帮助其缓解职业压力,旨在提升其身心健康水平和工作绩效。
1. 资料与方法
1.1 调查对象
本次调查的目标人群为不同等级医疗机构从业的35岁以下青年药师。纳入标准:①各级医疗机构在岗药师;②年龄小于35岁;③自愿参与问卷调查。
1.2 调查方法
参考课题组之前的工作[3]和相关文献[4-6],设计问卷并通过问卷星APP制作,在各级医疗机构药剂科微信群发布。问卷通过Cronbach信度分析,信度系数值为0.80(>0.7),表明研究数据信度质量良好。问卷采用不记名方式,不采集可识别的信息,问卷经过网络发放。为避免重复提交问卷,每个微信账号只允许提交一次。调查时间为2020年7月至9月。
1.3 调查内容
问卷分为4个部分,第一部分为填写者的基本信息。第二部分以五级Likert量表提出12个与职业相关压力问题,对其工作的各个要素(工作量、工作时间、薪资、工作与家庭关系、与同事及领导关系、自身身体状况等)进行评分,分别计1~5分,对每个项目的得分数相加获得压力总分。压力得分从最低12分到最高60分不等。总分越高,表示青年药师职业压力越大。第三部分涉及自身职业发展及对今后工作的未来期望。第四部分为填写者对职业压力处理方式的选择,除了预设选项,还留有一道开放式问题,填写者可自由陈述其对减缓职业压力的看法。
1.4 统计分析
数据分析采用SPSS 25.0软件进行。使用方差分析来检验组间的显著性差异(P<0.01)。
2. 结果
2.1 基本信息
共回收289份有效调查问卷。人口统计学信息(表1)包含了受访者的人口统计信息和执业信息。
表 1 人口统计学信息项目 频数(%) 性别 男 70(24.22) 女 219(75.78) 年龄 小于25 32(11.07) 26~30 104(35.99) 31~35 153(52.94) 受教育程度 专科以下 1(0.35) 大学专科 39(13.49) 大学本科 196(67.82) 硕士及以上 53(18.34) 医院级别 一级 42(14.53) 二级 44(15.22) 三级 203(70.24) 职称 药士 40(13.84) 药师 173(59.86) 主管药师 71(24.57) 副主任药师 5(1.73) 主任药师 0(0) 工作岗位 调剂 190(65.74) 临床药学 55(19.03) 静脉药物配置中心 28(9.69) 其他 16(5.54) 2.2 职业压力产生原因分析
调查显示:有许多与工作相关的压力因素导致青年药师,尤其是三级医院青年药师的满意度降低。心理压力和职业倦怠问题是影响青年药师工作积极性、服务质量和医患关系的重要因素[5]。通过对量表赋值统计,以24分及以下认为无过多职业压力,24~36分认为有一定职业压力,36分以上认为有较高职业压力,其中认为无过多职业压力者18人(6.23%),认为有一定职业压力者93人(32.18%),认为有较高职业压力者178人(61.59%)。有超过半数的青年药师认为有较高的职业压力(图1)。
通过方差分析,可得知性别、受教育程度、医院级别、工作岗位对于青年药师职业压力程度无显著性差异。
年龄段对于青年药师职业压力程度呈现出显著性差异(表2)。青年药师的年龄段对于其职业压力程度呈现出极显著性差异(P<0.01),在31~35岁这一年龄段的职业压力高于其他年龄段,且职业压力程度得分随着年龄段的增长而变高。
表 2 不同年龄段的青年药师压力评分结果($\bar x \pm s$ )组别 评分(分) <25岁(n=32) 28.28±10.71 26~30岁(n=104) 34.56±9.23 31~35岁(n=153) 36.34±10.86* *P<0.01,与<25岁组比较。 职称对于青年药师职业压力程度呈现出显著性差异(表3)。青年药师的职称对于其职业压力程度呈现出极显著性差异(P<0.01),职称越高,青年药师职业压力程度得分越高。中高级职称的晋升是青年药师的一大压力来源,对在繁忙的工作之余,须撰写论文、做课题,以期得到职称的晋升,这对于许多青年药师来说是非常困难的。
表 3 不同职称的青年药师压力评分结果($\bar x \pm s$ )组别 评分(分) 药士(n=40) 29.88±10.72 药师(n=173) 35.07±10.74 主管药师(n=71) 36.59±9.27 副主任药师(n=5) 39.80±8.35* *P<0.01,与药士组比较。 2.3 对职业规划、职业前途和重新择业可能的看法
通过3个问题调查分析青年药师对所从事职业的看法(表4)。在289名回答者中,只有65.05%的青年药师对自身工作有长期职业规划。
表 4 青年药师对药师职业相关问题的看法提问 选项 频数(%) 您目前是否有对药师工作的长期职业规划? 是 188(65.05) 否 101(34.95) 您是如何看待自己的前途的? 一片光明,信心十足 62(21.45) 感到困扰或担心 177(61.25) 没考虑过 50(17.3) 如果有重新选择的机会,您还会选择药师作为职业吗? 会 126(43.6) 不会 163(56.4) 以年龄段看,在25~30岁这一年龄段,有70.19%的青年药师对前途感到困扰或担心。以职称看,高级职称药师更多对前途感到困扰或担心。
如果能重新选择职业,在31~35岁的年龄段中,52.29%的青年药师不会再选择药师职业。对于药师、主管药师、副主任药师,同样超过半数(分别为60.12%、56.34%、60%)的青年药师不会再选择药师职业。超过一半的青年药师不愿意重新选择,提示药师这一职业对于青年来说并不是一项令人满意的工作。
3. 对策与讨论
本研究问卷调查表明,在医院工作的青年药师有超过半数感到职业压力过大。青年调剂药师面对调剂工作的巨大工作量可能无法做到以最好的态度面对每一个患者,而患者可能对药师服务期望过高,很容易发生冲突,加上青年药师对人际关系压力的心理承受力弱,处理医患矛盾的经验不足,对被投诉后受到批评、处罚,往往感到压力过大。即使是青年临床药师,他们自感与医生相比社会地位较低,职业期望无法得到满足;长期的疲劳和压力会影响临床药学工作质量和患者用药安全[6]。如何帮助青年药师改善心理情绪,调节职业压力,以能够促使他们用积极健康的心态投入到药学服务工作中去,成为当前医院药剂科管理者应当积极重视的问题。基于本文的调查,我们提出以下几方面的干预对策。
3.1 提高薪资待遇
在我们的调查中,有近9成青年药师希望提高薪资待遇。近年来,药事服务费、临床药学服务收费等一直是业界呼吁的热点议题,迄今尚未解决。随着临床药学工作的深入开展,药师在控制医疗费用方面正在起着积极的作用,临床药师的工作难度大,但薪酬水平有时不如传统调剂药学岗位,这一现状亟待改变。国家和医院有关部门应在绩效方面,对药师工作给予肯定,合理体现多劳多得、优劳多得[7],更好地激励青年药师参与药学服务工作。
3.2 参加各种体育活动
在我们的调查中半数青年药师愿意希望通过参加各种体育活动,释放自身压力。体育锻炼是常见的减压方式之一,调查表明[8],一定程度的体育锻炼可以有效降低工作压力,每周参加1~2次的运动可以促进心理健康,减缓压力程度。青年药师平时工作处于高压力、高疲劳状态,只有选择结合自身职业特点,科学的体育活动,才能达到强健身心,释放压力的作用。
3.3 组织团建
有4成多青年药师希望科室经常组织团建活动,与同事们一同参加户外活动或比赛,除了能增强员工之间的感情和沟通外,也能释放工作压力,使其保持良好的心情与乐观的态度。青年药师们更希望活动形式新颖、多样,切合当代青年药师的实际情况。
3.4 学习培训
有近5成的青年药师希望能增加外出学习培训机会。青年人志向远大、容易接受新事物。他们进入职业环境时间不长,需要榜样的引领和激励,树立良好的职业规范和正确的价值观念,激发工作学习的积极性和主动性。学习和培训,可让他们感受到关注和重视,坚定职业发展的信心。
本次调查显示,在289位青年药师中,有超过半数在医院工作时感到职业压力过大。职业压力是在所难免的,通过多方面不同对策的干预,帮助青年药师提高压力调节能力,如此,青年药师的压力能够得到缓解。本文未收集青年药师的薪酬待遇和个人生活空间数据,这些也是影响青年药师职业压力感受的重要因素之一。此外,由于本次调查采用的是自愿方式,一些不愿表露态度的药师不参与,可能会带来一定的偏倚。拟在今后的研究中深入予以探讨,以获得更加准确的结果。
-
表 1 梯度洗脱条件
时间(t/min) 乙腈(%) 0.1%甲酸溶液(%) 0 5 95 1 23 77 18 25 75 19 30 70 31 75 25 60 85 15 表 2 10批肾衰宁颗粒HPLC指纹图谱相似度
样品号 S1 S2 S3 S4 S5 S6 S7 S8 S9 S10 对照指纹图谱 S1 1.000 0.980 0.910 0.941 0.934 0.948 0.916 0.941 0.950 0.874 0.965 S2 0.980 1.000 0.934 0.934 0.932 0.945 0.951 0.946 0.978 0.867 0.973 S3 0.910 0.934 1.000 0.952 0.947 0.937 0.972 0.940 0.945 0.914 0.973 S4 0.941 0.934 0.952 1.000 0.990 0.984 0.951 0.971 0.923 0.940 0.986 S5 0.934 0.932 0.947 0.990 1.000 0.978 0.938 0.976 0.910 0.910 0.979 S6 0.948 0.945 0.937 0.984 0.978 1.000 0.954 0.987 0.931 0.923 0.986 S7 0.916 0.951 0.972 0.951 0.938 0.954 1.000 0.949 0.966 0.913 0.979 S8 0.941 0.946 0.940 0.971 0.976 0.987 0.949 1.000 0.928 0.890 0.980 S9 0.950 0.978 0.945 0.923 0.910 0.931 0.966 0.928 1.000 0.892 0.969 S10 0.874 0.867 0.914 0.940 0.910 0.923 0.913 0.890 0.892 1.000 0.937 对照指纹图谱 0.965 0.973 0.973 0.986 0.979 0.986 0.979 0.980 0.969 0.937 1.000 表 3 各成分线性关系
对照品 回归方程 r 线性范围(μg/ml) 橙皮苷 Y=2.391 8X–2.798 3 0.999 7 40~400 丹酚酸B Y=10.689X–5.578 3 0.999 8 10~100 大黄酚 Y=58.983X+121.99 0.999 9 7~350 表 4 加样回收率试验结果
成分 取样量(V/ml) 样品含量(m/μg) 加入量(m/μg) 测得量(m/μg) 回收率(%) 平均回收率(%) 橙皮苷 1.00 383.02 95.88 773.46 101.80 100.27 1.00 380.39 95.88 764.91 100.26 1.00 380.31 95.88 763.64 99.95 1.00 384.46 95.88 771.17 100.83 1.00 385.81 95.88 772.95 100.94 1.00 389.20 95.88 764.32 97.81 丹酚酸B 1.00 120.79 31.80 250.42 101.91 98.82 1.00 122.50 31.80 251.14 101.12 1.00 125.56 31.80 248.78 96.87 1.00 127.57 31.80 254.87 100.07 1.00 127.74 31.80 251.44 97.25 1.00 127.75 31.80 249.44 95.66 大黄酚 1.00 72.67 17.79 138.19 92.06 97.36 1.00 69.62 17.79 135.41 92.44 1.00 68.46 17.79 140.83 101.69 1.00 71.03 17.79 141.25 98.66 1.00 68.98 17.79 141.57 102.00 1.00 71.92 17.79 141.17 97.30 表 5 10批肾衰宁样品中3种成分的测定结果
药品批号 橙皮苷(μg/ml) 丹酚酸B(μg/ml) 大黄酚(μg/ml) 61103102 66.99 42.29 44.65 51103110 83.41 39.34 42.89 51103111 94.75 41.36 44.51 51103009 346 80.57 43.21 43.44 51103011 593 83.51 42.04 42.58 51103018 486 79.94 41.94 42.96 51103010 471 90.03 41.88 44.03 41103033 563 83.48 43.01 43.94 61103101 85,92 42.93 43.85 51103105 88.04 41.76 42.94 -
[1] 国家药典委员会. 中华人民共和国药典2015年版(一部)[S]. 2015: 1052-1053. [2] WANG S S, ZHANG J F, GUO M, et al. The efficacy of Shen shuaining capsule on chronic kidney disease: a systematic review and meta-analysis[J]. Evid Based Complement Alternat Med,2016,2016:7515413. [3] CHEN X J, GAO S H, RUAN M N, et al. Shen-Shuai-Ning granule decreased serum concentrations of indoxyl sulphate in uremic patients undergoing peritoneal Dialysis[J]. Biosci Rep,2018,38(5):BSR20171694. doi: 10.1042/BSR20171694 [4] 谢小洪, 黄鹤宁. 肾衰宁颗粒结合西医基础治疗慢性肾脏病4期疗效观察[J]. 中国处方药, 2014, 12(12):131. doi: 10.3969/j.issn.1671-945X.2014.12.113 [5] LIU W, WANG D M, LIU J J, et al. Quality evaluation of Potentilla fruticosa L. by high performance liquid chromatography fingerprinting associated with chemometric methods[J]. PLoS One,2016,11(2):e0149197. doi: 10.1371/journal.pone.0149197 [6] 李强, 杜思邈, 张忠亮, 等. 中药指纹图谱技术进展及未来发展方向展望[J]. 中草药, 2013, 44(22):3095-3104. doi: 10.7501/j.issn.0253-2670.2013.22.001 [7] 易智彪, 薄雯映, 许冬瑾, 等. 太子参HPLC指纹图谱研究[J]. 中草药, 2009, 40(8):1308-1310. doi: 10.3321/j.issn:0253-2670.2009.08.042 [8] 黄慧梅, 柳润辉. 中药复方药动学研究进展[J]. 药学实践杂志, 2014, 32(2):88-91. doi: 10.3969/j.issn.1006-0111.2014.02.003 [9] 李东晓, 桂雪虹, 陈为, 等. 通腑泻热灌肠液中大黄素及大黄酚含量测定[J]. 中药新药与临床药理, 2015, 26(3):372-377. [10] 周萍. 高效液相色谱法测定大明胶囊中大黄酚的含量[J]. 黑龙江科技信息, 2015(27):123. [11] 张小红, 肖雪, 梁洁, 等. HPLC法测定林芝地区丹参中丹参酚酸B含量[J]. 亚太传统医药, 2015, 11(11):45-46. [12] 谭丽荷. 陈皮四物片中橙皮苷的含量测定[J]. 中国当代医药, 2015, 22(9):88-90. [13] 姚荣成, 林琼芬, 张雯洁. HPLC法测定肾衰宁胶囊中大黄素与大黄酚的含量[J]. 中国药房, 2010, 21(36):3447-3449. [14] 杨柳, 张颖, 刘季田媛, 等. 牛膝各化学拆分组分指纹图谱研究[J]. 中医药信息, 2015, 32(6):16-19. [15] 胡志军, 陈建秋. HPLC测定不同基原陈皮药材中橙皮苷含量[J]. 中国实验方剂学杂志, 2012, 18(10):95-98. doi: 10.3969/j.issn.1005-9903.2012.10.027 -





 下载:
下载:




 下载:
下载: