-
肺脾气虚汤由法半夏,陈皮,党参,炙黄芪,茯苓,藿香,砂仁等七味中药组成,其中,炙黄芪、党参共为君药,补肺脾之气,益卫固表,法半夏、陈皮、茯苓,健脾祛湿,化痰利肺是为臣药,藿香芳香化浊,辟秽和中,是为佐药,砂仁行气调中,和胃醒脾,为使药。作为从第4版新型冠状病毒感染肺炎诊疗方案便被纳入中医治疗方案的方剂之一,该方主治新冠患者恢复期出现的肺脾气虚证,对气短、倦怠乏力、纳差呕恶、痞满、大便无力、便溏不爽、舌淡胖、苔白腻等症状具有良好疗效[1]。但治疗新冠的中药方剂均由多味中药组成,化学成分复杂,目前诸多文献均侧重于基于公开数据库查询方剂组成的各个药味所含的化合物开展网络药理学研究[2-5],而没有对方剂的化学成分群进行系统考察。其次,中药复方体内与体外之间化学成分具有重要关联,针对复方进入机体内的化学成分群进行分析是有助于发现活性物质的有效手段[6]。
目前尚未见肺脾气虚汤的化学成分及入血成分研究的报道,因此本研究通过UHPLC-Q-TOF/MS技术首次对肺脾气虚汤所含化学成分进行快速分析鉴定,并对化学成分的药材来源进行归属,在此基础上开展其血中药源性成分的辨识,以期为进一步阐明肺脾气虚汤的活性成分,并为今后质量控制提供科学依据。
-
超高效液相色谱-四极杆-飞行时间质谱仪(UHPLC-Q-TOF/MS)购自美国安捷伦公司,包含1290 Infinity型UHPLC及6530型Q-TOF/MS系统;CPA255D型1/10万电子天平购自德国Sartorius公司;Lyovapor L-200型冷冻干燥机购自瑞士Buchi公司;Centrifuge 5810R 高速台式冷冻离心机购自德国Eppendorf公司;SK7200H型超声波清洗器购自上海科导超声仪器有限公司;Milli-Q型纯化水系统购自美国Millipore公司;HC-800Y高速多功能粉碎机购自武义海纳电器有限公司。
-
法半夏(批号191115042)、陈皮(批号19090603)、党参(批号19102901)、炙黄芪(批号19650710)、茯苓(批号19122304)、藿香(批号19051410)、砂仁(批号19102211)等饮片均购自吴江上海蔡同德堂中药饮片有限公司,以上样品均经上海中医药大学陈万生教授鉴定为正品。
琥珀酸(批号A0727AS)、绿原酸(批号J0120AS)、芦丁(批号O0714AS)、芒柄花素(批号N0301AS)等对照品均购自大连美仑生物技术有限公司(纯度>97.0 %)。甲醇、乙腈为质谱纯(德国 Merck 公司);甲酸为质谱纯(美国 Thermo Fisher公司);超纯水由MILI-Q净水系统制备(美国Millipore公司);其他均为分析纯试剂。
-
本研究所用动物为8周龄雄性SD大鼠,SPF级,购自上海市计划生育科学研究所实验动物经营部(合格证编号20180006021172),大鼠饲养于温度(22~26 ℃)、湿度(40%~70%)、12 h明暗循环可控的室内环境,可自由进食饮水。
-
精密称取琥珀酸,加入超纯水配置成浓度为1.0 mg/ml的对照品储备液,分别精密称取绿原酸、芦丁、芒柄花素各对照品适量,加入含5% DMSO的甲醇分别配置成浓度为1.0 mg/ml的对照品储备液,所有储备液配制完成后均放于−20 ℃冰箱保存备用。精密吸取上述储备溶液各10 μl,置于1.5 ml离心管中,加入甲醇,涡旋混匀,配制成各对照品浓度均为10 μg/ml 的混合对照品溶液。
-
将方剂所有药材冷冻干燥,用高速粉碎机分别打粉并过四号筛,并按处方比例混合,精密称取约0.500 g,置于100 ml具塞锥形瓶中,精密加入10倍体积70 %甲醇,密塞、称定重量,超声波提取法提取(760 W,50 kHz)30 min,冷却,70 %甲醇补足失重,滤过,3 000 r/min离心10 min,取1.0 ml上清液于1.5 ml EP管中,12 000 r/min离心 10 min,取200 μl上清液于进样小瓶中,待进样分析。另取方剂10倍体积纯净水浸泡过夜,回流提取1.5 h后用纱布过滤,药渣用8倍体积水继续回流提取1 h,过滤并离心,合并上清液,减压浓缩,得到浸膏供入血成分分析研究。
-
SD大鼠给药前适应性喂养1周后,随机分为2组,即空白对照组与肺脾气虚汤给药组,每组6只。给药组大鼠灌胃给予方剂提取物(10倍临床给药剂量),空白对照组大鼠灌胃给予等体积水。给药1 h后眼眶静脉丛取血1.5 ml于5 ml促凝管中, 室温下静置2 h,4 °C下3 000 r/min离心10 min,取100 μl血清于1.5 ml EP管中,加入4倍体积甲醇,涡旋混匀1 min,4 ℃ 12 000 r/min离心15 min,取上清液,真空冷冻干燥后,加入100 μl 80% 甲醇复溶,涡旋混匀1 min,4 ℃ 12 000 r/min离心15 min,取上清液进行检测。
-
色谱柱:Waters ACQUITY UPLC BEH C18 色谱柱(2.1 mm×100 mm,1.7 μm);流动相:0.1 %甲酸水(A)-乙腈(B),色谱洗脱梯度见表1,后运行时间为 3 min;流速0.3 ml/min;柱温 30 ℃;进样体积 2 μl,检测波长 254 nm。
表 1 色谱洗脱梯度
时间(t/min) A(%) B(%) 0 95 5 3 95 5 15 65 35 29 5 95 30 5 95 采用电喷雾离子源(ESI),分别在正、负离子模式下采集数据,数据采集范围 m/z 100~1 700,离子源温度 350 ℃,毛细管电压正离子为 4.0 kV,负离子为 3.5 kV,雾化气压力 45 Psi,干燥气流速 11 L/min,鞘气流速 11 L/min,鞘气温度 350 ℃,碎片电压 140 V,碰撞能量 30 V。
-
基于中国知网、Pubmed、TCMSP等中英文在线数据库网站,查询肺脾气虚汤各味药材所含化学成分,并汇总其化学成分信息,导入Agilent PCDL Manager B.08 软件构建方剂化学成分数据库。
-
将采集得到的质谱数据导入到 Agilent MassHunter Qualitative Analysis 10.0软件中,利用前期建立的肺脾气虚汤化学成分数据库初步识别其所含化学成分(绝对峰高≥2 000,匹配容差<±5 ppm),接下来对初步识别的化学成分进行进一步确认。采用对照品及MS DIAL4.70软件结合MS FINDER 3.5.2软件对数据库及离子碎片比对功能确认化合物信息[7]。
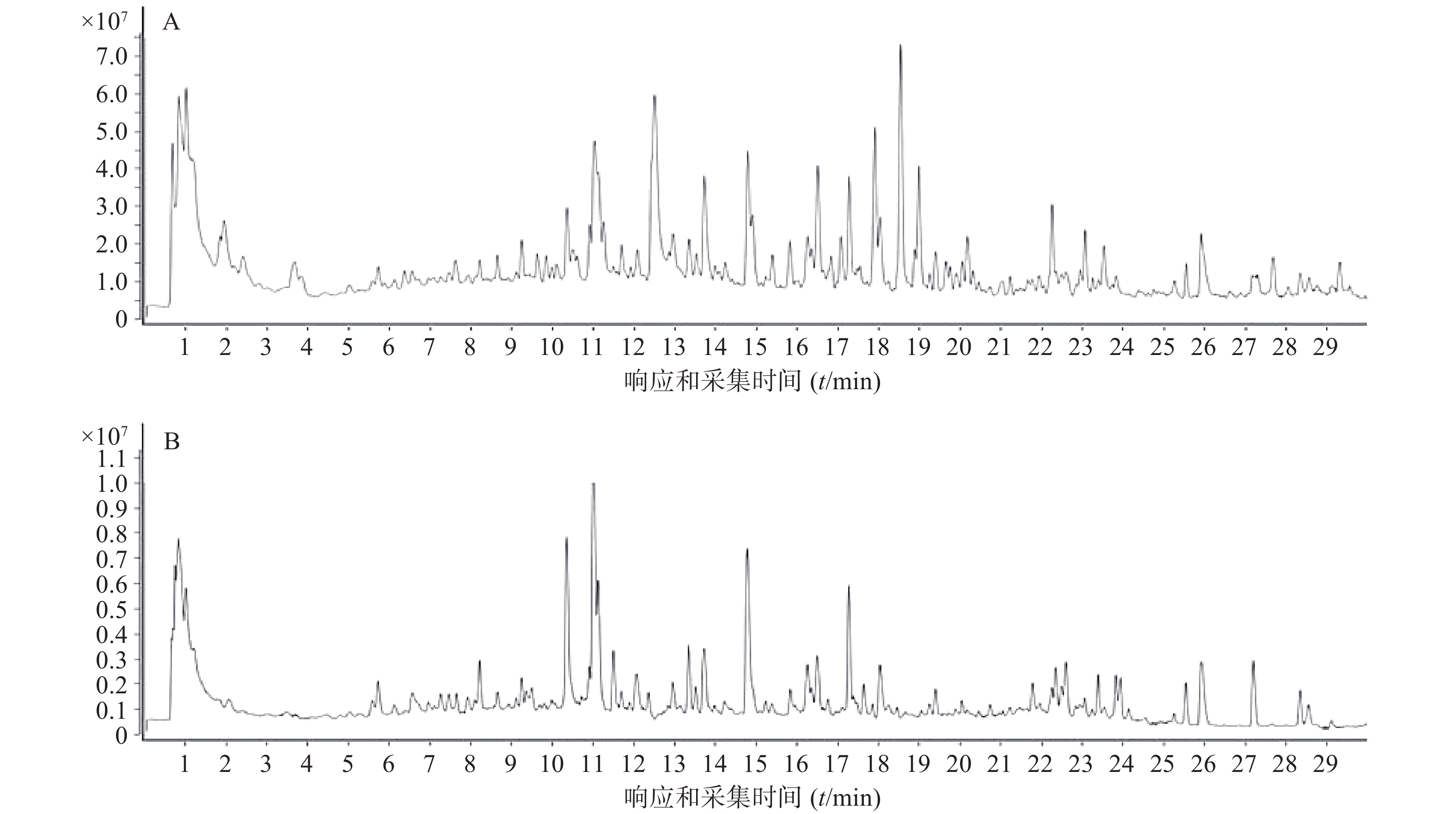
肺脾气虚汤在“2.2”及“2.4”项条件下得到的总离子流色谱图见图1。通过导入自建数据库得到肺脾气虚汤的初步鉴定结果,并进一步通过与对照品、MS FINDER数据库比对及查阅文献等方法最终共从肺脾气虚汤鉴定出56种化学成分,见表2。其中正离子模式下识别出8种化学成分,负离子模式下识别出46种化学成分。此外,大豆皂苷 I和茯苓酸在正、负两种模式下均被识别到。这些成分中有4种成分来源于法半夏[13-14],9种成分来源于陈皮,7种成分来源于党参[15-16],10种成分来源于茯苓[17-18],13种成分来源于炙黄芪[19-20],1种成分来源于藿香[21],3种成分来源于砂仁[22]。此外,也有化学成分为多个药材的共有成分,均在表格中标出。化合物来源占比最高的为炙黄芪、党参等药材,与其配伍占比相似。
表 2 肺脾气虚汤化学成分鉴定结果
编号 RT (t/min) m/z 离子模式 分子式 理论分子量 实测分子量
(Tgt)误差
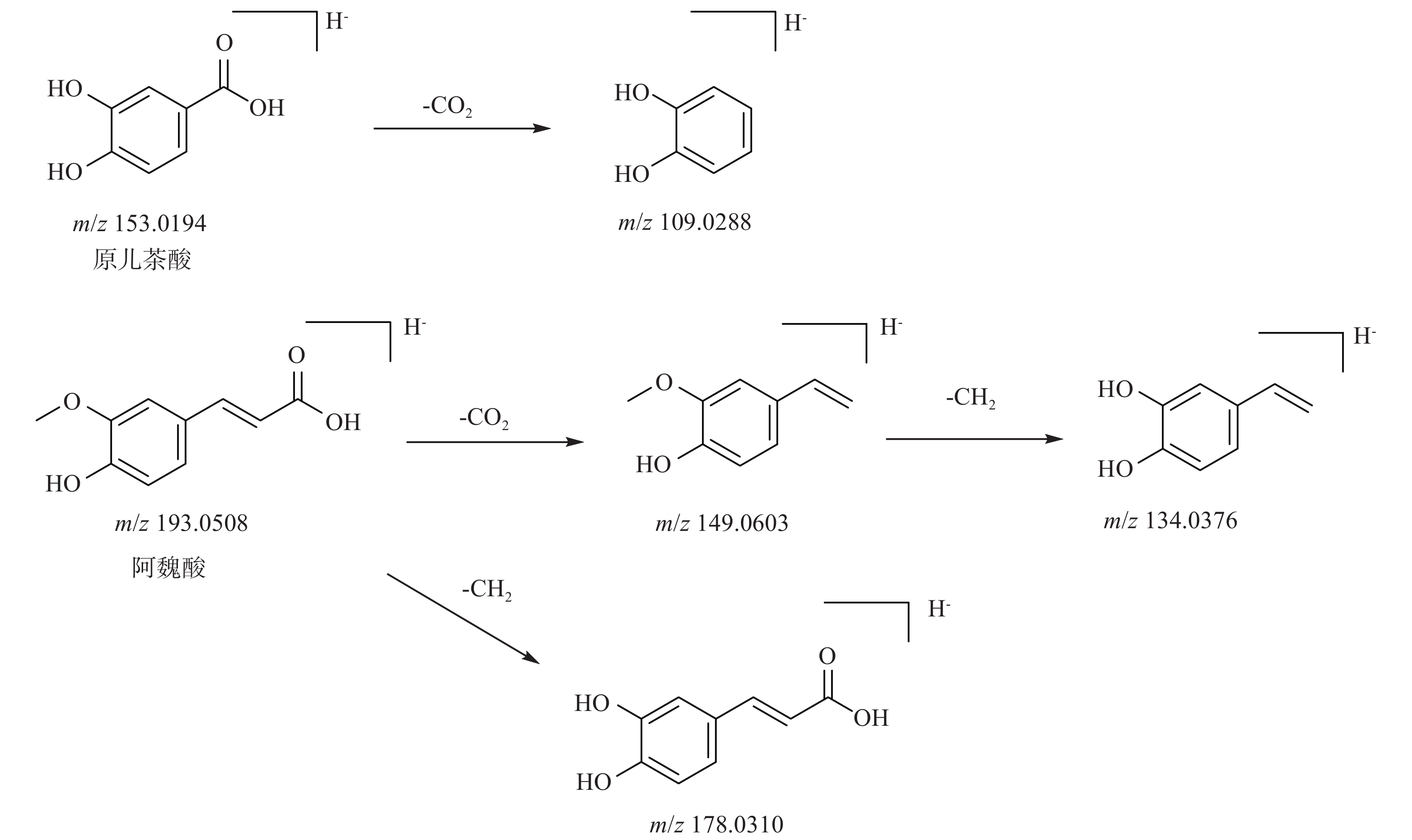
(Tgt, ppm)名称 类别 来源 1 0.702 175.1183 [M+H]+ C6H14N4O2 174.1111 174.1117 −3.57 L-精氨酸 氨基酸类 党参 2 0.766 195.0522 [M+Hac-H]−、[M-H]− C5H4N4O 136.0384 136.0385 −1.06 次黄嘌呤 生物碱类 党参,法半夏 3 1.073 282.0835 [M-H]− C10H13N5O5 283.0918 283.0917 0.45 鸟苷 生物碱类 法半夏,炙黄芪 4*# 1.153 117.0193 [M-H]− C4H6O4 118.0266 118.0266 −0.37 琥珀酸 有机酸类 党参,法半夏 5 1.807 124.0391 [M+H]+ C6H5NO2 123.0319 123.032 −1.2 烟酸 生物碱类 党参 6 1.875 284.1484 [M+H]+ C14H21NO5 283.141 283.142 −3.36 党参醇 生物碱类 党参 7 2.41 268.1534 [M+Na]+ , [M+H]+ C14H21NO4 267.1462 267.1471 −3.31 党参碱 生物碱类 党参 8* 5.723 355.1023 [M+K]+ C16 H18 O9 354.0954 354.0951 0.28 绿原酸 苯丙素类 党参,藿香,砂仁 9 5.905 169.0495 [M+K]+、[M+H]+ C8H8O4 168.0422 168.0423 −0.6 香草酸 酚类 党参,砂仁,法半夏 10 6.15 375.1294 [M-H]− C17H20N4O6 376.1366 376.1383 −4.53 核黄素 维生素类 炙黄芪 11# 7.141 153.0194 [M-H]− C7H6O4 154.0266 154.0266 0.25 原儿茶酸 酚类 藿香,砂仁 12 7.653 593.1518 [M-H]− C27H30O15 594.159 594.1585 0.87 忍冬苷 黄酮类 陈皮 13 8.211 741.2245 [M+FA-H]−、[M-H]− C33H42O19 742.2316 742.232 −0.54 柚皮苷4’-葡萄糖苷 黄酮类 陈皮 14 8.86 193.0508 [M-H]− C10H10O4 194.0581 194.0579 1.05 阿魏酸 酚酸类 党参,法半夏,炙黄芪,砂仁 15 8.917 163.0399 [M-H]− C9H8O3 164.0474 164.0473 0.32 4-羟基肉桂酸 酚类 炙黄芪 16* 9.247 609.146 [M-H]− C27H30O16 610.1531 610.1534 −0.49 芦丁 黄酮类 陈皮 17 9.35 595.1666 [M-H]− C27H32O15 596.174 596.1741 −0.24 圣草苷 黄酮类 陈皮 18 9.73 743.274 [M+Na]+ , [M+K]+ C32H48O18 720.2848 720.2841 1.05 铜锤玉带草炔苷B 聚乙炔苷 党参 19 10.033 521.13 [M+FA-H]−、[M-H]− C23H24O11 476.1313 476.1319 −1.21 奥刀拉亭-7-O-β-D-葡萄吡喃糖苷 黄酮类 炙黄芪 20# 10.294 137.0246 [M-H]− C7H6O3 138.0319 138.0317 1.67 对羟基苯甲酸 酚类 砂仁 21 10.357 579.1721 [M-H]− C27H32O14 580.1796 580.1792 0.64 柚皮芸香苷 黄酮类 陈皮 22 10.454 447.0946 [M-H]− C21H20O11 448.1022 448.1006 3.56 异红草素 黄酮类 陈皮 23 10.704 431.0988 [M-H]− C21H20O10 432.1063 432.1056 1.52 染料木苷 黄酮类 炙黄芪 24# 11.023 609.1824 [M-H]− C28H34O15 610.1899 610.1898 0.19 新橙皮苷 黄酮类 陈皮 25 11.125 359.0775 [M+FA-H]−、[M-H]− C17H14O6 314.0793 314.079 0.76 熊竹素 黄酮类 炙黄芪 26 12.833 285.041 [M-H]− C15H10O6 286.0484 286.0477 2.16 木犀草素 黄酮类 党参 27 13.334 593.1879 [M+FA-H]−、[M-H]− C28H34O14 594.1949 594.1949 0.15 香蜂草苷 黄酮类 陈皮 28 13.345 285.077 [M-H]− C16H14O5 286.0843 286.0841 0.6 甘草查尔酮B 黄酮类 炙黄芪 29 14.677 315.0875 [M-H]− C17H16O6 316.0949 316.0947 0.53 垂崖豆藤异黄烷醌 黄酮类 炙黄芪 30 15.144 163.0766 [M-H]− C10H12O2 164.084 164.0837 1.44 覆盆子酮 酚类 砂仁 31 15.896 255.0668 [M-H]− C15H12O4 256.0739 256.0736 1.26 异甘草素 黄酮类 炙黄芪,法半夏 32*# 16.761 313.072 [M+FA-H]− C16H12O4 268.0743 268.0738 0.72 芒柄花素 黄酮类 炙黄芪 33 16.396 991.5086 [M+FA-H]−、[M-H]− C47H78O19 946.5111 946.5137 −2.82 黄芪甲苷 VII 三萜类 炙黄芪 34 16.476 283.0613 [M-H]− C16H12O5 284.0686 284.0685 0.34 汉黄芩素 黄酮类 党参,炙黄芪 35 16.647 837.3905 [M-H]− C42H62O17 838.3977 838.3987 −1.2 甘草皂苷G2 三萜类 法半夏 36 16.966 297.0403 [M-H]− C16H10O6 298.0476 298.0477 −0.46 sophorophenolone 黄酮类 炙黄芪 37# 17.102 829.4583 [M+FA-H]−、[M-H]− C41H68O14 784.4599 784.4609 −1.33 黄芪甲苷 IV 三萜类 炙黄芪 38 18.241 941.5103 [M-H]− C48H78O18 942.5174 942.5188 −1.46 大豆皂苷I 三萜类 炙黄芪 18.246 943.5236 [M+H]+ C48 H78 O18 942.5149 942.5188 −4.13 大豆皂苷 I 炙黄芪 39 19.049 499.3421 [M-H]− C31H48O5 500.3495 500.3502 −1.29 茯苓酸H 三萜类 茯苓 40 19.908 891.4684 [M+Na]+ , [M+K]+ C45 H72 O16 868.4793 868.482 −3.12 黄芪甲苷 I 三萜类 炙黄芪 41# 21.531 469.3314 [M-H]− C30H46O4 470.3392 470.3396 −0.86 甘草次酸 三萜类 法半夏 42 21.793 471.3474 [M-H]− C30H48O4 472.3545 472.3553 −1.67 山楂酸 三萜类 藿香 43 21.963 541.3524 [M+Hac-H]−、[M-H]− C31H46O4 482.3382 482.3396 −2.83 猪苓酸C 三萜类 茯苓 44 22.214 483.3133 [M-H]− C30H44O5 484.3202 484.3189 2.81 茯苓酸B 三萜类 茯苓 45 22.339 483.348 [M+Hac-H]−、[M-H]− C31H48O4 484.3551 484.3553 −0.27 3-表去氢土莫酸 三萜类 茯苓 46 22.601 485.3635 [M-H]− C31H50O4 486.3706 486.3709 −0.58 块苓酸 酚类 茯苓 22.606 525.3319 [M+K]+、[M+H]+ C31 H50 O4 486.3693 486.3709 −3.31 茯苓 47 22.817 389.1231 [M-H]− C20H22O8 390.1306 390.1315 −2.23 云杉新苷 糖苷类 砂仁 48 25.242 513.3582 [M-H]− C32H50O5 514.3655 514.3658 −0.68 茯苓新酸 HM 三萜类 茯苓 49 25.527 525.3588 [M-H]− C33H50O5 526.3659 526.3658 0.15 3-表去氢茯苓酸 三萜类 茯苓 50# 25.902 527.3743 [M-H]- C33H52O5 528.3814 528.3815 −0.19 茯苓酸 三萜类 茯苓 51 25.982 455.3525 [M-H]− C30H48O3 456.3597 456.3603 −1.47 齐墩果酸 三萜类 党参 52# 27.189 279.2333 [M+FA-H]−、[M-H]− C18H32O2 280.2404 280.2402 0.62 亚油酸 脂肪酸类 党参,炙黄芪,法半夏 53# 27.394 241.2172 [M-H]− C15H30O2 242.2245 242.2246 −0.22 十五烷酸 脂肪酸类 法半夏 54 27.394 485.3265 [M-H]− C30H46O5 486.3334 486.3345 −2.31 茯苓酸G 三萜类 茯苓 55 28.339 255.2329 [M-H]− C16H32O2 256.2402 256.2402 −0.09 棕榈酸 脂肪酸类 法半夏 56# 28.532 281.2487 [M-H]− C18H34O2 282.256 282.2559 0.28 顺-10-十七碳烯酸甲酯 脂肪酸类 陈皮 注:*为通过与对照品比对确定,#为入血原形成分。 肺脾气虚汤含有多种有机酸类成分,如原儿茶酸、阿魏酸等,该类成分在质谱中易在能量的撞击下丢失CO2、CH2、CO等分子。如化合物11在7.141 min产生m/z 153.019 4[M-H]−峰,判断该化合物的分子式为C7H6O4,在二级质谱扫描下产生 m/z 109.028 8,推测其为m/z 153.019 4丢失一分子CO2产生的碎片离子,通过与对照品及MS FINDER数据库及文献综合比对,鉴定该化合物为原儿茶酸[23],裂解规律见图2。化合物14在8.86 min产生m/z 193.050 8[M-H]−的准分子离子峰,判断其分子式为C10H10O4,而二级质谱图中可观察到m/z 178.031 0、m/z 149.060 3、m/z 134.037 6等碎片离子,推测它们分别为准分子离子峰产生的[M-CH2-H]−峰、[M-CO2-H]−峰、[M-CO2-CO2-H]−峰,根据参考文献及MS FINDER数据库推测该化合物为阿魏酸[24]。
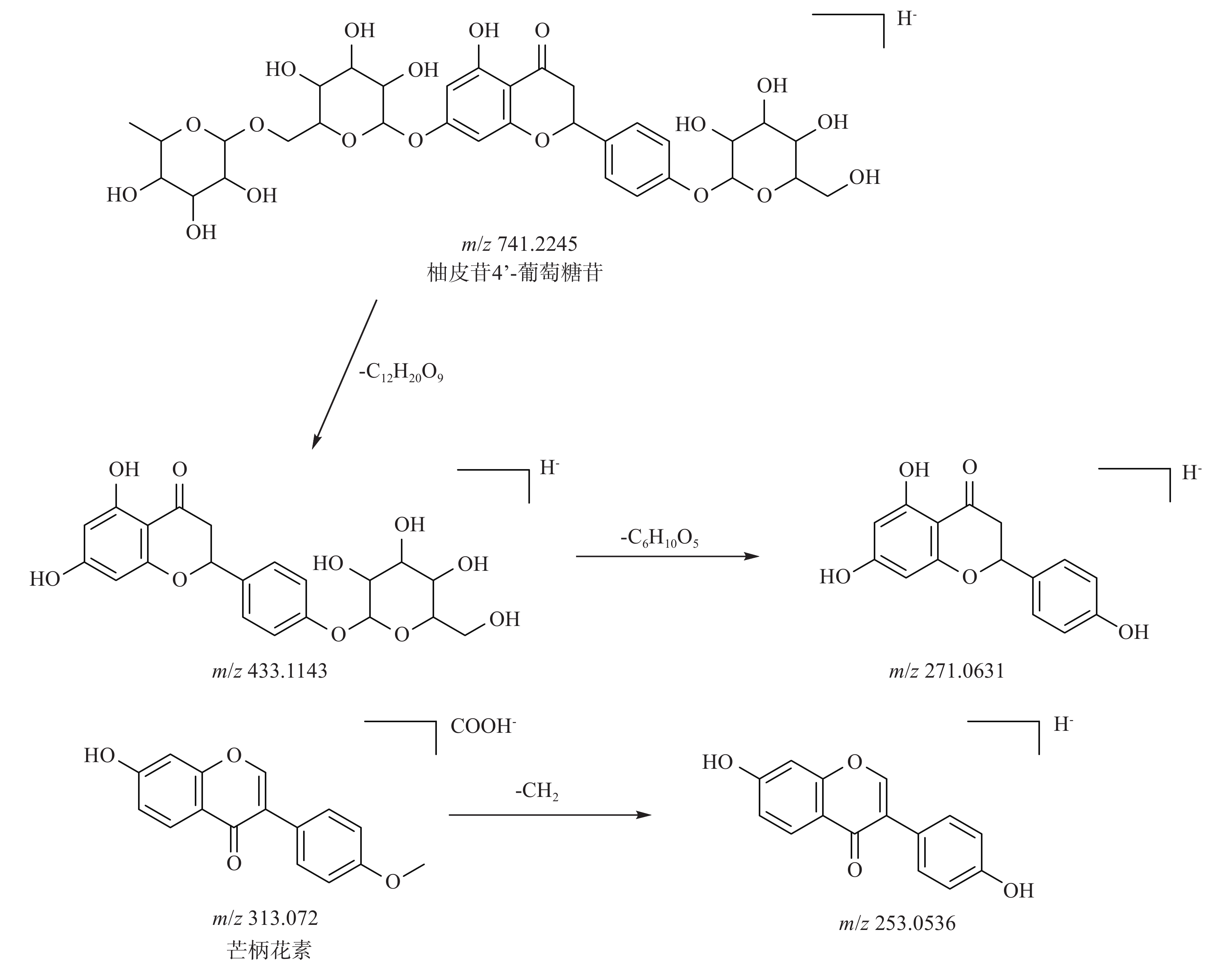
黄酮类成分为肺脾气虚汤中检测到的主要类别,该类成分易在质谱扫描下发生糖苷键的断裂、脱羰基、脱甲基及RDA裂解等[25]。如化合物13可在8.211 min观察到m/z 741.2245[M-H]−峰,判断其分子式为C33H42O19,在其质谱碎片中观察到m/z 433.1143[M-C12H20O9-H]−及m/z 271.0632[M-C12H20O9-C6H10O5-H]−,为其逐步丢失糖苷键产生的碎片离子,结合文献及MS FINDER数据库推测该化合物为柚皮苷4’-葡萄糖苷。化合物32可在16.761 min观察到其准分子离子峰m/z 313.0720,判断其分子式为C16H12O4,并观察到m/z 253.053 6,为该化合物脱去甲基产生的碎片离子[M-CH2-H]−,与对照品及MS FINDER数据库比对,鉴定该化合物为芒柄花素, 柚皮苷4’-葡萄糖苷及芒柄花素裂解规律见图3。
-
将血清样本数据导入Agilent MassHunter Qualitative Analysis 10.0软件中,并将3.1项中识别得到的化合物构建为带有保留时间的肺脾气虚汤入血成分数据库,根据化合物的保留时间及分子特征共筛选得到肺脾气虚汤的11种入血原形成分(图4,表2)。其中,茯苓酸来源于茯苓,琥珀酸来源于党参、法半夏,十五烷酸、棕榈酸来源于法半夏,原儿茶酸来源于藿香、砂仁,对羟基苯甲酸来源于砂仁,芒柄花素和黄芪甲苷IV来源于炙黄芪,新橙皮苷及顺-10-十七碳烯酸甲酯来源于陈皮,亚油酸来源于党参、炙黄芪和法半夏。
-
新冠肺炎患者恢复期常见的中医证候有肺脾气虚、气阴两虚和余邪未尽。另外,由于患者的脾胃失和气阴两虚,容易出现情志失调。肺脾气虚汤含有黄芪、党参、茯苓、陈皮、半夏、藿香、砂仁等,具有扶正祛邪、补肺固表、益气健脾、燥湿化痰、化浊除湿之功,为香砂六君子汤、参苓白术散、补中益气汤的主要组成药物[7-10]。从现代医学的角度来说,使用上述药物,可以有效防止恢复期患者出现凝血、炎症、免疫和器官功能障碍[11],以及稳定患者情绪防止病情演变的作用[12]。
根据我们的分析结果发现,入血原形成分中原儿茶酸、新橙皮苷等是具有代表性的有效成分,在现代药理学研究中均被证实有助于新冠肺炎患者的“扶正祛邪”。例如,来自于藿香的原儿茶酸由于具有多个酚羟基,已经被实验证实具有抑制蛋白酶3CLpro的功能[26],发挥抗炎活性[27];还可以通过改善海马和大脑皮层中的神经递质、内分泌因子改善抑郁大鼠的行为和神经生化改变[28]。新橙皮苷是黄酮类化合物的主要活性成分,具有很强的抗炎、抗氧化特性,以及神经保护和安神作用[29],近期研究表明其由于具有与人类AAK1蛋白和SARS-CoV-2 NSP16蛋白结合的潜力,被作为一种潜在的双重活性成分而受到关注[30-31]。黄芪甲苷 IV是黄芪的主要活性成分,在机体免疫系统、循环系统、泌尿系统、内分泌系统等多种系统具有正向调节作用[32-33]。上述成分经口服被吸收入血在体内进行循环,证实了方剂多成分多途径发挥功效的特点,是肺脾气虚汤发挥药效的物质基础。
-
本研究首次运用UHPLC-Q-TOF/MS 对肺脾气虚汤的化学成分和入血成分进行分析,所鉴别出的化合物为其发挥药效的物质基础,该方法准确性高、稳定性好、灵敏度高、分析时间短,证实了基于入血成分的活性成分识别是一种筛选中药活性物质的快速有效方法。
Identification of chemical constituents and blood-absorbed ingredients of FeiPi QiXu decoction by UHPLC-Q-TOF/MS
-
摘要:
目的 对肺脾气虚汤中的主要化学成分及SD大鼠口服后的入血成分进行鉴定,为分析其药效物质基础提供参考。 方法 采用超高效液相色谱-四级杆飞行时间串联质谱(UHPLC-Q-TOF/MS)技术对肺脾气虚汤提取液及SD大鼠口服肺脾气虚汤后的血清样本进行数据采集,并通过对照品、自建质谱数据库、MS FINDER数据库及查阅文献对其化学成分及入血成分进行快速鉴定。 结果 共从肺脾气虚汤中鉴定出56种化学成分,主要为黄酮类、三萜类、酚类成分,化合物大多来源于炙黄芪、陈皮、茯苓和党参;含药血清中检测到 11 种原形成分,包含芒柄花素、黄芪甲苷 IV和新橙皮苷等化合物。 结论 该研究较为全面的阐明了肺脾气虚汤化学成分组成及药材来源,并初步分析了其入血成分,为进一步对该方的药效物质基础及质量控制研究提供了科学依据。 -
关键词:
- 肺脾气虚汤 /
- UHPLC-Q-TOF/MS /
- 化学成分 /
- 入血成分
Abstract:Objective To identify the chemical constituents and blood-absorbed ingredients of FeiPi QiXu decoction, and provide reference for clarifying the material basis of its efficacy. Methods An ultrahigh performance liquid chromatography-quadrupole-time of flight-mass spectrometry (UHPLC-Q-TOF/MS) method was applied to analyze the data of FeiPi QiXu decoction extraction and the serum samples of SD rats after oral administration. The chemical constituents and blood-absorbed ingredients were quickly identified by chemical reference substance, self-built mass spectrometry database, MSFINDER database and the relevant literature. Results A total of 56 chemical constituents were identified from Feiqi Deficiency Decoction, mainly were flavonoids, triterpenoids and phenols. Most of the compounds came from Radix Astragali praeparata cum melle, Citri Reticulatae Pericarpium, Poria and Codonopsis Radix. 11 prototype compounds were identified in the serum, including Formononetin, Astragaloside IV and Neohesperidin. Conclusion This study comprehensively clarified the chemical composition and source of medicinal materials, and preliminarily analyzed its blood-absorbed ingredients, which could provide a scientific basis for further study on the pharmacodynamic material basis and quality control of FeiPi QiXu decoction. -
肺脾气虚汤由法半夏,陈皮,党参,炙黄芪,茯苓,藿香,砂仁等七味中药组成,其中,炙黄芪、党参共为君药,补肺脾之气,益卫固表,法半夏、陈皮、茯苓,健脾祛湿,化痰利肺是为臣药,藿香芳香化浊,辟秽和中,是为佐药,砂仁行气调中,和胃醒脾,为使药。作为从第4版新型冠状病毒感染肺炎诊疗方案便被纳入中医治疗方案的方剂之一,该方主治新冠患者恢复期出现的肺脾气虚证,对气短、倦怠乏力、纳差呕恶、痞满、大便无力、便溏不爽、舌淡胖、苔白腻等症状具有良好疗效[1]。但治疗新冠的中药方剂均由多味中药组成,化学成分复杂,目前诸多文献均侧重于基于公开数据库查询方剂组成的各个药味所含的化合物开展网络药理学研究[2-5],而没有对方剂的化学成分群进行系统考察。其次,中药复方体内与体外之间化学成分具有重要关联,针对复方进入机体内的化学成分群进行分析是有助于发现活性物质的有效手段[6]。
目前尚未见肺脾气虚汤的化学成分及入血成分研究的报道,因此本研究通过UHPLC-Q-TOF/MS技术首次对肺脾气虚汤所含化学成分进行快速分析鉴定,并对化学成分的药材来源进行归属,在此基础上开展其血中药源性成分的辨识,以期为进一步阐明肺脾气虚汤的活性成分,并为今后质量控制提供科学依据。
1. 仪器与试剂
1.1 仪器
超高效液相色谱-四极杆-飞行时间质谱仪(UHPLC-Q-TOF/MS)购自美国安捷伦公司,包含1290 Infinity型UHPLC及6530型Q-TOF/MS系统;CPA255D型1/10万电子天平购自德国Sartorius公司;Lyovapor L-200型冷冻干燥机购自瑞士Buchi公司;Centrifuge 5810R 高速台式冷冻离心机购自德国Eppendorf公司;SK7200H型超声波清洗器购自上海科导超声仪器有限公司;Milli-Q型纯化水系统购自美国Millipore公司;HC-800Y高速多功能粉碎机购自武义海纳电器有限公司。
1.2 药品与试剂
法半夏(批号191115042)、陈皮(批号19090603)、党参(批号19102901)、炙黄芪(批号19650710)、茯苓(批号19122304)、藿香(批号19051410)、砂仁(批号19102211)等饮片均购自吴江上海蔡同德堂中药饮片有限公司,以上样品均经上海中医药大学陈万生教授鉴定为正品。
琥珀酸(批号A0727AS)、绿原酸(批号J0120AS)、芦丁(批号O0714AS)、芒柄花素(批号N0301AS)等对照品均购自大连美仑生物技术有限公司(纯度>97.0 %)。甲醇、乙腈为质谱纯(德国 Merck 公司);甲酸为质谱纯(美国 Thermo Fisher公司);超纯水由MILI-Q净水系统制备(美国Millipore公司);其他均为分析纯试剂。
1.3 动物
本研究所用动物为8周龄雄性SD大鼠,SPF级,购自上海市计划生育科学研究所实验动物经营部(合格证编号20180006021172),大鼠饲养于温度(22~26 ℃)、湿度(40%~70%)、12 h明暗循环可控的室内环境,可自由进食饮水。
2. 试验方法
2.1 对照品溶液的制备
精密称取琥珀酸,加入超纯水配置成浓度为1.0 mg/ml的对照品储备液,分别精密称取绿原酸、芦丁、芒柄花素各对照品适量,加入含5% DMSO的甲醇分别配置成浓度为1.0 mg/ml的对照品储备液,所有储备液配制完成后均放于−20 ℃冰箱保存备用。精密吸取上述储备溶液各10 μl,置于1.5 ml离心管中,加入甲醇,涡旋混匀,配制成各对照品浓度均为10 μg/ml 的混合对照品溶液。
2.2 供试品溶液的制备
将方剂所有药材冷冻干燥,用高速粉碎机分别打粉并过四号筛,并按处方比例混合,精密称取约0.500 g,置于100 ml具塞锥形瓶中,精密加入10倍体积70 %甲醇,密塞、称定重量,超声波提取法提取(760 W,50 kHz)30 min,冷却,70 %甲醇补足失重,滤过,3 000 r/min离心10 min,取1.0 ml上清液于1.5 ml EP管中,12 000 r/min离心 10 min,取200 μl上清液于进样小瓶中,待进样分析。另取方剂10倍体积纯净水浸泡过夜,回流提取1.5 h后用纱布过滤,药渣用8倍体积水继续回流提取1 h,过滤并离心,合并上清液,减压浓缩,得到浸膏供入血成分分析研究。
2.3 血清样本的制备和前处理
SD大鼠给药前适应性喂养1周后,随机分为2组,即空白对照组与肺脾气虚汤给药组,每组6只。给药组大鼠灌胃给予方剂提取物(10倍临床给药剂量),空白对照组大鼠灌胃给予等体积水。给药1 h后眼眶静脉丛取血1.5 ml于5 ml促凝管中, 室温下静置2 h,4 °C下3 000 r/min离心10 min,取100 μl血清于1.5 ml EP管中,加入4倍体积甲醇,涡旋混匀1 min,4 ℃ 12 000 r/min离心15 min,取上清液,真空冷冻干燥后,加入100 μl 80% 甲醇复溶,涡旋混匀1 min,4 ℃ 12 000 r/min离心15 min,取上清液进行检测。
2.4 UHPLC-Q-TOF/MS分析条件
色谱柱:Waters ACQUITY UPLC BEH C18 色谱柱(2.1 mm×100 mm,1.7 μm);流动相:0.1 %甲酸水(A)-乙腈(B),色谱洗脱梯度见表1,后运行时间为 3 min;流速0.3 ml/min;柱温 30 ℃;进样体积 2 μl,检测波长 254 nm。
表 1 色谱洗脱梯度时间(t/min) A(%) B(%) 0 95 5 3 95 5 15 65 35 29 5 95 30 5 95 采用电喷雾离子源(ESI),分别在正、负离子模式下采集数据,数据采集范围 m/z 100~1 700,离子源温度 350 ℃,毛细管电压正离子为 4.0 kV,负离子为 3.5 kV,雾化气压力 45 Psi,干燥气流速 11 L/min,鞘气流速 11 L/min,鞘气温度 350 ℃,碎片电压 140 V,碰撞能量 30 V。
2.5 肺脾气虚汤化学成分数据库的建立
基于中国知网、Pubmed、TCMSP等中英文在线数据库网站,查询肺脾气虚汤各味药材所含化学成分,并汇总其化学成分信息,导入Agilent PCDL Manager B.08 软件构建方剂化学成分数据库。
3. 结果
3.1 肺脾气虚汤的化学成分鉴定结果
将采集得到的质谱数据导入到 Agilent MassHunter Qualitative Analysis 10.0软件中,利用前期建立的肺脾气虚汤化学成分数据库初步识别其所含化学成分(绝对峰高≥2 000,匹配容差<±5 ppm),接下来对初步识别的化学成分进行进一步确认。采用对照品及MS DIAL4.70软件结合MS FINDER 3.5.2软件对数据库及离子碎片比对功能确认化合物信息[7]。
肺脾气虚汤在“2.2”及“2.4”项条件下得到的总离子流色谱图见图1。通过导入自建数据库得到肺脾气虚汤的初步鉴定结果,并进一步通过与对照品、MS FINDER数据库比对及查阅文献等方法最终共从肺脾气虚汤鉴定出56种化学成分,见表2。其中正离子模式下识别出8种化学成分,负离子模式下识别出46种化学成分。此外,大豆皂苷 I和茯苓酸在正、负两种模式下均被识别到。这些成分中有4种成分来源于法半夏[13-14],9种成分来源于陈皮,7种成分来源于党参[15-16],10种成分来源于茯苓[17-18],13种成分来源于炙黄芪[19-20],1种成分来源于藿香[21],3种成分来源于砂仁[22]。此外,也有化学成分为多个药材的共有成分,均在表格中标出。化合物来源占比最高的为炙黄芪、党参等药材,与其配伍占比相似。
表 2 肺脾气虚汤化学成分鉴定结果编号 RT (t/min) m/z 离子模式 分子式 理论分子量 实测分子量
(Tgt)误差
(Tgt, ppm)名称 类别 来源 1 0.702 175.1183 [M+H]+ C6H14N4O2 174.1111 174.1117 −3.57 L-精氨酸 氨基酸类 党参 2 0.766 195.0522 [M+Hac-H]−、[M-H]− C5H4N4O 136.0384 136.0385 −1.06 次黄嘌呤 生物碱类 党参,法半夏 3 1.073 282.0835 [M-H]− C10H13N5O5 283.0918 283.0917 0.45 鸟苷 生物碱类 法半夏,炙黄芪 4*# 1.153 117.0193 [M-H]− C4H6O4 118.0266 118.0266 −0.37 琥珀酸 有机酸类 党参,法半夏 5 1.807 124.0391 [M+H]+ C6H5NO2 123.0319 123.032 −1.2 烟酸 生物碱类 党参 6 1.875 284.1484 [M+H]+ C14H21NO5 283.141 283.142 −3.36 党参醇 生物碱类 党参 7 2.41 268.1534 [M+Na]+ , [M+H]+ C14H21NO4 267.1462 267.1471 −3.31 党参碱 生物碱类 党参 8* 5.723 355.1023 [M+K]+ C16 H18 O9 354.0954 354.0951 0.28 绿原酸 苯丙素类 党参,藿香,砂仁 9 5.905 169.0495 [M+K]+、[M+H]+ C8H8O4 168.0422 168.0423 −0.6 香草酸 酚类 党参,砂仁,法半夏 10 6.15 375.1294 [M-H]− C17H20N4O6 376.1366 376.1383 −4.53 核黄素 维生素类 炙黄芪 11# 7.141 153.0194 [M-H]− C7H6O4 154.0266 154.0266 0.25 原儿茶酸 酚类 藿香,砂仁 12 7.653 593.1518 [M-H]− C27H30O15 594.159 594.1585 0.87 忍冬苷 黄酮类 陈皮 13 8.211 741.2245 [M+FA-H]−、[M-H]− C33H42O19 742.2316 742.232 −0.54 柚皮苷4’-葡萄糖苷 黄酮类 陈皮 14 8.86 193.0508 [M-H]− C10H10O4 194.0581 194.0579 1.05 阿魏酸 酚酸类 党参,法半夏,炙黄芪,砂仁 15 8.917 163.0399 [M-H]− C9H8O3 164.0474 164.0473 0.32 4-羟基肉桂酸 酚类 炙黄芪 16* 9.247 609.146 [M-H]− C27H30O16 610.1531 610.1534 −0.49 芦丁 黄酮类 陈皮 17 9.35 595.1666 [M-H]− C27H32O15 596.174 596.1741 −0.24 圣草苷 黄酮类 陈皮 18 9.73 743.274 [M+Na]+ , [M+K]+ C32H48O18 720.2848 720.2841 1.05 铜锤玉带草炔苷B 聚乙炔苷 党参 19 10.033 521.13 [M+FA-H]−、[M-H]− C23H24O11 476.1313 476.1319 −1.21 奥刀拉亭-7-O-β-D-葡萄吡喃糖苷 黄酮类 炙黄芪 20# 10.294 137.0246 [M-H]− C7H6O3 138.0319 138.0317 1.67 对羟基苯甲酸 酚类 砂仁 21 10.357 579.1721 [M-H]− C27H32O14 580.1796 580.1792 0.64 柚皮芸香苷 黄酮类 陈皮 22 10.454 447.0946 [M-H]− C21H20O11 448.1022 448.1006 3.56 异红草素 黄酮类 陈皮 23 10.704 431.0988 [M-H]− C21H20O10 432.1063 432.1056 1.52 染料木苷 黄酮类 炙黄芪 24# 11.023 609.1824 [M-H]− C28H34O15 610.1899 610.1898 0.19 新橙皮苷 黄酮类 陈皮 25 11.125 359.0775 [M+FA-H]−、[M-H]− C17H14O6 314.0793 314.079 0.76 熊竹素 黄酮类 炙黄芪 26 12.833 285.041 [M-H]− C15H10O6 286.0484 286.0477 2.16 木犀草素 黄酮类 党参 27 13.334 593.1879 [M+FA-H]−、[M-H]− C28H34O14 594.1949 594.1949 0.15 香蜂草苷 黄酮类 陈皮 28 13.345 285.077 [M-H]− C16H14O5 286.0843 286.0841 0.6 甘草查尔酮B 黄酮类 炙黄芪 29 14.677 315.0875 [M-H]− C17H16O6 316.0949 316.0947 0.53 垂崖豆藤异黄烷醌 黄酮类 炙黄芪 30 15.144 163.0766 [M-H]− C10H12O2 164.084 164.0837 1.44 覆盆子酮 酚类 砂仁 31 15.896 255.0668 [M-H]− C15H12O4 256.0739 256.0736 1.26 异甘草素 黄酮类 炙黄芪,法半夏 32*# 16.761 313.072 [M+FA-H]− C16H12O4 268.0743 268.0738 0.72 芒柄花素 黄酮类 炙黄芪 33 16.396 991.5086 [M+FA-H]−、[M-H]− C47H78O19 946.5111 946.5137 −2.82 黄芪甲苷 VII 三萜类 炙黄芪 34 16.476 283.0613 [M-H]− C16H12O5 284.0686 284.0685 0.34 汉黄芩素 黄酮类 党参,炙黄芪 35 16.647 837.3905 [M-H]− C42H62O17 838.3977 838.3987 −1.2 甘草皂苷G2 三萜类 法半夏 36 16.966 297.0403 [M-H]− C16H10O6 298.0476 298.0477 −0.46 sophorophenolone 黄酮类 炙黄芪 37# 17.102 829.4583 [M+FA-H]−、[M-H]− C41H68O14 784.4599 784.4609 −1.33 黄芪甲苷 IV 三萜类 炙黄芪 38 18.241 941.5103 [M-H]− C48H78O18 942.5174 942.5188 −1.46 大豆皂苷I 三萜类 炙黄芪 18.246 943.5236 [M+H]+ C48 H78 O18 942.5149 942.5188 −4.13 大豆皂苷 I 炙黄芪 39 19.049 499.3421 [M-H]− C31H48O5 500.3495 500.3502 −1.29 茯苓酸H 三萜类 茯苓 40 19.908 891.4684 [M+Na]+ , [M+K]+ C45 H72 O16 868.4793 868.482 −3.12 黄芪甲苷 I 三萜类 炙黄芪 41# 21.531 469.3314 [M-H]− C30H46O4 470.3392 470.3396 −0.86 甘草次酸 三萜类 法半夏 42 21.793 471.3474 [M-H]− C30H48O4 472.3545 472.3553 −1.67 山楂酸 三萜类 藿香 43 21.963 541.3524 [M+Hac-H]−、[M-H]− C31H46O4 482.3382 482.3396 −2.83 猪苓酸C 三萜类 茯苓 44 22.214 483.3133 [M-H]− C30H44O5 484.3202 484.3189 2.81 茯苓酸B 三萜类 茯苓 45 22.339 483.348 [M+Hac-H]−、[M-H]− C31H48O4 484.3551 484.3553 −0.27 3-表去氢土莫酸 三萜类 茯苓 46 22.601 485.3635 [M-H]− C31H50O4 486.3706 486.3709 −0.58 块苓酸 酚类 茯苓 22.606 525.3319 [M+K]+、[M+H]+ C31 H50 O4 486.3693 486.3709 −3.31 茯苓 47 22.817 389.1231 [M-H]− C20H22O8 390.1306 390.1315 −2.23 云杉新苷 糖苷类 砂仁 48 25.242 513.3582 [M-H]− C32H50O5 514.3655 514.3658 −0.68 茯苓新酸 HM 三萜类 茯苓 49 25.527 525.3588 [M-H]− C33H50O5 526.3659 526.3658 0.15 3-表去氢茯苓酸 三萜类 茯苓 50# 25.902 527.3743 [M-H]- C33H52O5 528.3814 528.3815 −0.19 茯苓酸 三萜类 茯苓 51 25.982 455.3525 [M-H]− C30H48O3 456.3597 456.3603 −1.47 齐墩果酸 三萜类 党参 52# 27.189 279.2333 [M+FA-H]−、[M-H]− C18H32O2 280.2404 280.2402 0.62 亚油酸 脂肪酸类 党参,炙黄芪,法半夏 53# 27.394 241.2172 [M-H]− C15H30O2 242.2245 242.2246 −0.22 十五烷酸 脂肪酸类 法半夏 54 27.394 485.3265 [M-H]− C30H46O5 486.3334 486.3345 −2.31 茯苓酸G 三萜类 茯苓 55 28.339 255.2329 [M-H]− C16H32O2 256.2402 256.2402 −0.09 棕榈酸 脂肪酸类 法半夏 56# 28.532 281.2487 [M-H]− C18H34O2 282.256 282.2559 0.28 顺-10-十七碳烯酸甲酯 脂肪酸类 陈皮 注:*为通过与对照品比对确定,#为入血原形成分。 肺脾气虚汤含有多种有机酸类成分,如原儿茶酸、阿魏酸等,该类成分在质谱中易在能量的撞击下丢失CO2、CH2、CO等分子。如化合物11在7.141 min产生m/z 153.019 4[M-H]−峰,判断该化合物的分子式为C7H6O4,在二级质谱扫描下产生 m/z 109.028 8,推测其为m/z 153.019 4丢失一分子CO2产生的碎片离子,通过与对照品及MS FINDER数据库及文献综合比对,鉴定该化合物为原儿茶酸[23],裂解规律见图2。化合物14在8.86 min产生m/z 193.050 8[M-H]−的准分子离子峰,判断其分子式为C10H10O4,而二级质谱图中可观察到m/z 178.031 0、m/z 149.060 3、m/z 134.037 6等碎片离子,推测它们分别为准分子离子峰产生的[M-CH2-H]−峰、[M-CO2-H]−峰、[M-CO2-CO2-H]−峰,根据参考文献及MS FINDER数据库推测该化合物为阿魏酸[24]。
黄酮类成分为肺脾气虚汤中检测到的主要类别,该类成分易在质谱扫描下发生糖苷键的断裂、脱羰基、脱甲基及RDA裂解等[25]。如化合物13可在8.211 min观察到m/z 741.2245[M-H]−峰,判断其分子式为C33H42O19,在其质谱碎片中观察到m/z 433.1143[M-C12H20O9-H]−及m/z 271.0632[M-C12H20O9-C6H10O5-H]−,为其逐步丢失糖苷键产生的碎片离子,结合文献及MS FINDER数据库推测该化合物为柚皮苷4’-葡萄糖苷。化合物32可在16.761 min观察到其准分子离子峰m/z 313.0720,判断其分子式为C16H12O4,并观察到m/z 253.053 6,为该化合物脱去甲基产生的碎片离子[M-CH2-H]−,与对照品及MS FINDER数据库比对,鉴定该化合物为芒柄花素, 柚皮苷4’-葡萄糖苷及芒柄花素裂解规律见图3。
3.2 肺脾气虚汤的入血成分鉴定
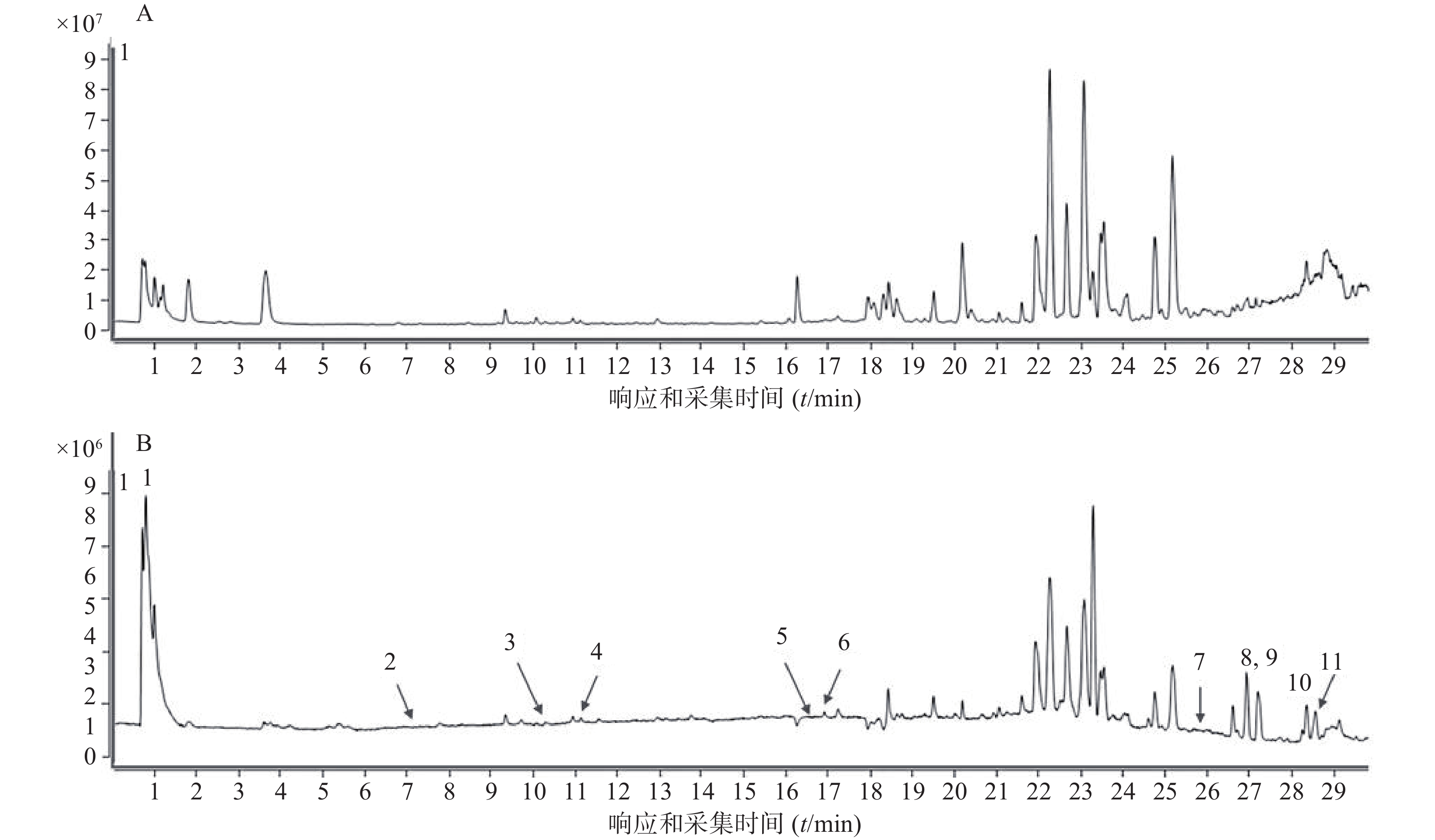
将血清样本数据导入Agilent MassHunter Qualitative Analysis 10.0软件中,并将3.1项中识别得到的化合物构建为带有保留时间的肺脾气虚汤入血成分数据库,根据化合物的保留时间及分子特征共筛选得到肺脾气虚汤的11种入血原形成分(图4,表2)。其中,茯苓酸来源于茯苓,琥珀酸来源于党参、法半夏,十五烷酸、棕榈酸来源于法半夏,原儿茶酸来源于藿香、砂仁,对羟基苯甲酸来源于砂仁,芒柄花素和黄芪甲苷IV来源于炙黄芪,新橙皮苷及顺-10-十七碳烯酸甲酯来源于陈皮,亚油酸来源于党参、炙黄芪和法半夏。
4. 讨论
新冠肺炎患者恢复期常见的中医证候有肺脾气虚、气阴两虚和余邪未尽。另外,由于患者的脾胃失和气阴两虚,容易出现情志失调。肺脾气虚汤含有黄芪、党参、茯苓、陈皮、半夏、藿香、砂仁等,具有扶正祛邪、补肺固表、益气健脾、燥湿化痰、化浊除湿之功,为香砂六君子汤、参苓白术散、补中益气汤的主要组成药物[7-10]。从现代医学的角度来说,使用上述药物,可以有效防止恢复期患者出现凝血、炎症、免疫和器官功能障碍[11],以及稳定患者情绪防止病情演变的作用[12]。
根据我们的分析结果发现,入血原形成分中原儿茶酸、新橙皮苷等是具有代表性的有效成分,在现代药理学研究中均被证实有助于新冠肺炎患者的“扶正祛邪”。例如,来自于藿香的原儿茶酸由于具有多个酚羟基,已经被实验证实具有抑制蛋白酶3CLpro的功能[26],发挥抗炎活性[27];还可以通过改善海马和大脑皮层中的神经递质、内分泌因子改善抑郁大鼠的行为和神经生化改变[28]。新橙皮苷是黄酮类化合物的主要活性成分,具有很强的抗炎、抗氧化特性,以及神经保护和安神作用[29],近期研究表明其由于具有与人类AAK1蛋白和SARS-CoV-2 NSP16蛋白结合的潜力,被作为一种潜在的双重活性成分而受到关注[30-31]。黄芪甲苷 IV是黄芪的主要活性成分,在机体免疫系统、循环系统、泌尿系统、内分泌系统等多种系统具有正向调节作用[32-33]。上述成分经口服被吸收入血在体内进行循环,证实了方剂多成分多途径发挥功效的特点,是肺脾气虚汤发挥药效的物质基础。
5. 结论
本研究首次运用UHPLC-Q-TOF/MS 对肺脾气虚汤的化学成分和入血成分进行分析,所鉴别出的化合物为其发挥药效的物质基础,该方法准确性高、稳定性好、灵敏度高、分析时间短,证实了基于入血成分的活性成分识别是一种筛选中药活性物质的快速有效方法。
-
表 1 色谱洗脱梯度
时间(t/min) A(%) B(%) 0 95 5 3 95 5 15 65 35 29 5 95 30 5 95 表 2 肺脾气虚汤化学成分鉴定结果
编号 RT (t/min) m/z 离子模式 分子式 理论分子量 实测分子量
(Tgt)误差
(Tgt, ppm)名称 类别 来源 1 0.702 175.1183 [M+H]+ C6H14N4O2 174.1111 174.1117 −3.57 L-精氨酸 氨基酸类 党参 2 0.766 195.0522 [M+Hac-H]−、[M-H]− C5H4N4O 136.0384 136.0385 −1.06 次黄嘌呤 生物碱类 党参,法半夏 3 1.073 282.0835 [M-H]− C10H13N5O5 283.0918 283.0917 0.45 鸟苷 生物碱类 法半夏,炙黄芪 4*# 1.153 117.0193 [M-H]− C4H6O4 118.0266 118.0266 −0.37 琥珀酸 有机酸类 党参,法半夏 5 1.807 124.0391 [M+H]+ C6H5NO2 123.0319 123.032 −1.2 烟酸 生物碱类 党参 6 1.875 284.1484 [M+H]+ C14H21NO5 283.141 283.142 −3.36 党参醇 生物碱类 党参 7 2.41 268.1534 [M+Na]+ , [M+H]+ C14H21NO4 267.1462 267.1471 −3.31 党参碱 生物碱类 党参 8* 5.723 355.1023 [M+K]+ C16 H18 O9 354.0954 354.0951 0.28 绿原酸 苯丙素类 党参,藿香,砂仁 9 5.905 169.0495 [M+K]+、[M+H]+ C8H8O4 168.0422 168.0423 −0.6 香草酸 酚类 党参,砂仁,法半夏 10 6.15 375.1294 [M-H]− C17H20N4O6 376.1366 376.1383 −4.53 核黄素 维生素类 炙黄芪 11# 7.141 153.0194 [M-H]− C7H6O4 154.0266 154.0266 0.25 原儿茶酸 酚类 藿香,砂仁 12 7.653 593.1518 [M-H]− C27H30O15 594.159 594.1585 0.87 忍冬苷 黄酮类 陈皮 13 8.211 741.2245 [M+FA-H]−、[M-H]− C33H42O19 742.2316 742.232 −0.54 柚皮苷4’-葡萄糖苷 黄酮类 陈皮 14 8.86 193.0508 [M-H]− C10H10O4 194.0581 194.0579 1.05 阿魏酸 酚酸类 党参,法半夏,炙黄芪,砂仁 15 8.917 163.0399 [M-H]− C9H8O3 164.0474 164.0473 0.32 4-羟基肉桂酸 酚类 炙黄芪 16* 9.247 609.146 [M-H]− C27H30O16 610.1531 610.1534 −0.49 芦丁 黄酮类 陈皮 17 9.35 595.1666 [M-H]− C27H32O15 596.174 596.1741 −0.24 圣草苷 黄酮类 陈皮 18 9.73 743.274 [M+Na]+ , [M+K]+ C32H48O18 720.2848 720.2841 1.05 铜锤玉带草炔苷B 聚乙炔苷 党参 19 10.033 521.13 [M+FA-H]−、[M-H]− C23H24O11 476.1313 476.1319 −1.21 奥刀拉亭-7-O-β-D-葡萄吡喃糖苷 黄酮类 炙黄芪 20# 10.294 137.0246 [M-H]− C7H6O3 138.0319 138.0317 1.67 对羟基苯甲酸 酚类 砂仁 21 10.357 579.1721 [M-H]− C27H32O14 580.1796 580.1792 0.64 柚皮芸香苷 黄酮类 陈皮 22 10.454 447.0946 [M-H]− C21H20O11 448.1022 448.1006 3.56 异红草素 黄酮类 陈皮 23 10.704 431.0988 [M-H]− C21H20O10 432.1063 432.1056 1.52 染料木苷 黄酮类 炙黄芪 24# 11.023 609.1824 [M-H]− C28H34O15 610.1899 610.1898 0.19 新橙皮苷 黄酮类 陈皮 25 11.125 359.0775 [M+FA-H]−、[M-H]− C17H14O6 314.0793 314.079 0.76 熊竹素 黄酮类 炙黄芪 26 12.833 285.041 [M-H]− C15H10O6 286.0484 286.0477 2.16 木犀草素 黄酮类 党参 27 13.334 593.1879 [M+FA-H]−、[M-H]− C28H34O14 594.1949 594.1949 0.15 香蜂草苷 黄酮类 陈皮 28 13.345 285.077 [M-H]− C16H14O5 286.0843 286.0841 0.6 甘草查尔酮B 黄酮类 炙黄芪 29 14.677 315.0875 [M-H]− C17H16O6 316.0949 316.0947 0.53 垂崖豆藤异黄烷醌 黄酮类 炙黄芪 30 15.144 163.0766 [M-H]− C10H12O2 164.084 164.0837 1.44 覆盆子酮 酚类 砂仁 31 15.896 255.0668 [M-H]− C15H12O4 256.0739 256.0736 1.26 异甘草素 黄酮类 炙黄芪,法半夏 32*# 16.761 313.072 [M+FA-H]− C16H12O4 268.0743 268.0738 0.72 芒柄花素 黄酮类 炙黄芪 33 16.396 991.5086 [M+FA-H]−、[M-H]− C47H78O19 946.5111 946.5137 −2.82 黄芪甲苷 VII 三萜类 炙黄芪 34 16.476 283.0613 [M-H]− C16H12O5 284.0686 284.0685 0.34 汉黄芩素 黄酮类 党参,炙黄芪 35 16.647 837.3905 [M-H]− C42H62O17 838.3977 838.3987 −1.2 甘草皂苷G2 三萜类 法半夏 36 16.966 297.0403 [M-H]− C16H10O6 298.0476 298.0477 −0.46 sophorophenolone 黄酮类 炙黄芪 37# 17.102 829.4583 [M+FA-H]−、[M-H]− C41H68O14 784.4599 784.4609 −1.33 黄芪甲苷 IV 三萜类 炙黄芪 38 18.241 941.5103 [M-H]− C48H78O18 942.5174 942.5188 −1.46 大豆皂苷I 三萜类 炙黄芪 18.246 943.5236 [M+H]+ C48 H78 O18 942.5149 942.5188 −4.13 大豆皂苷 I 炙黄芪 39 19.049 499.3421 [M-H]− C31H48O5 500.3495 500.3502 −1.29 茯苓酸H 三萜类 茯苓 40 19.908 891.4684 [M+Na]+ , [M+K]+ C45 H72 O16 868.4793 868.482 −3.12 黄芪甲苷 I 三萜类 炙黄芪 41# 21.531 469.3314 [M-H]− C30H46O4 470.3392 470.3396 −0.86 甘草次酸 三萜类 法半夏 42 21.793 471.3474 [M-H]− C30H48O4 472.3545 472.3553 −1.67 山楂酸 三萜类 藿香 43 21.963 541.3524 [M+Hac-H]−、[M-H]− C31H46O4 482.3382 482.3396 −2.83 猪苓酸C 三萜类 茯苓 44 22.214 483.3133 [M-H]− C30H44O5 484.3202 484.3189 2.81 茯苓酸B 三萜类 茯苓 45 22.339 483.348 [M+Hac-H]−、[M-H]− C31H48O4 484.3551 484.3553 −0.27 3-表去氢土莫酸 三萜类 茯苓 46 22.601 485.3635 [M-H]− C31H50O4 486.3706 486.3709 −0.58 块苓酸 酚类 茯苓 22.606 525.3319 [M+K]+、[M+H]+ C31 H50 O4 486.3693 486.3709 −3.31 茯苓 47 22.817 389.1231 [M-H]− C20H22O8 390.1306 390.1315 −2.23 云杉新苷 糖苷类 砂仁 48 25.242 513.3582 [M-H]− C32H50O5 514.3655 514.3658 −0.68 茯苓新酸 HM 三萜类 茯苓 49 25.527 525.3588 [M-H]− C33H50O5 526.3659 526.3658 0.15 3-表去氢茯苓酸 三萜类 茯苓 50# 25.902 527.3743 [M-H]- C33H52O5 528.3814 528.3815 −0.19 茯苓酸 三萜类 茯苓 51 25.982 455.3525 [M-H]− C30H48O3 456.3597 456.3603 −1.47 齐墩果酸 三萜类 党参 52# 27.189 279.2333 [M+FA-H]−、[M-H]− C18H32O2 280.2404 280.2402 0.62 亚油酸 脂肪酸类 党参,炙黄芪,法半夏 53# 27.394 241.2172 [M-H]− C15H30O2 242.2245 242.2246 −0.22 十五烷酸 脂肪酸类 法半夏 54 27.394 485.3265 [M-H]− C30H46O5 486.3334 486.3345 −2.31 茯苓酸G 三萜类 茯苓 55 28.339 255.2329 [M-H]− C16H32O2 256.2402 256.2402 −0.09 棕榈酸 脂肪酸类 法半夏 56# 28.532 281.2487 [M-H]− C18H34O2 282.256 282.2559 0.28 顺-10-十七碳烯酸甲酯 脂肪酸类 陈皮 注:*为通过与对照品比对确定,#为入血原形成分。 -
[1] 新型冠状病毒肺炎诊疗方案(试行第五版 修正版)[J]. 中国中西医结合杂志, 2020, 40(2): 136-138. [2] HUANG K, ZHANG P, ZHANG Z H, et al. Traditional Chinese Medicine (TCM) in the treatment of COVID-19 and other viral infections: Efficacies and mechanisms[J]. Pharmacol Ther,2021,225:107843. doi: 10.1016/j.pharmthera.2021.107843 [3] 徐宇琴, 陈燕, 傅真杰, 等. 基于网络药理学探究连花清瘟胶囊治疗新冠肺炎的作用机制[J]. 浙江中医药大学学报, 2021, 45(10):1154-1161,1168. [4] 雷卓异, 范晓茜. 基于网络药理学和分子对接探讨预防肺疾一号方预防新型冠状病毒肺炎(COVID-19)的作用机制[J]. 世界科学技术-中医药现代化, 2021, 23(10):3541-3550. [5] 杨嫄, 吴波, 陶国水, 等. 化湿败毒方治疗新型冠状病毒肺炎的网络药理学探究[J]. 山东中医药大学学报, 2022, 46(2):218-226. [6] XU H Y, ZHANG Y Q, WANG P, et al. A comprehensive review of integrative pharmacology-based investigation: a paradigm shift in traditional Chinese medicine[J]. Acta Pharm Sin B,2021,11(6):1379-1399. doi: 10.1016/j.apsb.2021.03.024 [7] 陈凯欣, 尹力为, 李滋平. 基于数据挖掘的各省新型冠状病毒肺炎中医药治疗方案用药规律研究[J]. 辽宁中医药大学学报, 2021, 23(5):100-107. [8] 张佳, 李晓东. 基于数据挖掘的各地区新冠肺炎恢复期中医药组方用药规律研究[J]. 湖北中医药大学学报, 2020, 22(6):117-121. doi: 10.3969/j.issn.1008-987x.2020.06.33 [9] 闫玉凤, 董平. 上海市新型冠状病毒肺炎恢复期患者中药饮片用药特点分析[J]. 江苏中医药, 2020, 52(4):80-83. [10] 邵灿灿, 王豪杰, 孟鹏飞, 等. 新型冠状病毒肺炎的中医认识及治疗现状[J]. 中医学报, 2020, 35(4):704-708. [11] MAO K M, TAN Q, MA Y L, et al. Proteomics of extracellular vesicles in plasma reveals the characteristics and residual traces of COVID-19 patients without underlying diseases after 3 months of recovery[J]. Cell Death Dis,2021,12(6):541. doi: 10.1038/s41419-021-03816-3 [12] 赵静, 刘剑锋, 王燕平, 等. 中药复方分期治疗新冠肺炎的网络药理学分析[J]. 世界科学技术-中医药现代化, 2020, 22(2):278-288. [13] 陶嘉磊, 单进军, 袁斌. MS-DAIL联合MS-FINDER鉴定中药黄酮类化合物[J]. 世界科学技术-中医药现代化, 2021, 23(10):3704-3711. [14] 王依明, 王秋红. 半夏的化学成分、药理作用及毒性研究进展[J]. 中国药房, 2020, 31(21):2676-2682. doi: 10.6039/j.issn.1001-0408.2020.21.20 [15] 谢琦, 程雪梅, 胡芳弟, 等. 党参化学成分、药理作用及质量控制研究进展[J]. 上海中医药杂志, 2020, 54(8):94-104. [16] GAO S M, LIU J S, WANG M, et al. Exploring on the bioactive markers of Codonopsis radix by correlation analysis between chemical constituents and pharmacological effects[J]. J Ethnopharmacol,2019,236:31-41. doi: 10.1016/j.jep.2019.02.032 [17] 邓桃妹, 彭代银, 俞年军, 等. 茯苓化学成分和药理作用研究进展及质量标志物的预测分析[J]. 中草药, 2020, 51(10):2703-2717. doi: 10.7501/j.issn.0253-2670.2020.10.013 [18] RÍOS J L. Chemical constituents and pharmacological properties of Poria Cocos[J]. Planta Med,2011,77(7):681-691. doi: 10.1055/s-0030-1270823 [19] SU H F, SHAKER S, KUANG Y, et al. Phytochemistry and cardiovascular protective effects of Huang-Qi (Astragali Radix)[J]. Med Res Rev,2021,41(4):1999-2038. doi: 10.1002/med.21785 [20] 戴瑜婷, 张雪燕, 王艺璇, 等. 黄芪的现代研究进展及其质量标志物的预测分析[J]. 中国中药杂志, 2022, 47(7):1754-1764. [21] 凡杭, 聂安政, 包莉, 等. 藿香化学成分与药理作用研究进展[J]. 中国野生植物资源, 2021, 40(11):45-53. doi: 10.3969/j.issn.1006-9690.2021.11.009 [22] 徐方方, 陈伟英, 蔡婉娜, 等. 砂仁的化学成分及质量控制方法的研究进展[J]. 世界中医药, 2020, 15(24):3881-3886,3894. doi: 10.3969/j.issn.1673-7202.2020.24.031 [23] 黄斌, 胡燕珍, 李雪, 等. 基于UPLC-Q-TOF-MS技术分析乌蕨中的化学成分[J]. 实用中西医结合临床, 2021, 21(9):155-159. [24] 秦伟瀚, 冉继春, 叶良红, 等. UPLC-Q/TOF法同时定性定量分析滇芹药材中主要化学成分[J]. 中草药, 2018, 49(15):3576-3582. doi: 10.7501/j.issn.0253-2670.2018.15.016 [25] 吴茵, 白万军, 魏欣. 基于UPLC-Q-TOF-MS技术分析木蝴蝶中化学成分[J]. 中国实验方剂学杂志, 2019, 25(2):196-200. [26] BAHUN M H, JUKI\U0107 M, OBLAK D, et al. Inhibition of the SARS-CoV-2 3CL pro main protease by plant polyphenols[J]. Food Chem, 2022, 373(Pt B): 131594. [27] HAQ M M, CHOWDHURY M A R, TAYARA H, et al. A report on multi-target anti-inflammatory properties of phytoconstituents from Monochoria hastata (Family: Pontederiaceae)[J]. Molecules,2021,26(23):7397. doi: 10.3390/molecules26237397 [28] THAKARE V N, PATIL R R, SURALKAR A A, et al. Protocatechuic acid attenuate depressive-like behavior in olfactory bulbectomized rat model: behavioral and neurobiochemical investigations[J]. Metab Brain Dis,2019,34(3):775-787. doi: 10.1007/s11011-019-00401-8 [29] WANG X H, DAI C, WANG J, et al. Therapeutic effect of neohesperidin on TNF-α-stimulated human rheumatoid arthritis fibroblast-like synoviocytes[J]. Chin J Nat Med,2021,19(10):741-749. [30] AL-SANEA M M, ABELYAN N, ABDELGAWAD M A, et al. Strawberry and ginger silver nanoparticles as potential inhibitors for SARS-CoV-2 assisted by in silico modeling and metabolic profiling[J]. Antibiotics (Basel),2021,10(7):824. doi: 10.3390/antibiotics10070824 [31] YANG R C, LIU H, BAI C, et al. Chemical composition and pharmacological mechanism of Qingfei Paidu Decoction and Ma Xing Shi Gan Decoction against Coronavirus Disease 2019 (COVID-19): in silico and experimental study[J]. Pharmacol Res,2020,157:104820. doi: 10.1016/j.phrs.2020.104820 [32] TAN Y Q, CHEN H W, LI J. Astragaloside IV: an effective drug for the treatment of cardiovascular diseases[J]. Drug Des Devel Ther,2020,14:3731-3746. doi: 10.2147/DDDT.S272355 [33] JIANG B, YANG Y J, DANG W Z, et al. Astragaloside IV reverses simvastatin-induced skeletal muscle injury by activating the AMPK-PGC-1α signalling pathway[J]. Phytother Res,2020,34(5):1175-1184. doi: 10.1002/ptr.6593 期刊类型引用(5)
1. 曾桂花. 当归补血汤、坎地沙坦、福辛普利联用对糖尿病肾病合并高血压患者的影响. 医学理论与实践. 2025(05): 796-799 .  百度学术
百度学术2. 石若玉,张柯欣,周晓洁,杨康,王希茜,张琳琪. 7种中成药治疗慢性肾小球肾炎炎症反应疗效的网状Meta分析. 中国中药杂志. 2023(22): 6200-6215 .  百度学术
百度学术3. 刘惠金. 整体化护理策略对慢性肾小球肾炎伴高血压病患者血压管理及肾功能的影响. 心血管病防治知识. 2023(27): 49-51 .  百度学术
百度学术4. 顾慧洁,方君. 金杏降压方联合非洛地平治疗原发性高血压的临床效果. 中外医学研究. 2023(36): 5-10 .  百度学术
百度学术5. 刘小明. Scr及hs-CRP在慢性肾小球肾炎合并高血压患者行坎地沙坦酯治疗前后变化的研究. 心血管病防治知识. 2023(30): 14-16 .  百度学术
百度学术其他类型引用(0)
-





 下载:
下载:
 下载:
下载:


