-
药品临床综合评价是药品供应保障决策的重要技术工具,是关乎人民群众健康、提升药物临床价值的基础性工作[1]。2019年国家卫生健康委下发《关于开展药品使用监测和临床综合评价工作》的通知,推进药品临床综合评价的开展;2021年发布《药品临床综合评价管理指南(试行2021年版)》,在评价方案的制定和质量控制指标体系方面有了明确指导,推动了药品临床综合评价工作规范发展。文献计量学是运用数学和统计方法对所有知识载体进行定量分析的交叉科学。CiteSpace是一款基于Java程序开发的,广泛应用于分析和展示某个学科领域的研究进展、研究趋势和研究前沿的可视化软件,是文献计量和网络分析的重要工具[2-3]。文献计量学分析现已运用于药物治疗疾病的临床综合评价,如阿利沙坦酯治疗原发性高血压[4]、稳心颗粒治疗心律失常[5]、地氯雷他定治疗荨麻疹等[6] 。本研究以《中国期刊全文数据库》(中国知网)、《中国学术期刊数据库》(万方)和《中文科技期刊数据库》(维普)为数据来源,收集了自该工作开展以来关于药品临床综合评价的相关文献,利用CiteSpace软件根据对文献的年发文量、作者、研究机构和关键词等进行文献计量分析,构建可视化图谱,展示自建库以来国内临床综合评价的研究的现状、发展脉络及热点;同时进行分析与思考,以期为后续的相关研究工作提供参考。
-
以中国知网、万方和维普数据库为数据来源。选择精准搜索、期刊文献,检索主题为“临床综合评价”,检索时间设定为建库至2022年8月31日。检出文献数量分别是中国知网1206篇、万方数据库201篇和维普数据库79篇。将检索得到文献的题录导入NoteExpress3.5.0软件,根据“题录类型”、“作者”、“年份”和“标题”字段进行查重,保留资料最完整的文献,并通过人工阅读全文的方式筛选符合纳入标准的文献。对检出文献进行数据清洗后,最后共纳入有效文献126篇。有效文献以refworks-CiteSpace 2021格式导出,以导出的数据文件命名“download_**.txt”的格式导入数据分析软件。
-
使用基于Java平台的文献计量学分析软件CiteSpace6.1.R3进行分析。首先,用该软件对原始数据进行去重复、转化和阈值参数设置:“Node Types”值分别选择institute、author、keyword;“Top N”值设定为50;时间设定为1978至2022,以4年为时间切片。选择机构(institute)、作者(author)、关键词(keywords)等节点进行分析。
-
根据各设置参数,对纳入的126篇相关文献进行年发文量、作者合作网络分析、研究机构合作网络分析和关键词合作网络分析,对关键词进行共现分析、聚类分析和突现分析,并结合人工文献阅读和谱图分析,深入分析临床综合评价。
-
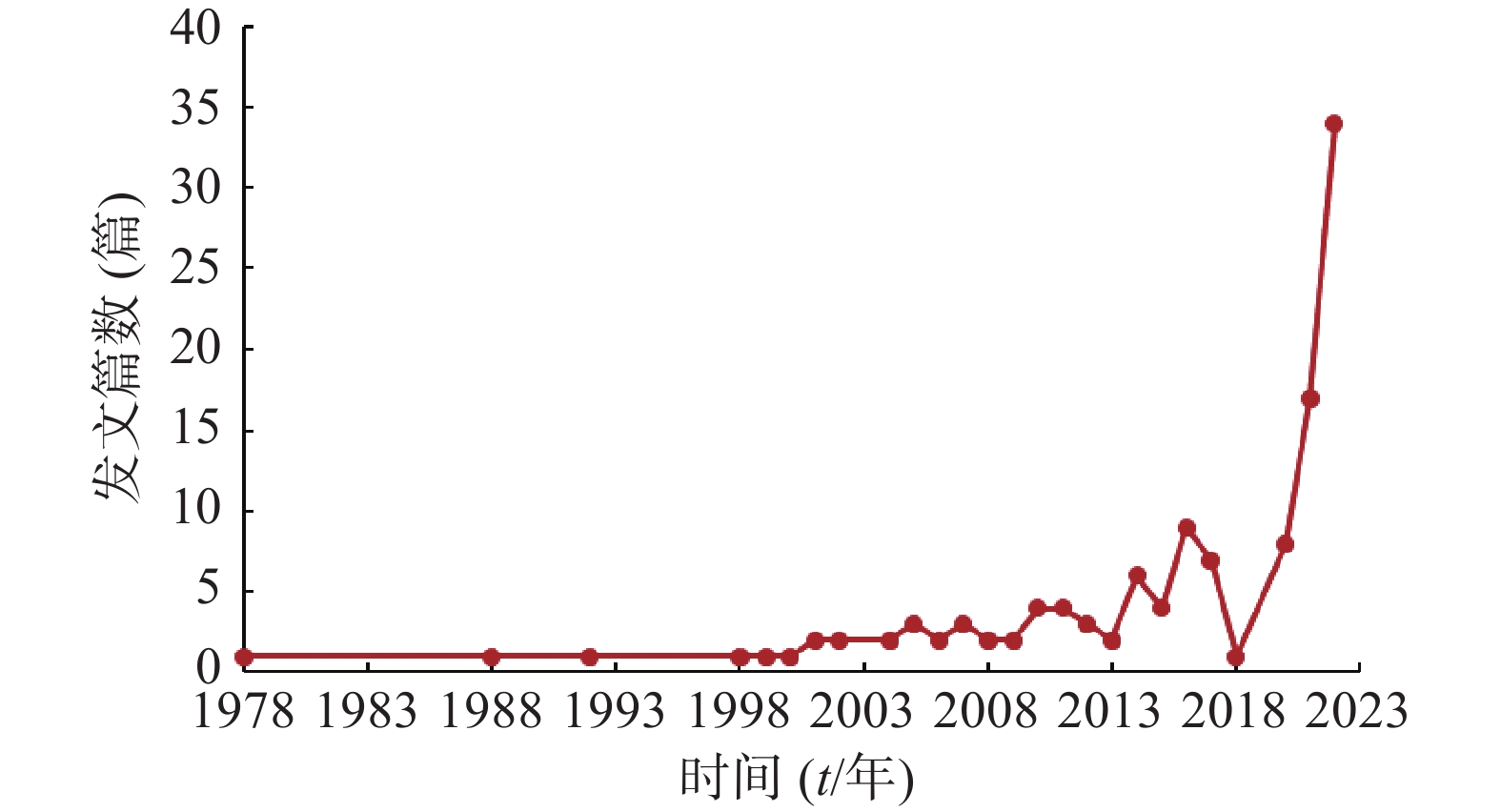
研究往年文献发文数量的趋势走向,可以反应临床综合评价研究的发展速度和未来走向。由图1可知,2015年之前药品临床综合评价相关发文量普遍偏低,在2019年至2022年连续四年间发文量逐年增长,处于持续发展状态。
-
共有133家机构发表临床综合评价文献,发文量前三名的研究机构分别是中国中医科学院中医临床基础医学研究所(15篇)、中国中医科学院西苑医院(6篇)、北京大学医药管理国际研究中心(5篇)。
对临床综合评价发表机构合作进行可视化分析,见图2。各发文机构存在广泛的合作,表现为医科/中医药高校(南方医科大学、北京中医药大学)及其附属医院,中国中医科学院及其附属医院,各类研究中心(国家卫生健康委卫生发展研究中心、中国中医药循证医学中心),综合性大学(暨南大学)及其附属医院这四大类合作紧密的机构。
-
共有51位作者发表临床综合评价相关文献,排名前10位作者见表1。发文量排名第1的作者为谢雁鸣(13篇),其次为王志飞(12篇)、张强(12篇)和崔鑫(11篇),发文强度最高的作者是谢雁鸣,引文半衰期最高的作者是张强。
表 1 临床综合评价发文量排名前10位作者
序号 作者姓名 发文量 发文强度(%) 引文半衰期 1 谢雁鸣 13 10.32 0.923 2 王志飞 12 9.52 0.916 3 张 强 12 9.52 0.958 4 崔 鑫 11 8.83 0.954 5 廖 星 6 4.76 0.667 6 王晓玲 5 3.97 0.800 7 贾露露 5 3.97 0.750 8 尉耘翠 5 3.97 0.800 9 韩 晟 5 3.97 0.800 10 戴泽琦 5 3.97 0.800 对临床综合评价发文作者合作网络进行可视化分析,见图3。发文量较多的作者之间存在合作关系,并形成稳定的团队。中国中医科学院中医临床基础医学研究所的谢雁鸣、王志飞、张强等人是临床综合评价研究的核心人物,做出了很大贡献。138条连线代表这些作者之间合作较多,研究内容相关性强。
-
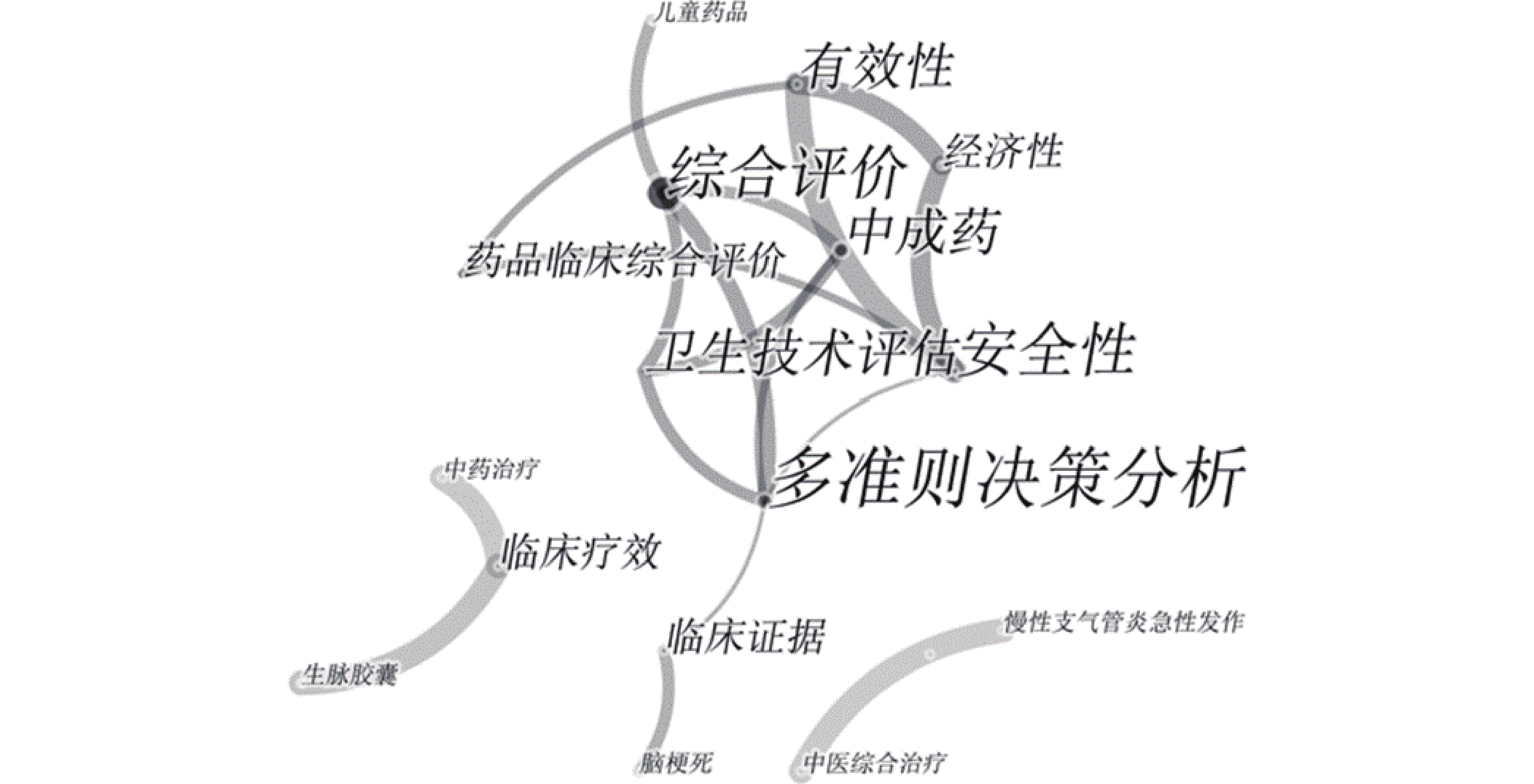
应用CiteSpace6.1.R3软件分析文献关键词得到10个共现性较强的关键词,其中有“综合评价”(34次)、“多准则决策分析”(13次)、“药品临床综合评价”(12次)、“中成药”(10次)、“安全性”(6次)、“有效性”(6次),高中心性关键词有“多准则决策分析”(0.3)、“安全性”(0.2)、“综合评价”(0.09),见图4。结合高频次关键词、高中心性关键词分布,可以基本得出该领域重点研究内容为多准则决策分析是主要研究方法,研究者最关注的研究对象是中成药,安全性和有效性则是重点关注的药品研究指标。
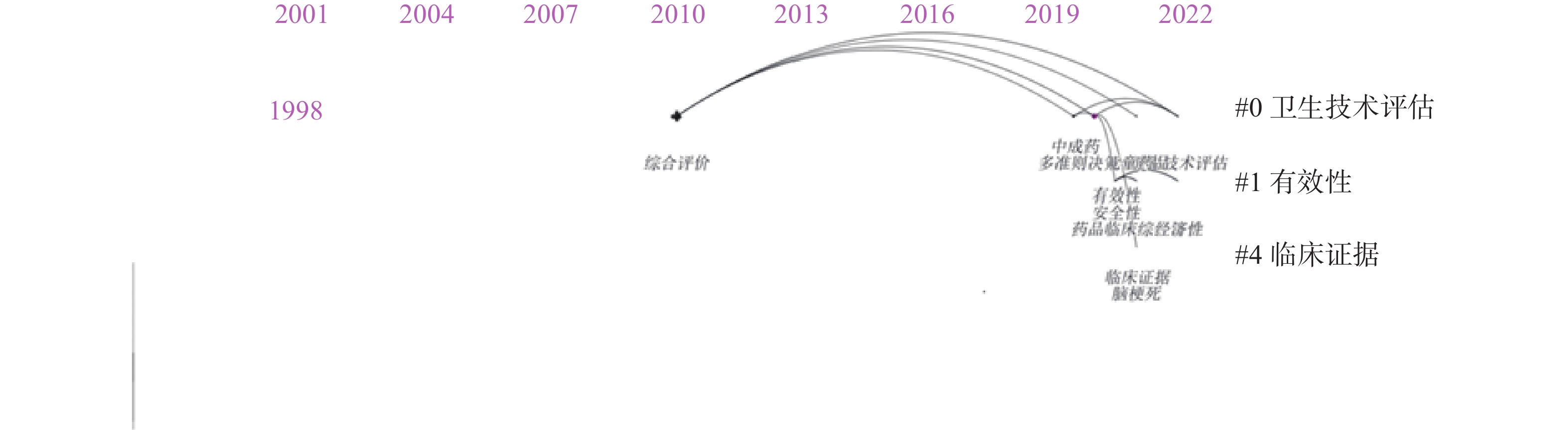
采用对数似然比(LLR)算法对文献中关系紧密的关键词进行聚类分析和时间线图可视化分析,见图5。分析得到的研究重点分别是卫生技术评估、有效性、临床证据。其中卫生技术评估是规模最大、文献数量最多的聚类,聚类时间跨度从2010年延续到2019年,突出反映该聚类在临床综合评价中占有重要地位。药品的有效性、安全性评价开始逐渐成为研究重点内容,形成稳定的方向。
分析结果获得了9个突现词,其中“临床疗效”开始时间是2006年,结束时间是2017年,强度数值超过3.4,表明这个突现词的影响力较大。突现词“中成药”出现时间为2020年,年份区间延续到2022年,推测该关键词可能是未来临床综合评价的研究热点。
-
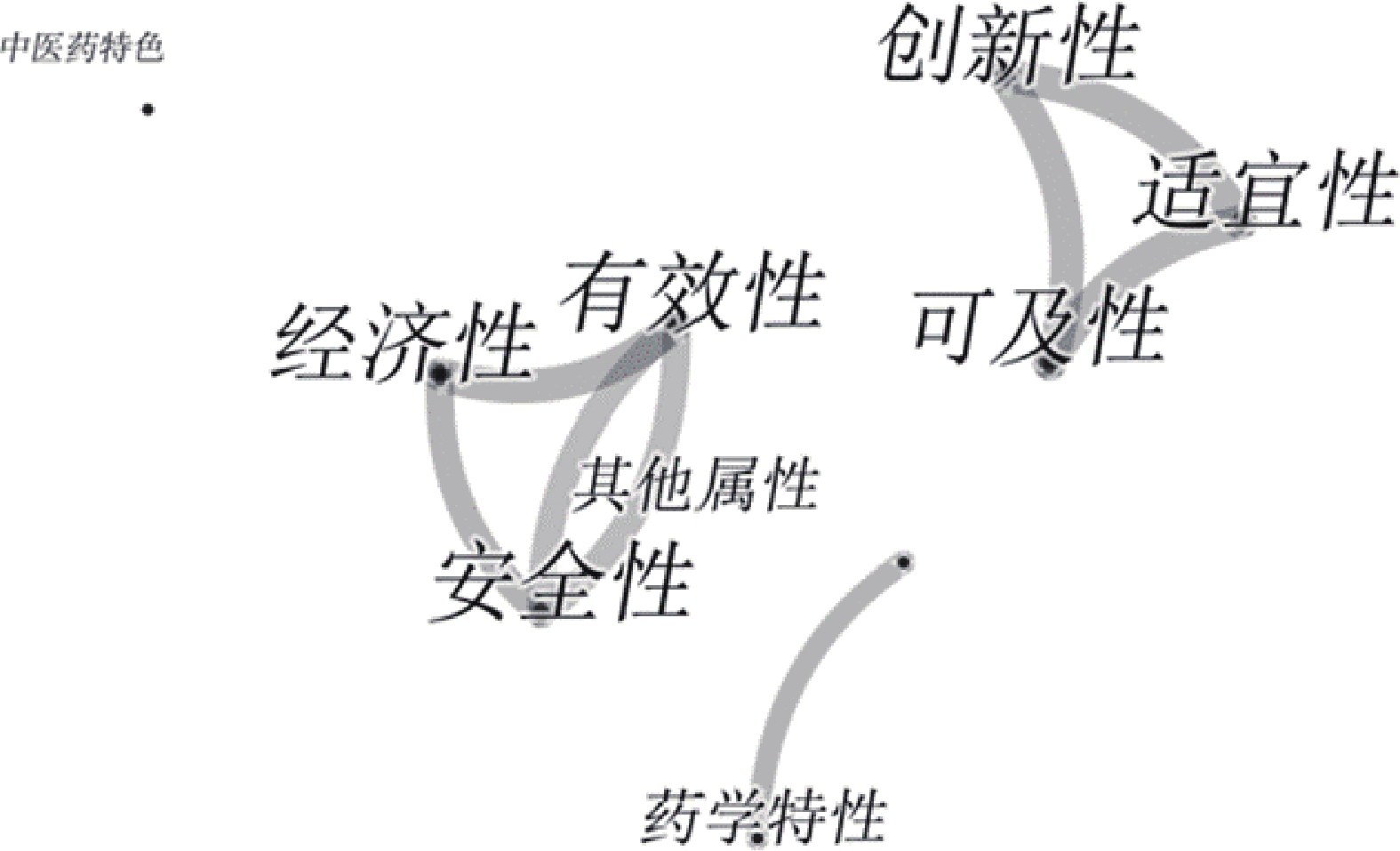
将“download_**”文件里的关键词信息设置为研究的维度,而后进行共现分析。用CiteSpace6.1.R3软件分析研究维度,其中排名前6位的维度分别为“有效性”(43次)、“安全性”(431次)、“经济性”(31次)、“适宜性”(22次)、“可及性”(22次)和“创新性”(22次),见表2。各研究维度之间的共现关系见图6,其中安全性和有效性共现次数最多,说明在各维度研究中,研究者普遍最关注药品的研究指标是安全性和有效性,其次是经济性和适宜性。
表 2 临床综合评价研究维度排名
序号 维度 词频 1 有效性 43 2 安全性 43 3 经济性 31 4 适宜性 22 5 可及性 22 6 创新性 22 7 中医药特色 6 8 药学特性 4 9 其他属性 2 -
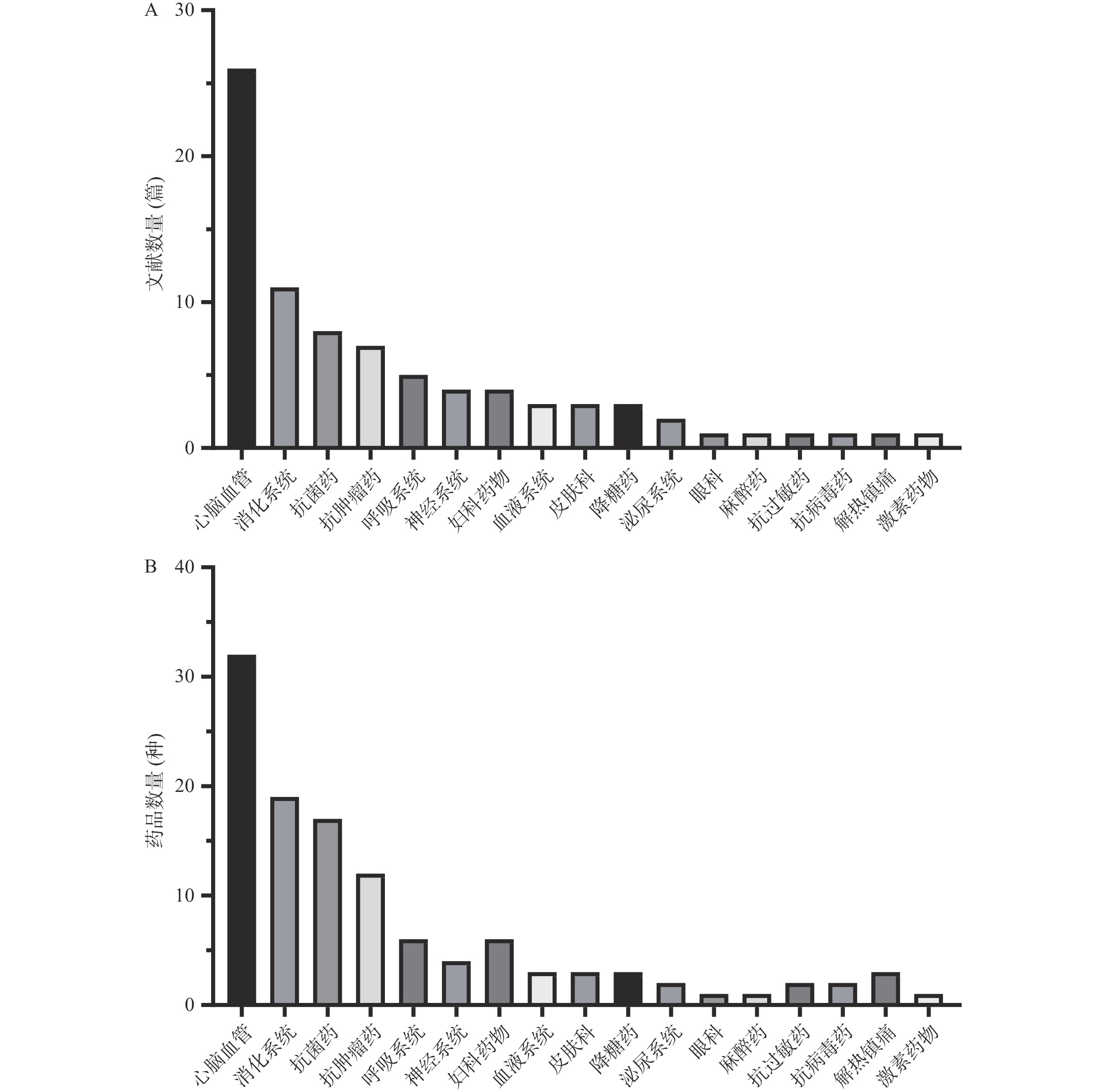
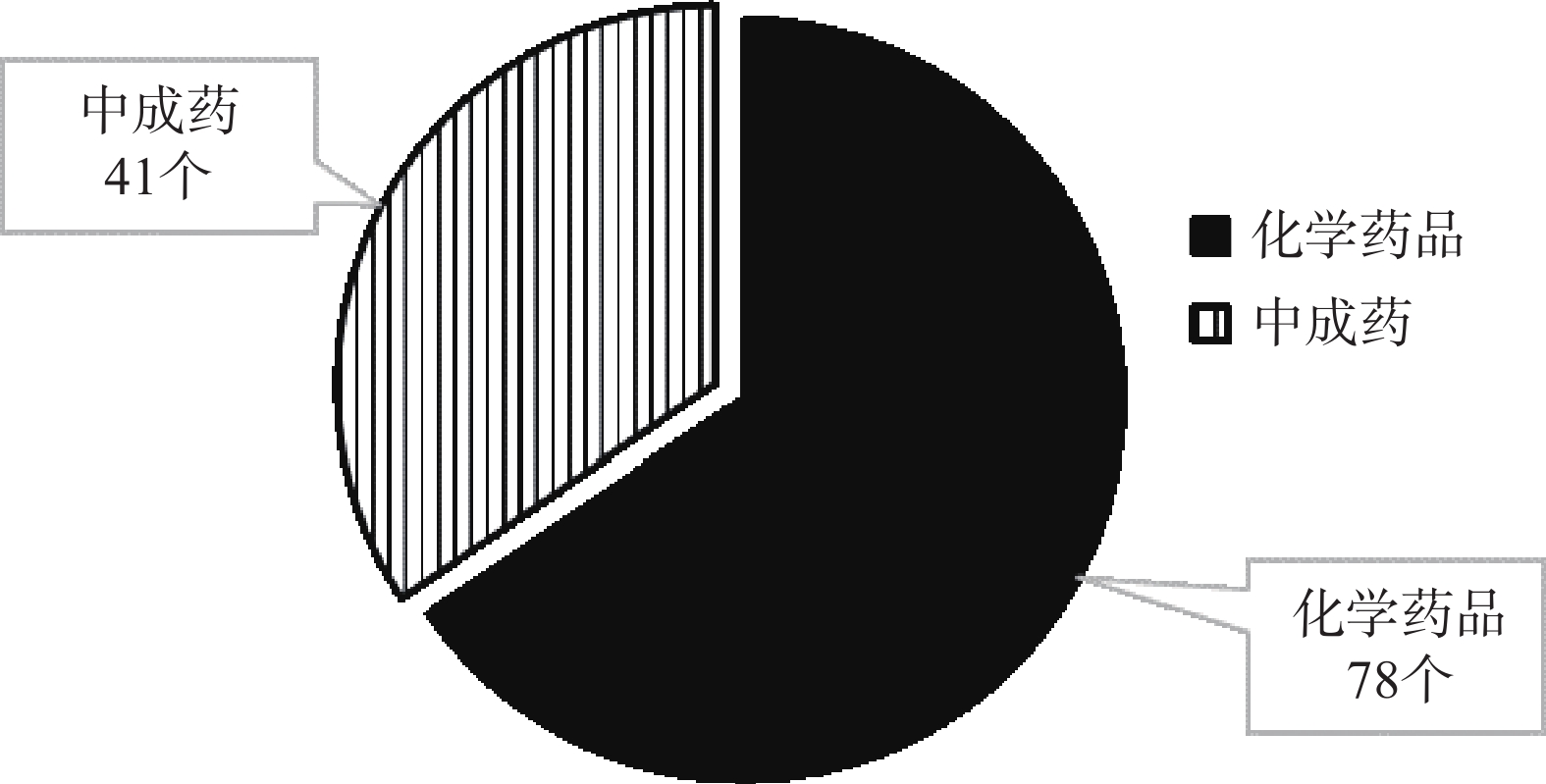
对本次纳入研究的文献所涉及的药物品种进行分析,排名前4的药物品种分别是心脑血管药物、消化系统药物、抗菌药物和抗肿瘤药物,见图7。其中心脑血管相关的文献数为26篇,涉及药品数量32个,消化系统相关的文献数为11篇,涉及药品数量19个,可见这两类常见病、慢性病受到研究者广泛的关注。比如,多项研究对索拉菲尼、仑伐替尼、FOLFOX4、银杏内酯注射液等开展药品临床综合评价[7-8]。此外,在所有的研究对象中,化学药品和中成药分别为78、41个,可见化学药品是临床综合评价的主要研究对象,中成药近年来也逐渐受到从业者的关注,见图8。
-
对本次纳入研究的文献所涉及的疾病进行分析,结果显示感染和脑卒中的文献频次均为8次,分别涉及16种和12种药物的临床综合评价,位列所有疾病分类首位。其次是肿瘤、心力衰竭和冠心病,见表3。可见临床上的常见病、多发病、慢病、难治性疾病因治疗周期长、治疗方案复杂等原因,其治疗药物在临床综合评价中容易受研究者关注。
表 3 文献所涉及的疾病分析结果
序号 疾病 文献频次 药品频次 1 感染 8 16 2 脑卒中 8 12 3 肿瘤 7 12 4 心力衰竭 5 6 5 冠心病 4 4 -
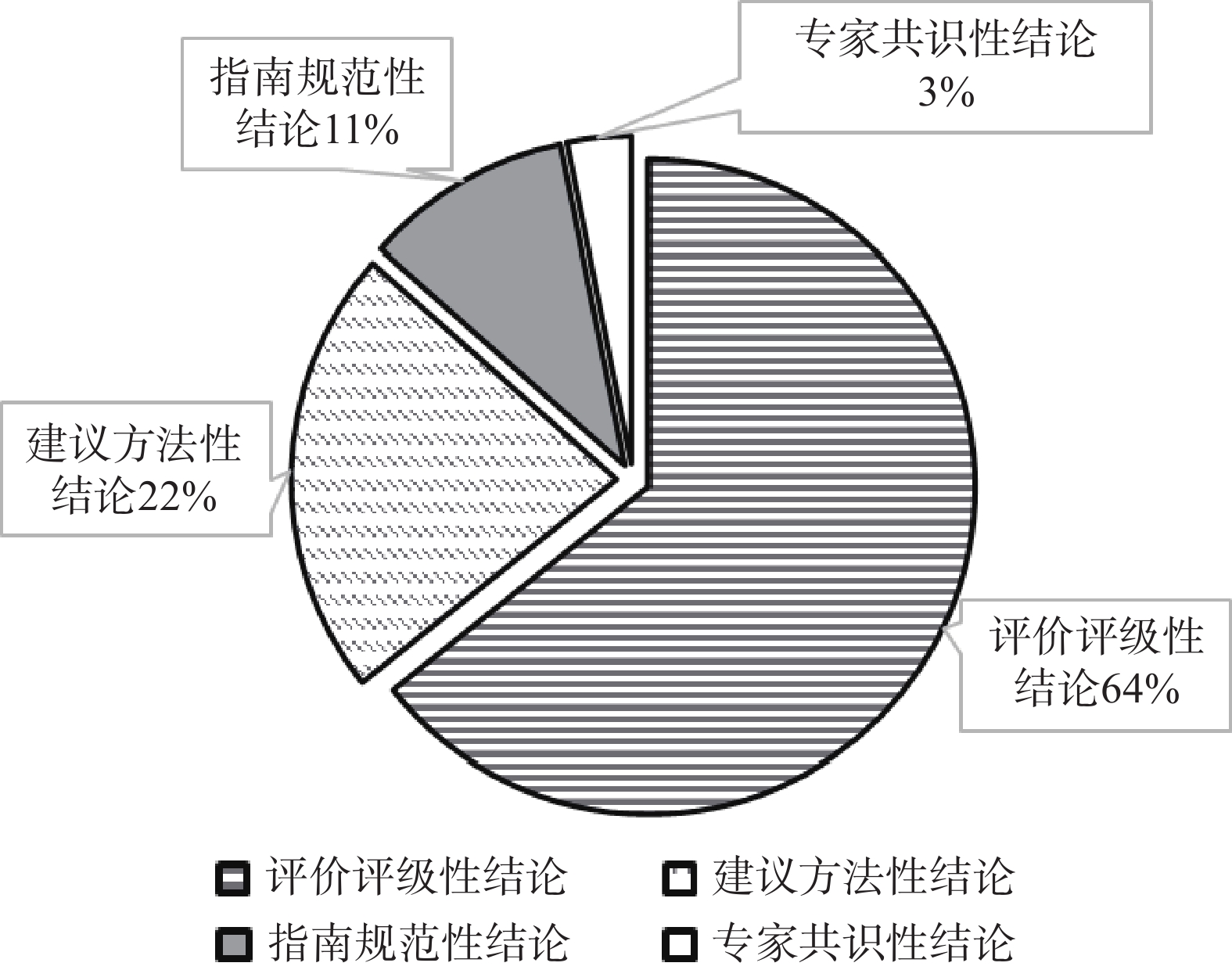
本次纳入研究的126篇文献中,其中提供了明确的药物治疗评级的结论文献共81篇,占总文献的64%;提供临床综合评价的建议及方法的结论文献共28篇,占22%;提供临床综合评价指南或规范的结论文献为13篇,占11%;形成专家共识性结论的文献4篇,占3%,见图9。
-
自2019年药品临床综合评价开展以来,在完善基本药物目录制度、促进临床合理用药等研究领域得到广泛应用,如宋子扬所在团队[9]通过卫生技术评估联合多准则决策分析建立我国儿童用药临床综合评价方法。本研究检索时间设定为建库至2022年,但药品临床综合评价的正式通知始于2019年。因此,大多数早于2019年发表的文献由于未按照规范进行临床综合评价均未被纳入分析。
在研究对象选择上,大部分研究以药品为切入点,如崔鑫等[10]对冠心舒通胶囊、段承阿鑫等[4]对阿利沙坦酯开展了临床综合评价,这些客观反映了药物的临床治疗价值。也有研究则以疾病为切入点:如王可可等[11]对骨质疏松症临床药物综合价值、符雨嫣等[12]对晚期肝癌一线系统治疗药品的临床综合评价,此类研究的结果常作为合理用药决策的参考。
在数据库的选择上,CiteSpace系统默认为单一数据库分析,可能导致分析结果存在片面性。本研究将中国知网、万方和维普这三个数据库中符合要求的文献数据导入NoteExpress3.5.0软件,对数据进行去重处理,再以“refworks”格式导出合并分析。此外,在外文数据库检索相关文献篇数过少,且不符合纳入分析要求,故未纳入分析。
目前中药大多存在科学基础薄弱,临床价值评估不清等问题。随着中医药的优势作用不断被认可[13],依托循证医学的中药临床综合评价工作势在必行[14-15]。本研究“中成药”词频呈现出最高共现性,如谢雁鸣、王志飞所在团队先后以天舒胶囊[16]、银杏内酯注射液[7]、热炎宁合剂[17]为例开展中成药临床综合评价,并形成了《中成药临床综合评价技术规范》[18],为中药的临床综合评价开展了示范性工作。就评价维度而言,中药在化学药品常用的6个维度上,增加中医药特性的维度(即“6+1”),主要对证候、组方、配伍、人用经验等中医药特有的方面进行评价[19],以体现中药独特的临床价值。
综上所述,虽然中药临床综合评价体系不断进步和完善,但仍存在评价研究质量有差异、核心要素不明显、技术层面不规范等系列问题[20-23]。如何利用现有评价方法提升药物综合临床评价的准确性和可靠性,仍是未来研究的课题。
Visual analysis of clinical comprehensive evaluation of drugs in China by bibliometric analysis
-
摘要:
目的 通过分析总结国内药品临床综合评价的研究现状,预测该领域的发展趋势,为进一步规范我国药品临床综合评价提供参考。 方法 利用《中国期刊全文数据库》(中国知网)、《中国学术期刊数据库》(万方)和《中文科技期刊数据库》(维普),检索建库至2022年临床综合评价的相关文献,获取文献的基本信息,评价文献质量,运用文献计量学及CiteSpace6.1.R3软件对研究作者、研究机构及关键词等内容进行可视化展示。 结果 经过筛选最终纳入126篇文献。分析结果显示:发文量有持续上升趋势,文献贡献最多的机构和作者分别是中国中医科学院和谢雁鸣。 结论 研究人员紧跟政策要求,以药品临床价值为导向开展了药品临床综合评价。建议研究人员进一步根据政府机构、医药行业、临床应用关注的重点和要求,组织开展综合评价。 Abstract:Objective To analyze the research status and predict the development trend of clinical comprehensive evaluation of drugs in China, and to provide reference for clinical comprehensive evaluation. Methods CNKI, Wanfang and VIP database were used to search the published articles of clinical comprehensive evaluation. Literature searching was set from the building time of the database to 2022, the basic information about the published articles was obtained for the evaluation of the literature quality. Bibliometrics and CiteSpace 6.1.R3 software were used to visualize the research authors, research institutions, and key words. Results After data screening, a total of 126 Chinese published articles were selected. The analysis showed that the numbers of published articles were rising continuously, and China Academy of Chinese Medical Sciences and Xie Yanming were the institute and the author with the maximum number of literatures, respectively. Conclusion The clinical comprehensive evaluation of drugs was conducted based on the clinical value of drugs, guided by the policy requirements. It is suggested that researchers should conduct the comprehensive evaluation according to the focus and requirements of government agencies, the pharmaceutical industry and the clinical applications. -
Key words:
- Clinical comprehensive evaluation /
- Bibliometric /
- CiteSpace /
- Information visualization
-
近年来,我国药品审评审批制度逐步完善,2005年原国家食品药品监督管理局发布《药品特别审批程序》,对突发公共事件亟需的应急药品可进行特别审批[1]。2016年原国家食品药品监督管理总局发布的《总局关于解决药品注册申请积压实行优先审评审批的意见》[2],首次明确了优先审评审批的范围、程序和工作要求。2020年国家药品监督管理局发布《突破性治疗药物审评工作程序(试行)》等3个文件的公告[3],进一步明确了3种药品加快审批途径。这一系列应急审批程序及加快审评工作规范的发布,对于应急药品供应、创新药物研发具有重要意义:①药品审批效率不断提高,创新药的研发时间明显缩短,适用患者可尽早获得需要的药物治疗;②激励创新药研发机构加大投入并提高创新能力;③在面对诸如新型冠状病毒肺炎(COVID-19)疫情时,开辟绿色通道,相关疫苗及治疗药物迅速上市,在抗击疫情过程中发挥了重要作用。但总体来说,我国的药品应急审批制度起步较晚,实践过程中还在不断摸索,该研究通过分析对比我国与美国、欧盟、日本等国家与地区的药品应急审批制度,探讨进一步优化我国药品应急审批制度的思路和措施。
1. 我国实施药品应急审批的相关制度及应用现状
国家市场监督管理总局2020年1月发布的《药品注册管理办法》[4],将我国药品加快上市注册程序分为突破性治疗、附条件批准、优先审评审批和特别审批程序。该4种程序的适用范围和审批阶段见表1。
表 1 我国药品应急审批程序对比名称 适用范围 申请阶段 突破性治疗药物 在药物临床试验期间,用于防治严重危及生命或严重影响生存质量的疾病且尚无有效防治手段或与现有治疗手段相比具有明显临床优势的创新药或改良新药等 在Ⅰ、Ⅱ期临床试验阶段,通常不晚于Ⅲ期临床试验开展前 附条件批准 治疗严重危及生命且尚无有效治疗手段的疾病的药品,药物临床试验已有数据证实疗效并能预测其临床价值的;公共卫生方面急需的药品,药物临床试验已有数据显示疗效并能预测其临床价值的;应对重大突发公共卫生事件急需的疫苗或者国家卫生健康委员会认定急需的其他疫苗,经评估获益大于风险的 药物临床试验期间 优先审评审批 临床急需的短缺药品、防治重大传染病和罕见病等疾病的创新药和改良型新药;符合儿童生理特征的儿童用药品新品种、剂型和规格;疾病预防、控制急需的疫苗和创新疫苗;纳入突破性治疗药物程序的药品;符合附条件批准的药品 上市许可申请前 特别审批 突发公共卫生事件时,国家药品监督管理局依法决定的应急所需防治药品 提出注册申请前 1.1 突破性治疗
纳入到“突破性治疗”审评通道的药物,药审中心会优先处理有关沟通交流,加强指导并促进药物研发进程;在申报上市环节,该药物可纳入优先审评审批程序,审评时限缩短;上市申请阶段,药审中心会滚动接收其申报资料,并优先安排核查、检验等,这一系列措施可大大缩减新药从研发到上市的时间。2020−2022年间,共有12个药品通过突破性治疗程序上市(表2)。
表 2 2016−2022年我国加快审批途经的注册申请数及获批品种数年份
(年)突破性治疗(件) 附条件批准的
品种数(个)优先审评 特别审批的
注册申请(件)纳入的注册申请 批准的新药上市申请 纳入的注册申请(件) 批准上市品种数(个) 2016 − − − 193 7 − 2017 − − − 230 50 − 2018 − − − 313 83 − 2019 − − − 253 82 − 2020 24 0 6 219 121 59 2021 53 5 38 115 131 81 2022 56 7 31 74 75 51 注:数据来源于NMPA官网。 1.2 附条件批准
“附条件批准”目的在于缩短药物临床试验的时间,使其尽早应用于无法继续等待的危重疾病或公共卫生方面急需的患者。符合附条件批准上市情形的药物,可使用替代终点、中间临床终点或早期临床试验数据来反映药物的有效性,当这些数据能够提示药品的获益大于风险时候,即可申请附条件批准上市。2020−2022年间,共有75个药品通过附条件批准程序上市(表2)。附条件批准可以有效缩短临床研发所需的时间,但也存在一定的风险。因对药品上市时临床安全性等要求的降低,增加了疗效不确定的可能性[5],存在安全有效性不足和资金浪费的风险,对于此类尚无充分证据的药品,平衡满足突发公共卫生事件药品需求和临床安全性可控,科学设计附条件批准方案,是监管部门面临的重要问题。
1.3 优先审评审批
“优先审评审批程序”自2016年发布以来,在实践经验基础上不断优化调整,适用范围更多地向具有明显临床价值、临床急需的药物聚焦,致力于将更多的临床价值显著、临床急需的短缺药品、防治重大传染病、罕见病、儿童用药、纳入突破性治疗程序、符合附条件批准的药品等纳入优先审评程序。同时加速审评时限,药品上市许可申请的审评时限一般为200个工作日,优先审评审批程序的审评时限缩短至130个工作日,其中临床急需境外已上市罕见病用药优先审评审批程序的审评时限为70个工作日。至2022年,共有1 300余件注册申请被纳入该程序,其中获批上市品种数为549个(表2)。
1.4 特别审批程序
“特别审批程序”其核心为出现突发公共卫生事件时,国家药品监督管理部门按照统一指挥、早期介入、快速高效、科学审批的原则,对应急处理所需药品进行特别审批,在申请受理、技术审评、抽样检验、行政审查等环节中优先处置,缩短审批时间。新冠肺炎疫情期间,特别审批程序在新冠病毒疫苗和治疗药物的审批中发挥了重大作用。2020年,共计59件与抗击新冠有关的中药、化学药、生物制品注册申请纳入该程序并完成技术审评,其中建议附条件批准上市1件,建议批准临床试验申请53件,增加适应证的补充申请5件。2021年与2022年分别审结81件及51件纳入特别审批程序的注册申请(均为新冠病毒疫苗和治疗药物),见表2。特别审批程序是一项制度性突破,但随着时间推移,该程序逐渐暴露出实施细节模糊、终止程序缺失等问题[6],不能适应当今国家公共卫生形势的新变化。
我国药品监管部门正在积极推进药品加快上市审评审批制度的改革,并形成初步的监管体制。2023年3月,药审中心总结抗疫应急审批经验,结合已有快速审批制度,制定了《药审中心加快创新药上市许可申请审评工作规范(试行)》[7]。随着改革的发展,更多深层次的问题也会随之暴露。为从根本上解决审评时限长、效率低等问题,药品监管部门应借鉴发达国家的一些加快审评审批政策,并结合中国国情构建一个具有中国特色的药品应急审评审批机制。
2. 国外实施药品应急审批的相关制度及现状
2.1 美国
美国食品药品监督管理局(FDA)建立了4种药品应急审批的途径,包括快速通道(FT)、突破性疗法认证(BT)、优先审评(PR)及加速审批(AA)[8]。① FT:FT可以在药物研发的任何阶段由企业向FDA申请,主要针对在治疗严重的或危及生命的疾病方面具有一定潜力的新药审批。对进入FT的药物,FDA将进行早期介入,以使该药物“少走弯路”,加快研发进程。此外,申请人还可以在早期与FDA沟通,分阶段递交申报资料,不必一次性提交完整的申报资料,而FDA的审批将基于所治疗疾病的严重程度,按风险/效益原则进行评价。②BT:BT主要针对临床试验周期较长的药物,要求申请者提交早期临床试验数据,在药物临床试验阶段助力审批加速。③PR:PR在申请新药上市时提出,FDA会在60 d内做出是否批准优先审评的决定,主要针对与已上市药品比较有显著改进的药品上市申请,并不要求是具有全新分子实体的创新药,但临床疗效必须优于已上市药物。PR的时间为6个月,PR通道并不影响临床试验阶段的周期长短,也不降低审评标准。④AA:AA可使用替代终点、中间临床终点作为许可基础,允许在确切的治疗效果证据未全部收集到之前批准新药上市,主要针对治疗严重的、危及生命的疾病的新药,其批准一般附有条件,即药品具有可观察到的重大短期临床效果,而长期临床疗效则需进一步研究证明。这4种程序之间既存在差异又相互关联,同一个药品申请可适用多种应急审批途经。2018−2022年,FDA年均批准近50个新药,其中约68%的新药使用了一个或多个应急审批途径,具体见表3。
表 3 2018−2022年FDA通过加快审批途经批准的新药情况年份
(年)批准新药总数(个) 加快审批途经批准的新药数量(个) 使用1个或多个加快途经的新药数量及
占批准总数的百分比[个(%)]快速通道 突破性治疗 优先审查 加速审批 2018 59 24 14 43 4 43(72.9) 2019 48 17 13 28 9 29(60.4) 2020 53 17 22 30 12 36(67.9) 2021 50 18 14 34 14 37(74.0) 2022 37 12 13 21 6 24(64.9) 注:数据来源于FDA官网。 此外,美国还建立了紧急使用授权(EUA)制度,即公共卫生处于紧急状态或存在陷入紧急状态的危险时,FDA可对未批准上市的医药产品或已获批准上市医药产品的其他用途进行授权[9]。同时,一旦官方宣布紧急情况结束时,所有基于该声明发布的EUA将不再有效。EUA的发布、更新和终止通知将在《联邦公报》(FR)上公布,并在FDA与美国疾病控制与预防中心(CDC)官网上公告。自2004年EUA制度建立以来,2009年之前FDA只发布过2个EUA。2009−2010年为应对H1N1流感,FDA为22个产品发布EUA,包括药品、诊断试剂和医疗器械。2012年以来,FDA先后对H7N9流感病毒、埃博拉病毒、寨卡病毒、COVID-19等发布多个EUA产品。截至2023年6月,FDA共批准了15个COVID-19治疗药物和4个疫苗的EUA[10]。
2.2 欧盟
欧洲药品审评管理局(EMA)承担欧洲的药品审评审批工作,拥有来自欧盟各国的超过4 000多名专家组成的团队。EMA采取了多种新药应急审批的途径,包括附条件上市许可(CMA)、AA、特殊情况授权(EC)、优先药物审批(PRIME)等。
CMA主要针对未被满足的医疗需求,允许在临床数据不完整的情况下进行早期批准上市,上市后完成确证性临床试验。CMA的有效期为一年,可每年续签。上市许可持有人必须在规定的时间内履行特定义务,包括完成正在进行的或新的研究,或收集额外的数据。一旦上市许可持有人履行了所规定的义务,并且完整的数据证实该药物的益处继续大于其风险,上市许可就可以转换为标准上市许可(不再受特定义务的约束)。对于任何药物,如果新数据显示该药物的益处不再大于其风险,EMA可以暂停或撤销上市许可。2006−2016年间,EMA共有30个附条件上市药物获批,其中11个转为标准授权,2个因为商业原因撤回,其余17个仍处于附条件上市中[11]。
AA可将审批时间从标准程序的210 d缩短至150 d。申请人应证明其申报的医药产品预计具有重大公共卫生利益,特别是从治疗创新的角度来看。另外,申请人应提供有关GMP和GCP方面的信息,以便将常规GCP和批准前的GMP检查纳入加速评估程序。
EC允许患者获得无法根据标准授权批准的药物,在特殊情况下,EMA可能在没有全面数据的情况下授予上市许可。无法获得全面数据的原因在于只有极少数患者患有这种疾病,或是收集有关药物疗效和安全性的完整信息是不道德的。与附条件的上市许可不同,特殊情况授权可能在授权后也无法获得全面的数据。这些药物取得特定的授权后有义务接受EMA的监测约束。
此外,EMA还于2016年3月启动了PRIME计划,该计划目的在于加强对未满足医疗需求的药物,尤其是有潜力带来重大治疗成果的药物开发的支持。PRIME建立在现有的监管框架基础上,通过尽早与药物研发企业合作,为企业提供科学建议和加速评估,并确保患者只参与旨在生成必要数据的必要试验,从而充分利用有限的资源,使药物能够更早地到达患者手中。2016年1月至2021年6月,共有384个药物申请加入PRIME,其中95个被纳入该计划,年平均纳入率为25% [12]。2019−2022年EMA通过AA途经批准的新药情况见表4。
表 4 2019−2022年EMA通过加快审批途经批准的新药年份
(年)批准新药
总数(个)加快审批途经批准的新药数量(个) 附条件
上市许可加速审批 优先药物
审批特殊情况
授权2019 66 8 3 0 1 2020 97 13 6 8 5 2021 92 13 3 6 4 2022 89 9 5 8 5 注:数据来源于EMA官网。 2.3 日本
日本药品与医疗器械管理局(PMDA)负责新药审批,药品应急审批程序包括优先审评、先驱审查认定、附条件审批、再生医学产品有条件和有时限的批准、紧急授权、特例审批等。“优先审评”主要用于具有重大临床价值创新药物及孤儿药的注册审评,2021年,PMDA共批准了144个新药,其中56个通过优先审评,平均审批时间为223 d,同期标准审批时间为300 d。同时,PMDA为了减少不同审查员之间可能存在的人为因素干扰,制定了细致的审查标准化手册,改善了不同机构之间可能存在的信息传递滞后、人员沟通困难等问题,将药品审批时间大幅缩短。
“先驱审查认定”制度自2015年起开始试行,2020年正式提升到法规级别[13]。申请先驱审查的药品需满足治疗方法的突破性与革新性,针对重大严重影响生命质量的疾病或无法根治的疾病等要求。纳入先驱审查认定制度的药品享有优先咨询、加强预评估、优先审查等权力,该制度的审批时限为6个月,比以往减少一半。截至2023年6月,共有200余个药品申请加入先驱审查认定,其中25个药品被成功纳入,该25个药品中的17个已获批上市[14]。其余快速审批制度的对比见表5,通过快速审批,PMDA共批准了9个新冠治疗药,8个新冠疫苗产品(截至2022年末)[15]。
表 5 日本平时与紧急情况下的药品审批制度对比对比项目 平时根据药品性质进行审批 紧急情况下的快速审批 附条件审批 再生医学产品有条件和
有时限的审批特例审批 紧急授权 对象 罕见病用药产品、开创性用药产品或特殊用途用药产品以及其他有特殊医疗需求的用药产品 非同源再生医学及其他产品(细胞/组织产品、基因产
品等)在外国(拥有与日本医药制度同等标准的制度的国家)销售的医药产品和其他产品 所有医药产品 制度宗旨 对医疗需求量大,但很难对足够数量的受试者进行临床试验以验证其疗效和安全性的医药产品给予批准 考虑到再生医学产品的特点(产品质量参差不齐,药理作用表现不一),对那些经少量病例证实安全且假定有效的产品予以批准 为了在紧急情况下防止健康危害的扩散,批准在外国销售的医药产品等 药品和其他产品的安全性已得到确认,其疗效也已得到推定,因此可获得批准,以防止紧急情况下健康危害的扩散 有效性 确认 推定 确认 推定 安全性 确认 确认 确认 确认 2.4 国外相关做法的优势
美国、欧盟、日本的药品优先审评目标定位明确,均以临床需求为目的,旨在加快临床急需药品的审评上市,形成覆盖全流程的多通道、多机制、多模式优先审评体系。制度中具有明确的适用范围、纳入标准、具体申请、受理、审核、审评流程及相关细则。法规体系层次清晰、完整,可操作性强。药审部门制定沟通方案和计划、提前沟通、主动指导。同时,为保证上市药品安全有效,各国针对通过优先审评上市的药品建立了更为严格的上市后监管制度,明确职能定位、监管范围、监管方式、申请人责任和义务,确保监管的科学、规范、有效。美国、日本在推进药品监管领域加快上市注册程序同时,还设置紧急授权使用药品作为应对公共卫生或突发事件的措施。以上这些,都对我国有很好的借鉴意义。
3. 我国药品应急审批制度的思考及启示
3.1 完善药品应急审批制度建设
确定药品需求导向,进一步优化应急审批制度中的药品纳入范围,明确和细化纳入标准。建立符合我国国情的药品优先审评上市后的监管制度,对药品上市后研究、限制性适用、信息公开、撤销上市或转为普通上市,以及相关的强制性手段、法律责任等都应予以明确细化的规定[16]。
建立我国药品EUA制度。我国《中华人民共和国突发事件应对法》对突发事件的预防和应急准备等作出了明确规定,但目前仍缺少关于药品紧急使用授权的法律依据。建议建立我国药品EUA制度,组建由国家卫生健康委员会、药品监管部门及相关部门组成的EUA专业领导工作组协调、管理、实施EUA。应急情况下可考虑对未经药品监管部门批准上市的药品,在具有基础研发数据,可以证明其安全性和有效性的前提下,启动EUA。EUA是在公共健康利益受到严重威胁和药品安全有效评价之间寻找的平衡,遵循“边审批、边使用、边评估、边调整”的原则,可以与加快注册评审同步进行,及时补充调整新药的使用限制。同时,出台EUA实施细则,明确规定实施EUA的条件、发布程序、审评流程和要求、终止或撤销、产品覆盖范围、信息公开、告知义务、责任保护等[17]。
3.2 增强政府职能和优化人员配置
目前的药品应急审批程序主要从促进申请人与药审中心沟通、调整上市标准这两方面来提高新药注册的效率。我国虽设置了药品审评专家咨询委员会,但人员配置数量较欧盟、日本等较少,在药品审评过程中需要召开会议解决问题,或是申请过程中存在争议主动征询意见时提供相应的技术指导与决策建议,发挥作用有限。应积极推动审评审批人才培养和队伍建设,扩大药审专家职能,实现人员配置的优化和审评通过率的提升。
药品的上市审批过程中,申请方与监管部门、检验机构之间存在信息交流滞后的问题,应尽快推广和加强药审中心受理人员及项目管理人员的提前介入,争取受理问题在申报前得到解决,降低企业的创新风险,同时防止审评资源的浪费与人力、物力的消耗。
3.3 加强快速审批药品上市后监管
美国、欧盟、日本药品优先审评制度中,药审部门侧重沟通指导,并重视上市后药品的安全性与有效性,建立了严格的上市后监管制度。现阶段,我国加快上市注册程序对新药的开发促进作用较为明显,通过快速审批程序注册上市的药品逐年增多,为避免相关药物上市后出现无期望的临床疗效或存在安全性问题,急需加强快速审批药品上市后的监管工作,保证审批药物的安全有效。新版《药品注册管理办法》引入药品“加快上市注册程序”的同时也明确设立了上市退出机制。为实现此类特殊审评通道药品上市前、后安全监管工作的顺利衔接,可借鉴EMA的经验,细化特殊审评药品准入条件,将上市前风险管理体系的建立作为关键审评因素,上市后设置额外监测、风险沟通等安全监管制度进行有效衔接,从而实现对用药风险的持续监测和动态管理。
4. 结语
随着公众对药品上市的效率以及对突发事件应急药品供应的需求提升,我国药监部门也尽力在保障药品安全有效的前提下,出台一系列政策以尽量缩短紧急必需用药的审评审批时间。在应对新冠疫情过程中,药品应急审批工作已取得了诸多进展。然而,对比国外药品快速审批程序,我国目前仍处于发展阶段,因此需认真总结既往的工作经验,并在实践过程中不断完善。同时借鉴一些国外先进模式和监管方式,进一步改善我国药品应急审批制度体系和流程,提升药品审批效率,提高应对突发事件的药品保障能力。
-
表 1 临床综合评价发文量排名前10位作者
序号 作者姓名 发文量 发文强度(%) 引文半衰期 1 谢雁鸣 13 10.32 0.923 2 王志飞 12 9.52 0.916 3 张 强 12 9.52 0.958 4 崔 鑫 11 8.83 0.954 5 廖 星 6 4.76 0.667 6 王晓玲 5 3.97 0.800 7 贾露露 5 3.97 0.750 8 尉耘翠 5 3.97 0.800 9 韩 晟 5 3.97 0.800 10 戴泽琦 5 3.97 0.800 表 2 临床综合评价研究维度排名
序号 维度 词频 1 有效性 43 2 安全性 43 3 经济性 31 4 适宜性 22 5 可及性 22 6 创新性 22 7 中医药特色 6 8 药学特性 4 9 其他属性 2 表 3 文献所涉及的疾病分析结果
序号 疾病 文献频次 药品频次 1 感染 8 16 2 脑卒中 8 12 3 肿瘤 7 12 4 心力衰竭 5 6 5 冠心病 4 4 -
[1] 《中国医疗机构药品临床综合评价质量控制体系共识》专家组. 中国医疗机构药品临床综合评价质量控制体系共识[J]. 中国药业, 2022, 31(15): 1-9. [2] 杨倩. 常见文献计量学工具的分析功能比较研究[J]. 情报探索, 2021,288(10): 87-93. [3] 肖秘苏, 张剑萍, 杨全军, 等. 基于CiteSpace的我国药品综合评价研究现状分析[J]. 中国药房, 2022, 33(8): 911-916. [4] 段承阿鑫, 隋宾艳, 艾丹丹, 等. 阿利沙坦酯治疗原发性高血压的临床综合评价[J]. 中国合理用药探索, 2022, 19(3): 46-55. [5] 魏瑞丽, 王志飞, 马晓昌, 等. 稳心颗粒治疗心律失常(气阴两虚证)的临床综合评价[J]. 中国中药杂志, 2021, 46(23): 6068-6077. [6] 刘璐, 甄路路, 任美娟, 等. 地氯雷他定治疗荨麻疹的临床综合评价[J]. 中国药房, 2022, 33(10): 1240-1246. [7] 唐显帅, 郑磊, 张明珠, 等. 基于循证医学证据和药物经济学模型的中成药临床综合评价[J]. 中国药房, 2022, 33(15): 1870-1875. [8] 刘福梅, 谢雁鸣, 王志飞, 等. 银杏内酯注射液治疗脑梗死的临床综合评价[J]. 中国中药杂志, 2022, 47(6): 1493-1500. [9] 宋子扬, 尉耘翠, 聂晓璐, 等. 基于卫生技术评估联合多准则决策分析建立我国儿童用药临床综合评价方法[J]. 药物流行病学杂志, 2019, 28(10): 681-686. [10] 崔鑫, 韩晟, 李军, 等. 冠心舒通胶囊治疗冠心病心绞痛心血瘀阻证的临床综合评价[J]. 中国中药杂志, 2022, 47(6): 1469-1475. [11] 王可可, 李思淼, 罗婕, 等. 骨质疏松症临床实践指南评价及药物综合价值研究[J]. 中国医院药学杂志, 2020, 40(1): 91-98. [12] 符雨嫣, 金春林, 孙辉, 等. 晚期肝癌一线系统治疗药品的临床综合评价[J]. 临床药物治疗杂志, 2021, 19(10): 66-70. [13] 杨思红, 赵晖, 梁宁, 等. 中医优势病种遴选和评价技术指导建议[J]. 中国中医基础医学杂志, 2022, 28(10): 1595-1601. [14] 廖星, 戴泽琦, 吴雪, 等. 采用EVIDEM框架开展中成药临床综合评价[J]. 中国中药杂志, 2022, 47(10): 2833-2840. [15] 戴泽琦, 徐思敏, 吴雪, 等. 多准则决策分析用于中成药临床综合评价的建议[J]. 中国中药杂志, 2022, 47(12): 3155-3160. [16] 王连心, 谢雁鸣, 王志飞, 等. 天舒胶囊治疗偏头痛(瘀血阻络证、肝阳上亢证)的临床综合评价[J]. 中国中药杂志, 2022, 47(6): 1501-1508. [17] 吕健, 王志飞, 谢雁鸣, 等. 热炎宁合剂治疗急性上呼吸道感染(热毒袭肺证)的临床综合评价[J]. 中国中药杂志, 2022, 47(6): 1476-1483. [18] 张强, 王志飞, 谢雁鸣, 等. 中成药临床综合评价技术规范[J]. 世界中医药, 2021, 16(22): 3394-3397, 3403. [19] 刘福梅, 谢雁鸣, 王志飞, 等. 碟脉灵(R)苦碟子注射液治疗脑梗死的临床综合评价[J]. 中国中药杂志, 2021, 46(23): 6105-6113. [20] 王海银, 符雨嫣, 覃肖潇, 等. 药品临床综合评价: 保障临床基本用药合理使用[J]. 中国卫生, 2021,432(8): 72-73. [21] 石秀园, 赵锐, 李璠, 等. 构建我国药品临床综合评价工作机制的思考[J]. 中国药房, 2020, 31(23): 2828-2833. [22] 张强, 王志飞, 谢雁鸣, 等. 中成药临床综合评价报告规范[J]. 中国中药杂志, 2021, 46(23): 6062-6067. [23] 夏如玉, 金雪晶, 柴倩云, 等. 运用多准则决策分析法的中药临床综合评价文献特征分析及设计要点[J]. 中医杂志, 2022, 63(2): 119-124. -





 下载:
下载:
 下载:
下载: