-
肥胖是一种慢性代谢性疾病,是指由于能量摄入超过消耗,导致体内脂肪积聚过多或分布异常而造成体重增加的一种疾病。肥胖会提高 2 型糖尿病、高血压、血脂异常、心血管疾病和某些癌症的发病率[1-3],降低生活质量并增加死亡风险。减肥手术是最有效的减肥方法[4],但手术有潜在的风险和限制,且无法满足全球范围内患者的医疗需求。改善饮食结构、生活方式以及增加身体活动等短期行为干预也不足以达成长期减肥的目的[5]。因此,药物治疗是中、重度肥胖患者以及有并发症的轻度肥胖患者的首要治疗选择[6]。
多年来,减肥药物有着坎坷曲折的研发历程,获批数量有限且许多已经上市的药物最终因心血管问题等不良反应而撤市,如盐酸氯卡色林(5-羟色胺2C受体激动剂)、西布曲明(抑制去甲肾上腺素和5-羟色胺再摄取)等。因此,全球各大药物监管机构对减肥药物的批准一直非常严格。目前,全球共有8种上市的减肥药物,包括赛利司他(脂肪酶抑制剂)、奥利司他(脂肪酶抑制剂)、复方芬特明-托吡酯(肾上腺素受体激动剂与α-氨基-3-羟基-5-甲基-4-异噁唑丙酸受体拮抗剂)、复方纳曲酮-安非他酮(肾上腺素吸收抑制剂与多巴胺摄取抑制剂)、二甲双胍(单磷酸腺苷活化蛋白激酶激动剂)、苄非他明(肾上腺素受体激动剂)以及最新批准的利拉鲁肽和司美格鲁肽(GLP-1受体激动剂)。然而,这些上市减肥药物的耐受性和安全性也受到挑战,如奥利司他会导致严重的脂肪泻;利拉鲁肽价格昂贵,存在恶心等胃肠道反应,不易推广。匮乏的减肥药物市场亟需基于新靶点的全新减肥药物以应对肥胖日益严峻的发病形势。
ORM(Orosomucoid),也称为α1酸性糖蛋白(AGP),是肝脏急性期反应蛋白[7]。ORM在人体中有2种亚型(ORM1和ORM2),小鼠中有3个亚型(ORM1、ORM2和ORM3),大鼠中仅有1种型。在人和小鼠体内,ORM1的组成水平远高于ORM2(5倍),并且只有ORM1可以被急性期刺激诱导。ORM具有转运药物、调节免疫、维持毛细血管屏障等功能[8]。团队前期研究发现,ORM具有能量代谢的调节作用,循环中的ORM可以作用于下丘脑的瘦素受体,激活JAK2-STAT3通路,抑制摄食、降低体重、改善胰岛素抵抗[9]。本团队进一步以ORM为靶点,筛选到了一个靶向上调内源性ORM的全新小分子化合物HMS-01,在瘦素缺陷的ob/ob肥胖小鼠和高脂喂食的肥胖小鼠上,均展示了良好的减肥效果,在国家重大新药创制资助下,已经进入到临床前研究阶段。这些研究均提示,ORM是一个治疗肥胖的全新潜在靶点[9], 靶向上调内源性ORM的小分子有可能发展为新型减肥药物。
然而,新的减肥药物研发面临高投入、低回报的困境,传统新药研发需要消耗10~15年的时间,以及约25亿美元的投入,而达到Ⅲ期临床试验最后阶段的药物中有 50% 最终无法被批准上市[10],每一次失败都会消耗大量的时间与资源。药物重定位是一种药物发现和开发的策略,旨在重新评估已经开发或研究的药物,以寻找其在新的疾病领域或治疗应用中的潜在价值。该策略的目的是最大化已有药物的利用,降低新药开发的时间和成本。本研究利用基因重组技术构建了含有ORM1启动子上游2 000个碱基对序列的荧光素酶报告基因,由于ORM主要由肝脏合成,通过血液分泌至全身发挥作用,于是选用AML12小鼠正常肝细胞构建了稳定表达LV-ORM1 启动子-LUC-PURO的细胞株,从而建立了一个以ORM为靶点的药物筛选平台和评价体系,用于高通量筛选上市药物库中靶向ORM的药物,为药物重定位发现潜在减肥药物奠定基础。
-
AML12小鼠正常肝细胞、HEK-293T上皮细胞、载体pGL4.20[luc2/Puro] 与pHBLV-CMV-MCS-EF1-puro、慢病毒包装辅助质粒pMD2.G和psPAX2均为实验室保存;DH5α感受态细胞(天根生化科技有限公司);ORM1 启动子基因序列来自NCBI数据库(NC_000070.7)。
-
Veriti™ 96 孔快速热循环仪(Thermo Fisher Scientific公司,美国);移液器、低温高速台式离心机(EPPENDORF公司,德国);电热恒温培养箱(上海跃进医疗器械有限公司);琼脂糖凝胶电泳仪、多功能水平电泳槽(上海天能科技有限公司);电热恒温水浴锅(上海一恒科技有限公司);倒置生物显微镜(重庆光电仪器总公司);全波长多功能酶标仪(BMG,德国)。
-
PCR引物和基因合成(生工生物工程股份有限公司);RNA提取试剂盒RNAeasy™动物RNA抽提试剂盒(上海碧云天生物技术有限公司);限制性内切酶KpnI、限制性内切酶Hind Ⅲ、限制性内切酶AgeI、限制性内切酶ApaI、限制性内切酶ClaI、限制性内切酶BamHI、转染试剂Lipofectamine 3000试剂盒(Thermo Fisher Scientific公司,美国);高保真聚合酶phanta Max-Super-Fidlity DNA polymerase(南京诺唯赞生物科技股份有限公司);PCR试剂盒2X Pro Taq 预混液、反转录试剂盒Evo M-MLV 反转录试剂预混液、SYBR Green Pro Taq HS 预混型 qPCR 试剂盒(湖南艾科瑞生物工程有限公司);琼脂糖凝胶 DNA 纯化回收试剂盒、质粒小提试剂盒(天根生化科技有限公司);HB-infusionTM 无缝克隆试剂盒(汉恒生物科技有限公司);转染试剂polybrene(Sigma,美国);Firefly-Glo萤光素酶报告基因检测试剂盒(大连美仑生物技术有限公司);FDA 上市药物库(陶术生物科技有限公司);测序由赛业生物科技有限公司完成。
-
提取小鼠新鲜的肝组织,使用RNAeasy™动物RNA抽提试剂盒提取总RNA,反转录为cDNA,用作PCR模板,保存于−20 ℃冰箱。
-
根据同源重组引物设计原则和参考小鼠ORM1(NC_000070.7)基因组序列设计引物(选取起始位点上游2 000个碱基对),采用同源重组法设计引物,上游引物加入KpnI酶切位点,下游引物加入Hind Ⅲ酶切位点,引物序列见表1。产物进行琼脂糖凝胶电泳,使用琼脂糖凝胶DNA回收试剂盒回收目的基因。
表 1 ORM1 启动子基因引物序列
引物名称 引物序列(5′—3′) ORM1-F GGGGTACCGTTCTCAGCATGTTGCATAAAT ORM1-R CCAAGCTTGCTGAGGGCACTCAGAGC 注:F: 正向引物; R: 反向引物。 -
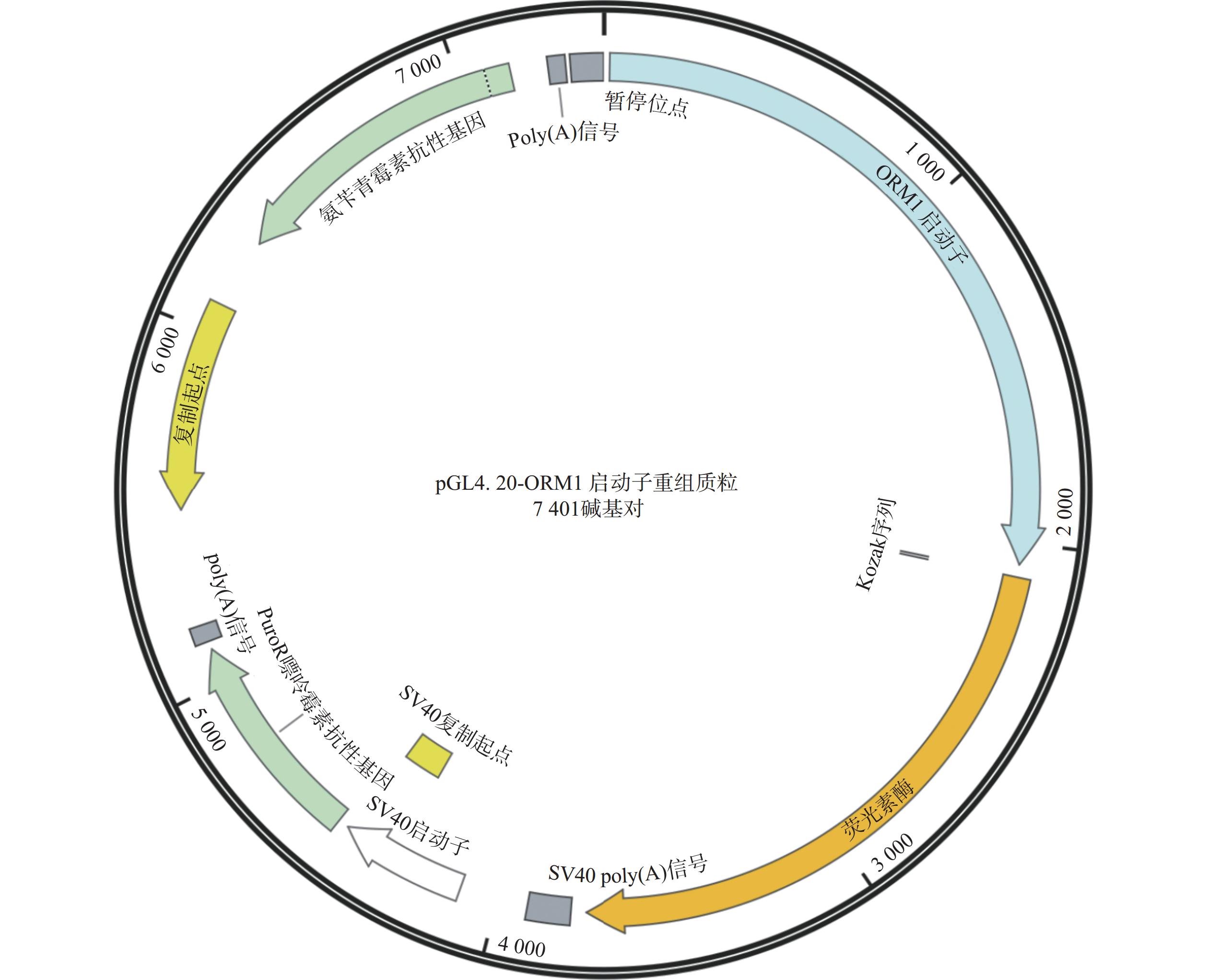
将PCR产物与载体质粒pGL4.20 [luc2 Puro](插入位点选择AgeI与ApaI)于37 ℃双酶切5 h,用同源重组酶将目的片段与载体质粒连接。使用DH5α感受态细胞将重组质粒进行转化后,接种于含有嘌呤霉素抗性的固体平板,用涂布器将重组质粒涂抹均匀,倒置37 ℃恒温箱培养12~16 h。将筛选出来的阳性克隆进行测序,随后进行菌液扩增和质粒抽提纯化。对提取的质粒进行浓度检测和A260/280检测,把质粒保存于−20 ℃冰箱。构建成功的重组载体命名为 pGL4.20-ORM1 启动子。根据Lipofectamine 3000试剂盒说明书,分别将pGL4.20-ORM1 启动子和pGL4.20转染至AML12小鼠正常肝细胞中,使用地塞米松(DXMS)来验证报告基因的有效性和可行性。
-
以pGL4.20-ORM1 启动子重组质粒为模板,设计引物,引物序列见表2。产物进行琼脂糖凝胶电泳,使用琼脂糖凝胶DNA回收试剂盒回收目的基因。
表 2 LV-ORM1 启动子-LUC-PURO基因引物序列
引物名称 引物序列(5′—3′) LV-ORM1
启动子-LUC-PURO-FGGACAGCAGAGATCCAGTTTATCGATGTTCTCAGCATGTTGCATAAATT LV-ORM1
启动子-LUC-PURO-RGAGCGATCGCAGATCCTTAGGATCCTTACACGGCGATCTTGCCGCCCTT 注:F: 正向引物; R: 反向引物。 将PCR产物与载体质粒pHBLV-CMV-MCS-EF1-PURO(插入位点选择ClaI与BamHI)于37 ℃双酶切5 h,用同源重组酶将目的片段与载体质粒连接。使用DH5α感受态细胞将重组质粒进行转化后,接种于含有嘌呤霉素抗性的固体平板,用涂布器将重组质粒涂抹均匀,倒置37 ℃恒温箱培养12~16 h。将筛选出来的阳性克隆,送赛业生物科技有限公司进行测序。测序成功之后,进行菌液扩增和质粒抽提纯化。对提取的质粒进行浓度检测和A260/280检测,把质粒保存于−20 ℃冰箱。构建成功的重组载体命名为LV-ORM1 启动子-LUC-PURO。同样方法构建LV-LUC-PURO作为对照载体。
-
提前传代HEK-293T细胞用于转染,将慢病毒包装辅助质粒pMD2.G 10 μg、psPAX2 5 μg和LV-ORM1 启动子-LUC-PURO 10 μg以及转染试剂75 µl混匀后静置,在室温下温育15 min后缓慢滴加至293T细胞中,于37 ℃、5% CO2细胞培养箱中培养。转染后16 h更换含10 % 胎牛血清 FBS的新鲜完全培养基。转染后 48 h和72 h,分别收集两次病毒上清液(48 h收集后置换新鲜完全培养基),将两次收集的上清液混合,进行离心浓缩和病毒管分装,−80°C冰箱保存。
-
将生长状态良好的HEK-293T细胞消化计数后稀释至 1×105个/ml, 加入96孔板,100 µl/孔,为每个病毒准备6个孔。放入37°C 、5% CO2 培养箱中培养。将病毒进行3倍梯度稀释,共6个稀释度,接种于293T细胞,继续培养48 h后,在荧光显微镜下观察结果。在观察结果前6 h需更换新鲜10% FBS完全培养基,从孔中吸出80 µl培养基,然后加入80 µl新鲜10 % FBS完全培养基,放入37°C、5% CO2 培养箱中培养。6 h后荧光显微镜下观察结果,荧光或活细胞百分比在10%~50% 的孔计算病毒滴度。目的病毒命名为LV-ORM1 启动子-LUC-PURO。同样方法,阴性对照病毒命名为LV-LUC-PURO。
-
将AML12小鼠正常肝细胞在含有10% FBS、1% ITS(10 µg/ml胰岛素+5.5 µg/µl转铁蛋白+5 ng/ml硒)、1% 双抗以及40 ng/ml DXMS的DMEM 培养基,于37 ℃、5% CO2饱和湿度的细胞培养箱内培养。AML12细胞在10 cm培养皿中细胞长满以后,用0.25%胰蛋白酶消化,离心收集细胞后稀释成密度为1.5×105个/ml的细胞悬液,接种于6孔板,每孔2 ml,使得第2天细胞的融合率在60% 左右,利于感染。设置实验组LV-ORM1 启动子-LUC-PURO和阴性对照组LV-LUC-PURO,为促进病毒的感染效率,首先,感染时弃原有培养基,添加含5% FBS的新鲜培养液2 ml,其次,添加助感染试剂polybrene,使其最终浓度为7 μg/ml。设置2个(10/20)感染复数(MOI)组,感染24 h后换新鲜完全培养基。在感染48 h后,观察慢病毒颗粒感染效率,倒置荧光显微镜下观察荧光比例以确定最佳感染效率,最终选定MOI=20的分组进行后续实验。
待细胞融合率达60% 时,用嘌呤毒素(0.8 μg/ml)浓度处理48 h,然后换新鲜的嘌呤毒素培养基继续处理,细胞密度超过80%时则进行传代处理,后续每隔2~3 d更换含嘌呤毒素培养基扩大培养,经过反复挑取抗药性细胞后获得的稳定转染细胞,命名为LV-AML12-ORM1 启动子-LUC-PURO。同样方法,阴性对照细胞株命名为LV-AML12-LUC-PURO。
-
使用TRIzol试剂提取组织总RNA,使用反转录试剂盒将其逆转录成cDNA,然后进行PCR扩增,采用2–ΔΔCT分析目的基因的相对表达量,引物序列见表3。
表 3 qPCR引物设计序列
引物名称 引物序列(5′—3′) Luciferase-F CGCACATATCGAGGTGGACA Luciferase-R GCAAGCTATTCTCGCTGCAC mGapdh-F GTCAAGGCCGAGAATGGGAA mGapdh-R CTCGTGGTTCACACCCATCA 注:qPCR: 实时荧光定量聚合酶链式反应; mGapdh:小鼠甘油醛-3-磷酸脱氢酶; F: 正向引物; R: 反向引物。 -
使用二甲基亚砜(DMSO)和DXMS来验证LV-AML12-ORM1 启动子-LUC-PURO作为药物筛选工具的有效性和可行性。将LV-AML12-ORM1 启动子-LUC-PURO稳转细胞株培养于96孔黑色侧壁透明底板,用10 μmol/L DXMS处理12 h,同时用0.1% DMSO作为溶剂对照组。参照荧光素酶报告基因检测试剂盒说明书,加入80 µl检测溶液,细胞充分裂解后在酶标仪中检测荧光素发光值。
为了评估本高通量细胞筛选平台的精确性和稳定性,使用Z′因子作为度量标准,Z′因子是高通量筛选中常用来评估和验证的主要统计参数之一:
$$Z^{\prime}=1-\frac{3 \sigma_{\mathrm{DMSO}}+3 \sigma_{\mathrm{DXMS}}}{\left|\mu_{\mathrm{DMSO}}-\mu_{\mathrm{DXMS}}\right|}$$ 式中σDMSO和σDXMS分别为阴性对照组和阳性对照组的标准差,μDMSO和μDXMS分别为阴性对照组和阳性对照组的平均值。若0.5<Z′≤1,则认为此筛选模型具有良好的精确性与稳定性。
-
基于对美国食品药品监督管理局(FDA)批准的药物库的筛选,选用陶术生物的FDA上市药物库,筛选可靶向升高ORM的药物。
-
实验数据使用软件 GraphPad Prism 9 进行作图和分析。两组间比较用t检验,以 P<0.05 为差异具有统计学意义。
-
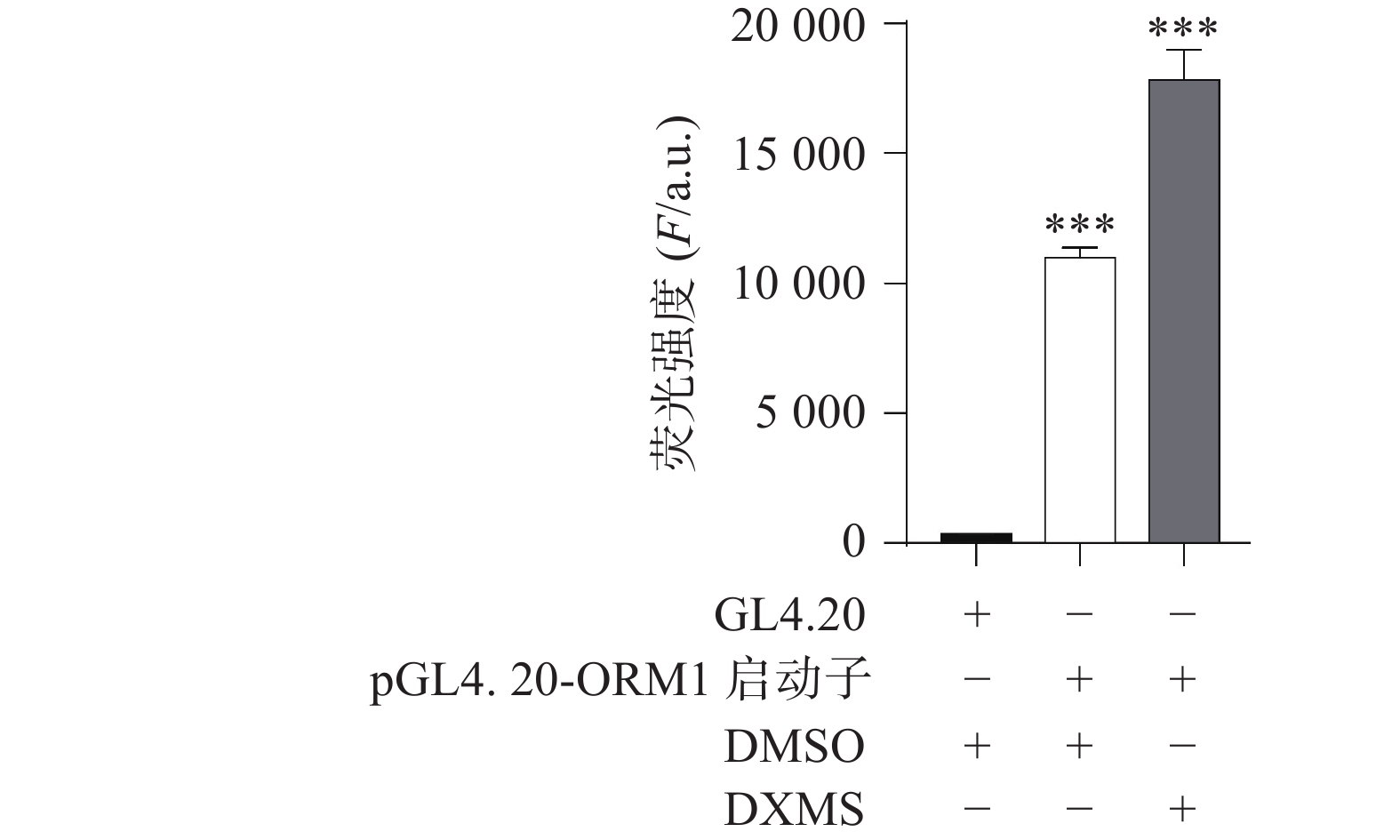
测序结果表明ORM1的启动子基因插入正确,如图1所示,序列信息无误。根据Lipofectamine 3000试剂盒说明书转染AML12细胞,使用荧光素酶报告基因试剂盒和酶标仪检测发光值,如图2所示,荧光素成功导入报告基因pGL4.20-ORM1 启动子中,并且可以被DXMS激活,证明该启动子的转录活性可用于稳转细胞株的构建。
-
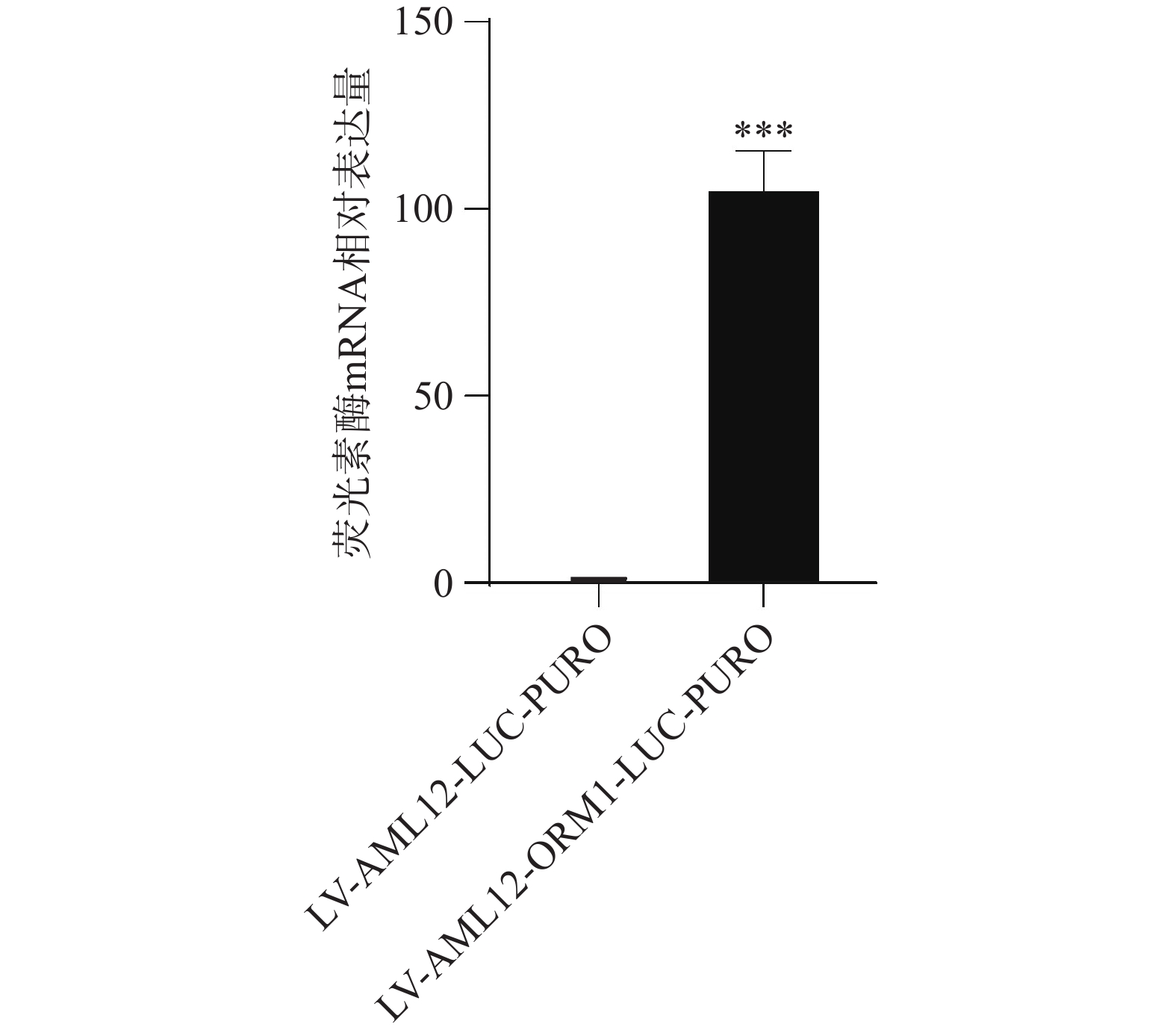
采用qPCR分别对稳转细胞株LV-AML12-LUC-PURO与LV-AML12-ORM1 启动子-LUC-PURO进行荧光素 mRNA水平检测,如图3所示,其中,荧光素基因在LV-AML12-ORM1 启动子-LUC-PURO稳转细胞中的相对表达量是对照组LV-AML12-LUC-PURO的104.06倍。
-
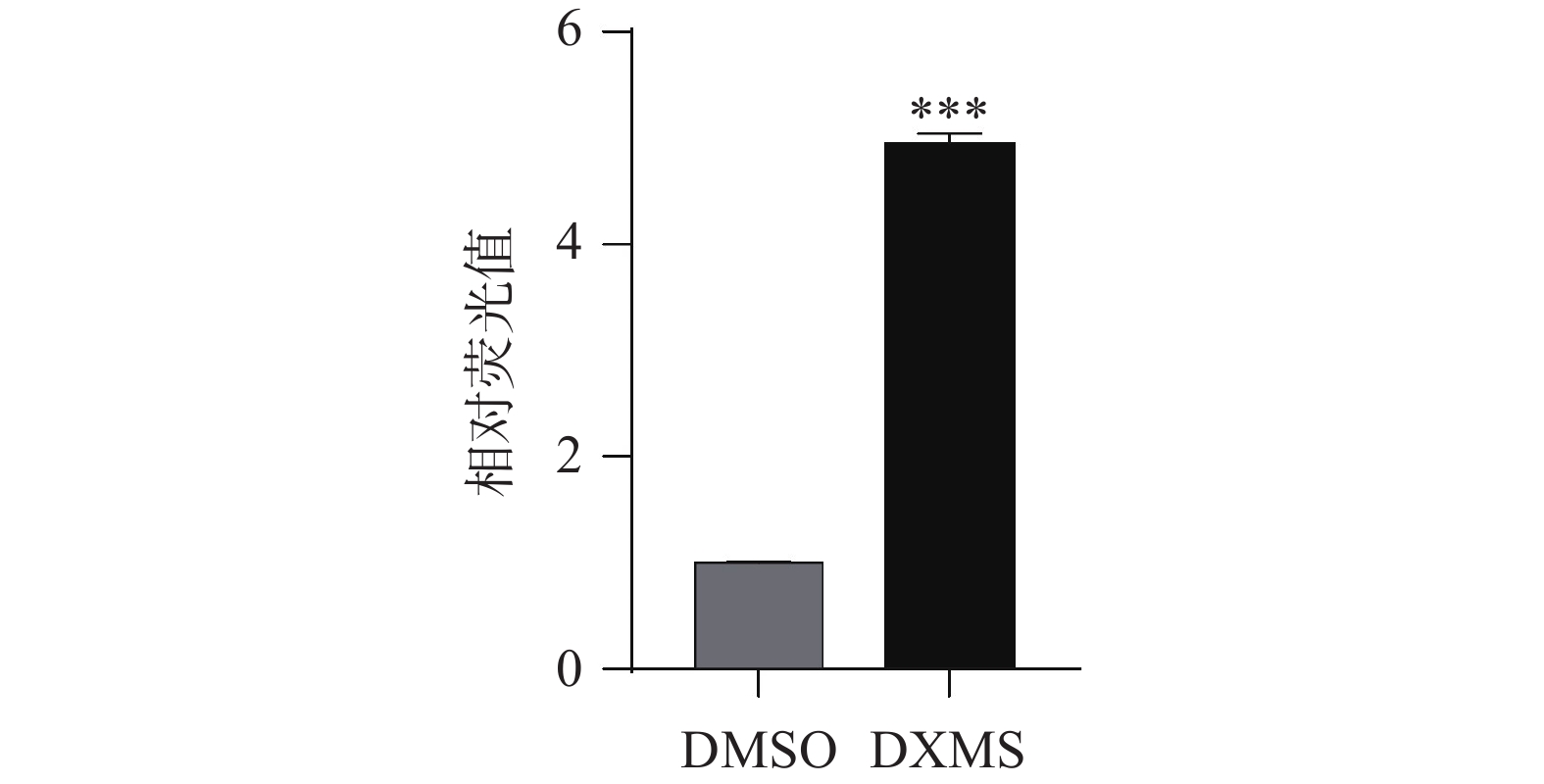
使用荧光素酶报告基因试剂盒和酶标仪检测发光值,如图4所示。DXMS的发光值是DMSO对照组的4.95倍。通过计算数据得Z′=0.77,说明此筛选平台可以作为一种高通量筛选的稳定方法。
-
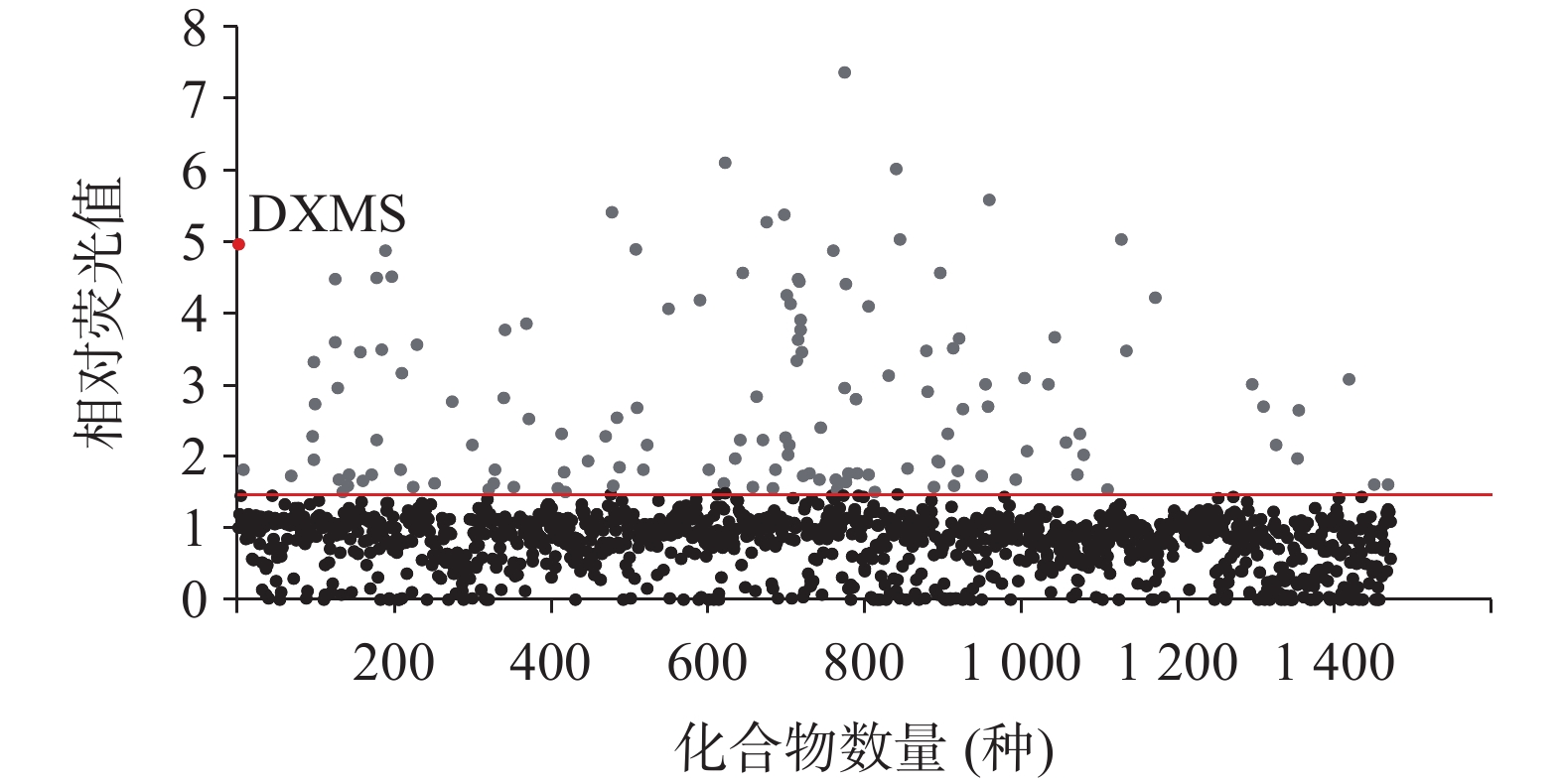
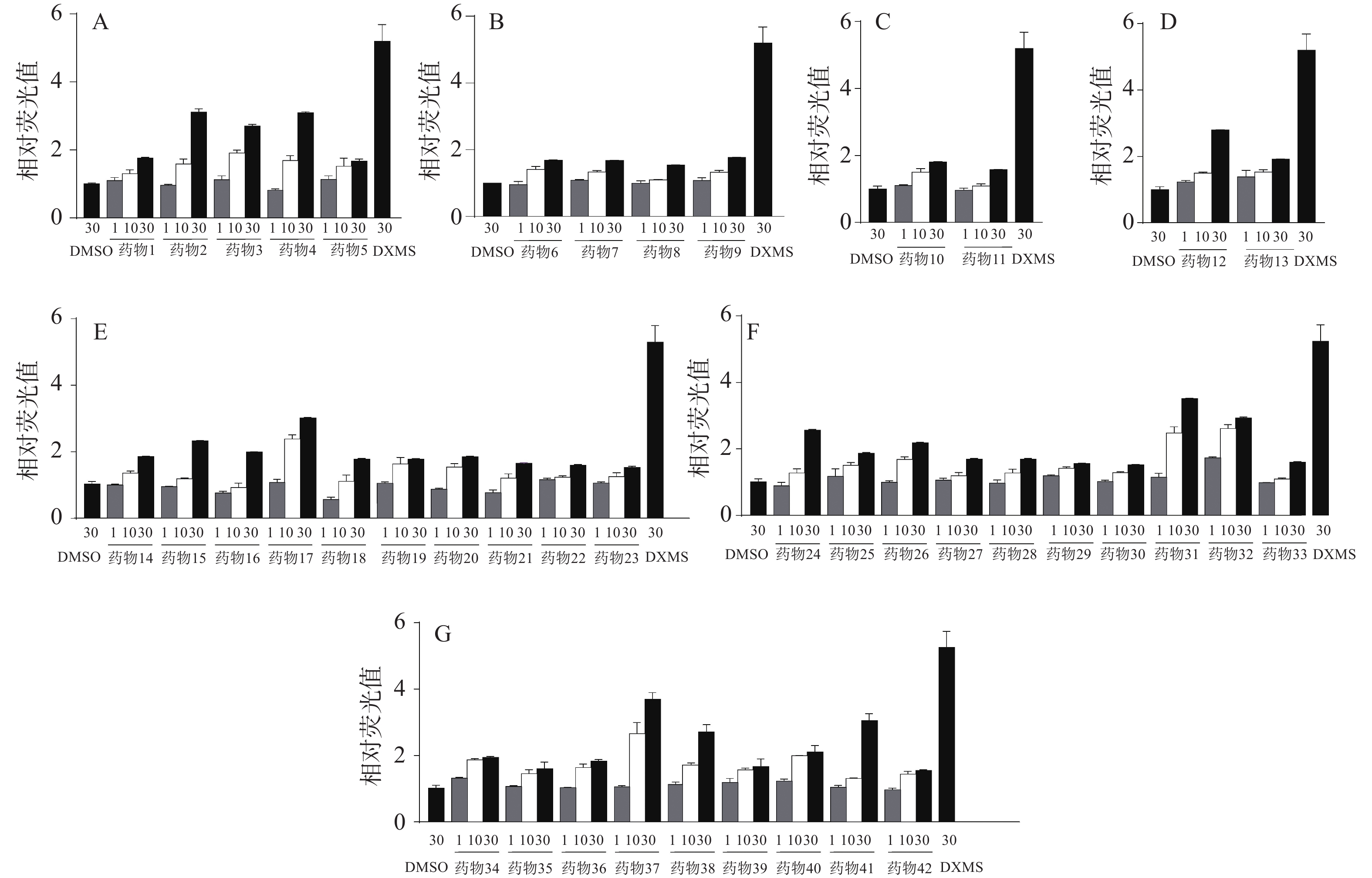
通过对陶术生物的FDA上市药物库1 470种化合物筛选,以30 μmol/L的较高浓度初筛,将荧光值比率>1.5的135种化合物作为初步命中的化合物,如图5所示。这135种药物中包含40种糖皮质激素类药物,但由于长期服用糖皮质激素易出现向心性肥胖,这与减肥的初衷相悖,所以将这些药物排除。之后将剩余的95种药物进行30、10、1 μmol/L浓度的复筛,避免单一浓度筛选实验出现假阳性。根据复筛结果,42种化合物呈现出量效关系的趋势,如图6所示,这些化合物的类别可分为抗肿瘤药(图6A)、抗生素(图6B)、抗炎药(图6C)、抗病毒药(图6D)以及其他药物(图6E~G)。
-
本课题组基于药物重定位的方法,通过构建带有ORM启动子的稳转细胞株作为高通量筛选平台,Z′因子的值为0.77,证明此细胞筛选平台可作为一种高通量筛选的稳定方法。经过初筛和复筛后,筛选出42种小分子药物,这些药物可能是潜在的以ORM作为靶点并能发挥减肥作用的药物。中国科学院上海生命科学研究院和上海中医药大学通过合作研究这种高通量化合物筛选发现的方式,成功发现舒尼替尼作为一种新的激活褐色脂肪组织(BAT)的小分子,是治疗肥胖等相关代谢性疾病的潜在药物[11]。
本课题组下一步将对这42种小分子药物进行体内验证实验,拟使用各个药物临床实验的安全范围内的剂量,在高脂饮食(HFD)小鼠模型中给药,观察药物能否显著抵抗高脂饮食诱导的肥胖,肝脏组织和血清中ORM的含量是否被上调,以及在ORM敲除的肥胖小鼠上观察药物的效应是否消除,从而确定其ORM靶点效应。
综上所述,本课题组为ORM靶向药物提供了一个快速细胞筛选平台,并从FDA上市药物库中筛选出了靶向上调ORM的潜在治疗肥胖的药物,为下一步减肥作用的观察奠定了基础。对这些药物及其潜在机制的研究可能会为减肥药物的发现和脂肪功能的新调节途径提供新的线索。
Establishment of a high-throughput screening platform based on drug repurposing targeting alpha-1-acid glycoprotein and discovery of potential weight loss drugs
-
摘要:
目的 α1酸性糖蛋白(ORM)是减肥药物研发的新靶点。基于药物重定位,拟从已上市药物的化合物库中寻找可以靶向ORM的潜在减肥药物。 方法 构建pGL4.20-ORM1 启动子重组质粒,验证后利用慢病毒载体构建稳定表达ORM1 启动子-LUC-PURO的AML12细胞株,利用该细胞株对上市药物库中化合物进行高通量筛选,通过酶标仪对细胞的荧光值进行表征。 结果 对1 470种化合物进行初筛和复筛,发现42种化合物可以提高ORM1启动子表达,可用于进一步的减肥效应评估。 结论 通过慢病毒载体成功构建了LV-AML12-ORM1 启动子-LUC-PURO稳定表达细胞株,为高效、稳定筛选靶向ORM的减肥药物奠定了基础。 Abstract:Objective Alpha-1-acid glycoprotein (ORM) was a new target for the development of weight loss drugs. To search for potential weight loss drugs that could target ORM from the compound library of already marketed drugs based on drug repurposing. Methods The pGL4.20-ORM1 promoter recombinant plasmid was contructed and validated, and then a lentiviral vector was utilized to establish stable AML12 cell lines expressing ORM1 promoter-LUC-PURO. This cell line was employed for high-throughput screening of compounds from the marketed drug library, and the luminescence value of the cells was characterized by enzyme marker. Results Primary screening and secondary screening of 1 470 compounds identified 42 compounds that increased ORM1 promoter expression and could be used for further weight loss effect assessment. Conclusion This study successfully constructed LV-AML12-ORM1 promoter-LUC-PURO stable expression cell lines using lentiviral vectors, laying a foundation for efficient and stable screening of weight loss drugs targeting ORM. -
Key words:
- drug repurposing /
- ORM /
- high-throughput screening /
- obesity /
- weight loss drugs
-
夏枯草消瘤合剂由中药夏枯草、牡蛎、生地黄、莪术、苍术、白术组成,是中医肿瘤学专家钱伯文教授的经验方。方中诸药配伍,以达化痰软坚,活血化瘀,补养气血的功效。其临床实验研究已证实,该药配合一线化疗方案治疗中晚期非小细胞肺癌患者,有助于提高患者的生存治疗和减少化疗所产生的毒副作用[1]。由该方制成的合剂在我院临床使用多年,前期研究对于组方中化学成分的研究仍限于迷迭香酸、咖啡酸的稳定性研究[2]。尽管方中一些单味药的化学成分已有报道[3-18],但是整个复方制剂的化学成分未见报道。由于组分的复杂性,复方的成分分析比单味药更具有挑战性,明确夏枯草消瘤方色谱图中各个色谱峰归属对于该复方的质量控制及体内深入研究具有重要意义。
高效液相-高分辨飞行时间质谱(HPLC-TOF/MS)串联技术对于中药复杂体系中化学成分分析和鉴定非常有效。其灵敏度高、操作简便、耗时短,可以在短时间获得化合物准确的相对分子质量,通过与所建立的已知化学成分数据库比对,可以快速的对被测成分进行分析鉴别[19-20]。因此,本文采用HPLC-TOF/MS技术,首次对夏枯草消瘤方中化学成分进行鉴别,并且对各成分进行药材归属,以进一步阐明夏枯草消瘤方的化学物质基础。
1. 材料和方法
1.1 仪器
Agilent 1100系列高效液相色谱仪(美国安捷伦公司),配有在线脱气机、四元泵、自动进样器、柱温箱和二级管阵列检测器;Agilent 6220高分辨飞行时间质谱仪(美国安捷伦公司),配有标准电子喷雾离子源(ESI);分析软件为 MassHunter 数据采集在线工作站和Qualiative Analysis 离线分析软件。
1.2 药品与试剂
咖啡酸(批号:110885-200102,纯度>98.5%)、迷迭香酸(批号:111871-201505,纯度>98.5%)对照品,均购自中国食品药品检定研究院,甲醇和甲酸为色谱纯(Fisher,USA),其余试剂均为分析纯,水为纯水。
夏枯草、生地黄、莪术、麸炒苍术、麸炒莪术、牡蛎、煅牡蛎均由上海中医药大学附属岳阳中西医结合医院中药房提供(见表1)。药材及饮片均经第二军医大学药学院生药学教研室黄宝康教授鉴定。
表 1 药材信息药材名称 批号 药材来源 夏枯草 180207 上海康桥药业有限公司 生地黄 180302 上海同济堂药业有限公司 莪术 180306 上海虹桥中药饮片有限公司 麸炒白术 2018031001 上海上药华宇药业有限公司 麸炒苍术 180407 上海虹桥中药饮片有限公司 牡蛎 2017102006 上海上药华宇药业有限公司 煅牡蛎 180301 上海同济堂药业有限公司 2. 方法
2.1 对照品溶液的制备
分别精密称取咖啡酸、迷迭香酸对照品3.22、5.68 mg置10 ml量瓶中,加甲醇稀释定容,配成浓度分别为322、568 μg/ml的母液,精密吸取母液 1 ml 置于 10 ml 量瓶,加甲醇定容后,即得对照品溶液。
2.2 供试品溶液的制备
精密称取夏枯草4.2 g、牡蛎8.4 g、煅牡蛎8.4 g、地黄4.2 g、莪术4.2 g、白术(麸炒)2.1 g、苍术(麸炒)2.1 g,以上七味,充分润湿,分别加8倍量与4倍量水煎煮两次,每次煮沸后于85 ℃保温20 min,煎液滤过,合并滤液,滤液浓缩至相对密度1.10以上(80 ℃),离心,取上清液;精密吸取夏枯草消瘤方溶液上清液5 ml,置于50 ml容量瓶中,加甲醇定溶,摇匀,经0.22 μm微孔滤膜滤过,取续滤液,即得夏枯草消瘤方样品溶液。
2.3 色谱条件
色谱柱:ACE C18(3.0 mm×150 mm),流动相A相为甲醇,B相为水(含0.1%甲酸),梯度洗脱:0~5 min:5%A,5~10 min:5%~15%A,10~30 min:15%~45%A,30~40 min:45%~70%B,40~50 min:70%~90%B;进样量2 μl,流速为0.4 ml/min;柱温为25 ℃;运行时间为50 min。
2.4 质谱条件
采用ESI离子源,正、负离子模式均进行检测,雾化器为高纯氮气,具体参数如下:正离子模式:毛细管电压3500 V,干燥器温度350 ℃,干燥器流速10L/min,雾化器压力40 psig,碎片电压160 V;参比离子m/z121.9856,1033.9881;扫描范围m/z100-1200。测定样品之前,使用调谐液校准质量轴,以保证质量精度误差小于1×10-6。
2.5 夏枯草消瘤方化学成分数据库的建立
根据国内外专业数据库中科院化学专业数据库、Pubmed、Chemspider等,以及国内外相关研究文献,收集了夏枯草消瘤合剂方中六味中药化学成分名称及分子式共760个。采用安捷伦“formula-database generator”软件(含各元素精确质量数),根据各成分碳、氢、氧的个数,计算精确相对分子质量、M+H和M-H准分子离子峰相对分子质量的相应的化学成分数据库。
3. 结果和讨论
3.1 夏枯草消瘤合剂的相关图谱
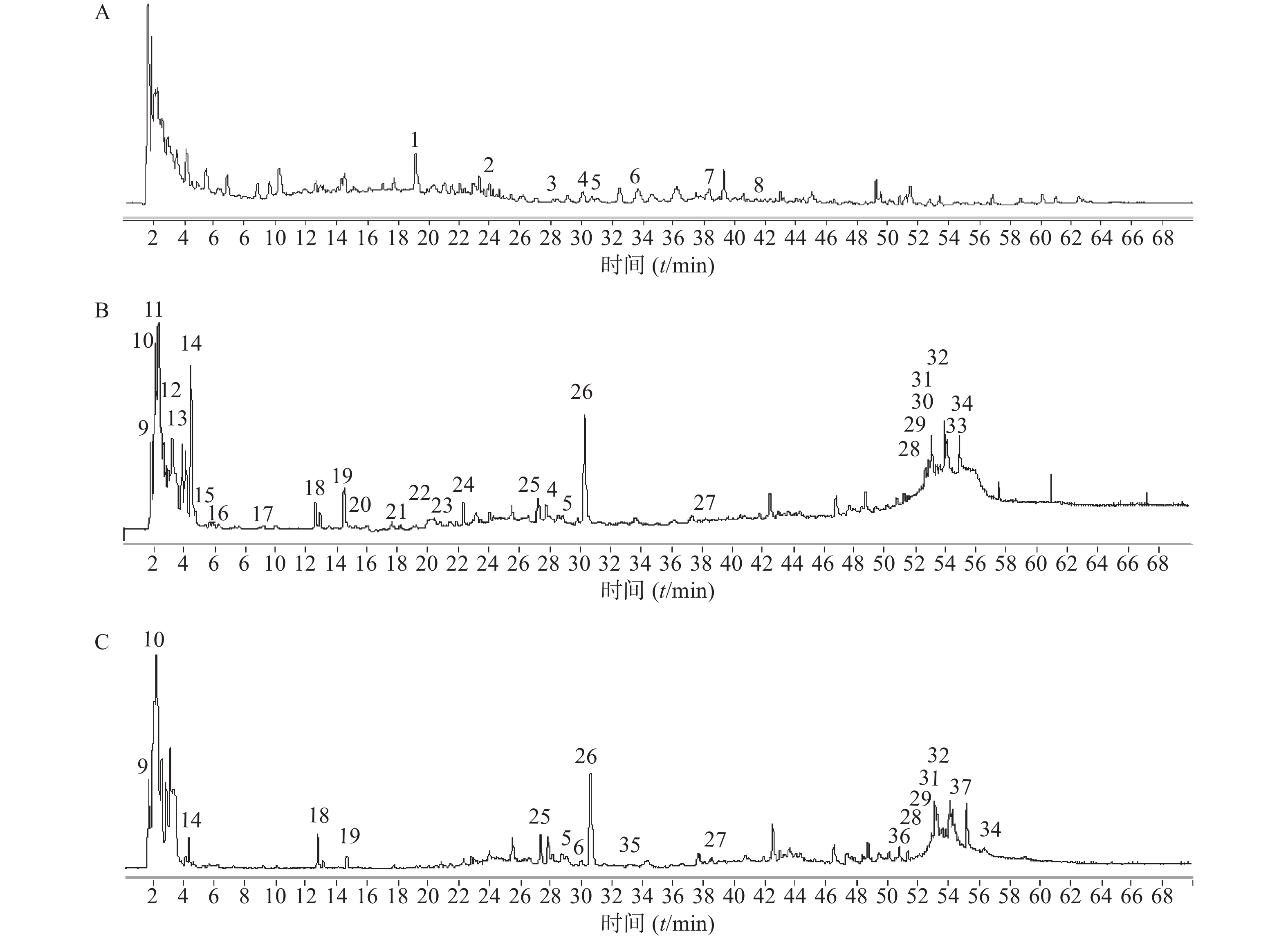
夏枯草消瘤方样品溶液的总离子流图见图1。其中图1A为正离子160 V模式,图1B为负离子160 V模式,图1C为负离子260 V模式。
3.2 利用对照品鉴别化合物
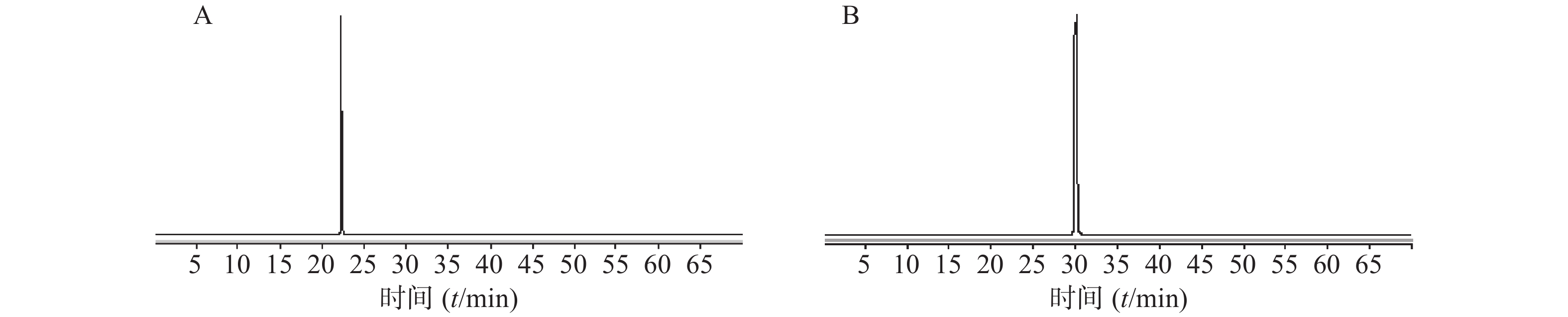
实验中利用已有的2个对照品,在负离子模式、碎片电压160 V条件下,无偏差的鉴别出咖啡酸、迷迭香酸,对照品总离子流图见图2。
3.3 利用精确质量数和同位素分布鉴别化合物
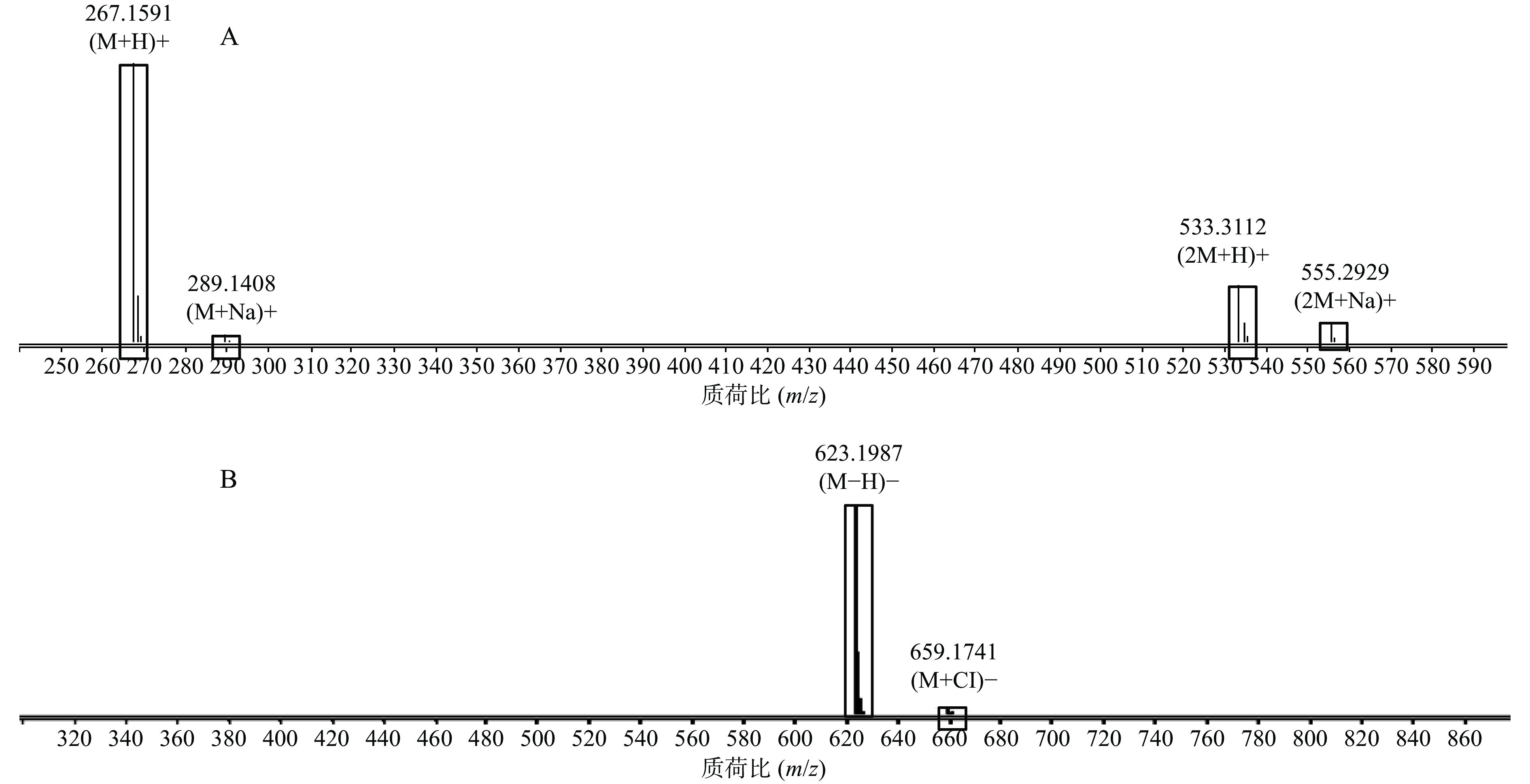
正离子模式下以图1中2号峰疣孢酚为例,说明夏枯草消瘤方色谱峰的鉴别过程。保留时间为24.032 min,色谱图中的准分子离子为267.1591。利用Qualiative Analysis数据分析软件的计算功能计算精确质量数的可能元素组成(5×10−6),并比对数据库中已知化合物的质荷比,初步确定元素组成为C15H22O4,为疣孢酚的(M+H)+。计算该准分子离子的核素分布情况,从图3A可以看出同位素分布的理论值(方框所示)与实际值(方框内峰所示)吻合良好,确定此峰为疣孢酚。同理可得负离子模式下图1中18号峰,地黄苷D的解析过程(图3B)。
3.4 夏枯草消瘤合剂化学成分鉴别结果
根据飞行时间质谱测得精确的相对分子质量,比对所建立的数据库,应用Qualiative Analysis 质谱分析软件计算分子组成,将理论值与实测值进行比对,结合上述对照品鉴别结果及相关文献报道,对夏枯草消瘤合剂中药材在正、负离子模式下所得色谱图中色谱峰进行分析,初步鉴别出37个化学成分,结果见表2、表3。对于部分未见区分的同分异构体,后期可考虑调节碎片电压获得化合物的裂解规律进行区分。
表 2 夏枯草消瘤合剂中化学成分的正离子模式鉴别结果序号 相对时间(min) 化合物 分子式 M+H 实验值(m/z) 理论值(m/z) 误差(×10–6) 来源 1 19.174 7-羟基异喹啉 C9H7NO [M+H]+ 146.060 8 146.052 8 –0.72 地黄. 2 24.032 Verrucarol C15H22O4 [M+H]+ 267.159 1 267.151 8 0.06 莪术 3 28.388 白术内酯Ⅱ C15H20O2 [M+H]+ 233.153 3 233.146 3 1.49 白术. 41) 30.653 芦丁 C27H30O16 [M+H]+ 611.160 8 611.153 4 –0.27 夏枯草 51) 30.703 槲皮素-3-O-β-D-葡萄糖苷 C21H20O12 [M+H]+ 465.102 9 465.095 5 –0.25 夏枯草 61) 33.713 伞形酮 C9 H6 O3 [M+H]+ 163.038 7 163.031 7 1.54 夏枯草 7 38.337 白术内酯Ⅲ C15H20O3 [M+H]+ 249.148 2 249.141 2 2.05 白术 81) 41.969 十四烷基柠檬酸 C20H36O7 [M+H]+ 389.252 9 389.246 1 1.31 白术 注:1)表示正负模式下测得 表 3 夏枯草消瘤合剂中化学成分的负离子模式鉴别结果序号 相对时间(min) 化合物 分子式 M+H 实验值(m/z) 理论值(m/z) 误差(×10–6) 来源 91) 1.999 精氨酸 C6H14N4O2 (M-H)– 173.104 3 173.111 7 0.56 地黄 101) 2.109 葡萄糖酸 C6H12O7 (M-H)– 195.051 1 195.058 3 –0.23 夏枯草 11 2.789 苹果酸 C4H6O5 (M-H)– 133.014 3 133.021 5 –0.61 夏枯草 12 2.842 柠檬酸 C7H12O6 (M-H)– 191.019 5 191.027 0 1.04 夏枯草 13 3.305 二氢梓醇 C15H24O10 (M+CHO2)– 409.134 8 409.136 9 0.88 地黄 141) 4.441 梓醇 C15H22O10 (M+CHO2)– 407.118 8 407.121 2 2.01 地黄 15 4.724 尿嘧啶核苷 C9H12N2O6 (M-H)– 243.062 2 243.069 5 0.43 地黄 16 5.869 络氨酸 C9H11NO3 (M-H)– 180.066 4 180.073 9 1.28 地黄 17 9.186 鸟苷 C10H13N5O5 (M-H)– 282.084 1 282.091 7 1.12 地黄 181) 12.586 地黄苷D C27H42O20 (M+CHO2)– 731.225 6 731.226 9 –0.57 地黄 191) 14.46 丁香酸 C9H10O5 (M-H)– 197.045 3 197.052 8 1.48 地黄 20 14.562 益母草苷 C15H24O9 (M+Cl)– 383.111 1 383.642 0.88 地黄 21 18.189 原儿茶酸 C7H6O3 (M-H)– 137.024 5 137.031 7 –0.75 夏枯草 22 19.253 2, 3-二氢 -7-甲氧基-4 -甲基 -1H-1,
5 -苯并二氮卓 -2-酮C11H12N2O2 (M-H)– 203.082 5 203.089 9 0.52 苍术 23 21.839 地黄苦苷 C16H26O8 (M-H)– 345.155 3 345.162 8 0.41 地黄 24 22.327 咖啡酸 C9H8O4 (M-H)– 179.035 1 180.049 5 –0.9 白术 251) 27.255 异迷迭香酸苷 C24H26O13 (M-H)– 521.130 8 521.137 3 –1.42 夏枯草 42) 28.487 芦丁 C27H30O16 (M-H)– 609.146 1 609.153 4 0.08 夏枯草 52) 28.61 槲皮素-3-O-β-D-葡萄糖苷 C21H20O12 (M-H)– 463.088 1 463.095 5 0.26 夏枯草 261) 30.296 迷迭香酸 C18H16O8 (M-H)– 359.077 2 359.084 5 0.18 夏枯草 271) 38.237 异地黄苷 C31H40O15 (M-H)– 651.229 1 651.236 7 0.59 地黄 281) 52.394 表莪术酮 C15H28O2 (M-H)– 239.201 4 239.208 9 1.07 莪术 291) 52.687 肉豆蔻酸 C14H28O2 (M-H)– 227.201 7 227.208 9 –0.12 夏枯草 301) 52.748 熊果酸 C30H48O3 (M-H)– 455.353 455.306 3 0.17 夏枯草 311) 53.606 亚油酸 C18H32O2 (M-H)– 279.232 8 279.240 2 0.55 夏枯草 321) 53.911 软脂酸 C16H32O2 (M-H)– 255.233 4 255.240 2 –1.71 夏枯草 33 54.095 油酸 C18H34O2 (M-H)– 281.249 0 281.255 9 –1.43 夏枯草 341) 54.92 硬脂酸 C18H36O2 (M-H)- 283.264 5 283.271 5 –0.93 苍术 35 33.114 6-0-E阿魏酰基筋骨草醇 C25H32O12 (M-H)– 523.181 7 523.189 4 0.73 地黄 36 51.355 麝香草酚 C10H14O (M-H)– 149.097 1 149.104 5 0.28 夏枯草 37 54.305 11-十八烯酸- C18H34O2 (M-H)– 281.248 6 282.225 9 0.09 夏枯草 注:1)表示负模式下碎片电压160V和260V测得;2)表示正负模式下测得。 3.5 讨论
对色谱条件的摸索,考察了甲醇-水、乙腈-水系统,发现甲醇的洗脱效果优于乙腈,且各色谱峰分离效果更好,加入0.1%甲酸可以改善峰型,并提高质谱响应,故采用甲醇-0.1%甲酸水为流动相。由于本组方含有药材较多,组方内所含成分比较复杂,因此选择大梯度洗脱,以期最大程度地得到其中的化合物保留。质谱检测比较了正、负离子两种扫描模式,由于组方中所含多种化合物响应模式各有不同,因此,选择正、负离子两种扫描模式同时进行监测。对于碎片电压的选择,本方中大部分化学成分在160 V时以准分子离子峰形式稳定存在,有少量化学成分在负离子模式下260V时以准分子离子峰形式稳定存在,图谱本底较低,因此选择160 V、260 V的碎片电压可以最大限度地对复方中的成分进行鉴别。
4. 结论
本研究运用 HPLC-TOF/MS 技术快速鉴别夏枯草消瘤合剂中37种化学成分,其中正离子模式碎片电压160 V条件下8个;负离子模式碎片电压160 V条件下28个,碎片电压260 V条件下19个;正负离子均有响应4个,负离子模式两种碎片电压下均有响应16个,并对成分进行了药材归属。该方法在传统的植物化学分离提取基础上对色谱峰进一步明确化,为夏枯草消瘤方的质量控制、体内的深入研究及临床应用奠定了良好的基础。
-
表 1 ORM1 启动子基因引物序列
引物名称 引物序列(5′—3′) ORM1-F GGGGTACCGTTCTCAGCATGTTGCATAAAT ORM1-R CCAAGCTTGCTGAGGGCACTCAGAGC 注:F: 正向引物; R: 反向引物。 表 2 LV-ORM1 启动子-LUC-PURO基因引物序列
引物名称 引物序列(5′—3′) LV-ORM1
启动子-LUC-PURO-FGGACAGCAGAGATCCAGTTTATCGATGTTCTCAGCATGTTGCATAAATT LV-ORM1
启动子-LUC-PURO-RGAGCGATCGCAGATCCTTAGGATCCTTACACGGCGATCTTGCCGCCCTT 注:F: 正向引物; R: 反向引物。 表 3 qPCR引物设计序列
引物名称 引物序列(5′—3′) Luciferase-F CGCACATATCGAGGTGGACA Luciferase-R GCAAGCTATTCTCGCTGCAC mGapdh-F GTCAAGGCCGAGAATGGGAA mGapdh-R CTCGTGGTTCACACCCATCA 注:qPCR: 实时荧光定量聚合酶链式反应; mGapdh:小鼠甘油醛-3-磷酸脱氢酶; F: 正向引物; R: 反向引物。 -
[1] SERAVALLE G, GRASSI G. Obesity and hypertension[J]. Pharmacol Res, 2017, 122:1-7. doi: 10.1016/j.phrs.2017.05.013 [2] ALPERT M A, OMRAN J, BOSTICK B P. Effects of obesity on cardiovascular hemodynamics, cardiac morphology, and ventricular function[J]. Curr Obes Rep, 2016, 5(4):424-434. doi: 10.1007/s13679-016-0235-6 [3] TWIG G, YANIV G, LEVINE H, et al. Body-mass index in 2.3 million adolescents and cardiovascular death in adulthood[J]. N Engl J Med, 2016, 374(25):2430-2440. doi: 10.1056/NEJMoa1503840 [4] WOLFE B M, KVACH E, ECKEL R H. Treatment of obesity: weight loss and bariatric surgery[J]. Circ Res, 2016, 118(11):1844-1855. doi: 10.1161/CIRCRESAHA.116.307591 [5] BLÜHER M. Obesity: global epidemiology and pathogenesis[J]. Nat Rev Endocrinol, 2019, 15(5):288-298. doi: 10.1038/s41574-019-0176-8 [6] SQUADRITO F, ROTTURA M, IRRERA N, et al. Anti-obesity drug therapy in clinical practice: evidence of a poor prescriptive attitude[J]. Biomed Pharmacother, 2020, 128:110320. doi: 10.1016/j.biopha.2020.110320 [7] RUAN Y, XIANG K F, ZHANG H M, et al. Orosomucoid: a promising biomarker for the assessment of exercise-induced fatigue triggered by basic combat training[J]. BMC Sports Sci Med Rehabil, 2022, 14(1):100. doi: 10.1186/s13102-022-00490-6 [8] 徐栋平. 急性期蛋白ORM在缺血性脑卒中的保护作用及其机制研究[D]. 上海: 第二军医大学, 2018. [9] SUN Y, YANG Y L, QIN Z, et al. The acute-phase protein orosomucoid regulates food intake and energy homeostasis via leptin receptor signaling pathway[J]. Diabetes, 2016, 65(6):1630-1641. doi: 10.2337/db15-1193 [10] KORT E, JOVINGE S. Drug repurposing: claiming the full benefit from drug development[J]. Curr Cardiol Rep, 2021, 23(6):62. doi: 10.1007/s11886-021-01484-5 [11] QIU Y, SUN Y M, XU D Q, et al. Screening of FDA-approved drugs identifies sutent as a modulator of UCP1 expression in brown adipose tissue[J]. EBioMedicine, 2018, 37:344-355. doi: 10.1016/j.ebiom.2018.10.019 -





 下载:
下载:
 下载:
下载: