-
抗感染药物是指用以治疗病原体(病毒、衣原体、支原体、立克次体、细菌、螺旋体、真菌、蠕虫等)所致感染的各种药物,是临床常用的重要治疗药物之一[1]。然而,近年来随着抗感染药物品种增加、仿制药入市及临床不合理使用,导致其不良反应呈现逐步上升的趋势[2]。此外,羁押人员属于特殊群体,生活空间及范围受限、健康意识相对较差,易发生及传播感染性疾病,故而监管场所配备的医疗卫生机构对感染性疾病提供有效的抗感染治疗对羁押人员健康至关重要[3]。然而,目前鲜见针对羁押人员使用抗感染药物所致ADR特点及规律的研究。
帕累托图分析法(又称ABC分析法)是一种分析管理技术,它运用数理统计方法对事物及质量问题进行排队,抓主要矛盾,反映“关键的少数和次要的多数”的关系[4]。帕累托图分析法可用于药事管理领域,利于分析ADR及推动临床合理用药[5]。笔者率先将帕累托图法用于羁押人员抗感染类药物导致ADR的分析,明晰导致ADR的药物、种类及累及器官和(或)系统,为羁押人员合理使用抗感染药物提供科学依据。
-
收集2011年1月至2018年10月上报国家ADR监测系统的抗感染类药物ADR报告158例,依据国家ADR监测中心对ADR的判定方法,统计内容包括患者性别、年龄、既往过敏史、剂量、给药途径、引起ADR的药物种类、剂型、ADR累及器官及主要临床表现等。
-
将涉及ADR的药品按《新编药物学》(第17版)药品分类方法进行分类,对各类抗感染药物导致的ADR、累及器官和(或)系统、临床表现等病例数进行统计,并进行编号。以药物分类和各系统临床表现的例数序号为横坐标,以累计构成比为纵坐标,绘制帕累托图。帕累托图分析通常是将相关因素根据累计构成比不同,将影响因素分为A、B、C三类。其中,累计构成比在0%~80%区间的,称为主要因素,记为A类;累计构成比在80%~90%为次要因素,记为B类;累计构成比在90%~100%为一般因素,记为C类[4]。
-
158例抗感染类药物所致的ADR中,以男性为主(90.51%),20~59岁年龄人群ADR均占20%以上(表1)。
表 1 发生ADR患者的性别与年龄分布(n=158)
年龄(岁) 男性(例) 女性(例) 总例数 构成比(%) 20~29 33 1 34 21.52 30~39 30 3 33 20.88 40~49 35 2 37 23.42 50~59 38 7 45 28.48 ≥60 7 2 9 5.70 合计 143 15 158 100 -
158例ADR报告中,109例(68.99%)羁押人员联合使用药物,49例(31.01%)使用单药治疗;静脉滴注34例(21.52%),口服给药124例(78.48%)。关联性评价:肯定107例(67.72%),很可能48例(30.38%),可能3例(1.90%)。
-
158例抗感染类药物所致ADR药品分类见表2,帕累托图分析结果见图1。第1~2项累计构成比在0%~80%区间,为主要因素(A类),导致ADR的药物依次为抗结核类药物(利福平、异烟肼、吡嗪酰胺、乙胺丁醇、链霉素)和头孢菌素类药物(头孢唑啉、头孢曲松、头孢拉定)。第3项累计构成比在80%~90%区间,为次要因素(B类),导致ADR的药物主要是磺胺甲唑。第4~8项(抗病毒类、青霉素类、氨基糖苷类、氟喹诺酮类和硝咪唑类)累计构成比在90%~100%区间,为一般因素(C类)。
表 2 导致ADR药物种类分布(n=158)
序号 药品分类 例数 构成比(%) 累计构成比(%) 因素类型 1 抗结核药 103 65.19 65.19 A 2 头孢菌素 23 14.56 79.75 A 3 磺胺类 14 8.86 88.61 B 4 抗病毒类 8 5.06 93.67 C 5 青霉素类 3 1.90 95.57 C 6 氨基糖苷类 3 1.90 97.47 C 7 氟喹诺酮类 2 1.27 98.73 C 8 硝咪唑类 2 1.27 100.00 C -
抗感染类药物ADR累及器官和(或)系统及临床表现见表3,帕累托图分析结果见图2。第1~2项累计构成比在0%~80%区间,为主要因素(A类),系统损害主要累及肝胆系统、皮肤及其附件。第3项累计构成比在80%~90%区间,为次要因素(B类),系统损害主要体现全身性反应。第4~8项累计构成比在90%~100%区间,为一般因素(C类)。
表 3 ADR累及器官和(或)系统及临床表现
序号 累及系统 主要临床表现 例数 构成比(%) 累计构成比(%) 因素类型 1 肝胆系统 肝功能异常、肝细胞损害、肝炎、转氨酶升高、尿素氮升高 95 60.13 60.13 A 2 皮肤及其附件 皮疹、瘙痒、荨麻疹、斑丘疹 30 18.99 79.12 A 3 全身性反应 过敏性休克、变态反应、发热 17 10.76 89.88 B 4 血液系统 白细胞减少、贫血、骨髓抑制、血小板减少 6 3.80 93.68 C 5 消化系统 恶心、呕吐、腹泻、十二指肠溃疡 4 2.53 96.21 C 6 中枢及外周神经系统 耳鸣、神经炎、头晕、共济失调、惊觉、谵妄、脑电图异常 3 1.90 98.11 C 7 心血管系统 潮红、低血压、心悸 2 1.26 99.37 C 8 泌尿系统 肾功能异常 1 0.63 100.00 C -
在158例ADR病例中,严重ADR有62例(39.24%),新的ADR 3例(1.90%)。21例(33.33%)严重ADR经及时停药和(或)对症处理后痊愈;经对症处理后好转或痊愈的有65.08%(41例)。主要临床表现为肝功能损害、骨髓抑制、十二指肠溃疡,涉及的药物种类主要为抗结核类、头孢菌素类,主要累及肝胆系统和消化系统。新的ADR主要表现为脑电图异常、共济失调、肾功能异常,涉及的药物种类主要为抗病毒类、磺胺类,主要累及中枢及外周神经系统、泌尿系统。
-
在158例ADR病例中,男性发生ADR的比例高于女性,年龄集中在20~59岁,这主要与羁押人员中男性占比较高有关。经帕累托图分析发现,抗结核药物和头孢菌素类药物累计构成比高达79.75%,为主要因素;磺胺类药物累计构成比在80%~90%,为次要因素;其余均为一般因素。这与国家ADR监测年度报告及对非羁押人群的研究不一致[5-7],羁押人员中存在男性中青年结核病患者较多、长疗程使用一线结核药、心理压力大拖延病情、抗菌药物品种少导致大量使用头孢菌素等因素,都会导致ADR的发生。
本院ADR发生率最高的是口服给药途径(78.48%),其次是静脉滴注给药(21.52%),这与国家ADR监测年度报告及社会医院报道的静脉给药引起的不良反应占比最高不一致[6, 8];归因于本院ADR报告来源主要与羁押人员中结核病患者长疗程口服抗结核药物治疗有关。在ADR转归方面,痊愈93例(58.86%),好转62例(39.24%),持续3例(1.89%)。多数ADR的临床表现较轻,停药后经过处理即可好转或痊愈。本研究显示,引起3例新的ADR的药物为复方磺胺甲唑、链霉素、阿米卡星;62例严重ADR的药物主要为异烟肼和利福平,长疗程联用一线抗结核药物是造成肝损的主要诱因。然而,抗结核药剂量递增也会增加抗结核类药物性肝损伤的发生率[9],建议临床医师加强肝功能监测频次,并给予保肝药治疗,且应严格依据抗结核药物说明书和结核病治疗指南,规范使用抗结核药物的剂量。
抗结核药导致的ADR占比最高(65.19%),主要是利福平(122例,24.25%)、异烟肼(107例,21.79%)、吡嗪酰胺(102例,20.77%)、[1]乙胺丁醇(101例,20.57%)、链霉素(14例,2.85%)。羁押场所因其社会影响、环境的特殊性,结核病一直受到社会广泛关注[10]。羁押场所空间有限、人员流动性大、集中关押、羁押时间长,易导致疾病传播,结核病发病率是社会人群的几十倍甚至上百倍[11]。另外,营养不良、基础肝病、生理和病理等因素是发生抗结核药药物性肝损伤的危险因素[12]。本研究发现,抗结核药物是导致羁押人员发生ADR的主要药物,主要累及肝胆系统,诱发肝损伤是最常见的不良反应,可致急性肝功能衰竭甚至死亡,这主要与羁押场所环境、人员特点及药物本身毒性有关[11, 13]。应确保在押人员合理使用抗结核药物,并定期监测肝功能,以提高用药的安全性和有效性。
头孢菌素类抗菌药物占比次之(14.56%),主要是头孢唑啉钠注射剂(13例,2.65%)、头孢拉定胶囊(5例,1.02%)、注射用头孢拉定(2例,0.41%)和头孢曲松钠(3例,0.61%)。头孢菌素类抗菌药主要为一代和三代头孢菌素,这与本院的药品供应及医生的用药习惯有关。头孢菌素是导致在押人员发生ADR又一类重要药物,主要表现为各种过敏反应,严重者发生过敏性休克。其ADR的发生与药物β内酰胺环及侧链取代基结构、聚合物、生产工艺、使用剂量过大等密切相关,也与在押人员的体质、基础疾病和个体差异等相关[11, 14]。羁押人员需使用抗菌药时,临床医师应根据《抗菌药物临床应用指导原则》选择抗菌药物品种及剂量,掌握联合用药指征及警惕抗菌药物交叉过敏反应。此外,在药物使用环节,医护人员要注意溶媒、药物浓度、滴注速度、储存条件(遮光或避光)等影响因素,减少抗菌药物的滥用和避免ADR的发生。
-
综上,笔者采用帕累托图法,首次对羁押人员抗感染类药物发生ADR的情况进行分析,找出反映该特殊群体抗感染药物导致ADR发生的关键的少数和次要的多数之间的关系,进而找出导致ADR发生的抗感染药物、种类及累及的器官和(或)系统。本研究提醒临床,需重点监控羁押人员抗结核药物和头孢菌素类抗菌药物的合理使用,以减少或避免ADR的发生。然而,采取有效干预后,帕累托图的主要、次要和一般问题之间可能会相互转化[15]。应适时更新本院抗感染药物的帕累托图,以及时知晓导致ADR药物的变化趋势。
Analysis on 158 detainees with adverse reactions due to anti-infective drugs
-
摘要:
目的 分析上海市监狱总医院抗感染类药物所致不良反应的特点及规律,为羁押人员合理用药和药物警戒提供依据。 方法 收集本院2011年1月至2018年10月呈报国家药品不良反应监测中心的抗感染类药物ADR病例,应用帕累托图分析法研究导致ADR的抗感染药物的种类、累及器官和(或)系统的主要及次要因素。 结果 共收集158例抗感染药物所致的ADR病例,男性143例(90.51%),集中在20~59岁。经帕累托图分析发现,ADR主要涉及8类抗感染药物(抗结核药物、头孢菌素类药物、磺胺类药物、抗病毒类药物、青霉素类药物、氨基糖苷类药物、氟喹诺酮类和硝基咪唑类药物),ADR主要累及肝胆系统、皮肤及其附件、全身性反应和血液系统,以肝功能异常、肝功能损害、皮疹和过敏反应最为常见。 结论 应用帕累托图法揭示的“关键的少数和次要的多数”来分析羁押人员抗感染药物所致的ADR,重点关注抗结核药物及头孢菌素类药物的治疗,减少或避免ADR的发生。 Abstract:Objective To analyze the characteristics and trends of adverse drug reactions (ADR) induced by anti-infective drugs in Shanghai Prison General Hospital and provide a guideline of rational drug use and pharmacovigilance for detainees. Methods The anti-infective drug induced ADR cases reported to the national ADR monitoring center in our hospital from January 2011 to October 2018 were collected. The primary and secondary factors of types, organs and (or) systems affected by anti-infective drugs that lead to ADR were studied with Pareto diagram. Results 158 ADR cases caused by anti-infective drugs were collected. 143 cases (90.51%) were male in 20-59 years old. Pareto diagram analysis showed that ADRs mainly involved eight kinds of anti-infective drugs (antituberculosis drugs, cephalosporins, sulfonamides, antiviral drugs, penicillin, aminoglycosides, fluoroquinolones and nitroimidazoles). ADRs mainly involved in hepatobiliary and blood system. Both topical and systemic reactions were reported. Abnormal liver function, liver injury, rash and allergic reaction were the most common. Conclusion Pareto diagram method reflected the "critical minority and minor majority" analysis on detainees with ADRs caused by anti-infective drug. It was recommended to focus on anti-tuberculosis drugs and cephalosporin drugs to reduce or avoid the occurrence of ADR. -
Key words:
- adverse drug reaction /
- anti-infective drug /
- detainee /
- Pareto diagram analysis
-
紫茶生长于非洲肯尼亚海拔1 500~2 000 m的地区,主要成分为多酚类物质。现代药理研究表明,天然植物中的多酚具有抗肿瘤[1]、抗氧化[2]、抗菌[3]、抗衰老[4]等功效。课题组前期研究发现,紫茶提取物中多酚的纯度不高,直接影响相关制剂的开发。近年来,大孔吸附树脂的应用越来越广泛,尤其是在天然药物有效成分分离和纯化方面具有显著优势[5-8]。本实验以紫茶为研究对象,探索大孔吸附树脂对紫茶总多酚的纯化工艺,以期制备出纯度较高的紫茶总多酚,为其进一步开发利用提供理论依据。
1. 仪器与试药
UV-2550型紫外分光光度计(日本岛津);AUX220型电子分析天平(精度:0.1 mg,日本岛津);HH-2数显恒温水浴锅(江苏金坛市友联仪器研究所)。KQ-500B型超声波清洗器(昆山超声仪器有限公司)。
肯尼亚紫茶(批号:20181030,火烈鸟茶叶有限公司);没食子酸对照品(批号:110831-201605,中国食品药品检定研究院);铁氰化钾(温州市化学用料厂);ADS-17、D101、D301、AB-8、X-5型大孔吸附树脂(安徽三星树脂科技有限公司);氯化铁、盐酸、乙醇等试剂(西陇科学股份有限公司),以上试剂均为分析纯,水为纯化水。5种大孔吸附树脂的物理参数详见表1。
表 1 5种型号大孔吸附树脂物理参数型号 外观 极性 粒径(l/nm) 比表面积(m2/g) 平均孔径(l/μm) ADS-17 白色不透明球状颗粒 氢键 0.3~1.25 90~150 25~30 D101 白色半透明球状颗粒 非极性 0.3~1.25 480~520 25~28 D301 浅黄色半透明球状颗粒 中极性 0.3~1.25 550~600 48~58 AB-8 白色不透明球状颗粒 弱极性 0.3~1.25 480~520 130~140 X-5 白色不透明球状颗粒 非极性 0.3~1.25 500~600 290~300 2. 方法与结果
2.1 紫茶总多酚的含量测定
2.1.1 对照品溶液的制备
精密称取干燥至恒重的没食子酸对照品28.4 mg,置于100 ml量瓶中,加纯化水溶解并稀释至刻度,摇匀制备成母液。精密吸取1 ml母液置10 ml量瓶中,加纯化水稀释至刻度,配制成浓度为28.4 μg/ml的对照品溶液,置于冰箱中2~8 ℃避光保存。
2.1.2 供试品溶液的制备
称取紫茶粉末5.0 g,置于圆底烧瓶中,加入50%乙醇500 ml,加热回流提取30 min,放冷至室温,将药液滤过除去沉淀,滤液用50%乙醇补足减失的重量并稀释至500 ml。精密吸取1 ml稀释液,置于100 ml量瓶中,加水稀释至刻度,即得。
2.1.3 线性关系及方法学考察
分别精密吸取浓度为28.4 μg/ml的没食子酸对照品溶液0.2、0.3、0.5、0.8、1.0和1.2 ml于25 ml量瓶中,依次加入0.1 mol/L FeCl3溶液1.0 ml、1%K3[Fe(CN)6]溶液2.0 ml和0.1 mol/L HCl溶液0.5 ml,用纯化水稀释至刻度,摇匀,于室温下避光放置60 min。以相应试剂为空白,在775 nm处测定吸光度。以没食子酸质量浓度(X,μg/ml)为横坐标,以吸光度(Y)为纵坐标,绘制标准曲线,得回归方程:Y=0.769 9X+0.027 3(r=0.999 7),表明没食子酸浓度在0.227~1.363 μg/ml范围内与吸光度呈良好的线性关系。方法学考察结果表明,专属性良好,平均回收率为100.28%,RSD为2.09%;精密度和重复性试验的RSD小于3%。显示本方法准确可靠。
2.2 大孔吸附树脂的预处理
取5种不同型号的大孔吸附树脂在95%乙醇中浸泡24 h,使其充分溶胀,将浸泡后的树脂装柱,用95%乙醇以5 ml/min的体积流量冲洗,直至流出液澄清,之后用2倍体积的4%盐酸溶液浸泡3 h,用纯化水以5 ml/min的体积流量冲洗至中性,再用2倍体积的5%氢氧化钠溶液浸泡3 h,用纯化水以5 ml/min的体积流量冲洗至中性,最后用95%乙醇浸泡保存,临用时以5 ml/min体积流量的纯化水冲洗至中性。
2.3 静态吸附行为考察
2.3.1 大孔吸附树脂的筛选
取预处理后的ADS-17、D101、D301、AB-8、X-5型大孔吸附树脂约1 g,精密称定,共5份,置于50 ml具塞磨口锥形瓶中。加入质量浓度为50 μg/ml(以多酚含量计)的紫茶总多酚提取液20 ml,在30 ℃水浴的条件下振荡吸附24 h。吸附结束后,滤过,取续滤液按照“2.1”项下方法测定总多酚的含量,计算各树脂在30 ℃下对紫茶总多酚的吸附量和吸附率。然后,将上述吸附饱和的大孔树脂取出,用纯化水清洗后,分别加入70%乙醇20 ml,在30 ℃水浴的条件下振荡24 h,进行静态解吸,计算其解吸率,结果见表2。计算公式如下:
表 2 不同类型大孔树脂对紫茶总多酚的静态吸附率和解吸率树脂型号 吸附量(μg/g) 吸附率(%) 解吸量(μg/g) 解吸率(%) ADS-17 554.9 68.98 459.0 82.72 D101 621.6 77.74 341.4 54.93 D301 817.4 100.00 107.4 13.14 AB-8 701.8 82.20 598.2 86.73 X-5 727.8 89.90 600.8 81.13 吸附量=(C0−C1)V1/M
吸附率=(C0−C1)/C0
解吸量= C2 V2/M
解吸率=C2 V2/[(C0−C1)V]
其中,C0、C1为吸附前和吸附后吸附液中多酚的质量浓度,C2为解吸附后多酚的质量浓度,V1和V2分别为吸附液和解吸液体积,M为大孔树脂的质量。
由表2结果可知,大孔树脂D301对紫茶总多酚具有较强的吸附效果,其吸附率达到100%,其余4种树脂的吸附率从高到低依次是X-5、AB-8、D101、ADS-17。由此可见,不同类型的树脂对紫茶总多酚的吸附性能各不相同。这可能是由于树脂的内部结构、分子极性以及多酚的溶解度等对树脂吸附多酚能力的影响。多酚由于分子中酚羟基的存在,其分子极性较低,因而在与极性较弱或者非极性的树脂进行吸附时效果更好。采用50%的乙醇进行解吸,可以看出5种树脂的解吸率差异较大,AB-8树脂的解吸效果最好,解吸率达86.73%,X-5树脂次之。综合紫茶总多酚提取液的静态吸附和解吸试验,AB-8型树脂和X-5型树脂对紫茶总多酚的吸附效果和解吸效果均较好,而AB-8型树脂价格相对低廉,从节省成本的角度考虑,优先采用AB-8型树脂对其进行纯化。
2.3.2 静态吸附和解吸曲线的绘制
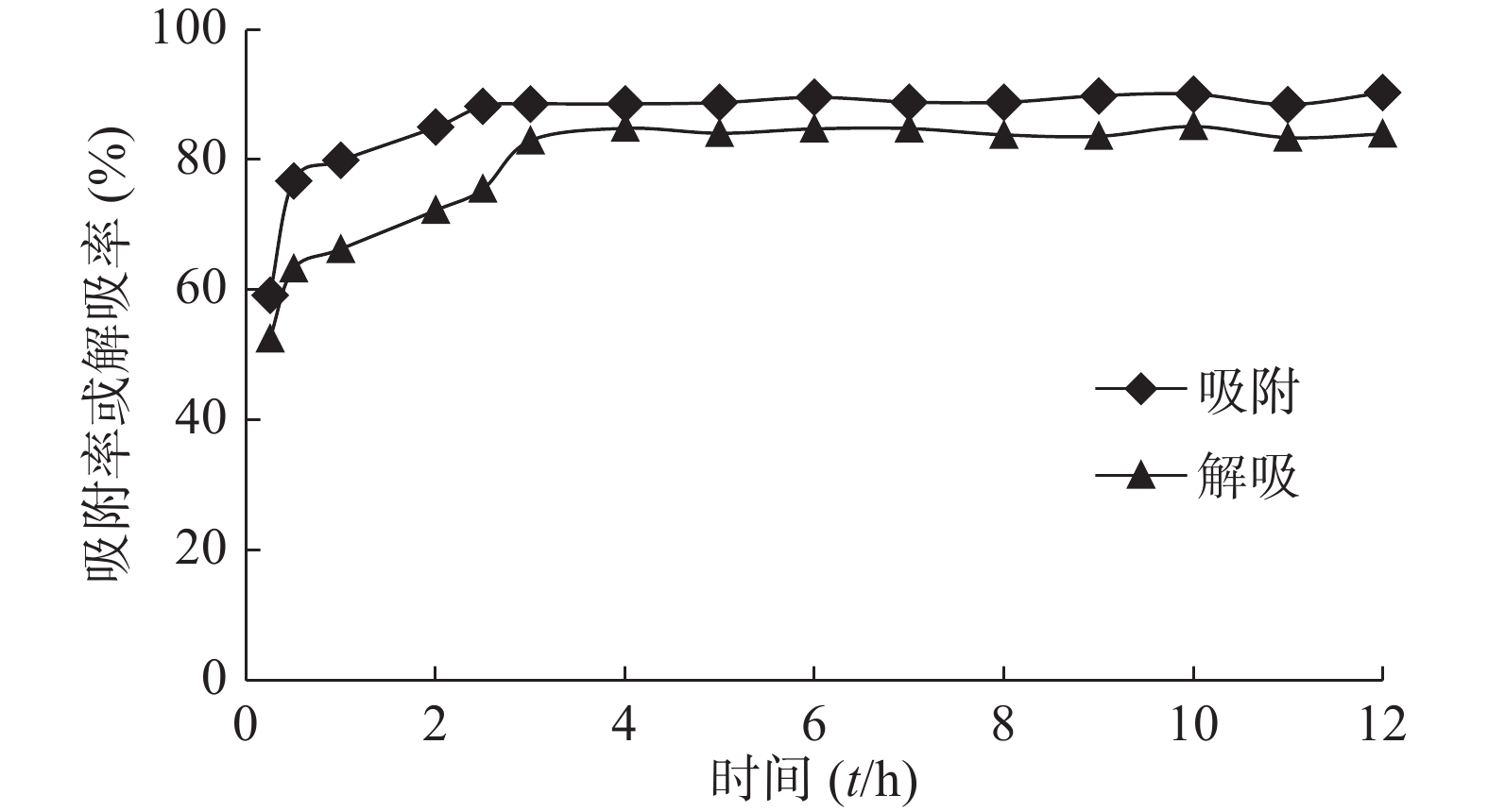
取预处理后的AB-8型大孔吸附树脂约1 g,精密称定,共15份,分别置于50 ml具塞磨口锥形瓶中,加入质量浓度为50 μg/ml的紫茶总多酚提取液20 ml,在25 ℃水浴的条件下振荡吸附12 h,每隔一段时间取出1个磨口锥形瓶,测定其总多酚的质量浓度,计算对应时间的吸附率,绘制静态吸附动力学曲线。然后,采用静态解吸试验的方法处理已吸附结束的树脂,进行静态解吸动力学试验,同样每隔一段时间取出1个磨口锥形瓶,测定其总多酚的质量浓度,计算对应时间的解吸率,绘制静态解吸动力学曲线,结果见图1。
由图1可知,在测定的时间点内,AB-8型大孔吸附树脂对紫茶总多酚的吸附量随着时间的延长而逐渐增多,经过2.5 h以后,树脂对紫茶总多酚的吸附量趋于平衡,对应的吸附率为88.27%。在0~5 h内,树脂的解吸率呈上升趋势,并在4 h达到最大值84.86%,在随后的时间里,解吸率随着时间的延长变化不大。
2.3.3 吸附液pH值对吸附率的影响
取预处理好的AB-8型大孔吸附树脂1 g,精密称定,共7份,分别置于50 ml具塞磨口锥形瓶中,分别加入质量浓度为50 μg/ml并用0.1 mol/L的盐酸和0.1 mol/L的氢氧化钠溶液调节pH值为2、3、4、5、6、7、8的紫茶总多酚提取液,在30 ℃水浴的条件下振荡吸附2.5 h,测定吸附液中紫茶总多酚的质量浓度,计算吸附率,结果见表3。
表 3 pH值对紫茶总多酚吸附率和解吸率的影响pH值 吸附量(μg/g) 吸附率(%) 2 702.4 89.79 3 712.4 90.79 4 700.3 87.77 5 706.3 89.07 6 652.5 85.71 7 641.7 83.19 8 558.4 71.54 由表3可知,吸附液pH值对紫茶总多酚的吸附率有较大影响。在pH值为2时,AB-8型大孔吸附树脂对此质量浓度下的紫茶总多酚吸附率达89.79%。因此,确定上样液的pH值为2。
2.4 动态吸附行为考察
2.4.1 泄露曲线的绘制
取预处理后的AB-8型树脂10 g,精密称定,室温下将质量浓度为250.0 μg/ml(调至pH为2)的紫茶总多酚提取液(供试品溶液用水稀释)以1.0 ml/min体积流量湿法加至树脂柱中,分段收集流出液,流出液每20 ml收集1份,测定吸光度,计算对应的总多酚含量,绘制泄露曲线。当流出液中总多酚的质量浓度达到上样液质量浓度的1/10,达到泄露点,认为此时为最佳上柱体积,结果见图2。在第2份流出液时,紫茶总多酚已经开始泄露,在第3份流出液中,总多酚的质量浓度为26.5 μg/ml,达到上样液质量浓度的1/10,因此选择上柱体积为60 ml,即3 BV。
2.4.2 上样液质量浓度的影响
取预处理好的AB-8型树脂10 g,精密称定,装入1.5 cm×20 cm的层析柱中,共5份,分别加入质量浓度为250、375、500、625、750、1 000 μg/ml的上样液(pH为2)各60 ml(3 BV),以1.0 ml/min的流速上柱,收集流出液,按“2. 1”项下方法测定总多酚含量,计算各质量浓度下的吸附率,确定最佳上样质量浓度。结果显示,各上样质量浓度下的吸附率分别为74.50%、77.56%、69.77%、60.59%、56.73%、43.61%。由此可见,上样液质量浓度对大孔吸附树脂吸附性能有显著影响,在考察范围内吸附率总体呈现出先上升后下降的趋势。当质量浓度小于375 μg/ml时,随着上样液质量浓度增加,动态吸附率呈现上升的趋势;分析原因可能是在此较低的浓度范围内,紫茶多酚有较大的机会与大孔树脂的内表面接触,进而加速扩散至树脂孔道内,形成吸附作用。而当质量浓度大于375 μg/ml时,随着质量浓度继续增加,位于孔道内的紫茶总多酚分子的扩散运动受到抑制,导致树脂对多酚的吸附能力降低。因此,选择上样液质量浓度为375 μg/ml。
2.4.3 上样液体积流量的影响
取预处理的AB-8型大孔吸附树脂10 g,精密称定,以湿法上柱法装入1.5 cm ×20 cm的层析柱中,共4份,轻敲柱壁,使柱内树脂平衡,打开下端阀门,控制体积流量使柱内纯化水流出,在液面距树脂1 cm时,将紫茶总多酚上样液(质量浓度为375 μg/ml,pH为2,上样量为3 BV)分别以1.0、2.0、3.0、4.0 ml/min的体积流量上柱,同时收集下端流出液,测定吸光度,计算吸附率,确定最佳上样体积流量。结果显示,吸附率分别为79.37%、79.78%、72.73%、64.73%,当上样体积流量为2.0 ml/min时,AB-8型大孔吸附树脂对紫茶总多酚的吸附率最大,故选择上样体积流量为2.0 ml/min。
2.4.4 径高比对动态吸附性能的影响
取预处理的AB-8型大孔吸附树脂10 g,精密称定,以湿法上柱法装入1.5 cm ×40 cm的层析柱中,分别设置径高比(柱直径与树脂填充高度比值)为1∶6、1∶9、1∶12、1∶15,将紫茶总多酚上样液(质量浓度为375 μg/ml,pH为2)分别以2.0 ml/min的体积流量上柱,对应的药液上样量分别为3、4.5、6、9 BV,收集下端流出液,测定吸光度,计算吸附率,确定最佳径高比。结果显示,吸附率分别为79.81%、78.37%、76.73%、68.54%。径高比1∶6和1∶9对吸附率影响不大。此后,在考察范围内,随着径高比值的降低,吸附率也呈现下降的趋势,可能是由于树脂层过高导致上样液穿透能力差所致。
2.4.5 洗脱剂体积分数的影响
取预处理后的AB-8型大孔吸附树脂10 g,精密称定,共5份,以湿法缓慢装入1.5 cm×20 cm的层析柱(径高比为1∶6,下同),将质量浓度为375 μg/ml上样液(调节pH为2)3 BV以2.0 ml/min的体积流量通过树脂柱,待吸附饱和后,分别用纯化水及25%、50%、75%、90%乙醇溶液各3 BV以1.0 ml/min的流速进行洗脱,收集洗脱液,测定其吸光度,计算解吸率,确定最佳洗脱剂体积分数。结果:解吸率分别为17.52%、62.96%、91.04%、81.41%、84.67%,由此可见,50%乙醇对紫茶总多酚的解吸作用最强,故选择洗脱剂的体积分数为50%。
2.4.6 洗脱剂用量的影响
取预处理后的AB-8型大孔吸附树脂10 g,精密称定,以湿法缓慢装入1.5 cm×20 cm的层析柱中,将375 μg/ml的上样液(pH为2)3 BV以2 ml/min的体积流量通过树脂柱,待吸附饱和后,用50%乙醇以1.0 ml/min的流速进行洗脱,洗脱溶剂用量分别为1、2、3、4、5 BV,收集洗脱液,测定其吸光度,计算洗脱率,确定最佳洗脱剂用量。结果:解吸率分别为54.68%、83.37%、90.29%、91.48%、91.45%,表明当50%乙醇用量在1~3 BV时,随着用量的增加,对紫茶总多酚的解吸率呈上升的趋势,随后继续增加洗脱剂的用量,解吸率不再增加,表明此时树脂上吸附的总多酚已被充分洗脱,没有必要再增加洗脱剂的用量,故确定洗脱剂的用量为4 BV。
2.4.7 洗脱剂体积流量对洗脱效果的影响
取预处理后的AB-8型大孔吸附树脂约10 g,精密称定,以湿法缓慢装入1.5 cm×20 cm的层析柱中,将375 μg/ml上样液(pH为2)3 BV以2.0 ml/min的体积流量通过树脂柱,待吸附饱和后,用50%乙醇溶液4 BV分别以1.0、2.0、4.0、6.0 ml/min的体积流量进行洗脱,计算解吸率,确定最佳体积流量。结果:对应的解吸率分别为92.47%、93.76%、91.97%、85.18%,表明紫茶总多酚的洗脱率随着洗脱体积流量的加大先升高后减小,故选择最佳洗脱体积流量为2 ml/min。
2.5 最佳工艺的验证
称取4份预处理后的大孔吸附树脂约10 g,精密称定,以湿法缓慢装入1.5 cm×20 cm层析柱中(径高比为1∶6),将紫茶提取物预先用石油醚(60~90 ℃)除去脂溶性色素,参考“2.1.2”项下方法加水稀释以制备浓度为375 μg/ml(pH为2)的紫茶总多酚溶液3 BV(总多酚质量为22.5 mg,质量分数40.2%,干膏56.0 mg),并以2 ml/min体积流量上样,待吸附饱和后,先用3 BV水去除杂质,然后用50%乙醇溶液4 BV以2 ml/min的体积流量洗脱,分别收集洗脱液,按照紫茶总多酚定量测定方法,计算总多酚洗脱量及洗脱率,再将洗脱液水浴蒸干,低温烘至恒重,计算干膏的量;精密称取干膏适量,测定总多酚的含量。结果见表4。
表 4 纯化工艺验证结果编号 加入量
(m/mg)纯化前 洗脱量
(m/mg)洗脱率
(%)纯化后 干膏量(m/mg) 质量分数(%) 干膏量(m/mg) 质量分数(%) 平均质量分数(%) RSD(%) 1 22.5 56.0 40.2 20.8 92.4 29.4 70.7 69.8 1.27 2 21.0 93.3 30.6 68.6 3 20.9 92.8 30.0 69.7 4 20.6 91.6 29.4 70.1 由纯化工艺验证结果可见,经过4次验证试验,50%乙醇洗脱条件下总多酚的平均洗脱率为92.5%,紫茶总多酚干膏量由56.0 mg减少至平均29.9 mg,质量分数从40.2%升至平均69.8%,表明建立的纯化工艺对紫茶总多酚有较好的分离、纯化效果。
3. 讨论
大孔吸附树脂是一种具有多孔立体结构和选择性吸附功能的高分子材料,目前已广泛应用于中药的活性成分如黄酮、皂苷、生物碱及多酚等成分的分离与纯化。其中,目前采用大孔树脂对多酚类成分进行纯化的有天麻总多酚[9]、白簕叶总多酚[10]、过岗龙总多酚[11]、茶梗中茶多酚[12]等,这都提示了大孔树脂精制多酚类有效成分的可行性。影响大孔树脂的分离纯化有多方面的因素,在选择合适的大孔树脂时,应综合考虑各种影响因素,如树脂的极性、比表面积以及上样液的质量浓度、洗脱液浓度等,以获得最佳的分离效果。在利用大孔树脂纯化时,应尽量滤去上样液中的沉淀,这样既能提高总多酚的纯化率,也能提高树脂的使用寿命。本研究中的样品采用50%乙醇提取后用纯化水进行稀释,当样品溶于水中时,由于多酚类物质能被大孔树脂吸附,而色素及多糖等物质不能吸附而被洗脱掉。而在改为乙醇洗脱时,树脂的吸附效果减弱,被吸附的多酚能被乙醇洗脱。
本研究通过对5种不同型号的大孔吸附树脂的吸附和解吸进行考察,确定了AB-8型大孔吸附树脂纯化紫茶总多酚的最佳工艺条件,为该产品的进一步开发奠定了基础。
-
表 1 发生ADR患者的性别与年龄分布(n=158)
年龄(岁) 男性(例) 女性(例) 总例数 构成比(%) 20~29 33 1 34 21.52 30~39 30 3 33 20.88 40~49 35 2 37 23.42 50~59 38 7 45 28.48 ≥60 7 2 9 5.70 合计 143 15 158 100 表 2 导致ADR药物种类分布(n=158)
序号 药品分类 例数 构成比(%) 累计构成比(%) 因素类型 1 抗结核药 103 65.19 65.19 A 2 头孢菌素 23 14.56 79.75 A 3 磺胺类 14 8.86 88.61 B 4 抗病毒类 8 5.06 93.67 C 5 青霉素类 3 1.90 95.57 C 6 氨基糖苷类 3 1.90 97.47 C 7 氟喹诺酮类 2 1.27 98.73 C 8 硝咪唑类 2 1.27 100.00 C 表 3 ADR累及器官和(或)系统及临床表现
序号 累及系统 主要临床表现 例数 构成比(%) 累计构成比(%) 因素类型 1 肝胆系统 肝功能异常、肝细胞损害、肝炎、转氨酶升高、尿素氮升高 95 60.13 60.13 A 2 皮肤及其附件 皮疹、瘙痒、荨麻疹、斑丘疹 30 18.99 79.12 A 3 全身性反应 过敏性休克、变态反应、发热 17 10.76 89.88 B 4 血液系统 白细胞减少、贫血、骨髓抑制、血小板减少 6 3.80 93.68 C 5 消化系统 恶心、呕吐、腹泻、十二指肠溃疡 4 2.53 96.21 C 6 中枢及外周神经系统 耳鸣、神经炎、头晕、共济失调、惊觉、谵妄、脑电图异常 3 1.90 98.11 C 7 心血管系统 潮红、低血压、心悸 2 1.26 99.37 C 8 泌尿系统 肾功能异常 1 0.63 100.00 C -
[1] 孙吉, 何鸽飞, 陈志宏, 等. 长沙市2016年抗感染药物所致新的严重的药品不良反应分析[J]. 药物流行病学杂志, 2019, 28(5):323-327. [2] 朱琳, 卢健, 刘春莹, 等. 2014—2018年咸阳市第一人民医院抗感染药物不良反应分析[J]. 现代药物与临床, 2020, 35(3):563-566. [3] 朱恺, 成浩. 无锡市监管场所羁押人员HIV感染状况与危险因素分析[J]. 预防医学情报杂志, 2017, 33(9):878-881. [4] 黄莹, 刘飞, 孔玲娟, 等. 质量管理工具对412例药品不良反应报告的分析[J]. 临床合理用药杂志, 2020, 13(3):165-167. [5] 刘桦, 周佳纯, 范国荣. 上海交通大学附属第一人民医院2013-2016年128例严重药品不良反应帕累托图分析[J]. 药学服务与研究, 2018, 18(5):385-388. [6] 国家药品监督管理局. 国家药品不良反应监测年度报告[EB/OL].[2019-10-18)[2020-04-07]. http://www.nmpa.gov.cn/WS04/CL2138/359373.html [7] 何程程, 蒋程. 我院抗感染药物致不良反应的帕累托图分析[J]. 中国现代医生, 2018, 56(5):114-116, 120. [8] 曹畅, 文晓丽, 林文华, 等. 应用鱼骨图及帕累托图进行2621例药品不良反应分析[J]. 药学实践杂志, 2018, 36(1):88-92. doi: 10.3969/j.issn.1006-0111.2018.01.019 [9] 杨学敏, 沈宝荣, 刘鹏园, 等. 抗结核药致药物性肝损伤危险因素的Logistic回归分析[J]. 中国医院药学杂志, 2019, 39(1):67-71. [10] 黄智忠, 周银发, 陈江芬, 等. 福建省某羁押场所在押人员结核病核心信息知晓情况调查分析[J]. 安徽预防医学杂志, 2019, 25(2):149-150, 146. [11] 唐勤, 瞿伟华, 张毅. 上海地区羁押人员结核分枝杆菌耐药现状分析[J]. 国际检验医学杂志, 2014, 35(3):354-356. doi: 10.3969/j.issn.1673-4130.2014.03.046 [12] 田贞贞, 刘永梅, 刘芳, 等. 抗结核治疗中导致肝损伤的危险因素分析[J]. 解放军预防医学杂志, 2019, 37(9):90-92. [13] 韩珂卿, 栾飞, 刘道恒, 等. 结核病专科医院药品不良反应回顾性分析[J]. 临床肺科杂志, 2019, 24(8):1459-1462. doi: 10.3969/j.issn.1009-6663.2019.08.025 [14] 苏洽玉. 574例药品不良反应报告[J]. 中国医院用药评价与分析, 2019, 19(2):251-253. [15] 张旭, 牛佳, 吴晓彧, 等. 静脉用药调配中心不合理用药处方的帕累托图分析[J]. 中国药物警戒, 2017, 14(3):183-185. doi: 10.3969/j.issn.1672-8629.2017.03.014 -





 下载:
下载:


 下载:
下载:



