-
过程分析技术(process analytical technology,PAT)通过对关键质量数据包括原始物料质量、中间物料质量和工艺过程参数进行实时监测以确保成品质量[1]。其中,近红外光谱(near infrared spectroscopy,NIRS)分析技术是PAT的核心技术之一,其独特优势在于测试方便、分析速度快、分析效率高,非常适用于在线分析[2]。目前该技术在国外药企已有很多应用,如对流化过程中干燥终点的控制[3]、监测包衣过程[4]、测定片剂中原料药和辅料的含量[5]等。
硫酸羟氯喹是临床上治疗类风湿性关节炎、系统性红斑狼疮的常用药物[6-8]。硫酸羟氯喹制粒工艺为湿法制粒,而湿法制粒的产品质量控制主要在制粒过程中。为缩小批间差异和改善工艺,利用PAT技术建立定量或定性模型以检测颗粒水分、混合均匀度和粒径等一系列指标,而水分含量既影响粒径分布也影响混匀程度,故需要优先测量[9]。目前,硫酸羟氯喹颗粒在干燥过程中使用快速水分测定仪测定水分含量,以监测干燥终点。这种分析方法在干燥过程中取样测定水分,会带来人为干扰因素,且水分测定仪的测量时间较长,在等待测量结果时,流化床内的物料水分仍在不断变化。使用NIR分析技术对硫酸羟氯喹颗粒的水分含量进行实时监测,将有助于提高硫酸羟氯喹的生产效率、降低因等待测量结果时物料水分仍在不断降低带来的生产风险,以及提高产成品的质量,有助于向生产全自动化发展。目前,国内使用NIR分析技术监测物料水分含量的报道以离线方式居多[10-13]。课题组之前建立了硫酸羟氯喹颗粒离线水分定量模型[10],本研究在此基础上先在小试部分建立在线水分定量模型,并在试运行情况良好的基础上将模型转移到车间生产线。结果表明该模型能满足生产过程在线监测硫酸羟氯喹颗粒水分的需求。
-
Thermo Antaris MX近红外光谱仪、TQ Analyst 9.5软件(美国Thermo Fisher公司),HX204卤素水分测定仪(瑞士Mettler-Toledo公司),硫酸羟氯喹颗粒(上海上药中西制药有限公司),MATLAB 2014a(美国MathWorks公司),DPL-0.5型多功能制粒/包衣机(重庆精工制药机械有限责任公司),DG400流化床(上海东富龙科技股份有限公司)。
-
在流化床锅体的下半部分安装蓝宝石窗口,并将Thermo Antaris MX近红外光谱仪的探头固定于窗口上,取样口在流化床的另一侧。将制粒后的湿颗粒倒入流化床中进行干燥,实验所用样品是在流化床干燥过程中从取样口实时取出得到的样品:流化床开始进风干燥并开始连续采集样品光谱,光谱采集完成后立即取样。因物料温度在30 ℃前样品水分变化较快,故取样间隔时间较短,每隔30 s取一次样品;在物料温度高于35 ℃时水分变化较慢,取样的间隔时间延长,每隔2 min取一次样品,待物料温度继续上升到55 ℃时停止干燥(覆盖了工艺范围以得到全面的样品光谱信息)。一批物料需分成4锅流化床完成,每做一锅流化床采集约10个样本,一批可采集约40个样品,共12批采集519个样品建立模型。
-
用水分测定仪测定样品的水分质量含量为1.00%~7.50%(涵盖了工艺优化值1.00%~4.00%)。
-
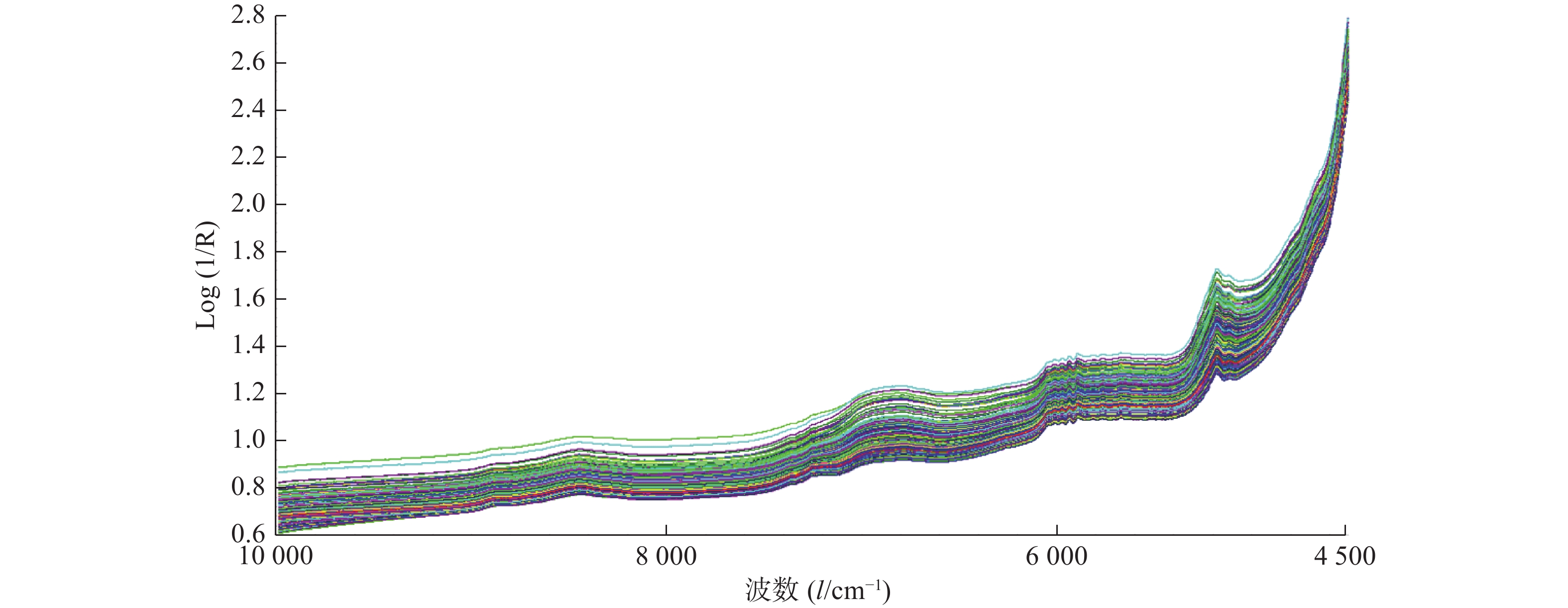
使用近红外光谱仪以漫反射光纤探头的采集方式连续采集干燥过程中的样品的近红外光谱。光谱的扫描范围为10 000~4 500 cm−1,扫描次数为64次,分辨率为8 cm−1,增益值为8×,每次采集光谱前均进行背景光谱的采集,采集得到的近红外光谱如图1所示。
-
利用TQ Analyst 9.5软件结合化学计量学的PLS算法,建立硫酸羟氯喹颗粒含水量的定量分析模型。首先采用Chauvenet准则检验结合杠杆值-学生化残差图鉴别并剔除异常样本[14],进而采用SPXY分类算法将其余样本划分为校正集和验证集。通过一系列参数,包括校正集误差均方根(RMSEC)、验证集误差均方根(RMSEP)和相关系数R等评价模型进行考察[15]。当模型相关系数R越接近1,说明模型拟合效果好,分析准确度越高。当RMSEC和RMSEP值越小且越彼此接近,即|RMSEP-RMSEC|趋近0,表明模型具有好的稳定性,且当RMSEP值较小时,模型具有较高预测能力。
-
异常样本会对NIR模型产生很大的影响,例如误导光谱变量的选择,影响模型的参数估计,降低模型的预测准确度和稳定性[16-18]。采用Chauvenet准则检验结合杠杆值-学生化残差图,鉴别并剔除13个异常样本:23、58、61、70、79、95、96、97、139、223、276、350和473。
-
在NIR模型建立的过程中如何挑选具有代表性的样本,对最终模型的预测准确性与稳定性有很大影响。SPXY[19]分类方法是近红外样本分类中一种常用的方法,同时考虑了样本的光谱和浓度特征。进行模型建立的样本共有519份,在“2.4.1”项下剔除了13份样品,将剩余506份样品使用SPXY分类法进行分类,344份样品作为校正集,162份样品作为验证集。主成分分析结果表明,样本的验证集均匀分布在校正集中。
-
光谱预处理方法包括MSC、SNV及求导等一系列算法。MSC通过数学方法将光谱中的散射信号与化学信息进行分离,用于消除由于样品颗粒分布不均及颗粒大小不同所产生的散射对其光谱的影响。SNV的作用与MSC基本相同,均是用于消除由于颗粒散射及光程差异给光谱带来的影响[15]。
对光谱进行求导,同时运用Savitzky-Golay(S-G)平滑滤波,或者Karl Norris平滑滤波对光谱进行平滑。求导可以增强光谱信号,平滑可以滤除噪声。从表1可以看出NIR光谱经过MSC、一阶导数以及Karl Norris平滑,能得到较好的数据处理结果。
表 1 不同光谱预处理方法得到的模型参数
预处理方法 RMSEC
(%)RMSEP
(%)RMSECV
(%)R 无预处理方法 0.457 0.499 0.489 0.9206 MSC1 0.467 0.409 0.481 0.9309 SNV2 0.469 0.411 0.483 0.9306 MSC+一阶导数 0.537 0.506 0.585 0.8962 MSC+二阶导数 0.457 0.745 0.867 0.7647 MSC+一阶导数+Norris3 0.408 0.435 0.446 0.9372 SNV+一阶导数 0.537 0.506 0.585 0.8962 SNV+二阶导数 0.456 0.745 0.867 0.7647 SNV+一阶导数+Norris 0.405 0.436 0.446 0.9372 注:1表示多元散射校正;2表示标准归一化变换;3表示平滑滤波。 -
选择合适的波段用于模型的建立,对最终所建模型的预测准确度和稳定性有重要的影响。为了得到NIR光谱的特征信息,首先对前3个主成分的载荷向量进行分析[20],图2A为前3个主成分全光谱范围的载荷图。由PC1载荷图可知,光谱在4 935~5 336 cm−1和6 911~7 297 cm−1附近的波段范围包含更多的特征信息。由PC2和PC3载荷图可知,在上述波段附近也包含较多的光谱信息。同时,与得到求导后的一阶光谱(图2B)相比较,确定上述两个波段与水分之间确实具有较强的相关性,是NIR光谱中水分的主要吸收峰,可用于水分模型的建立。
-
主因子数的选择在建立模型的过程中至关重要,选择正确的主因子数既能完全利用NIR光谱信息,还能避免出现过拟合现象。根据TQAnlyst9.5中的PRESS图,以RMSECV和PRESS最小时所对应的主因子数即为最佳主因子数(本研究中主因子数为6)。
-
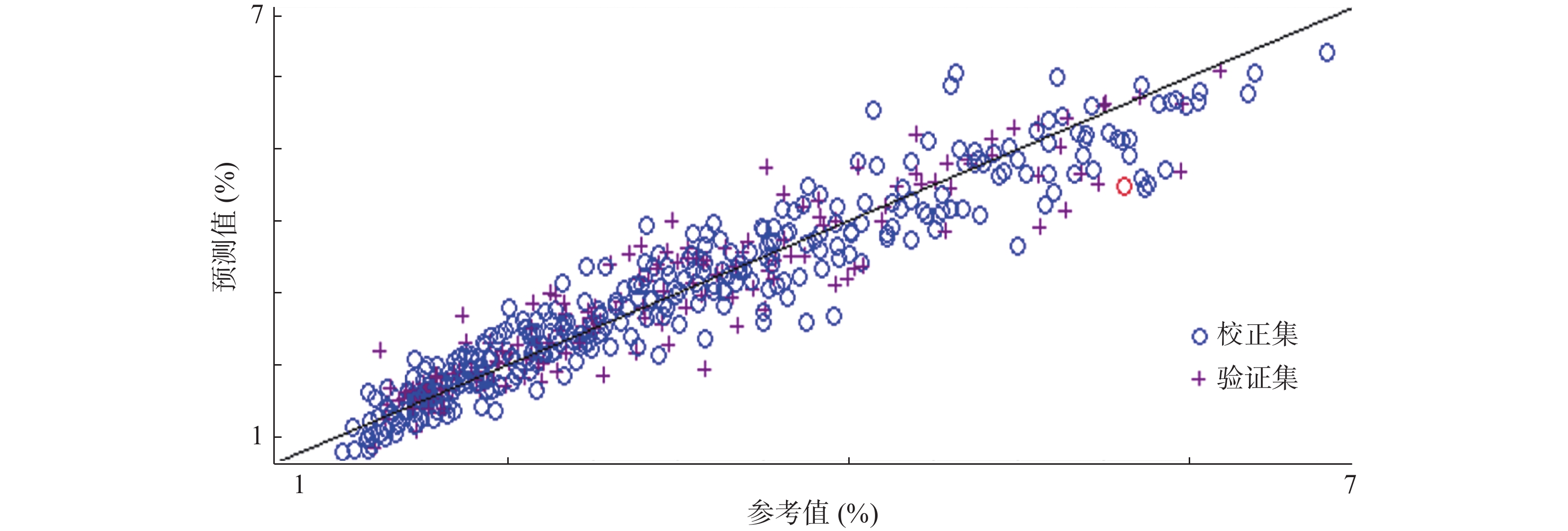
根据SPXY分类法得到的校正集建立模型,用验证集对模型进行验证。以MSC+一阶导数+Karl Norris平滑为光谱的预处理方式,选择的建模波段为4 935~5 336 cm−1和6 911~7 297 cm−1,结合化学计量学中的PLS算法建立NIR定量分析模型(图3):RMSEC为0.408,相关系数为0.952 9;RMSEP为0.435,相关系数为0.936 6;主因子数为6。从图3可以看出校正集和验证集的数据点在模型范围(1.00%~7.50%)内分布均匀,且校正集分布在验证集的范围内,表明用校正集建立的模型对验证集的验证有效,同时|RMSEP−RMSEC|的数值为0.027,趋近于0,以上结果均表明所建模型较为稳定。
-
RPD值是验证集标准偏差与预测集标准偏差的比值,即RPD=SDV/SEP。本研究以RPD值对模型进行评价。其中,SDV为验证集所有样本浓度值的标准偏差,SEP为预测集标准偏差。验证集样本的性质分布越均匀,SEP值越小,RPD值越大。本研究中,通过计算得到RPD值为5.18(大于5),表明模型的预测结果可以接受[10]。
-
将建立完成的模型应用于一批物料(PAT190601-6)的干燥过程,按“2.1”项下操作,采集所取样品光谱。将采集的光谱导入“2.4.6”项下建立的模型,得到光谱的预测值,用快速水分测定仪测定每份样品的参考值。预测集的RMSEP=0.265。将预测集样本的预测值与参考值进行配对样本t检验,显著性水平设为0.05。检验结果|t|=0.195,小于t双尾临界值1.990,F=1.10<1.46,说明预测值与参考值之间无统计学差异。图4为预测值与参考值水分变化曲线,从图中可以看出两个曲线的重合性较好,进一步表明模型的误差较小,稳定性较好(鉴于流化床体积,一个批次样品需要分为4份进入流化床干燥)。
-
在模型已初步建立完成并应用情况较好的小试基础上,将仪器移入车间,开始对大生产过程中物料水分变化进行实时检测。将蓝宝石窗口置于流化床底部,探头切合于窗口,取样口于窗口的对面处。考虑到仪器所处环境的改变可能对光谱产生影响,包括吸收峰的偏移、展宽、吸收强度的非线性变化等[21],需要对模型在车间的可应用性重新评价。
对一批物料(PAT-191223)进行干燥实验,该批样品需分两批进入流化床,每批采集3~4 g样品后,用水分测定仪测定水分值。预测集的RMSEP=0.265。将预测集样本的预测值与参考值进行配对样本t检验,显著性水平设为0.05。检验结果|t|=0.265,小于t双尾临界值2.110,F=0.78<3.18,说明预测值与参考值之间无统计学差异。
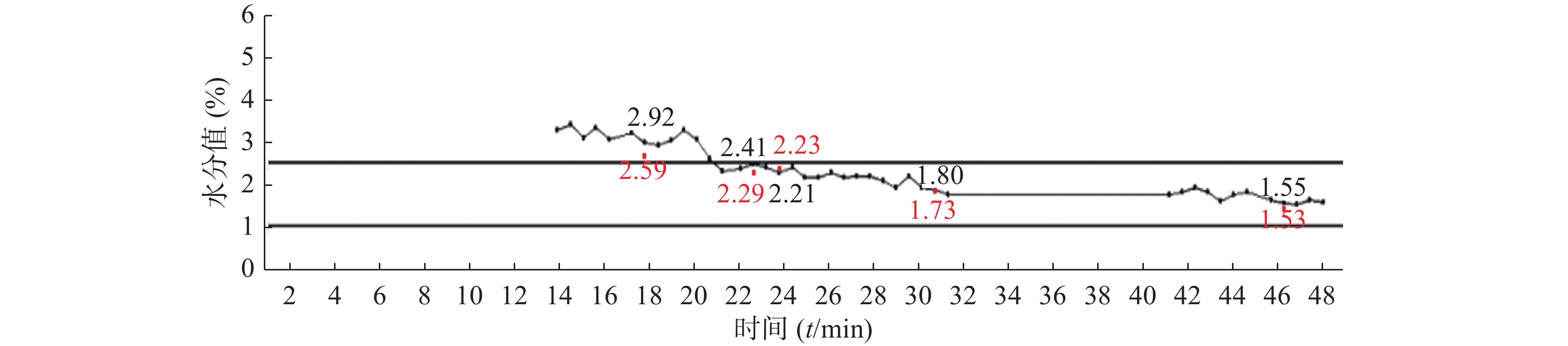
将模型导入Result Operation软件,可实时反映物料(PAT-191223)的水分值变化,由图5可见水分值平稳下降、直至趋于稳定。在干燥过程中,在线取出5份样品,用水分测定仪测量参考值并标于图中(红色为参考值,黑色为预测值)。可见预测值与参考值的重合性较好,表明模型的误差较小且稳定性较好。
-
模型的误差有两个来源:①探头与取样口间隔较远,降低了采集得到的光谱与样品的空间对应性,对模型的准确度带来影响;②取样口的通道较窄,会造成湿物料堆积,对样品的水分值造成影响。解决方法:①光谱采集完成后立即取样,可以保证光谱与样品的时间对应性,对于提高空间对应性的解决方法是可在窗口附近安装取样口;②及时清理取样口堆积的物料,避免对样品水分值产生影响。
-
工艺要求硫酸羟氯喹颗粒水分值为1.00%~4.00%,模型预测范围为1.00%~7.50%,包含了工艺要求的范围,可应用此模型缩小批间的水分差异。例如,当预测值在2.00%时停止干燥,为工艺的改善和提高提供基础。从图5可以看出,部分时间段的水分值上下波动,而非持续下降,且在接近干燥终点时,水分值在2.00%处波动,且无明显下降趋势。原因可能为采集得到的NIR光谱反映的是表层样品的光谱,无法准确反映较深处即流化床锅体内部的物料水分情况,而下一张光谱有可能为内部的物料吹到窗口处采得,因此,预测的水分值略有升高。
-
本实验采集了11批次药品用于含水量模型的建立。由于在硫酸羟氯喹的实际生产过程中,原辅料的不同批次之间存在批间差异,此外,生产过程中存在影响硫酸羟氯喹颗粒质量的其他因素,这也导致不同批次的硫酸羟氯喹颗粒之间也存在批间差异。故在建立模型时尽可能包含较多批次,以包含更多批间差异,虽然模型的误差可能会增加,但可提高后期模型在实际大生产中的可应用性。因此,在以后的生产过程中仍需不断累计数据,更新并完善模型。
Establishment of online quantitative model for moisture content determination of hydroxychloroquine sulfate particles by near infrared spectroscopy
-
摘要:
目的 为实时检测硫酸羟氯喹颗粒在流化床干燥过程中的水分含量变化,建立颗粒水分的在线近红外光谱定量模型。 方法 物料颗粒在流化床的干燥过程中,实时取样并用水分测定仪测量颗粒水分,采用多元散射校正(multiplicative signal correction, MSC)、一阶导数和Karl Norris平滑的光谱预处理方法,选择近红外4 935~5 336 cm−1和6 911~7 297 cm−1两个波段,运用偏最小二乘回归(partial least squares, PLS)建立基于近红外光谱的水分定量分析模型。 结果 所建模型的校正误差均方根(RMSEC)为0.408,相关系数Rc为0.952 9。预测误差均方根(RMSEP)为0.435,相关系数Rp为0.936 6,验证集标准偏差与预测标准偏差的比值(RPD)为5.18。并将该模型应用于车间生产过程中,t检验结果表明,预测值与参考值之间无显著性差异。 结论 该法所建立的在线水分定量模型准确度较高且较为可靠稳定,该模型可应用于生产过程,以在线监测物料颗粒的水分变化。 Abstract:Objective To establish an online quantitative analysis model for moisture content assay of hydroxychloroquine sulfate particles by near infrared (NIR) spectroscopy. Methods The NIR spectra were collected in real time when the material particles were dried in the fluidized bed. Meanwhile the water content of the particles was measured with the standard moisture tester. The multiplicative signal correction (MSC) and first derivative followed by Karl Norris smoothing were used for spectra pretreatment. Two spectral range (4 935−5 336 cm−1 and 6 911−7 297 cm−1) were selected for the quantitative model with the partial least squares (PLS) regression. Results The quantitative calibration model had good correlation coefficients with Rc value=0.952 9 and Rp value=0.936 6. The root mean square error of calibration (RMSEC) was 0.408 and the root mean square error of prediction error (RMSEP) was 0.435. The ratio of standard deviation of validation set to prediction standard deviation (RPD) was 5.18. There was no significant difference between the predicted value and the reference value by t test when the established model was applied in large-scale production. Conclusion The online model established for monitoring water content has high accuracy and stability, which can be applied in industrial scale process to monitor the particle moisture in real time. -
防暑清热饮是由广藿香、白茅根、菊花、薄荷、枸杞等药材配伍而成的中药复方制剂。方中广藿香为君药,白茅根、菊花为臣药,薄荷为佐药,枸杞为使药,诸药合用,具有芳香化湿、清热解毒、解渴生津之功效[1]。课题组前期已采用紫外分光光度法对防暑清热饮中总多糖和总黄酮进行质量控制[2]。为了更为全面地控制防暑清热饮的质量,本实验参考现有文献[3-16],采取RP-HPLC法同时测定方中多个活性成分含量,现报道如下。
1. 仪器与试药
高效液相色谱仪(AngiLent 1200型,DAD检测器,美国安捷伦科技有限公司),分析天平(AUX220,日本岛津公司)。防暑清热饮(批号:20200120,202002101,202002102,规格:100 ml/瓶,第九〇九医院药剂科),绿原酸对照品(批号:110753-200413)、3,5-O-二咖啡酰奎宁酸(批号:111782-201807)、蒙花苷(批号:111528-201710)和广藿香酮(批号:111822-201904)均购自中国食品药品检定研究院,木犀草素-7-O-β-D-葡糖苷(批号:GZDD-0115,贵州迪大生物科技有限责任公司),甲醇、乙腈为色谱纯,其他试剂为分析纯,水为纯化水。
2. 含量测定
2.1 色谱条件及系统适用性
色谱柱ZORBAX-SB-C18 (250 mm ×4.6 mm,5 μm),流动相为0.2%磷酸水溶液(A)-乙腈(B),梯度洗脱0~30 min,88%~82%A;30~45 min,82%~78%A;45~65 min,78%~35%A;65~75 min,35%A;75~78 min,35%~30%A;78~80 min,30%~88%A;80~82 min,88%A;流速为1.0 ml/min,检测波长为327 nm,柱温为30 ℃,进样量20 μl,理论塔板数按3,5-O-二咖啡酰奎宁酸计算应不低于8 000。
2.2 溶液的制备
2.2.1 对照品溶液
分别精密称定绿原酸、木犀草素-7-O-β-D-葡糖苷、3,5-O-二咖啡酰奎宁酸对照品适量,置于同一10 ml容量瓶中,加甲醇溶解并定量稀释成每1 ml中含绿原酸2.15 mg、木犀草素-7-O-β-D-葡糖苷1.05 mg、3,5-O-二咖啡酰奎宁酸3.00 mg。分别精密称定蒙花苷和广藿香酮对照品适量置于同一25 ml容量瓶中,加甲醇溶解并定量稀释成每1 ml中含蒙花苷0.21 mg和广藿香酮0.05 mg,作为对照品储备液。精密量取各对照品储备液5 ml,置同一25 ml量瓶中,加甲醇稀释至刻度,摇匀,得混合对照品母液。
2.2.2 供试品溶液
精密量取防暑清热饮5 ml,置10 ml容量瓶中,加水稀释至刻度,摇匀,即得供试品溶液。
2.2.3 阴性对照溶液
按处方量制备不含广藿香、白茅根、菊花和薄荷的阴性样品,按“2.2.2”项下供试品方法制备阴性对照溶液。
2.3 专属性考察
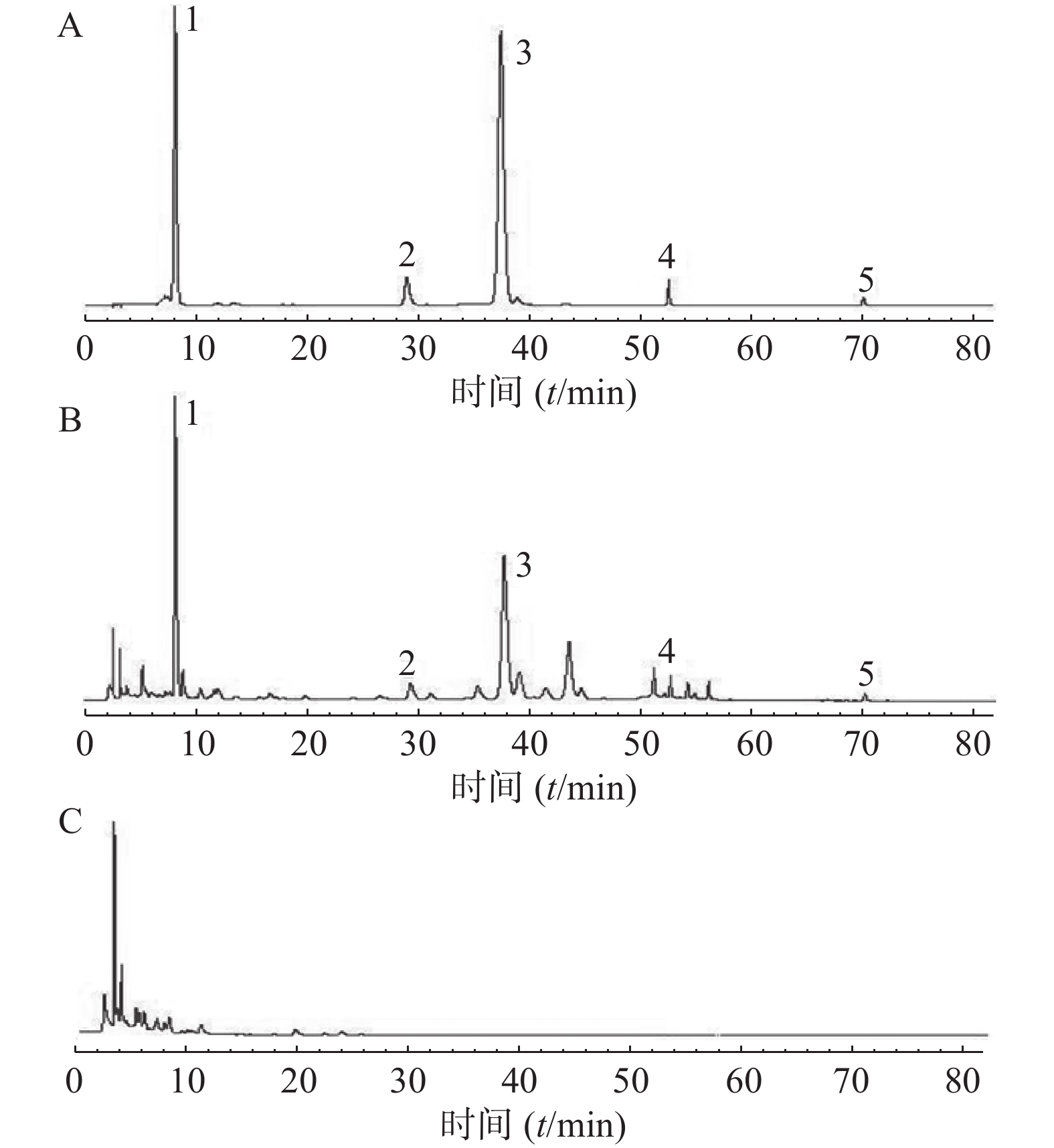
分别取对照品溶液、供试品溶液、阴性对照溶液,按“2.1”项下色谱条件下进样,记录色谱图。结果阴性溶液无干扰,方法专属性良好,见图1。
2.4 线性关系考察
分别精密吸取对照品母液按比例稀释,在上述色谱条件下,分别进样20 μl,以质量浓度X(μg/ml)为横坐标、峰面积Y为纵坐标绘制标准曲线,得线性回归方程,见表1。
表 1 回归方程及线性范围化合物名称 回归方程 r 线性范围(μg/ml) 绿原酸 Y=13.496X-63.194 0.999 9 43.00~430.00 木犀草素-7-O-β-D-葡糖苷 Y=19.707X-169.310 0.999 7 21.00~210.00 3,5-O-二咖啡酰奎宁酸 Y=4.659X-0.895 0.999 7 60.00~600.00 蒙花苷 Y=6.5862X+6.154 0.999 6 4.20~42.00 广藿香酮 Y=11.788X+2.109 0.999 6 1.02~10.20 2.5 精密度试验
取混合对照品溶液,连续进样6次,记录色谱峰面积,绿原酸、木犀草素-7-O-β-D-葡糖苷、3,5-O-二咖啡酰奎宁酸、蒙花苷、广藿香酮峰面积的RSD分别为0.29%、0.30%、0.32%、0.45%、0.45%,表明仪器精密度良好。
2.6 重复性试验
按“2.2.2”项下方法制备供试品溶液6份(批号:20200120),并按“2.1”项下色谱条件进行含量测定。结果显示,防暑清热饮中绿原酸、木犀草素-7-O-β-D-葡糖苷、3,5-O-二咖啡酰奎宁酸、蒙花苷、广藿香酮峰面积的RSD分别为0.56%、0.68%、0.70%、0.94%、1.75%,表明方法重复性良好。
2.7 稳定性试验
将供试品溶液在室温下放置,分别于0、2、4、8、12、24 h进样20 μl,记录色谱峰面积,结果显示,防暑清热饮中绿原酸、木犀草素-7-O-β-D-葡糖苷、3,5-O-二咖啡酰奎宁酸、蒙花苷、广藿香酮峰面积的RSD分别为0.64%、1.16%、0.71%、0.59%、1.36%,结果表明供试品溶液在24 h内稳定性良好。
2.8 加样回收率试验
精密量取已知含量的防暑清热饮2.5 ml,共6份,置10 ml容量瓶中,再分别精密加入对照品适量,加水稀释至刻度,按“2.1”项下色谱条件操作,进样20 μl,记录峰面积,测定其含量,计算平均加样回收率,结果见表2。
表 2 防暑清热饮加样回收率试验结果(n=6)成分 样品含量(m/μg) 加入量(m/μg) 测得量(m/μg) 回收率(%) 平均回收率(%) RSD(%) 绿原酸 369.44 376.00 745.10 99.91 102.03 1.63 369.44 376.00 748.25 100.75 369.44 376.00 756.12 102.84 369.44 376.00 749.80 101.16 369.44 376.00 764.27 105.01 369.44 376.00 754.89 102.51 木犀草素-7-O-β-D-葡糖苷 209.79 210.00 425.37 102.65 102.38 1.51 209.79 210.00 428.48 104.14 209.79 210.00 425.15 102.55 209.79 210.00 419.79 100.00 209.79 210.00 428.48 104.14 209.79 210.00 421.50 100.81 3,5-O-二咖啡酰奎宁酸 452.68 484.00 939.25 100.53 102.39 1.23 452.68 484.00 947.23 102.18 452.68 484.00 956.31 104.06 452.68 484.00 942.56 101.22 452.68 484.00 949.64 102.68 452.68 484.00 954.57 103.70 蒙花苷 42.88 42.00 85.58 101.67 103.14 1.87 42.88 42.00 85.42 101.30 42.88 42.00 87.42 106.05 42.88 42.00 87.13 105.37 42.88 42.00 85.42 101.30 42.88 42.00 86.21 103.16 广藿香酮 7.91 8.20 16.10 99.86 104.01 2.33 7.91 8.20 16.40 103.52 7.91 8.20 16.56 105.47 7.91 8.20 16.43 103.89 7.91 8.20 16.76 107.91 7.91 8.20 16.39 103.40 2.9 样品测定
取3个批号的防暑清热饮样品(批号:20200120,202002101,202002102),各3份,按“2.2.2”项下方法制备防暑清热饮供试品溶液,按“2.1”项下色谱条件操作,进样20 μl,记录峰面积,计算含量,结果见表3。
表 3 3批防暑清热饮含量测定结果(n=3, μg/ml)批号 绿原酸 木犀草素-7-O-β-D-葡糖苷 3,5-O-二咖啡酰奎宁酸 蒙花苷 广藿香酮 20200120 147.97±0.73 83.61±0.53 181.99±0.15 17.26±0.48 3.16±0.30 202002101 142.35±0.15 75.19±1.07 162.42±0.16 14.16±0.86 1.74±0.54 202002102 163.00±0.06 80.24±0.88 215.19±0.04 17.63±0.78 2.09±2.38 3. 讨论
现代药理学研究表明广藿香酮具有抗菌、抗炎、抗氧化、杀虫以及抑制肿瘤细胞的生长等多种生物活性;绿原酸、3,5-O-二咖啡酰奎宁酸属于苯丙素类化合物,具有解热镇痛、抗氧化作用;木犀草素-7-O-D-葡糖苷和蒙花苷属于黄酮类化合物,具有免疫调节、抗氧化、抗炎、抑菌抗病毒等作用。对单味药材进行分析,广藿香中含有广藿香酮;菊花、广藿香、白茅根和薄荷均含有绿原酸;菊花中含有3,5-O-二咖啡酰奎宁酸;菊花和薄荷中含有蒙花苷。中药复方制剂成分复杂,在保证达到检测要求的条件下,综合考虑选择绿原酸、木犀草素-7-O-β-D-葡糖苷、3,5-O-二咖啡酰奎宁酸、蒙花苷、广藿香酮作为液相色谱法检测的指标性成分[17-21]。
本实验分别考察了甲醇-0.1%磷酸、甲醇-0.2%磷酸、乙腈-0.1%磷酸、乙腈-0.2%磷酸4个洗脱溶剂系统作为流动相,结果发现乙腈-0.2%磷酸作为流动相色谱峰时,峰形和分离效果较好,梯度洗脱比等度洗脱分离更好。由于本品为水溶性溶液,被测活性成分极性相对较大,故使流动相起始和结束比例保持一致,即乙腈-0.2%磷酸(12∶88),以确保所测成分在正确的保留时间出峰。
在190~400 nm范围内进行全波长扫描,广藿香酮、3,5-O-二咖啡酰奎宁酸、蒙花苷、绿原酸和木犀草素-7-O-β-D-葡糖苷最大吸收波长分别为308、327、330、325和348 nm,综合考虑选择327 nm作为检测波长。
本实验供试品溶液制备简便,由于本品为液体制剂,用水稀释后直接进样,在该色谱条件下无干扰,故考虑稀释后直接进样。
本实验建立的含量测定方法简便、准确、灵敏,可作为防暑清热饮的质控方法,因不同批次有效成分含量相差较大,考虑可能是药材受产地或采收季节的影响,也可能是该制剂提取工艺稳定性的问题,还需进一步考察,后续需要经过多批次测定以确定质控标准。
-
表 1 不同光谱预处理方法得到的模型参数
预处理方法 RMSEC
(%)RMSEP
(%)RMSECV
(%)R 无预处理方法 0.457 0.499 0.489 0.9206 MSC1 0.467 0.409 0.481 0.9309 SNV2 0.469 0.411 0.483 0.9306 MSC+一阶导数 0.537 0.506 0.585 0.8962 MSC+二阶导数 0.457 0.745 0.867 0.7647 MSC+一阶导数+Norris3 0.408 0.435 0.446 0.9372 SNV+一阶导数 0.537 0.506 0.585 0.8962 SNV+二阶导数 0.456 0.745 0.867 0.7647 SNV+一阶导数+Norris 0.405 0.436 0.446 0.9372 注:1表示多元散射校正;2表示标准归一化变换;3表示平滑滤波。 -
[1] FDA. Guidance for industry PAT—A framework for innovative pharmaceutical development, manufacturing and quality assurance. 2004. https://www.fda.gov/media/71012/download. [2] 褚小立. 近红外光谱分析技术实用手册[M]. 北京: 机械工业出版社. 2016: 127-129. [3] FINDLAY W P, PECK G R, MORRIS K R. Determination of fluidized bed granulation end point using near-infrared spectroscopy and phenomenological analysis[J]. J Pharm Sci,2005,94(3):604-612. doi: 10.1002/jps.20276 [4] MOLTGEN C V, PUCHERT T, MENEZES J C, et al. A novel in-line NIR spectroscopy application for the monitoring of tablet film coating in an industrial scale process[J]. Talanta,2012,92:26-37. doi: 10.1016/j.talanta.2011.12.034 [5] KARANDE A D, HENG P W, LIEW C V. In-line quantification of micronized drug and excipients in tablets by near infrared (NIR) spectroscopy: Real time monitoring of tabletting process[J]. Int J Pharm,2010,396(1-2):63-74. doi: 10.1016/j.ijpharm.2010.06.011 [6] 年秀玲. 类风湿性关节炎应用硫酸羟氯喹治疗的安全性和疗效探析[J]. 北方药学, 2016, 13(12):145. [7] 王文灵. 硫酸羟氯喹治疗风湿病的临床效果研究[J]. 中国现代药物应用, 2016, 10(12):138-139. [8] 魏薇, 何金昌, 余素君. 羟氯喹治疗系统性红斑狼疮的效果评析[J]. 当代医药论丛, 2017, 15(16):138-139. [9] YAMAMOTO Y, SUZUKI T, MATSUMOTO M, et al. Evaluation of the degree of mixing of combinations of dry syrup, powder, and fine granule products in consideration of particle size distribution using near infrared spectrometry[J]. Chem Pharm Bull,2012,60(5):624-631. doi: 10.1248/cpb.60.624 [10] 李沙沙, 陈辉, 赵云丽, 等. 硫酸羟氯喹颗粒水分含量测定近红外定量模型的建立[J]. 沈阳药科大学学报, 2019, 36(7):593-599. [11] 王维皓, 张永欣, 冯伟红, 等. 基于近红外光谱及组合间隔偏最小二乘法的天南星中水分及总黄酮含量测定研究[J]. 中国中医药信息杂志, 2017, 24(7):72-75. [12] 王遥琼, 王维皓. 近红外光谱用于甘草中甘草苷、甘草酸及水分测定[J]. 中国实验方剂学杂志, 2016, 22(19):59-62. [13] 张翠, 柴欣生. 近红外光谱法快速测定甘蔗渣水分和糖分含量[J]. 中华纸业, 2011, 32(22):55-58. [14] CHEN Y, XIE M Y, ZHANG H, et al. Quantification of total polysaccharides and triterpenoids in Ganoderma lucidum and Ganoderma atrum by near infrared spectroscopy and chemometrics[J]. Food Chem,2012,135(1):268-275. doi: 10.1016/j.foodchem.2012.04.089 [15] 杜敏. 中药近红外光谱检测影响因素的研究[D]. 北京中医药大学, 2013. [16] FERNANDEZ PIERNA J A, WAHL F, de NOORD O E, et al. Methods for outlier detection in prediction[J]. Chem Intell Lab Sys,2002,63(1):27-39. doi: 10.1016/S0169-7439(02)00034-5 [17] 闵顺耕, 李宁, 张明祥. 近红外光谱分析中异常值的判别与定量模型优化[J]. 光谱学与光谱分析, 2004, 24(10):1205-1209. [18] 刘蓉, 陈文亮, 徐可欣, 等. 奇异点快速检测在牛奶成分近红外光谱测量中的应用[J]. 光谱学与光谱分析, 2005, 25(2):207-210. [19] GALVAO R K, ARAUJO M C, JOSE G E, et al. A method for calibration and validation subset partitioning[J]. Talanta,2005,67(4):736-740. doi: 10.1016/j.talanta.2005.03.025 [20] 孔霁虹. 青霉素类产品专属在线混合均匀度监测体系设计[D]. 山东大学, 2014. [21] 张学博, 冯艳春, 胡昌勤. 近红外多元校正模型传递的进展[J]. 药物分析杂志, 2009, 29(8):1390-1399. 期刊类型引用(12)
1. 黄紫薇,罗喜,王希,张伶俐. 基于网络药理学和分子对接探讨川牛膝治疗继发性闭经的作用机制. 河南中医. 2024(02): 224-230 .  百度学术
百度学术2. 祝小欢,孙伟伟,储心乔,徐琳. 肾虚血瘀方联合温肾促孕灸法对子宫内膜异位囊肿合并不孕症患者排卵情况、妊娠结局的影响. 河北中医. 2024(05): 730-735 .  百度学术
百度学术3. 杨博,谭凤岐. 补肝肾活血汤联合孕三烯酮治疗子宫内膜异位症临床观察. 实用中医药杂志. 2024(09): 1749-1750 .  百度学术
百度学术4. 唐婷婷,石德志,曹杰,肖莲莲,房雨彤,李秋桐,郑云枫,嵇晶,程建明. 基于网络药理学及实验验证探究石南藤镇痛活性成分的作用机制. 中国新药与临床杂志. 2024(11): 866-872 .  百度学术
百度学术5. 陈丽华,肖丽. 新生化片联合卡孕栓对剖宫产子宫收缩性乏力产后出血的预防效果. 罕少疾病杂志. 2023(04): 60-61 .  百度学术
百度学术6. 谢津,陈亚娟,赵静,周文博,胡巧玲,靳亮,曹媛媛,宋彩霞,侯丽洁. 自拟参芪活血消癥汤联合地诺孕素治疗子宫内膜异位症的效果及对Th17/Treg免疫平衡的影响. 现代中西医结合杂志. 2023(05): 696-699 .  百度学术
百度学术7. 林戴. 活血化瘀中药药理作用分析. 内蒙古中医药. 2023(04): 150-152 .  百度学术
百度学术8. 邵艳社,许雪梅,杨宝芹,李会娟,姬霞. 木犀草素调控HPGD表达抑制子宫内膜间质细胞侵袭和迁移. 安徽医科大学学报. 2023(10): 1706-1711 .  百度学术
百度学术9. 祝洁,薛晓鸥,贺稚平,严培嘉,张嘉蔚,孙海芸. 乌丹丸对寒凝血瘀型EMS模型大鼠内膜血管生成及细胞外调节蛋白激酶-血管内皮生长因子/基质金属蛋白酶9通路的影响. 世界中西医结合杂志. 2022(04): 645-651 .  百度学术
百度学术10. 黄博威,刘启鸿,温劲羽,张慧玲,赵红佳. 基于网络药理学探讨十一味参芪制剂治疗肿瘤作用机制研究. 福建中医药. 2022(07): 16-20 .  百度学术
百度学术11. 陈小菊,徐传花. 从瘀、热、毒论治子宫内膜异位症. 亚太传统医药. 2022(09): 182-186 .  百度学术
百度学术12. 曹慧,贺小林,张状金. 化瘀消异定痛汤联合穴位埋线治疗子宫内膜异位症30例. 湖南中医杂志. 2021(10): 8-11 .  百度学术
百度学术其他类型引用(4)
-





 下载:
下载:
 下载:
下载: