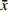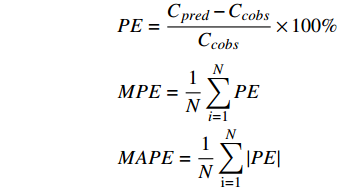-
万古霉素是治疗耐甲氧西林金黄色葡萄球菌(MRSA)感染的一线用药,其治疗窗窄,血药浓度与疗效、不良反应及耐药菌株的产生密切相关[1-3]。目前,临床上借助治疗药物监测(TDM)来监测万古霉素稳态谷浓度,以评估临床疗效及不良反应。然而,TDM具有滞后性,不能用于制订给药方案及预测目标浓度;且在万古霉素给药后,如未达治疗窗,则需反复多次监测血药浓度,方能找到合适的给药方案。因此,一些医院引入万古霉素个体化给药系统,用以辅助临床决策万古霉素给药方案,目的是规避TDM的不足。
万古霉素个体化给药系统旨在利用群体药代动力学模型(PPK)模拟个体化给药,国内外已开发的系统有Vancomycin-calculator、TDMS2000、ClinCalc、GlobalRPh.com及JPKD[4-8]等。然而,因建模数据集的人口学特征各有不同,PPK模型对不同人群的模拟性能存在差异[9-10]。由于上述系统主要是以西方国家人群数据计算出的PPK参数模型,在应用于中国人群时,常出现明显误差[11]。
2017年焦正教授团队研发了个体化给药系统Smart Dose,该系统是基于中国人群的万古霉素PPK模型,使用贝叶斯算法,可设计及调整万古霉素的给药方案;适应人群包括使用万古霉素的普通成人以及特殊人群(新生儿、老年人、神经外科患者)等[12]。Smart Dose功能包括制定万古霉素初始方案、万古霉素调整方案及自定义用药方案。本研究将对Smart Dose用于中国人群万古霉素稳态谷浓度的效能预测进行评价,探讨其在万古霉素个体化给药过程中的作用意义。
-
纳入2018年12月至2019年4月海军军医大学(第二军医大学)长海医院接受万古霉素治疗的患者,进行常规TDM监测。收集资料包括:①患者基本信息及用药指征,如姓名、年龄、性别、身高、体重、入出院时间、血常规、血清肌酐值、病原微生物检查、药敏试验结果等;②万古霉素TDM监测方案,如万古霉素血药浓度(谷)、给药方案、给药时间、滴注时长、采血时间等。
纳入标准:①2018年12月至2019年4月在长海医院住院期间使用万古霉素,且至少测定了1次万古霉素谷浓度的患者;②年龄≥18岁;③万古霉素用药量满4个维持剂量;④准确记录给药时间及采血时间;⑤用药前后均进行了肾功能检查。
排除标准:①年龄<18岁;②基本资料及肾功能检查结果缺失的患者;③万古霉素用药量不足4个维持剂量的患者;④给药时间及血药浓度监测采血时间未记录或不准确的患者;⑤行腹膜透析或者血液透析治疗的患者。
-
仪器:ARCHITECTi1000SR全自动免疫分析仪、Abbott离心机(美国雅培公司)。
试药:万古霉素(规格:0.5 g,Eli Lilly Japan KK, Seishin Laboratorie);万古霉素(规格:0.5 g,浙江医药有限公司新昌制药厂);万古霉素校准品(0、5、10、25、50和100 μg/ml);LiquichekTM TDM质控品(批号:27740,美国伯乐),包含Level 1[7.34(6.29–8.40)μg/ml]、Level 2 [21.8(18.2–25.3)μg/ml]和Level 3 [38.8(32.3–45.2)μg/ml]。最低定量限为2.5 μg/ml,允许误差为±24%。
血样采集:患者在万古霉素给药4~5个半衰期,血药浓度达到稳态后,于下一次给药前30 min采集外周静脉血,采用化学发光微粒子免疫分析法(CMIA)测得的万古霉素稳态谷浓度;如调整剂量,则按剂量调整给药3~4个半衰期后,下一次给药前30 min采血复查。
-
Smart Dose万古霉素个体化给药系统是应用R语言中的rjags程序包调用JAGS软件, 实现最大后验贝叶斯法(MAPB)估算;该系统根据患者基本资料(性别、年龄、体重及身高),肾功能检查(肌酐值)及给药方案(给药剂量、给药时间、滴注时间、采血时间)预测万古霉素谷浓度。
将预测浓度分为初始预测浓度和调整预测浓度,初始预测浓度是根据患者年龄﹑性别﹑体重和肌酐、给药方案等参数估算出的初始稳态谷浓度;调整预测浓度是将大于等于一个万古霉素谷浓度实测值代入系统后,测算出新的药动学参数,进而预测得出的后续稳态谷浓度,即调整预测浓度。依据上述方法得出并比较Smart Dose对初始预测浓度和调整预测浓度的预测效能。
Smart Dose系统设置了不同人群模块,根据模块将患者来源分为神经外科患者和非神经外科患者两组,根据现有数据对预测结果进行对比分析,比较不同来源的患者的初始浓度预测效能。
将年龄中位数分为高年龄组(≥59岁)和低年龄组(<59岁);给药前肌酐清除率以中位数分为高清除率组(≥90.97 ml/min)和低清除率组(<90.97 ml/min);谷浓度以中位数分为高浓度组(≥8.16 mg/L)和低浓度组(<8.16 mg/L);根据单日给药剂量不同,分为高剂量组(>1500 mg/d)和低剂量组(≤1500 mg/d);根据中华人民共和国成人体质量判定诊断标准[13],依据BMI指数将患者分为肥胖组(≥28 kg/m2)和非肥胖组(<28 kg/m2);对各组分别进行初始浓度预测值与实测值的比较,探究以上因素对初始预测效能的影响。
-
运用SPSS 21.0软件进行数据统计,对浓度预测值与实测值采用配对t检验及Bland-Altman图进行分析评价;实测值与预测值的差异,采用百分误差(PE)、平均百分比误差(MPE)以及平均绝对百分比误差(MAPE)表示。
$$ \begin{array}{l} PE = \displaystyle\frac{{{C_{pred}} - {C_{cobs}}}}{{{C_{cobs}}}} \times 100\% \\ MPE = \displaystyle\frac{1}{N}\sum\limits_{i = 1}^N {} PE\\ MAPE = \displaystyle\frac{1}{N}\sum\limits_{{\rm{i}} = 1}^N {|PE} | \end{array}$$ -
共纳入71例患者,其中男性患者48例,占总人数的67.6%;送检患者主要为颅内感染20例、肺部感染18例、感染性心内膜炎13例,骨关节置换术后感染7例,腹腔感染6例,其他感染7例;初始给药方案1000 mg,q12 h 50例;500 mg,q8 h 14例;500 mg,q12 h 6例;其他给药方案1例;万古霉素均采取静脉滴注方式给药。基本资料见表1。
表 1 万古霉素抗感染患者人口学统计资料
基本信息参数 例数/占比[n(%)] 中位数(最小值;最大值) 均数($ \bar x$±s) 年龄(a/y) 71(100) 59(18;97) 57.35±19.87 <59 35(49.3) 45(18;58) 40.66±12.63 ≥59 36(50.7) 74(59;97) 73.58±9.24 体重(m/kg) 71(100) 67(38;96) 67.53±13.76 给药前肌酐清除率(ml/min) 71(100) 90.97(27.78;232.07) 100.25±46.51 <90.97 35(49.3) 66.57(27.78;90.18) 64.39±18.11 ≥90.97 36(50.7) 120.52(90.97;232.07) 135.11±38.36 谷浓度(c/mg/L) 71(100) 8.16(1.12;52.54) 10.91±8.71 <8.16 35(49.3) 5.61(1.12;7.86) 5.17±2.00 ≥8.16 36(50.7) 13.80(8.16;52.54) 16.84±9.10 万古霉素日剂量(m/mg) 71(100) 2000(1000;2000) 1767.61±394.89 ≤1500 20(28.2) 1000(1000;1500) 1175.00±244.68 >1500 51(71.8) 2000(2000;2000) 2000.00±0.00 BMI(kg/m2) 71(100) 23.88(14.84;32.87) 24.07±4.09 <28 57(80.3) 22.89(14.84;27.77) 22.58±3.01 ≥28 14(19.7) 29.41(28.96;32.87) 30.11±1.30 注:使用MDRD公式计算CLCR肌酐清除率 -
初始预测浓度组纳入71例初始浓度实测值,调整预测浓度组纳入22例调整浓度实测值。结果显示,初始浓度实测值与预测值的百分误差平均值为35.5%,允许的最大误差范围F30=34.3%;调整浓度实测值与预测值的百分误差平均值仅为11.2%,允许的最大误差范围F30=63.6%。初始浓度预测值与实测值误差(PE=35.47±74.49,MPE=35.5%,MAPE=57.9%)和调整浓度预测值与实测值误差(PE=−11.16±31.71,MPE=−11.2%,MAPE=25.4%)之间有差异有统计学意义(P=0.01),调整浓度预测值误差更低,即调整浓度预测值更接近于实测值。Smart Dose预测值与实测值的Bland-Altman图如图1所示;两组预测误差的PE、MPE和MAPE见表2。
表 2 Smart Dose预测万古霉素稳态谷浓度的效能
预测浓度分组 PE(%) MPE(%) MAPE(%) 初始预测浓度 35.47±74.49 0.355 0.579 调整预测浓度 −11.16±31.71 −0.112 0.254 -
神经外科组纳入21例万古霉素初始浓度实测值;非神经外科组纳入50例初始浓度实测值。
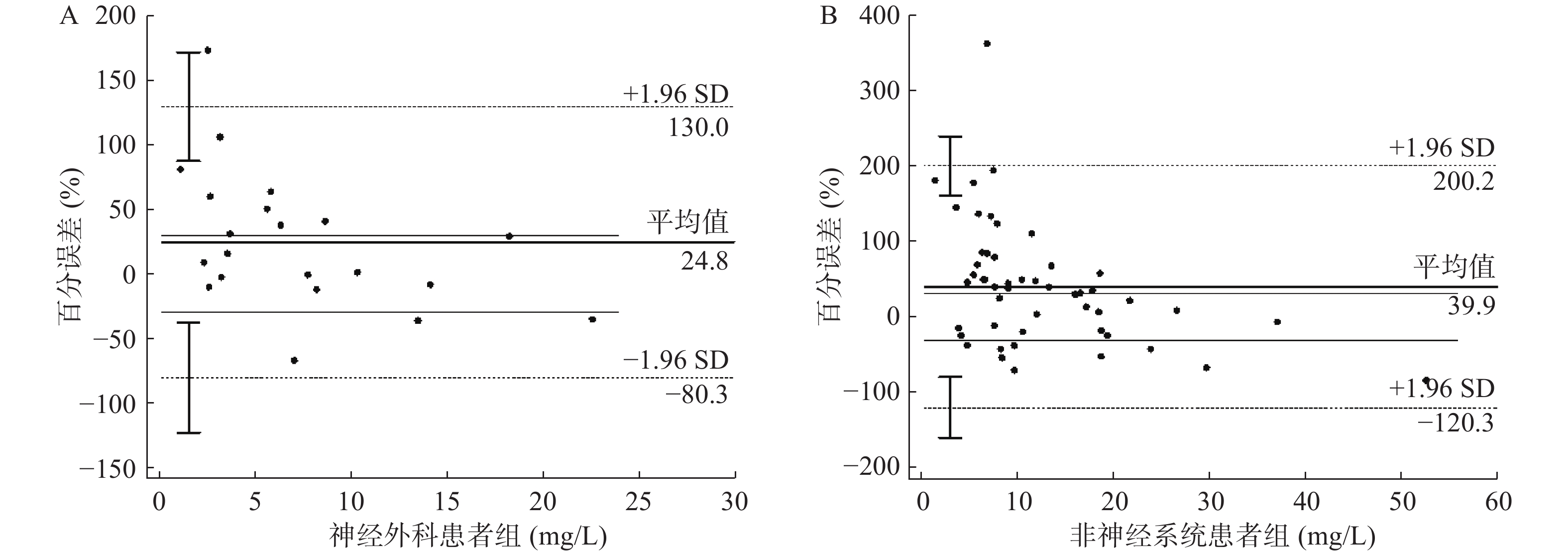
Smart Dose预测结果显示,与非神经外科组患者(PE=39.93±81.75,MPE=39.9%,MAPE=64.8%)相比,神经外科组患者(PE=24.84±53.65,MPE=24.8%,MAPE=41.5%)的PE,MPE及MAPE均低于非神经外科患者组,差异有统计学意义(P=0.03),即神经外科组患者的初始浓度预测值更接近于真实值。预测结果的Bland-Altman图如图2所示;两组预测误差的PE、MPE及MAPE见表3。
表 3 Smart Dose针对非神经外科患者组和神经外科患者组初始稳态谷浓度的预测效能
预测浓度分组 PE(%) MPE(%) MAPE(%) 神经外科患者组 24.84±53.65 0.248 0.415 非神经外科患者组 39.93±81.75 0.399 0.648 -
根据年龄中位数分为高年龄组(≥59岁)和低年龄组(<59岁),高年龄组和低年龄组分别纳入36例和35例万古霉素血药浓度初始实测值。将给药前肌酐清除率以中位数分为高清除率组(≥90.97 ml/min)和低清除率组(<90.97 ml/min),分别纳入36例和35例万古霉素血药浓度初始实测值;将谷浓度以中位数分为高浓度组(≥8.16 mg/L)和低浓度组(<8.16 mg/L),分别纳入36例和35例万古霉素血药浓度初始实测值。根据单日给药剂量不同,分为高剂量组(>1500 mg/d)和低剂量组(≤1500 mg/d),分别纳入51例和20例万古霉素血药浓度初始实测值。根据BMI指数将患者分为肥胖组(≥28 kg/m2)和非肥胖组(<28 kg/m2),肥胖组和非肥胖组分别纳入14例和57例万古霉素血药浓度初始实测值。分别比较各组间的PE、MPE、MAPE(见表4)。结果表明,Smart Dose对于高浓度组的初始浓度预测值更准确(P=0.001),对于不同的年龄(P=0.589)、肌酐清除率(P=0.537)、日剂量(P=0.386)、BMI(P=0.760)初始浓度的预测效能相仿。
表 4 Smart Dose对不同情况患者初始稳态谷浓度的预测效能
分组 PE(%) MPE(%) MAPE(%) 高年龄组 58.52±75.42 0.585 0.651 低年龄组 11.76±66.54 0.118 0.491 高清除率组 36.96±69.89 0.370 0.622 低清除率组 33.94±79.95 0.339 0.535 高浓度组 1.66±44.01 0.017 0.363 低浓度组 70.24±83.52 0.702 0.801 高剂量组 33.12±63.19 0.331 0.541 低剂量组 41.45±99.41 0.415 0.676 肥胖组 42.97±49.87 0.430 0.536 非肥胖组 33.63±79.63 0.336 0.590 -
本研究在评价新型万古霉素个体化给药系统Smart Dose临床效用的方向上,针对其预测效能(PE、MPE及MAPE)进行数据分析。根据系统本身模块设置,将所收集数据分为初始预测浓度组与调整预测浓度组,分析结果显示Smart Dose调整预测浓度在PE、MPE及MAPE方面均优于初始浓度预测值,即调整浓度预测值与实测值的接近程度优于初始浓度预测值与实测值[12],提示Smart Dose系统更适合用于调整给药方案;建议患者先进行万古霉素血药浓度的TDM监测,获得一个实测浓度值后,再利用Smart Dose进行浓度调整,其结果会更加接近真实值。这可能因为调整预测浓度带入了前一次实测浓度、准确的滴注时间及采血时间,经过贝叶斯法得到新的药动学参数(表观分布容积、表观清除率)后,再根据给药方案进行预测。国内外多篇文献报道表明,药代动力学结合贝叶斯法能够更为准确地预测万古霉素血药浓度,且准确的给药时间、采血时间、滴注时间能够辅助预测[14-16]。
有研究表明,神经外科术后患者万古霉素的清除率高于非神经外科患者,而万古霉素在患者发生脑膜炎时可以透过血脑屏障进入脑脊液[17-18],可见,神经外科患者在使用万古霉素时自身药动学参数有别于非神经外科患者,Smart Dose系统在研制时亦将二者区分[12]。故本研究将所收集数据分为神经外科患者组和非神经外科患者组,结果发现,Smart Dose对神经外科患者组预测效能(PE、MPE及MAPE)优于非神经外科患者组。这可能与系统本身将神经外科患者药动学参数模板单独建立,区别于普通患者有关。
本研究浓度数据离散程度较大,这可能与样本中存在高龄、自身的肾功能不全的患者有关,部分高龄或ICU患者实验室检查肌酐值普遍偏低[19-20],此时不能单纯以肌酐值来衡量患者的肾功能;危重患者炎症反应、应激反应剧烈,可导致有效血容量不足,临床中可能会采用液体复苏保证有效的循环血量,因此,可能会影响万古霉素的药物分布和消除[20]。此外,老年重症患者肌酐清除率往往成为影响谷浓度的主要因素,降低了年龄及体重的影响,结果出现了一定的偏差[21]。同时,本研究发现高浓度组患者预测准确性较低浓度组高,这可能因为部分谷浓度在限定量以下的患者初始浓度实测值的准确性本身存在偏差,而低浓度患者在应用Smart Dose等个体化给药系统进行稳态谷浓度预测时,极有可能出现绝对误差过大的情形。再者,在TDM监测中,Smart Dose采用的荧光偏振免疫法与本实验的化学微粒发光法测量结果可能存在差异,需要矫正,否则直接使用结果可能出现误差增大的现象[22-23]。因此,临床药师需结合患者本身情况和疾病特点,优化个体药动学参数,以Smart Dose做为辅助手段来为临床合理用药提供依据。
本研究收集样本例数有限,仅Smart Dose关于万古霉素初始给药方案及调整给药方案两个模块进行效能评估,未对自定义给药方案(可用于模拟停药)进行评估。后续将扩大临床研究,完善对万古霉素个体化给药系统Smart Dose的效能评估,为合理应用Smart Dose用于临床万古霉素初始给药方案制定及调整提供科学依据。
Evaluation of Smart Dose's predictive effectiveness on vancomycin blood concentration
-
摘要:
目的 评价个体化给药决策支持系统Smart Dose应用于中国人群治疗药物监测的临床效用。 方法 使用Smart Dose系统预测患者万古霉素谷浓度,分析谷浓度预测值与实测值之间的差异,以评价该系统对于万古霉素血药浓度的预测效能。 结果 Smart Dose调整浓度预测值与实测值之间的差异,平均百分比误差,平均绝对百分比误差小于初始浓度预测值与实测值之间的差异。神经外科组患者初始浓度预测值与实测值的差异比非神经外科组患者小,预测效能优于非神经外科组。高谷浓度组和低年龄组(<59岁)的初始浓度预测值更接近于实测值。不同的BMI对于初始浓度的预测效能相仿。 结论 Smart Dose系统更适合于万古霉素调整浓度的预测。用于初始浓度预测时,神经外科组、高谷浓度及低年龄组的预测值更准确。不同的BMI对于初始浓度预测效能相仿。 Abstract:Objective To evaluate clinical utility of the personalized drug delivery decision support system, Smart Dose, applied to the monitoring of therapeutic drugs in Chinese population. Methods Use Smart Dose system to predict the trough concentration of vancomycin in patients, analyze the difference between the predicted value and the measured value of the trough concentration, and to evaluate the prediction performance of the system for vancomycin blood concentration. Results Smart Dose adjusts the difference between the predicted value of concentration and the measured value, the average percentage error, and the average absolute percentage error is less than the difference between the predicted value of initial concentration and the measured value. The difference between the initial concentration prediction value and the measured value of the neurosurgery group was smaller than that of the non-neurosurgery group, and the prediction efficiency was better than that of the non-neurosurgery group. The predicted initial concentration of the high trough concentration group and the low-age group (<59 years old) are closer to the measured value. The predictive performance of different BMI for the initial concentration is similar. Conclusion Smart Dose system is more suitable for predicting the adjusted concentration of vancomycin; When used for initial concentration prediction, the prediction values of neurosurgery group, high trough concentration, and low age group are more accurate. Different BMI has similar performance in predicting initial concentration. -
Key words:
- vancomycin /
- therapeutic drug monitoring /
- software
-
表 1 万古霉素抗感染患者人口学统计资料
基本信息参数 例数/占比[n(%)] 中位数(最小值;最大值) 均数( $ \bar x$ ±s)年龄(a/y) 71(100) 59(18;97) 57.35±19.87 <59 35(49.3) 45(18;58) 40.66±12.63 ≥59 36(50.7) 74(59;97) 73.58±9.24 体重(m/kg) 71(100) 67(38;96) 67.53±13.76 给药前肌酐清除率(ml/min) 71(100) 90.97(27.78;232.07) 100.25±46.51 <90.97 35(49.3) 66.57(27.78;90.18) 64.39±18.11 ≥90.97 36(50.7) 120.52(90.97;232.07) 135.11±38.36 谷浓度(c/mg/L) 71(100) 8.16(1.12;52.54) 10.91±8.71 <8.16 35(49.3) 5.61(1.12;7.86) 5.17±2.00 ≥8.16 36(50.7) 13.80(8.16;52.54) 16.84±9.10 万古霉素日剂量(m/mg) 71(100) 2000(1000;2000) 1767.61±394.89 ≤1500 20(28.2) 1000(1000;1500) 1175.00±244.68 >1500 51(71.8) 2000(2000;2000) 2000.00±0.00 BMI(kg/m2) 71(100) 23.88(14.84;32.87) 24.07±4.09 <28 57(80.3) 22.89(14.84;27.77) 22.58±3.01 ≥28 14(19.7) 29.41(28.96;32.87) 30.11±1.30 注:使用MDRD公式计算CLCR肌酐清除率 表 2 Smart Dose预测万古霉素稳态谷浓度的效能
预测浓度分组 PE(%) MPE(%) MAPE(%) 初始预测浓度 35.47±74.49 0.355 0.579 调整预测浓度 −11.16±31.71 −0.112 0.254 表 3 Smart Dose针对非神经外科患者组和神经外科患者组初始稳态谷浓度的预测效能
预测浓度分组 PE(%) MPE(%) MAPE(%) 神经外科患者组 24.84±53.65 0.248 0.415 非神经外科患者组 39.93±81.75 0.399 0.648 表 4 Smart Dose对不同情况患者初始稳态谷浓度的预测效能
分组 PE(%) MPE(%) MAPE(%) 高年龄组 58.52±75.42 0.585 0.651 低年龄组 11.76±66.54 0.118 0.491 高清除率组 36.96±69.89 0.370 0.622 低清除率组 33.94±79.95 0.339 0.535 高浓度组 1.66±44.01 0.017 0.363 低浓度组 70.24±83.52 0.702 0.801 高剂量组 33.12±63.19 0.331 0.541 低剂量组 41.45±99.41 0.415 0.676 肥胖组 42.97±49.87 0.430 0.536 非肥胖组 33.63±79.63 0.336 0.590 -
[1] 张致平. 抗耐药菌药物研究进展[J]. 中国临床药理学杂志, 2003, 19(1):50-56. doi: 10.3969/j.issn.1001-6821.2003.01.014 [2] 李光辉. 万古霉素临床应用剂量中国专家共识[J]. 中华传染病杂志, 2012, 30(11):641-646. doi: 10.3760/cma.j.issn.1000-6680.2012.11.001 [3] RYBAK M J, LE J, LODISE T P, et al. Executive summary: therapeutic monitoring of vancomycin for serious methicillin-resistant Staphylococcus aureus infections: a revised consensus guideline and review of the American Society of Health-system Pharmacists, the Infectious Diseases Society of America, the Pediatric Infectious Diseases Society, and the Society of Infectious Diseases Pharmacists[J]. Pharmacotherapy,2020,40(4):363-367. doi: 10.1002/phar.2376 [4] FEWEL N P. Vancomycin-calculator[CP/OL]. (2020-06-26) [2016-07-22]. http://Vancomycin-Calculator.com. [5] ANDERSON P. Vancomycin dosing calculator. TDMS2000[CP/OL]. (2020-06-26). http://tdms2000.com. [6] KANE S P. Vancomycin calculator. ClinCalc[CP/OL]. (2020-06-29)[2016-05-21]. http://clincalc.com/Vancomycin/default.aspx. [7] MCAULEY D. Aminoglycoside-vancomycin dosing. GlobalRPh[CP/OL](2020-06-29)[2016-05-21]. http://globalrph.com/aminoglycosides.htm. [8] 何娟, 杨婉花. 基于群体药动学的万古霉素个体化给药模式的建立和临床应用[J]. 中国临床药学杂志, 2015, 24(1):27-31. [9] 凌静, 蒋艳, 胡楠, 等. 免费万古霉素个体化给药软件预测谷浓度的效能评估[J]. 中国医院药学杂志, 2018, 38(22):2328-2331. [10] FEWEL N P. Comparison of open-access vancomycin dosing websites[J]. J Clin Pharm Ther,2017,42(2):128-131. doi: 10.1111/jcpt.12466 [11] 何娜, 闫盈盈, 苏珊, 等. 基于药代动力学方法支持的万古霉素个体化给药现状[J]. 中国临床药理学杂志, 2018, 34(1):63-65, 69. [12] 高玉成, 焦正, 黄虹, 等. 万古霉素个体化给药决策支持系统的研制[J]. 药学学报, 2018, 53(1):104-110. [13] 中华人民共和国国家卫生和计划生育委员会. 成人体重判定: WS/T 428—2013[S]. 北京: 中国标准出版社, 2013. [14] TASA T, METSVAHT T, KALAMEES R, et al. DosOpt: a tool for personalized Bayesian dose adjustment of vancomycin in neonates[J]. Ther Drug Monit,2017,39(6):604-613. doi: 10.1097/FTD.0000000000000456 [15] PAI M P, NEELY M, RODVOLD K A, et al. Innovative approaches to optimizing the delivery of vancomycin in individual patients[J]. Adv Drug Deliv Rev,2014,77:50-57. doi: 10.1016/j.addr.2014.05.016 [16] 陈冰, 杨婉花. 群体药代动力学在万古霉素治疗药物监测的应用[J]. 中国临床药理学杂志, 2011, 27(9):713-717. doi: 10.3969/j.issn.1001-6821.2011.09.018 [17] LIN WU F L, LIU S S, YANG T Y, et al. A larger dose of vancomycin is required in adult neurosurgical intensive care unit patients due to augmented clearance[J]. Ther Drug Monit,2015,37(5):609-618. doi: 10.1097/FTD.0000000000000187 [18] KIM A J, LEE J Y, CHOI S A, et al. Comparison of the pharmacokinetics of vancomycin in neurosurgical and non-neurosurgical patients[J]. Int J Antimicrob Agents,2016,48(4):381-387. doi: 10.1016/j.ijantimicag.2016.06.022 [19] 李青栋, 万献尧, 李缺缺, 等. 重症监护病房内急性肾损伤患者胱抑素C与肌酐估算肾小球滤过率的动态对比研究[J]. 中华全科医师杂志, 2014, 13(3):228-230. doi: 10.3760/cma.j.issn.1671-7368.2014.03.025 [20] 尹燕燕, 朱婧, 姜利. ICU患者万古霉素血药浓度不达标的相关因素分析[J]. 中国医药导报, 2018, 15(21):110-113. [21] 周庆涛, 贺蓓, 沈宁, 等. 肾清除率对老年重症肺炎患者体内万古霉素谷浓度的影响[J]. 中华结核和呼吸杂志, 2016, 39(2):105-109. doi: 10.3760/cma.j.issn.1001-0939.2016.02.006 [22] 程丽静, 赵冠人, 冯端浩. CMIA法与FPIA法检测环孢素A血药浓度的比较研究[J]. 中国药房, 2013, 24(42):3971-3973. [23] CHEN C Y, LI M Y, MA L Y, et al. Precision and accuracy of commercial assays for vancomycin therapeutic drug monitoring: evaluation based on external quality assessment scheme[J]. J Antimicrob Chemother,2020,75(8):2110-2119. -





 下载:
下载: