-
随着人口老龄化进程加快,以脑、脊髓结构或功能损伤导致的中枢神经系统(CNS)疾病的发病率和病死率逐年上升[1]。尽管对CNS疾病病因的认识已有重大进展,但是新药研发进程依旧进展缓慢,主要原因是CNS疾病发病机制复杂,以及在药物研发阶段缺少可靠有效的评价手段[2]。随着系统生物学技术的不断发展,1999年Nicholson等[3]提出的代谢组学通过研究生物体受到外界刺激或基因缺陷所导致的代谢终产物的变化情况,为研究疾病的发病机制和药物疗效评估提供了一种新手段。来源于患者或疾病动物模型的生物体样本,如血液、尿液、组织提取液等的代谢组学研究是目前的主要研究方向,但是实验研究需要大量样本数据支持,且受到伦理以及生物体内外混杂因素的影响,具有一定的局限性。细胞是构成生物体结构和功能的基本单位,体外细胞模型可建立单一症状的疾病模型、具有可控性强、有利于进行大规模药物筛选等特点而备受研究人员青睐。细胞代谢组学是以细胞为研究对象,通过现代分析方法监测细胞反应及药物作用于细胞后的代谢变化,在探寻CNS疾病的病理生理机制及治疗干预效果中展现出巨大潜力[4]。本文拟从细胞代谢组学的研究流程及其在中枢神经系统疾病中的应用进行综述,以期为从细胞层面探索中枢神经系统疾病发病机制和新药研发提供参考。
-
细胞代谢组学通过现代分析方法对细胞新陈代谢后产生的差异代谢物进行定性、定量研究。介于细胞内和细胞外代谢之间的密切关系,完整的细胞代谢组学研究包括细胞内指纹(细胞内所有代谢物)和细胞外足迹(细胞外介质所有代谢物)两部分[5],其主要流程为细胞培养、样品前处理、分析检测、代谢组学数据处理(图1)。
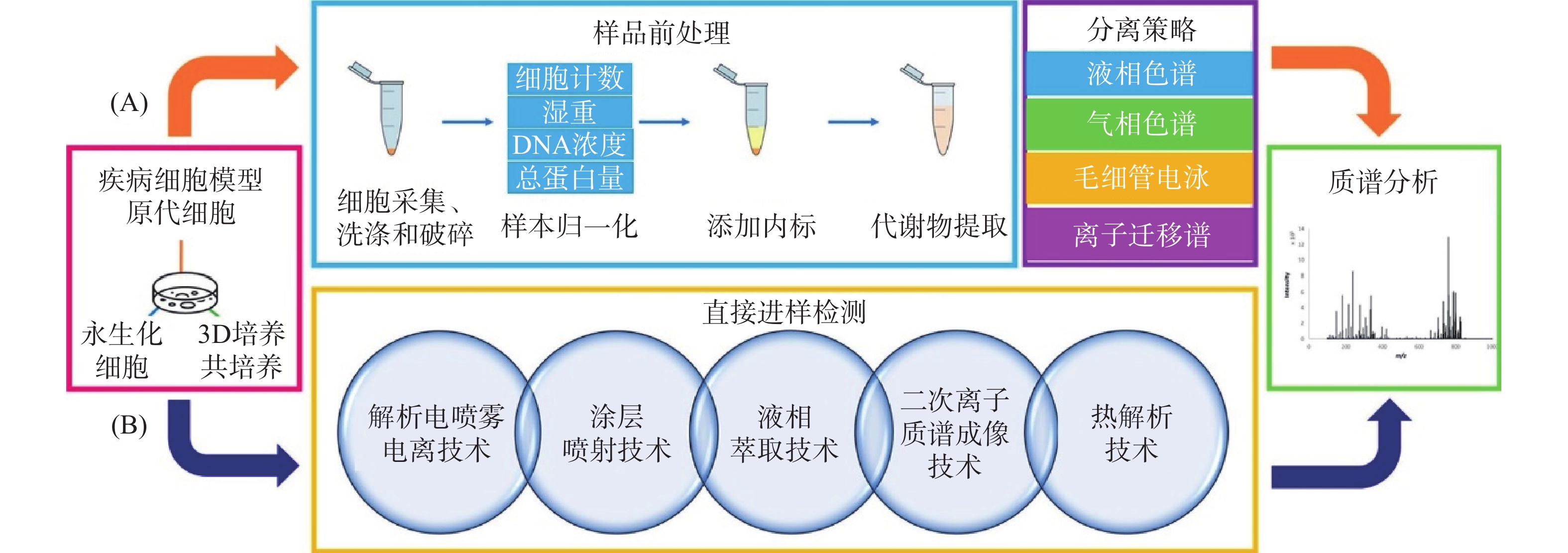
图 1 细胞代谢组学工作流程[6]
-
细胞类型和培养方法的选择对模拟疾病状态和深入了解疾病的代谢框架至关重要。来源于生物体的原代细胞是疾病研究的理想细胞模型,但其寿命有限,纵向研究具有一定挑战性。因此,能够快速分裂的癌细胞和永生化细胞被广泛用于体外模型的构建中。有研究表明,体外和体内细胞培养条件不同易导致细胞特性的改变[7]。为了能更准确地模拟体内微环境,自20世纪初建立以来,改进细胞培养技术的尝试从未停止,如在二维单层培养的基础上,研发出三维培养技术、旋转式细胞培养系统、多细胞共培养等培养模式,更加贴近细胞在生物体的生存环境[8-10]。
提取目标代谢物是细胞代谢组学分析的关键步骤。一些代谢物在样品前处理过程中受到干燥-重构的影响易产生损失或变异,因而优化样品前处理方法、建立细胞代谢组学标准化分析流程显得尤为重要[11]。Wilkins等[12]比较胰蛋白酶消化、刮刀刮取、−80 ℃甲醇淬灭以及−80 ℃甲醇淬灭后去除甲醇这4种常用的细胞代谢物提取方法,结果显示,−80 ℃甲醇快速淬灭得到的细胞代谢物稳定性和富集程度较好,且样品在−80 ℃甲醇条件下可以储存长达1个月而没有明显的代谢物降解。Ser等[13]发现温度和添加剂对细胞代谢物的影响很小,而使用磷酸盐缓冲溶液或水洗涤样品对代谢物影响较大,并提出用冷甲醇提取且不经任何洗涤可以满足绝大多数代谢物的提取。随着质谱等检测仪器的不断开发和进步,不经任何前处理将采集到的细胞代谢物直接进样分析也成为了可能[14]。
-
核磁共振波谱法(NMR)和质谱法(MS)是细胞代谢组学研究的常用分析方法。NMR可追踪代谢物流动来识别活跃的代谢途径、测量代谢通量或相应的示踪剂代谢变化,所需样品量少,具有出色的重现性、定量以及鉴定未知代谢物的能力。Saborano等[15]提出一种基于NMR法的哺乳动物细胞系和原代细胞系代谢研究框架,可用于糖酵解、戊糖磷酸循环等多种代谢途径分析。具体工作流程为将含有13C或15N标记的前体物质引入细胞培养基中培养细胞,使用甲醇-氯仿-水提取代谢物,通过异核单量子相干谱(HSQC)、二维NOE谱(NOESY)等技术采集带标记代谢物的光谱信息,探寻细胞系中健康和疾病状态的代谢差异。然而,NMR相对较低的灵敏度使其无法测量低丰度的代谢物。越来越多新型NMR方法包括多维NMR技术、快速脉冲NMR技术、核磁共振显微技术等也逐渐应用于细胞代谢组学研究,为生物标志物的寻找提供了有力手段。
MS的优势在于其灵敏度高、覆盖面广、可与多种色谱技术联用实现代谢物的有效分离。气相色谱-质谱联用法(GC-MS)可用于氨基酸、核苷酸和脂肪酸等挥发性代谢物的分析,具有较强的针对性。为简化样品制备过程中对挥发性代谢物的衍生化步骤,Araujo等[16]优化了一种基于顶空固相微萃取(HS-SPME)结合GC-MS方法,通过纤维涂层对细胞外代谢物中挥发性组分萃取后直接进样分析,可实时监测挥发性有机物的代谢过程。液相色谱-质谱联用法(LC-MS)包括反相液相色谱(RPLC)和亲水作用液相色谱(HILIC)与MS的联用,其中RPLC总体上表现出比HILIC更好的适用性和重复性,被广泛应用于细胞代谢物的分析中,尤其适用于非极性和弱极性代谢物,而HILIC对亲水性、极性和离子性代谢物如糖、氨基酸和核酸有更好的分离效果[17]。Sun等[18]采用UHPLC-QQQ/MS法对细胞外代谢物进行分析,液相分离条件的优化分别考察了7根反相UHPLC柱和5根HILIC柱,以峰面积、半峰宽、拖尾因子、峰面积CV(%)、保留时间及其SD值共6个指标评价分离效果,最终选择了其中的1根反相UHPLC柱和流动相,单次检测时间仅17 min,实现了同时检测氨基酸、糖类等93种代谢物,为开展实时监测细胞代谢物水平变化提供了可能性。
考虑到细胞间存在异质性,为获得更加丰富的细胞代谢物信息,现代生命科学研究将目光投向了单个细胞。微流控芯片可以在与细胞大小相当的微通道内进行细胞培养、样品制备、分离检测等一系列操作,是单细胞代谢组学分析的重要技术平台[19],相比于LC-MS,微流控芯片质谱法操作简单,可直接进样分析,但存在选择性差和离子抑制等问题,Xu等[20]将微流控芯片与纳米电喷雾电离质谱相联用,通过对金纳米颗粒进行特异性标记,大大提高单细胞水平内源代谢物检测的灵敏度和兼容性。得益于质谱成像仪器的快速发展,空间分辨代谢组学技术可以对目标代谢物在细胞中的分布进行定位,提供多维度代谢组学信息,是目前单细胞代谢组学研究的强有力工具[21]。
-
代谢物的存在和浓度变化可以直接体现细胞对周围化学和物理微环境的反应,具有高度动态性和未知性,庞大的数据集使得细胞代谢组学的数据分析和解释需借助生物信息学[22]。基于R、Python、C/C++ 等编程语言的代谢组学数据处理的软件资源有很多,但是尚未研发出通用的数据处理软件,需要用户根据分析目的对多种软件程序整合后优化使用[23]。Zhou等[24]在IP4M代谢组学数据分析集成平台的基础上,开发出IMAP集成代谢组学分析平台,不仅可以实现一站式完整的代谢组数据分析,而且有多种可供选择的分析方法和工作流程,可用于建立和验证预测模型以及相关的网络构建和分析,适用于批量或有特殊要求的数据分析。孙海涛等[25]提出了一种基于开源软件Mzmine和谱峰预识别算法,多个计算资源并行的云计算代谢组学数据处理方法,所提出的并行数据处理方法与单计算节点相比,计算速度得到显著提升且大大降低了研究费用,可满足海量代谢组学的数据处理需求。
-
CNS疾病影响着全球数百万患者的生命健康,其发病机制复杂,涉及神经细胞凋亡、神经炎症、氧化应激、兴奋性损伤等多种病理特征,给疾病的早期诊断和预后评估带来了很大的困难。构建单一病理状态的体外细胞模型,可以进行大规模的靶向研究和药物筛选,大大缩短了新药研发时间[26]。尽管已有各种类型的CNS疾病体外细胞模型,但其中只有少数被用于代谢组学研究。随着细胞代谢组学在探索CNS疾病发病机制以及药物作用特点中的作用日益突出,越来越多潜在的生物标志物被发现。表1归纳了2015年以来有关细胞代谢组学在CNS疾病研究的一些应用实例,包括常见CNS疾病相应的细胞模型构建、细胞代谢组学分析手段、差异代谢物筛选、通路分析及药物干预结果等。
表 1 细胞代谢组学在中枢神经系统疾病药物研究中的应用
疾病 研究对象 研究药物 检测手段 主要研究结果 参考文献 阿尔茨海默病 PC12细胞
(Aβ25~35)柚皮苷 GC-MS 筛选出甘氨酸、谷氨酸等27种AD差异代谢物,影响氨基酸代谢、碳水化合物代谢及脂质代谢等代谢通路 [27] 脑微血管内皮细胞(Aβ1~42) 丹参 UHPLC-QTOF- MS 发现了33个差异代谢物,涉及精氨酸和脯氨酸代谢、谷胱甘肽代谢等多条代谢通路 [28] SH-SY5Y细胞
(冈田酸)丹参、知母 UHPLC-QTOF- MS 发现了色氨酸、苯丙氨酸等45个潜在AD生物标志物,涉及12条代谢通路,筛选出与丹参相关的30种差异代谢物,与知母相关的7种差异代谢物 [29] SH-SY5Y细胞
(谷氨酸)人参皂苷 Rb1 1H NMR 发现谷氨酸、牛磺酸等7种差异代谢物,涉及5条不同的代谢通路 [30] 帕金森病 SH‐SY5Y细胞
(MPP+)胶质细胞源性神经营养因子 LC‐MS/MS 三酰甘油、磷脂酰胆碱等多种脂质代谢物受到影响 [31] SH-SY5Y细胞
(6-OHDA)花茶 UPLC-TOF-MS 发现多种与神经保护作用相关的代谢物 [32] SH-SY5Y细胞
(A53T基因突变)L-天冬酰胺酶 GC-MS/MS 可以调节谷氨酰胺代谢起到神经保护作用 [33] 抑郁症 PC12细胞
(皮质酮)阿魏酸 UPLC-QTOF-MS 发现24个差异代谢物,涉及氨基酸代谢、能量代谢和甘油磷脂代谢等代谢通路 [34] PC12细胞
(皮质酮)甘草苷 LC-MS 鉴定出谷氨酸、谷胱甘肽等11种潜在差异代谢物,涉及8条不同的代谢通路 [35] PC12细胞
(皮质酮)香附 UPLC-Q-TOF-MS 发现鞘磷脂、甘油磷脂等11种潜在差异代谢物 [36] PC12细胞 氯胺酮、羟基去甲氯胺酮对映体 GC-MS和CE-MS 发现甘油酸盐、柠檬酸盐、亮氨酸等49种潜在生物标志物 [37] 星形胶质细胞 氟西汀 1H NMR 发现17种潜在生物标志物,涉及脂质和氨基酸代谢通路 [38] 星形胶质细胞 文拉法辛 1H NMR 发现赖氨酸、酪氨酸、谷氨酸等31 种涉及能量、氨基酸和脂质代谢的差异代谢物 [39] -
阿尔茨海默病(AD)是一种常见于老年人的神经退行性疾病,临床表现为记忆力减退、认知和交流功能障碍[40]。常用的AD细胞模型有:β淀粉样蛋白(Aβ)诱导神经毒性模型、Tau蛋白异常磷酸化模型、氧化应激模型和基因转染模型[41]。Aβ聚集沉积易使细胞产生突触受损、线粒体功能障碍以及促进Tau蛋白病理化,当前AD防治的研究热点也集中于Aβ[42]。Aβ是由淀粉样前体蛋白(APP)经分泌酶水解产生,APP的异常突变与AD的发展密切相关,Xiong等[43]对APP过表达的转基因(N2a/APP695swe)细胞用作AD体外模型的可行性进行验证,并将其应用于缬氨霉素改善AD的作用机制研究,GC-MS结果显示,缬氨霉素作用N2a/APP695swe细胞3 h后Aβ1~42和Aβ1~40水平降低,此时,三磷酸腺苷(ATP)水平和柠檬酸、苹果酸、丙酮酸等ATP相关代谢产物显著增加。但是6~12 h其ATP代谢产物却呈现水平下降趋势,提示缬氨霉素的作用时间应加以控制,才能有效促进ATP产生,起到改善AD的作用。有研究指出载脂蛋白E(APOE)不同亚型携带者患AD的风险不尽相同,可能与影响大脑葡萄糖摄取有关。为了解构成APOE相关遗传风险的分子机制,Williams等[44]采用稳定同位素示踪技术探究APOE中3种亚型基因产生的星形胶质细胞葡萄糖代谢差异,结果显示,相较于E2和E3,受E4影响的星形胶质细胞葡萄糖摄取受损,相应的糖代谢、三羧酸循环以及戊糖磷酸途径发生变化,谷胱甘肽合成增加,详见图2所示。与人类APOE表达E4基因的小鼠模型的研究结果相印证[45],证实了AD发病与遗传基因的相关性。为深入了解E4和代谢损伤对大脑影响的生物学基础,进一步阐明AD的发病机制提供了科学依据。
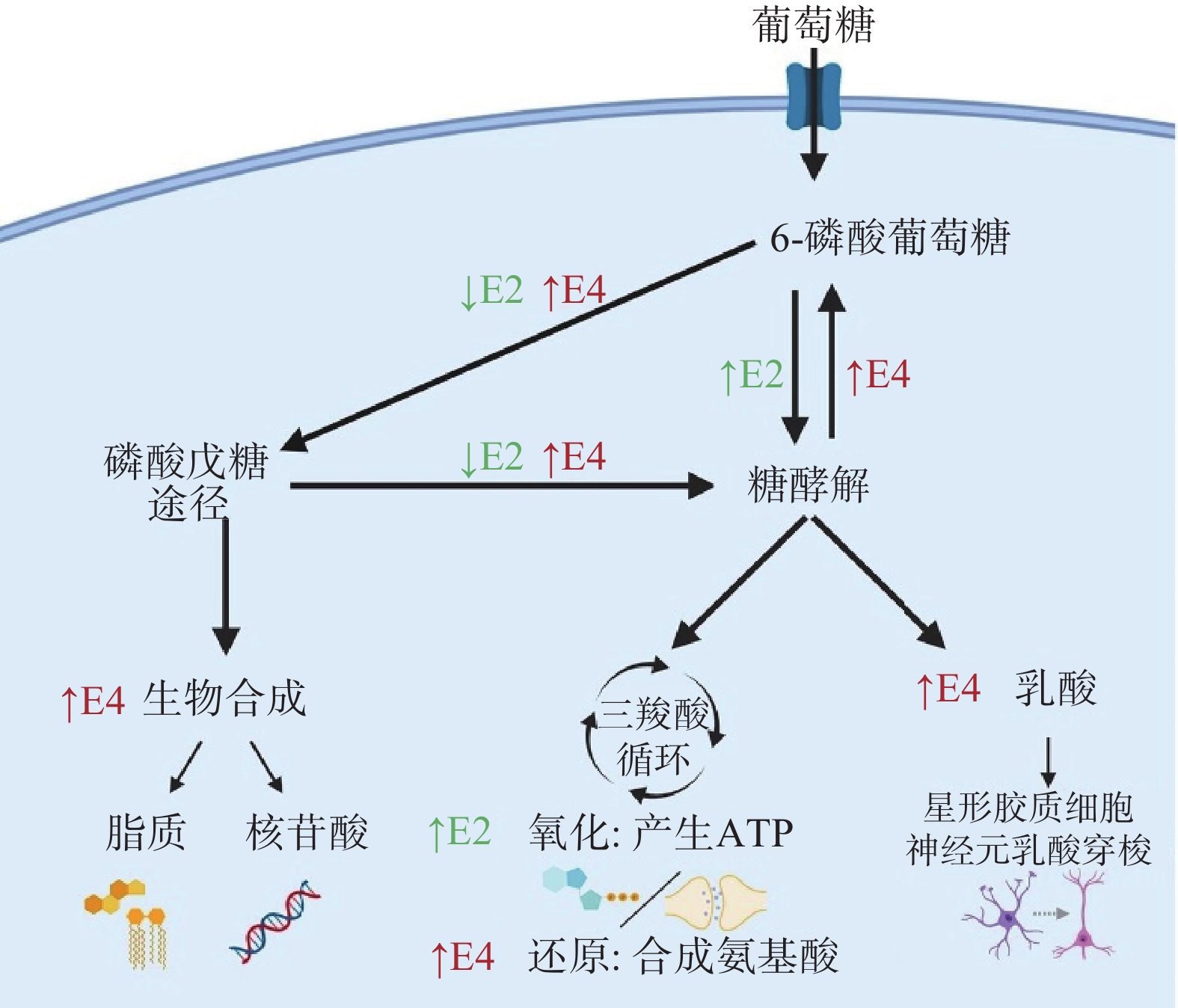
图 2 不同亚型的载脂蛋白E对星形胶质细胞葡萄糖代谢的影响[44]
-
帕金森病(PD)为第二大中枢神经退行性疾病,患者常出现运动迟缓、静止性震颤和强直等症状。PD 是一种由遗传、环境和生活方式等多因素共同作用的疾病,其病理特征表现为黑质多巴胺能神经元损伤丢失和α-突触核蛋白聚集[46]。神经毒素如百草枯、6-羟基多巴胺(6-OHDA)、1-甲基-4-苯基-四氢吡啶离子(MPP+)可诱导细胞多巴胺能神经元变性死亡,从而产生类似帕金森的病理特征,所建立的细胞模型可操作性强、重复性好,是目前最常用的PD细胞造模方法。Lei等[47]采用NMR与直接输注电喷雾电离质谱(DI-ESI-MS)联用的代谢组学方法探究百草枯诱导SH-SY5Y细胞产生的代谢谱变化,结果显示,磷酸戊糖途径中6-磷酸葡萄糖、6-磷酸果糖等代谢物增加,糖酵解与TCA 循环受到抑制。Xicoy等[48]运用LC-MS法研究6-OHDA诱导的SH-SY5Y细胞的脂类代谢变化,结果发现除了磷脂酰丝氨酸水平降低外,磷脂酰胆碱、磷脂酰甘油、磷脂酰肌醇和胆固醇水平变化情况均与PD患者血浆代谢组学结果相同[49]。进一步探究降胆固醇他汀类药物对该PD模型的神经保护作用,发现他汀类药物未展现相应的保护作用,反而是低剂量的胆固醇使SH-SY5Y细胞免受6-OHDA毒性,提示该细胞模型不适用于胆固醇参与的PD发生发展机制的研究。星形胶质细胞是人脑中含量最丰富的细胞类型,在维持PD患者大脑胆固醇稳态扮演着重要角色[50]。近年来,星形胶质细胞在PD发病机制中作用开始被发现。Sonninen等[51]通过UPLC-Q-TOF-MS法探究星形胶质细胞的代谢变化,发现LRRK2和GBA基因突变的PD星形胶质细胞出现α-突触核蛋白生成增加、钙水平升高、溶血磷脂酰乙醇胺等多种氨基酸代谢改变。
-
缺血性脑卒中(IS)是中风的一种常见形式,涉及神经炎症、氧化应激、兴奋性中毒等病理机制,患病后易导致脑损伤或残疾,严重者将危及生命,对人类健康构成极大威胁[52]。IS患者因急性血管闭塞所引起的脑组织缺血、缺氧,易使细胞自由基受损、钙离子超载、能量代谢紊乱,因此保护细胞免受缺氧缺糖的影响,是体外研究IS的思路之一。脑微血管内皮细胞是IS中损伤最严重的细胞,韩晨阳等[53]采用HPLC法发现该细胞在体外缺氧缺糖环境下产生ATP、二磷酸腺苷(ADP)含量降低,磷酸腺苷(AMP)含量增加等异常能量代谢变化,而这些病理变化与IS造成的细胞损伤相似。进一步探究丁苯酞对该模型的作用机制发现,丁苯酚可以有效调节细胞在氧糖剥离条件下产生的能量紊乱、钙离子超载。Wang等[54]运用GC-MS法研究杜仲防治IS的作用,采用缺氧缺糖条件下的脑微血管内皮细胞造模,发现杜仲具有促进苯丙氨酸代谢,抑制线粒体活性氧产生的作用。上述IS体外细胞模型的构建采用的是物理方法,即将细胞置于缺糖或缺血培养基与缺氧环境下培养,对设备要求较高,需将连二亚硫酸钠(Na2S2O4)、氯化钴(CoCl2)等化学性缺氧试剂用于IS模型的构建。王宇翔[55]在PC12细胞的无糖培养基中加入Na2S2O4建立氧糖剥离模型,采用HPLC法探究染料木黄酮对所构建细胞模型的保护作用,通过测定细胞神经递质类氨基酸随时间含量变化情况,发现染料木黄酮可逆转缺氧缺糖所引起的谷氨酸、天冬氨酸等兴奋性氨基酸水平变化,发挥神经保护作用。
-
抑郁症是一种复杂的精神障碍疾病,以持续的心境低落为主要临床特征。谷氨酸循环和糖皮质激素浓度异常与抑郁症的发生发展密切相关,目前体外实验主要使用皮质酮、谷氨酸诱导细胞产生神经损伤构建抑郁症细胞模型。Zhang等[56]采用超高效液相色谱结合四极杆飞行时间质谱法(UPLC-QTOF-MS)探究皮质酮对PC12细胞的细胞毒性机制,鉴定出15种潜在生物标志物,涉及甘油磷脂代谢、鞘脂代谢、脂肪酸氧化、甘油脂代谢和甾醇脂物在内的5种代谢途径,为后续实验研究提供了有力支撑。何小燕等[57]运用1H-NMR法探究谷氨酸和皮质酮诱导下PC12细胞的代谢差异,结果显示两种刺激方式产生的代谢物不同,但影响的代谢通路却无显著差别,提示将差异代谢物与其代谢通路结合分析的重要性。中医药具有多层次、多靶点的整体调控作用,在防治抑郁症方面具有独特优势。但由于相关中医学证候模型的缺乏,在一定程度上制约了中医药防治抑郁症的进一步发展。付爽等[58]使用含10%肝郁脾虚证的血清诱导肝癌HepG2细胞构建抑郁症证候模型,对所建立的抑郁症肝郁脾虚证细胞模型与肝郁脾虚证血清进行代谢组学分析,发现了溶血磷脂酰胆碱、卵磷脂、甘油磷酰胆碱等19个相同的代谢差异物,涉及9条代谢通路,该证候细胞模型的建立为中医药辩证治疗的科学性和有效性提供了依据。
-
细胞代谢组学通过“细胞模型-生物标志物-疾病机制/作用功效”的对应关系,对细胞代谢产物进行分析,从细胞水平认识疾病,为中枢神经系统疾病的防治打开一扇新的大门。但是仍面临着一些挑战:①理想的细胞模型应该与相应疾病有高度的相似性、可重复性和可操作性,但是疾病的发生发展往往与多个细胞相关,因此需要在确保研究结果可靠的基础上选择合适的细胞造模方法。②细胞代谢物丰富但是含量少,虽然使用液氮或低温有机溶剂对细胞进行萃取可以最大程度上减少代谢物的损失,但是不同细胞模型所采用的前处理方法不尽相同,目前尚未有标准化前处理流程可以适用所有细胞代谢物的提取分析。③细胞代谢组学的分析对象是相对分子质量小于1 000的代谢物,需要不断更新、优化高通量和高分辨率的分析仪器,提高代谢物的检测灵敏度,以获取更多的细胞代谢物数据。④细胞代谢组学隶属于体外研究的范畴,与生物体复杂的代谢变化存在着一定的差异,为提高研究结果的准确性和可靠性,未来细胞代谢组学的研究方向需整合多组学和多学科的信息,以期更加全面的了解CNS病理机制,获取疾病相关生物标志物信息,进一步评价药物的药效,从而为CNS疾病的新药研发提供参考依据[59-60]。相信随着更多细胞模型的构建以及分析技术的不断发展,细胞代谢组学在CNS疾病研究中将会有更广阔的应用前景。
Application of cellular metabolomics in central nervous system diseases
-
摘要: 细胞代谢组学是代谢组学的重要分支,通过细胞代谢组学技术可以动态监测细胞反应及药物作用于细胞后的代谢变化,寻找具有潜在价值的生物标志物,阐明疾病的病理生理机制及药物治疗干预效果,近年来已被广泛应用于疾病机制、药效评价、新药研发等领域。综述细胞代谢组学的研究流程及其在中枢神经系统疾病中的应用,以期为深入研究中枢神经系统疾病的发病机制和药物防治提供理论依据。Abstract: Cell metabolomics is an important branch of metabolomics, which could dynamically monitor cell response and metabolic changes after drugs acting on cells, and look for potential biomarkers. Cell metabolomics has been widely used in illustration of disease mechanism, evaluation of drug efficacy and development of new drug through elucidating the pathophysiological mechanism of the disease and the effect of drug treatment intervention. The researches process of cellular metabolomics and its application in central nervous system diseases were reviewed in order to provide theoretical basis for in-depth study of the pathogenesis and prevention and treatment of central nervous system diseases.
-
Key words:
- cellular metabolomics /
- central nervous system diseases /
- cell model /
- biomarkers
-
松科(Pinaceae)植物马尾松(Pinusmassoniana Lamb.)主要产于江苏、安徽、河南、陕西及长江中下游各省区,资源丰富[1]。松叶“味苦,温;暖,无毒”,具有祛风燥湿、杀虫、止痒之功用。水煎、浸酒以外用或内服[2]用于治风湿痿痹、跌打损伤、湿疮、疥癣、慢性气管炎等症以及预防感冒、流脑。文献报道马尾松叶中的主要化学成分为挥发油、黄酮、多糖、木脂素和树脂等,现代药理研究表明马尾松叶提取物具有抗氧化、抗衰老、抑菌等多方面活性[3-15]。
近年来由于抗生素的滥用、器官移植、免疫抑制剂以及HIV患者的增多,深部真菌感染发病率逐年上升,其中白念珠菌是最主要的致病菌。氮唑类药物氟康唑是临床上首选的抗白念珠菌(Candida albicans)感染药物。但是长期和重复给药导致白念珠菌对氟康唑耐药越来越强。目前联合用药是恢复耐药真菌对治疗药物的敏感度,提高耐药菌对氟康唑的敏感性,治疗深部耐药菌感染的一种有效的治疗途径。从天然活性成分中寻找与现有的抗真菌药物联合发挥协同作用的小分子化合物是近年来的研究方向之一[16-20]。本文选用接近“传统水煎或浸酒法”的传统中药提取方法,用乙醇加热提取后,石油醚再萃取的方法得到马尾松叶低极性部位,通过测定马尾松叶低极性部位协同氟康唑抗耐药白念珠菌的MIC80值,同时,采用气相色谱-质谱的方法对低极性部位的化学成分进行分析鉴定,初步探究其联合氟康唑的体外抗真菌活性。
1. 材料
1.1 试剂与设备
Thermo Trace GC Ultra气相色谱、Thermo DSQ Ⅱ质谱、Xcalibur工作站(美国赛默飞世尔公司);马尾松叶(浙江东阳市,经海军军医大学黄宝康教授鉴定为马尾松Pinusmassoniana Lamb.);所有试剂均为分析纯;水为重蒸水;载气为高纯氦气。
氟康唑注射液(上海信谊金朱药业有限公司);黄芩素(上海历鼎生物技术有限公司);二甲基亚砜(DMSO,中国医药集团上海化学试剂公司);白念珠菌103(Candida albicans103,海军军医大学长海医院真菌室提供)。
1.2 马尾松叶低极性部位的制备
取干燥马尾松叶,粉碎,称取二份,每份50.0 g,分别用150 ml石油醚和80%乙醇加热回流提取1h,滤过;滤渣再分别用150 ml石油醚和80%乙醇加热回流提取1 h,滤过。分别合并两次滤液,滤液用旋转蒸发仪减压浓缩,回收溶剂,得石油醚提取物(简称醚提取物)2.5 g和80%乙醇提取物(简称醇提取物)8.0 g。取干燥后的醇提取物5.0 g,加入水100 ml混溶,获得混悬液。混悬液用50 ml石油醚萃取3次,合并浓缩石油醚萃取液,获得石油醚浸膏(简称醚浸膏)即马尾松叶低极性部位0.8 g。取125 mg醚浸膏,置于100 ml量瓶中,加入80%甲醇,超声、加热使其几近完全溶解,放置、冷却;再加入80%甲醇定容,摇匀、放置;吸取1 ml定容后的浸膏液,微孔滤膜过滤后待测。
1.3 色谱-质谱条件
色谱柱TR - 35MS石英毛细管(30 m×0.25 mm,0.25 μm),程序升温,起始温度40 ℃,保持2 min后以10 ℃/min的速度升至300 ℃并保持5 min;汽化温度250 ℃,进样量1 μl;分流比10∶1。载气为高纯氦气,流速1.0 ml/min。离子源:EI源;离子源温度为250 ℃;电子能量:70 eV;扫描范围:50~650 m/z。
2. 方法
2.1 抑菌实验方法
菌株选用临床分离耐药菌株白念珠菌103(氟康唑的MIC80>128.0 μg/ml)。采用美国临床和实验室标准协会(CLSI)提出的RPMI1640 培养基微量稀释法,取无菌96孔板,于每排1号孔加RPMI1640液体培养基100 μl作空白对照;3~12号孔各加新鲜配制的菌液100 μl,菌液浓度范围为(1~5)×103cfu/ml;2号孔分别加菌液160 μl和受试药物溶液40 μl;12号孔不含药物,只加菌液100 μl作阳性生长对照。2~11号孔进行倍比稀释,使各孔的最终药物(醚提取物、醇提取物和醚浸膏)浓度分别为250.0、125.0、62.5、31.25、15.63、7.81、3.91、1.95、0.98和0.49 μg/ml,对照品黄芩素浓度分别为128.0、64.0、32.0、16.0、8.0、4.0、2.0、1.0、0.5和0.25 μg/ml,各孔中DMSO含量均低于1%,氟康唑溶液的终浓度为8.0 μg/ml。96孔板于30℃恒温培养箱培养24 h后取出,读取受试药物与氟康唑(8.0 μg/ml)联用时的MIC80值。微量稀释法测试结果见表1。
表 1 马尾松叶3种提取物与氟康唑联用对体外白念珠菌103活性(MIC80)试验结果化合物 MIC80 联合抑菌浓度
分数指数
(FICI)联合作用 单用(μg/ml) 与氟康唑联用(μg/ml)* 醚提取物 >250.0 >250.0 1.031 无关 醇提取物 >250.0 7.81 0.047 协同 醚浸膏 >250.0 31.25 0.094 协同 黄芩素 16.0 4.0 0.281 协同 氟康唑 >128.0 − − − *与8 μg/ml 氟康唑联合使用 协同药效的判定采用联合抑菌浓度分数指数(FICI),即联用抑菌时每种药物所需最低抑菌浓度(MIC)与单用这种药物抑菌时所需MIC的比值的和。当FICI≤0.5时,两种药物的相互作用效果被定义为具有协同作用;当FICI>0.5时,认为两种药物无相互作用。
2.2 色谱-质谱分析方法
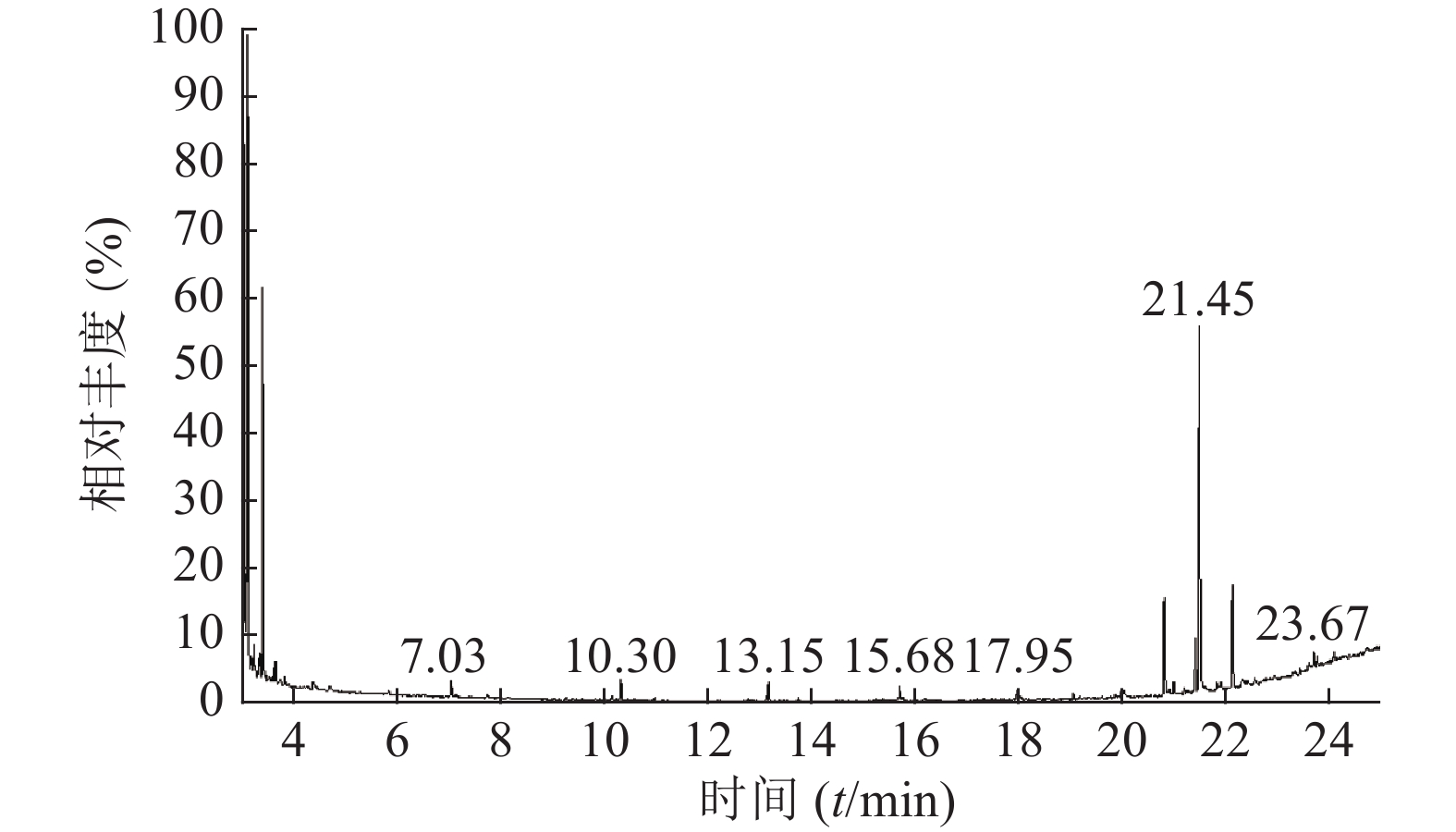
按“1.3”项下实验条件对马尾松叶低极性部位进行分析,25 min得到马尾松叶低极性化学成分的总离子流图(图1)。共检测出30个峰,通过检索NIST08光谱数据库,按60%以上匹配率(SI和RSI均大于600,最大值1 000),并结合质谱裂解规律确定其化学成分。运用峰面积归一法通过Xcalibur化学工作站数据处理系统,测得各个化学成分在石油醚部位中的质量百分数。
3. 结果与分析
由表1可见,各受试药物单用时,对照品黄芩素的MIC80为16.0 μg/ml,提示了其具有一定的抗菌活性,其他的化合物的MIC80均大于250 μg/ml。各受试药物与氟康唑(8.0 μg/ml)联用后,对照品黄芩素、醇提取物及醚浸膏的MIC80降至4.0~31.25 μg/ml,相应的FICI值均小于0.5,显示黄芩素、醇提取物、醚浸膏分别与氟康唑联用对耐药白念珠菌均具有协同活性,但醇提取物和醚浸膏的协同活性不及对照品黄芩素,醚浸膏协同活性小于醇提取物。醚提取物单用及与氟康唑联用的MIC80均大于250 μg/ml,FICI大于0.5,显示其单用及与氟康唑联用均没有协同氟康唑抗耐药白念珠菌活性。
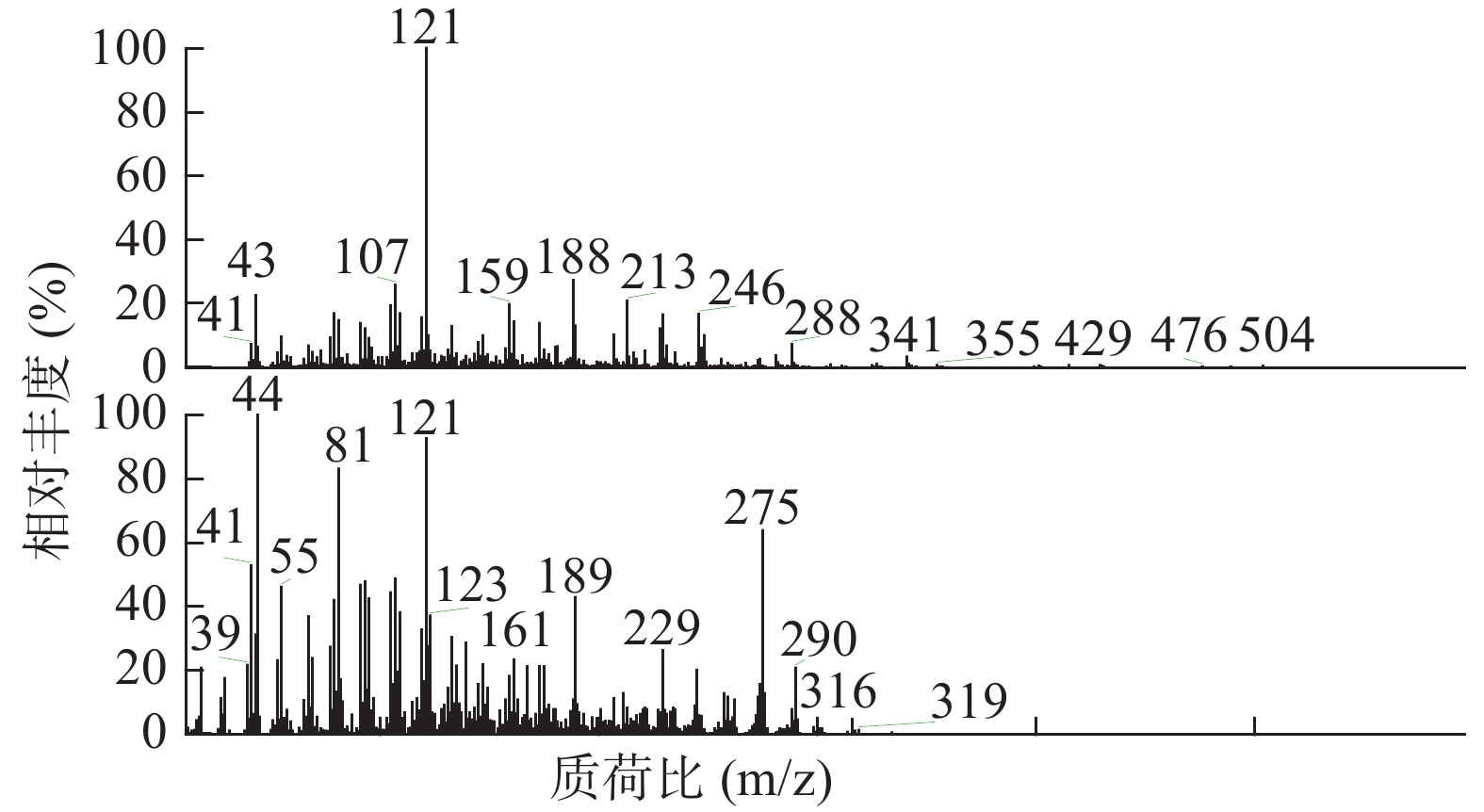
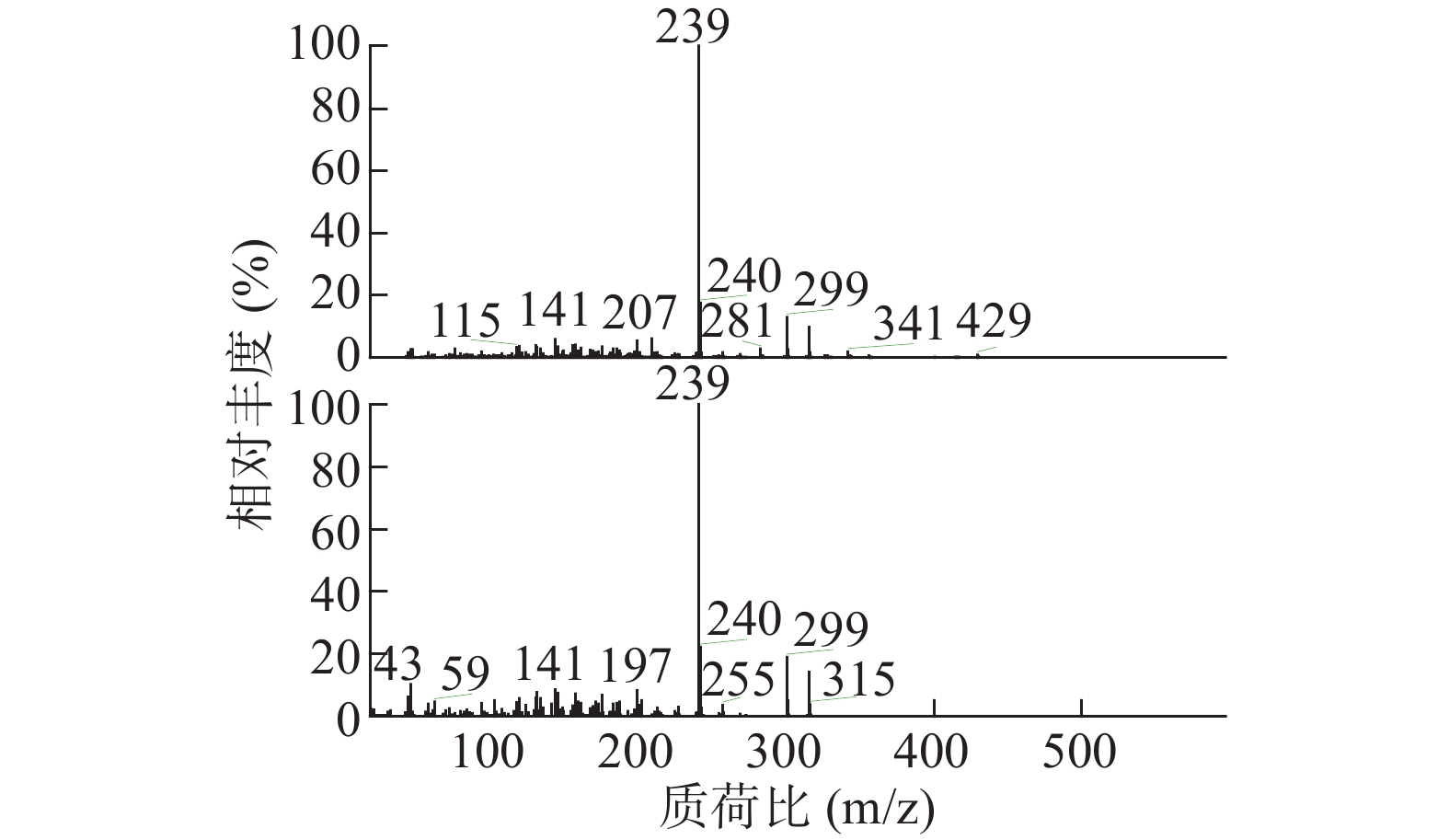
如表2所示,本次GC-MS检测出30种成分,鉴定出17个化合物。统计出本次所测马尾松叶的低极性化学成分中含有烷烃4个(6.1%),甾烷类5个(4%),脂肪酸1个(0.75%),二萜5个(53.99%),其他峰均提示为聚硅氧烷(35.16%),其中含量较高的化学成分是:玛瑙酸(8.38%,见图2)、脱氢枞酸甲酯(8.41%,见图3)。
表 2 马尾松叶低极性化学成分分析结果序号 保留时间(min) 相似度SI值 相似度RSI值 化合物 含量(%) 1 10.30 821 850 正十五烷 1.52 2 13.15 797 840 2,6,11,15-四甲基-十六烷 2.23 3 15.68 781 822 2,6,10-三甲基-十四烷 1.37 4 17.95 709 727 3-乙基-5-(2-乙基丁基)-十八烷 0.98 5 19.03 661 770 泪柏醚 0.68 6 19.96 641 684 1-单烯丙基甘油三甲基硅醚 0.75 7 20.00 639 670 3,3-亚乙基二氧基-5β-胆甾烷 1.00 8 20.78 688 700 玛瑙酸/贝壳杉萘甲酸 8.38 9 20.88 621 690 N-[24-氧代-3α-(三甲基硅氧基)-5β-胆安-24-基]甘氨酸甲酯 0.51 10 20.96 636 739 24, 25-二羟基维生素D3 / 24R, 25-二羟胆钙化醇 1.11 11 21.16 609 633 17-乙酰氧基-4,4,10,13-四甲基-7-氧代-2,3,4,7,8,9,10,11,12,13,14,15,16,17-十四氢-1H-环戊烷(a)菲-3-基,乙酸 0.61 12 21.38 777 915 隐青霉酸甲酯 / 山莨菪碱酸甲酯 /海松酸甲酯 4.62 13 21.45 626 636 3-羟基-2,5,5,8a-四甲基-1,4,4a,5,6,7,8,8a-八氢萘-1-羧酸,2-三甲基硅乙基酯 31.90 14 21.79 645 662 3,11,18-三乙酰氧基-3,19:14,15-二环氧孕烷-20-酮 0.77 15 21.87 625 765 1,1,3,3,5,5,7,7,9,9,11,11,13,13,15,15-十六甲基八硅氧烷 1.50 16 22.09 841 889 脱氢枞酸甲酯 8.41 17 22.29 676 788 1,1,3,3,5,5,7,7,9,9,11,11,13,13-十四甲基七硅氧烷 1.30 4. 讨论
近年来研究发现马尾松叶提取物具有抗真菌活性:马尾松叶石油醚、氯仿等溶剂的提取物以及不同比例的乙醇水提取物可以抑制曲霉、青霉、啤酒酵母的生长;马尾松叶乙醇提取物对枯萎病、灰霉菌有显著的抑菌活性;马尾松叶水提物对白色念珠菌有较弱抑菌性[21-25]。但马尾松叶提取物对氟康唑耐药白念珠菌的协同抗菌活性未见报道。
本研究发现,马尾松叶的醇提取物和醚浸膏单独使用时均不及黄芩素,没有抗耐药白念珠菌活性,但联用氟康唑(8 μg/ml)后,醇提取物和醚浸膏均表现出协同活性,醇提取物的活性更好,而醚提取物无论是单独使用还是联用氟康唑都没有抗耐药白念珠菌活性。醚浸膏与醚提取物相比,提取方法的改变,导致了提取物抑菌效果的有无。醚浸膏的活性应该源于乙醇加热提取获得的更丰富、含量更高的化学成分,尽管醚浸膏的主要成分也是低极性成分,但与醚提取物相比无论在含量和组成上均应不同。醚提取物含有更丰富的挥发油等低极性成分,但是可能缺少了一些重要的活性抗真菌成分,导致其没有协同抗耐药真菌作用。我们进一步对活性部位醚浸膏进行了GC-MS化学成分分析,结果表明,其化学成分与文献报道的采用水蒸气和超临界CO2提取法获得的马尾松叶挥发油成分相比差异大。活性部位醚浸膏中化合物结构类型和数量比文献报道的直接提取的挥发油少,且没有以蒎烯、莰烯为主的单萜和以石竹烯等为主的倍半萜,仅有烷烃类少量化合物重合[26-31]。活性部位醚浸膏采用了乙醇加热提取后,再经石油醚萃取得到,加热提取可能导致了蒎烯、莰烯、石竹烯等低沸点萜类化合物的丢失,但分子量更大的二萜类化学成分含量升高(53.99%)。二萜类化学成分中脱氢枞酸甲酯、海松酸甲酯是主要化学成分,两者也是松香酸的主要成分。有文献报道松香酸具有抗赤霉菌、灰霉菌等多种抗真菌活性[32-35]。因此,醚浸膏中的二萜类化合物可能是其协同氟康唑抗耐药白念珠菌作用的重要活性成分,值得进一步研究。此外,Zuzana研究发现云杉提取物中的β-谷甾醇抑制微生物生长,同时低浓度的脱氢枞酸甲酯破坏细胞壁,两者相互协同可能是云杉提取物对青霉菌、链格孢菌、米根霉的抑菌活性的关键[36]。本研究获得的醚浸膏中也含有丰富的树脂酸(13.03%)和甾烷(4%)。树脂酸和甾烷的协同可能也是醚浸膏具有协同氟康唑抗耐药白念珠菌活性的原因,这一点也值得进一步研究。
综上所述,本文首次报道了马尾松叶乙醇提取物以及马尾松叶低极性部位具有协同氟康唑抗耐药白念珠菌作用,并首次对马尾松叶低极性部位进行了GC-MS分析,鉴别的化合物除了烷烃、脂肪酸、脱氢枞酸甲酯外其它11种成分都是首次从该植物中发现,丰富了马尾松叶的化学成分。
-
图 1 细胞代谢组学工作流程[6]
图 2 不同亚型的载脂蛋白E对星形胶质细胞葡萄糖代谢的影响[44]
表 1 细胞代谢组学在中枢神经系统疾病药物研究中的应用
疾病 研究对象 研究药物 检测手段 主要研究结果 参考文献 阿尔茨海默病 PC12细胞
(Aβ25~35)柚皮苷 GC-MS 筛选出甘氨酸、谷氨酸等27种AD差异代谢物,影响氨基酸代谢、碳水化合物代谢及脂质代谢等代谢通路 [27] 脑微血管内皮细胞(Aβ1~42) 丹参 UHPLC-QTOF- MS 发现了33个差异代谢物,涉及精氨酸和脯氨酸代谢、谷胱甘肽代谢等多条代谢通路 [28] SH-SY5Y细胞
(冈田酸)丹参、知母 UHPLC-QTOF- MS 发现了色氨酸、苯丙氨酸等45个潜在AD生物标志物,涉及12条代谢通路,筛选出与丹参相关的30种差异代谢物,与知母相关的7种差异代谢物 [29] SH-SY5Y细胞
(谷氨酸)人参皂苷 Rb1 1H NMR 发现谷氨酸、牛磺酸等7种差异代谢物,涉及5条不同的代谢通路 [30] 帕金森病 SH‐SY5Y细胞
(MPP+)胶质细胞源性神经营养因子 LC‐MS/MS 三酰甘油、磷脂酰胆碱等多种脂质代谢物受到影响 [31] SH-SY5Y细胞
(6-OHDA)花茶 UPLC-TOF-MS 发现多种与神经保护作用相关的代谢物 [32] SH-SY5Y细胞
(A53T基因突变)L-天冬酰胺酶 GC-MS/MS 可以调节谷氨酰胺代谢起到神经保护作用 [33] 抑郁症 PC12细胞
(皮质酮)阿魏酸 UPLC-QTOF-MS 发现24个差异代谢物,涉及氨基酸代谢、能量代谢和甘油磷脂代谢等代谢通路 [34] PC12细胞
(皮质酮)甘草苷 LC-MS 鉴定出谷氨酸、谷胱甘肽等11种潜在差异代谢物,涉及8条不同的代谢通路 [35] PC12细胞
(皮质酮)香附 UPLC-Q-TOF-MS 发现鞘磷脂、甘油磷脂等11种潜在差异代谢物 [36] PC12细胞 氯胺酮、羟基去甲氯胺酮对映体 GC-MS和CE-MS 发现甘油酸盐、柠檬酸盐、亮氨酸等49种潜在生物标志物 [37] 星形胶质细胞 氟西汀 1H NMR 发现17种潜在生物标志物,涉及脂质和氨基酸代谢通路 [38] 星形胶质细胞 文拉法辛 1H NMR 发现赖氨酸、酪氨酸、谷氨酸等31 种涉及能量、氨基酸和脂质代谢的差异代谢物 [39] -
[1] GRIBKOFF V K, KACZMAREK L K. The need for new approaches in CNS drug discovery: why drugs have failed, and what can be done to improve outcomes[J]. Neuropharmacology,2017,120:11-19. doi: 10.1016/j.neuropharm.2016.03.021 [2] MARTINELLI C, PUCCI C, BATTAGLINI M, et al. Antioxidants and nanotechnology: promises and limits of potentially disruptive approaches in the treatment of central nervous system diseases[J]. Adv Healthc Mater,2020,9(3):e1901589. doi: 10.1002/adhm.201901589 [3] NICHOLSON J K, LINDON J C, HOLMES E. 'Metabonomics': understanding the metabolic responses of living systems to pathophysiological stimuli via multivariate statistical analysis of biological NMR spectroscopic data[J]. Xenobiotica,1999,29(11):1181-1189. doi: 10.1080/004982599238047 [4] CUPERLOVIC-CULF M, BADHWAR A. Recent advances from metabolomics and lipidomics application in Alzheimer's disease inspiring drug discovery[J]. Expert Opin Drug Discov,2020,15(3):319-331. doi: 10.1080/17460441.2020.1674808 [5] BALCERCZYK A, DAMBLON C, ELENA-HERRMANN B, et al. Metabolomic approaches to study chemical exposure-related metabolism alterations in mammalian cell cultures[J]. Int J Mol Sci,2020,21(18):6843. doi: 10.3390/ijms21186843 [6] DOMENICK T M, GILL E L, VEDAM-MAI V, et al. Mass spectrometry-based cellular metabolomics: current approaches, applications, and future directions[J]. Anal Chem,2021,93(1):546-566. doi: 10.1021/acs.analchem.0c04363 [7] ABDEEN A A, LEE J M, KILIAN K A. Capturing extracellular matrix properties in vitro: Microengineering materials to decipher cell and tissue level processes[J]. Exp Biol Med (Maywood),2016,241(9):930-938. doi: 10.1177/1535370216644532 [8] VAN GORSEL M, ELIA I, FENDT S M. 13 C tracer analysis and metabolomics in 3D cultured cancer cells[J]. Methods Mol Biol,2019,1862:53-66. [9] CHEN Z Y, JIANG N, GUO S, et al. Effect of simulated microgravity on metabolism of HGC-27 gastric cancer cells[J]. Oncol Lett,2020,19(5):3439-3450. [10] 杨盛, 何然, 张飞燕, 等. 细胞共培养模型及其在中枢神经系统疾病研究中的应用[J]. 药学学报, 2016, 51(3):338-346. doi: 10.16438/j.0513-4870.2015-0583 [11] MATHON C, BOVARD D, DUTERTRE Q, et al. Impact of sample preparation upon intracellular metabolite measurements in 3D cell culture systems[J]. Metabolomics,2019,15(6):92. doi: 10.1007/s11306-019-1551-0 [12] WILKINS J, SAKRIKAR D, PETTERSON X M, et al. A comprehensive protocol for multiplatform metabolomics analysis in patient-derived skin fibroblasts[J]. Metabolomics,2019,15(6):83. doi: 10.1007/s11306-019-1544-z [13] SER Z, LIU X J, TANG N N, et al. Extraction parameters for metabolomics from cultured cells[J]. Anal Biochem,2015,475:22-28. doi: 10.1016/j.ab.2015.01.003 [14] BODZON-KULAKOWSKA A, CICHON T, GOLEC A, et al. DESI-MS as a tool for direct lipid analysis in cultured cells[J]. Cytotechnology,2015,67(6):1085-1091. doi: 10.1007/s10616-014-9734-z [15] SABORANO R, ERASLAN Z, ROBERTS J, et al. A framework for tracer-based metabolism in mammalian cells by NMR[J]. Sci Rep,2019,9(1):2520. doi: 10.1038/s41598-018-37525-3 [16] ARAÚJO A M, MOREIRA N, LIMA A R, et al. Analysis of extracellular metabolome by HS-SPME/GC-MS: Optimization and application in a pilot study to evaluate galactosamine-induced hepatotoxicity[J]. Toxicol Lett,2018,295:22-31. doi: 10.1016/j.toxlet.2018.05.028 [17] STOLL D R, HARMES D C, STAPLES G O, et al. Development of comprehensive online two-dimensional liquid chromatography/mass spectrometry using hydrophilic interaction and reversed-phase separations for rapid and deep profiling of therapeutic antibodies[J]. Anal Chem,2018,90(9):5923-5929. doi: 10.1021/acs.analchem.8b00776 [18] SUN Z Y, JI Q Q, EVANS A R, et al. High-throughput LC-MS quantitation of cell culture metabolites[J]. Biologicals,2019,61:44-51. doi: 10.1016/j.biologicals.2019.07.003 [19] PÖHÖ P, LIPPONEN K, BESPALOV M M, et al. Comparison of liquid chromatography-mass spectrometry and direct infusion microchip electrospray ionization mass spectrometry in global metabolomics of cell samples[J]. Eur J Pharm Sci,2019,138:104991. doi: 10.1016/j.ejps.2019.104991 [20] XU S, LIU M, BAI Y, et al. Multi-Dimensional Organic Mass Cytometry: Simultaneous Analysis of Proteins and Metabolites on Single Cells. Angew Chem Int Ed Engl. 2021, 60(4): 1806-1812. [21] LIU R M, YANG Z B. Single cell metabolomics using mass spectrometry: techniques and data analysis[J]. Anal Chim Acta,2021,1143:124-134. doi: 10.1016/j.aca.2020.11.020 [22] SHULAEV V. Metabolomics technology and bioinformatics[J]. Brief Bioinform,2006,7(2):128-139. doi: 10.1093/bib/bbl012 [23] MISRA B B. New software tools, databases, and resources in metabolomics: updates from 2020[J]. Metabolomics,2021,17(5):49. doi: 10.1007/s11306-021-01796-1 [24] ZHOU D, ZHU W J, SUN T, et al. iMAP: a web server for metabolomics data integrative analysis[J]. Front Chem,2021,9:659656. doi: 10.3389/fchem.2021.659656 [25] 孙海涛, 杨志强, 李葆红, 等. 基于LC/MS的代谢组学数据并行处理研究[J]. 质谱学报, 2015, 36(6):535-542. doi: 10.7538/zpxb.2015.36.06.0535 [26] 陈衬心, 张建永, 蒲家志. 细胞代谢组学及其在中药研究中的应用[J]. 遵义医学院学报, 2017, 40(5):583-586. doi: 10.3969/j.issn.1000-2715.2017.05.024 [27] 张悦, 徐占玲, 孙慧峰, 等. 柚皮苷对Aβ25-35诱导PC12细胞保护作用的代谢组学研究[J]. 中成药, 2021, 43(6):1641-1644. [28] ZHANG M Y, LIU Y, LIU M, et al. UHPLC-QTOF/MS-based metabolomics investigation for the protective mechanism of Danshen in Alzheimer's disease cell model induced by Aβ_1–42[J]. Metabolomics,2019,15(2):1-13. [29] 王辉, 蔡颖, 刘敏, 等. 基于UHPLC-QTOF/MS的细胞代谢组学对丹参和知母防治阿尔茨海默病的药效比较研究[J]. 药学学报, 2021, 56(9):2394-2402. [30] 杨银平, 律广富, 张乔, 等. 基于细胞代谢组学技术的人参皂苷Rb1对SH-SY5Y细胞保护机制研究[J]. 分析化学, 2019, 47(1):49-58. [31] MU P P, LIU Y T, JIANG S M, et al. Glial cell line-derived neurotrophic factor alters lipid composition and protein distribution in MPP+-injured differentiated SH-SY5Y cells[J]. J Cell Physiol,2020,235(12):9347-9360. doi: 10.1002/jcp.29738 [32] KATCHBORIAN-NETO A, SANTOS W T, NICÁCIO K J, et al. Neuroprotective potential of Ayahuasca and untargeted metabolomics analyses: applicability to Parkinson’s disease[J]. J Ethnopharmacol,2020,255:112743. doi: 10.1016/j.jep.2020.112743 [33] ZHANG Q X, GAO Y Y, ZHANG J H, et al. L-asparaginase exerts neuroprotective effects in an SH-SY5Y-A53T model of Parkinson's disease by regulating glutamine metabolism[J]. Front Mol Neurosci,2020,13:563054. doi: 10.3389/fnmol.2020.563054 [34] YIN C L, LU R G, ZHU J F, et al. The study of neuroprotective effect of ferulic acid based on cell metabolomics[J]. Eur J Pharmacol,2019,864:172694. doi: 10.1016/j.ejphar.2019.172694 [35] LI X, QIN X M, TIAN J S, et al. Liquiritin protects PC12 cells from corticosterone-induced neurotoxicity via regulation of metabolic disorders, attenuation ERK1/2-NF-κB pathway, activation Nrf2-Keap1 pathway, and inhibition mitochondrial apoptosis pathway[J]. Food Chem Toxicol,2020,146:111801. doi: 10.1016/j.fct.2020.111801 [36] JIA H M, LIU Y, YU M, et al. Neuroprotective effect of cyperi rhizome against corticosterone-induced PC12 cell injury via suppression of Ca2+ overloading[J]. Metabolites,2019,9(11):244. doi: 10.3390/metabo9110244 [37] FACCIO A T, RUPEREZ F J, SINGH N S, et al. Stereochemical and structural effects of (2R, 6R)-hydroxynorketamine on the mitochondrial metabolome in PC-12 cells[J]. Biochim Biophys Acta BBA Gen Subj,2018,1862(6):1505-1515. doi: 10.1016/j.bbagen.2018.03.008 [38] BAI S J, ZHOU C J, CHENG P F, et al. 1H NMR-based metabolic profiling reveals the effects of fluoxetine on lipid and amino acid metabolism in astrocytes[J]. Int J Mol Sci,2015,16(4):8490-8504. [39] SUN L, FANG L, LIAN B, et al. Biochemical effects of venlafaxine on astrocytes as revealed by 1 H NMR-based metabolic profiling[J]. Mol Biosyst,2017,13(2):338-349. doi: 10.1039/C6MB00651E [40] PARASKEVAIDI M, ALLSOP D, KARIM S, et al. Diagnostic biomarkers for Alzheimer's disease using non-invasive specimens[J]. J Clin Med,2020,9(6):1673. doi: 10.3390/jcm9061673 [41] 邓婷, 余志杰, 徐颖, 等. AD细胞模型的建立及评价方法研究进展[J]. 中国药理学通报, 2020, 36(4):470-475. [42] PANZA F, LOZUPONE M, LOGROSCINO G, et al. A critical appraisal of amyloid-β-targeting therapies for Alzheimer disease[J]. Nat Rev Neurol,2019,15(2):73-88. doi: 10.1038/s41582-018-0116-6 [43] XIONG X M, LI S J, HAN T L, et al. Study of mitophagy and ATP-related metabolomics based on β-amyloid levels in Alzheimer's disease[J]. Exp Cell Res,2020,396(1):112266. doi: 10.1016/j.yexcr.2020.112266 [44] WILLIAMS H C, FARMER B C, PIRON M A, et al. APOE alters glucose flux through central carbon pathways in astrocytes[J]. Neurobiol Dis,2020,136:104742. doi: 10.1016/j.nbd.2020.104742 [45] JOHNSON L A, TORRES E R, WEBER BOUTROS S, et al. Apolipoprotein E4 mediates insulin resistance-associated cerebrovascular dysfunction and the post-prandial response[J]. J Cereb Blood Flow Metab,2019,39(5):770-781. doi: 10.1177/0271678X17746186 [46] SOMMER A, WINNER B, PROTS I. The Trojan horse - neuroinflammatory impact of T cells in neurodegenerative diseases[J]. Mol Neurodegener,2017,12(1):78. doi: 10.1186/s13024-017-0222-8 [47] LEI S L, ZAVALA-FLORES L, GARCIA-GARCIA A, et al. Alterations in energy/redox metabolism induced by mitochondrial and environmental toxins: a specific role for glucose-6-phosphate-dehydrogenase and the pentose phosphate pathway in paraquat toxicity[J]. ACS Chem Biol,2014,9(9):2032-2048. doi: 10.1021/cb400894a [48] XICOY H, BROUWERS J F, KALNYTSKA O, et al. Lipid analysis of the 6-hydroxydopamine-treated SH-SY5Y cell model for Parkinson's disease[J]. Mol Neurobiol,2020,57(2):848-859. doi: 10.1007/s12035-019-01733-3 [49] CHAN R B, PEROTTE A J, ZHOU B W, et al. Elevated GM3 plasma concentration in idiopathic Parkinson’s disease: a lipidomic analysis[J]. PLoS One,2017,12(2):e0172348. doi: 10.1371/journal.pone.0172348 [50] WANG C J, YANG T T, LIANG M Y, et al. Astrocyte dysfunction in Parkinson's disease: from the perspectives of transmitted α-synuclein and genetic modulation[J]. Transl Neurodegener,2021,10(1):39. doi: 10.1186/s40035-021-00265-y [51] SONNINEN T M, HÄMÄLÄINEN R H, KOSKUVI M, et al. Metabolic alterations in Parkinson's disease astrocytes[J]. Sci Rep,2020,10(1):14474. doi: 10.1038/s41598-020-71329-8 [52] VIRANI S S, ALONSO A, APARICIO H J, et al. Heart disease and stroke statistics—2021 update[J]. Circulation,2021,143(8):e254-e743. [53] 韩晨阳, 张晓玲, 官俏兵, 等. 丁苯酞对于糖氧剥夺条件下人脑微血管内皮细胞能量代谢的影响及保护作用[J]. 中国临床药理学与治疗学, 2018, 23(12):1329-1334. [54] WANG Y J, GUAN X, GAO C L, et al. Medioresinol as a novel PGC-1α activator prevents pyroptosis of endothelial cells in ischemic stroke through PPARα-GOT1 axis[J]. Pharmacol Res,2021,169:105640. doi: 10.1016/j.phrs.2021.105640 [55] 王宇翔. 染料木黄酮对缺血缺氧PC12细胞生存状态及相关生理生化指标的影响[D]. 天津: 南开大学, 2015. [56] ZHANG H Y, ZHENG H, ZHAO G, et al. Metabolomic study of corticosterone-induced cytotoxicity in PC12 cells by ultra performance liquid chromatography-quadrupole/time-of-flight mass spectrometry[J]. Mol Biosyst,2016,12(3):902-913. doi: 10.1039/C5MB00642B [57] 何小燕, 陈建丽, 向欢, 等. 谷氨酸和皮质酮诱导的PC12抑郁症细胞模型差异性的~1H NMR代谢组学研究[J]. 药学学报, 2017, 52(2):245-252. [58] 付爽, 谢紫烨, 俞婵娟, 等. 血清诱导的肝郁脾虚证细胞模型的建立方法研究[J]. 中国中药杂志, 2018, 43(14):2999-3005. doi: 10.19540/j.cnki.cjcmm.20180327.008 [59] GONZÁLEZ-RIANO C, DUDZIK D, GARCIA A, et al. Recent developments along the analytical process for metabolomics workflows[J]. Anal Chem,2020,92(1):203-226. doi: 10.1021/acs.analchem.9b04553 [60] 徐佳, 刘其南, 翟园园, 等. 细胞代谢组学样品前处理研究进展[J]. 中国细胞生物学学报, 2018, 40(3):418-425. 期刊类型引用(2)
1. 杨逸鑫,彭芳. 基于代谢组学的中医药防治肝纤维化的研究进展. 中南药学. 2023(01): 155-160 .  百度学术
百度学术2. 李佩岐,康杰,王珂瑶,王慧敏,韩宇峰,王婷慧,崔亮,张剑,邓瑞强,段智变. 复方中药水提物对腹水综合征肉鸡肝脏TGF-β1/Smad通路的影响. 中国畜牧兽医. 2022(05): 1860-1869 .  百度学术
百度学术其他类型引用(3)
-





 下载:
下载:
 下载:
下载:


