-
20世纪60年代末期,美国科学家Barnett Rosenberg在研究电场对细菌生长影响的实验中,首次观察到铂化合物能抑制细胞生长的现象,从而揭开了铂类抗肿瘤药物发展的序幕。经过40多年的临床验证,顺铂、卡铂等铂类化合物在恶性肿瘤化疗中的作用得到充分确认。顺铂被发现具有抗癌活性,但其肾、胃肠道等毒性较为严重。在顺铂的结构基础上加以改造,第二代铂类抗肿瘤药物卡铂问世。卡铂降低了顺铂的毒性、但仍有较重的毒副作用,而且和顺铂交叉耐药,限制了其临床应用[1]。
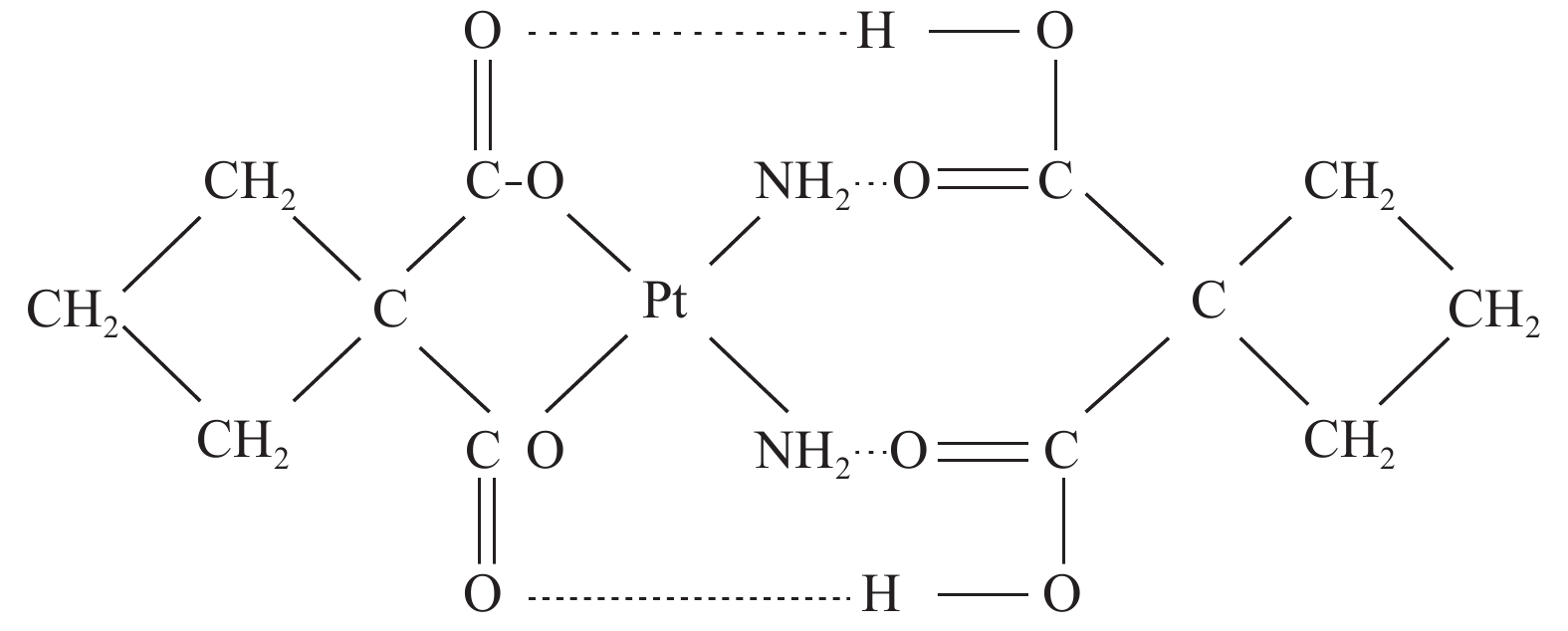
双环铂是我国自主研发的铂类化合物,是继顺铂、卡铂之后的新型铂类抗癌药物。双环铂化学名为顺-(1,1-环丁二羧酸)二氨合铂(Ⅱ),其分子结构(见图1[2])中除含环丁二羧酸基团外,同时以强氢键结合另外一个环丁二羧酸而形成铂络合物。
双环铂作为超分子笼状化合物,可在人体内导向性地与异常DNA的碱基络合,靶向准确杀死癌细胞,发挥抗癌治疗作用。体外细胞和动物实验发现双环铂对多种癌症细胞均有抑制激增的作用,对肝癌、胃癌、前列腺癌、卵巢癌、肺癌等具有较强的抗肿瘤活性,且毒副作用较同类铂络合物低[3-5]。鉴于该药临床应用时间短,相关参考文献较少,本文对我院收治使用双环铂治疗恶性肿瘤患者的疗效及副反应等进行了回顾性总结,为临床用药提供参考。
-
收集2017年1月至2018年8月我院收治使用双环铂治疗的肿瘤患者,41例患者中满足入组条件共20例。其中男性16例,女性4例,年龄18~85岁,中位年龄57.85岁。其中肺癌8例,食管癌1例,胰腺癌2例,膀胱癌1例,胸腺瘤1例,鼻咽癌1例,胃癌1例,淋巴瘤1例,前列腺癌1例,子宫内膜癌1例,脑肿瘤2例。入选标准:①入组患者经病理学或细胞学检查确诊,已经手术或不具备手术条件的肿瘤患者;②化疗前血常规、肝肾功能、心电图等基本正常,符合化疗标准;③KPS评分≥70分,预计生存期≥3个月;④至少以双环铂注射液为基础连续完成2个周期化疗,有明确客观评价指标,可评价近期疗效,筛选详情见图2,患者一般临床特征统计见表1。
表 1 20例患者一般临床特征统计
项目 数量[n(%)] 项目 数量[n(%)] 年龄(岁) 57.85(18−85) 转移部位 <50 5(25) 内脏 9(45) ≥50−60 5(25) 肝脏 1(5) >60 10(50) 仅淋巴结节 4(20) 性别 多发脏器转移 6(30) 女 4(20) 骨转移 1(5) 男 16(80) 双环铂治疗周期 初/复诊 2期 2(10) 初诊 3(15) 3期-4期 11(55) 复诊 17(85) >5期 7(35) KPS评分 其他同期用药 ≤70 6(30) 化疗药 8(40) 70-80 0 PD-1 11(55) 90 14(70) 无 5(25) -
入组患者化疗2~4个周期后根据CT、超声检查确定可测量病灶的变化,按照WHO实体瘤的近期疗效RECIST1.0标准评定疗效。完全缓解(CR):所有目标病灶消失;部分缓解(PR):基线病灶长径总和缩小≥30%;稳定(SD):基线病灶长径总和缩小但未达PR;进展(PD):基线病灶长径总和≥20%或出现新病灶。疾病缓解率(RR)=CR+PR,疾病控制率(DCR)=CR+PR+SD,毒副反应按WHO抗癌药物制定的毒性评定标准分为0~Ⅳ度[6]。根据卡氏评分(Karnofsky performance status,KPS)对患者治疗前和化疗2周期后的生活质量进行评估,总分为0~100分,得分越高表示生活质量越好。KPS评分较治疗前增加≥10分为改善,减少≥10分为下降,增加或减少在10分以内为稳定。t检验用于检验用药前后疗效分析结果,当P<0.05时,表明用药效果显著。
-
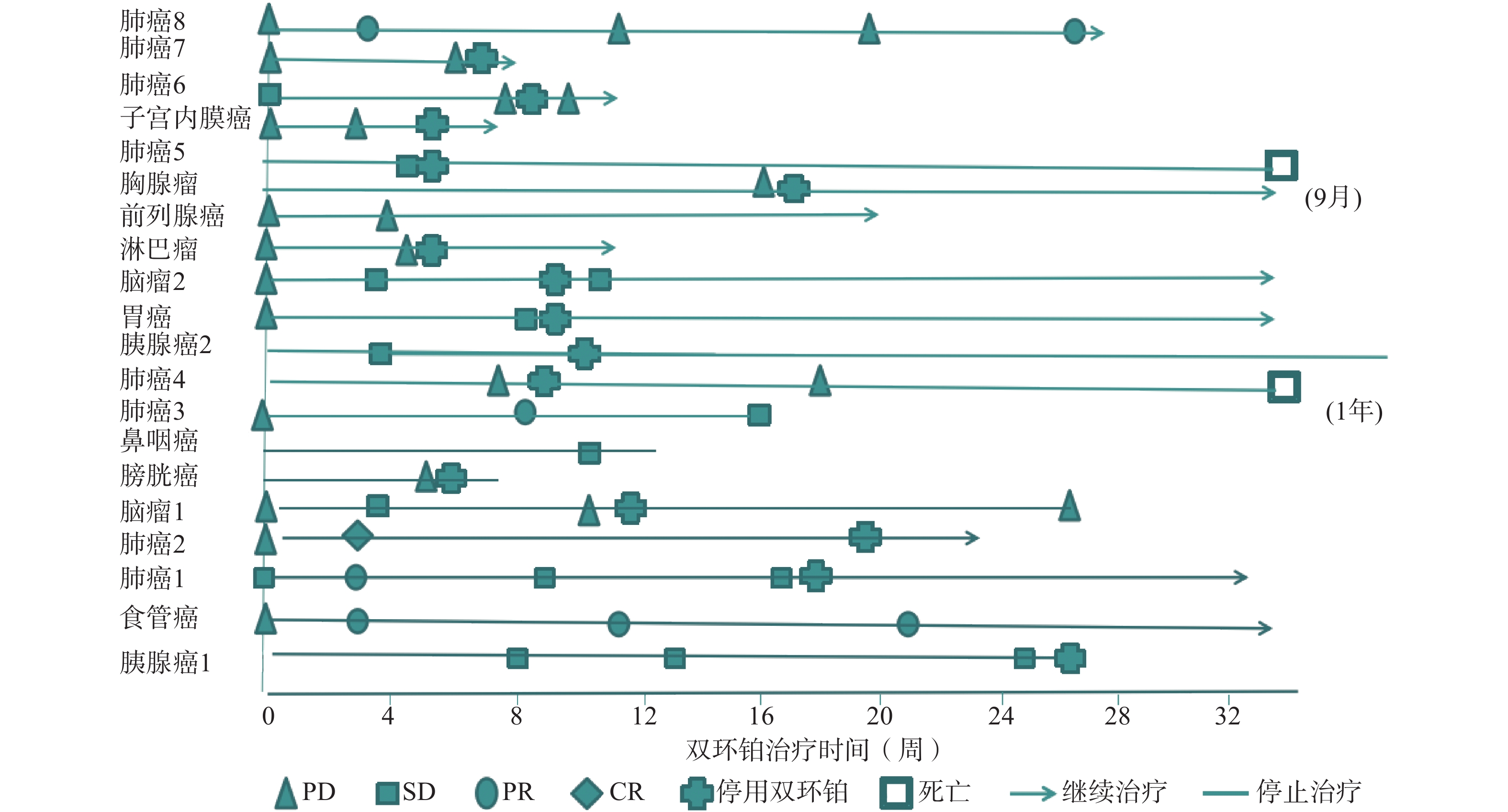
全组患者均可评价近期疗效,20例患者中有11例患者在处于疾病进展(PD)期开始使用双环铂单药或联合用药治疗。入组患者中近期疗效评价完全缓解(CR) 1例(5%),为肺癌;部分缓解(PR)4例(20%),其中肺癌3例,食管癌1例;稳定(SD)7例(35%),其中胰腺癌2例、鼻咽癌1例、胃癌1例、肺癌1例、脑肿瘤2例;进展(PD)8例(40%),其中膀胱癌1例、肺癌3例、淋巴瘤1例、前列腺癌1例、胸腺瘤1例、子宫内膜癌1例。总有效率RR(CR+PR)为25%,疾病控制率DCR(CR+PR+SD)为60%,其中一例肺腺癌患者在经一线(卡铂+紫杉醇)、二线(依托泊苷+顺铂)治疗获益6个月后处于疾病进展(PD),肿瘤标记物明显升高的情况下换用双环铂+伊立替康化疗3周期后评价PR。不同肿瘤有效率、控制率见表2。患者化疗联合用药有紫杉醇(白蛋白结合型)、氟尿嘧啶、尼妥珠单抗、贝伐珠单抗、帕博利珠单抗等。有4例同时联合其他化疗药和帕博利珠单抗,其中食管癌1例,评价PR;肺癌1例,评价PR;胃癌1例,评价SD;子宫内膜癌1例,评价PD。联合用药的近期疗效评估见表3,患者经双环铂治疗周期的疗效变化见图3。
表 2 20例恶性肿瘤患者用双环铂治疗的疗效
肿瘤类型 例数 完全缓解 部分缓解 稳定 进展 缓解率(%) 控制率(%) 肺癌 8 1 3 1 3 50 62.5 子宫内膜癌 1 1 0 0 胰腺癌 2 2 0 100 脑瘤 2 2 0 100 鼻咽癌 1 1 0 100 胸腺瘤 1 1 0 0 淋巴瘤 1 1 0 0 膀胱癌 1 1 0 0 前列腺癌 1 1 0 0 胃癌 1 1 0 100 食管癌 1 1 100 100 合计 20 1 4 7 8 25 60 表 3 双环铂与其他化疗药联用或单用疗效评估
疗效 用药例数(占比) 联合化疗药 联合单抗PD-1 单用 完全缓解(CR) 1 部分缓解(PR) 4 2 稳定(SD) 3 3 2 进展(PD) 1 5 3 合计 8(40%) 11(55%) 5(25%) -
根据KPS评分标准,治疗后KPS评分为(88±10.95),高于治疗前的(80.5±10.33),差异有统计学意义(P<0.05)。
-
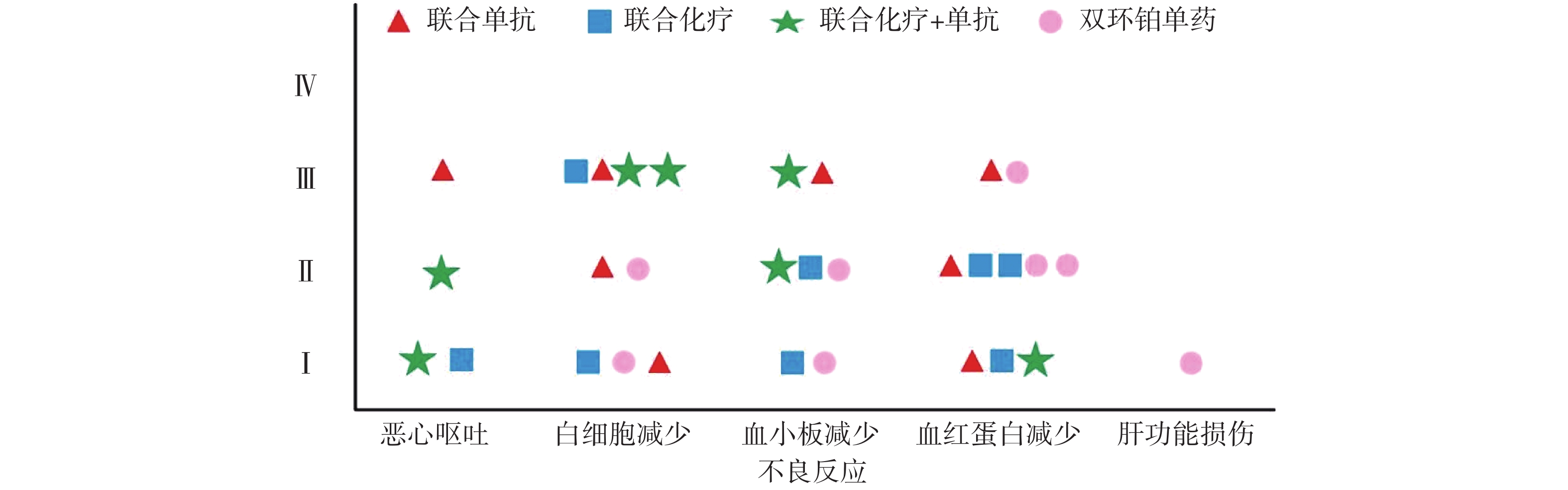
全组共完成80个周期化疗,毒副作用骨髓抑制和消化道反应最为常见,多为Ⅰ~Ⅱ度,无Ⅳ度。20例患者中白细胞减少发生率为45%,血小板和血红蛋白减少率分别为35%和50%。白细胞Ⅰ、Ⅱ度减少5例占25%,血红蛋白Ⅰ、Ⅱ度减少有8例占40%。消化道反应主要表现是恶心呕吐,其中Ⅰ度2例占10%,Ⅱ度、Ⅲ度各1例占比5%,Ⅰ度肝功能损伤1例占5%,详见表4和图4。
表 4 20例患者出现不良发应例数及发生率
类型 不良反应例数 发生率(%) 无 Ⅰ Ⅱ Ⅲ Ⅳ 恶心呕吐 16 2 1 1 0 20 白细胞减少 11 3 2 4 0 45 血小板减少 13 2 3 2 0 35 血红蛋白减少 10 3 5 2 0 50 肝功能损伤 19 1 0 0 0 5 -
据肿瘤流行病学资料显示,肺癌是对人类生命和健康威胁最大的恶性肿瘤之一,筛选入组的20例患者中有8例是肺癌患者。非小细胞肺癌是肺癌最常见的组织学类型,约占肺癌总数的80%,且多数患者就诊时已近晚期,局部病变发生转移失去手术机会。对于体能状态好,不可手术切除的肺癌患者推荐以铂类为基础的联合化疗是肺癌治疗的一线方案。目前,卡铂联合紫杉醇治疗晚期非小细胞肺癌方案较为成熟,Chen等[7]报道该方案治疗晚期非小细胞肺癌有效率为40%。一项比较双环铂联合紫杉醇方案与卡铂联合紫杉醇方案治疗非小细胞肺癌的临床研究显示:两组的有效率和中位疾病进展时间没有显著差异,但试验组双环铂的3年生存率显著优于对照组卡铂[8]。
晚期肿瘤主要的治疗手段是化疗,选择合理的化疗方案可提高患者生活质量,延长生存期。本文选用双环铂化疗方案治疗的20例患者中,单药治疗占比25%,联用其他化疗药(紫杉醇、氟尿嘧啶等)占比40%,联用单抗(帕博利珠、尼妥珠、贝伐珠单抗等)占比55%,其中20%患者同时联合化疗药和帕博利珠单抗治疗。帕博利珠单抗是近几年出现的一种新型抗肿瘤免疫药物,国际多项临床研究表明该类药物在肺癌、恶性黑色素瘤、头颈部肿瘤中显示出较好的疗效。本研究入组患者大于3线治疗共13例(65%),且多为肿瘤晚期或经手术放化疗后复发伴脏器、淋巴等多发转移,治疗后患者生活质量提高,疗效总有效率为25%,疾病控制率达60%。从图3可见20例患者中有11例患者在评估疾病进展(PD)后选用双环铂单药或联合用药治疗后评价近期疗效,其中CR 1例、PR 3例、SD 3例,有效率和疾病控制率分别是36%和64%,这说明双环铂在抑制肿瘤生长方面具有一定的优势,是有前途的抗癌药物。
本研究中消化道反应和骨髓抑制是化疗副反应中最为常见和严重的,这与双环铂临床前动物实验研究发现的主要毒性是血液系统毒性和消化系统毒性相吻合[9]。从图4可见本组研究中骨髓抑制的不良反应主要集中在白细胞减少和血红蛋白减少,其次是血小板减少,程度为Ⅰ~Ⅲ级。Ⅲ度骨髓抑制发生率较高,多在化疗3周后出现,双环铂联合单抗治疗者发生的概率较大。全组无Ⅳ度骨髓抑制和胃肠道反应,无过敏反应、无严重肾功能损伤。消化道反应主要表现在恶心呕吐,这也是很多肿瘤患者恐惧化疗的重要原因之一。本组病例化疗前后给予患者盐酸帕洛司琼注射液、盐酸昂丹司琼注射液、注射用托烷司琼等止吐用药,因此发生恶心呕吐的不良反应率较低,且绝大部分患者可以耐受,不影响后续治疗。其他辅助用药包括细胞保护,预防过敏,预防神经毒性,保肝、营养支持及对症处理,所有症状对症治疗后好转,多数患者经对症治疗后均可耐受。
综上所述,双环铂以其高效、低毒的特性可用于很多晚期肿瘤的治疗,特别是为多次化疗后不能耐受或产生多药耐药的癌症患者提供了新的用药选择。但本组病例数不多,单药治疗病例数较少,双环铂治疗的远期疗效及不良反应有待继续观察,值得开展大样本临床研究以进一步评价其疗效和毒性。
A retrospective analysis of the efficacy and safety of dicycloplatin in the treatment of malignant tumor
-
摘要:
目的 观察双环铂治疗恶性肿瘤的近期疗效及不良反应。 方法 回顾性分析我院自2017年1月至2018年8月使用双环铂治疗恶性肿瘤患者的病例,至少化疗2个周期后评价疗效及不良反应。 结果 平均化疗4个周期的20例患者中,其中完全缓解(CR)1例,部分缓解(PR)4例,稳定(SD)7例,进展(PD)8例,总有效率25%,疾病控制率60%,生活质量KPS评分较治疗前提高(P<0.05)。化疗期间主要毒副作用,表现为骨髓抑制和胃肠道反应。患者白细胞减少、血小板减少、血红蛋白减少、恶心呕吐、肝功能损伤发生率分别是45%、35%、50%、20%、5%。 结论 以双环铂为主的化疗方案治疗恶性肿瘤有较好的疗效,不良反应较轻可耐受,值得临床进一步观察和应用。 Abstract:Objective To observe the short-term efficacy and adverse reactions of dicycloplatin in the treatment of malignant tumors. Methods A retrospective analysis was performed in our hospital from January 2017 to August 2018 using dicycloplatin to treat patients with malignant tumors. The efficacy and adverse reactions were evaluated after at least 2 cycles of chemotherapy. Results Among the 20 patients with an average of 4 cycles of chemotherapy, 1 had complete remission (CR), 4 had partial remission (PR), 7 had stable diseases (SD), 8 had progression (PD). The total efficacy was 25%. The control rate was 60%. The KPS scores for quality of life was higher than that before treatment (P<0.05). The main adverse effects during chemotherapy were bone marrow suppression, gastro-intestinal reactions. The incidence of leukopenia, thrombocytopenia, reduced hemoglobin, nausea vomiting and liver damage was 45%, 35%, 50%, 20%, and 5%, respectively. Conclusion Dicycloplatin-based chemotherapy has a good curative effect on malignant tumors, and the adverse reactions are mild and tolerable, which deserves further clinical observation and application. -
Key words:
- discycloplatin /
- malignant tumor /
- clinical therapy /
- effectiveness evaluation /
- side effects
-
药品的调剂发放是门诊药房药师工作中非常重要的组成部分,门诊药师的药学服务工作也都围绕着药品的调剂发放展开。随着医药科技发展,门诊处方量不断增加,以及药品集中采购带来的药品更替增加,都给门诊药品的调剂发放带来了巨大的压力。
笔者所在医院是一所大型综合性医院,工作日平均门诊量在10 000人次左右,日均处方4 000张以上,每个发药窗口日均处方量500张以上,窗口药师工作压力巨大,极易出错。“军卫一号”发药系统自1997年在本院开始使用至今,软件老旧,功能不足。为适应我院的实际情况,提高工作效率,改善工作质量,特开发了“门诊发药辅助系统”。该系统充分利用各类条形码便捷输入的特点,在药品核对、处方权管理、效期管理、用药交待等多个环节辅助药师工作,可以有效降低差错,提高效率,增强药品管控能力。现将本系统的设计与使用情况做简要介绍。
1. 系统设计
1.1 系统环境
以医院信息系统(HIS)为数据基础,结合MS SqlServer 2008数据库管理系统作为数据储存平台,以Windows XP以上操作系统为开发及运行平台,Delphi和DotNet作为开发语言,构建了客户端(C/S)形式的应用程序。
1.2 系统结构
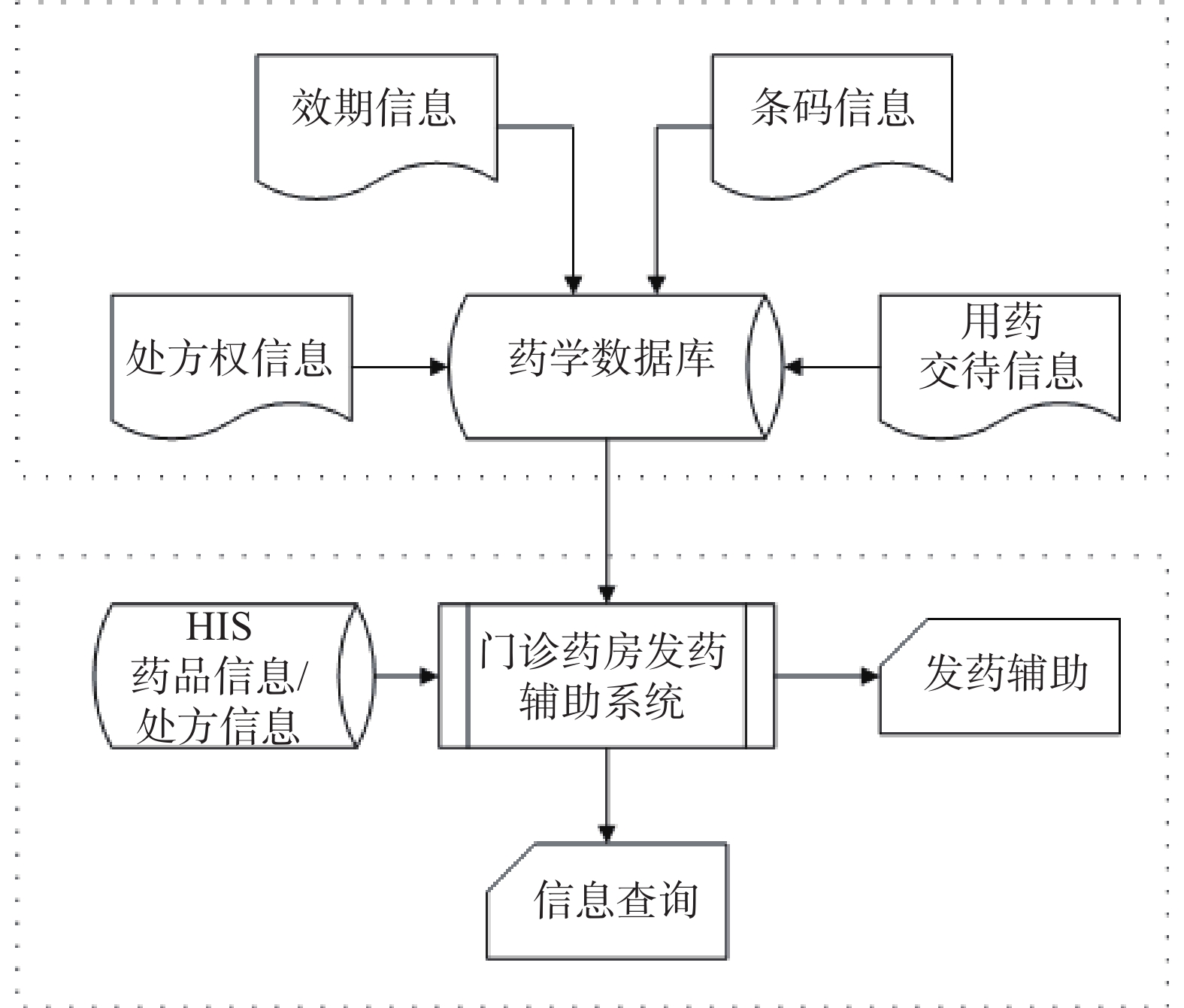
系统主要分后台数据维护和前台发药辅助两部分。后台数据维护部分负责对条形码、处方权、效期等提示信息进行维护,前台发药辅助部分提供即时的信息显示和查询功能。详细结构见图1。
2. 系统功能
条形码识别是该系统构建的核心。药品包装上的条形码一般有商品码和监管码两种[1]。2012年开始国家提出了对药品电子监管信息平台的建设工作,2016年国家又出台了《关于推动食品药品生产经营者完善追溯体系的意见》,虽然药品追溯体系的建立一波三折,但是至今国家药品监管码仍然已经覆盖了超过80%的中国药品企业和95%的国家重点关注品种[2]。本系统采用商品码和监管码并行查询的方式,对患者、处方和药品进行识别。
2.1 数据维护部分
条码信息、处方权信息和效期信息统一由数据维护程序录入系统。①药师通过程序的条码录入模块查询HIS储存的药品信息,然后扫描药盒上的商品码和监管码,把条码与相应的药品匹配。②负责管理处方权登记的药师可通过程序的处方权管理模块搜索HIS中储存的医生信息,在程序中设置医生所拥有的处方权限。③负责库存管理药师可通过程序的效期管理模块查询药品信息,并对药品的效期信息进行维护。
用药交待模块的数据直接从门诊用药咨询登记系统读取,平时由门诊咨询药师在咨询登记过程中根据咨询的情况随时维护,保证资料库中有最新、最简洁、最常用的药品信息直接为前台药师提供帮助。
2.2 发药辅助部分
由于原“军卫一号”发药系统的源代码无法修改,并且在现有的工作条件下,窗口药师工作繁忙,无法抽出时间进行过多的输入操作,所以系统把患者ID、条形码监管码等信息输入统一在一个输入口,通过系统后台监控药师扫码过程,做到功能无缝切换。药师只需扫描一次条码,系统即可查询并显示该患者当日所有就诊科室开具的多个处方信息。
2.2.1 药品核对
药品核对部分的工作流程见图2。
原有的发药流程中,药师只能依据经验,逐一核对患者的取药单据、电脑信息、处方和药品。引入新的“门诊发药辅助系统”后,药师只需扫描患者手中收据或者取药凭条上包含患者ID号信息的条码,发药系统搜索定位到该患者处方。此时辅助系统接收到扫描信息,自动完成输入焦点切换、查询并显示处方明细等一系列操作。药师直接扫描药品包装上的商品码或监管码进行药品核对。对于品种正确的药品,系统弹出显示框放大该药品信息,药师进一步核对药品数量。如果处方中没有该药品,则系统弹出提示告知药师确认。以往的药品核对工具只能对药品品种进行核对,缺乏对药品数量的敏感性[3]。该系统通过放大及颜色刺激的方式对数量做出提示,既可避免逐盒扫描药品对发药速度的影响,又可在一定程度上降低人工核对导致的数量差错。
显示的处方明细中以不同的字体颜色和底色向药师提示不同的情况。背景灰色表示该药品未录入条码,背景黄色表示该药品已扫码发放,红色字体表示该药品信息有异常。协助药师快速了解处方药品情况,提高发药效率。
2.2.2 处方权管理
处方权限的提示集成在扫码显示的处方明细界面中。显示的信息包括了医生的姓名及所在科室。文字为绿色则提示该医生有麻精药品处方权限,可以开具特殊药品处方,进一步点击医生姓名可显示HIS中储存的医生签名图片;文字为红色则提示该医生没有进行过麻精药品处方权限登记,如果开具特殊药品,需要有权限的医师在处方上再次签字确认。由于门诊医生人数众多,流动量大,该功能可帮助药师快速确定医生权限,不需要查阅处方权登记本,把更多精力放在对处方合理性的审核上。
2.2.3 效期管理
药品的效期提示同样集成在处方明细界面中,直接以颜色作为标识。如果辅助系统查询到处方中的某种药品包含近效期药品,则以醒目的绿色字体提示药师,药师需要仔细核对药品每个最小包装,确认是否可以正常发放。
2.2.4 用药交待
药品辅助咨询的信息以提示框的形式在处方明细界面供药师查询显示。药品信息以蓝色字体显示,则提示该药品包含提示信息。药师双击该药名即可弹出提示框显示该药品的储存方式、注意事项、用法用量、相互作用等需要提示患者的信息或者患者经常提问的信息,进一步强化药师的药学服务能力。
3. 应用效果
为考察发药辅助系统的实际应用效果,并对系统功能的进一步改进提供帮助,笔者针对门诊药师重点关注的调配差错、发药效率和对药师的影响等方面进行调查分析。
3.1 对调配差错影响
门诊药房作为与患者直接沟通的窗口,差错的出现对于患者影响的意义巨大,直接影响患者是否能安全有效的使用药物,影响患者对医院药学服务的信任程度。但是由于药品数量多,药师工作压力大,且存在药名相似、包装相似、一品多规等多种干扰因素,总是难以避免产生人为的调剂差错。据统计,美国每年用药差错中58%是由于药名、包装相似引起的品种差错[4],国内的报告中品种差错也达到了40%左右[5-6]。使用该系统后,对于品种差错,系统会自动提示错误,相当于在发药环节增加了计算机核对步骤,由原来的双核对增加到了三核对,同时高亮的已发药品显示还能帮助药师检查是否有漏发、多发的情况,可以有效降低药师发药的差错。在辅助系统稳定工作1年后,笔者对系统使用前后1年内的发药差错情况进行统计分析,差错数据来源除由患者找回的发药差错外,还包括在盘点过程中发现账物不符并排除其他情况后推断为发药差错的差错。其中数量差错包括多发、少发、漏发等情况,品种差错包括由于药名相似、剂型相似或包装相似等引起的差错,其他为患者拿错,遗落等原因引起的差错,所有差错均是经核实并登记的发药差错。结果如表1。
表 1 发药辅助系统使用前后发药差错对比差错类型 系统使用前 系统使用后 例数 占比(%) 例数 占比(%) 数量差错 41 49 15 60 品种差错 33 39 4 16 其他 10 12 6 24 总计 84 100 25 100 总差错率(‰)(差错数/年处方数) 0.107 0.027 3.2 对发药效率的影响
启用发药辅助系统后,药师在发药过程中增加了扫码环节,单个药品核对用时有所增加。但经过笔者对所在单位门诊发药高峰时段(10:00-11:30)使用发药辅助系统前后单个患者平均取药时间进行统计。结果显示使用发药辅助系统后,患者取药消耗的时间反而有所减少。高峰时段患者总取药时间中位数由原来的8 min 52 s,缩短到了现在的6 min 21 s。综合考虑药师发药时的各种情况,在当前调配量过剩的情况下,虽然发药扫码过程消耗了额外的时间,但是药师在系统的辅助下,只要逐品种扫码发放药品,核对数量,不需要额外花精力去确认药品是否漏发或发重,可以更快的核对处方、核对药品,在患者多科室看病,开具药品品种较多时,效果尤其明显。处方权提示和用药交代提供的内容帮助药师更快的应对发药过程中出现的情况,有效的提高了总体工作效率。
3.3 药师评价
通过对门诊药师开展系统使用情况的问题调研,反馈的情况统计如表2。
表 2 发药辅助系统药师反馈意见汇总(n=32)药师反馈意见 赞同人数 赞同人数占比(%) 系统可减少差错 30 94 系统可提高效率 23 72 有助于增强事件处理能力 20 63 增加了工作量 3 9 系统有助于药师工作 32 100 药师普遍认为该辅助系统有助于减少差错、降低发药药师的工作压力。通过对反馈问题的深入了解,主要不认可的问题在于部分年龄比较大的药师,经验丰富,工作更依赖于自身经验,对于新引入的计算机软件有一定的排斥心理,需要更多的时间逐渐适应系统操作。另外有个别药品外包装既没有商品码,也没有监管码,无法识别,只能人工核对药品信息。
4. 讨论
2015年国家食药总局就要求“2016年1月1日后生产的药品制剂应做到全部赋码”,2019年4月19日,国家药品监督管理局正式发布了《药品信息化追溯体系建设指导》和《药品追溯码编码要求》两项药品信息化追溯体系标准,编码规则确定了20位溯源码前7位为药品标识码或者符合ISO相关国际标准,但至今仍有部分药品既无监管码也没有商品码。笔者对所在医院门诊药房现有919种药品进行了统计,有58%的药品包装有商品码,有73%的药品包装印有监管码,条码总计覆盖了79%的药品。按药品消耗量计算,可扫码药品占门诊总发药量的93.8%。不能扫码的药品主要为医院制剂、针剂和部分瓶装普药。如果把这些药品全部纳入扫码,需要额外做大量的工作。对于医院制剂,可以与制剂部门沟通在药品包装上加印自制的条形码,其他药品需要在实际工作中仔细核对,进一步结合工作研究出既不影响效率又能提高准确率的方案。
应用该发药辅助系统后,总的差错数量大幅减少,数量差错也有明显减少,但品种差错仍然存在。主要原因是虽然辅助系统提供了多一层核对,但是药师过于依赖该系统,弱化了自身的核对,造成错误。同时高强度的工作也是导致药师注意力不集中,出现发药差错的影响因素。
门诊发药辅助系统功能涵盖了药师发药工作的多个环节,功能全面。系统以发药核对为核心功能,既整合了处方权管理、效期管理和药学服务等功能模块,同时各个模块之间又相对独立,可根据需求逐步添加。处方权管理模块在麻精药品管理中引入了信息化控制,能够进一步规范麻精药品的使用,确保制度落实。咨询辅助模块在协助药师回答患者问题的同时,也强化了药师的业务能力,有助于提高药师地位。药师咨询能力的提升,也有助于减少医患纠纷的发生[7]。
市售的大型发药系统虽然发药准确率可达到万分之二,但是设备引进及维护费用巨大,且对药房环境条件、药品剂型、包装等有诸多限制[8]。整个扫码发药过程中只需要在每个窗口添加条码扫描设备,维护简单,无需过多的硬件或资金投入。该程序的使用,用较低的成本优化了药学服务,提高了发药准确率,对药学服务的发展具有重要意义。
-
表 1 20例患者一般临床特征统计
项目 数量[n(%)] 项目 数量[n(%)] 年龄(岁) 57.85(18−85) 转移部位 <50 5(25) 内脏 9(45) ≥50−60 5(25) 肝脏 1(5) >60 10(50) 仅淋巴结节 4(20) 性别 多发脏器转移 6(30) 女 4(20) 骨转移 1(5) 男 16(80) 双环铂治疗周期 初/复诊 2期 2(10) 初诊 3(15) 3期-4期 11(55) 复诊 17(85) >5期 7(35) KPS评分 其他同期用药 ≤70 6(30) 化疗药 8(40) 70-80 0 PD-1 11(55) 90 14(70) 无 5(25) 表 2 20例恶性肿瘤患者用双环铂治疗的疗效
肿瘤类型 例数 完全缓解 部分缓解 稳定 进展 缓解率(%) 控制率(%) 肺癌 8 1 3 1 3 50 62.5 子宫内膜癌 1 1 0 0 胰腺癌 2 2 0 100 脑瘤 2 2 0 100 鼻咽癌 1 1 0 100 胸腺瘤 1 1 0 0 淋巴瘤 1 1 0 0 膀胱癌 1 1 0 0 前列腺癌 1 1 0 0 胃癌 1 1 0 100 食管癌 1 1 100 100 合计 20 1 4 7 8 25 60 表 3 双环铂与其他化疗药联用或单用疗效评估
疗效 用药例数(占比) 联合化疗药 联合单抗PD-1 单用 完全缓解(CR) 1 部分缓解(PR) 4 2 稳定(SD) 3 3 2 进展(PD) 1 5 3 合计 8(40%) 11(55%) 5(25%) 表 4 20例患者出现不良发应例数及发生率
类型 不良反应例数 发生率(%) 无 Ⅰ Ⅱ Ⅲ Ⅳ 恶心呕吐 16 2 1 1 0 20 白细胞减少 11 3 2 4 0 45 血小板减少 13 2 3 2 0 35 血红蛋白减少 10 3 5 2 0 50 肝功能损伤 19 1 0 0 0 5 -
[1] GIACCONE G. Clinical perspectives on platinum resistance[J]. Drugs,2000,59(Supplement 4):9-17. doi: 10.2165/00003495-200059004-00002 [2] 颜冬梅, 屠凌岚, 彭小英, 等. 铂类抗癌新药双环铂的体内外抗肿瘤活性[J]. 中国现代应用药学杂志, 2007, 10(5):353. [3] LI G Q, CHEN X G, WU X P, et al. Effect of dicycloplatin, a novel platinum chemotherapeutical drug, on inhibiting cell growth and inducing cell apoptosis[J]. PLoS One,2012,7(11):e48994. doi: 10.1371/journal.pone.0048994 [4] 闫长会, 施畅, 李玉风, 等. 新铂类药物双环铂与顺铂、卡铂体内毒性的比较研究[J]. 中国新药杂志, 2005, 14(10):1156-1159. doi: 10.3321/j.issn:1003-3734.2005.10.010 [5] CHANG H Y, CHANG S, YU F L, et al. Comparison of toxicities of bicycloplatin with cisplatin and carboplatin[J]. Chin J New Drugs,2005,14:1156-1159. [6] MILLER A B, HOOGSTRATEN B, STAQUET M, et al. Reporting results of cancer treatment[J]. Cancer,1981,47(1):207-214. doi: 10.1002/1097-0142(19810101)47:1<207::AID-CNCR2820470134>3.0.CO;2-6 [7] CHEN Y M, PERNG R P, LEE Y C, et al. Paclitaxel plus carboplatin, compared with paclitaxel plus gemcitabine, shows similar efficacy while more cost-effective: A randomized phase II study of combination chemotherapy against inoperable non-small-cell lung cancer previously untreated[J]. Ann Oncol,2002,13(1):108-115. doi: 10.1093/annonc/mdf009 [8] 曾赟, 史美祺, 周国仁, 等. 双环铂联合紫杉醇治疗晚期非小细胞肺癌的Ⅱ期随机双盲多中心临床研究[J]. 南通大学学报(医学版), 2011, 31(5):327-329. doi: 10.3969/j.issn.1674-7887.2011.05.005 [9] 林飞, 吕廉, 杨旭清, 等. 双环铂及其衍生物对大鼠靶器官毒性损伤的比较[J]. 癌变. 畸变. 突变, 2005, 17(5):276-279. 期刊类型引用(2)
1. 罗敏,陈欢,赵福坤,苏穆,王远敏. 决策树支持下SmartDose在神经外科万古霉素个体化用药中的应用. 遵义医科大学学报. 2023(06): 605-611 .  百度学术
百度学术2. 杨浩,熊雄,刘长江. 骨科术后患者万古霉素峰谷浓度的影响因素及群体药动学预测比较. 中国医院药学杂志. 2023(24): 2722-2728 .  百度学术
百度学术其他类型引用(2)
-





 下载:
下载:

 下载:
下载: