-
口腔溃疡膜是海军军医大学附属长征医院的特色院内制剂,该制剂主要由克霉唑、硫酸新霉素、冰片、盐酸达克罗宁、地塞米松磷酸钠等成分组成,呈微黄色至淡黄色半透明膜。临床用于治疗多发性口腔溃疡。溃疡是口腔疾病的常见表现,口腔黏膜溃疡病因可分为4类:感染性、免疫性、外伤性和肿瘤性[1]。地塞米松磷酸钠属糖皮质激素,经常用于加速溃疡愈合、减轻口腔溃疡的局部症状[2];克霉唑是一种常用于治疗真菌感染的抗真菌药物[3]。口腔溃疡膜能保护局部溃疡面,延长局部作用时间、提高药物浓度,具有定位释放、使用方便等优点[4]。本制剂室唐蕾等[5]通过测定口腔溃疡膜中克霉唑和地塞米松磷酸钠的含量建立了一套操作简单、准确性好的HPLC含量测定方法,适用于口腔溃疡膜的质量标准控制。但随着制剂标准的提高,在《军队医疗机构制剂许可证》验收细则中明确规定:配制制剂的原料药应符合法定药品标准,辅料及直接接触制剂的包装材料应符合法定标准。因此,一些原料药及辅料在更换药用标准后,按照原先的样品前处理方法测得的含量一直偏低。本文以口腔溃疡膜中主要有效成分地塞米松磷酸钠和克霉唑的含量为指标,对口腔溃疡膜中有效成分的提取工艺进行研究,并进一步优化地塞米松磷酸钠和克霉唑的含量测定方法。
-
Agilent 1260型高效液相色谱仪(美国Agilent公司):包含G7104C(四元泵)输液泵,G7129C自动进样器,G7116A柱温箱,G7115A DAD检测器;色谱柱为Agilent Zobax SB-C18柱(250 mm×4.6 mm,5 μm,美国Agilent公司);Sartorius 天平(型号:BSA124S-CW,十万分之一天平,赛多利斯科学仪器有限公司);超声仪(SK7200H型,上海科导超声仪器有限公司);Eppendorf移液器(德国);WL-901 Vortex旋涡振荡混和器(海门市其林贝尔仪器制造有限公司)。
-
地塞米松磷酸钠对照品(批号:ZN1107XA)、克霉唑对照品(批号:H01S9Z68980),购自上海源叶生物科技有限公司;甲醇(色谱纯,德国Fisher公司);娃哈哈纯净水(纯净水,杭州娃哈哈集团有限公司);磷酸二氢钾等其余试剂均为分析纯。口腔溃疡膜(批号:190919、190923、190926,每片含地塞米松磷酸钠0.4 mg,克霉唑6.53 mg,海军军医大学附属长征医院制剂中心自制)。
-
色谱柱:Agilent Zobax SB-C18柱(250 mm×4.6 mm,5 μm);流动相:甲醇−0.05 mol/L磷酸二氢钾溶液(70∶30, 用磷酸溶液调pH值4.4~4.5);紫外检测波长:230 nm;流速:1.0 ml/min;柱温:30 ℃;采集时间:30 min,进样量:20 μl。
-
精密称取地塞米松磷酸钠16.328 mg置于10 ml量瓶中,加甲醇-水(7∶3)溶解并稀释至刻度,摇匀,得浓度为1.632 8 mg/ml的地塞米松磷酸钠对照品储备液。精密称取克霉唑对照品20.058 mg置于10 ml量瓶中,加甲醇-水(7∶3)溶解并稀释至刻度,摇匀,得浓度为2.005 8 mg/ml的克霉唑对照品储备液。
-
分别精密量取地塞米松磷酸钠、克霉唑对照品储备液适量,加甲醇-水(7∶3)配制成含地塞米松磷酸钠16.328 μg/ml和克霉唑200.58 μg/ml的混合对照品溶液。
-
取口腔溃疡膜剪成3~5 mm大小的碎片,精密称取样品0.2 g,置于100 ml容量瓶中,加入30 ml水,超声30 min,取出,放冷,加入甲醇并稀释至刻度,摇匀,即得。
-
参照本课题组前期实验方法,制备阴性对照品溶液[5]。
-
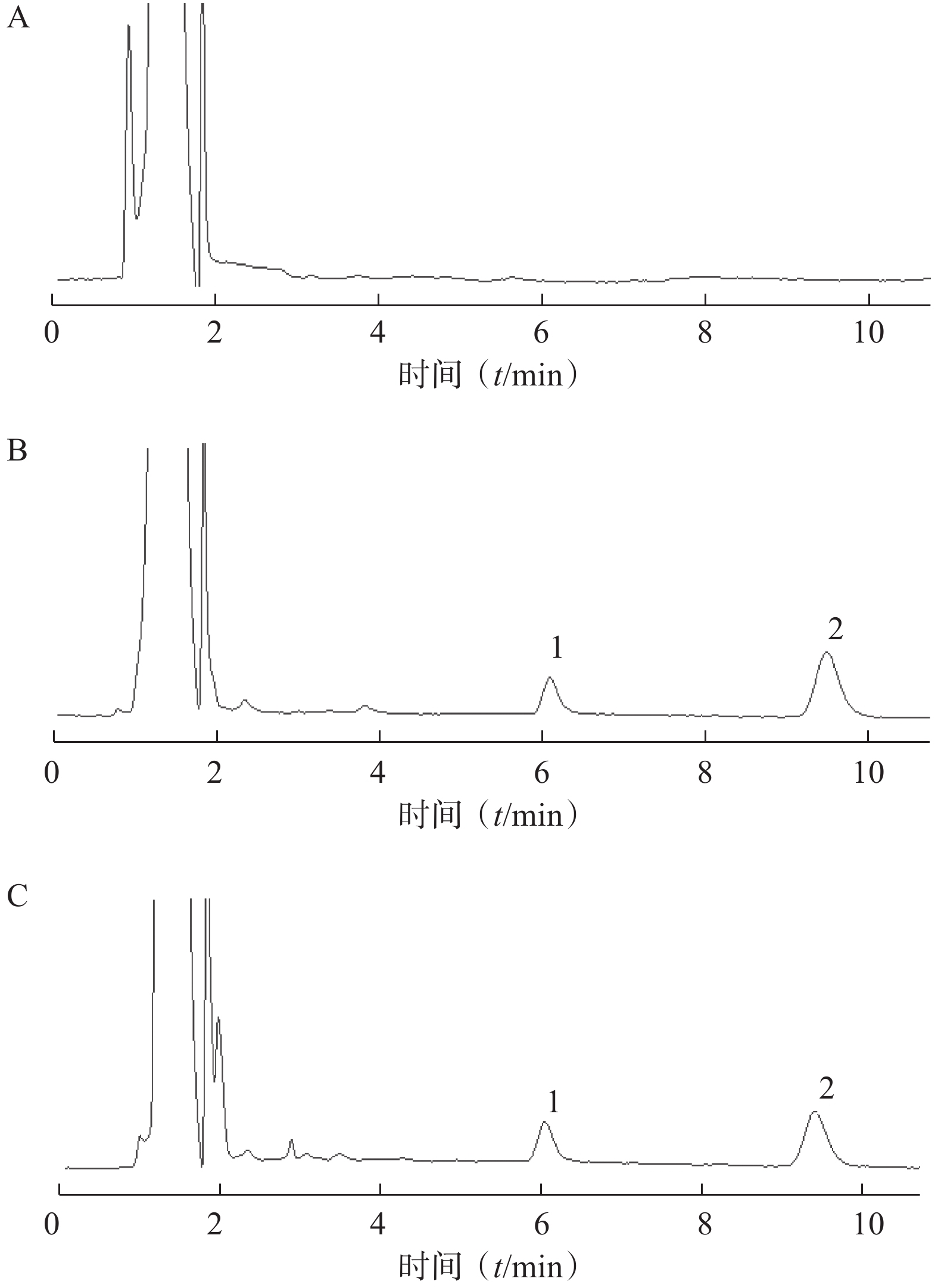
分别取混合对照品溶液(地塞米松磷酸钠、克霉唑)和供试品溶液,按“2.1”项下色谱条件测定,记录色谱图,结果见图1。图中显示供试品溶液中地塞米松磷酸钠和克霉唑保留时间与对照品溶液相应色谱峰的保留时间一致。地塞米松磷酸钠和克霉唑与其相近的其他峰分离完全(分离度>1.5),即本试验条件下地塞米松磷酸钠和克霉唑与其他组分分离完全。
-
精密量取“2.2.2”项下混合对照品溶液适量,稀释成以下浓度的混合对照品溶液:地塞米松磷酸钠0.482 0、0.816 4、1.632 8、4.082 0、8.164 0、16.328 0 μg/ml;克霉唑5.014 5、10.029 0、20.058 0、50.14 50、100.290 0、200.580 0 μg/ml,按“2.1”项下色谱条件进行测定,并记录色谱峰面积。以峰面积为纵坐标(Y),对照品质量浓度为横坐标(C),绘制标准曲线,并进行线性回归,结果见表1。
表 1 地塞米松磷酸钠和克霉唑的线性关系考察
成分 回归方程 r 线性范围(μg/ml) 地塞米松磷酸钠 Y=34.961C+27.986 0.999 9 0.482 0~16.328 0 克霉唑 Y=32.366C+24.092 0.999 8 5.014 5~200.580 0 -
取同一批口腔溃疡膜(批号:190919),按“2.2.3”项方法制备供试品溶液,按“2.1”项色谱条件进行测定,连续进样6次,记录峰面积。计算地塞米松磷酸钠和克霉唑峰面积RSD分别为0.65%和0.33%,表明仪器精密度良好。
-
取同一批口腔溃疡膜(批号:190919),按“2.2.3”项方法平行制备6份供试品溶液,按“2.1”项色谱条件进行测定,记录峰面积。计算地塞米松磷酸钠和克霉唑峰面积RSD分别为0.56%和0.54%,表明该方法重复性良好。
-
取同一批口腔溃疡膜(批号:190919),按“2.2.3”项方法制备供试品溶液,按“2.1”项色谱条件,分别在0、2、4、6、12、24 h进样测定,记录峰面积。计算地塞米松磷酸钠和克霉唑峰面积RSD值分别为0.94%和1.33%,表明供试品溶液在室温放置24 h内稳定性良好。
-
精密称取已知含量的样品(批号:190919)0.2 g,共6份,置于100 ml容量瓶中,加入各对照品适量,按“2.2.3”项方法制备供试品溶液,按“2.1”项色谱条件进样测定,记录峰面积,计算加样回收率。结果地塞米松磷酸钠和克霉唑的平均加样回收率分别为(103.97±1.02)%和(104.23±0.63)%,表明本法回收率良好。
-
取3批口腔溃疡膜,按“2.2.3”项方法制备供试品溶液,按“2.1”项色谱条件进行测定,计算样品中地塞米松磷酸钠和克霉唑的含量,结果见表2。
表 2 口腔溃疡膜中地塞米松磷酸钠和克霉唑的含量测定结果(n=3,
$\bar x$ ±s)批号 含量[标示量(%)] 地塞米松磷酸钠 克霉唑 190919 76.600 0±0.005 2 86.800 0±0.011 3 190923 85.900 0±0.011 5 99.100 0±0.025 9 190926 74.900 0±0.043 7 85.700 0 ±0.067 6 -
本研究根据口腔溃疡膜的特性,对溶剂种类、溶剂提取顺序进行考察,由于口腔溃疡膜中含羧甲基纤维素钠,这是由一种天然纤维素衍生的阴离子水溶性聚合物[6],易溶于水,因此需要一定比例的水将膜剂破坏,才能释放出膜剂中的有效成分地塞米松磷酸钠和克霉唑。
-
取口腔溃疡膜剪成3~5 mm大小的碎片,精密称取样品0.2 g,置于100 ml容量瓶中,加入甲醇35 ml,超声30 min,取出,放冷,加入15 ml水,混匀后用甲醇-水(7∶3)定容,摇匀,即得。
-
取口腔溃疡膜剪成3~5 mm大小的碎片,精密称取样品0.2 g,置于100 ml容量瓶中,加入30 ml水,超声30 min,取出,放冷,加入甲醇并稀释至刻度,摇匀,即得。
-
取口腔溃疡膜剪成3~5 mm大小的碎片,精密称取样品0.2 g,置于100 ml容量瓶中,加入甲醇-水(7∶3)30 ml,超声30 min,取出,放冷,加入甲醇-水(7∶3)稀释至刻度,摇匀,即得。
用以上不同溶剂提取口腔溃疡膜,每份样品、每种溶剂平行提取3次,按“2.1”项所述色谱条件测定地塞米松磷酸钠和克霉唑含量,结果见表3。实验结果显示:水超声提取和70%甲醇超声提取对口腔溃疡膜中有效成分的提取效果相当,但水超声提取相对简单,故选用水超声提取30 min为最佳提取工艺。
-
在液相色谱条件优化实验中,比较了不同pH时的采集时间,结果发现:pH在4.4~4.5时采集时间为30 min,较之于前缩短了5 min,方法更便捷。
表 3 不同溶剂对口腔溃疡膜有效成分提取率的影响[n=3,实测值/标示量(%)]
提取方法 地塞米松磷酸钠 克霉唑 甲醇超声提取 67.46 74.49 71.58 79.06 73.09 72.64 水超声提取 108.29 101.28 104.08 101.03 105.88 103.38 70%甲醇超声提取 104.27 95.00 109.52 100.52 106.89 103.54 本研究基于HPLC同时测定口腔溃疡膜中地塞米松磷酸钠、克霉唑含量的方法,经提取工艺的优化和全面的方法学考察,成功用于测定样品中地塞米松磷酸钠和克霉唑的含量,该法简便可靠,可为口腔溃疡膜的质量控制提供依据,也为其质量标准研究奠定了基础。
Investigation of the extraction method and content determination of the active components from oral ulcer film
-
摘要:
目的 考察不同溶剂对口腔溃疡膜中有效成分地塞米松磷酸钠和克霉唑的提取率,优化有效成分含量测定方法。 方法 采用不同提取溶剂(甲醇、水、70%甲醇)对口腔溃疡膜中的有效成分进行提取,用HPLC法进行含量测定,得到最佳提取方法。 结果 纯水对口腔溃疡膜中地塞米松磷酸钠和克霉唑有最好的提取效果。地塞米松磷酸钠在0.482~16.328 μg/ml范围内呈良好的线性关系(r=0.999 9),平均回收率为(103.97±1.02)%;克霉唑在5.014 5~200.580 0 μg/ml范围内呈良好的线性关系(r=0.999 8),平均回收率为(104.23±0.63)%。 结论 本研究建立的纯水提取方法操作简单,提取效率高,含量测定方法操作简便,准确性、重复性好。 Abstract:Objective To investigate the extraction methods for active components from oral ulcer film and optimize the determination methods of active components dexamethasone sodium phosphate and metronazole. Methods Different extraction solvents(methanol, water and 70% methanol aqueous) were applied to extract the active components dexamethasone sodium phosphate and metronazole from oral ulcer film, which contents were quantified by a HPLC method. Results the extraction solvent water had the best efficacy and more simpler compared to the other two solvents. Clotriazole showed a good linear relationship within 5.014 5-200.5800 μg/ml (r=0.999 8), and the average extraction recovery was (104.23±0.63)%, and for dexamethasone sodium phosphate, a good linear relationship was obtained in the range of 0.482-16.328 μg/ml (r=0.9999), and the average extraction recovery was (103.97±1.02)%. Conclusion The water extraction method established in this study was simple and efficient, which showed features of simplicity, accuracy and repeatable. -
Key words:
- oral ulcer film /
- dexamethasone sodium phosphate /
- clotrimazole /
- content determination /
- HPLC
-
奥卡西平(oxcarbazepine, OXC)是第二代抗癫痫药物,可用于儿童全面强直-阵挛发作,部分伴或不伴继发性全面发作的一线治疗[1],其具有与传统的抗癫痫药物(AEDs)如苯妥英钠、卡马西平和丙戊酸钠相同的疗效,但其对肝药酶和自身的诱导作用小,药物间相互作用较少,临床上可用于替代传统的AEDs。OXC是卡马西平(carbamazepine, CBZ)的一种10-酮类衍生物,但两者之间的药动学存在差异,OXC的耐受性好且不良反应少[2]。OXC是无活性的前体药物,在体内经过肝脏内细胞溶质芳基酮还原酶的作用转化为具有药理活性的中间代谢产物单羟基卡马西平(monohydroxy carbamazepine, MHD)[3-4]。国际抗癫痫联盟推荐MHD血清浓度的参考范围为3~35 μg/ml[5],有研究表明,当血药浓度高于30 μg/ml时,容易发生药物不良反应,且在许多患者中,不良反应间歇性的发生与MHD浓度的波动有关[6]。在临床用药中也发现OXC服药后的药物浓度个体化差异大,年龄、性别、体重、肝肾功能等均会影响MHD的药动学参数[7],故需要对其血药浓度进行监测。本研究在参考既往研究的基础上[8-12],对色谱条件进行了优化,并简化了血样处理的过程,建立了HPLC法测定OXC活性代谢产物MHD血药浓度的方法,该方法快速、简单、准确、选择性好、灵敏度高,为临床监测血药浓度、调整给药剂量提供了手段。
1. 仪器与材料
1.1 仪器
Agilent 1200高效液相色谱仪(美国Agilent公司);H1850R型台式高速冷冻离心机(湖南湘仪实验室仪器开发有限公司);DHG-9145A型电热恒温鼓风干燥箱(上海恒科仪器有限公司);SHB-B95A型循环水式多用真空泵(郑州长城科工贸有限公司);Discovery DV215CD型分析天平(美国OHAUS公司);Vortex-5型涡旋混合器(江苏海门市其林贝尔仪器制造有限公司)。
1.2 材料
MHD对照品(美国CATO公司);内标:奥硝唑(中国食品药品检定研究院);甲醇、乙腈(色谱纯,上海科丰化学试剂有限公司);空白血浆(医院血库提供);超纯水(实验室自制)。
2. 实验方法
2.1 色谱条件
色谱柱:ZORBAX Eclipse XDB-C18(150 mm×4.6 mm,5 μm),预柱为Eclipse XDB-C18(4.6 mm×12.5 mm,5 μm);流动相:水-乙腈(80:20,V/V);流速:1.0 ml/min;柱温:35 ℃;进样量:10 μl;双波长检测:在192 nm处检测MHD,318 nm处检测奥硝唑。
2.2 溶液及血浆样品的配制
2.2.1 储备液的配制
精密称取MHD对照品10 mg于10 ml的量瓶中,用甲醇溶解配制成浓度为1 mg/ml的储备液,置于−20 ℃下保存。
2.2.2 内标工作液的配制
精密称取奥硝唑1.4 mg于10 ml的量瓶中,用甲醇溶解配制成浓度为140 μg/ml的内标工作液,置于−20 ℃下保存。
2.2.3 血浆标准曲线和质控样品的配制
分别精密量取适量储备液,用甲醇稀释成20、50、100、200、300、400、500 μg/ml浓度梯度的标准对照溶液。取以上6个标准对照溶液,加入适量空白血浆,得2、5、10、20、30、40、50 μg/ml系列浓度的血浆标准曲线样品。同法配制相应的低、中、高浓度的血浆质控样品(QC),使得MHD对应的浓度分别为5、15、40 μg/ml。
2.3 血浆样品的预处理
取200 μl血浆样品,加入200 μl内标工作液、400 μl甲醇,涡旋混合30 s,10 ℃条件下13 000 r/min离心10 min,取上清液直接进样。
3. 结果
3.1 专属性试验
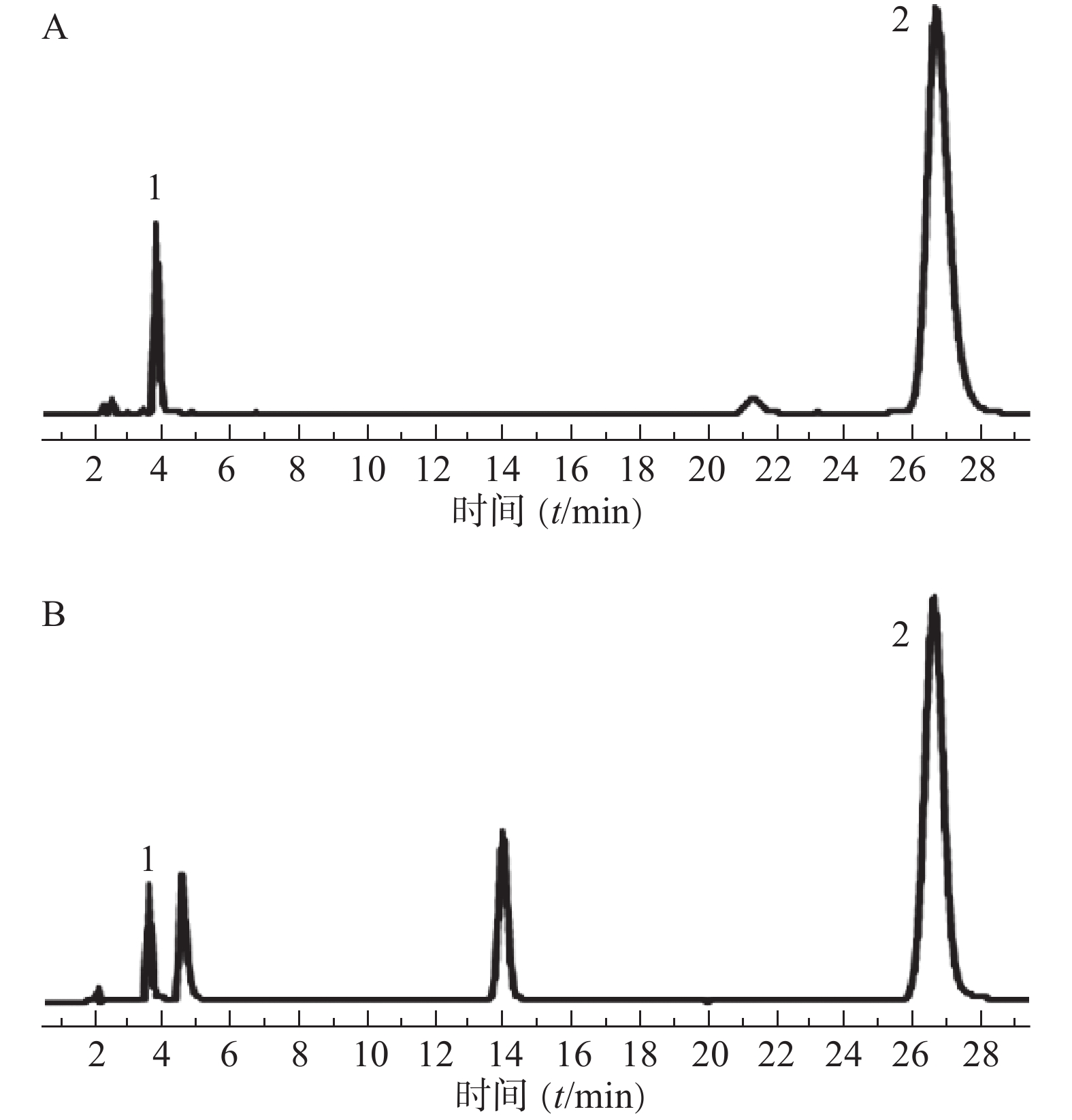
通过考察6份不同生物来源的空白血浆样品色谱图、空白血浆样品加入MHD对照品和内标的色谱图,以及临床实际用药后的患者血浆样品色谱图,以此反映方法的专属性。由图1可见,在本实验条件下,被测物MHD与内标的色谱峰分离良好,且血浆中的内源性物质不干扰测定。MHD和内标的保留时间分别为9.5 min和6.1 min。
3.2 标准曲线与线性范围
取上述浓度为2、5、10、20、30、40、50 μg/ml的血浆标准曲线样品按“2.3”项下方法处理。经HPLC法分析,以测得OXC的峰面积与内标峰面积之比(Y)作为纵坐标,以血浆MHD浓度(X)为横坐标,得到回归方程为:Y=0.047 1X+0.022 2(r=0.998 6)。线性范围:根据标准曲线,MHD血药浓度在2~50 μg/ml范围内线性关系良好,其定量下限浓度为2 μg/ml。
3.3 日内、日间精密度和准确度
配制定量下限、低、中、高(2、5、15、40 μg/ml)4种浓度的QC样品各6个,按“2.3”项下方法处理后测定,连续测定3 d,以当天的标准曲线计算QC样品的测定浓度,计算日内、日间精密度以及准确度。经测定,MHD的日内、日间精密度RSD均小于15%,准确度在95.57%~100.59%之间,均符合生物样品的测定要求,结果见表1。
表 1 单羟基卡马西平日内、日间精密度和准确度(n=6)理论浓度
(μg/ml)实测浓度
(μg/ml)RSD(%) RE(%) 日内精密度 日间精密度 2 1.85±0.16 8.64 12.21 −3.63 5 4.93±0.24 4.86 7.68 −4.43 15 14.32±0.37 6.86 6.16 −3.11 40 41.80±1.26 3.03 5.33 0.59 3.4 提取回收率
配制低、中、高(5、15、40 μg/ml)3种浓度的QC样品各6个,按“2.3”项下方法处理。同时另取18份空白血浆,除了不加系列对照品溶液和内标外,按“2.3”项下方法处理,在获得的上清液中加入MHD和内标溶液至相应浓度。进样分析,以每一浓度中2种不同处理方法的峰面积比值计算提取回收率。经测定,本法中MHD的平均提取回收率在89.62%~95.32%之间;内标的平均提取回收率为98.76%,符合生物学样品的分析要求,结果见表2。
表 2 单羟基卡马西平、MHD和内标提取回收率试验结果(n=6)化合物 浓度(μg/ml) 提取回收率(%) MHD 5 89.62±4.82 15 94.67±6.76 40 95.32±4.90 内标 140 98.76±5.92 3.5 稳定性试验
3.5.1 室温稳定性试验
取低、中、高(5、15、40 μg/ml)3种浓度的QC样品各5份,测定即时血药浓度,并在室温条件下放置4 h和10 h后测定样品血药浓度,求得RSD和RE值。经测定MHD血浆样品在室温下放置10 h后仍稳定,RSD均小于4.47%,RE值在1.50%~2.98%之间,结果见表3。
表 3 奥卡西平代谢产物单羟基卡马西平稳定性试验结果 (n=5)储存条件 理论浓度(μg/ml) 实测浓度(μg/ml) RSD(%) RE(%) 室温10 h 5 5.15±0.19 3.60 2.98 15 15.39±0.69 4.47 2.62 40 40.60±0.40 0.98 1.50 冻融3次 5 5.47±0.15 2.83 9.41 15 15.79±0.32 2.06 5.24 40 40.75±1.10 2.71 1.86 处理后36 h 5 5.39±0.27 5.09 7.74 15 15.66±0.58 3.70 4.39 40 39.46±1.80 4.57 −1.34 −20 ℃,30 d 5 5.16±0.23 4.39 3.19 15 14.62±0.39 2.64 −2.53 40 40.37±0.58 1.44 0.93 3.5.2 冻融稳定性试验
取低、中、高(5、15、40 μg/ml)3种浓度的QC样品各5份,测定即时血药浓度,并于−20 ℃冰箱中冷冻保存24 h后室温下解冻1 h后测定,反复冻融3次,求得RSD和RE值。经测定MHD血浆样品反复冻融3次后仍能保持稳定,RSD均小于2.83%,RE值在1.86%~9.41%之间,结果见表3。
3.5.3 处理后的血浆样品在自动进样器中储存的稳定性试验
取低、中、高3个浓度水平的血浆QC样品(5、15、40 μg/ml)各5份,测定即时血药浓度,然后放置在自动进样器内12 h、36 h后再次测定,求得RSD和RE值。经测定处理后的MHD血浆样品在进样器内放置36 h仍能保持稳定,RSD均小于5.09%,RE值在−1.34%~7.74%之间,结果见表3。
3.5.4 长期稳定性试验
取低、中、高3个浓度水平的血浆质控样品(5、15、40 μg/ml)各5份,测定即时血药浓度,并置于−20 ℃冰箱中冻存30 d后取出解冻后测定,求得RSD和RE值。经测定MHD血浆样品在−20 ℃冰箱中冻存30 d后仍能保持稳定,RSD均小于4.39%,RE值在−2.53%~3.19%之间,结果见表3。
4. 讨论
目前,有关MHD的检测方法的文献很多,其中,高效液相色谱法和高效液相色谱-质谱联用法都有报道,后者虽有灵敏度高、专属性强的特点,但其仪器昂贵,且需专业人员进行操作,很难在大部分的医疗机构普及[13-15]。另外,国内外文献报道中多使用固液萃取法或液液萃取法进行血样的前处理,但这种处理过程相对复杂、耗时,且经济成本较高[11, 16]。本方法采用甲醇沉淀蛋白进行血样的前处理,建立了HPLC法测定人血浆中MHD血药浓度的方法,整个过程操作简单、快速,样品分析时间较短,适用于临床大量样品的连续检测。
文献报道的流动相有乙腈-10 mmol/L磷酸二氢钾溶液(33∶67,V/V)[12]、水-乙腈(65∶35,V/V)[17]、水-甲醇-乙腈(64∶30∶6,V/V/V)[18]等。本方法采用了水-乙腈,按不同的配比进行试验,发现当水-乙腈的比例为80∶20时,色谱峰的峰形、出峰时间及分离度最佳。文献采用卡马西平[17]、苯巴比妥[19]和奥硝唑[20]等作为内标,本研究通过筛选发现奥硝唑的保留时间为6.1 min,不仅与MHD的保留时间相近,又能与其有很好的分离,且其性质稳定,满足内标的要求。
本实验建立的测定人血浆中OXC活性代谢产物MHD的HPLC法,MHD线性回归方程中的r=0.998 6,说明血药浓度在2~50 μg/ml范围内具有良好的线性关系,日内、日间精密度RSD均小于15%,准确度在95.57%~100.59%之间,MHD及内标的平均提取回收率在89.62%~98.76%之间。血浆样品的稳定性试验证明,在室温放置10 h、反复冻融、处理后放置进样器36 h以及低温保存30 d的情况下,样品未见明显降解,仍能保持稳定。本研究建立的HPLC法操作快速简单,精密度、回收率高,稳定性好,专属性强,不受血浆中内源性物质的干扰,结果准确可靠,且灵敏度高,适用于奥卡西平临床血药浓度的监测。
目前癫痫治疗主要以药物治疗为主,奥卡西平是第二代抗癫痫药物,我国诸多癫痫病专家也建议将其作为癫痫部分性发作和全面强直阵挛发作的首选药物[21]。但奥卡西平使用过程中可能出现瘙痒、荨麻疹、血管性水肿等超敏反应,包括Stevens Johnson综合征中毒性表皮坏死松解症[22]等,还可引起低钠血症、头晕、胃肠道不适等不良反应,有文献报道,其疗效及不良反应可能与血药浓度密切相关[23],因此开展奥卡西平血药浓度的测定,能提高药物治疗的疗效,同时可以有效避免或减少可能产生的药物不良反应,提高癫痫患者服药的依从性。本研究建立了测定人血浆中MHD血药浓度的方法,应用于临床,为临床个体化给药提供依据,值得临床推广使用。
-
表 1 地塞米松磷酸钠和克霉唑的线性关系考察
成分 回归方程 r 线性范围(μg/ml) 地塞米松磷酸钠 Y=34.961C+27.986 0.999 9 0.482 0~16.328 0 克霉唑 Y=32.366C+24.092 0.999 8 5.014 5~200.580 0 表 2 口腔溃疡膜中地塞米松磷酸钠和克霉唑的含量测定结果(n=3,
$\bar x$ ±s)批号 含量[标示量(%)] 地塞米松磷酸钠 克霉唑 190919 76.600 0±0.005 2 86.800 0±0.011 3 190923 85.900 0±0.011 5 99.100 0±0.025 9 190926 74.900 0±0.043 7 85.700 0 ±0.067 6 表 3 不同溶剂对口腔溃疡膜有效成分提取率的影响[n=3,实测值/标示量(%)]
提取方法 地塞米松磷酸钠 克霉唑 甲醇超声提取 67.46 74.49 71.58 79.06 73.09 72.64 水超声提取 108.29 101.28 104.08 101.03 105.88 103.38 70%甲醇超声提取 104.27 95.00 109.52 100.52 106.89 103.54 -
[1] FITZPATRICK S G, COHEN D M, CLARK A N. Ulcerated lesions of the oral mucosa: clinical and histologic review[J]. Head Neck Pathol,2019,13(1):91-102. doi: 10.1007/s12105-018-0981-8 [2] GIANNETTI L, MURRI DELLO DIAGO A, LO MUZIO L. Recurrent aphtous stomatitis[J]. Minerva Stomatol,2018,67(3):125-128. [3] GAGINI T, BORBA-SANTOS L P, MESSIAS RODRIGUES A, et al. Clotrimazole is highly effective <italic>in vitro</italic> against feline <italic>Sporothrix brasiliensis</italic> isolates[J]. J Med Microbiol,2017,66(11):1573-1580. doi: 10.1099/jmm.0.000608 [4] 王治国, 程军. 口腔溃疡局部用药应注意的问题[J]. 人民军医, 2017, 60(12):1227-1228, 1232. [5] 唐蕾, 江春霞, 朴淑娟, 等. 用HPLC法同时测定口腔溃疡膜中克霉唑和地塞米松磷酸钠的含量[J]. 药学服务与研究, 2016, 16(6):457-459. [6] OHNISHI A, HASHIMOTO K, OZONO E, et al. Anaphylaxis to carboxymethylcellulose: add food additives to the list of elicitors[J]. Pediatrics,2019,143(3):e20181180. doi: 10.1542/peds.2018-1180 -





 下载:
下载:
 下载:
下载:



