-
近年来,我国高血脂、肥胖症以及代谢综合征等疾病的患病人数不断增加,非酒精性脂肪肝患病率已呈现上升势头[1]。非酒精性脂肪肝(NAFLD)是一种非酒精造成的肝组织病理学改变的代谢应激相关性疾病[2]。主要临床表现为不同程度的乏力,伴随血清肝功能指标升高,严重时可导致肝硬化,威胁着患者生命健康。目前临床治疗NAFLD有了新的发展,新型药物逐渐出现,但是,患者的临床疗效以及相关肝功能的恢复情况有待进一步研究[3]。国内研究表明[4, 5],硫普罗宁联合谷胱甘肽治疗NAFLD患者,可明显改善血清肝功能,缓解症状,对于非酒精性脂肪肝的治疗具有一定临床意义。
-
自2018年3月至2019年9月,选取我院收治的非酒精性脂肪肝患者84例,随机分为对照组和观察组,每组42人,其中对照组男28例,女14例,平均年龄(51.36±6.42)岁,分级:轻度7例,中度28例,重度7例,合并高脂血症19例、高血压13例、2型糖尿病8例;观察组男26例,女16例,平均年龄(52.17±7.02)岁,分级:轻度5例,中度29例,重度8例,合并高脂血症20例、高血压11例、2型糖尿病11例。两组患者在性别、年龄、分级、合并症等基线资料差异不显著(P>0.05,表1),具有可比性。
表 1 两组患者基本资料比较
组别 例数 性别 平均年龄/岁 分级 合并症 男 女 轻度 中度 重度 高脂血症 高血压 2型糖尿病 对照组 42 28 14 51.36±6.42 7 28 7 19 13 8 观察组 42 26 16 52.17±7.02 5 29 8 20 11 11 t/χ2 0.21 0.55 0.42 0.62 P 0.65 0.58 0.81 0.73 -
诊断标准:非酒精性脂肪肝诊断参照《中华医学会肝脏病学分会脂肪肝和酒精性肝病学组2010年制定的NAFLD》[6]诊断标准。
纳入标准:①符合非酒精性脂肪肝诊断标准;②25~65岁;③患者近期均未服用保护肝脏类药物;④患者均接受回访,并配合开展工作;⑤本医院伦理委员会通过该项研究。排除标准:①患者年龄<25岁或>65岁者;②酒精性或者病毒性肝炎患者;③存在心脏、肝脏、肾脏等严重疾病的患者;④不接受回访,或者不能配合临床治疗的患者;⑤基本临床资料不全者。
-
两组患者均予以开展适量性的体育锻炼和低脂饮食,对照组给予硫普罗宁(江苏迪赛诺制药有限公司,批准文号:国药准字H20055040)治疗,用法如下:0.2 g/次,3次/d。观察组在对照组的基础上加用谷胱甘肽(山东金城生物药业有限公司,批准文号:国药准字H20123300)治疗,用法如下:1.2 g/次,3次/d。所有患者治疗30 d为一疗程,治疗3疗程。
-
采用全自动生化分析仪测定两组患者肝功能指标[谷草转氨酶(AST)、谷丙转氨酶(ALT)、谷氨酰转移酶(GGT)]和血脂水平;采用夹心酶联免疫吸附试验法检测患者肝纤维化指标:Ⅲ型前胶原(PCⅢ)、Ⅳ型胶原(PCⅣ)、层黏蛋白(LN)。
-
统计学处理采用SPSS 25.0,t检验:计量资料,χ2检验:计数资料。P<0.05为差异显著,具有统计学意义。
-
经治疗,两组ALT、AST、GGT水平较治疗前明显下降(P<0.05),治疗后观察组ALT、AST、GGT水平低于对照组(P<0.05),存在统计学差异,见表2。
表 2 两组患者治疗前后肝功能指标比较(U/L)
组别 例数 ALT AST GGT 对照组:治疗前 42 101.12±29.85 57.44±19.54 88.27±24.34 治疗后 51.28±18.24# 48.25±12.23# 56.34±18.72# 观察组:治疗前 42 103.11±28.46 58.07±18.33 79.15±23.87 治疗后 38.24±20.13#* 41.13±11.87#* 42.26±16.32#* #P<0.05,与组内治疗前比较;*P<0.05,与对照组治疗后比较 -
治疗前,两组血清血脂(TC、TG、LDL-C)水平不存在差异,不具有统计学意义(P>0.05);治疗后观察组上述血清水平低于对照组(P<0.05),差异具有统计学意义,见表3。
表 3 两组患者治疗前后血脂水平比较(mmol/L)
组别 例数 TC TG LDL-C 对照组:治疗前 42 7.12±1.25 4.44±1.54 4.57±1.24 治疗后 4.52±1.24# 3.25±1.23# 3.15±1.12# 观察组:治疗前 42 7.06±1.46 4.37±1.33 4.61±1.23 治疗后 3.84±0.93#* 2.13±1.17#* 2.56±1.06#* #P<0.05,与组内治疗前比较;*P<0.05,与对照组治疗后比较 -
治疗组治疗后PCⅢ、PCⅣ、LN水平同对照组比较,存在显著差异(P<0.05),差异有统计学意义,见表4。
表 4 两组患者治疗前后肝纤维化指标比较(μg/L)
组别 例数 PCⅢ PCⅣ LN 对照组:治疗前 42 124.51±22.45 72.45±12.15 113.24±21.42 治疗后 103.71±21.42# 59.21±11.28# 97.26±19.23# 观察组:治疗前 42 125.26±23.17 72.52±13.21 114.17±22.31 治疗后 92.54±17.86#* 53.81±12.63#* 85.62±18.67#* #P<0.05,与组内治疗前比较;*P<0.05,与对照组治疗后比较 -
NAFLD是一种非长期饮酒所致,无明显肝损伤的临床病理综合征。其主要的特征是弥漫性肝细胞大泡性脂肪变[7]。流行病学调查显示,其发病率已超过病毒性以及酒精性引起的肝病。NAFLD主要包括脂肪性肝炎、单纯性脂肪肝、肝硬化三种类型[8]。目前关于NAFLD的发病机制临床上尚无明确,较为公认的就是“二次打击”学说,即由胰岛素抵抗和氧化应激、脂质过氧化、炎性细胞因子释放形成。如得不到及时治疗,最终可引发肝细胞癌[9]。因此,NAFLD及时有效治疗显得尤为必要。现有治疗方法上没有特效药,主要进行针对性的治疗,如调节血脂、缓解肝功能损伤等。
研究证实[10],硫普罗宁、谷光甘肽片等是近年来可明显缓解NAFLD患者病情,改善肝功能的药物。硫普罗宁是一类含游离巯基的甘氨酸衍生物。该药物可以结合自由基,进而将自由基清除,另外可以升高肝细胞内线粒体ATP酶的活性,增加肝细胞内线粒体ATP,保护线粒体某些巯基的功能,促进肝糖原的出现,并达到抑制脂质代谢的目的,最终改善肝细胞的功能和结构,修复肝细胞以及再生;其次参与调节肝细胞中糖、脂肪、蛋白质的代谢,转化多余的脂肪,将积累在肝脏的三酰甘油清理出去;最后可以把肝细胞内谷胱甘肽维持在一定水平,实现抑制肝细胞内脂质的转化。硫普罗宁被临床上广泛应用于治疗肝病,具有效果显著、不良反应小的优势。董晋钢等[11]研究证实,硫普罗宁可明显降低酒精性肝病患者血清ALT、AST、TC、TG水平以及血清PCⅢ、PCⅣ、LN等水平,疗效较好,且安全性高。谷胱甘肽是一种可中和氧自由基的甘油醛磷酸脱氢酶以及乙二醛酶和磷酸丙糖脱氢酶辅基,通过参与机体内糖、脂质、蛋白质的代谢,减少脂质的过氧化和应激作用;另外可有效抑制和中和氧自由基,减少机体产生氧自由基,从而保护肝细胞膜及促进肝功能恢复[12]。刘俊英等[13]研究显示,谷胱甘肽可明显降低纤维化大鼠肝组织RGN mRNA相对表达量及蛋白表达相对表达量,纤维化明显减轻,提示该药物可能在肝纤维化发生发展过程中起重要作用。上述两种药物联合使用,可减轻脂肪肝和纤维化程度,有效改善肝功能指标,促进肝功能恢复,且安全可靠。本研究发现经治疗,两组ALT、AST、GGT水平较治疗前明显下降,观察组治疗后,ALT、AST、GGT水平明显低于对照组,差异具有统计学意义;治疗后观察组血清TC、TG、LDL水平明显低于对照组,差异具有统计学意义;治疗组患者PCⅢ、PCⅣ、LN水平同对照组比较,均显著降低,同国内外研究结果基本一致[14-15]。
综上所述,应用硫普罗宁联合谷胱甘肽治疗非酒精性脂肪肝,可促进肝功能的恢复,降低血脂水平,降低肝纤维化程度,值得临床推广。
Effect of tiopronin combined with glutathione on biochemical indicators of patients with non-alcoholic fatty liver
-
摘要:
目的 观察硫普罗宁联合谷胱甘肽对非酒精性脂肪肝患者谷丙转氨酶(ALT)、谷草转氨酶(AST)、谷氨酰转移酶(GGT)、血脂和层黏蛋白(LN)水平的影响。 方法 选择我院从2018年3月至2019年9月收治的非酒精性脂肪肝患者84例,随机分为对照组和观察组,各42例。对照组给予硫普罗宁进行治疗,观察组在此基础上联合谷胱甘肽进行治疗。记录并比较治疗前后患者的ALT、AST、GGT、LN和血脂水平。 结果 经治疗,ALT、AST、GGT水平较治疗前明显下降(P<0.05),治疗后观察组ALT、AST、GGT水平低于对照组,差异有统计学意义(P<0.05);治疗前,两组血清的总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白胆固醇(LDL-C)没有统计学差异(P>0.05);治疗后观察组上述血清水平低于对照组(P<0.05),差异有统计学意义;观察组治疗后血清Ⅲ型前胶原(PCⅢ)、Ⅳ型胶原(PCⅣ)、LN水平均低于对照组,差异显著,具有统计学意义(P<0.05)。 结论 应用硫普罗宁联合谷胱甘肽治疗非酒精性脂肪肝,能促进肝功能的恢复,降低TC、TG、LDL的浓度,值得临床推广。 Abstract:Objective To observe the effect of tiopronin combined with glutathione on the levels of alanine aminotransferase (ALT), aspartate aminotransferase (AST), glutamyltransferase (GGT),blood fat and laminin (LN) in patients with non-alcoholic fatty liver. Methods A total of 84 non-alcoholic fatty liver patients admitted to our hospital from March 2018 to September 2019 were selected and randomly divided into control group and observation group, with 42 cases in each group. The control group was treated with tiopronin, and the observation group was treated with glutathione and tiopronin. The levels of ALT, AST, GGT and blood fat were recorded and compared before and after treatment. Results After treatment, the levels of ALT, AST and GGT in the two groups were significantly lower than before treatment (P<0.05). After treatment, the levels of ALT, AST, and GGT in the observation group were different from those in the control group, which was statistically significant (P<0.05). Before treatment, there was no difference in serum TC, TG, and LDL levels between the two groups, which was not statistically significant (P>0.05). The above-mentioned serum levels of the observation group after treatment were lower than those in the control group, and there was a difference, which was statistically significant (P<0.05); the levels of PCⅢ, PCⅣ, and LN in the treatment group after treatment were significantly lower than those of the control group. The difference was statistically significant (P<0.05). Conclusion The application of tiopronin combined with glutathione in the treatment of non-alcoholic fatty liver can promote the recovery of liver function and reduce the concentrations of TC, TG and LDL, which is worthy of clinical promotion. -
Key words:
- tiopronin /
- glutathione /
- non-alcoholic fatty liver /
- LN /
- ALT /
- AST
-
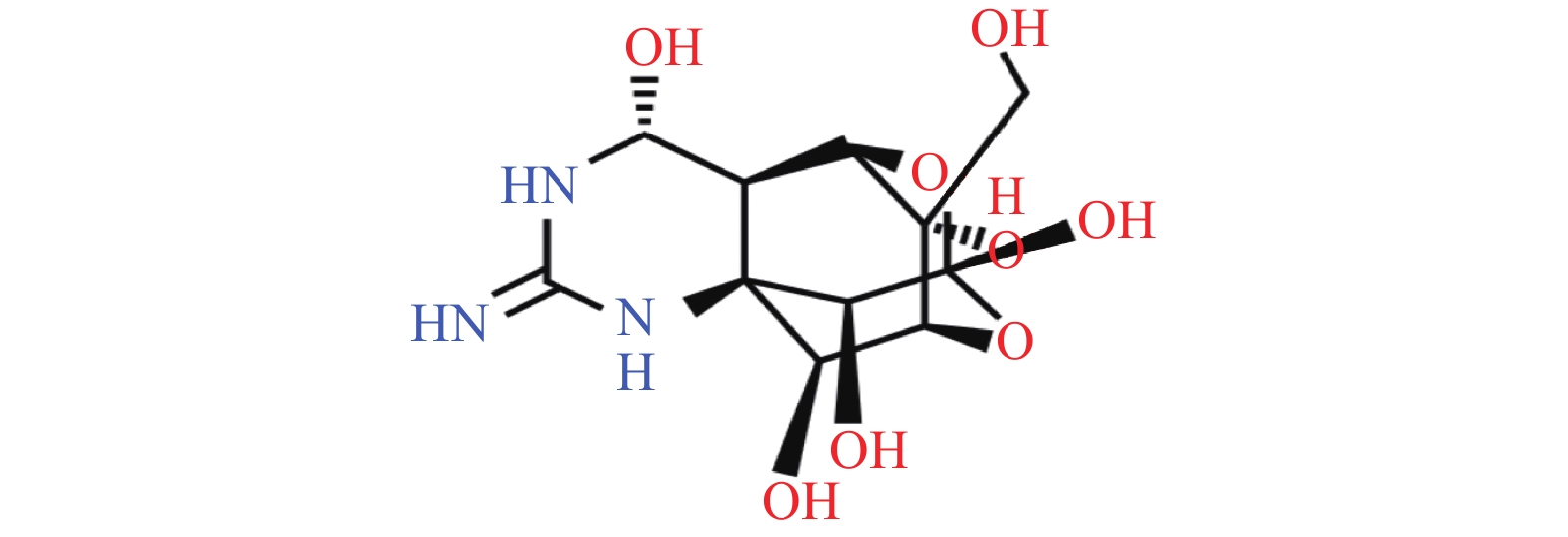
河豚毒素(TTX)属于氨基全氢化喹唑啉化合物,分子式为C11H17O8N3,分子量为319。其分子结构类似于生物碱[1],呈独特的笼形,如图1。河豚毒素粗品为黄褐色粉末,纯品为白色晶体,呈弱碱性,容易潮解,微溶于水溶液,易溶于无机酸水溶液,且在弱酸条件下稳定;对于热不敏感,但在高温下毒性会增强,强酸强碱条件下其结构可被破坏[2]。
河豚毒素是一种高效的神经类毒素,由于能够特异性的阻断Na+离子通道,进而产生麻痹作用,因此低浓度的河豚毒素被认为是一种优良的神经类候选药物,一直受到科研人员尤其是新药研发人员的关注[3]。目前已有将河豚毒素作为止痛药[4-5]和成瘾戒断药[6]的相关探索和研究。由于河豚毒素在药学领域有着广阔前景,关于其药学应用的研究报道逐年增多,但大多集中在分析方法[7]、药理机制[8]或药物载体研究[9],对其可成药性的相关研究报道较少。本文按照新药研发要求,建立高效液相反相离子对色谱法,对河豚毒素在不同溶剂中的溶解性和不同pH环境中的稳定性进行考察,为河豚毒素的处方前研究积累数据,为其进一步临床应用提供有力支撑。
1. 材料
1.1 仪器
LC-2030C高效液相色谱仪(日本岛津制作所);AL-104电子天平(METTLER TOLEDO,瑞士);数显pH计(sartorius,德国);紫外可见分光光度计(安捷伦科技(中国)有限公司);循环水式真空泵(上海豫康科教仪器设备有限公司);SECURA125-1CN型十万分之一电子天平(赛多利斯,德国);Arium@ mini 超纯水机(赛多利斯,德国)。
1.2 试药
河豚毒素原料药(中洋生物科技江苏有限公司,批号:20220089,含量88%);河豚毒素对照品(泰州康特生物工程有限公司,批号:201206,含量≥99%);磷酸、98%甲酸、柠檬酸、磷酸二氢钠、磷酸氢二钠、磷酸二氢钾、磷酸氢二钾、氢氧化钠、庚烷磺酸钠、磷酸二氢铵、乙酸铵、盐酸、30% H2O2和冰醋酸均为分析纯试剂(国药集团化学试剂有限公司)。
2. 方法
2.1 色谱条件
色谱柱为Shim-pack GISI C18-AQ(4.6×250 mm,5 μm);流动相为5 mmol/L庚烷磺酸钠-25 mmol/L磷酸二氢铵,等度洗脱;进样量为10 μl;柱温:25 ℃;流速1 ml/min;检测波长为196 nm;检测时长为40 min。
2.2 对照品储备液的制备
取TTX对照品适量,精密称定,用0.1%磷酸溶液溶解并稀释制成浓度为1.0 mg/ml的TTX对照品储备液。
2.3 供试品储备液的制备
取TTX原料药适量,精密称定,用0.1%磷酸溶液溶解并稀释制成浓度为1.0 mg/ml的供试品储备液。
2.4 溶解度试验测试溶液的制备
按照《中国药典》(2020版)四部通则8004缓冲液配制方法,配制pH值分别为3.5、4.5、5.0、6.5、7.0、7.4、8.0的缓冲液[10]。称取研成细粉的TTX原料药各2 mg,分别置于4 ml不同pH值的缓冲液(25±2 ℃)中,30 min内每隔5 min强力振摇30 s,观察溶解情况,如无目视可见颗粒,视为完全溶解。如完全溶解则继续加入研成细粉的TTX原料药,同法操作直至饱和,取适量经滤膜滤过,作为溶解度试验测试溶液。
2.5 强酸与强碱破坏试验测试溶液的制备
取研成细粉的TTX原料药约1 mg,置于10 ml容量瓶中,分别用0.1 mol/L盐酸和0.1 mol/L氢氧化钠溶液溶解并定容,置于70 ℃下反应20 min。精密量取各反应溶液适量,冷却至室温,分别加入对应体积的0.1 mol/L氢氧化钠或0.1 mol/L盐酸进行中和并终止反应。取适量样品经滤膜过滤后作为强酸与强碱破坏试验测试溶液。
2.6 氧化破坏试验测试溶液的制备
取研成细粉的TTX原料药约1 mg,置于10 ml容量瓶中,加入30% H2O2溶液溶解定容后,室温反应10 min。精密量取反应溶液适量,经滤膜过滤,作为氧化破坏试验测试溶液。
2.7 稳定性试验测试溶液的制备
取研成细粉的TTX各适量,精密称定,分别用PBS缓冲液(pH值=7.4)、0.1%甲酸溶液、0.1%柠檬酸溶液溶解,并稀释制成浓度为0.1 mg/ml的TTX溶液,然后分别置于4 ℃、25 ℃、37 ℃中储存,在第1、2、3、5、7、14、21、28 d各取适量经滤膜过滤,作为温度适应性测试溶液。
3. 结果
3.1 方法学验证结果
3.1.1 系统适用性
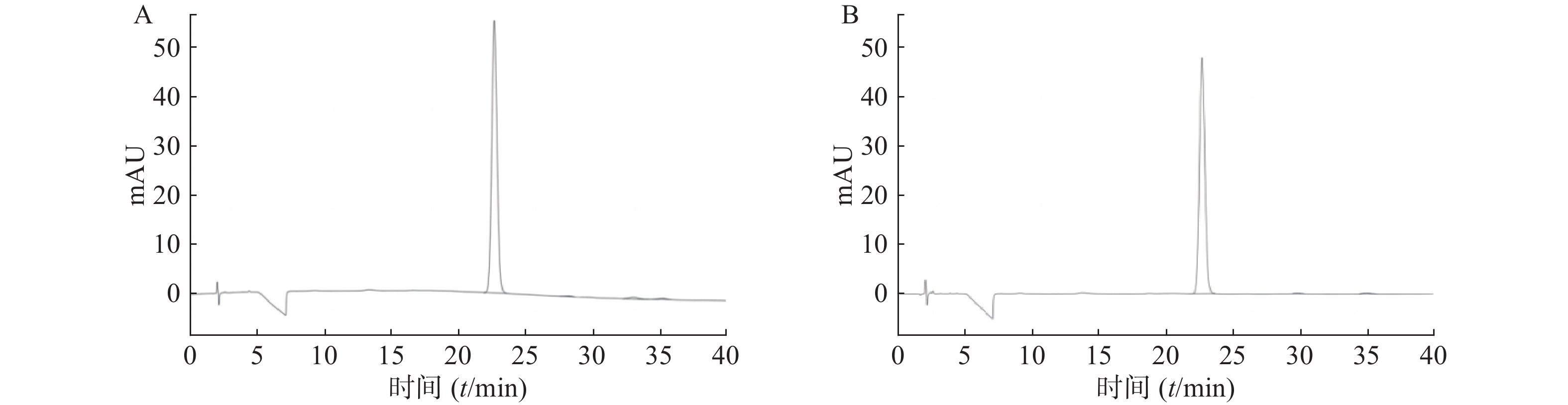
分别将对照品储备液及供试品储备液用0.1%磷酸溶液稀释至0.1 mg/ml,作为对照品溶液和供试品溶液,按“2.1”项进行测试。如图2所示,TTX的保留时间为22.665 min。理论板数为14 501,供试品溶液中主峰与邻峰的分离度为6.4。结果表明,此色谱条件可以满足TTX相关测试要求。
3.1.2 标准曲线
取对照品储备液,用0.1%磷酸溶液配制浓度为4、10、20、40、80 μg/ml的TTX对照品测试溶液,按“2.1”项进行测试。以浓度为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,得回归方程为Y=12 601.2X–2 263.69(r=0.999 9)。结果表明,TTX的浓度与峰面积在测试范围内呈良好线性关系。
3.1.3 准确度与精密度
取对照品储备液,用0.1%磷酸溶液分别稀释至10、20、40 μg/ml的溶液各3份,按“2.1”项进行测试,计算其含量的平均值为101.000%,RSD为0.60%,表明该方法准确度良好,满足测试要求。
3.1.4 进样重复性及稳定性
取供试品溶液,按“2.1”项重复测试6次,计算得到的RSD为0.17%,表明该方法重复性良好。室温分别放置0、2、4、6、8、10、12、24、48 h后按“2.1”进行测试。计算得到的RSD为1.48%,表明供试品溶液在48 h内稳定性良好。
3.2 溶解度及稳定性考察结果
3.2.1 溶解度考察结果
由表1结果可看出,TTX几乎不溶于碱性水溶液,但溶解度随着pH值降低而逐渐增大,易溶于pH值为3.5的酸性水溶液。
表 1 TTX在不同pH值水溶液中的溶解度pH值 3.5 4.5 5.0 6.5 7.0 7.4 8.0 $ \bar{\rm{x}} $(mg/ml) 264.63 31.35 4.64 1.02 0.47 0.21 0.05 SD(mg/ml) 5.54 0.75 0.08 0.046 0.015 0.002 7 0.001 3.2.2 破坏试验结果
实验结果表明,强碱对TTX的破坏能力最强,在0.1mol/L氢氧化钠溶液中、70 ℃条件下反应20 min后,TTX被完全降解。强酸对TTX的破坏能力次之,TTX在70 ℃、0.1mol/L HCl溶液中反应20 min后的降解率为60.78%;氧化对TTX的破坏能力相对最弱,在30% H2O2溶液中反应20 min后的降解率为17.06%。
3.2.3 稳定性考察结果
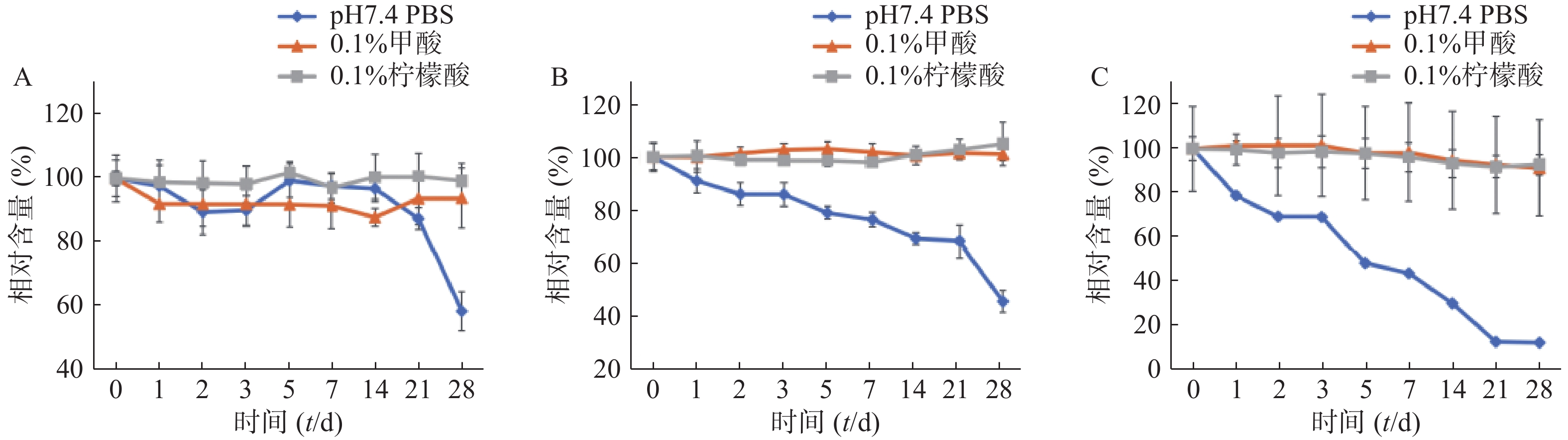
不同介质、不同温度条件下TTX稳定性试验结果见图3。当溶剂为pH值=7.4的PBS溶液时,不同温度下TTX均表现出降解趋势,在25 ℃与37 ℃条件下保存28 d的TTX溶液降解率均超过50%,在37 ℃时PBS溶液中的TTX降解率更高达88.07±0.27%,提示在后续剂型研究中,需注意TTX在体外释放液中的稳定性。以0.1%甲酸溶液或0.1%柠檬酸溶液为溶剂的TTX溶液则较为稳定,在25 ℃和37 ℃下保存28 d含量均未表现出显著性变化。
4. 讨论
TTX作为一种具有广泛应用前景的潜在镇痛药物,其在药理和作用机制方面的相关研究已有较多报道[11-13],但对于其理化性质和成药性研究的报道极少。本研究建立了高效液相反相离子对色谱法,测定TTX在不同溶剂中的溶解性,并考察温度、溶剂pH值和氧化剂对其稳定性的影响。实验结果表明TTX在酸性条件下具有较高的溶解度,前期试验还表明TTX不溶于乙醇,二氯甲烷等有机溶剂。稳定性试验结果显示TTX在强碱溶液中较不稳定,实验条件下20 min即被强碱全部降解,而在酸性条件、氧化环境中较为稳定。不同温度稳定性试验结果同样显示,TTX在0.1%甲酸或柠檬酸溶液中4周内稳定性均良好;而在pH值=7.4 PBS中降解较为迅速,即使在4 ℃条件下,pH值=7.4 PBS中28 d的降解率仍然接近50%,37 ℃条件下28 d降解率接近90%。研究结果可为TTX处方设计及制备工艺提供实验依据,并提示研究者在开展TTX剂型研究和体外释放研究时应重点关注其稳定性和降解情况。
-
表 1 两组患者基本资料比较
组别 例数 性别 平均年龄/岁 分级 合并症 男 女 轻度 中度 重度 高脂血症 高血压 2型糖尿病 对照组 42 28 14 51.36±6.42 7 28 7 19 13 8 观察组 42 26 16 52.17±7.02 5 29 8 20 11 11 t/χ2 0.21 0.55 0.42 0.62 P 0.65 0.58 0.81 0.73 表 2 两组患者治疗前后肝功能指标比较(U/L)
组别 例数 ALT AST GGT 对照组:治疗前 42 101.12±29.85 57.44±19.54 88.27±24.34 治疗后 51.28±18.24# 48.25±12.23# 56.34±18.72# 观察组:治疗前 42 103.11±28.46 58.07±18.33 79.15±23.87 治疗后 38.24±20.13#* 41.13±11.87#* 42.26±16.32#* #P<0.05,与组内治疗前比较;*P<0.05,与对照组治疗后比较 表 3 两组患者治疗前后血脂水平比较(mmol/L)
组别 例数 TC TG LDL-C 对照组:治疗前 42 7.12±1.25 4.44±1.54 4.57±1.24 治疗后 4.52±1.24# 3.25±1.23# 3.15±1.12# 观察组:治疗前 42 7.06±1.46 4.37±1.33 4.61±1.23 治疗后 3.84±0.93#* 2.13±1.17#* 2.56±1.06#* #P<0.05,与组内治疗前比较;*P<0.05,与对照组治疗后比较 表 4 两组患者治疗前后肝纤维化指标比较(μg/L)
组别 例数 PCⅢ PCⅣ LN 对照组:治疗前 42 124.51±22.45 72.45±12.15 113.24±21.42 治疗后 103.71±21.42# 59.21±11.28# 97.26±19.23# 观察组:治疗前 42 125.26±23.17 72.52±13.21 114.17±22.31 治疗后 92.54±17.86#* 53.81±12.63#* 85.62±18.67#* #P<0.05,与组内治疗前比较;*P<0.05,与对照组治疗后比较 -
[1] 吴挺丰, 廖献花, 钟碧慧. 中国部分地区非酒精性脂肪肝病的流行情况[J]. 临床肝胆病杂志, 2020, 36(6):1370-1373. doi: 10.3969/j.issn.1001-5256.2020.06.039 [2] 郭宏雅, 付远飞, 刘惠婷, 等. 血府逐瘀汤与加味二陈汤对小鼠非酒精性脂肪肝的作用比较[J]. 中国实验方剂学杂志, 2020, 26(12):71-77. [3] 唐标, 尹抗抗. 降脂理肝汤对高脂饮食诱导的非酒精性脂肪肝病大鼠非经典的细胞焦亡途径的影响[J]. 中国免疫学杂志, 2020, 36(3):267-271. doi: 10.3969/j.issn.1000-484X.2020.03.003 [4] 叶长江, 叶志伟. 中药联合硫普罗宁与多烯磷脂酰胆碱治疗非酒精性脂肪肝40例[J]. 中西医结合肝病杂志, 2016, 26(5):302-304. [5] MO'MEN Y S, HUSSEIN R M, KANDEIL M A. A novel chemoprotective effect of tiopronin against diethylnitrosamine-induced hepatocellular carcinoma in rats: Role of ASK1/P38 MAPK-P53 signalling cascade[J]. Clin Exp Pharmacol Physiol,2020,47(2):322-332. doi: 10.1111/1440-1681.13204 [6] 韩静, 李亚伟, 刘艳萍, 等. 银杏黄酮对非酒精性脂肪肝大鼠肝脏组织中脂质和炎症因子水平的影响[J]. 郑州大学学报(医学版), 2020, 55(1):100-103. [7] 何剑, 阳学风. 甘草酸二铵肠溶胶囊联合硫普罗宁肠溶片治疗非酒精性脂肪肝的临床研究[J]. 中国临床药理学杂志, 2019, 35(9):833-835. [8] ROMUALDO G R, SILVA E D A, DA SILVA T C, et al. Burdock (Arctium lappaL.) root attenuates preneoplastic lesion development in a diet and thioacetamide-induced model of steatohepatitis-associated hepatocarcinogenesis[J]. Environ Toxicol,2020,35(4):518-527. doi: 10.1002/tox.22887 [9] QI J, KIM J W, ZHOU Z X, et al. Ferroptosis affects the progression of nonalcoholic steatohepatitis via the modulation of lipid peroxidation-mediated cell death in mice[J]. Am J Pathol,2020,190(1):68-81. doi: 10.1016/j.ajpath.2019.09.011 [10] 吴敏, 吴克芹. 还原型谷胱甘肽与硫普罗宁治疗药源性肝病的疗效研究[J]. 中国现代药物应用, 2020, 14(8):159-160. [11] 董晋钢, 董晋瑛. 美他多辛联合硫普罗宁治疗酒精性肝病的疗效观察[J]. 中国药房, 2017, 28(8):1091-1094. doi: 10.6039/j.issn.1001-0408.2017.08.23 [12] YANG H, YANG T T, HENG C, et al. Quercetin improves nonalcoholic fatty liver by ameliorating inflammation, oxidative stress, and lipid metabolism in db/db mice[J]. Phytother Res,2019,33(12):3140-3152. doi: 10.1002/ptr.6486 [13] 刘俊英, 刘洋, 李涵, 等. 谷胱甘肽复方注射液对免疫性肝纤维化大鼠肝组织钙调素表达的影响[J]. 中华肝脏病杂志, 2019, 27(8):628-633. doi: 10.3760/cma.j.issn.1007-3418.2019.08.008 [14] 庞红全, 王刚, 杨帆, 等. 还原型谷胱甘肽联合自拟降脂方对酒精性脂肪肝患者血清酶及脂质过氧化水平的影响[J]. 解放军医药杂志, 2016, 28(7):78-81. doi: 10.3969/j.issn.2095-140X.2016.07.021 [15] VALACHOVA K, SVIK K, BIRO C, et al. Skin wound healing with composite biomembranes loaded by tiopronin or captopril[J]. J Biotechnol,2020,310:49-53. doi: 10.1016/j.jbiotec.2020.02.001 -





 下载:
下载:
 下载:
下载: 

