-
慢性肾小球肾炎又称慢性肾炎,是终末期肾病最主要的病因之一[1]。它以蛋白尿、血尿、高血压等为主要临床表现。治疗方法多以对症支持治疗或免疫抑制剂、激素为主 [2]。坎地沙坦酯是一种非肽类血管紧张素受体阻滞剂(ARB),目前在世界各地被广泛用作口服降压药,可有效的改善肾功能,减少24 h尿蛋白(24 h Upro)[3]。昆仙胶囊是一种中成药,因其具有类激素、免疫制剂等作用被广泛应用于临床,多用于风湿性关节炎、肾炎等疾病。据Meta分析报道,昆仙胶囊的不良反应包括生殖毒性、肝损害、肾功能障碍等,但不良反应率明显低于雷公藤片[4]。目前还未确定是否可以联合使用昆仙胶囊和ARB来改善原发性肾小球肾炎的治疗。本研究采用随机对照设计,观察昆仙胶囊联合坎地沙坦酯治疗慢性肾小球肾炎合并高血压患者的疗效及对血脂水平和炎症反应的影响。
-
2017年11月至2019年12月,我们招募了101名参与者,随机分配到观察组或对照组,对照组50例,观察者51例。患者的基线特征如表1所示,对照组和观察组的年龄、病程等特征均无统计学差异(P>0.05)。
表 1 两组患者一般资料比较
特征 对照组 观察组 n=50 n=51 年龄 45.74±9.75 44.92±9.68 男性,n(%) 29(58.00%) 31(60.78%) 病程(年) 4.64±2.07 4.12±1.63 SBP(mmHg) 154.24±8.45 151.98±7.98 DBP(mmHg) 95.40±4.46 96.69±5.27 24 h尿蛋白(g) 1.73±0.63 1.68±0.56 Scr(μmol/L) 148.01±20.49 149.76±21.05 BUN(mmol/L) 11.62±1.66 11.90±1.80 TG(mmol/L) 2.10±0.23 2.02±0.21 TC(mmol/L) 6.25±1.09 6.31±0.83 LDL-C(mmol/L) 4.21±1.08 4.26±0.89 HDL-C(mmol/L) 1.10±0.13 1.12±0.15 IL-6(pg/ml) 171.22±19.47 175.28±23.71 hs-CRP(mg/L) 3.58±0.78 3.57±0.74 纳入标准[5-6] :符合2010年第十一届全国中西医结合肾病学术会议制订的有关慢性肾小球肾炎的相关诊断标准;有蛋白尿等临床表现。收缩压(SBP)为140~180 mmHg,舒张压(DBP)为90~109 mmHg。
排除标准:糖尿病;过敏性紫癜性肾炎;系统性红斑狼疮肾炎;透析;肾移植;血压<90/60 mmHg;一直或最近(<1年)使用糖皮质激素、免疫抑制剂治疗;最近2周内有服用保护肾功能,降低胆固醇、三酰甘油、低密度脂蛋白胆固醇,升高高密度脂蛋白胆固醇,缓解炎症的其他中成药或汤剂的;在过去4周内,曾接受RAS阻滞剂治疗的患者;妊娠或哺乳期;大脑、肝脏、心血管或造血系统严重功能障碍,或其它可能影响患者生活的严重疾病;易过敏或已知对药物过敏;以及同期参加另一项临床研究的。
本院伦理委员会批准了该协议。所有参与者及其家属在接受任何与研究相关的程序之前都将签署书面知情同意书。参与者及其家属将有足够的时间阅读知情同意书,并在提供书面同意之前询问试验的细节。
-
常规治疗:2组均进行低盐低蛋白饮食、纠正水电解质失调和酸碱平衡紊乱、抗凝等常规治疗。对照组在常规治疗的基础上服用坎地沙坦酯(浙江永宁药业股份有限公司,国药准字H20050323,规格:0.8 mg /片),每次 8 mg, 每日服用1次。治疗组服用昆仙胶囊((广州白云山陈李济药厂有限公司生产,商品名:陈李济,批准文号:国药准字Z20060267,批号:K31010,规格:0.3 g/粒)和坎地沙坦酯。连服12周。如果患者出现过度低血压、慢性肾小球肾炎加重或临床重大不良事件,则停止治疗。治疗前后测量血压(BP)和心率,并进行实验室检查(血液和尿液分析)。饮食习惯不允许发生重大改变。
-
疗效评定标准[5-6]:显效:临床症状基本消失,血脂、肾功能等指标恢复正常,24 h尿蛋白定量<0.2 g,患者的收缩压/舒张压≤130/85 mmHg;有效:临床症状明显改善,肾功能、血脂等指标改善,24 h尿蛋白定量减少大于40%,收缩压/舒张压仍大于130/85 mmHg,收缩压下降15~30 mmHg;无效:临床症状、血脂、肾功能等指标及24 h尿蛋白定量无明显好转。总有效率=(显效+有效)/总例数×100%。
-
所有患者治疗前后的血压变化;取清洁中段尿,采用尿液干化学分析仪测24 h尿蛋白;采集空腹静脉血,离心后取血清检测血脂四项水平,及肾功能指标Scr和尿素氮(BUN)、炎症因子(IL-6、hs-CRP)水平。
-
安全指标将包括白细胞计数的减少、肝功能异常、高钾血症和其他不良事件。不良事件被记录下来,它们与研究药物的可能关联被归类为以下类别之一:相关的、可能不相关的和与研究药物无关的。与研究药物相关的、可能相关的和可能相关的事件被认为是药物不良反应。
-
所有分析均使用SAS 9.2软件进行。统计学显著性水平设为0.05。计量资料采用(
$\bar x $ ±s)表示,描述,组间或组内比较行t检验;计数资料行卡方检验。 -
治疗后,观察组和对照组的SBP、DBP均显著下降(P<0.05),且观察组显著低于对照组(P<0.05),见表2。
表 2 两组患者治疗前后血压变化(
$\bar x $ ± s )组别 SBP(mmHg) DBS(mmHg) 治疗前 治疗后 治疗前 治疗后 对照组 154.24±8.45 138.24±10.38* 95.40±4.46 84.02±4.71* 观察组 151.98±7.98 127.14±12.09*# 96.69±5.27 78.22±6.72*# *P<0.05,与同组治疗前比较;#P<0.05,与对照组治疗后比较。 -
治疗后,观察组和对照组肾功能指标(24 hUpro、BUN、Scr)均显著下降(P<0.05),且观察组显著低于对照组(P<0.05),见表3。
表 3 两组患者治疗前后24 Upro、BUN、Scr的变化(
$\bar x $ ±s )组别 24 Upro(g) Scr(μmol/L) BUN(mmol/L) 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 对照组 1.73±0.63 0.93±0.58* 148.01±20.49 105.01±18.32* 11.62±1.66 7.11±1.06* 观察组 1.68±0.56 0.71±0.13*# 149.76±21.05 92.76±15.37*# 11.90±1.80 6.29±0.96*# *P<0.05,与同组治疗前比较;#P<0.05,与对照组治疗后比较。 -
治疗12周后,观察组和对照组血脂指标TG、TC、LDL-C均显著下降(P<0.05),且观察组显著低于对照组(P<0.05),;两组血脂指数HDL-C显著升高,且观察组显著高于对照组(P<0.05),见表4。
表 4 治疗12周后血脂四项的变化(
$\bar x $ ±s )组别 TG(mmol/L) TC(mmol/L) LDL-C(mmol/L) HDL-C(mmol/L) 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 对照组 2.10±0.23 1.65±0.31* 6.25±0.78 5.47±0.59* 4.21±1.08 3.45±0.53* 1.10±0.13 1.31±0.16* 观察组 2.02±0.21 1.47±0.23*# 6.31±0.83 4.50±0.64*# 4.26±0.89 2.40±0.78*# 1.12±0.15 1.43±0.18*# *P<0.05,与同组治疗前比较;#P<0.05,与对照组治疗后比较。 -
治疗12周后,观察组和对照组炎症因子(IL-6、hs-CRP)均显著下降(P<0.05),且观察组显著低于对照组(P<0.05),见表5。
表 5 治疗12周后血炎症因子IL-6、hs-CRP的变化(
$\bar x $ ±s )组别 IL-6(pg/ml) Hs-CRP(mg/L) 治疗前 治疗后 治疗前 治疗后 对照组 171.22±19.47 115.22±15.31* 3.58±0.78 2.68±0.64* 观察组 175.28±23.71 93.28±15.48* 3.57±0.74 1.75±0.52* *P<0.05,与同组治疗前比较;#P<0.05,与对照组治疗后比较。 -
观察组的总有效率为96.1%(49/51),高于对照组82.0%(41/50),具有统计学意义(χ2=4.27,P=0.039)。且两组均无不良反应的发生,见表6。
表 6 两组患者临床疗效比较[n(%)]
组别 例数 显效 有效 无效 总有效(率) 对照组 50 16(32.0%) 25(50.0%) 9(18.0%) 41(82.0%) 观察组 51 29(56.9%) 20(39.2%) 2(3.9%) 49(96.1%)* *P<0.05,与对照组比较。 -
慢性肾小球肾炎与免疫介导的炎症性疾病相关,在终末期肾病中频繁发生,严重影响患者的生存。生物学和临床观察的结果表明,它以血尿、蛋白尿、动脉高血压为主要表现 [7-8]。多项研究发现慢性肾炎患者体内尿蛋白、Scr、BUN等肾功能指标升高的同时,伴随血脂异常,炎症因子hs-CRP和IL-6偏高[9-10], 与本临床观察的结果一致。
治疗慢性肾小球肾炎最为主要的目的是抑制或延缓肾功能的恶化。用于减缓疾病进展的方法是饮食控制和药物控制,常见的治疗药物有肾素-血管紧张素系统阻滞剂,包括血管紧张素转化酶抑制剂(ACEI)和ARBs[11]。与ACEI相比,ARB还可以作为由非ACE途径形成的Ang II的拮抗剂[12]。另一个优点是,与ACEI不同,ARB不影响缓激肽新陈代谢,这意味着这些药物作为不良反应与干咳的发生相关的频率要低得多[13-14]。在各种非糖尿病肾病中,ARBs可以减少24 h Upro,稳定了全身和肾脏的血压,防止肾脏疾病的发展 [15]。
而坎地沙坦酯是ARBs药物中的一种,作为一种降压药已在国际上获得了专家们的广泛认可。该药在多种高血压动物模型的实验结果中发现,其均有降压作用[16],同时也能有效的减少慢性肾小球肾炎患者的尿蛋白,除此之外,也能延缓肾小球硬化的进展,抑制肾小管间质纤维化改变[17]。Kurokawa等发现使用2、4、8 mg剂量的坎地沙坦酯治疗慢性肾小球肾炎12周时,8 mg的疗效最好。坎地沙坦酯可以显著地降低24 h Upro,改善肾功能(Scr和BUN在治疗后显著降低)[18]。用坎地沙坦酯治疗12周时收缩压和舒张压显著下降,这提示,血压的降低程度可能是坎地沙坦酯导致的尿蛋白排泄减少的原因之一[19]。由本临床观察发现坎地沙坦酯可以降血压、显著降低了24 hUpro、BUN、Scr、TG、TC、LDL-C及炎症因子IL-6和hs-CRP,并能显著上调HDL-C水平。但是昆仙胶囊联合坎地沙坦酯治疗的效果比单用坎地沙坦酯的效果更佳。
昆仙胶囊由昆明山海棠、淫羊藿、菟丝子、枸杞4种中药组成。其中昆明山海棠是最重要的成分,因为它的提取物含有雷公藤内酯醇,具有抗炎、免疫抑制等重要作用;淫羊藿苷是淫羊藿的主要提取物,有抗炎等作用;甜菜碱是枸杞子的重要提取物之一,有造血、保护肝脏等作用;黄酮类为菟丝子最重要的提取物,有护肝等作用[19]。以往的研究表明,昆仙胶囊可以下调慢性肾小球肾炎患者中的炎症因子,抑制炎症反应[20]。张宁等也发现昆仙胶囊能显著抑制炎症因子IL-6、hs-CRP的表达[21]。张楠[22]等发现昆仙胶囊用于治疗慢性肾小球炎症的总有效率高达90%,并且能显著降低Scr、ALT、ALB。
本研究在昆仙胶囊联合坎地沙坦酯治疗12周后,血压、蛋白尿、肾功能指标、炎症因子、血脂TG、TC、LDL-C显著降低,并且临床疗效总有效率为96.1%,而且这些指标明显优于单独使用坎地沙坦酯。除此之外,本研究并无明显不良反应,表明两者联合治疗慢性肾小球肾炎效果确切,安全可靠。
综上所述,慢性肾小球肾炎患者在常规治疗的同时加用昆仙胶囊联合坎地沙坦酯治疗可提高临床疗效,改善肾功能,调节血脂,减轻炎症反应。
Observation on the effect of Kunxian capsule combined with candesartan cilexetil in the treatment of chronic nephritis with hypertension
-
摘要:
目的 探讨昆仙胶囊联合坎地沙坦酯对慢性肾炎合并高血压患者的血压、肾功能、血脂及炎症因子的影响。 方法 选择2017年11月至2019年12月在本院收治的101名慢性肾小球肾炎患者,将患者随机分为观察组(51例)和对照组(50例)。对照组在常规治疗的基础上使用坎地沙坦酯治疗,观察组在对照组的基础上使用昆仙胶囊治疗,比较两组的临床疗效及不良反应。 结果 观察组总有效率显著高于对照组(P<0.05),两组治疗后血压、肾功能指标(24 h Upro、BUN、Scr)、血脂指标(TG、TC、LDL-C)、炎症因子(IL-6、hs-CRP)均显著降低,且观察组显著低于对照组(P<0.05)。治疗后两组血脂指数HDL-C显著升高,且观察组血脂指数HDL-C显著高于对照组(P<0.05)。 结论 昆仙胶囊联合坎地沙坦酯治疗慢性肾炎合并高血压患者可提高临床疗效,改善肾功能,调节血脂,减轻炎症反应。 Abstract:Objective To investigate the effect of Kunxian capsule combined with candesartan axetil on blood pressure, renal function, blood lipids and inflammatory factors in patients with chronic glomerulonephritis complicated with hypertension. Methods 101 patients with chronic glomerulonephritis who were admitted to our hospital from November 2017 to December 2019 were selected and randomly divided into observation group (51 cases) and control group (50 cases). The control group was treated with candesartan cilexetil on the basis of conventional treatment, and the observation group was treated with Kunxian capsule on the basis of the control group. The clinical efficacy and adverse reactions of the two groups were compared. Results The total effective rate of the observation group was significantly higher than that of the control group (P<0.05). After treatment, the blood pressure, renal function indexes (24 h Upro, BUN, Scr), blood lipid indexes (TG, TC, LDL-C), and inflammatory factors of the two groups (IL-6, hs-CRP) significantly decreased, and the observation group was significantly lower than the control group (P<0.05). After treatment, the blood lipid index HDL-C of the two groups increased significantly, and the blood lipid index HDL-C of the observation group was significantly higher than that of the control group (P<0.05). Conclusion Kunxian capsule combined with candesartan axetil can enhance the clinical efficacy, improve renal function, regulate blood lipids and reduce inflammation in patients with chronic glomerulonephritis complicated with hypertension. -
Key words:
- chronic glomerulonephritis /
- hypertension /
- Kunxian capsule /
- candesartan axetil /
- clinical effect
-
随着腹腔镜技术在普外科、妇科、泌尿外科等领域的广泛应用,在一些外科疾病如胆囊结石,阑尾炎,子宫肌瘤的治疗上,腹腔镜手术正在逐渐取代传统开腹手术。较传统手术而言,腹腔镜手术具有较高诊断准确率和治疗能力[1],且具有手术出血量少、肠蠕动恢复早、术后疼痛轻、术后恢复快、下床活动时间早、住院时间短、手术口美观、术后并发症降低等优势[1-2]。然而,无论是传统手术和腹腔镜手术,术后感染依然是影响患者预后的重要并发症。对于腹腔镜手术如何直接改变腹腔微生物群落种类及数量,目前还没有相关报道。
通过DNA测序对微生物种群进行鉴定(菌种鉴定)是比传统生化鉴定更为先进、更为准确的鉴定方法。16S rDNA是编码原核生物(主要为细菌)核糖体小亚基rRNA(16S rDNA)的DNA序列,长度约为1540~bp,存在于所有细菌染色体基因组中。16S rDNA分子大小适中,突变率小,目前是细菌系统分类学研究中最常用的基准序列。16S rDNA测序不依赖菌种本身的性质,使得它对所有菌种均可使用。通过对16S rDNA的测序,可以快速、直观地明确细菌群落多样性的变化。
本研究通过制作新西兰兔腹腔镜探查术模型,对术后动物腹腔积液进行细菌16S rDNA测序,对比分析腹腔积液中的微生物多态性,探索腹腔镜术后的微生物变化情况,可为腹腔镜手术的术后感染提供有效防治依据。
1. 材料与仪器
1.1 动物
雄性2月龄新西兰兔6只(上海甲干生物科技有限公司),体重约为2 kg,分别设置模型组(n = 3)和对照组(n = 3)。
1.2 仪器
ABI GeneAmp® 9700 型PCR仪;NanoDrop2000型分光光度计;CQZ2000720型便携一体式电子腹腔镜,腹腔镜镜头型号为J1000B型、J1030B型(上海卓外医疗电子科技有限公司);手提式高压蒸汽灭菌器DSX-24L-I(上海申安医疗器械厂)。
1.3 药物与器材
2%戊巴比妥钠溶液(0.4 g戊巴比妥钠粉末溶于20 ml 0.9%氯化钠注射液);碘伏溶液;液氮;0.9%氯化钠注射液;手术器械(打孔器、手术刀、组织剪、血管钳、镊子、布巾钳、圆针三角针、手术单)。
2. 方法
2.1 动物分组
随机将6只新西兰兔分成两组,分别设置模型组(n = 3)和对照组(n = 3),模型组麻醉后给予腹腔镜探查术,术后关闭腹腔;对照组麻醉后开腹,然后关闭腹腔。
2.2 制作模型
对模型组新西兰兔称重,耳缘静脉注射2%戊巴比妥钠(剂量1 ml/kg),麻醉成功后(呼吸平稳,角膜反射消失,身体肌肉松软),脱毛备皮,固定,生理盐水清洗皮肤,碘伏溶液消毒皮肤3次(范围为伤口周围15 cm)。铺手术巾,铺巾钳固定。沿腹正中线上切开皮肤,向下分离肌肉筋膜,切开腹膜,腹腔镜打孔器深入腹腔,插入腹腔镜套筒。将腹腔镜沿腹膜伸进去,到达肝脏表面,探查肝脏及胆囊约2 min。取出腹腔镜及套筒,消毒手术区域,关闭腹腔,缝合手术切口,敷料固定。对对照组进行相同操作,但不进行腹腔镜探查术。待新西兰兔麻醉苏醒后,送回动物饲养中心饲养。
2.3 组织取材
腹腔镜术后模型制备一周后,动物取材。新西兰兔称重,备皮,分别对模型组动物和对照组动物固定、消毒、铺巾,沿腹正中线行5 cm切口,打开腹膜腔,用无菌注射器深入到腹腔后部最低处,吸取约1.5 ml腹腔液体,放入相应编号的EP管中(并备份),液氮冷藏,随后进行16S rDNA测序。
2.4 细菌16S rDNA测序
根据 E.Z.N.A.® soil DNA kit (美国Omega Bio-tek公司)进行腹腔液体微生物群落的DNA抽提,使用338F(5′-ACTCCTACGGGAGGCAGCAG-3′)和806R (5′-GGACTACHVGGGTWTCTAAT-3′)对 16S rDNA基因V3-V4 可变区进行 PCR 扩增。在Miseq PE300/NovaSeq PE250平台(美国Illumina公司)进行测序(上海美吉生物医药科技有限公司)。使用Fastp软件对原始测序序列进行质控,使用Flash软件进行拼接后,在美吉生物的I-Sanger平台上进行生物信息学分析。
3. 结果
3.1 模型组相比于对照组微生物群落种类增加
以最小二乘法对样本做判别分析(PLS-DA),寻找物种丰度矩阵和样品分布/分组信息的最大协方差,在门水平和种水平上,模型组样本与对照组样本组内聚合良好、组间区分明显(图1A、图1B)。结果显示为两组样本细菌的种类均一度良好。对两组样本数据做Venn图分析,显示两者共有的OTU数目为957,模型组OTU数目为2206,对照组OTU数目为592。模型组腹水OTU含量高于对照组,表明模型组细菌种类较对照组明显升高(图1C)。
3.2 新西兰兔腹腔镜手术后细菌种类和数量均增加
对样本数据进行α多样性分析,菌落丰富度Sobs及Ace值越高提示微生物群落丰度越高,结果显示模型组比对照组微生物群落丰度更高(图2A、图2B)。在微生物群落多样性分析中,Shannon指数提示,数值越高多样性越大;Simpson指数提示,数据越小多样性越大。得出模型组在微生物群落丰度和多样性方面均高于对照组(图2C、图2D)。从Alpha多样性指数表中可得出同样的结论(表1)。
表 1 Alpha多样性指数表组别 Sobs指数 Ace指数 Shannon指数 Simpson指数 对照组C1 701 712.782842 5.213487 0.016805 对照组C2 535 555.895755 2.418362 0.263764 对照组C3 894 912.018376 4.549837 0.054558 模型组M1 1885 1899.991681 6.43408 0.005768 模型组M2 882 892.237411 5.444351 0.018387 模型组M3 1284 1301.268936 6.109346 0.005465 通过对样本的OTU分类学分析,对样本测序结果中的菌种、菌属等进行聚类,通过对97%相似水平的OTU代表序列进行分类学分析,在丰度-均匀度曲线中,水平方向是物种丰度,曲线在横轴上的宽度越大,提示丰度越高。曲线的形状反映了物种的均匀度,曲线越平缓,物种越丰富。模型组相对于对照组曲线宽度更宽,更平缓。提示模型组细菌种类数量以及含量高于对照组(图2E)。
3.3 模型组的杂菌数量及其他菌群高于对照组
对样本数据进行微生物组成成分分析,在对照组中其他菌群数量占整体菌群数量的35.08%(图3A),而模型组其他菌群数量占整体菌群数量的65.04%(图3B),说明经过腹腔镜手术后,不明原因的其他菌群数量升高。模型组较对照组菌群占比升高的菌群有出血败血性巴斯德菌、草酸桿菌科、普雷沃菌、瘤胃球菌、正皮氏罗尔斯顿菌等。由此得出结论:腹腔镜手术后杂菌的数量显著增加,且以出血败血性巴斯德菌、草酸桿菌科、普雷沃菌、瘤胃球菌、 正皮氏罗尔斯顿菌等升高为主。
3.4 新西兰兔腹腔镜手术后巴斯德菌明显增加。
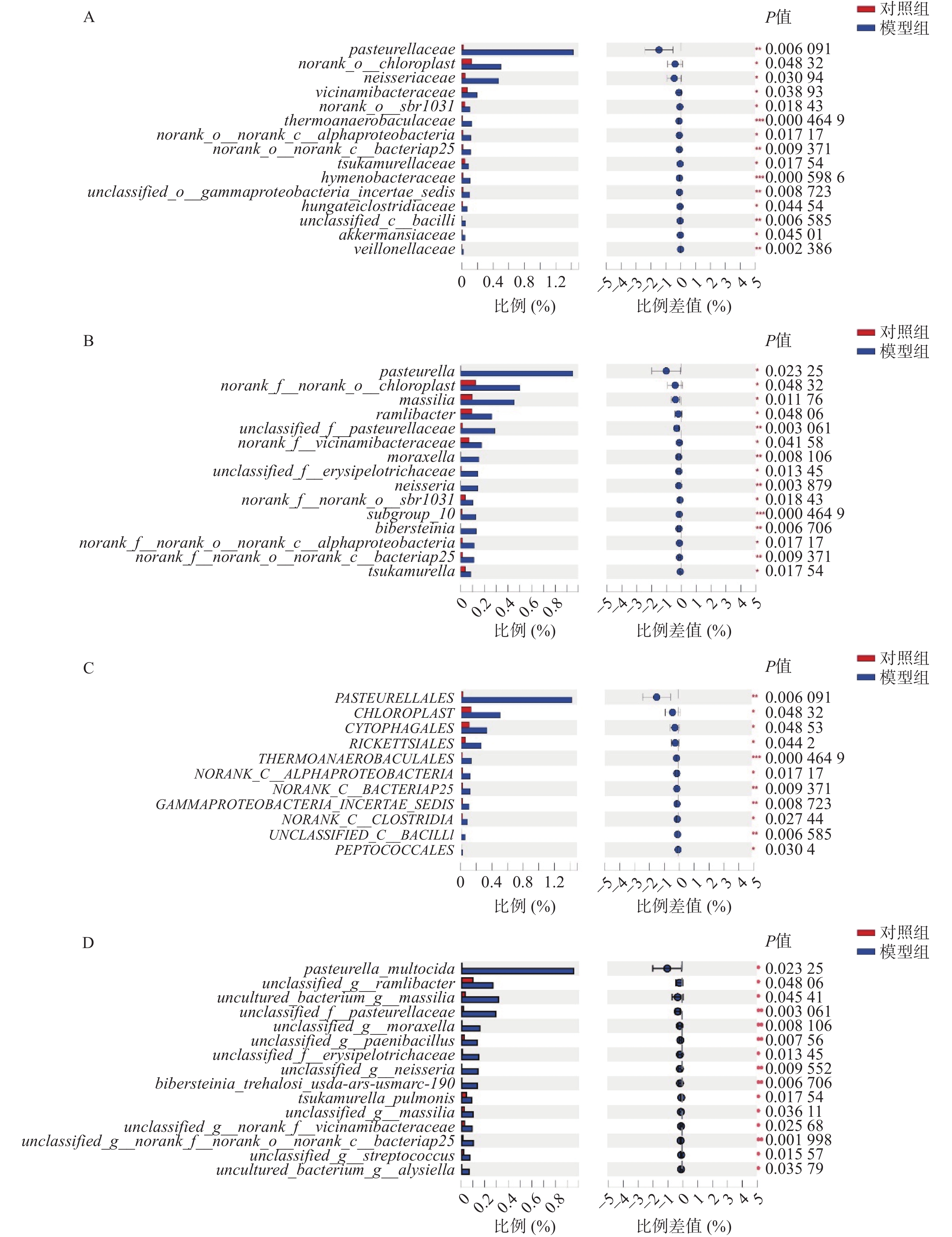
微生物组在目、科、属、种水平上进行物种差异性分析。在目水平上,得出以下微生物群落升高:巴斯德菌目、马赛菌目、沙壤土杆菌目、莫拉菌目、奈瑟菌目、山羊海藻百伯史坦菌目、冢村氏菌目; 在科水平上,发现以下微生物群落升高:巴斯德菌科、奈瑟菌科、紫杉霉菌科、热苜蓿菌科、冢村氏菌科、膜杆菌科、虎蛆科、Akk菌科 、韦荣氏球菌科;在属水平上,发现以下微生物群落升高:巴斯德菌属、马赛菌属、莫拉菌属、奈瑟菌属、山羊海藻百伯史坦菌属、冢村氏菌属;在种水平上,发现以下微生物群落升高: 巴斯德菌、类芽孢杆菌、奈瑟菌、拉姆利杆菌、马赛菌、赤藓科菌、冢村氏菌、马赛菌、链球菌属。通过分析,发现在目、科、属、种上模型组均有增长且增长较为明显的菌种为巴斯德菌(图4A~图4D)。
4. 讨论
随着腹腔镜手术大量应用于临床,相比于传统手术而言,术后感染虽有所下降[3],但由于植入材料的应用,腹腔术后感染发生率依然很高。有研究表明,在腹腔镜术后患者的术后感染中革兰阴性菌占半数以上,以大肠埃希菌、铜绿假单胞菌、鲍氏不动杆菌、肺炎克雷伯杆菌、嗜血菌属为主;革兰阳性菌以溶血葡萄球菌、金黄色葡萄球菌、表皮葡萄球菌、粪肠球菌为主;真菌以念球菌属、光滑假丝酵母菌、白假丝酵母菌为主[3-5]。在这些术后感染的病人中,感染的部位主要集中在肺部、腹部和尿道[5],从而引起相应术后并发症。
本研究通过对新西兰兔进行腹腔镜探查手术,发现模型组与对照组在样本菌群的聚合度良好,并且在模型组中,菌群的多样性和丰度比对照组高。在进行两组样本微生物群落对比分析中发现,在属水平上模型组的其他菌群占比由35%上升至65%。表明菌群群落数量在腹腔镜手术术后显著升高,且以草酸杆菌科、有益杆菌、巴斯德菌、瘤胃球菌、黄杆菌升高为主,其中巴斯德菌、瘤胃球菌、正皮氏罗尔斯顿菌、黄杆菌导致人感染疾病。研究发现,巴斯德菌是一种来源于动物的革兰阴性球菌,可引起蜂窝织炎、腹膜炎、菌血症、心内膜炎、脑膜炎和化脓性关节炎等疾病[6],严重者病死率可达到31%[7]。瘤胃球菌是一种革兰阳性厌氧菌,是人类正常肠道菌群的一员[8],可以导致炎症性肠病[9]。正皮氏罗尔斯顿菌是革兰阴性杆菌,容易侵袭免疫功能低下的患者,可导致严重的菌血症和肾盂肾炎[10]。有研究表明,在195名呼吸功能衰竭患者中有黄杆菌定植,但均未出现相应的并发症。微生物菌群物种差异性分析发现,在科、目、种、属水平上,模型组较对照组在巴斯德菌、奈瑟菌、冢村氏菌、热苜蓿菌、叶绿体、噬纤维菌等均有不同程度上升,而其中巴斯德菌、奈瑟菌、冢村氏菌可导致人类发病。据相关研究显示。冢村氏菌是一种革兰阳性、专性需氧、弱抗酸细菌,可导致人体肺部感染[11]。奈瑟菌可导致人体感染尿道炎、脑膜炎[12]。
本研究发现巴斯德菌、瘤胃球菌、正皮氏罗尔斯顿菌、黄杆菌、奈瑟菌、冢村氏菌在模型组呈现显著上升趋势,这些菌种可引起腹腔、尿道、肺部感染,出现严重的腹膜炎、肠梗阻,尿道炎以及脑膜炎,甚至导致病人死亡,对腹腔镜腹腔感染控制有一定的指导意义。由于本次为动物实验,可能存在手术室条件有限,手术者操作不规范等将细菌带入腹腔情况,能否在临床病人身上得出同样的结论,还需要做进一步的研究。
-
表 1 两组患者一般资料比较
特征 对照组 观察组 n=50 n=51 年龄 45.74±9.75 44.92±9.68 男性,n(%) 29(58.00%) 31(60.78%) 病程(年) 4.64±2.07 4.12±1.63 SBP(mmHg) 154.24±8.45 151.98±7.98 DBP(mmHg) 95.40±4.46 96.69±5.27 24 h尿蛋白(g) 1.73±0.63 1.68±0.56 Scr(μmol/L) 148.01±20.49 149.76±21.05 BUN(mmol/L) 11.62±1.66 11.90±1.80 TG(mmol/L) 2.10±0.23 2.02±0.21 TC(mmol/L) 6.25±1.09 6.31±0.83 LDL-C(mmol/L) 4.21±1.08 4.26±0.89 HDL-C(mmol/L) 1.10±0.13 1.12±0.15 IL-6(pg/ml) 171.22±19.47 175.28±23.71 hs-CRP(mg/L) 3.58±0.78 3.57±0.74 表 2 两组患者治疗前后血压变化(
$\bar x $ ± s )组别 SBP(mmHg) DBS(mmHg) 治疗前 治疗后 治疗前 治疗后 对照组 154.24±8.45 138.24±10.38* 95.40±4.46 84.02±4.71* 观察组 151.98±7.98 127.14±12.09*# 96.69±5.27 78.22±6.72*# *P<0.05,与同组治疗前比较;#P<0.05,与对照组治疗后比较。 表 3 两组患者治疗前后24 Upro、BUN、Scr的变化(
$\bar x $ ±s )组别 24 Upro(g) Scr(μmol/L) BUN(mmol/L) 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 对照组 1.73±0.63 0.93±0.58* 148.01±20.49 105.01±18.32* 11.62±1.66 7.11±1.06* 观察组 1.68±0.56 0.71±0.13*# 149.76±21.05 92.76±15.37*# 11.90±1.80 6.29±0.96*# *P<0.05,与同组治疗前比较;#P<0.05,与对照组治疗后比较。 表 4 治疗12周后血脂四项的变化(
$\bar x $ ±s )组别 TG(mmol/L) TC(mmol/L) LDL-C(mmol/L) HDL-C(mmol/L) 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 对照组 2.10±0.23 1.65±0.31* 6.25±0.78 5.47±0.59* 4.21±1.08 3.45±0.53* 1.10±0.13 1.31±0.16* 观察组 2.02±0.21 1.47±0.23*# 6.31±0.83 4.50±0.64*# 4.26±0.89 2.40±0.78*# 1.12±0.15 1.43±0.18*# *P<0.05,与同组治疗前比较;#P<0.05,与对照组治疗后比较。 表 5 治疗12周后血炎症因子IL-6、hs-CRP的变化(
$\bar x $ ±s )组别 IL-6(pg/ml) Hs-CRP(mg/L) 治疗前 治疗后 治疗前 治疗后 对照组 171.22±19.47 115.22±15.31* 3.58±0.78 2.68±0.64* 观察组 175.28±23.71 93.28±15.48* 3.57±0.74 1.75±0.52* *P<0.05,与同组治疗前比较;#P<0.05,与对照组治疗后比较。 表 6 两组患者临床疗效比较[n(%)]
组别 例数 显效 有效 无效 总有效(率) 对照组 50 16(32.0%) 25(50.0%) 9(18.0%) 41(82.0%) 观察组 51 29(56.9%) 20(39.2%) 2(3.9%) 49(96.1%)* *P<0.05,与对照组比较。 -
[1] ZHANG L, WANG F, WANG L, et al. Prevalence of chronic kidney disease in China: a cross-sectional survey[J]. Lancet,2012,379(9818):815-822. doi: 10.1016/S0140-6736(12)60033-6 [2] 李小莉, 赵波, 陈文慧, 等. 贝前列素钠联合羟苯磺酸钙治疗慢性肾小球肾炎疗效观察[J]. 疑难病杂志, 2016, 15(6):595-597,601. doi: 10.3969/j.issn.1671-6450.2016.06.012 [3] NODA M, SHIBOUTA Y, INADA Y, et al. Inhibition of rabbit aortic angiotensin II (AII) receptor by CV-11974, a new nonpeptide AII antagonist[J]. Biochem Pharmacol,1993,46(2):311-318. doi: 10.1016/0006-2952(93)90420-2 [4] 曹艳, 运乃茹, 邹爱英. 雷公藤多苷片致不良反应的meta分析[J]. 中国药房, 2018, 29(1):125-130. [5] 吴炜飞, 程志群, 施向东. 雷公藤多苷联合缬沙坦治疗慢性肾小球肾炎合并高血压患者的临床疗效及对炎症因子的影响[J]. 中国生化药物杂志, 2016, 36(8):101-104. [6] 华斐. 雷公藤多甙片对慢性肾小球肾炎患者血清IL-6 、IL-8及T细胞亚群的影响[J]. 国际泌尿系统杂志, 2019, 39(6):1077-1080. doi: 10.3760/cma.j.issn.1673-4416.2019.06.032 [7] BERTHIER CC, KRETZLER M, DAVIDSON A. A systems approach to renal inflammation in SLE[J]. Clin Immunol,2017,185:109-118. doi: 10.1016/j.clim.2016.08.015 [8] SETHI S, FERVENZA FC. Standardized classification and reporting of glomerulonephritis[J]. Nephrol Dial Transplant,2019,34(2):193-199. doi: 10.1093/ndt/gfy220 [9] 巩昭勇, 黄芳, 薛丕良, 等. 活血益肾汤联合氯沙坦钾治疗慢性肾小球肾炎疗效及对血脂和炎症反应的影响[J]. 现代中西医结合杂志, 2019, 28(23):2587-2589. doi: 10.3969/j.issn.1008-8849.2019.23.021 [10] 毛娅妮, 田少江. 补肾清利活血汤联合奥美沙坦酯治疗慢性肾小球肾炎疗效观察[J]. 现代中西医结合杂志, 2017, 26(10):1111-1113. doi: 10.3969/j.issn.1008-8849.2017.10.031 [11] ZHOU A, YU L, LI J, et al. Renal protective effects of blocking the intrarenal renin-angiotensin system: angiotensin II type I receptor antagonist compared with angiotensin-converting enzyme inhibitor[J]. Hypertens Res,2000,23(4):391-397. doi: 10.1291/hypres.23.391 [12] URATA H, KINOSHITA A, PEREZ D M, et al. Cloning of the gene and cDNA for human heart chymase[J]. J Biol Chem,1991,266(26):17173-17179. doi: 10.1016/S0021-9258(19)47355-9 [13] 涂晓, 杨梦蝶, 李亚妤, 等. 昆仙胶囊与雷公藤多苷片治疗慢性肾脏病的疗效及安全性比较[J]. 浙江中医药大学学报, 2021, 45(6):582-587,602. [14] REMUZZI A, PERICO N, SANGALLI F, et al. ACE inhibition and ANG II receptor blockade improve glomerular size-selectivity in IgA nephropathy[J]. Am J Physiol,1999,276(3):F457-F466. [15] MACKINNON M, SHURRAW S, AKBARI A, et al. Combination therapy with an angiotensin receptor blocker and an ACE inhibitor in proteinuric renal disease: a systematic review of the efficacy and safety data[J]. Am J Kidney Dis,2006,48(1):8-20. doi: 10.1053/j.ajkd.2006.04.077 [16] ITO K, IMANISHI M, KITO G. Comparison of the hypotensive effects of TCV-116 and losartan in chronic renal hypertensive dogs[EB/OL]. 1996 [17] NODA M, MATSUO T, FUKUDA R, et al. Effect of candesartan cilexetil (TCV-116) in rats with chronic renal failure[J]. Kidney Int,1999,56(3):898-909. doi: 10.1046/j.1523-1755.1999.00614.x [18] KUROKAWA K, ABE K, SARUTA T, et al. Antiproteinuric effect of candesartan cilexetil in patients with chronic glomerulonephritis[J]. J Renin Angiotensin Aldosterone Syst,2002,3(3):167-175. doi: 10.3317/jraas.2002.037 [19] 邓晓蔚, 熊有明, 张维, 等. 昆仙胶囊联合百令胶囊治疗慢性肾小球肾炎临床研究[J]. 中国药业, 2019, 28(9):53-55. doi: 10.3969/j.issn.1006-4931.2019.09.015 [20] TANG Y, ZHANG Y, LI L, et al. Kunxian capsule for rheumatoid arthritis: inhibition of inflammatory network and reducing adverse reactions through drug matching[J]. Front Pharmacol,2020,11:485. doi: 10.3389/fphar.2020.00485 [21] 张宁, 易无庸. 昆仙胶囊临床应用进展[J]. 中医临床研究, 2014, 6(7):147-148. doi: 10.3969/j.issn.1674-7860.2014.07.083 [22] 张楠, 郭晓琴, 田云凤, 等. 昆仙胶囊对慢性肾小球肾炎的临床疗效观察[J]. 中国中西医结合肾病杂志, 2020, 21(12):1096-1097. doi: 10.3969/j.issn.1009-587X.2020.12.020 -






 下载:
下载:


 下载:
下载: 






