-
肝区疼痛是肝癌患者最为常见的症状之一,初诊发生率为25%,晚期发生率为60%~80%,其中1/3为重度疼痛[1]。随着对癌痛治疗的不断深入,阿片类药物具有高效、多种途径使用、不良反应少、耐受性好及可调整剂量的优势 [2]。然而,60%~90%的癌症患者使用阿片类镇痛药会出现阿片类药物相关性便秘(OIC) [3]。便秘症状有时超过了疼痛本身,严重影响患者的生活质量,甚至有患者因无法忍受OIC而停止使用阿片类药物,从而放弃治疗 [4]。对于晚期肝癌患者,便秘则尤为致命,因便秘不缓解会导致肠道代谢产物无法及时排出,毒素被肠道吸收易引起机体自身中毒,患者可出现烦躁不安、恶心、腹胀、食欲下降等症状,甚至引发肝性脑病,从而加重疾病进展[5]。晚期肝癌患者普遍门静脉压力增高,在用力屏气排便时极易诱发消化道出血,从而可能危及生命。
对于OIC的治疗,欧洲姑息治疗协会建议优先考虑将泻药作为预防措施[6]。泻药是常见的治疗OIC的药物之一。传统泻药可分为缓泻剂和强效泻药,乳果糖是强效泻药的一种。然而,很多患者使用传统泻药的治疗效果并不理想。此外,过度使用传统泻药可能导致患者产生耐受性,并引起一系列不良反应,如脱水、腹胀和皮炎等,这些反应也可能会使患者放弃治疗[7]。
根据中医理论,便秘以潜在病因大致分为实证和虚症。中医内科学将便秘分为实秘和虚秘。针对肝癌晚期OIC患者与其他癌症OIC患者的不同,选择神阙穴进行穴位贴敷与消化器官位置比邻,敷贴能激发各经气作用全身发挥培元固本、回阳救脱、和胃理肠的治疗作用。而消胀通便膏在“枳术丸”及“调胃承气汤”基础之上,结合肝癌患者中医证型,经过临证反复验证优化而成,可外贴神阙穴,缓解肝癌患者OIC。因此,本研究以口服乳果糖为对照,评估消胀通便膏治疗肝癌晚期OIC的疗效,以期进一步指导临床实践。
-
选取2021年6月至2022年12月在海军军医大学第三附属医院中西医结合科(本院)诊治的120名晚期肝癌合并OIC患者作为研究对象。采用随机数字表法将患者分为对照组与试验组,每组各60例。本研究经所在医院伦理委员会批准(伦理批准号:EHBHKY2023-H016-P001),每位患者均签署知情同意书。
-
①符合罗马Ⅳ OIC诊断标准[8]; ②巴塞罗那肝癌临床分期晚期及终末期的肝癌患者[9]; ③使用阿片类药物≥7 d; ④预计生存期>3个月; ⑤年龄>18岁;⑥意识清晰并签署知情同意书。
-
①有严重心肺功能、严重凝血功能障碍的患者;②合并肠道疾病的患者;③不能配合者和精神病患者;④神阙穴附近存在皮肤破损;⑤对所用药物产生过敏反应者;⑥正在参与其他临床试验。
-
①因病情变化无法参与完整疗程或用挽救性泻药;②在研究期间患者自行更换药物;③患者自行退出。
-
两组患者均在住院期间接受健康宣教:①三阶梯止痛相关知识;②逐步形成合理的排便习惯;③适量饮水,保证饮食中摄入足够的膳食纤维和优质蛋白;④保持每日适量的运动;⑤维持情绪稳定并积极乐观。
-
在常规治疗的基础上选择乳果糖口服溶液(进口药品注册证号:H20171057,荷兰Abbott Biologicals B.V.公司)缓解便秘情况,口服治疗,起始剂量每日30 ml,维持剂量每日10 ml至25 ml,症状缓解后停药[10]。
-
在常规治疗的基础上选择神阙穴进行消胀通便膏穴位贴敷,将枳实、生白术、厚朴、生大黄、芒硝、冰片、大腹皮,用药比例为6∶6∶6∶6∶3∶1∶6,打磨成粉,每次取10 g,用食醋调和涂抹在无纺布自粘敷料上贴敷神阙穴。从出现OIC症状起贴,根据子午流注理论择卯时(5点至7点)开始敷贴[11]。每日一贴,每贴4 h,7 d为一个疗程,贴敷前后清洗脐部皮肤,若贴敷期间患者出现腹泻即停药。患者在出院后可使用自研穴位贴敷药剂家庭定量制备装置(专利号:ZL202121038992.9)方便制取。
-
主要评价指标为便秘症状改善情况、生活质量评价以及治疗后综合评价(经济成本、及腹泻发生次数以及阿片类药物使用剂量是否有变化)。
-
便秘症状中包括排便间隔、粪便性状、排便时间、排便困难程度。采用问卷调查的方式收集资料。运用便秘患者症状自评量表(PAC-SYM)分别在治疗前、治疗第14天、治疗第28天进行评估。
PAC-SYM的Cronbach’a系数为0.91,各维度Cronbach’a系数为0.81~0.90,具有较好的内部一致性效度[12]。PAC-SYM由粪便性状、直肠症状和腹部症状3个部分共12个条目构成,对排便次数减少、排便费力、排便疼痛、排便不尽感、粪质坚硬、粪量少、胃痛、腹部痉挛疼痛腹部胀满、有便意但难以排出、直肠出血或撕裂、直肠烧灼感等症状进行评估。每个条目采用Likert5点评分法进行评价,按症状严重程度由无到非常严重分别计为 0~4 分。总分为各条目得分的平均分,得分越高便秘症状越严重。
-
运用癌症治疗功能评价系统之肝胆量表(FACT-Hep)(第四版)来评价治疗晚期肝癌患者便秘问题后的生活质量。分别在治疗前、治疗第14天、治疗第28天进行评估。FACT-Hep的各维度Cronbach’a系数为0.798~0.878,具有较好的内部一致性效度[13]。FACT-Hep内含5个方面的评分:身体状况(PWB)、社交/家庭状况(SWB)、感情状况(EWB)、功能状况(FWB)、肝胆特意模块(HEP),其条目数分别为7、7、6、7、19,每条条目计分为0、1、2、3、4分。总分为所有条目相加,得分越高则生活质量越低,反之则生活质量越高。
-
治疗后综合评价包括经济成本、治疗过程中发生腹泻的次数以及阿片类药物使用剂量是否有变化。
-
采用 SPSS 21.0 统计软件进行数据分析。对于计量资料(即连续变量)需先对正态性检验,对于正态分布的数据采用平均值±标准差,非正态分布的应采用中位数法,两组间比较采用t 检验,计数资料以相对数表示,组间比较采用χ2检验。 以P<0.05为差异有统计学意义。
-
共纳入120例患者,干预期间脱落14例患者,9例患者因病情变化无法参与完整疗程,5例患者使用挽救性泻药。最终对照组52人、试验组54人完成调查。两组患者基本资料比较差异无统计学意义(P>0.05),见表1。
表 1 两组患者一般资料比较
项目 对照组 试验组 t/χ2 P 性别 − − 0.406 0.524 男 33 31 − − 女 19 23 − − 年龄(岁) 59.75±15.81 61.43±15.49 −0.551 0.583 文化程度 − − 2.944 0.229 初小 3 6 − − 中学 28 34 − − 专科及以上 21 14 − − 婚姻状况 − − 0.597 0.440 已婚 36 41 − − 离婚或丧偶 16 13 − − 独居 − − 0.366 0.545 是 10 13 − − 否 42 41 − − -
在治疗后14 d时,两种治疗方法对缓解便秘症状并没有显著的差异。然而,当治疗时间延长至28 d时,观察到两组之间的差异具有统计学意义。
在本次研究的对照组中,有5位患者因为逐渐对乳果糖产生耐受性而需要采用灌肠等挽救性治疗方法,导致这些患者退出了研究。这表明乳果糖在疗效上在初期表现出了显著的效果,但随着时间的推移,其疗效逐渐减弱。与之相比,消胀通便膏外贴在长期治疗中表现出更好的效果,如表2所示。
表 2 两组患者便秘自评量表治疗前、治疗后对比
治疗天数 对照组 试验组 t/χ2 P 治疗前 2.57±0.72 2.49±0.74 0.551 0.583 治疗后14 d 1.86±0.62 1.64±0.66 1.715 0.089 治疗后28 d 1.45±0.56 1.05±0.37 4.323 <0.001 -
从生活质量的角度来看,试验组表现出明显优势,使用消胀通便膏外贴相对于口服乳果糖对患者的生活质量影响更小。
缓解患者OIC能确保止痛药物的规范使用,采用脐部贴敷这种易于接受的方式有效降低治疗方式对生活的干扰,较好改善了患者的生活质量。这些因素共同作用,进一步提高了患者的生活质量,见表3。
表 3 两组患者治疗前、治疗后生活质量比较
治疗天数 对照组 试验组 t/χ2 P 治疗前 100.42±12.59 99.89±16.46 0.187 0.852 治疗后14 d 91.67±12.57 89.39±15.65 0.827 0.41 治疗后28 d 91.85±9.81 84.35±10.48 3.797 <0.001 -
从经济成本方面,试验组的经济成本明显低于对照组,这使得患有终末期肿瘤的患者能够将有限的资源更专注于提高生活质量和缓解躯体症状,减轻了治疗的财务压力。
以腹泻发生率来说,在研究周期中对照组的腹泻发生率显著高于试验组。这表明乳果糖在不同患者中的效果存在不可控的差异。特别是对于肿瘤终末期的患者,由于腹泻引起的体液丢失和电解质紊乱可能导致更为严重的后果,这种差异更加凸显了试验组的优势。
对比两组止痛药物的使用剂量,研究结果显示试验组阿片类药物的使用剂量相较于对照组呈现出放缓的增长趋势。这一变化可能归因于试验组患者便秘症状的缓解以及生活质量的提升,这两者共同作用,在一定程度上缓解了患者的疼痛感,见表4。
表 4 两组患者治疗后综合评价对比
评价项目 对照组 试验组 t/χ2 P 经济成本(元) 146.39±21.70 95.50±4.81 16.81 <0.001 发生腹泻的次数 4.83±3.02 2.56±1.42 4.981 <0.001 阿片类药物使用
剂量增加(例数)42 35 21.736 <0.001 -
中医普遍认为阿片类药物主要提取自传统中草药“罂粟壳”,其性温燥烈,具有辛香走窜的特点。长期摄入该类药物,容易导致机体燥热内郁、影响气血运行,导致便秘症状[14-15]。按照WHO癌痛三阶梯止痛原则进行癌痛规范化治疗,对癌症患者躯体功能、认知、情绪以及生活质量都有极大的改善。因此,阿片类药物在晚期癌症疼痛患者中必不可少。而肝癌患者有其特殊性,中医认为肝癌属于中医学的“积聚”、“臌胀”、“胁痛”等范畴。在《黄帝内经·灵枢》中记载:“肝脉急甚为恶言,微急为肥气,在胁下如覆杯”,可见肝癌与其他癌症有显著的区别,在辩证施治上亦有不同。对患者来说,一但发生便秘又会引起消化道出血、肝性脑病等症状,因此肝癌患者发生便秘的危险性与严重性远高于其他癌症患者[16]。
本研究选用的消胀通便膏是在“枳术丸”及“调胃承气汤”基础之上,结合肝癌患者中医证型所优选。穴位贴敷法的机理有两种主要观点。首先,穴位贴敷法利用经络的敏感性,可以将药物效应扩大,特别适合于薄角质皮肤区域;其次,穴位贴敷法的药物能够透过皮肤角质层,迅速扩散到全身,达到治疗目的,消胀通便膏中的生大黄、大腹皮、枳实等成分具有通便、促进肠道蠕动等作用[17]。在腧穴理论指导下,选择神阙穴作为穴位贴敷法的应用穴位,其穴位位于脐部,为全身经络之海,经络之总枢,贴敷其中可激发全身各经络之气。根据子午流注理论选择卯时进行穴位贴敷用药,卯时大肠经最旺,开穴之时用药效果最好。
综上所述,消胀通便膏在晚期肝癌OIC的患者中具有显著的缓解症状、改善生活质量和降低经济成本的作用。其具有操作简便,患者接受度、配合度高等特点,值得临床推广应用。
Application of eliminating flatulence and laxative cream in advanced hepatocellular carcinoma patients with opioid-associated constipation
-
摘要:
目的 探讨消胀通便膏在晚期肝癌阿片类药物相关性便秘(OIC)中的应用情况。 方法 选取2021年6月至2022年12月在海军军医大学第三附属医院诊治的120名晚期肝癌合并OIC患者作为研究对象。采用随机数字表法将患者分为对照组(乳果糖+常规治疗)与试验组(消胀通便膏+常规治疗),比较两组排便情况、生活质量以及治疗后的综合评价(包括经济成本、腹泻发生次数以及阿片类药物使用剂量是否有变化)。 结果 干预28 d后,两组患者在缓解OIC方面均有较好的效果(P<0.05),对于晚期肝癌患者生活质量、经济成本及腹泻次数方面,试验组均显著优于对照组(P<0.05)。 结论 在治疗晚期肝癌患者OIC中,使用外敷消胀通便膏和口服乳果糖液均可缓解便秘症状。其中,消胀通便膏更易被患者接受,且在生活质量和经济成本方面更优,对提高患者满意度和安全性是一个更佳的选择。 -
关键词:
- 阿片类药物相关性便秘 /
- 晚期肝癌 /
- 穴位贴敷 /
- 中药膏剂
Abstract:Objective To evaluate the curative effect ofeliminating flatulence and laxative cream on patients with advanced hepatocellular carcinoma and opioid-associated constipation(OIC). Methods 120 patients with advanced liver cancer complicated with OIC who were treated at the Third Affiliated Hospital of Naval Medical University from June 2021 to December 2022 were selected as the study subjects. The patients were divided into a control group(lactulose+conventional treatment)and an experimental group(eliminating flatulence and laxative cream + conventional treatment)using a randomized numerical table method. Two groups were compared in terms of defecation, quality of life, and comprehensive post-treatment evaluation(economic cost, number of occurrences of diarrhea, and whether or not there was a change in the dosage of opioids used). Results After 28 d of intervention, both groups showed better results in relieving OIC(P<0.05), and the experimental group was significantly better than the control group in terms of the quality of life of patients with advanced hepatocellular carcinoma, the economic cost and the number of diarrhea(P<0.05). Conclusion In the treatment of OIC in patients with advanced hepatocellular carcinoma, constipation could be relieved by using both topicaleliminating flatulence and laxative cream and oral lactulose solution. Among them, antieliminating flatulence and laxative cream was more acceptable to patients and superior in terms of quality of life and economic cost, which could be a better choice for improving patient satisfaction and safety. -
老药新用是药物设计的重要途径之一,采用此方法可以获得药物研究所需的先导化合物,迄今为止已有许多成功的案例,特别是在新型冠状病毒肺炎治疗药物研究中采用此策略,获得了很多有价值的药物[1-3]。阿司匹林从发明至今已有百年的历史,最初用于解热、镇痛和抗炎。随着医学科学的发展,在临床上发现阿司匹林的新用途,能够抑制血小板的聚集,抑制心脑血管疾病的发生[4-5]。因此,从上市药物中寻找新的适应证或将其作为先导物进行结构优化的老药新用设计方法成为药物研究的有效手段[6-7]。
1. 仪器与试剂
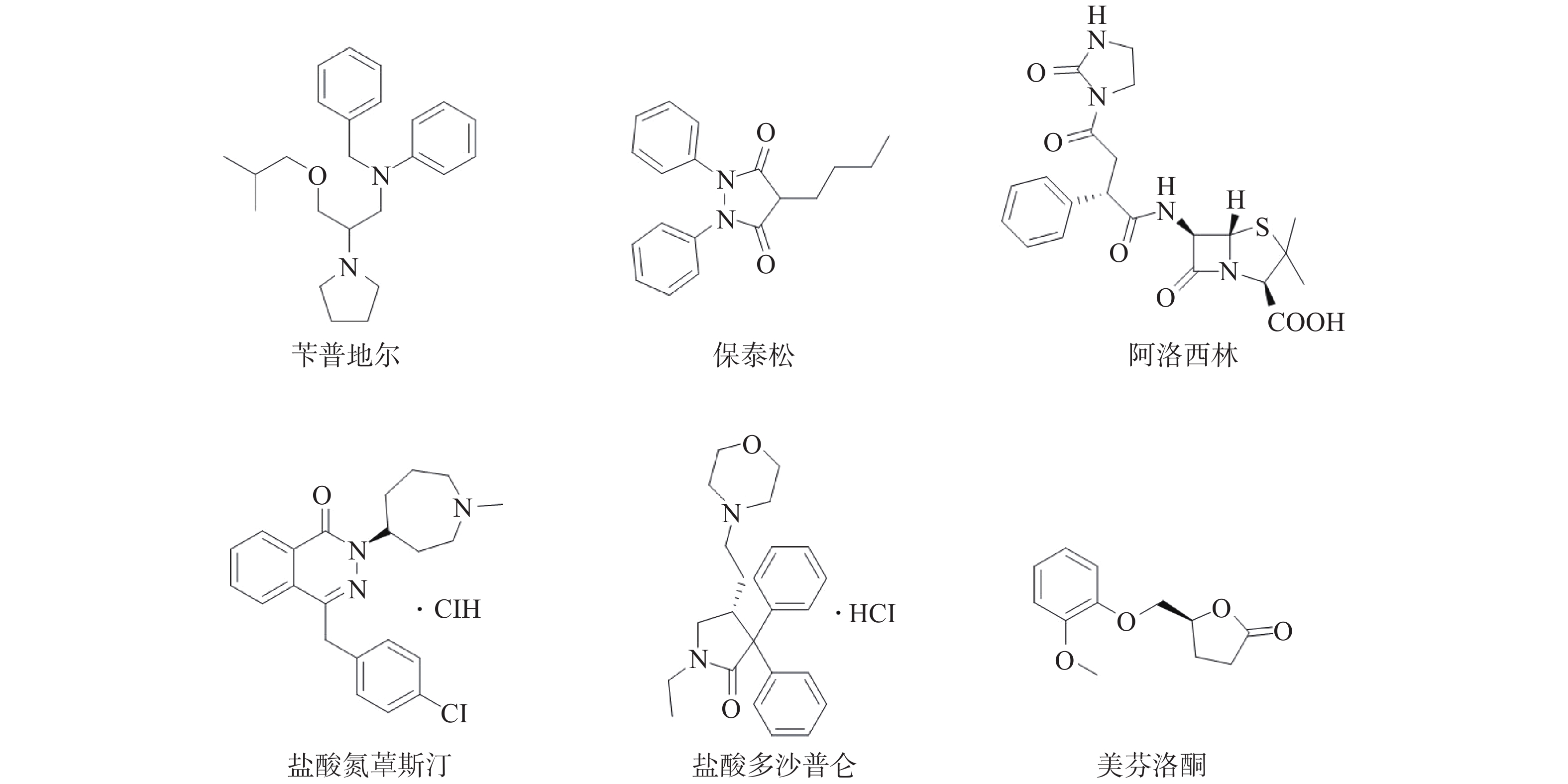
实验所用试剂均为分析纯;6种药物原料药:苄普地尔、保泰松、阿洛西林、盐酸氮䓬斯汀、盐酸多沙普伦、美芬洛酮(南京多点化工有限公司);还原型辅酶Ⅱ(NADPH,东京化学工业有限公司);混合人肝微粒体(美国BD Gentest公司)。
Biotek Synergy H2多功能酶标仪、MK-2全自动酶标仪、戴安公司Ultimate3000液相色谱系统(包括三元输液泵、柱温箱、自动进样器和真空脱气机)和AB公司4000Q-Trap型串联质谱仪,配有电喷雾电离源,以及AB公司Analyst (version 1.5.1)、LightSight (version 2.2.1)数据采集及分析软件。
2. 实验方法
2.1 p53-MDM2蛋白结合抑制活性测试[8]
将荧光肽(PMDM-F,Anaspec)用缓冲溶液(100 mmol/L磷酸钾、0.02%叠氮化钠、100 μg/ml牛丙种球蛋白,用蒸馏水定容至500 ml,pH 7.5)稀释至10 nmol/L,加入到梯度稀释的MDM2癌基因蛋白中,30ºC避光孵育30 min。荧光各向异性值用Biotek Synergy H2多功能酶标仪读取,蛋白结合常数根据荧光各向异性值用Mathematica 9软件拟合得到。
将购买的6个药物溶于二甲基亚砜(DMSO),缓冲液稀释至所需要浓度(最终缓冲液中含有1%DMSO)。然后将20 μl化合物加入到60 μl含有10 nmol/L PMDM-F肽和100 nmol/L MDM2蛋白的溶液中,30ºC避光孵育1 h。荧光各向异性值用Biotek Synergy H2多功能酶标仪读取,蛋白结合常数根据荧光各向异性值用Mathematica 9软件拟合得到。
2.2 蛋白印迹试验[9]
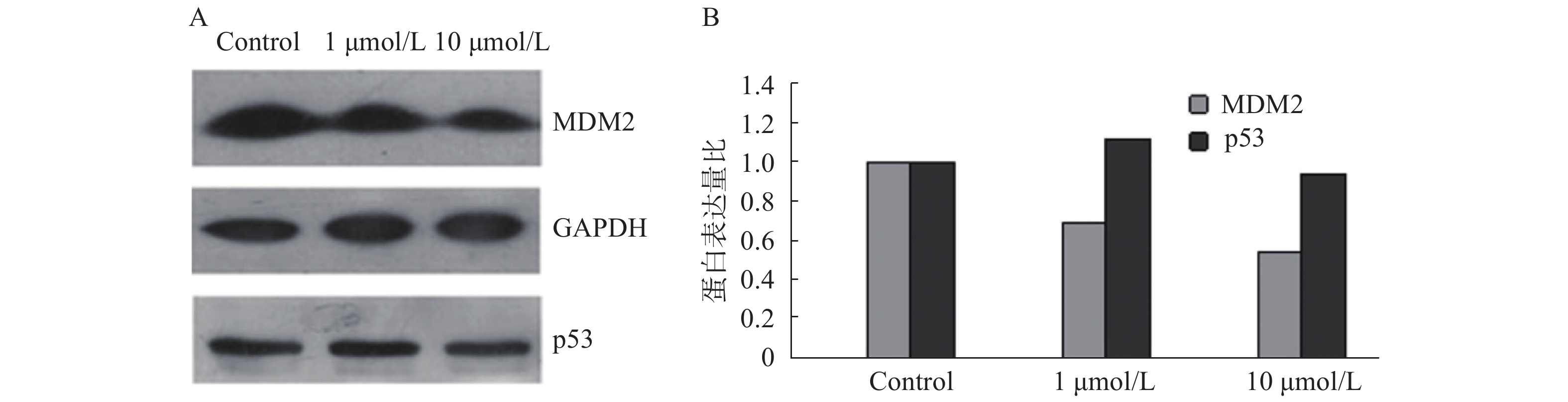
将人肺腺癌上皮细胞(A549)培养,待细胞生长至70%~80%时,加药处理。药物处理不同时间后,用0.25%胰酶消化,离心收集细胞,再用胞浆蛋白核蛋白裂解液4 ℃裂解,提取胞浆蛋白及核蛋白。采用12 %SDS-PAGE凝胶电泳,将蛋白转移到固相支持膜(PVDF膜)上,封闭液室温封闭1~2 h,用等渗缓冲盐溶液(tris-buffered saline tween-20, TBST)洗膜5 min,洗3次。采用TBST稀释抗体,4 ℃孵育过夜,TBST洗膜5 min,洗3次。然后用TBST稀释HRP标记的二抗,室温孵育1 h,TBST洗膜5 min,洗3次。暗室内采用ECL显色,X线片曝光成像。以甘油醛-3-磷酸脱氢酶(GAPDH)为内参照,分析成像光片灰度值,并以对照组为基准进行量化。
2.3 体外抗肿瘤活性测试[10]
样品配制:用DMSO溶解后,加入磷酸缓冲盐溶液(PBS)配成1000 μg/ml的溶液或均匀的混悬液,然后用含DMSO的PBS稀释。
MTT比色法:96孔板每孔加入浓度为(5~6)×104个/ml的细胞悬液100 μl,置37ºC,5% CO2培养箱内。24 h后,加入样品液,10 μl/孔,设双复孔,37ºC、5% CO2作用72 h。每孔加入5 mg/ml的MTT溶液20 μl,作用4 h后加入溶解液,100 μl/孔,置培养箱内,溶解后用MK-2全自动酶标仪测定570 nm处A值,计算IC值。
IC(%) =[(空白对照孔A值-给药孔A值) /空白对照孔A值]×100%
根据不同浓度的IC值,进行线性回归,计算出抑制肿瘤细胞生长50%的药物浓度,即IC50。
2.4 体外代谢研究[11]
每个孵育体系总体积为200 µl,介质为100 mmol/L磷酸缓冲液(PBS,pH7.4),包括终浓度为1 mg/ml的肝微粒体蛋白、50 µmol/L的苄普地尔和2 mmol/L的还原型辅酶Ⅱ(NADPH),用37°C水浴进行孵育,60 min后加入同体积冰冷乙腈终止反应。被终止反应的肝微粒体孵化样品,离心5 min(13000 r/min),取出全部上清液置于10 ml试管中,于40ºC空气流下吹干,残留物以100 μl乙腈/水(10: 90, V/V)复溶,取10 μl进行HPLC/Q-Trap MS分析。色谱条件为色谱柱为Kromasil® C18(150 mm×2.1 mm,5 μm),Agilent C18保护柱(12.5 mm ×2.1 mm,5 μm)。流动相:乙腈(A)–10 mmol/L甲酸铵水溶液(B),梯度洗脱:0~2 min,10% A;10~15 min,90% A;15.1~18 min,10% A;流速为0.3 ml/min;柱温为室温;进样量为10 μl。质谱条件为电喷雾离子化源(ESI),正离子检测。雾化温度为500 ℃,电喷雾电压为5200 V,气帘气流速20 L/min,雾化气50 L/min,辅助气流速50 L/min。扫描方式为MRM\MIM簇发EPI。
3. 结果
3.1 p53-MDM2蛋白相互作用抑制活性
课题组在针对p53-MDM2靶标进行虚拟筛选过程中,发现Wayne等已运用计算机构象筛选法对ZINC数据库中3244个FDA已批准上市药物进行了筛选,鉴别出与p53-MDM2抑制剂Nutlin-3a结构不同,但具有类似形状电荷分布的化合物[12]。然后,通过Autodock软件与MDM2蛋白进行分子对接,根据结合能获得打分函数排名前15的化合物,但未用分子药理学实验证实其作用靶标。因此,课题组购买了可售的6个药物(图1)。对这6个药物进行蛋白结合抑制活性实验,以Nutlin-3为阳性对照药,结果见表1。
表 1 蛋白结合抑制活性和体外抗肿瘤活性测试结果化合物 Ki
(μmol/L)IC50
(μmol/L)U-2OS
(wt-p53)Saos-2
(p53 null)A549
(wt-p53)NCI-H1299
(p53 null)Nutlin-3 0.093 12.2 8.38 2.18 1.97 美芬诺酮 5.79 >100 >100 8.43 >100 盐酸氮䓬斯汀 216.3 6.38 3.80 1.54 4.32 苄普地尔 0.456 2.58 1.56 1.04 1.39 保泰松 155.5 71.31 >100 91.45 >100 阿洛西林 NA >100 >100 >100 >100 盐酸多沙普仑 NA >100 >100 60.68 >100 从表1中可以看出,6个药物中美芬诺酮、盐酸氮䓬斯汀、苄普地尔和保泰松4个药物体现出一定的p53-MDM2蛋白结合抑制活性,其余2个药物无活性。其中,钙离子拮抗剂苄普地尔的Ki值达到0.456 μmol/L,显示出优异的p53-MDM2蛋白结合抑制活性。
为验证苄普地尔是否能抑制p53-MDM2蛋白结合,采用免疫印迹试验测定相关蛋白的表达变化,结果如图2。从图中可以看出,苄普地尔对p53蛋白表达作用相对较小,并且随着苄普地尔浓度上升到10 μmol/L,反而出现下降。但苄普地尔能显著降低MDM2蛋白的表达,而且呈剂量依赖关系,初步说明苄普地尔能明显抑制p53-MDM2蛋白结合。
3.2 体外抗肿瘤活性研究
课题组选择骨肉瘤(U-2OS、Saos-2)和肺癌(A549、NCI-H1299) 2组细胞株进行了6个药物的体外抗肿瘤活性测试(表1)。从表1中可以看出,苄普地尔对4种细胞株均具有优秀的抗肿瘤活性,其IC50值均低于3 μmol/L,优于阳性对照药Nutlin-3。而美芬诺酮尽管具有中等的p53-MDM2蛋白结合抑制活性(Ki=5.79 μmol/L),但除对A549具有较好的抗肿瘤活性,其余细胞株均未显示出活性。令人意外的是盐酸氮䓬斯汀尽管具有较弱的p53-MDM2蛋白结合抑制活性,但对4种肿瘤细胞株也显示出较好的活性。
3.3 苄普地尔的体外代谢研究
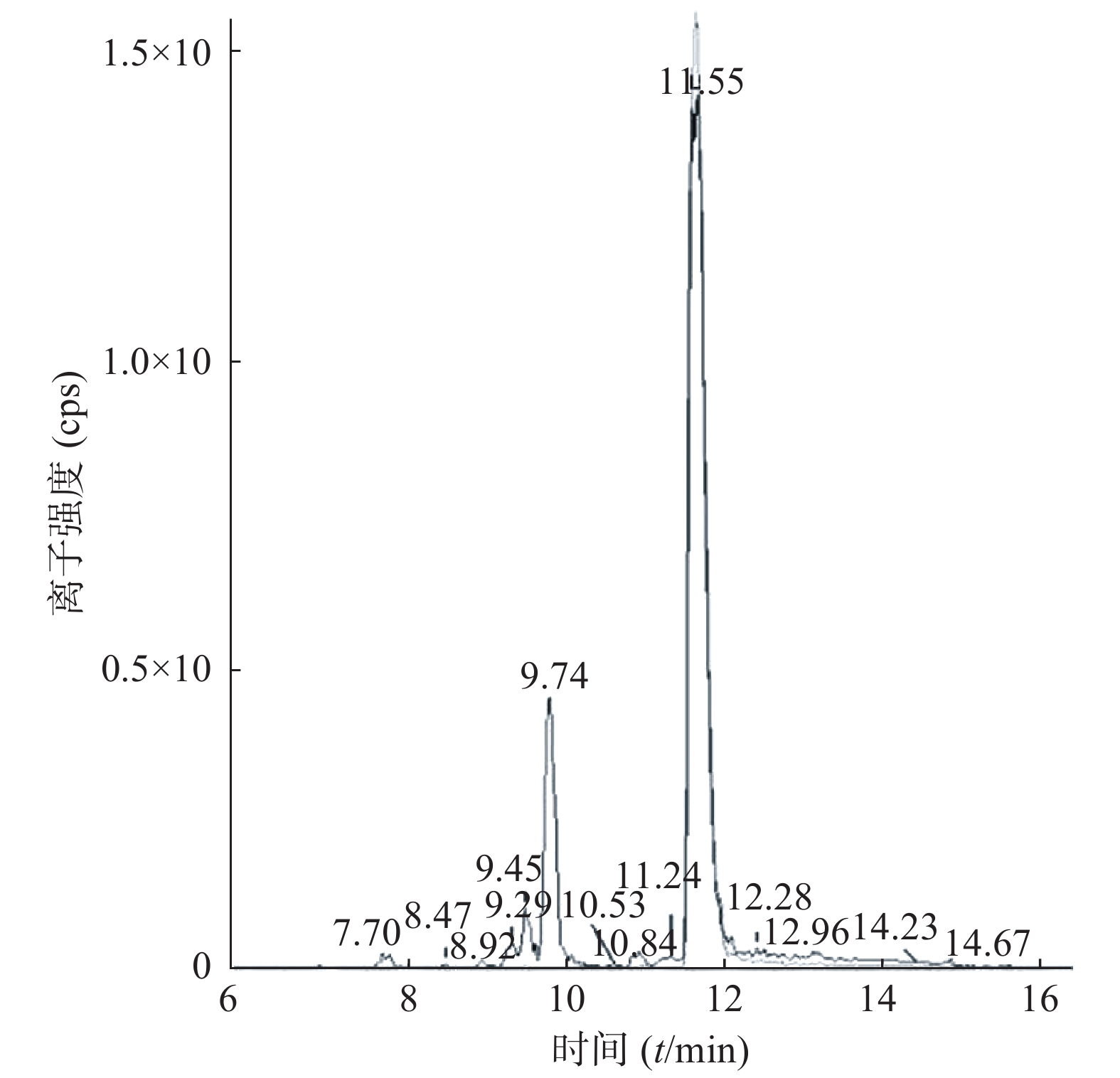
课题组进一步对苄普地尔开展了人肝微粒体中代谢产物研究,结果见表2、图3和图4。发现在经人肝微粒孵化后的样品中除原形药物(M0,m/z 367)外,在保留时间为9.8 min处检测到1个色谱峰,命名为M1,其m/z为383。推测其分子式组成为C24H34N2O2,比原形增加1个O,可能为单氧化代谢产物。在MS/MS扫描质谱图中,由M1获得的主要碎片离子为m/z 312、212、184(图4),其中m/z 312、212比原形的主要碎片离子m/z 296、196,相对分子质量增加16,而碎片184与原形的相同,且未见相对分子质量少18的碎片,推测其为苯环羟基化代谢产物。
表 2 苄普地尔在肝微粒体孵化体系中的代谢产物信息编号 代谢途径 质荷比 分子式 保留时间(t/min) M0 原形 367 C24H34N2O 11.6 M1 氧化 383 C24H34N2O2 9.8 4. 结论
基于老药新用的药物设计思想,课题组验证发现钙离子拮抗剂苄普地尔具有优秀的抗肿瘤活性和较强的p53-MDM2蛋白结合抑制活性。进一步通过免疫印迹试验发现,苄普地尔能显著降低MDM2蛋白的表达,而且呈剂量依赖。体外代谢研究发现,苄普地尔在人肝微粒体中的代谢产物主要是苯环羟基化单氧化代谢产物。研究结果表明,苄普地尔可作为p53-MDM2蛋白结合小分子抑制剂先导化合物,用于后续的结构优化设计研究。
-
表 1 两组患者一般资料比较
项目 对照组 试验组 t/χ2 P 性别 − − 0.406 0.524 男 33 31 − − 女 19 23 − − 年龄(岁) 59.75±15.81 61.43±15.49 −0.551 0.583 文化程度 − − 2.944 0.229 初小 3 6 − − 中学 28 34 − − 专科及以上 21 14 − − 婚姻状况 − − 0.597 0.440 已婚 36 41 − − 离婚或丧偶 16 13 − − 独居 − − 0.366 0.545 是 10 13 − − 否 42 41 − − 表 2 两组患者便秘自评量表治疗前、治疗后对比
治疗天数 对照组 试验组 t/χ2 P 治疗前 2.57±0.72 2.49±0.74 0.551 0.583 治疗后14 d 1.86±0.62 1.64±0.66 1.715 0.089 治疗后28 d 1.45±0.56 1.05±0.37 4.323 <0.001 表 3 两组患者治疗前、治疗后生活质量比较
治疗天数 对照组 试验组 t/χ2 P 治疗前 100.42±12.59 99.89±16.46 0.187 0.852 治疗后14 d 91.67±12.57 89.39±15.65 0.827 0.41 治疗后28 d 91.85±9.81 84.35±10.48 3.797 <0.001 表 4 两组患者治疗后综合评价对比
评价项目 对照组 试验组 t/χ2 P 经济成本(元) 146.39±21.70 95.50±4.81 16.81 <0.001 发生腹泻的次数 4.83±3.02 2.56±1.42 4.981 <0.001 阿片类药物使用
剂量增加(例数)42 35 21.736 <0.001 -
[1] TACHI K, AGYEI-NKANSAH A, ARCHAMPONG T. Hepatocellular carcinoma in Ghana: a retrospective analysis of a tertiary hospital data[J]. Pan Afr Med J, 2020, 36:43-50. [2] SURESH N V, HARRIS J, CHORATH K, et al. Clinical practice guidelines in the management of breakthrough cancer pain: a systematic review using the appraisal of guidelines for research and evaluation(AGREE II)instrument[J]. Pain Manag Nurs, 2022, 23(4):411-417. doi: 10.1016/j.pmn.2022.02.010 [3] 陈泽刚, 赵春妮, 张林松. 便秘通对癌症患者阿片类药物相关便秘的疗效及安全性研究[J]. 中国全科医学, 2019, 22(25):3144-3148. [4] SCARBOROUGH B M, SMITH C B. Optimal pain management for patients with cancer in the modern era[J]. CA Cancer J Clin, 2018, 68(3):182-196. doi: 10.3322/caac.21453 [5] 侯玉丽, 郭鸿雁, 王忠, 等. APRI与血氨联合对肝硬化并肝性脑病的诊断价值评估[J]. 北京医学, 2018, 40(4):289-292,385. [6] National Health Commission of the People’s Republic of China. 癌症疼痛诊疗规范(2018年版)[J]. 临床肿瘤学杂志, 2018, 23(10):937-944. [7] MIA S H, MICHAEL I B, STEPHANIE A, et al. Oxycodone for cancer-related pain[J]. Cochrane Database Syst Rev, 2022, 6(6):CD003870. [8] 方秀才. 罗马Ⅳ诊断标准在慢性便秘诊断中的应用[J]. 中华胃肠外科杂志, 2016, 19(12):1321-1323. doi: 10.3760/cma.j.issn.1671-0274.2016.12.001 [9] LI J W, GOH B B G, CHANG P E, et al. Barcelona Clinic Liver Cancer outperforms Hong Kong Liver Cancer staging of hepatocellular carcinoma in multiethnic Asians: real-world perspective[J]. World J Gastroenterol, 2017, 23(22):4054. doi: 10.3748/wjg.v23.i22.4054 [10] 李虹义, 魏振军, 刘端祺. 阿片类药物相关性便秘的诊疗[J]. 中国肿瘤临床, 2015, 42(12):603-607. doi: 10.3969/j.issn.1000-8179.20141909 [11] 邹玲, 代金刚. 基于“子午流注”理论解析中医时辰导引及其应用[J]. 中医药学报, 2021, 49(7):6-9. [12] 宋玉磊, 林征, 林琳, 等. 中文版便秘患者症状自评量表的信度与效度研究[J]. 护理学杂志, 2012, 27(7):73-76. doi: 10.3870/hlxzz.2012.07.073 [13] 万克艳, 李微, 杨铮, 等. 基于FACT-Hep量表的肝癌患者生活质量影响因素分析[J]. 广东医学, 2015, 36(18):2889-2893. [14] 薛楚, 刘思雪, 黄芳. 罂粟科植物罂粟、延胡索和岩黄连镇痛作用的研究进展[J]. 药学研究, 2019, 38(5):290-294. [15] 袁伟琛, 李慧杰, 齐元富. 中医药治疗恶性肿瘤相关性便秘研究进展[J]. 山东中医药大学学报, 2022, 46(6):776-781. [16] 张强, 邵明义, 王琳琳, 等. 中医药治疗原发性肝癌研究述评[J]. 河南中医, 2021, 41(3):454-457. [17] 张天宏, 刘秀凤, 王华, 等. 姜砂半夏纳米贴治疗疾病终末期患者恶心呕吐疗效及对肿瘤患者QOL影响[J]. 药学实践与服务, 2023, 41(6):380-384. -





 下载:
下载:

 下载:
下载: 

