-
苦参为豆科植物苦参(Sophora flavescens Ait.)的干燥根,春秋二季采挖,除去根头及支根后洗净、干燥,或趁鲜切片、干燥,是我国传统中药,在全国大部分地区均产;味苦,性寒,归心、肝、胃、大肠、膀胱经,具有清热解毒、燥湿、杀虫、利尿及抗炎镇痛的功效,能够用于治疗热痢、便血、黄疸尿闭、赤白带下、皮肤瘙痒、湿疹、湿疮等症状,最早记载于《神农本草经》[1]。苦参的多种复方制剂已在临床上广泛应用,其中主要有效成分包括苦参碱和氧化苦参碱[2]。现代药理学研究表明,苦参具有抗炎、抗肿瘤、抗心律失常以及抗病原微生物等多种药理作用[3]。本文将对苦参的化学成分、药理作用、复方制剂及苦参碱的结构修饰进展进行综述,以期为苦参的临床应用及新药研发提供理论依据。
-
现代研究表明,苦参因含丰富的化学成分而具有多种药理作用,其中苦参碱和氧化苦参碱作为中药苦参最主要的活性成分,在抗炎、抗肿瘤、抗心律失常、抗病原微生物等多方面作用显著。现将苦参碱和氧化苦参碱的药理作用进行概述。
-
苦参碱和氧化苦参碱对多种慢性或急性炎症均具有良好的抗炎作用[3,5]。有研究表明,苦参碱能够抑制脂多糖(LPS)诱导的巨噬细胞分泌白细胞介素-6(IL-6)、IL-1β和肿瘤坏死因子(TNF-α)等炎症因子[6];苦参碱抑制炎症因子产生与其抑制核转录因子κB(NF-κB)和丝裂原活化蛋白激酶(MAPK)信号通路有关。苦参碱抑制促炎因子的产生,可预防无乳链球菌感染引起的细胞损伤[7]。苦参碱还可以改善阿尔兹海默症小鼠的学习和记忆障碍以及神经炎症,这一作用主要是通过抑制对海马组织中小胶质细胞活化和还原型辅酶ⅡNADPH)氧化酶的表达来实现的[8]。过敏性接触性皮炎(ACD)是一种高度流行的炎症和免疫性皮肤病,常伴有持续的疼痛和瘙痒,氧化苦参碱可通过抑制环氧化酶、炎症介质前列腺素的合成以及花生四烯酸的代谢转化来产生镇痛、止痒和抗炎作用[9]。此外,苦参碱可通过抑制NF-κB信号通路,减少炎症和改善肺血管重塑,逆转肺动脉平滑肌细胞的增殖和凋亡的不平衡,从而治疗缺氧性肺动脉高压[10]。
-
苦参碱和氧化苦参碱作为中药苦参的主要有效成分,可通过多种途径发挥抗肿瘤作用。有研究发现氧化苦参碱通过增加肿瘤细胞G0/G1期、减少S期,从而使肿瘤细胞的增殖停留在G2/M期,达到抑制肿瘤细胞增殖的作用[11]。另外苦参碱还可以增强非编码小RNA 分子miR-22的表达,阻断丝裂原活化的细胞外信号调节激酶/细胞外调节蛋白激酶(MEK/ERK)信号通路,促进结肠癌细胞的凋亡并抑制结肠癌细胞的进一步生长[12]。细胞侵袭和迁移是肿瘤的主要生物学特征之一[13],也是临床上治疗肿瘤的难点,氧化苦参碱能够参与调节多种肿瘤细胞的侵袭性转移[14],其中最有可能通过激活NF-κB信号通路达到抗肿瘤作用[15]。端粒酶作为一种基本的核蛋白反转录酶,能够控制端粒的长度,端粒酶活性在正常细胞中较低,在癌细胞中上调,导致无限的细胞增殖和肿瘤生长[16],有结果显示苦参碱能够剂量依赖的降低端粒酶的活性,因此苦参的抗肿瘤作用还可能与端粒酶有关[17]。
有研究发现,肝癌细胞经苦参碱处理后数量逐渐减少,且形态逐渐变圆,开始出现不完整的细胞,甚至出现细胞碎片,同时与调控肿瘤细胞增殖、发育和死亡相关的信号通路ERK1/2-MAPK表达显著下调,这也表明了苦参碱可通过该信号通路抑制肝癌细胞的存活[18-19]。有实验研究氧化苦参碱对5-氟尿嘧啶耐药结肠癌细胞的体外致敏情况,结果表明,氧化苦参碱可以调节肿瘤细胞的上皮-间质转化并抑制NF-κB信号通路,进而作为一种潜在药物来改善5-氟尿嘧啶化学耐药性[20]。
-
心律失常是心血管疾病中非常重要的一种疾病,是由心脏起搏和传导功能障碍引起的心跳节律和频率异常,在中医学中主要表现为心悸,是心血管疾病的常见症状和多发病之一[21]。《神农本草经》中有记载:“苦参…主心腹气结,癥瘕积聚,黄疸,溺有余沥,逐水,除痈肿。”《名医别录》有关于苦参具有宁神定悸功效的记载:“苦参…养肝胆气,安五脏,定志,益精,利九窍”。
研究表明,氧化苦参碱预处理心室肌细胞后,不仅能够抑制乌头碱诱导的大鼠心律失常,还能延缓心律失常的发作、缩短持续时间,降低死亡率[22]。病理性心脏纤维化也是心血管疾病的常见特征[23]。苦参碱能够显著抑制心脏成纤维细胞的增殖、迁移及胶原蛋白的产生,可能是通过调节小鼠的核糖体蛋白S5/p38丝裂原活化蛋白激酶(RPS5/p38 MAPK)信号转导来实现这一作用,从而减轻心脏纤维化[24]。在氧化苦参碱缓解心律失常的过程中,还伴随着多种离子通道的变化,氧化苦参碱通过降低L型钙电流(ICa,L)、增强瞬时外向钾电流(Ito)和抑制内向整流钾电流(IK1)来缩短大鼠心室肌细胞动作电位的持续时间[25]。在体内氧化苦参碱经进一步的代谢可以转化为苦参碱,二者均具有通过调节钠电流和钙电流通道达到抗心律失常的作用[26]。
-
苦参具有广谱抗菌活性,其有效成分对多种细菌和真菌微生物,如大肠杆菌、烟曲霉菌具有明显的抑制作用[27-28]。有结果表明,氧化苦参碱能够通过抑制真菌烟曲霉的生长、生物膜的形成、真菌细胞的完整性和分生孢子的黏附能力来降低真菌的负荷能力以及产生的相应炎症反应[27]。另一结果发现细菌生物膜的形成能力与耐药性之间呈正相关,苦参碱能够通过调控群体的感应系统来抑制大肠杆菌菌株生物膜的形成进而发挥较好的抗菌效果[28]。
-
复方苦参注射液(CKI)是一种中成药制剂,主要是由苦参和土茯苓,以及醋酸、氢氧化钠、聚山梨酯80等辅料经过一系列现代制剂工艺加工制成,主要成分包括黄酮类、生物碱类、糖苷类以及酚酸类等,具有清热利湿、凉血解毒、散瘀止痛的功效,可用于抗炎[29]、抗肿瘤[30]和抗纤维化[31]。
抗肿瘤作用是CKI主要的临床应用。研究显示,CKI可以联合不同的化疗方案治疗晚期结肠癌,具有协同治疗效果、减轻副作用、缓解疼痛和治疗癌症腹水的作用,且其安全性良好[32]。苦参碱和氧化苦参碱是CKI中的主要活性成分,CKI与化疗联合治疗胃癌的过程中,氧化苦参碱可能通过作用于TGFβ Ⅱ型受体(TβRⅡ),进而调节TGFβ/Smad信号通路,控制细胞周期并抑制胃癌细胞的增殖[33];另一项研究显示,CKI通过调控TNF信号通路诱导的血管细胞黏附分子-1(VCAM1)来抑制胃癌的上皮-间充质样细胞转化,有效抑制胃癌细胞的生长和转移[34]。CKI能够降低放射性肺炎患者的辐射损伤程度和毒性,这一作用可能与CKI有效成分苦参碱和氧化苦参碱的抗氧化作用有关,另有研究显示,CKI通过阻断瞬时受体电位香草酸亚型1(TRPV1)抑制ERK减少肿瘤相关促炎细胞因子的产生,并减轻癌症相关疼痛[35-36]。
-
苦参凝胶来源于《金匮要略》中的苦参汤,是由苦参中的苦参总碱制成,制剂组成较为简单,与复方制剂相比较具有质量稳定可控、疗效明确、无药物间相互作用、不良反应较少的优势,且水凝胶是一种聚合物在水中溶胀形成的药物传递系统,具有较高的含水量,适合用于黏膜、皮肤等给药途径[37]。苦参凝胶可在阴道内长时间滞留,具有抗菌、保护阴道黏膜等优点,是治疗妇科慢性炎症的理想药物[38]。苦参凝胶与氟康唑胶囊联合使用能够提高药物的抗真菌活性,治疗霉菌性阴道炎[39];在临床上对慢性宫颈炎患者采用苦参凝胶进行术后治疗,能够显著提升患者的治疗效果,促进患者进一步康复[40]。
-
在临床上,苦参相关复方制剂还可以与其他制剂联合使用,以发挥更强的抗炎、抗病原微生物等作用。当归苦参丸与克林霉素磷酸酯凝胶联合应用能够治疗累及面部及毛囊皮脂腺的炎症性皮肤疾病,有效降低炎症反应[41];五味苦参胶囊联合水杨酸制剂治疗溃疡性结肠炎,抑制炎症因子表达,增强肠道屏障功能[42];复方苦参止痒软膏联合糠酸莫米松乳膏使用,对临床上慢性湿疹的治疗具有显著效果,患者的症状与炎症表现均有明显的改善,机体的免疫功能增强,值得临床推广应用[43]。
-
苦参碱具有抗肿瘤、抗纤维化、抗炎、抗心律失常等多种药理活性[44],然而其临床应用还存在一些问题,例如苦参碱的活性相对较弱,在体外的有效浓度为50~200 μmol/L;脂溶性较低,生物利用度差,体内半衰期短,一项关于苦参碱在大鼠中药代动力学的研究表明,苦参碱的生物利用度仅为18.5%;苦参碱的毒性最常见的是肝毒性和神经毒性[45-46]。有研究表明,氧化苦参碱和苦参碱对小鼠均有一定的毒性,但氧化苦参碱的毒性明显弱于苦参碱,推测其毒性差异可能与苦参碱环状结构中的叔胺结构氧化为季胺有关,故有必要对苦参碱进一步进行结构改造和化学修饰,以获得更好的生物活性[47-48]。
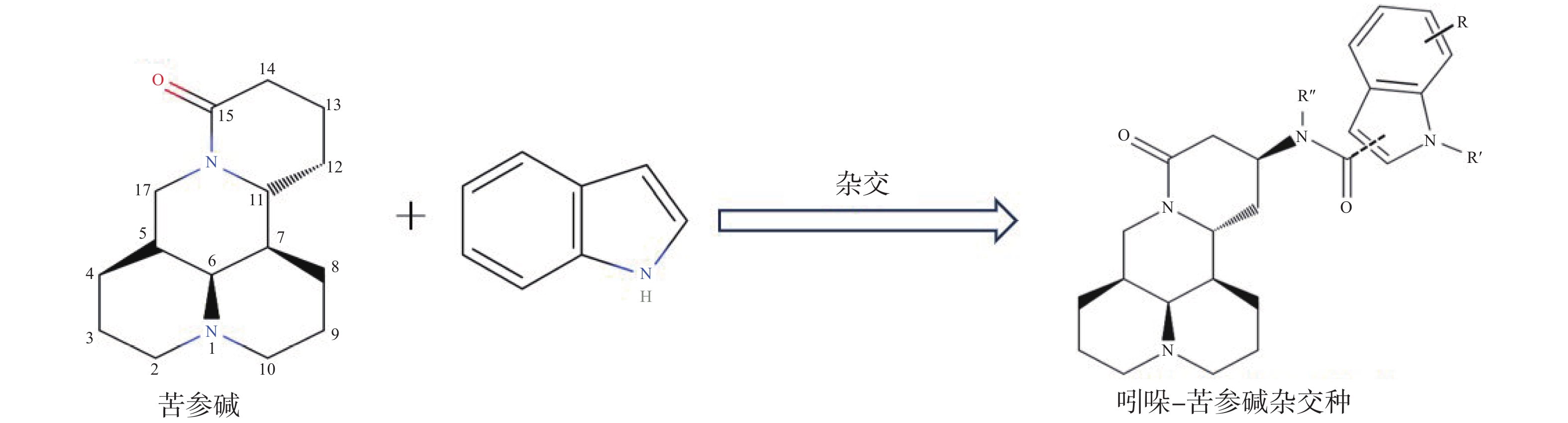
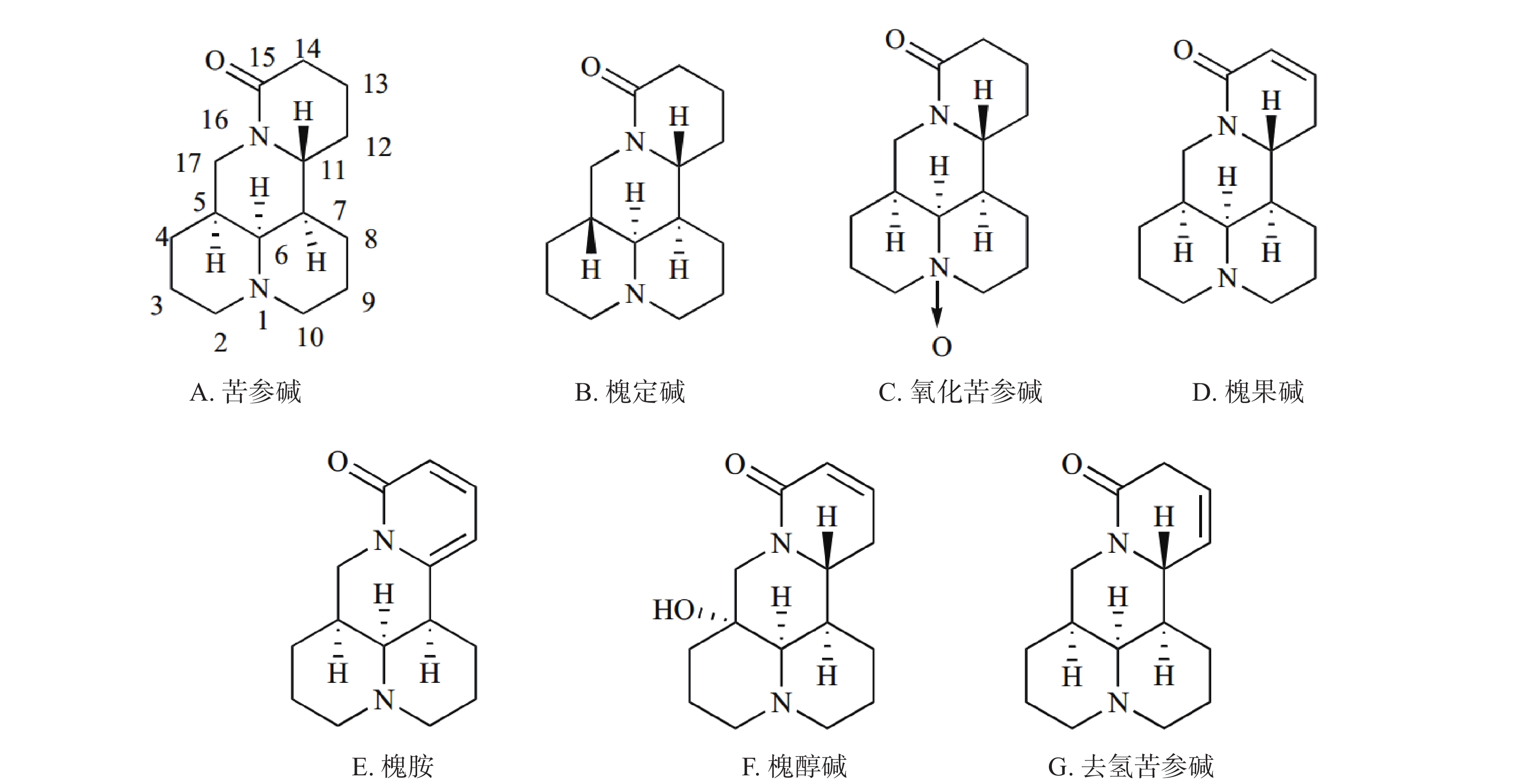
苦参碱(C15H24N2O)具有独特的双喹啉四环结构,包含有A/B喹啉环和C/D喹啉环两个不对称的喹啉片段(图1A)。近年来,药物学专家在研究苦参碱衍生物时,常以苦参碱的C-13、C-14、C-15及D环开环等方面作为切入点来进行苦参碱的结构改造。
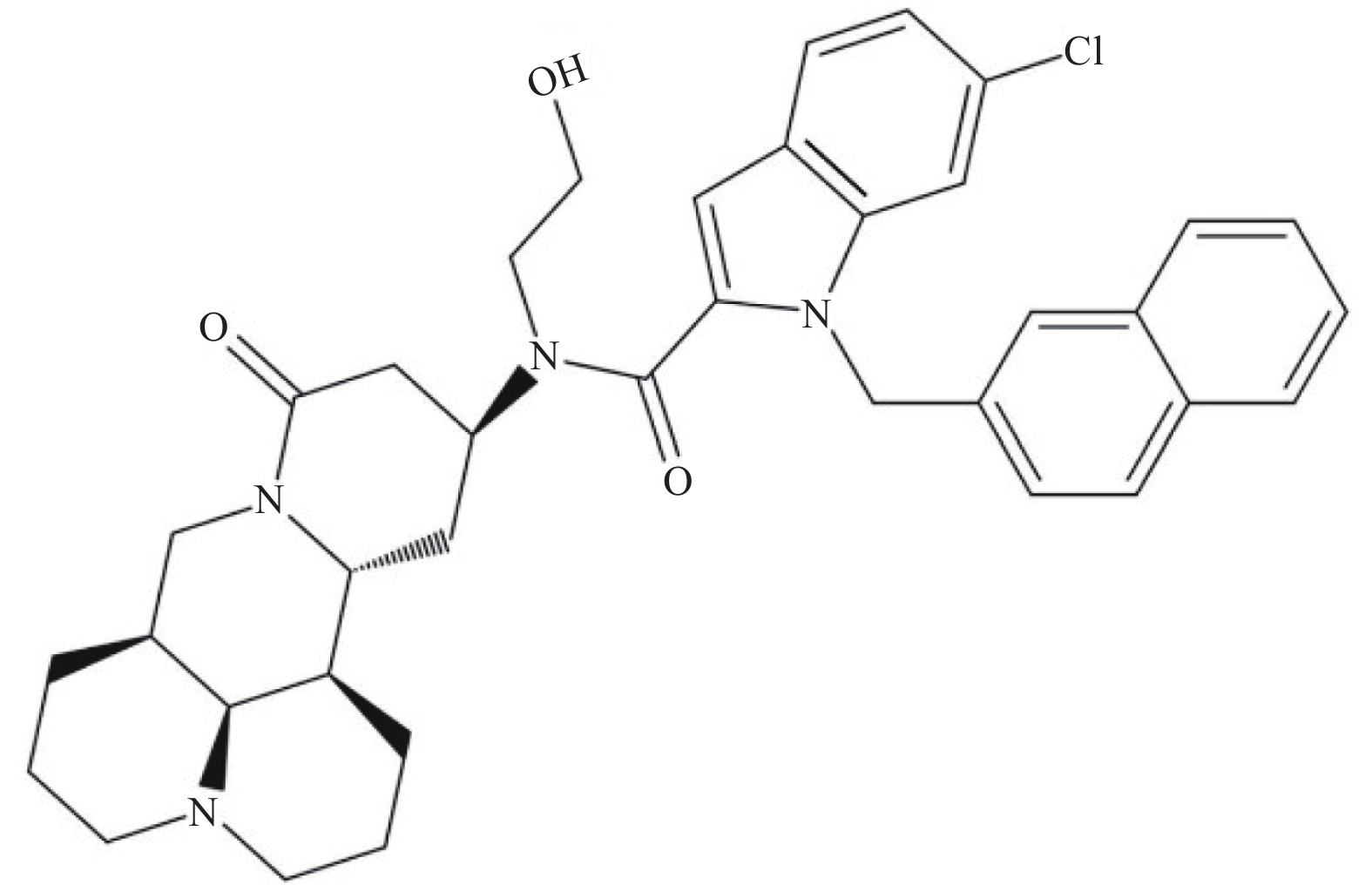
C-13位是提高苦参碱药理活性最常见的修饰位点之一,Li等[49]研究发现在苦参碱的C-13位引入吲哚支架,设计合成一系列吲哚-苦参碱杂交种(图2),其中杂交种8 g(图3)的抗癌活性和对癌细胞的选择指数显著高于苦参碱,进一步研究发现8 g靶向作用于线粒体,可破坏细胞内的能量供应,抑制癌细胞的增殖,因此可作为一种重要的潜在抗癌剂。
有研究显示,在苦参碱的C-14位引入苯甲酰基,进而合成一系列苦参碱衍生物,其中大部分苦参碱衍生物对多种癌细胞,如肺癌细胞A594、乳腺癌细胞MCF-7、胃癌细胞SGC-7901和肝癌细胞Bel-7402的IC50值比苦参碱低17~109倍,并且抑制肿瘤细胞的迁移,展现出更强的抗癌作用[50]。
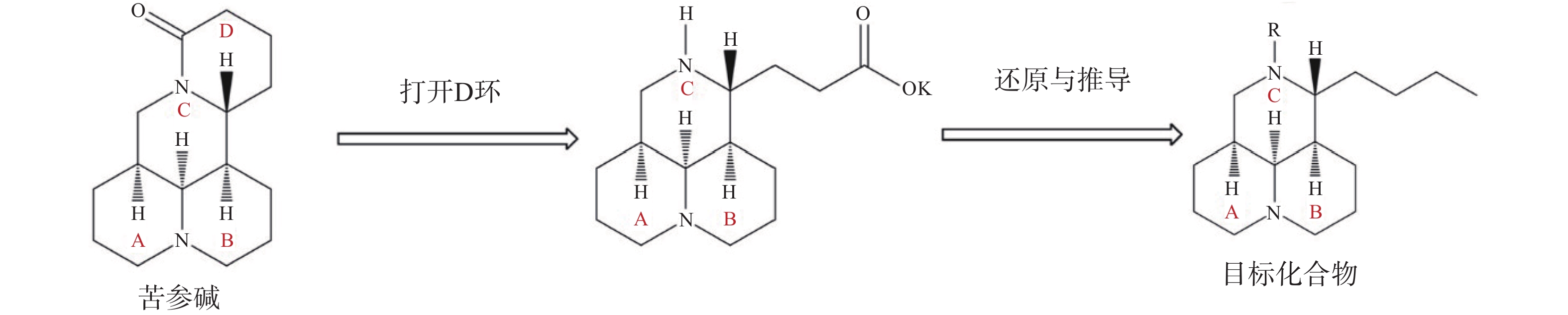
苦参碱D环打开后,可将C-11侧链还原为丁基,并进一步在氮原子上引入磺酰基、酰基或烷基等,得到多种苦参碱衍生物(图4)。与苦参碱相比,这些化合物在体内和体外均表现出良好的抗烟草花叶病毒(TMV)活性,这可能是与氮及侧链上的取代基有关[51]。
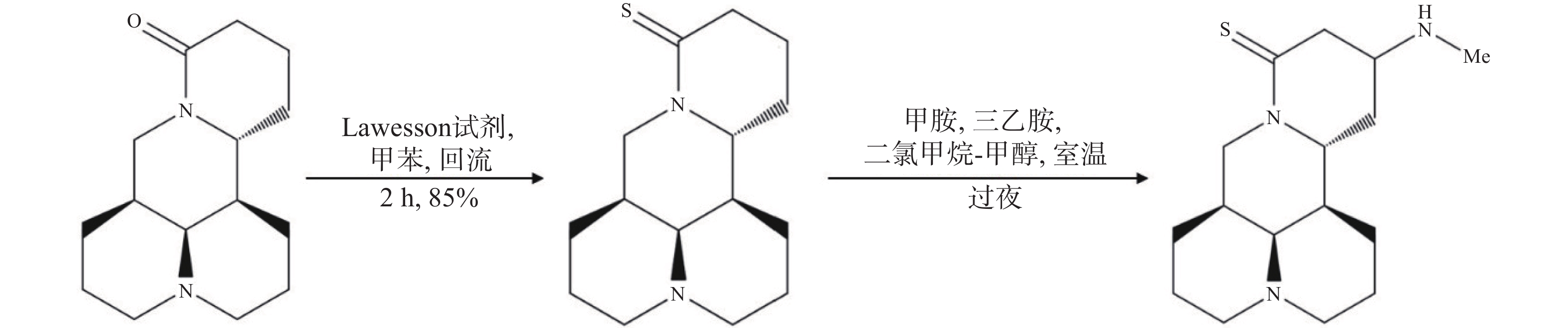
苦参碱结构改造方法还包括将苦参碱转化为硫代苦参碱,并在酮β位引入多种氨基,合成一系列苦参碱衍生物,其中,Hu等[52]合成的MASM(C16N3H27S),又称M19,即(6aS, 10S, 11aR, 11bR, 11cS)-10甲氨基-十二氢-3a, 7-二氮杂苯并 [de] 蒽-8-硫酮(图5),具有较好的药理作用,与苦参碱相比具有更好的抗炎和抗纤维化的作用以及更低的毒性和副作用[53]。MASM的体外有效作用浓度为1~20 μmol/L;MASM的抗炎活性较苦参碱和槐果碱相比也有显著提高,1~10 mg/kg的MASM抗炎和抗纤维化作用与30~100 mg/kg的苦参碱相当[54]。有研究显示,MASM经灌胃给药后约1.3 h即可达到血浆药物峰值浓度,与苦参碱达峰时间2.1 h相比,口服MASM可以快速吸收,更快地发挥药理作用[55];毒性实验结果显示,MASM对小鼠的体重、肝肾等器官重量和生化指标的不良影响均很小或无影响,表明了MASM的无毒性或低毒性[55]。另有结果表明,脓毒症发作后仅使用1 mg/kg的MASM治疗即可减少全身和组织炎症反应,减轻多器官损伤,提高总生存率,这可能是与RPS5介导的抑制NF-κB和MAPK的激活以及降低促炎介质的表达有关[47];MASM还能够抑制星形胶质细胞激活,降低其炎症反应,改善血脑屏障功能,维持星形胶质细胞的功能,具有显著缓解免疫性脑脊髓炎的发展的功能[54];此外MASM能够显著抑制肝癌细胞的增殖,诱导细胞凋亡和生长停滞,有望为治疗肝细胞癌提供新的治疗方法[56]。
-
苦参作为临床上常用的中药,应用广泛,且在《神农本草经》中具有重要的地位,在现代临床研究中,苦参能够具有很高的药用价值和科研价值主要是其包含苦参碱和氧化苦参碱等有效成分。然而,由于苦参中有效成分的活性相对较低,生物利用度差且存在毒性作用,严重影响了苦参的药效,因此可以将苦参碱进行结构修饰来增强药物的活性、降低用量和药物的毒性作用。目前,对于苦参化学成分及药理作用的研究有了一定的进展,但一些机制研究还有待进一步完善,同时苦参碱衍生物的深入研究对中药苦参的进一步开发和利用也具有重要意义。
Research progress on Sophora Flavescens of Traditional Chinese Medicine
-
摘要: 中药苦参为豆科植物苦参的干燥根,始载于《神农本草经》。苦参中含有多种活性成分,主要包括苦参碱和氧化苦参碱,具有抗炎、抗肿瘤、抗心律失常与抗病原微生物等多种药理作用,临床上苦参复方制剂主要包括复方苦参注射液、苦参凝胶等,可用于治疗多种癌症,改善皮肤、黏膜瘙痒疼痛等多种症状。由于苦参碱生物利用度较差,因此需要对苦参碱进行结构改造,其中,苦参碱衍生物MASM仅需较低浓度即可对脓毒症和肝纤维化等疾病具有较好的治疗效果。主要对苦参的化学成分、药理作用、复方制剂及苦参碱的结构修饰进行论述,旨在为中药苦参的临床应用和新药研发提供理论依据。Abstract: Sophora Flavescens is the dried root of the leguminous plant Sophora Flavescens Ait. It was first published in Shen Nong's Herbal Classic. Sophora Flavescens contains a variety of active ingredients, mainly including matrine and oxymatrine, with anti-inflammatory, anti-tumor, anti-arrhythmia and disease-resistant pathogenic microorganisms and other pharmacological effects. Clinically, the compound preparations of Sophora Flavescens include Compound KuShen injection and KuShen gel and so on, which can be used to treat many types of cancers and improve skin, mucous pruritus, pain and other symptoms. Due to the poor bioavailability of matrine, which structure needs to be reformed. MASM, matrine derivative, only needs a low concentration to have a good therapeutic effect on sepsis and liver fibrosis. In this article, the chemical composition, pharmacological effects, compound preparations and structural modification of matrine were mainly discussed, aiming to provide a theoretical basis for the clinical application of Sophora Flavescens and the research and development of new drugs.
-
Key words:
- Sophora flavescens Ait /
- matrine /
- oxymatrine /
- pharmacological effect /
- MASM
-
多剂量滴眼液须使用抑菌剂,以防止使用过程中和货架期内微生物污染和繁殖,但是抑菌剂对眼的伤害不容忽视,多国药典及抑菌剂管理规范[1]均要求处方中抑菌剂的浓度必须在有效性和安全性方面得到合理性支持,保证抑菌剂浓度最低但又能发挥抑菌作用,并规定滴眼液标签必须注明抑菌剂种类和标示量,且实际含量应在标示量的±20%以内。《中国药典》2020版收载了45个滴眼剂品种,只有12个列入抑菌剂检查项,仅占26.7%[2-4]。目前市售滴眼液标签多数未按照《中国药典》2020版四部通则0105眼用制剂[5]要求标明抑菌剂种类和标示量,滴眼液中抑菌剂的使用和质量安全控制缺乏有效监管。
目前滴眼液允许使用的抑菌剂主要有六大类:羟苯酯类、季铵盐类、有机酸类、醇类、酚类和有机汞类,如硫柳汞。硫柳汞在滴眼剂、滴鼻剂、疫苗、化妆品中广泛使用,然而,汞对人体具有潜在的危害,摄入过量的汞可造成神经系统、肾脏、皮肤的损伤。滴眼剂中抑菌剂浓度过高会对眼上皮细胞产生损伤,有研究者在对药源性角膜上皮病变病例研究时发现,有患者使用防腐剂为硫柳汞的滴眼剂后引起了明显的点状角膜上皮损害[6-8]。《中国药典》2020年版三部通则
3115 “含量测定法”中收载硫柳汞测定方法[4],采用滴定法和原子吸收分光光度法,二部[3]各论阿昔洛韦滴眼剂项下采用高效液相色谱方法,另外文献资料收载的测定法主要有:原子荧光光谱分析法、冷原子吸收光谱法、硫氰酸铵滴定法、二硫腙滴定法、二硫腙比色法等[9-12],这些方法的共同点是有机汞首先被消解成无机汞,然后测定无机汞的含量。上述方法操作步骤繁琐,专属性不强,不适用于复杂药物制剂中痕量加入的有机汞防腐剂快速准确检测。为此,本研究建立了一种通用型HPLC法用于测定滴眼液中抑菌剂硫枊汞的含量。1. 仪器与试药
Waters高效液相色谱仪;美国赛多利斯MSE225S型电子天平。硫柳汞(含量97.0%,批号T1605112,Aladdin公司);醋酸苯汞(纯度:97.0%,批号P27127,Sigma公司)。甲醇、三乙胺为色谱纯,磷酸为分析纯,水为超纯水。
以收集到的4个制药企业(A、B、C|、D)生产的6批滴眼液为供试品,处方中硫柳汞含量均不同(企业A双氯芬酸钠滴眼液批号150301、150802、160801;企业B阿昔洛韦滴眼液批号16090401;企业C盐酸林可霉素滴眼液批号160501;企业D苄达赖氨酸滴眼液批号3160703)。
2. 方法与结果
2.1 色谱条件
色谱柱资生堂MGII-C18柱(4.6 mm×250 mm,5 μm),以1%三乙胺溶液(磷酸调节pH值至3.0)为流动相A,以甲醇为流动相B;按表1进行梯度洗脱;柱温为40 ℃;检测波长为222 nm;流速为1 ml/min;进样体积20 µl。
表 1 梯度洗脱程序时间(min) 流动相A(%) 流动相B(%) 0 50 50 2 50 50 17 10 90 20 10 90 20.1 50 50 27 50 50 2.2 溶液制备
2.2.1 系统适用性考察溶液配制
精密称取硫柳汞对照品约10 mg,置100 ml量瓶中,用水溶解并稀释至刻度,摇匀;另取硝酸苯汞对照品约10 mg,置100 ml量瓶中,用甲醇超声溶解并稀释至刻度,摇匀;取上述两种液体等量混合,即得。
2.2.2 对照品溶液制备
取硫柳汞对照品适量,精密称定,加水溶解并稀释成0.2 mg/ml的溶液作为对照品储备液;精密量取储备液适量,加水分别稀释制成20 μg/ml溶液(或根据供试品硫柳汞含量不同制备成其他相同浓度的对照品),作为对照品溶液。
2.2.3 供试品溶液制备
取滴眼液直接进样。
2.3 方法学考察
2.3.1 专属性试验
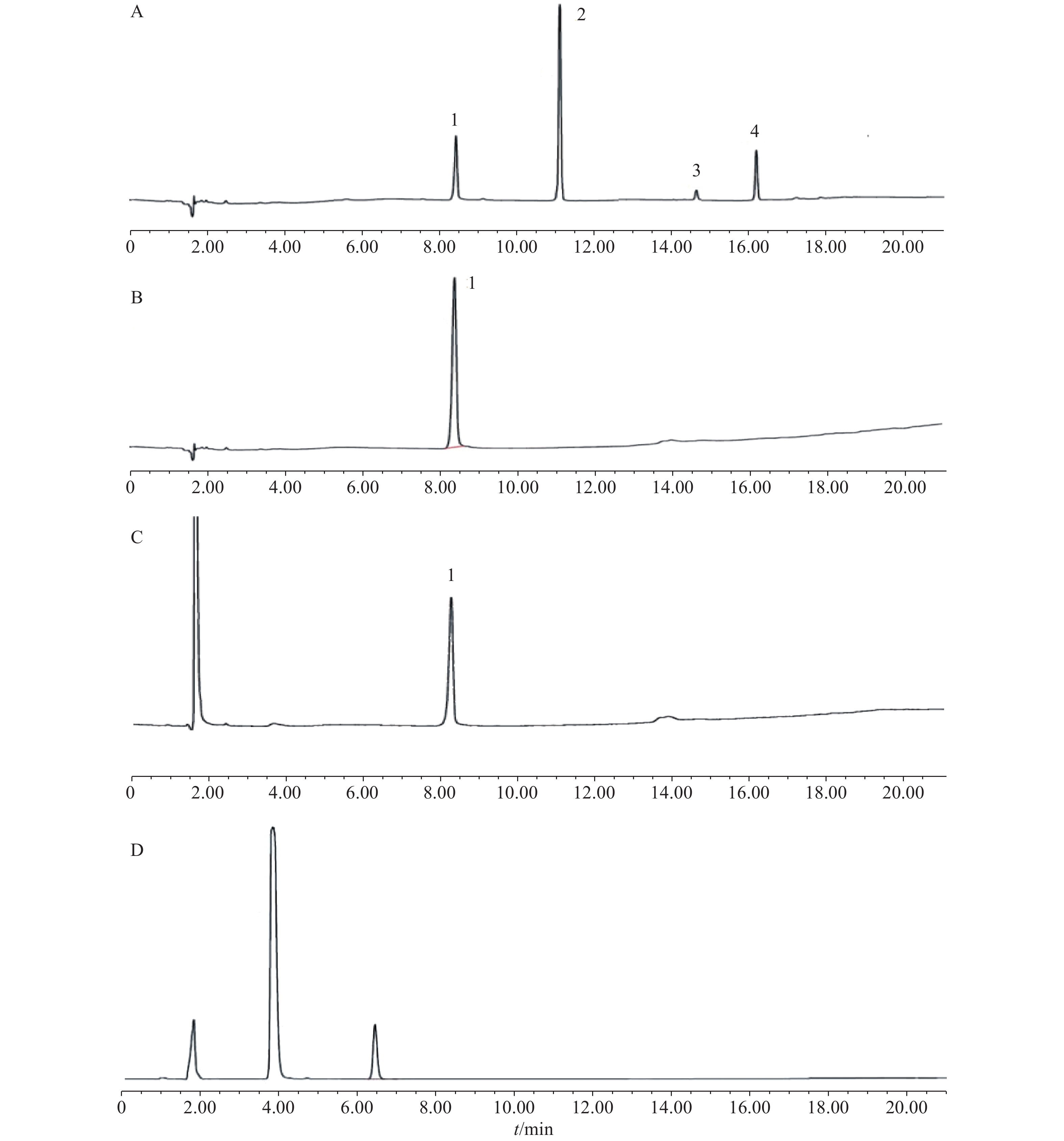
精密量取“2.2.1”项下系统适用性考察溶液、对照品溶液、供试品溶液(含硫柳汞)、滴眼液(不含硫柳汞)各20 μl,按“2.1”项色谱条件进样,记录色谱图,见图1。硫柳汞对照品溶液和硝酸苯汞对照品溶液混合后生成1-苯基汞-2-硫代乙基汞-水杨酸盐,以及其他产物,色谱图应存在4个色谱峰分别为:主峰硫柳汞、1-苯基汞-2-硫代乙基汞-水杨酸盐、硝酸苯汞以及一个杂质或其他反应产物,配制该溶液主要是考察专属性,筛选色谱柱和考察色谱系统的改变对分离的影响。图1A表明系统适用性考察用混合溶液各色谱峰之间均完全分离,系统适用性良好。图1D表明不含硫柳汞的滴眼液在硫柳汞峰处无色谱峰,不影响测定,可对未知抑菌剂的滴眼剂是否含有硫柳汞进行筛查。
2.3.2 线性关系考察
取硫柳汞对照品适量,精密称定,用水稀释成每1 ml约含硫柳汞4、10、20、60、80和200 μg的溶液,按“2.1”项下色谱条件试验。以对照品的质量浓度(μg/ml)为横坐标(X),峰面积为纵坐标(Y),绘制标准曲线,计算回归方程。硫柳汞回归方程为Y=
54413 X–77901 ,r=1.0,结果表明:硫柳汞在4.3~216.7 µg/ml范围内有良好的线性关系。精密量取线性对照品最低浓度约4.3 μg/ml的溶液,测得信噪比接近10∶1,将其作为定量限溶液,即定量限为4.3 μg/ml。2.3.3 精密度试验
精密量取“2.2.2”项下20 μg/ml硫柳汞对照品溶液,按“2.1”项下色谱条件连续进样6次,记录峰面积,计算RSD。结果硫柳汞峰面积的RSD为0.2%,表明仪器精密度良好。
2.3.4 稳定性试验
由于供试品溶液取原液没有制备过程,因此稳定性试验取对照品溶液进行,按“2.2.2”方法制备对照品溶液(23.2 μg/ml),取对照品溶液避光室温放置10 h,分别于1、3、5、7、9、10 h,取样分析,记录色谱图,比较硫柳汞峰面积变化情况,峰面积RSD为0.7%,显示稳定性较好。对照品溶液放置过夜后再次测定,峰面积有较明显降低,显示硫柳汞水溶液配制10小时内使用较好。
2.3.5 重复性试验
取三个企业A、B、C三批样品(批号分别为160801、16090401、160501)原液做为供试品溶液,按“2.1”项下色谱条件直接进样分析,平行测定6份,按外标法以峰面积计算硫柳汞的含量,考察方法重复性。结果RSD分别为0.7%、0.2%和3.4%,表明重复性良好。
2.3.6 中间精密度试验
在不同的日期换用不同的液相色谱仪和实验操作者,重复“2.3.5重复性试验”的操作,按“2.1”项下色谱条件连续进样,平行测定6份,作为中间精密度,合并重复性试验的6份测定结果考察方法中间精密度,12份结果硫柳汞含量RSD分别为0.5%、0.7%和2.7%。参考《中国药典》2020年版四部[5]指导原则9101“分析方法验证指导原则”,重复性试验精密度要求,含量为0.01%,RSD应小于4%,上述含量最大为0.015%,RSD均小于3%,表明中间精密度良好。
2.3.7 加样回收率试验
2.3.7.1 空白辅料溶液制备
按B企业阿昔洛韦滴眼液处方(抑菌剂为硫柳汞,标示量为20 μg.ml−1)制备,取甲基纤维素、氯化钠、无水磷酸氢二钠适量,加水稀释至
1000 ml,放置过夜,即得。2.3.7.2 对照品溶液制备
精密称取硫柳汞对照品(纯度97.0%)21.77 mg,置100 ml量瓶中,加水适量,振摇溶解并稀释至刻度,摇匀,作为对照品储备液。精密量取5 ml,置50 ml量瓶中,加水稀释至刻度,摇匀,作为对照品溶液。
2.3.7.3 供试品溶液(自制滴眼液)配制
精密量取对照品储备液2、5、3、5 ml,分别置25、50、25、25 ml量瓶中,加空白辅料溶液稀释至刻度,摇匀,即得80%、100%、120%、200%回收率供试品溶液(每浓度平行配制3份)。按“2.1”项下色谱条件进样20 μl,按外标法计算回收率,硫柳汞的回收率为98.3%~106.2%,平均回收率为102.1%,RSD为2.7%,结果见表3。
表 2 硫柳汞回收率试验结果阿昔洛韦
滴眼液投入量
(μg/ml)测得量
(μg/ml)回收率
(%)平均回
收率(%)RSD% 80%供试品 16.89 16.84 99.69% 102.1 2.7 16.73 99.08% 16.60 98.27% 100%供试品 21.12 21.41 101.39% 21.26 100.68% 21.08 99.81% 120%供试品 25.34 25.98 102.54% 25.99 102.56% 26.09 102.97% 200%供试品 42.23 44.74 105.94% 44.86 106.22% 44.59 105.58% 2.3.8 耐用性试验
取“2.2.1”项系统适用性考察溶液和批号为
150301 滴眼液样品,考察方法耐用性。结果表明,在不同的柱温(30、35、40 ℃)、流速(0.9、1.0、1.1 ml·ml−1)、流动相A的pH值(2.8、3.0、3.2、3.5)、流动相组成(初始有机相B比例40%、45%、50%、55%、60%)和不同色谱柱(资生堂公司MGII、Waters Sunfire、Phenomenex Luna)条件下测定系统适用性考察溶液,硫柳汞与各峰分离度好,样品150301 批硫柳汞含量测定结果RSD为2.8%,所建立的方法耐用性良好。2.4 样品测定
取4个制药企业6批含抑菌剂为硫柳汞的样品,以样品原液做为供试品溶液(n=2)。
对照品溶液制备:针对已知抑菌剂为硫柳汞且已知浓度的样品,取硫柳汞对照品适量,精密称定,加水溶解并稀释制成与供试品溶液中硫柳汞浓度相当的溶液;针对未知抑菌剂种类和浓度的滴眼剂筛查硫柳汞的含量,对照品溶液浓度可采用20 μg/ml或40 μg/ml(避光保存,10 h内使用)。
按“2.1”项下色谱条件进样分析,用外标法计算硫柳汞的含量(n=2),结果见表4。
表 3 样品测定结果序号 生产
企业品种名称 样品批号 标示量
(μg/ml)含量
(μg/ml)1 企业A 双氯芬酸钠滴眼液 150301 40 36.11 2 企业A 双氯芬酸钠滴眼液 150802 40 37.87 3 企业A 双氯芬酸钠滴眼液 160801 40 38.41 4 企业B 阿昔洛韦滴眼液 16090401 20 18.19 5 企业C 盐酸林可霉素滴眼液 160501 200 151.74 6 企业D 苄达赖氨酸滴眼液 3160703 30 26.30 3. 结果与讨论
3.1 检测波长的选择
USP收载的硫柳汞钠测定方法中,测定波长为222 nm[12],《中国药典》2020年版二部[3]各论阿昔洛韦滴眼液项下硫柳汞钠测定波长为262 nm。本文采用PDA检测器扫描,显示222 nm吸收强度大于262 nm,并且这两个波长处峰对称性以及与相邻杂质的分离情况一致,因此,测定波长选择为222 nm。
3.2 方法的适用性
本课题研究方法作为可以检测多种滴眼剂中抑菌剂硫柳汞含量的通用方法,需要具备普遍适用性。本课题专属性研究工作还包括将收集到的42种滴眼剂(不含抑菌剂硫柳汞,分别含羟苯甲酯、羟苯乙酯、苯扎溴铵、苯扎氯铵、三氯叔丁醇等)进样分析,考察是否在硫柳汞保留时间有出峰情况,同时回收试验将企业提供的十四种未加抑菌剂滴眼液进样分析,包含滴眼液常用的附加剂,均无干扰,方法专属性较好。
本课题研究方法拟用于各种不同活性成分的滴眼液中硫柳汞的测定,为了考察色谱条件变化对目标峰特性、分离度的影响,采用硫柳汞与硝酸苯汞混合液作为系统适用性考察溶液,硫柳汞与硝酸苯汞均在pH3.0~pH3.5、甲醇比例50%以上出峰较好,色谱峰对称性优于乙腈,因此采用pH3.0的甲醇系统作为流动相。。
3.3 样品测定结果的讨论
本次收集的6批样品,硫柳汞含量测定结果经药检机构复核基本一致。其中只有B企业1批阿昔洛韦滴眼液(批号16090401)在《中国药典》2020年版二部有硫柳汞含量测定方法,其他5批样品质量标准中均无抑菌剂含量测定方法,对批号为16090401的样品用所建立的方法与药典方法进行了比较,结果一致。根据样品测定结果,滴眼液中硫柳汞含量普遍低于处方标示量,并且测定结果显示随储存时间长含量下降多,尤其是企业C批号为160501的滴眼剂,硫柳汞标示量为200 μg/ml,实际测定结果低于标示量的80%,为151.74 μg/ml。经分析可能是由于硫柳汞不稳定,易在贮存过程中降解或见光分解[13],另外有文献报道“硫柳汞作防腐剂时易与塑料瓶有反应,故用塑料瓶包装的滴眼剂不宜添加该防腐剂”[14],这也可能是硫枊汞实测量低于标示量的原因之一。本文样品测定中6批样品均采用低密度聚乙烯瓶包装,贮存时间过长,硫柳汞可能与药包材反应造成含量下降。故建议生产企业注意滴眼液的贮存条件,另外对产品的包装材料进行相容性研究,从而避免不适用药品包装材料对产品质量的影响。
3.4 方法评价
本文建立的滴眼剂中抑菌剂硫柳汞的HPLC含量测定方法既可以对已知抑菌剂为硫柳汞和已知浓度的样品进行定量分析,亦可对未知抑菌剂种类和浓度的滴眼剂进行硫柳汞添加监督筛查及含量测定,具有准确性好、线性范围广、耐用性强、普适性高的特点,所建立方法可作为滴眼剂中抑菌剂硫柳汞含量测定通用检测方法,为抑菌剂合理使用、质量控制和安全评价提供参考。
-
[1] 国家药典委员会. 中华人民共和国药典(一部) 2020年版[S]. 北京: 中国医药科技出版社, 2020: 211. [2] SUN P, ZHAO W J, WANG Q, et al. Chemical diversity, biological activities and traditional uses of and important Chinese herb Sophora[J]. Phytomedicine, 2022, 100:154054. doi: 10.1016/j.phymed.2022.154054 [3] SUN X Y, JIA L Y, RONG Z, et al. Research advances on matrine[J]. Front Chem, 2022, 10:867318. doi: 10.3389/fchem.2022.867318 [4] LONG G Q, WANG D D, WANG J, et al. Chemical constituents of Sophora flavescens Ait. and cytotoxic activities of two new compounds[J]. Nat Prod Res, 2022, 36(1):108-113. doi: 10.1080/14786419.2020.1765340 [5] HUAN D Q, HOP N Q, SON N T. Oxymatrine: a current overview of its health benefits[J]. Fitoterapia, 2023, 168:105565. doi: 10.1016/j.fitote.2023.105565 [6] 杨雪梅, 吴刚. 苦参碱抑制LPS诱导巨噬细胞IL-1β、TNF-α分泌及机制研究[J]. 中国免疫学杂志, 2016, 32(6):820-824,837. doi: 10.3969/j.issn.1000-484X.2016.06.011 [7] LI L X, NIU H, ZHAN J W, et al. Matrine attenuates bovine mammary epithelial cells inflammatory responses induced by Streptococcus agalactiae through inhibiting NF-κB and MAPK signaling pathways[J]. Int Immunopharmacol, 2022, 112:109206. doi: 10.1016/j.intimp.2022.109206 [8] LI J, CHENG X Y, YANG H, et al. Matrine ameliorates cognitive deficits via inhibition of microglia mediated neuroinflammation in an Alzheimer’s disease mouse model[J]. Pharmazie, 2020, 75(7):344-347. [9] ZHU T, ZHOU D, ZHANG Z, et al. Analgesic and antipruritic effects of oxymatrine sustained-release microgel cream in a mouse model of inflammatory itch and pain[J]. Eur J Pharm Sci, 2020, 141:105110. doi: 10.1016/j.ejps.2019.105110 [10] LI M X, YING M F, GU S L, et al. Matrine alleviates hypoxia-induced inflammation and pulmonary vascular remodelling via RPS5/NF-κB signalling pathway[J]. J Biochem Mol Toxicol, 2024, 38(1):e23583. doi: 10.1002/jbt.23583 [11] YING X J, JIN B, CHEN X W, et al. Oxymatrine downregulates HPV16E7 expression and inhibits cell proliferation in laryngeal squamous cell carcinoma Hep-2 cells in vitro[J]. Biomed Res Int, 2015, 2015:150390. [12] ZHUANG X Y, DONG A H, WANG R C, et al. Ursolic acid benzaldehyde chalcone, leads to inhibition of cell proliferation and arrests cycle in G1/G0 phase in colon cancer[J]. Saudi J Biol Sci, 2018, 25(8):1762-1766. doi: 10.1016/j.sjbs.2017.04.006 [13] ZHANG Y E, STUELTEN C H. Alternative splicing in EMT and TGF-β signaling during cancer progression[J]. Semin Cancer Biol, 2024, 101:1-11. doi: 10.1016/j.semcancer.2024.04.001 [14] CAO X J, HE Q Q. Anti-tumor activities of bioactive phytochemicals in Sophora flavescens for breast cancer[J]. Cancer Manag Res, 2020, 12:1457-1467. doi: 10.2147/CMAR.S243127 [15] HALIM C E, XINJING S L, FAN L, et al. Anti-cancer effects of oxymatrine are mediated through multiple molecular mechanism(s) in tumor models[J]. Pharmacol Res, 2019, 147:104327. doi: 10.1016/j.phrs.2019.104327 [16] RASOULI S, DAKIC A, WANG Q E, et al. Noncanonical functions of telomerase and telomeres in viruses-associated cancer[J]. J Med Virol, 2024, 96(5):e29665. doi: 10.1002/jmv.29665 [17] LI H J, WANG J M, TIAN Y T, et al. Effect of matrine on Fas, VEGF, and activities of telomerase of MCF-7 cells[J]. Chin J Integr Tradit West Med, 2013, 33(9):1247-1251. [18] LIU L, LIAO J Z, HE X X, et al. The role of autophagy in hepatocellular carcinoma: friend or foe[J]. Oncotarget, 2017, 8(34):57707-57722. doi: 10.18632/oncotarget.17202 [19] YU H P, ZHU B L, YANG W, et al. Matrine inhibits proliferation and migration of HepG2 cells by downregulating ERK1/2 signaling pathways[J]. J Cancer Res Ther, 2020, 16(2):209-214. doi: 10.4103/jcrt.JCRT_331_19 [20] LIANG L, WU J, LUO J, et al. Oxymatrine reverses 5-fluorouracil resistance by inhibition of colon cancer cell epithelial-mesenchymal transition and NF-κB signaling in vitro[J]. Oncol Lett, 2020, 19(1):519-526. [21] STRONATI G, GUERRA F, URBINATI A, et al. Tachycardiomyopathy in patients without underlying structural heart disease[J]. J Clin Med, 2019, 8(9):1411. doi: 10.3390/jcm8091411 [22] ZHANG X N, GAO Y Q, ZHOU Y T, et al. Pharmacological mechanism of natural drugs and their active ingredients in the treatment of arrhythmia via calcium channel regulation[J]. Biomedecine Pharmacother, 2023, 160:114413. doi: 10.1016/j.biopha.2023.114413 [23] MARUYAMA K, IMANAKA-YOSHIDA K. The pathogenesis of cardiac fibrosis: a review of recent progress[J]. Int J Mol Sci, 2022, 23(5):2617. doi: 10.3390/ijms23052617 [24] ZHANG X, HU C, ZHANG N, et al. Matrine attenuates pathological cardiac fibrosis via RPS5/p38 in mice[J]. Acta Pharmacol Sin, 2021, 42(4):573-584. doi: 10.1038/s41401-020-0473-8 [25] CAO Y G, JING S, LI L, et al. Antiarrhythmic effects and ionic mechanisms of oxymatrine from Sophora flavescens[J]. Phytother Res, 2010, 24(12):1844-1849. doi: 10.1002/ptr.3206 [26] WANG Z Y, ZU T H, HUANG X Z, et al. Comprehensive investigation of the content and the origin of matrine-type alkaloids in Chinese honeys[J]. Food Chem, 2023, 402:134254. doi: 10.1016/j.foodchem.2022.134254 [27] LIU W C, TIAN X, GU L W, et al. Oxymatrine mitigates Aspergillus fumigatus keratitis by suppressing fungal activity and restricting pyroptosis[J]. Exp Eye Res, 2024, 240:109830. doi: 10.1016/j.exer.2024.109830 [28] SUN T, LI X D, HONG J, et al. Inhibitory effect of two traditional Chinese medicine monomers, berberine and matrine, on the quorum sensing system of antimicrobial-resistant Escherichia coli[J]. Front Microbiol, 2019, 10:2584. doi: 10.3389/fmicb.2019.02584 [29] HARATA-LEE Y, QU Z P, BATEMAN E, et al. Compound Kushen injection reduces severity of radiation-induced gastrointestinal mucositis in rats[J]. Front Oncol, 2022, 12:929735. doi: 10.3389/fonc.2022.929735 [30] WANG W, YOU R L, QIN W J, et al. Anti-tumor activities of active ingredients in Compound Kushen Injection[J]. Acta Pharmacol Sin, 2015, 36(6):676-679. doi: 10.1038/aps.2015.24 [31] YANG Y, SUN M Y, LI W D, et al. Rebalancing TGF-β/Smad7 signaling via Compound Kushen injection in hepatic stellate cells protects against liver fibrosis and hepatocarcinogenesis[J]. Clin Transl Med, 2021, 11(7):e410. doi: 10.1002/ctm2.410 [32] WU J Y, MA X Y, WANG X M, et al. Efficacy and safety of compound Kushen injection for treating advanced colorectal cancer: a protocol for a systematic review and meta-analysis[J]. Heliyon, 2024, 10(5):e26981. doi: 10.1016/j.heliyon.2024.e26981 [33] JIN Z S, HUANG Z H, WU C, et al. Molecular insights into gastric cancer: The impact of TGFBR2 and hsa-mir-107 revealed by microarray sequencing and bioinformatics[J]. Comput Biol Med, 2024, 172:108221. doi: 10.1016/j.compbiomed.2024.108221 [34] HUANG Z H, WU C, ZHOU W, et al. Compound Kushen Injection inhibits epithelial-mesenchymal transition of gastric carcinoma by regulating VCAM1 induced by the TNF signaling pathway[J]. Phytomedicine, 2023, 118:154984. doi: 10.1016/j.phymed.2023.154984 [35] LIU J, YU Q X, WANG X S, et al. Compound Kushen injection reduces severe toxicity and symptom burden associated with curative radiotherapy in patients with lung cancer[J]. J Natl Compr Canc Netw, 2023, 21(8): 821-830. e3. [36] ZHAO Z Z, FAN H T, HIGGINS T, et al. Fufang Kushen injection inhibits sarcoma growth and tumor-induced hyperalgesia via TRPV1 signaling pathways[J]. Cancer Lett, 2014, 355(2):232-241. doi: 10.1016/j.canlet.2014.08.037 [37] LIU Y, HUANG J J, LI S C, et al. Advancements in hydrogel-based drug delivery systems for the treatment of inflammatory bowel disease: a review[J]. Biomater Sci, 2024, 12(4):837-862. doi: 10.1039/D3BM01645E [38] WANG X, CHEN W Y, JIN Y G, et al. Effect of Sophora flavescens alkaloid on aerobic vaginitis in gel form for local treatment[J]. Chung I Tsa Chih Ying Wen Pan, 2017, 37(3):314-320. [39] WANG N M, CUI L, MA C F, et al. Clinical observation on treatment of mycotic vaginitis with Sophora gel combined with Fluconazole capsules[J]. China J Chin Mater Med, 2015, 40(5):978-980. [40] 曾丽敏. 苦参凝胶治疗慢性宫颈炎的效果研究[J]. 世界复合医学, 2021, 7(12):155-158. [41] 檀龙海, 王俊霞, 黄晶, 等. 当归苦参丸联合克林霉素磷酸酯凝胶治疗玫瑰痤疮的临床研究[J]. 现代药物与临床, 2023, 38(7):1733-1736. [42] 陈爱东, 温超, 艾江, 等. 五味苦参胶囊联合水杨酸制剂治疗溃疡性结肠炎的效果及对IL-1β、Caspase-1、VACM-1水平的影响[J]. 中华养生保健, 2023, 41(16):30-33. [43] 陈奇. 复方苦参止痒软膏联合糠酸莫米松乳膏治疗慢性湿疹的临床效果[J]. 临床合理用药, 2023, 16(20):137-139,147. [44] LIN Y D, HE F M, WU L, et al. Matrine exerts pharmacological effects through multiple signaling pathways: a comprehensive review[J]. Drug Des Devel Ther, 2022, 16:533-569. doi: 10.2147/DDDT.S349678 [45] GU Y M, LU J Y, SUN W, et al. Oxymatrine and its metabolite matrine contribute to the hepatotoxicity induced by Radix Sophorae tonkinensis in mice[J]. Exp Ther Med, 2019, 17(4):2519-2528. [46] LU Z G, LI M H, WANG J S, et al. Developmental toxicity and neurotoxicity of two matrine-type alkaloids, matrine and sophocarpine, in zebrafish (Danio rerio) embryos/larvae[J]. Reprod Toxicol, 2014, 47:33-41. doi: 10.1016/j.reprotox.2014.05.015 [47] XU J, WANG K Q, XU W H, et al. The matrine derivate MASM prolongs survival, attenuates inflammation, and reduces organ injury in murine established lethal sepsis[J]. J Infect Dis, 2016, 214(11):1762-1772. doi: 10.1093/infdis/jiw445 [48] SUN B, XU M. Matrine inhibits the migratory and invasive properties of nasopharyngeal carcinoma cells[J]. Mol Med Rep, 2015, 11(6):4158-4164. doi: 10.3892/mmr.2015.3276 [49] LI L Y, LI J R, MA L Y, et al. SAR-guided development of indole-matrine hybrids as potential anticancer agents via mitochondrial stress/cytochrome c/caspase 3 signaling pathway[J]. Bioorg Chem, 2023, 134:106341. doi: 10.1016/j.bioorg.2023.106341 [50] WU L C, LIU S B, WEI J R, et al. Synthesis and biological evaluation of matrine derivatives as anti-hepatocellular cancer agents[J]. Bioorg Med Chem Lett, 2016, 26(17):4267-4271. doi: 10.1016/j.bmcl.2016.07.045 [51] NI W J, WANG L Z, SONG H J, et al. Synthesis and evaluation of 11-butyl matrine derivatives as potential anti-virus agents[J]. Molecules, 2022, 27(21):7563. doi: 10.3390/molecules27217563 [52] HU H G, WANG S Z, ZHANG C M, et al. Synthesis and in vitro inhibitory activity of matrine derivatives towards pro-inflammatory cytokines[J]. Bioorg Med Chem Lett, 2010, 20(24):7537-7539. doi: 10.1016/j.bmcl.2010.09.075 [53] XU W H, HU H G, TIAN Y, et al. Bioactive compound reveals a novel function for ribosomal protein S5 in hepatic stellate cell activation and hepatic fibrosis[J]. Hepatology, 2014, 60(2):648-660. doi: 10.1002/hep.27138 [54] FAN Z Y, CHEN Y P, CHEN L, et al. The matrine derivate MASM inhibits astrocyte reactivity and alleviates experimental autoimmune encephalomyelitis in mice[J]. Int Immunopharmacol, 2022, 108:108771. doi: 10.1016/j.intimp.2022.108771 [55] LI L Y, LU F F, DING S Q, et al. Pharmacokinetic, tissue distribution, metabolite, and toxicity evaluation of the matrine derivative, (6aS, 10S, 11aR, 11bR, 11cS)-10-methylaminododecahydro-3a, 7a-Diaza-benzo (de) anthracene-8-thione[J]. Molecules, 2024, 29(2):297. doi: 10.3390/molecules29020297 [56] LIU Y, QI Y, BAI Z H, et al. A novel matrine derivate inhibits differentiated human hepatoma cells and hepatic cancer stem-like cells by suppressing PI3K/AKT signaling pathways[J]. Acta Pharmacol Sin, 2017, 38(1):120-132. doi: 10.1038/aps.2016.104 -





 下载:
下载:
 下载:
下载: