-
肾脏移植术是目前终末期肾病最有效的治疗方法,其中免疫抑制剂的使用是影响移植患者长期生存的重要因素之一。如何才能减少免疫抑制剂不良反应的发生、提高免疫抑制效果,临床医师和药师一直在不断探索解决方案。
百令胶囊是一种上市多年的补益中成药,其原料为中药冬虫夏草中分离出的中华束丝孢菌的发酵菌粉,其主要化学成分有虫草生物碱、多糖、氨基酸、麦角甾醇、多种维生素、微量元素及D-甘露醇等,这些成分是补肺肾、益精气等功效[1-2]的物质基础。临床上对虫草制剂保护肾脏的作用研究进行了广泛深入的研究报道,其主要机制为,通过促进细胞外基质降解、抑制氧化应激、调节细胞生长因子、改善脂质代谢、抑制肾组织早期炎症反应和减少肾细胞凋亡等多种途径、多个靶点来抑制肾脏疾病的发生和发展[3-4]。近年来,虫草制剂作为免疫调节剂已被广泛应用于器官移植术后患者的治疗。
本研究回顾性研究分析了60例肾移植受者应用百令胶囊在促进肾功能恢复、减少环孢素A(CsA)和他克莫司(FK506)等免疫抑制剂的用量和毒性、减轻肝功能损害等方面的资料。
-
将2018−2020年在联勤保障部队第910医院就诊的60例同种异体肾移植术后患者,在基础免疫抑制剂方案相同的情况下,按是否加用百令胶囊分为两组:对照组35例,男21例,女14例,平均年龄(39.6±8.8)岁,18例服用CsA(瑞士诺华制药公司),17例服用FK506(安斯泰来制药有限公司);治疗组25例,男15例,女10例,平均年龄(39.2±7.1)岁,12例服用CsA加百令胶囊,13例服用FK506加百令胶囊。
-
所有患者均在术后第3天起口服CsA 4.5 mg/(kg·d)或FK506 0.1 mg /(kg·d);泼尼松自40 mg/d,之后每天递减5 mg至20 mg/d,维持,1年后减为10 mg/d,维持;治疗组术后3 d开始增加口服百令胶囊1 g,tid。所有患者均根据血肌酐(SCr)水平和CsA或FK506的血药浓度进行用药剂量调整。百令胶囊的剂量在1年内基本保持不变。
-
患者肾移植术后4周内,每周常规空腹检测2次血、尿常规,肝、肾功能,血药浓度,血清总蛋白(TP)和白蛋白(ALB),血尿酸(UA)等,术后 8~12周期间每周常规空腹检测以上指标至少1次,12~24周期间每2周检测1次上述指标,24~ 48周每4周检测上述指标1次,上述检测均在同一医疗机构内完成。用SCr、尿素氮(BUN)和24 h尿蛋白量(24 h-UPro)、UA、尿红细胞、尿白细胞等指标观察比较肾移植24、48周后的肾功能;用天冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、总胆红素(TBIL)、直接胆红素(DBIL)、24 h-UPro、总蛋白、ALB和总胆固醇(TC)分别测定肾移植24、48周后的肝功能。并分别进行红细胞计数、白细胞计数、血小板(PLT)计数等血常规检查。
-
各组数据以(
$ \bar{x}\pm s $ )表示,行两组间对应指标的 t检验;两组间对应指标比较行χ2检验。P<0.05为差异有统计学意义。 -
两组SCr和BUN比较,差异无统计学意义(P>0.05);24 h-UPro、UA、尿红细胞、尿白细胞在48周后治疗组显著低于对照组(P<0.05,P<0.01),见表1。
表 1 术后24、48周两组肾功能和尿常规比较(
$ \bar{x}\pm s $ )组别 例数 时间 SCr(μmol/L) BUN(mmol/L) 24 h-UPro(μg) UA(μmol/L) 尿红细胞 (个/μl) 尿白细胞(个/μl) 对照组 35 24周 98.21±23.46 7.72±2.81 0.18±0.02 455.96±121.17 11.36±3.89 8.72±1.39 35 48周 95.82±28.13 7.88±1.99 0.19±0.02 477.62±98.91 20.46±1.77 9.61±2.97 治疗组 25 24周 97.44±25.25 7.69±2.55 0.18±0.02 403.74±131.23* 11.47±1.33 6.36±1.59 25 48周 96.57±26.17 7.84±2.12 0.17±0.02* 382.57±118.32* 11.83±2.01* 5.39±1.22** * P<0.05,** P<0.01,与对照组比较 -
两组血常规结果显示,血白细胞和红细胞数在肾移植术后的 24周前比较,两组差异无统计学意义,治疗组此两项在肾移植48周后显著高于对照组(P<0.05);治疗组淋巴细胞数在移植 24~48周后均显著高于对照组(P<0.05),见表2。
表 2 术后24、48周两组血常规比较 (
$ \bar{x}\pm s $ )组别 例数 时间 白细胞(×1012/L) 红细胞(×1012/L) 淋巴细胞(×109/L) 血小板(×109/L) 对照组 35 24周 7.21±1.45 4.56±1.17 2.49±0.80 211.55±50.42 35 48周 6.82±2.11 4.42±0.91 3.01±0.91 211.34±70.59 治疗组 25 24周 7.04±2.26 4.64±1.29 3.05±1.21* 215.70±66.24 25 48周 7.27±1.17* 4.97±1.12* 3.47±1.08* 206.10±59.84 * P<0.05,与对照组比较 -
治疗组AST、ALT、血总胆红素及血直接胆红素值、TC显著低于对照组(P<0.05,P<0.01);治疗组TP、血清白蛋白值显著高于对照组(P<0.05),见表3。
表 3 术后24、48周两组肝功能、血清蛋白及胆红素比较(
$ \bar{x}\pm s $ )组别 例数 时间 肝转氨酶(U/L) 血清蛋白(g/L) 胆红素(μmol/L) 胆固醇(mmol/L) AST ALT TP ALB TBIL DBIL TC 对照组 35 24周 22.42±6.12 27.35±7.08 60.62±14.81 38.19±9.50 14.82±3.61 4.77±1.56 4.62±0.59 35 48周 21.55±5.71 29.69±5.96 63.33±15.44 40.55±6.57 12.71±2.97 4.51±0.96 4.85±0.66 治疗组 25 24周 14.89±6.22* 25.88±6.79 62.07±15.12 40.33±6.99 13.09±2.57 5.01±1.43 4.33±0.71 25 48周 13.92±3.29* 19.8.9±6.1.4* 66.46±18.43* 44.17±8.58* 9.78±2.69** 3.81±1.23* 4.21±0.82* * P<0.05,** P<0.01,与对照组比较 -
治疗组CsA及FK506用量在48周后显著低于对照组(P<0.05),见表4、表5。
表 4 术后1~48周两组免疫抑制剂FK506的用量比较 (
$ \bar{x}\pm s $ )组别 例数 1周 4周 12周 24周 48周 对照组 17 0.10±0.02 0.10±0.02 0.09±0.03 0.09±0.01 0.08±0.02 治疗组 12 0.10±0.01 0.10±0.03 0.09±0.02 0.08±0.02 0.07±0.01* * P<0.05,与对照组比较 表 5 术后1~48周两组免疫抑制剂CsA的用量比较 (
$ \bar{x}\pm s $ )组别 例数 1周 4周 12周 24周 48周 对照组 18 4.5±0.9 4.5±1.5 4.3±1.2 4.2±1.3 3.5±1.2 治疗组 13 4.5±1.0 4.5±1.1 4.2±1.3 4.0±1.5 3.3±1.1* * P<0.05,与对照组比较 -
CsA是由11个氨基酸组成的环状多肽,是土壤中一种真菌的活性代谢物,英国于1978年首次将其应用于临床肾移植,是一种强效免疫抑制剂。FK506是日本藤泽药品工业株式会社从链霉菌属中分离出来的大环内酯类抗生素,被广泛用于减少或阻断外科移植、移植物抗宿主病以及自身免疫疾病治疗中出现的免疫排斥反应,其作用机制是抑制多种细胞因子,如白细胞介素-2、γ干扰素的产生,阻断T细胞活化,且抑制细胞毒性T细胞的增殖和白细胞介素-2受体的表达,也是肾脏移植患者的首选免疫抑制药物。但二者的缺点是均具有明显的毒副作用,特别是肾毒性对移植肾的长期存活影响较大[5-6]。CsA多见肾小球血栓、肾小管受阻、蛋白尿、管型尿等肾毒性;FK506也存在潜在肾毒性。因此,在临床应用中建议监测包括SCr、肌酐清除率及排尿量等肾功能指标。
在本研究中,肾移植术后患者在用药48周后,治疗组与对照组对SCr、BUN等方面的影响没有统计学差异。而在使用百令胶囊后,患者尿沉渣中红细胞、白细胞、24 h-UPro显著低于未使用者,说明使用百令胶囊者的移植肾脏得到了一定保护,肾炎症状、蛋白尿和低蛋白血症也得到改善;另一方面,用药24周后的治疗组比对照组UA显著减少,提示百令胶囊在预防或者减少肾移植术后发生痛风并发症方面有潜在益处。
本研究进一步提示,两组患者在肾移植术后的前24周内血中红细胞及白细胞比较无统计学差异,这可能是因为在术后早期,大量免疫抑制剂的冲击应用强有效地抑制了机体造血系统的活力,而此时使用百令胶囊在短期内并不能改善免疫抑制剂造成的骨髓抑制反应。但在术后用药48周后,治疗组血中红细胞及白细胞相较于对照组有显著升高的趋势,百令胶囊促进造血功能的长期效果得以体现。从术后用药24周后的淋巴细胞指标来看,治疗组较对照组明显增加,这可能与百令胶囊刺激造血干细胞的产生、分化[7]有关。另有研究表明,天然药物冬虫夏草、冬虫夏草发酵菌及其制剂中均含有虫草多糖、生物碱、腺苷、麦角甾醇、多种氨基酸、多种维生素、D-甘露醇及微量元素等化学成分[8-9],这些成分中有些是核酸、蛋白质合成的前体,可刺激骨髓造血干细胞的产生,促进其生长、增殖,有利于骨髓造血功能的快速恢复,因此具有显著的促生血作用[10]。另外,百令胶囊中还有一些活性成分,例如,腺苷可以通过对T淋巴细胞、B淋巴细胞及NK细胞刺激活化从而提高细胞免疫功能,是一种作用较广的免疫增强剂;同时,其对淋巴细胞转化又有一定的促进作用,故具有双向免疫调节效应[11]。另有研究报道,冬虫夏草及其制剂在改善肾脏微循环、减轻尿蛋白等方面也具有良好的治疗效果,在联合西药治疗肾脏疾病过程中可以减少相关并发症的发生,如今在临床上已被广范用于肾脏疾病的保护性治疗[12-13]。
长期的免疫抑制剂如CsA、FK506的使用亦会导致肝功能受损,因此在使用过程中还要严密监测肝功能情况。本研究中,两组患者肝功能比较数据表明,百令胶囊对肾移植术后患者的肝功能恢复有显著改善,如可促进胆红素分泌和排泄,这提示冬虫夏草制剂对肝细胞可能具有保护作用。有研究资料表明,冬虫夏草制剂中维生素与多胺类及其他成分可以清除细胞内的氧自由基,保护细胞免受损伤[5]。核苷酸和核苷能促进肠道正常的发育、成熟和修复,对维持机体正常的免疫功能和肝脏的正常功能也有重要意义[14]。肾移植患者使用百令胶囊还可以减轻其他免疫抑制药物的肝毒性,加快有害物质的清除,减轻肝细胞损伤,并促进受损肝细胞的恢复。本次研究中,治疗组TP、血清白蛋白值显著高于对照组,这可能与冬虫夏草菌粉中含有的多种氨基酸和肽类成分有关,这些成分可促进蛋白质合成,纠正血浆氨基酸紊乱,与巨噬细胞和淋巴细胞转化以及白介素-1生成等免疫抑制作用呈正相关[15]。
两组免疫抑制剂用量比较提示,在肾移植术后前24周内基础免疫抑制剂CsA及FK506的用量无明显差异,在术后的前3个月内,是受者与供者器官的激烈较量期,免疫抑制剂的用量必须用足,两组的用量与基础用量的差异均不是很大,这期间的免疫抑制剂的用量调整也极为谨慎。肾移植48周后,从免疫抑制剂CsA、FK506的用量来看,两组用量均比初始量明显降低,这是根据两种药物的毒副作用监测而进行的剂量调整。两种药物的治疗组均显著少于对照组,这一现象可能是由于百令胶囊在发挥免疫调节作用,但具体机制还有待于进一步研究阐明。
Clinical effect of Bailing capsule on patients after renal transplantation
-
摘要:
目的 回顾性分析联勤保障部队第910医院(本院)60例肾移植术后患者服用百令胶囊的临床效果,探讨百令胶囊对肾移植术后患者的肾功能及其他机体系统的影响。 方法 从医院HIS系统抽调2018−2020年于本院就诊的60例同种异体肾移植术后患者用药资料,依照不同的免疫抑制剂给药方案分成2组,分别为对照组35例:霉酚酸酯(MMF)联合环孢素A(CsA)或他克莫司(FK506);治疗组25例:MMF联合CsA或FK506同时联合百令胶囊。术后检测肝、肾功能,血、尿常规及尿酸等;随访并分别记录1、4、12、24、48周免疫抑制剂CsA和FK506的使用量。 结果 治疗组尿中红细胞数量、白细胞数量、血谷草转氨酶和谷丙转氨酶、血清尿酸、总胆红素、直接胆红素显著少于对照组,而血清总蛋白、白蛋白显著高于对照组;治疗组血红细胞、白细胞数量在肾移植术后12~48周显著高于对照组,淋巴细胞在肾移植术后24~48周显著高于对照组。治疗组CsA或FK506的用量在术后48周之后显著低于对照组。 结论 百令胶囊能有效减轻肾移植术后患者的常见并发症状,并具有减少免疫抑制剂使用量等效果,可作为一种较理想的免疫调节剂用于肾移植术后患者的治疗。 Abstract:Objective To study the effect of Bailing capsule on renal function and other organ systems in 60 patients after renal transplantation in No. 910 Hospital of Joint Logistics Support Force. Methods 60 patients with renal allograft in 2018−2020 were divided into 2 groups according to different immunosuppressive regimens. In the control group, 35 cases were treated with MMF + CsA or FK506; in the treatment group, 25 cases were treated with MMF + CsA or FK506 + Bailing capsule. Blood and urine routine, liver and renal function and uric acid were measured after operation. The dosage of immunosuppressive drugs was recorded in stages at 48 weeks. Results The urinary red and white blood cell counts, blood aspartate transaminase and alanine transaminase, serum uric acid, total bilirubin and direct bilirubin in the treatment group were significantly less than those in the control group, while the serum total protein and albumin were significantly higher than those in the control group. The number of red blood cells and white blood cells in the treatment group was significantly higher than that in the control group at 12-48 weeks after kidney transplantation, and that in the lymphocyte group was significantly higher than that in the control group at 24-48 weeks after kidney transplantation. The dosage of CsA and FK506 in the treatment group was significantly lower than that in the control group after 48 weeks. Conclusion Bailing capsule could protect liver and kidney, stimulate hematopoiesis, improve hypoalbuminemia and reduce the dosage of immunosuppressant, which could be an ideal immunomodulator. -
Key words:
- Bailing capsule /
- tacrolimus /
- cyclosporine A /
- renal transplantation /
- immunoregulation
-
中药挥发性成分(VOCs)是指中药中一类具有芳香气并易挥发的成分,其化学组成复杂,主要包括挥发油类以及其他分子量较小、易挥发的化合物,例如萜类、脂肪族、芳香族化合物等。VOCs具有发汗解表、芳香开窍、镇咳祛痰、理气、驱风、抑菌、镇痛、杀虫等多种功效。作为中药学研究的热点之一,高效率、高标准的检测药材中VOCs十分关键。因此,利用现代化方法来实现对中草药挥发性成分的细致分析,意义巨大。
VOCs常用气相色谱-质谱联用(GC-MS)方法进行分析,虽分离能力强,但样品需要预处理且分析时间长。气相色谱-离子迁移谱(GC-IMS)法结合了GC突出的分离能力和IMS快速响应、高灵敏度的特点,具有样品准备简便、高灵敏度、高分辨率等显著优势,结合化学计量学分析中药材VOCs所呈现图谱,可实现对药材VOCs无损、快速区分[1]。
1. 气相色谱–离子迁移谱联用技术原理
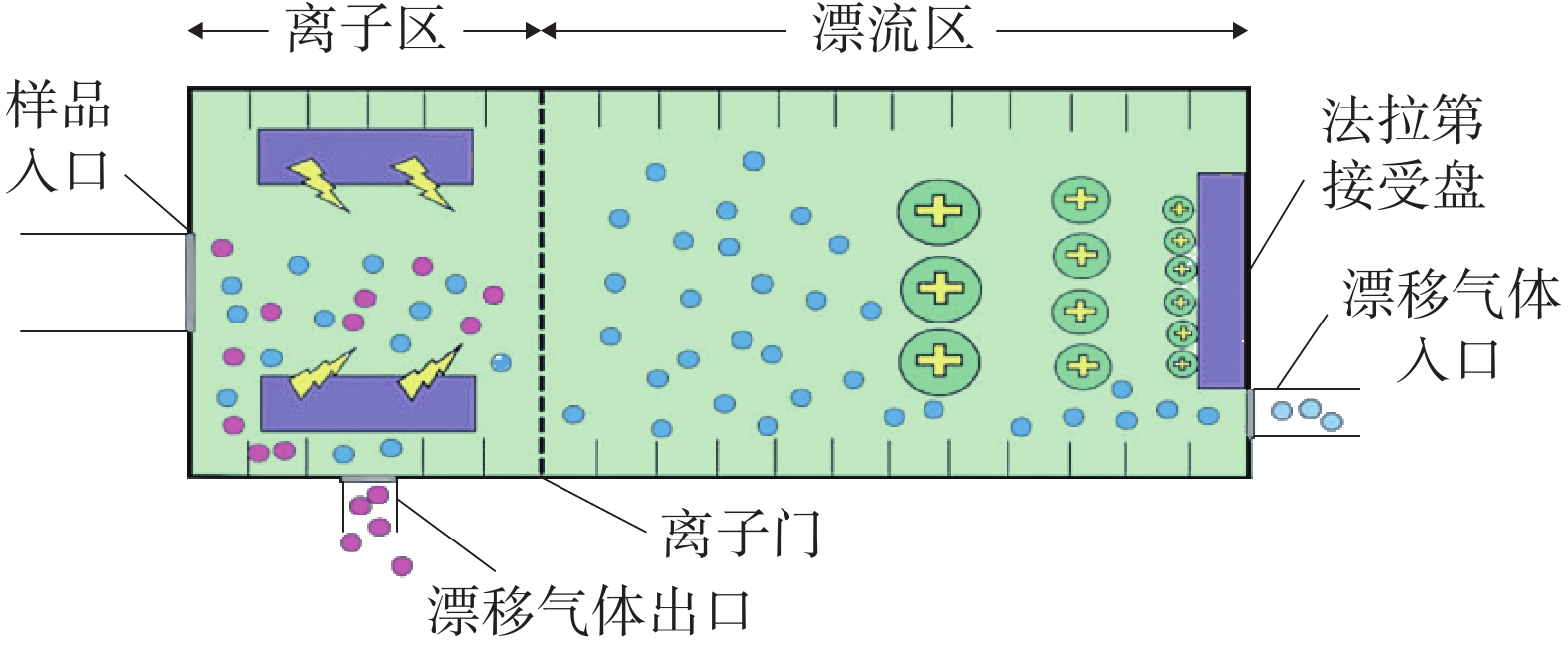
GC-IMS 技术的基本原理[2]是通过将样品混合物引进气相色谱仪进行分离,样品分子和载气分子在离子源放射性物质的作用下发生一系列反应形成产物离子,这些产物离子在不同的电场驱动下通过离子门进入迁移区,与逆向而来的中性迁移气体分子发生碰撞而损失能量。产物离子在电场中的迁移速率不同,到达检测器上的时间不同,从而使样品差异化分离(如图1),最后可得到一个包含有离子迁移时间(X轴),气相色谱保留时间(Y轴),离子强度(Z轴)的三维谱图(如图2)。
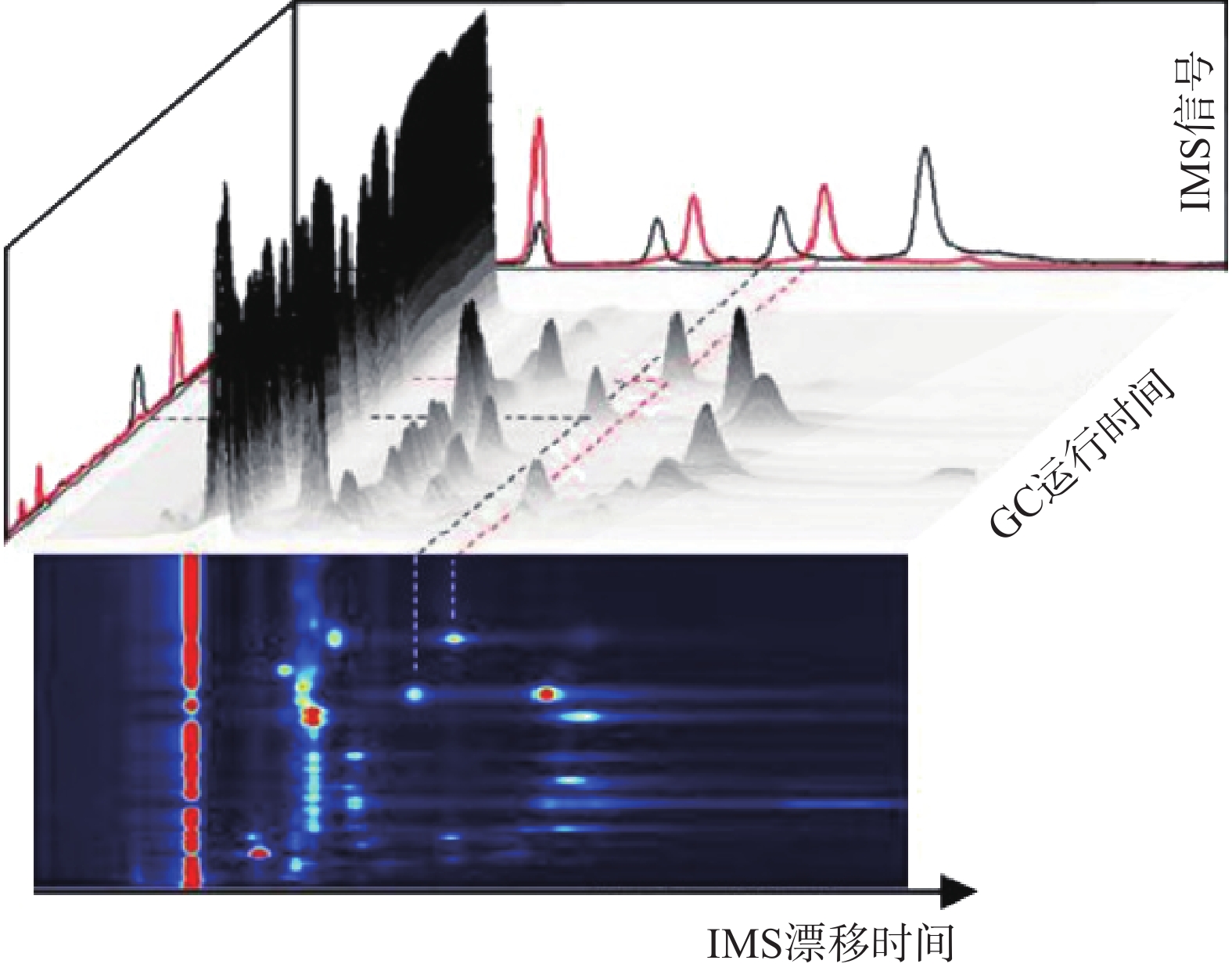 图 2 气相色谱-离子迁移谱联用技术结果三维谱图[3]
图 2 气相色谱-离子迁移谱联用技术结果三维谱图[3]顶空-气相色谱-离子迁移谱(HS-GC-IMS)是应用于检测药材中VOCs最为广泛的方式之一 [3]。其原理是首先将样品中的VOCs通过热孵育和振摇使之从药材中逸出,随后抽取顶空气体进行分析,避免复杂基质干扰,再使之进入气相色谱(GC)、离子迁移谱(IMS)中,得到相应谱图。HS-GC-IMS无需样品预处理,在分析复杂样品或需要快速检测场景方面更具优势。
自从1972年第一张经过GC分离的IMS谱图出现[2],早期主要用于军事领域(如化学战剂检测)和毒品筛查的先进技术逐渐面向市场,应用于研究(如图3),引进国内后广泛使用于中药研究。现阶段,通过GC-IMS捕捉到中药材中的微量VOCs,将其应用于区分中药的不同种类和产地、监控中药炮制过程以及中药复方组分分析等[4],为中药材的产地及真伪鉴别提供可靠的依据,同时也为质量控制和药效研究等方面提供数据支持。
2. 在中药鉴定中的应用
2.1 同属不同种的中药鉴别
同属不同种之间的中药材亲缘关系比较接近,在VOCs种类差异上不显著,利用GC-IMS技术善于捕捉挥发性化合物种类微小差异的特点,可对样品进行品种鉴别。
陈皮中主要含有三萜类、挥发油类等几百种成分,有平喘止咳、调节血管等药理作用[5-6],刘主洁等[7]和Lv等[8]采用HS-GC-IMS对陈皮和广陈皮样品中VOCs进行研究,分析二者的特征信号,以邻氨基苯甲酸二甲酯为广陈皮最明显的特征标记物,柠檬烯、癸醛等也可作为广陈皮的特征信号,利用这些特征信号可对陈皮和广陈皮进行区分。山莓是覆盆子的混淆品之一,为保证用药安全有效,有必要对两者进行区分[9],严爱娟等[10]采用GC-IMS技术检测山莓和覆盆子VOCs,明确鉴定出覆盆子特征成分较山莓多,其中癸醛、1-辛烯-3-醇等在覆盆子样品中的含量更高,苯甲醛、2-丁酮等在山莓样品中的含量更高,以此来实现山莓和覆盆子的区分。彭旭阳等[11]采用GC-IMS分析新疆和田地区“梭梭”和“红柳”肉苁蓉这两种不同寄主肉苁蓉挥发性物质之间的不同,找到了二者主要差异物质为苯甲醛、庚醛等。
2.2 中药不同产地鉴别
道地药材是指生长在特定的自然生态环境中,经过一系列技术培育和加工而成,且被公认为比其他地方生产的同种药材的质量和治疗效果好的药材[12]。但随着产地的迁移、品种的引入,在外观性状上对道地药材和其他产地的中药进行简单鉴别已经不能满足需求。
王振洲等[13]采用GC-IMS对来自不同产区的人参VOCs进行检测,发现2,5-二甲基吡嗪和2,6-二甲基吡嗪等VOCs在吉林集安四年生人参中含量较高,而吉林敦化四年生人参中含量相对较低,由此鉴别四年生吉林集安和敦化的人参。西洋参同属于五加科人参属,成功引种进入我国后,辽宁、吉林和山东是其主产区[14],王燕等[15]使用GC-IMS技术对美国、加拿大、山东等五个不同产地的西洋参进行研究,共鉴定出53种VOCs,其中美国西洋参中2-庚酮等成分的含量较高,而加拿大产α-蒎烯等成分的含量显著高于其它产区,中国产芳樟醇等成分的含量较高,其中吉林产地的含量是辽宁、山东产地的2.60和3.60倍,通过这些显著差异可对西洋参进行产地溯源和鉴别。
李曼祎等[16]使用GC-IMS技术对新疆、宁夏、内蒙古、青海四个主要产区的枸杞进行化学成分测定,分析出了四个地区含量差异较大的16种物质,发现内蒙古枸杞区别于另外三个产地特有的物质为正丁醇,同时筛选出了叶醇等五种标记性物质对枸杞产地进行区分。Li[17]等分别采用HS-SPME-GC-MS和HS-GC-IMS检测河北、河南、江苏、浙江、安徽以及山东6个不同地区的五味子,结果显示安徽的五味子萜类物质含量较高,同时该研究也证明了HS-GC-IMS对样品的分类效果优于HS-SPME-GC-MS。山东为瓜萎的道地产区[18],河北也是瓜萎的重要产区,不同产地的瓜萎可能在品质及所含成分上有所差别,从而对药效也会产生一定的影响[19-20]。张敏敏等[19]采用GC-IMS在瓜萎皮样品中共鉴定出醛类和醇类等88种VOCs,分析发现山东瓜蒌皮中2-庚酮、正壬醛等物质的含量低于河北瓜蒌皮,但1-己醇、糠醇等含量更高的结论,通过这些差异基本实现了两地区瓜萎皮的区分。Li等[21]采用HS-GC-IMS联合PCA建立松茸特征图谱,对分别来自云南和四川的松茸样品以及它们的菌盖和菌柄进行研究,发现虽然指纹图谱相似度较高,但各自也有其特征性挥发物:苯乙醛和糠醇等仅在云南产松茸的菌柄中被发现,戊烷仅在四川产松茸的菌柄中被发现,戊醛仅在云南产松茸的菌盖中检出,甲基吡嗪仅在四川产松茸的菌盖中检出,通过特征性挥发物的不同,可对分别产自云南和四川的松茸进行区分。
2.3 中药复方中主成分的鉴别
中药复方成分众多且复杂,确保其质量符合标准、疗效可靠、使用安全是关键,采用HPLC特征图谱进行分析是目前公认的良好方法之一[22]。GC-IMS检测灵敏度高、分离效果好,是对HPLC表征中药复方质量分析的有益补充。
Yuan等[23]设置了对照组、慢性不可预测轻度应激(CUMS)组和CUMS+百合鸡子黄汤组,采用HS-GC-IMS等方法对百合鸡子黄汤治疗CUMS大鼠粪便中挥发性化合物含量进行研究,鉴定出了11个生物标志物,找出了对照组大鼠粪便样品中甲硫醚含量较高,而CUMS组则较低,同时百合子鸡汤组抑郁表现出保护性干预作用;Yin等[24]采用HS-GC-IMS对开心散中的挥发性化合物进行分析,鉴别出β-细辛酮等十种VOCs可作为开心散的质量标记物,进一步为开心散质量控制及药效机制等的相关研究奠定基础;李巍等[25]利用HS-GC-IMS对清感秋饮中的VOCs进行定性定量分析,共鉴定出120种VOCs,其中,紫苏属酮、β-石竹烯等可能为其主要药效成分。
3. 在中药加工炮制中的应用
中药的加工炮制是提高临床疗效的重要手段,也是保证临床用药安全的重要措施[26]。应用不同的炮制方法可能会引起中药中的化学成分发生含量加减、成分转化与破坏等变化,采用GC-IMS技术对中药加工炮制过程中的VOCs进行动态监控,对于炮制工艺的规范、制定更优炮制方案等具有指导意义。
干燥是中药材和饮片加工制备过程中的重要且关键的环节之一,而中药中的VOCs易受干燥工艺的影响,对于富含VOCs的中药,准确控制干燥工艺有利于减少有效成分的损失。陈树鹏等[27]采用GC-IMS等技术确定烘干样品的整体香气属性优于晒干样品,这可能是由于烘干工艺对环境温度的调整使得烘干过程更有利于果香、柑橘香以及甜香香气保留。其中苯乙酸乙酯、乙酸乙酯等 12 种物质为晒干主要成分,2-甲基-1-丁醇、(E)-2-己烯-1-醇等为烘干主要成分;Wang等[24]在8S-GC-IMS技术的辅助下,了解了柑橘皮干燥以及不同条件下挥发性成分情况,研究柑橘皮各成分在不同干燥温度下的缺失,其中,70 ℃下干燥会导致2,2-苯基-1-苦基肼基和铁还原抗氧化能力显著降低。Yu等[29]通过GC-MS比较总离子色谱图中的峰面积与苯乙酸乙酯的峰面积,将VOCs的含量进行半定量再通过GC-IMS呈现图谱对结果进行比较,确定VOCs的身份,从而证实晒干有利于两个品种的网纹柑橘中萜醇类化合物的保存,热风干燥有利于脂肪族醛和倍半萜的保存,而冷冻干燥是保存酯类和酚类物质的最佳方法;Zhou等[30]对肉苁蓉进行酒制增效后粉碎、超微粉碎、醇提、水提等处理,采用HS-GC-IMS方法检测其VOCs并建立指纹图谱,发现增效处理的肉苁蓉VOCs的种类和含量有所减少,分析原因可能为各种化学物质之间在处理过程中会发生化学变化,而新鲜肉苁蓉则保存了更多种类的VOCs,超微粉碎处理和水提处理后的肉苁蓉挥发性化合物主要以醛类为主。除此之外,将其它中药基于GC-IMS技术在不同炮制方法中的应用汇总于表1。
表 1 GC-IMS技术在炮制研究方面的应用作者 药材及炮制方法 采用方式 实例 高以丹等 [31] 柴达木枸杞
冷冻干燥、自然阴干、热风烘干GC-IMS 从枸杞样品中鉴定出反-2-壬烯醛、2,4-庚二烯醛等52种VOCs,表明冷冻干燥法比自然阴干、热风烘干以及微波干燥更好,能够有效保留枸杞中的VOCs,使枸杞保持较高的品质。 时海燕等 [32] 六神曲
生品、炒品、焦品HS-GC-IMS 从六神曲生品、炒品和焦品中鉴别出60种化合物通过比较种类和差异,得出炒神曲比焦神曲健胃消食的效果更好。 林秀敏等 [33] 当归
酒洗、酒炙、酒浸GC-IMS 2-十一烯醛、丙酮等为酒洗与酒浸当归的主要差异性物质,2-十一烯醛、丙酮等为酒洗与酒炙当归的主要差异性物质,2-十一烯醛、辛酸乙酯等为酒浸与酒炙当归的主要差异性物质。 武旭等 [34] 胆南星
发酵炮制GC-IMS 发酵炮制有助于胆南星矫味矫臭 王雨晨等 [35] 太子参
常温晾干、晒干、热风干燥、
真空冷冻干燥GC-IMS 40 ℃热风干燥可以有效保留太子参样品中的VOCs,与晒干、晾干样品无差异,但真空冷冻干燥对太子参挥发性成分的影响较大,会造成挥发性成分以及风味的损失 焦焕然等 [36] 侧柏叶
常温晾干、晒干,热风干燥、
变温干燥GC-IMS 40 ℃和60 ℃热风干燥能够较好地保留瓜蒌样品中的核苷类和黄酮类成分 4. 与电子鼻联用
国内外也有许多采用GC-IMS与电子鼻联用对中药挥发性成分进行研究。电子鼻是一种通过模拟人嗅觉系统对检测物质进行品质评价的感官仪器,其原理是通过传感器阵列对气味分子进行检测和响应,将产生的信号经过预处理后送入模式识别系统,通过指纹图谱对挥发性成分或是气体进行定量或定性分析[37]。两种技术的联用为实验的结果研究提供了更高的准确度。
Feng等 [38]采用GC-IMS、GC-MS对不同地理标志的八种花椒的VOCs进行测定,证明了两种方法均可用于对不同花椒的分类,但相较之下GC-IMS操作时间更短,且有能够检测到含量很低物质,结果表明红花椒比青花椒能够释放出更多的萜烯、酯类和更少的醇类,同时该研究还与电子鼻联用表征花椒中的香气物质,W1W、W2W和W5S传感器对花椒样品VOCs的响应更强,说明花椒产品中可能含有更高丰度的萜烯、有机硫化物和氮氧化物。陈小爱等 [39]利用GC-MS、GC-IMS和电子鼻技术联用,分析老香黄在发酵期间的VOCs变化,GC-MS共鉴别出包括醇类等八个种类的46种VOCs,GC-IMS则检测出包括杂环类等九个类别的38种VOCs,同时电子鼻PCA有效区分了不同发酵时间的样品,发现发酵6个月后老香黄挥发性组分开始发生较大的变化,其中柠檬烯等14种是发酵期间含量较高且相对稳定的成分,发酵过程中产生的庚醛、糠醛等是构成老香黄特有气味的特征性成分。王世丽等 [40]通过电子鼻辨识南北柴胡气味特征物质与GC-IMS检测其挥发性成分,发现南北柴胡中短链烷烃、醛类等物质差异较大,癸醛、异戊烯醛等可作为南柴胡的特征物质,2-甲基丙酸、3-甲基丁醇可作为北柴胡的特征物质,此外乙酸、乙酸甲酯等成分在北柴胡中显著高于南柴胡。
5. 总结和展望
GC-IMS在中药研究中的应用前景非常广阔,不仅可以对同属不同种、不同产地来源、不同采收期以及不同贮存时间的中药VOCs进行分析鉴别,还可以帮助分析炮制前后中药VOCs含量变化以及在复方中寻找质量标志物,为药物质量控制与药效研究提供帮助。另外,随着技术的不断进步和中药现代化需求的增加,GC-IMS可以与特征图谱相结合,构建特征指纹图谱;也可以与电子鼻等其他分析手段融合,发挥出新的效果,让其所能提供的信息更加全面。但该项技术作为新兴科技仍需解决许多问题,比如应探索融合数据库的体系架构[41]。目前,GC-IMS通常使用的数据库为NIST出版的标准质谱图,对于中药VOCs的专业数据库搭建还不全面,部分VOCs需要自行判断建立文档保存入库,对实验进程造成不便。由于中药挥发性成分复杂,GC-IMS可能因峰重叠导致部分成分无法准确定性,例如分析复方丹参片时,GC-IMS仅能明确鉴定其中60%的化合物,需GC-MS辅助验证。而且GC-IMS对象单一,无法检测多糖、生物碱等非挥发性成分,难以全面评价中药质量。
总的来说,GC-IMS技术为中药研究提供了一种新的科学工具,有利于推动中药科学研究深入,也为中药产业的发展走向国际化和标准化提供支持。
-
表 1 术后24、48周两组肾功能和尿常规比较(
$ \bar{x}\pm s $ )组别 例数 时间 SCr(μmol/L) BUN(mmol/L) 24 h-UPro(μg) UA(μmol/L) 尿红细胞 (个/μl) 尿白细胞(个/μl) 对照组 35 24周 98.21±23.46 7.72±2.81 0.18±0.02 455.96±121.17 11.36±3.89 8.72±1.39 35 48周 95.82±28.13 7.88±1.99 0.19±0.02 477.62±98.91 20.46±1.77 9.61±2.97 治疗组 25 24周 97.44±25.25 7.69±2.55 0.18±0.02 403.74±131.23* 11.47±1.33 6.36±1.59 25 48周 96.57±26.17 7.84±2.12 0.17±0.02* 382.57±118.32* 11.83±2.01* 5.39±1.22** * P<0.05,** P<0.01,与对照组比较 表 2 术后24、48周两组血常规比较 (
$ \bar{x}\pm s $ )组别 例数 时间 白细胞(×1012/L) 红细胞(×1012/L) 淋巴细胞(×109/L) 血小板(×109/L) 对照组 35 24周 7.21±1.45 4.56±1.17 2.49±0.80 211.55±50.42 35 48周 6.82±2.11 4.42±0.91 3.01±0.91 211.34±70.59 治疗组 25 24周 7.04±2.26 4.64±1.29 3.05±1.21* 215.70±66.24 25 48周 7.27±1.17* 4.97±1.12* 3.47±1.08* 206.10±59.84 * P<0.05,与对照组比较 表 3 术后24、48周两组肝功能、血清蛋白及胆红素比较(
$ \bar{x}\pm s $ )组别 例数 时间 肝转氨酶(U/L) 血清蛋白(g/L) 胆红素(μmol/L) 胆固醇(mmol/L) AST ALT TP ALB TBIL DBIL TC 对照组 35 24周 22.42±6.12 27.35±7.08 60.62±14.81 38.19±9.50 14.82±3.61 4.77±1.56 4.62±0.59 35 48周 21.55±5.71 29.69±5.96 63.33±15.44 40.55±6.57 12.71±2.97 4.51±0.96 4.85±0.66 治疗组 25 24周 14.89±6.22* 25.88±6.79 62.07±15.12 40.33±6.99 13.09±2.57 5.01±1.43 4.33±0.71 25 48周 13.92±3.29* 19.8.9±6.1.4* 66.46±18.43* 44.17±8.58* 9.78±2.69** 3.81±1.23* 4.21±0.82* * P<0.05,** P<0.01,与对照组比较 表 4 术后1~48周两组免疫抑制剂FK506的用量比较 (
$ \bar{x}\pm s $ )组别 例数 1周 4周 12周 24周 48周 对照组 17 0.10±0.02 0.10±0.02 0.09±0.03 0.09±0.01 0.08±0.02 治疗组 12 0.10±0.01 0.10±0.03 0.09±0.02 0.08±0.02 0.07±0.01* * P<0.05,与对照组比较 表 5 术后1~48周两组免疫抑制剂CsA的用量比较 (
$ \bar{x}\pm s $ )组别 例数 1周 4周 12周 24周 48周 对照组 18 4.5±0.9 4.5±1.5 4.3±1.2 4.2±1.3 3.5±1.2 治疗组 13 4.5±1.0 4.5±1.1 4.2±1.3 4.0±1.5 3.3±1.1* * P<0.05,与对照组比较 -
[1] 祝明, 金樟照, 陈勇, 等. 百令胶囊的指纹图谱鉴别研究[J]. 中成药, 2007, 29(9):1254-1256. [2] 付宝慧, 王颖. 虫草菌丝体与天然虫草化学成分比较研究[J]. 中国社区医师, 2018, 34(30):7,9. [3] 刘晓利, 吴玉梅. 冬虫夏草治疗糖尿病肾病作用机制研究进展[J]. 山东医药, 2015, 55(46):98-100. [4] 陈仁慈, 项洁琼, 陈洪宇. 冬虫夏草治疗糖尿病肾病疗效的系统评价[J]. 中国中西医结合肾病杂志, 2017, 18(2):141-146. [5] 石炳毅, 袁铭. 中国肾移植受者免疫抑制治疗指南(2016 版)[J]. 器官移植, 2016, 7(5):327-331. [6] LINDHOLM A, DAHLQVIST R, GROTH G G, et al. A prospective study of cyclosporine concentration in relation to its therapeutic effect and toxicity after renal transplantation. Br J Clin Pharmacol, 1990, 30(3): 443-452. [7] KAHAN B D, KARLIX J L, FERGUSON R M, et al. Pharmacodynam ics, pharmacokinetics, and safety of multiple doses of FTY720 in stable renal transplant patients: a multicenter, randomized, placebo controlled, phase study[J]. Transplantation, 2003, 76(7):1079-1084. doi: 10.1097/01.TP.0000084822.01372.AC [8] 王征, 刘建利. 虫夏草化学成分研究进展[J]. 中草药杂志, 2009, 40(7):1157-1160. [9] 邓跃毅, 陈以平, 贺学林, 等. 冬虫夏草制剂延缓慢性肾衰竭的机理研究[J]. 中国中西医结合肾病杂志, 2001, 2(7):381-383. [10] YU L, ZHAO J, ZHU Q, et al. Macrophage biospec ificex traction and high performance liquid chromatogra phy for hypothesis of mimunological active components in Cordyceps sinensis[J]. J Pharm Biomed Anal, 2007, 44(12):439-443. [11] 朱运锋, 谌贻璞, 芮宏亮, 等. 虫草菌粉对慢性马兜铃酸肾病大鼠模型肾间质纤维化的保护作用[J]. 中华医学杂志, 2007, 87(38):2667-2671. doi: 10.3760/j.issn:0376-2491.2007.38.002 [12] 刘春燕, 陈云霞, 苏俊平, 等. 百令胶囊对糖尿病肾病患者肾功能的影响[J]. 河北医药, 2016, 45(1):52-54. [13] 钟广芝, 胡鹏飞. 百令胶囊联合环磷酰胺和醋酸泼尼松治疗肾病综合征的临床研究[J]. 现代药物与临床, 2016, 31(7):1028-1031. [14] 郑瑜倩, 程巧鸳, 祝明. HPLC同时测定百令胶囊中5种核苷类成分的含量[J]. 中国实验方剂学杂志, 2015, 21(5):61-64. [15] SHAHED A R, KMI S I, SHOSKES D A. Down regulation of apoptotic and inflammatory genes by Cordyceps sinensis extract in rat kidney folloing ischemia/reperfusion[J]. Transplant Proc, 2001, 33(6):2986-2987. doi: 10.1016/S0041-1345(01)02282-5 -





 下载:
下载:

 下载:
下载: 






