-
隐丹参酮(CTS)是中药丹参的有效成分之一,国内外研究证明CTS具有抗肿瘤、抗炎、神经保护、心血管保护、抗纤维化和调节代谢紊乱等药理特性,具有广阔的临床应用前景。抗肿瘤作用是近年来隐丹参酮药理活性研究的热点问题之一[1]。隐丹参酮对肺癌、肝胆癌、胃癌、食管癌、乳腺癌、前列腺癌、胰腺癌、结直肠癌、骨肉瘤癌、黑色素瘤、横纹肌瘤、食管鳞状癌等多种恶性肿瘤表现出一定的抑制活性,其抗肿瘤机理包括抑制肿瘤细胞增殖、迁移和侵袭,诱导细胞凋亡,调节免疫以及抑制包括STAT3在内的多种信号通路[2-4]。由于CTS中等强度的药理活性和选择性,近年来研究人员对CTS进行了大量结构修饰,期望获得靶点明确且药理活性更强的CTS衍生物,从而开发并应用于临床治疗。本文就隐丹参酮及其衍生物在抗肿瘤方面的作用及其机制进行综述。
-
癌细胞的主要特点是具有无限的增殖能力。研究表明,CTS可以抑制多种肿瘤细胞增殖,包括胰腺癌细胞BxPC-3、慢性髓性白血病细胞K562/ADR、胶质瘤细胞U87、人卵巢癌细胞Hey、前列腺癌细胞DU145、乳腺癌细胞MCF7、食管鳞状细胞癌ESCC等[5]。
-
细胞凋亡又称细胞程序性死亡,对于维持组织稳态和消除不需要或受损细胞起重要作用。研究发现,CTS可以诱导多种肿瘤细胞凋亡,包括骨髓瘤细胞U266、人结肠癌细胞系SW620 Ad300和HCT116、人胃癌细胞MKN-45、肝癌细胞Hepa1-6、非小细胞肺癌细胞A549 和H460 、黑色素瘤细胞A375、横纹肌肉瘤细胞Rh30等[6]。
-
高侵袭性和转移是癌细胞恶性特征,转移是癌症死亡的主要原因。因此,抑制癌细胞转移能有效降低癌症死亡率。研究发现,CTS能够抑制卵巢癌细胞A2780的迁移和侵袭[7]。此外,CTS还可以抑制食管癌细胞EC109、膀胱癌细胞T24、人舌鳞癌细胞CAL27、小鼠结肠癌细胞CT26等多种肿瘤细胞的迁移和侵袭[5]。
-
隐丹参酮不仅能够直接抑制多种肿瘤细胞的生长,还可以诱导机体产生抗肿瘤免疫反应,从而间接发挥抗肿瘤效应。研究发现,隐丹参酮能够通过增加CD4+T细胞的细胞毒作用,抑制人非小细胞肺癌H446细胞和乳腺癌MCF7细胞的生长[8]。此外,隐丹参酮还可以通过诱导小鼠树突状细胞成熟,促进抗原提呈功能,进而诱导T细胞活化增殖,抑制Lewis肺癌细胞的增殖[9]。肿瘤相关巨噬细胞 (TAM) 是肿瘤组织中浸润的巨噬细胞,具有异质性,可分为M1和M2表型。M2表型的TAM能够促进肿瘤生长和转移,相反,M1表型则具有肿瘤抑制和促炎特性。研究发现,隐丹参酮和PD-L1联合治疗能够诱导巨噬细胞向M1极化,从而抑制小鼠肝癌Hepa1-6移植瘤的生长[10]。
-
耐药是导致肿瘤复发和治疗失败的主要原因。研究表明,CTS能够逆转慢性骨髓性白血病细胞K562对伊马替尼的耐药性[11],改善A549细胞对顺铂的耐药性[12]。此外,CTS还可以逆转P-糖蛋白(p-gp)过表达的结肠癌细胞SW620 Ad300对多柔比星和伊立替康的多重耐药[13]。
-
除了具有以上活性之外,CTS还可以与其他不同抗癌药物或细胞因子协同发挥抗肿瘤作用。例如,CTS和紫杉醇的联合用药比单独用药更能有效诱导舌鳞状细胞癌CAL27和SCC-9细胞的凋亡[14]。新近研究发现,CTS与小剂量的抗PD-L1抗体合用对小鼠Lewis 肺癌的生长抑制作用明显优于CTS单独应用[9]。
-
自噬,即Ⅱ型程序性细胞死亡,作为凋亡之外的另一种可以杀死细胞的途径,是一种抑制癌细胞生长的新方法。研究显示,CTS可通过诱导结肠癌SW620 Ad300细胞和A549细胞自噬促进细胞死亡[15-16]。
-
CTS抑制肿瘤细胞增殖、迁移和侵袭,诱导细胞凋亡,以及调节免疫等作用的机制十分广泛,涉及靶点STAT3、酪氨酸蛋白磷酸酶SHP2、DNA拓扑异构酶和信号通路磷酸酰肌醇3-激酶(PI3K)/丝氨酸/苏氨酸激酶Akt等。
-
STAT3由Janus激酶(JAKs)激活,参与肿瘤增殖、凋亡、血管生成及免疫逃逸等。STAT3在大多数恶性肿瘤中被组成性激活,异常的STAT3信号传导是肿瘤恶性进展的重要过程。当705位酪氨酸残基磷酸化后,STAT3被激活,单体STAT3通过其SH2结构域形成二聚体,并从细胞质转移到细胞核中,调节其靶基因的表达,例如,上调cyclin D1、survivin、Mcl-1、MYC、BCL-XL表达,下调 p53表达,促进肿瘤细胞增殖和存活;上调MMP2/9、Twist1、Vimentin表达,促进肿瘤转移;上调TGF-β、IL-6/10、PD-1、PD-L1、VEGF表达,下调CD80/86、MHCII、TNF、IL-12、CCL5、CXCL10等表达,抑制肿瘤微环境免疫功能[17]。研究发现,CTS能够直接与STAT3的SH2结构域结合,特异性抑制STAT3 Tyr705的磷酸化,抑制STAT3二聚化[18-19],相比之下,姜黄素还能抑制Jak2的表达[20]。在人胰腺癌BxPC-3细胞中,CTS能够抑制BxPC-3细胞的STAT3信号通路进而抑制细胞增殖,诱导细胞凋亡,达到抗肿瘤的作用[21]。另外,CTS作为p-STAT3抑制剂,能够有效阻断IL-6介导的STAT3活化,抑制肿瘤增殖,逆转BCR-ABL激酶非依赖性耐药途径[11]。此外,CTS和紫杉醇联合治疗能够有效地抑制舌鳞状癌TSCC细胞增殖和迁移,其作用机制同样与抑制STAT3信号通路相关[14]。沉默信息转录调控因子3(SIRT3)是一种蛋白质去乙酰化酶,参与癌症、心血管、神经系统等疾病的发展过程。研究发现CTS能够通过抑制STAT3/SIRT3 信号通路抑制人卵巢癌A2780 细胞增殖[22]。 上述研究表明,抑制STAT3信号通路对于CTS抗肿瘤至关重要,且CTS是一种特异性的STAT3抑制剂。
-
含Src同源2结构域蛋白酪氨酸磷酸酶(SHP2)由基因PTPN11编码,PTPN11突变引起SHP2催化活性异常增加。研究发现,肺癌、结肠癌、黑色素瘤、神经母细胞瘤、肝癌和急性髓性白血病等病人均发现有PTPN11突变[23]。SHP2是一种非受体蛋白酪氨酸磷酸酶,参与Ras-Erk、PI3K-Akt、Jak-Stat和NF-κB多条信号通路传导,调控细胞的增殖、迁移和凋亡等过程[24]。研究证明,CTS能与SHP2直接结合,是一个混合型蛋白酪氨酸磷酸酶抑制剂,抑制SHP2 的IC50为22.50μmol/L,抑制SHP1的IC50为39.50μmol/L。用SHP2 siRNA敲减Hela细胞中SHP2后,CTS抑制Hela细胞生长的敏感性降低,提示SHP2是CTS的一个靶点,但是,CTS仍然可以进一步抑制SHP2敲减细胞生长,说明CTS还有其它作用靶点[25]。此外,有研究发现,CTS能够上调胶质瘤细胞 U87 SHP2蛋白酪氨酸磷酸酶活性,抑制STAT3 Tyr705的磷酸化,从而在体内外表现出抑制恶性胶质瘤活性[26]。
-
DNA拓扑异构酶 (topos),包括DNA拓扑异构酶1(topo1)和DNA拓扑异构酶2(topo2),其中topo2因其在有丝分裂中的关键作用被认为是抗癌治疗的重要靶点[27]。研究表明,CTS能够显著降低前列腺癌PC3细胞中topo 2a的mRNA、蛋白和酶活性水平,并且在裸鼠异种移植模型中表现出良好的抗肿瘤作用[28]。
-
活性氧与肿瘤的发展密切相关,其过度产生可诱导多种生物学效应,包括抑制细胞增殖、诱导细胞凋亡和自噬等[29]。研究发现,CTS能够促进胃癌MKN-28 细胞ROS的累积,通过调控MAPK和AKT信号通路诱导G2/M周期阻滞[30];通过ROS-线粒体途径,上调cleaved caspases-3、促凋亡蛋白Bax和下调抗凋亡蛋白Bcl-2,从而诱导黑色素瘤细胞凋亡[31];诱导横纹肌肉瘤Rh30细胞ROS产生,激活JNK/p-38,抑制Erk1/2,导致细胞凋亡[32];刺激SW620 Ad300细胞中的ROS产生,诱导p38 MAPK激活,导致NF-κB从细胞质转移到细胞核中,最终导致自噬发生[15];刺激HepG2和MCF-7细胞产生ROS,激活内质网(ER)应激,增强不同抗癌药物或细胞因子(Fas/Apo-1、TNF-α、顺铂、依托泊苷或5-FU)诱导的细胞凋亡[33]。
-
雄激素受体(AR)和雌激素受体(ER)分别是治疗前列腺癌PCa和乳腺癌的主要靶点。研究发现CTS可以通过抑制AR二聚化有效抑制AR活性,从而抑制AR+ PCa细胞的生长[34];在异种移植动物模型中,CTS可以有效抑制人前列腺癌CWR22Rv1细胞的生长和AR靶基因的表达[35]。此外,CTS还能够抑制乳腺癌细胞的生长,通过竞争性地结合ERα抑制E2诱导的ER转录活性和ER靶基因的表达[36];同时,CTS可以有效地抑制体内异种移植瘤模型中ER信号,发挥抗肿瘤作用[37]。
-
磷酸肌醇3-激酶(PI3K)/蛋白质丝氨酸苏氨酸激酶(Akt)信号通路参与肿瘤的发生、生长、存活和转移。有研究发现CTS可抑制PI3K/AKT信号通路,增加caspase-3、caspase-9、PARP和Bax的表达,降低Bcl-2、survivin、细胞凋亡抑制蛋白的表达,诱导非小细胞肺癌细胞的凋亡[38-39]。酪氨酸激酶胰岛素生长因子1受体(IGF-1R)在肿瘤细胞的生长、分化和进展中起关键的作用。研究表明,CTS能够通过下调IGF-1R/PI3K/Akt信号通路抑制人肺癌细胞的增殖[40]。此外,有文献报导CTS可以通过调节PI3K/Akt/mTOR信号,抑制结肠癌CT26细胞的侵袭[41]。在裸鼠异种移植实验中,CTS能够显著抑制小鼠体内异种移植物的生长,其作用机制与抑制PI3K/AKT/NF-κB信号通路有关[42]。以上研究表明PI3K/AKT信号通路可能是CTS抗肿瘤的有效信号通路之一。
-
CTS虽然具有广谱的抗肿瘤活性,但是其药理作用中等,疏水性强且难吸收,口服生物利用度只有2.1%,这些缺点严重阻碍了其开发和应用[43]。近年来,针对CTS存在的问题,人们尝试对CTS进行结构改造,期望获得生物活性高、水溶性好的化合物。刘航[44]等基于CTS是一种STAT3抑制剂,通过对CTS及其骨架类似物进行修饰,设计合成了CTS衍生物62个,其中新化合物46个,通过报告基因法检测发现有27个新化合物对STAT3转录抑制效果优于CTS,IC50最低0.5976 μmol/L。Wang等基于STAT3的药物设计策略,设计合成了一种亲和力和抑制活性更强的新型CTS衍生物LYW-6,该化合物与STAT3结合解离常数Kd约为6.6μmol/L,能够显著抑制STAT3磷酸化、二聚化、核转位以及转录活性。在细胞水平上,LYW-6能选择性抑制高STAT3活性的结肠癌细胞增殖、迁移,促进凋亡,体内可抑制结肠癌的生长和转移,是一个具有开发前景的抗肿瘤活性化合物[45]。为了改善CTS的水溶性,Xu等合成了几种CTS的钠盐衍生物,结果发现这些衍生物比CTS更易溶解,同时保留了CTS的生物活性,其中钠盐衍生物PTS33可以有效地抑制二氢睾酮DHT诱导AR反式激活和PCa细胞生长[46]。
-
CTS具有广谱的抗肿瘤活性,该活性与抑制肿瘤细胞增殖、迁移和侵袭,诱导细胞凋亡,逆转耐药性,诱导自噬等作用相关。除直接作用于肿瘤细胞外,CTS还可以通过增强CD4+T细胞的细胞毒作用、诱导DC细胞成熟和促使巨噬细胞M1型极化,间接杀伤肿瘤细胞。分子机制研究表明,CTS可直接结合STAT3和SHP2,有效调节JAK/STAT3、NF-κB、PI3K/AKT和IGF-1R等信号通路发挥抗肿瘤作用。隐丹参酮特异性抑制STAT3信号通路,而不抑制STAT家族中的其他蛋白,是其一大特点。因为尽管其他天然产物也有抗肿瘤作用,但不是特异性STAT3抑制剂,例如姜黄素,是一种STAT抑制剂,但在治疗24 h后降低了STAT3的表达。虽然CTS表现出良好的药理活性,但水溶性差和生物利用度低等问题限制了其广泛应用。因此,基于靶点STAT3,以CTS作为先导化合物,设计并合成一系列CTS衍生物,有望开发出新型STAT3抑制剂用于癌症治疗。
Progress on the antitumor activity of cryptotanshinone and its derivatives
-
摘要: 隐丹参酮是中药丹参的有效成分之一,对多种肿瘤显示很好的活性。其抗肿瘤效应包括抑制细胞增殖、诱导肿瘤细胞凋亡、抑制细胞迁移和侵袭、调节机体免疫功能和逆转药物耐药性等。抗肿瘤直接靶点有信号转导和转录激活因子3(STAT3)、酪氨酸蛋白磷酸酶SHP2、DNA拓扑异构酶2(top2) ,其它的作用机制包括诱导活性氧(ROS)产生、调控雌、雄激素受体信号、抑制PI3K/AKT信号通路等。此外,近年来研究人员还设计合成了许多隐丹参酮衍生物,并对其抗肿瘤作用进行了研究。本文主要就隐丹参酮及其衍生物抗肿瘤活性研究进展进行综述,希望能够有助于隐丹参酮及其衍生物在抗肿瘤方面的药物研发。Abstract: Cryptotanshinone is one of the effective components of traditional Chinese medicine salvia miltiorrhiza which shows good activities against a variety of tumors. Its anti-tumor effects include inhibition of tumor cell proliferation, induction of cell apoptosis, inhibition of cell migration and invasion, regulation of immune function and reversal of drug resistance. The direct anti-tumor targets include signal transducer and activator of transcription 3 (STAT3), tyrosine protein phosphatase SHP2, DNA topoisomerase 2, and other mechanisms of action include the induction of reactive oxygen species (ROS) production, regulation of estrogen and androgen receptor signaling, and inhibition of PI3K/AKT signaling pathway. In addition, many cryptotanshinone derivatives have been designed and synthesized to study the antitumor effects. The research progress of the antitumor activity of cryptotanshinone and its derivatives were reviewed in this paper to give references to the anti-tumor drug development of cryptotanshinone and its derivatives.
-
Key words:
- cryptotanshinone /
- derivatives /
- anti-tumor /
- mechanism
-
抑郁症是一种使人衰弱的精神障碍,其特征是持续情绪低落,对几乎所有活动都失去兴趣或愉悦感,并与疲劳、睡眠障碍、焦虑和神经认知障碍症状有关[1],是全球残疾的第三大原因。抑郁症患者工作低下、具有较高的自杀倾向,严重影响患者的生活,造成沉重的社会经济负担[2]。由于疫情的影响,社会心理健康问题正在急剧增加[3,4]。目前,临床上使用的大多数抗抑郁药都具有耐药性,并伴有各种不良反应。因此,寻找安全性更高、不良反应更少的抑郁症治疗方法具有重要意义。既往研究表明,炎症反应在抑郁症中起着至关重要的作用[5]。抑郁症患者血液及额叶皮层中的促炎细胞因子增加[6,7]。抗炎治疗可以产生抗抑郁作用,而抗抑郁药可以减弱抑郁症中促炎细胞因子的表达[8,9]。因此,抑制神经炎症是治疗抑郁症的重要方向。
百合知母汤是中国东汉张仲景医典《金匮要略》中记载的一种经典中药方剂,用于治疗“百合病”[10]。中医“百合病”被认为与现代抑郁症的表现具有较高的相似性[11]。目前,百合知母汤在中医临床上被广泛用于治疗抑郁症[12]。药理学研究表明,百合知母汤在动物模型中具有显著的抗抑郁作用[13]。然而,百合知母汤治疗抑郁症的作用机制并未完全明了。前期研究发现百合知母汤能够通过抑制CUMS抑郁模型小鼠的神经炎症,降低海马IL-1β、 IL-6和TNF-α等促炎细胞因子的表达,来发挥抗抑郁作用[14]。鉴于NLRP1炎症小体在炎症反应过程中的重要的作用[15],且最近研究发现NLRP1炎症小体在抑郁症的发展过程中扮演重用角色[16]。该研究基于NLRP1炎症小体的活化,对百合知母汤的抗抑郁作用进行进一步的探索。
1. 材料和方法
1.1 百合知母汤的制备
取百合药材400 g、知母药材200 g,浸泡0.5 h后,加10倍量水,煎煮两次,每次2 h,煎液过滤后,将两次滤液混合并浓缩至600 ml。
1.2 实验试剂
Muramyl dipeptide(MDP)购自Sigma-Aldrich公司;IL-1β、IL-6、TNF-α、5-HT、NE、DA试剂盒和ELISA试剂盒均购自美国R&D公司;BSA购自美国Sigma-Aldric公司;去离子水采用Milli-Q纯水机制备(Millipore公司);NLRP1、ASC、caspase-1、BDNF、TrkB、ERK、AKT、mTOR、β-actin等抗体均购自 Cell Signaling公司; BCA蛋白测定试剂盒与RIPA裂解液购自碧云天公司。
1.3 实验动物
雄性C57BL/6J小鼠8周龄,体质量22 g~25 g,购自浙江维通利华实验动物技术有限公司,生产许可证: SCXK(浙)[2019-0001]。所有小鼠均在标准条件下饲养(12 h光/暗循环,温度:22 ℃~24 ℃,湿度:55%±10%),在整个实验过程小鼠自由摄取食物和水。实验前对所有小鼠进行适应性喂养1周。该研究经上海交通大学医学院附属仁济医院伦理委员会审批通过,实验操作严格按照动物福利和伦理原则进行。
1.4 CUMS模型建立
CUMS造模过程参考前期研究,通过给予小鼠不同刺激构建抑郁症模型小鼠,主要过程如下:①禁食24 h;②禁水 24 h;③空瓶刺激 1 h;④昼夜照明 24 h;⑤笼子倾斜45◦ ,24 h;⑥潮湿垫料24 h;⑦摇笼30 min;⑧夹尾1 min;⑨冰水游泳5 min。小鼠每天接受不同的应激,持续5周。
1.5 动物分组及给药
根据前期研究[14],百合知母汤给药采用6 g生药量/kg(相当于百合4 g,知母2 g)和12 g生药量/kg(相当于百合8 g,知母4 g)两个剂量。将30只雄性C57BL/6J小鼠随机分为5组(n=6):对照组、模型组、百合知母汤低剂量组(百合知母汤,6 g/kg,i.g.)、百合知母汤高剂量组(百合知母汤,12 g/kg,i.g.)、百合知母汤+MDP组(百合知母汤,12 g/kg,i.g.;MDP,脑立体定位注射)。除对照组外,各组小鼠接受CUMS刺激,持续5周,对照组被放置在不受干扰的笼子里。从第6周开始,给药组按剂量通过灌胃给予百合知母汤浓缩液,1次/d,持续4周。模型组小鼠给予等量的蒸馏水。为考察NLRP1在百合知母汤抗抑郁过程中的重要作用,设立百合知母汤+MDP组,给药前接受脑立体定位注射NLRP1激活剂MDP,过程如下:经异氟烷麻醉的小鼠俯卧位固定于脑立体定位仪上,将眼中线靠后 2~3 cm 处用 75% 乙醇消毒、剪皮露出头骨,用注射器针头将头骨表层骨膜轻挑剥离,前后囟在同一水平,暴露前囟(冠状缝)。选择小鼠双侧海马CA1 区为注射位置,进针 1.6 mm 至海马区,注射MDP,剂量5 mg/kg,结束后使用可吸收缝合线进行无菌缝合。
1.6 行为学考察
1.6.1 蔗糖偏好实验
每只小鼠置于单独的笼子里孤养,放置2瓶含有1%蔗糖溶液,进行24 h的适应。然后其中一瓶蔗糖溶液用蒸馏水代替,进行另一次24 h的适应。随后禁水、禁食 24 h。最后,放置2个预先称重的含有1%蔗糖溶液或蒸馏水的瓶子。3 h后,记录蔗糖溶液消耗量和水消耗量,计算蔗糖偏好指数。
1.6.2 悬尾实验
用胶带固定每只小鼠的尾部,头部向下,离台面50 cm。在实验过程中,将小鼠隔开以避免互相干扰。记录6 min内小鼠的累计不动时间。
1.6.3 强迫游泳实验
在室温下,将每只小鼠分别放入直径12 cm的塑料桶中,桶中装满25 cm深的水。在正式实验前24 h,进行15 min的预游泳适应训练。记录5 min内小鼠的累计漂浮不动时间。
1.6.4 旷场实验
将小鼠单独放置在敞箱装置中,给予6 min的自由探索时间,使其适应,然后记录其4 min内穿越的格子数。
1.7 神经递质和炎症因子水平的测定
各组小鼠用10%(w/v)水合氯醛深度麻醉。迅速取脑,置于冰上。分离海马,液氮预冷冻,于−80 ℃下储存,分析用。检测时,取海马,加入磷酸盐缓冲液(PBS:137 nmol/L NaCl、2.7 nmol/L KCl、10 nmol/L Na2HPO4、1.8 nmol/L KH2PO4),于冰上匀浆,4 ℃下以
12000 r/min,离心10 min,收集上清液。使用ELISA试剂盒检测小鼠海马中的炎症因子水平。IL-1β、IL-6、TNF-α、5-HT、NE 和DA的水平,操作均按照说明书进行。1.8 免疫荧光染色
迅速取小鼠大脑放置冰上,分离海马,用液氮预冷冻,并在−80 ℃下储存。使用冷冻切片机将海马组织切成5 μm的切片。切片用PBS缓冲液洗涤2次。然后用含0.5% Triton X-100的PBS 缓冲液透化,并用0.5% BSA固定,加入一抗,4℃,孵育过夜。加入荧光素标记的二抗孵育(室温,1 h)。通过荧光显微镜对切片成像。
1.9 Western blot法检测蛋白的表达水平
取小鼠海马组织,加入含1%蛋白酶抑制剂的RIPA裂解液,于冰上研磨,在4℃下,
12000 r/min,离心10 min。收集上清液,用BCA蛋白浓度测定试剂盒测定蛋白浓度后,用10%十二烷基硫酸钠/聚丙烯酰胺凝胶电泳(SDS-PAGE)分离总蛋白,分离后转移到聚偏氟乙烯(PVDF)膜上,用5%牛血清白蛋白(BSA)在室温下封闭2 h,随后孵上一抗,4 ℃,孵育过夜。过夜后用TBST洗涤3次,每次洗涤10 min。然后与辣根过氧化物酶标记的二抗孵育1 h,TBST洗涤3次,每次10 min。最后使用ECL显影液进行显影。1.10 统计分析
使用GraphPad Prism 8.0(GraphPad Software,USA)进行统计分析。数据以平均值±标准差(SD)表示。使用单向方差分析和Tukey HSD检验评估各组之间的差异。P<0.05的显著性水平被认为是统计学显著性的指示。
2. 结果
2.1 百合知母汤对CUMS小鼠行为学影响
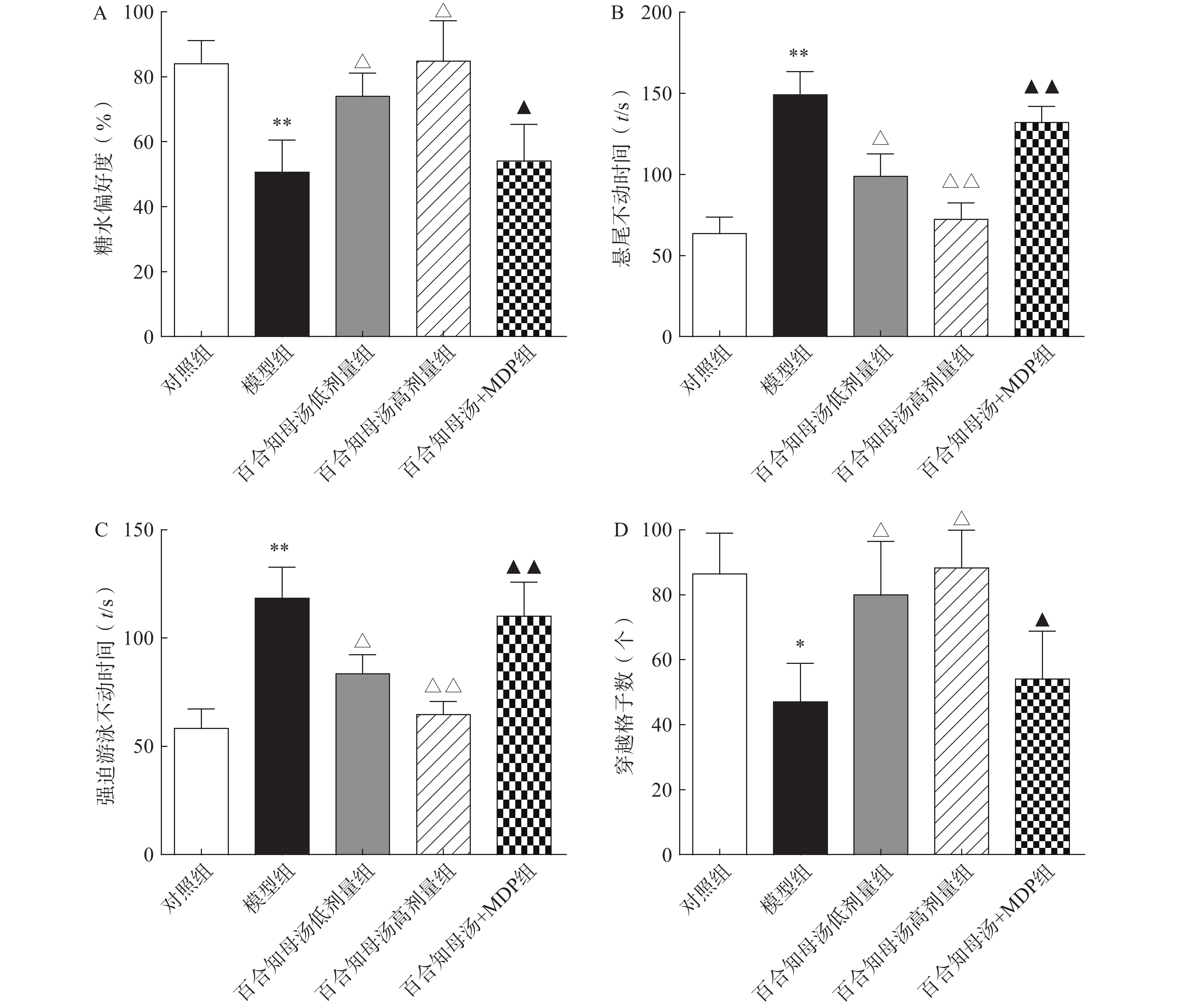
为了评估百合知母汤的药理作用,首先进行糖水消耗实验、悬尾实验、强迫游泳实验和旷场实验,观察百合知母汤对CUMS小鼠行为学的影响。如图1所示,与对照组相比,CUMS模型组在糖水消耗实验中的蔗糖消耗百分比和旷场实验中的格子穿越数显著减少(P<0.01,P<0.05),而悬尾实验和强迫游泳实验的不动时间显著增加(P<0.01)。而百合知母汤能显著提高这些参数(P<0.05,P<0.01),并呈明显的剂量依赖性。表明百合知母汤能改善抑郁小鼠的行为学特征。值得注意的是,NLRP1炎症小体激活剂MDP能够显著的逆转百合知母汤对抑郁症小鼠行为学的作用(P<0.05,P<0.01),提示百合知母汤通过抑制NLRP1炎症小体活化来发挥抗抑郁作用。
2.2 百合知母汤对CUMS小鼠神经递质变化的影响
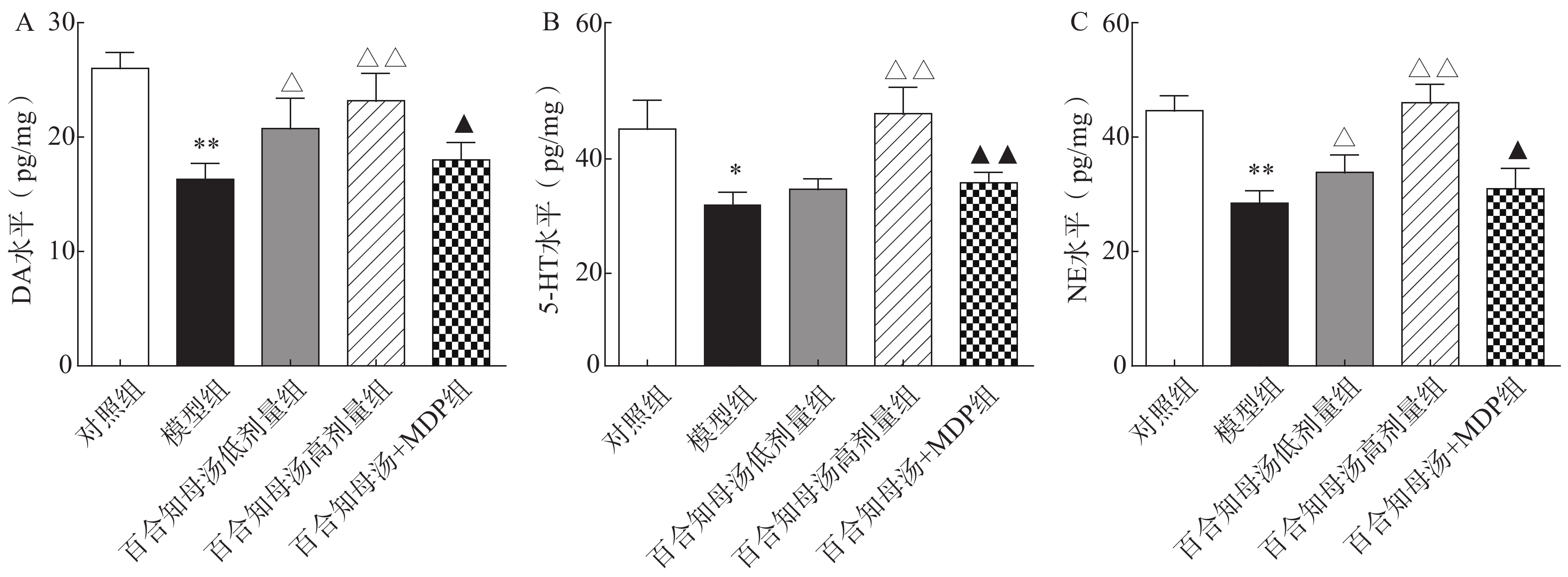
中枢神经系统单胺类神经递质水平降低与抑郁症的产生具有密切关系。图2结果表明,CUMS模型组的DA、5-HT、NE水平与对照组相比显著降低(P<0.05,P<0.01),而CUMS+BZD6组和CUMS+BZD12组上述神经递质的含量明显高于模型组(P<0.05,P<0.01)。NLRP1激活能够显著的逆转百合知母汤对上述神经递质的影响(P<0.05,P<0.01)。
2.3 百合知母汤对抑郁症相关炎症因子的影响
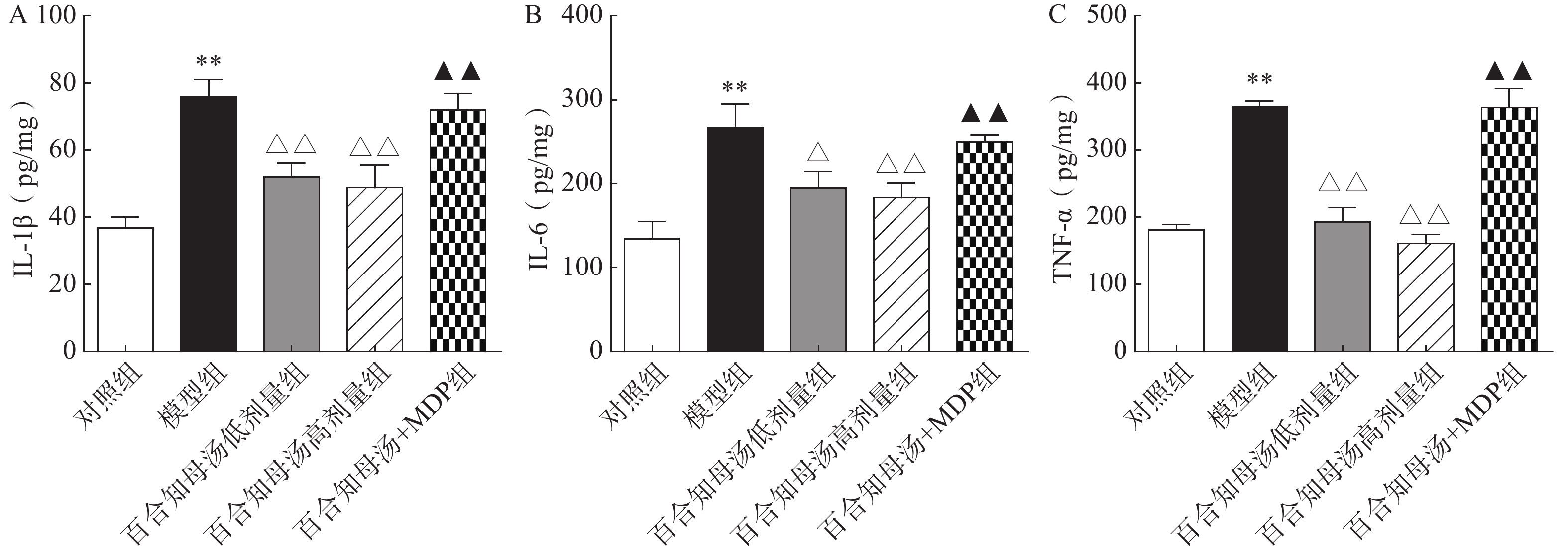
越来越多的研究表明炎症在抑郁症的病因中起着关键作用。因此,用ELISA法测定了几种关键的促炎细胞因子。如图3所示,与对照组相比,CUMS模型组小鼠海马中的IL-1β、IL-6和TNF-α水平显著升高(P<0.01),而百合知母汤显著抑制了由CUMS引起的这些炎症因子的升高(P<0.05,P<0.01),NLRP1激活剂MDP能够显著的逆转百合知母汤对上述神经递质的影响(P<0.01)。
2.4 百合知母汤对小鼠海马NLRP1炎症小体的影响
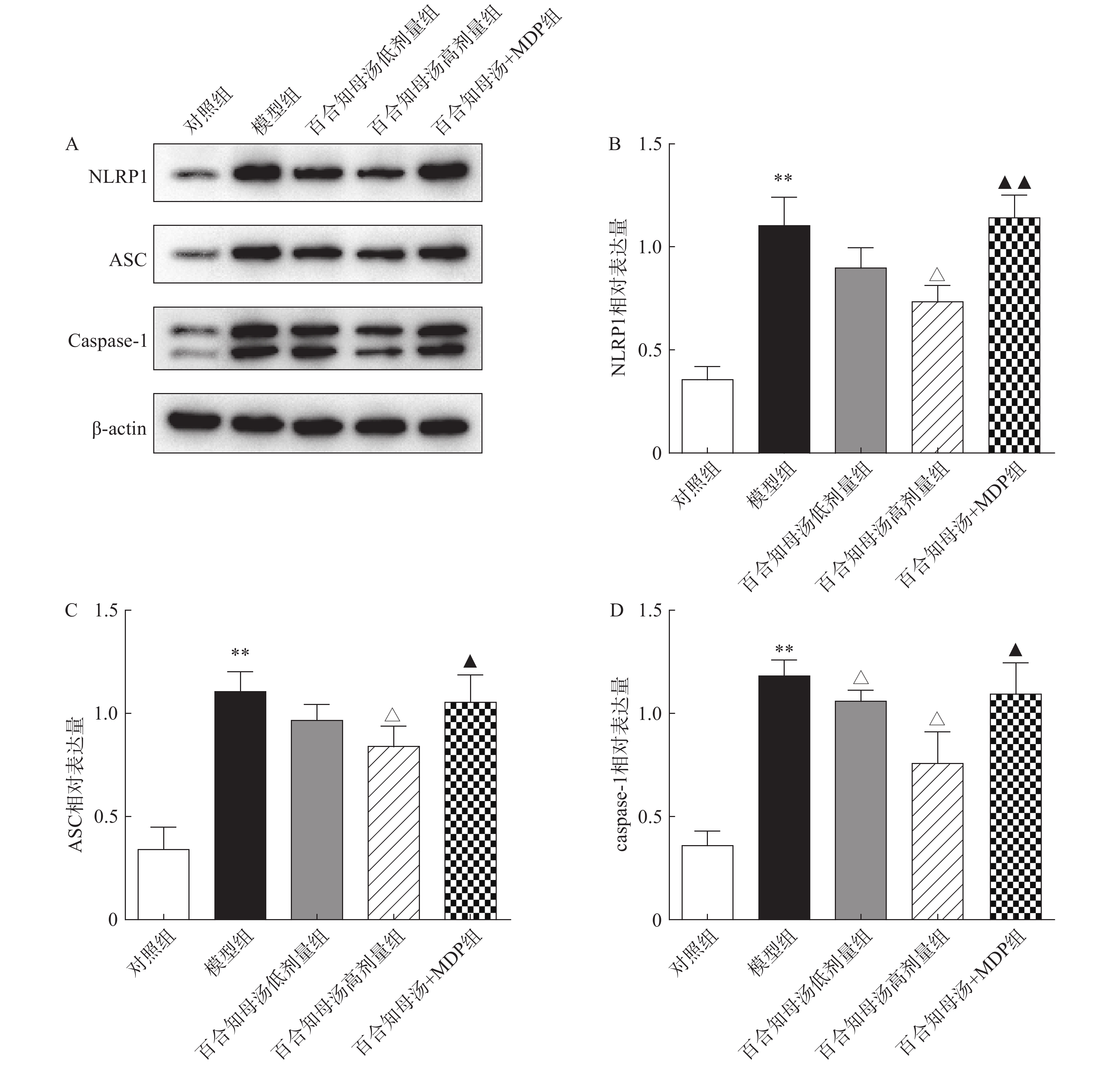
NLRP1炎症小体在神经炎症相关疾病中扮演重用角色,NLRP1炎症小体的活化能促进各种炎症因子的产生[17]。因此,采用Western blot检测NLRP1炎症小体的活化。图4结果显示,CUSM刺激显著增加了NLRP1、ASC和caspase-1的蛋白表达(P<0.01),表明NLRP1炎症小体在CUSM抑郁模型中被激活。而百合知母汤显著抑制了由CUMS引起NLRP1、ASC和caspase-1表达升高(P<0.05)。表明百合知母汤能抑制NLRP1炎症小体的激活。值得注意的是,NLRP1激活剂MDP能够显著逆转百合知母汤对上述蛋白表达的抑制作用(P<0.05,P<0.01),进一步表明百合知母汤通过抑制NLRP1炎症小体活化来发挥抗神经炎症的作用。
2.5 百合知母汤对小鼠海马BDNF表达的影响
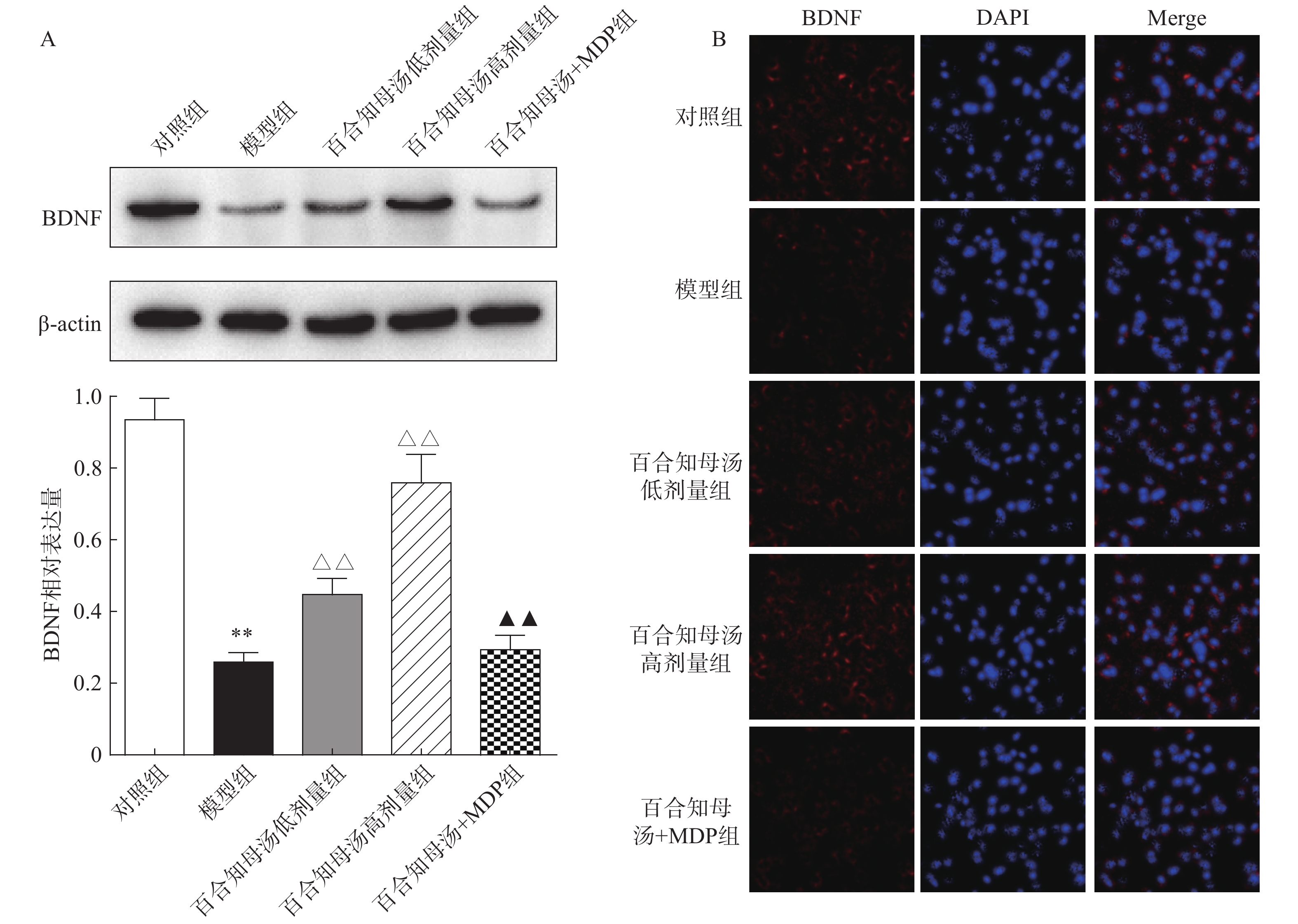
由于BDNF与抑郁症的发生发展密切相关[18],通过Western blot检测BDNF在不同组小鼠海马中的表达(图5A)。与对照组相比,CUMS模型组小鼠海马表达BDNF水平显著降低(P<0.01),而百合知母汤以量效依赖方式显著上调BDNF表达水平(P<0.01)。MDP能够显著阻断百合知母汤对BDNF表达水平的作用(P<0.01)。
随后,用免疫荧光对小鼠海马的BDNF表达进行检测(图5B)。结果发现,与对照组相比,CUMS模型组小鼠海马表达BDNF水平显著降低,而百合知母汤治疗组BDNF表达水平显著上调。NLRP1激活剂MDP能够显著的逆转百合知母汤对BDNF表达水平表达的上调作用。
2.6 百合知母汤对小鼠海马TrkB和下游ERK/AKT/mTOR通路相关蛋白表达的影响
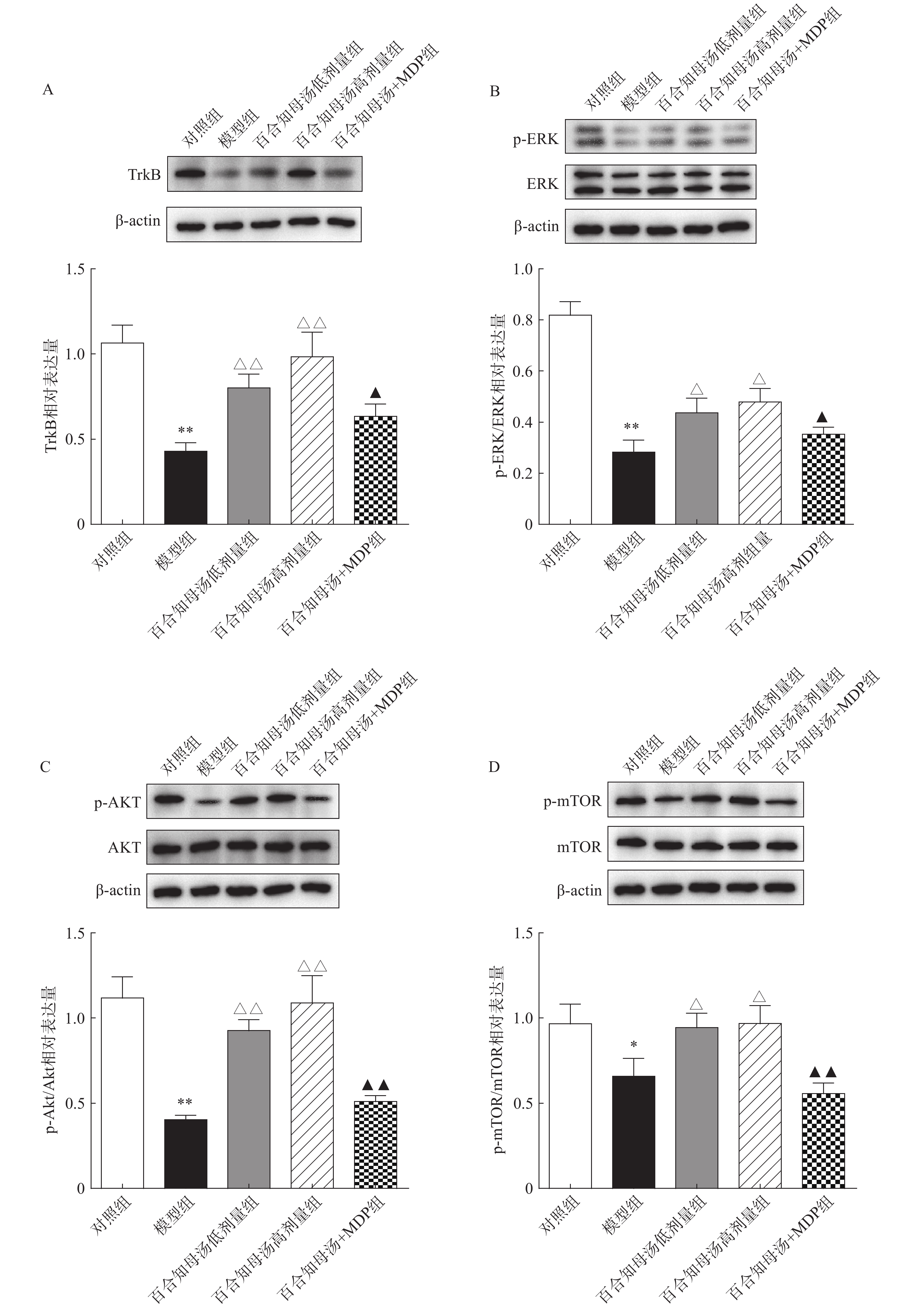
BDNF能够与TrkB结合,从而激活AKT/mTOR级联反应,最终通过调节突触蛋白合成和细胞骨架发育来增强树突的复杂性[19]。因此,继续探讨百合知母汤对TrkB及下游ERK/AKT/mTOR通路关键蛋白表达的影响。百合知母汤对小鼠海马TrkB表达的影响如图6A所示。与对照组相比CUMS模型组小鼠海马TrkB的表达显著降低(P<0.01),百合知母汤给药组小鼠海马TrkB的表达水平显著升高(P<0.01)。而MDP能够逆转百合知母汤对TrkB表达水平的上调作用(P<0.05)。
如图6B-D所示,与对照组相比,CUMS组小鼠海马ERK、AKT和mTOR的磷酸化水平显著降低,而百合知母汤给药可显著促进抑郁小鼠ERK、AKT和mTOR的磷酸化水平(P<0.05,P<0.01)。NLRP1激活剂MDP能够显著的逆转百合知母汤对上述蛋白磷酸化水平的促进作用(P<0.05,P<0.01)。
3. 讨论
神经炎症是一种对组织损伤的先天免疫反应,在许多中枢神经系统疾病中发挥着重要作用,被认为与抑郁症的发生发展息息相关[20, 21]。大量证据表明,海马体的神经炎症对抑郁和焦虑障碍的发展至关重要。神经性疼痛诱导的抑郁样行为的发作与海马TNF及其受体TNFR1水平的增加相关[22]。敲减海马中IL-1β可以减轻LPS诱导的小鼠焦虑和抑郁样行为[23]。而给予IL-1受体拮抗剂可以改善神经性疼痛对抑郁样行为的影响[24]。以上研究结果表明,海马神经炎症在抑郁症的病理过程中起着重要作用。
炎症小体是先天免疫反应的关键成分,据报道与炎症相关神经系统疾病的机制有关[25]。NLRP1炎症小体由受体蛋白NLRP1、衔接蛋白ASC和效应蛋白caspase-1组成,在神经炎症相关疾病中起重要作用。NLRP1可被多种刺激激活,包括炭疽杆菌致死毒素、弓形虫、胞壁酰二肽、宿主细胞内ATP耗竭等[21]。NLRP1炎症小体的激活导致Caspase-1的直接成熟,随后诱导促炎细胞因子(如IL-1β和IL-18)的产生,从而触发神经炎症反应[26]。据报道,NLRP1炎症小体驱动的炎症途径与许多神经系统疾病有关,如脑损伤、神经退行性疾病、伤害感受和癫痫[27]。
百合知母汤抗抑郁作用及其机制既往已有研究[13,14],然而基于NLRP1炎症小体的活化对其抗抑郁机制的研究未见报道。该研究旨在通过探讨百合知母汤对NLRP1炎症小体的活化作用来阐释百合知母汤抗抑郁的作用机制。结果显示,百合知母汤抑制了CUMS抑郁症小鼠海马NLRP1、ASC和Caspase-1的表达升高。表明百合知母汤能够抑制NLRP1炎症小体的活化。为了证实百合知母汤通过NLRP1/Caspase-1通路发挥抗抑郁作用,采用NLRP1激活剂MDP注射抑郁症小鼠。结果发现,MDP逆转了百合知母汤对CUMS小鼠的抑郁样行为和神经炎症的改善作用。因此,百合知母汤可能通过抑制NLRP1炎症小体的活化,以调节抑郁症小鼠的神经炎症反应,来发挥抗抑郁作用。
BDNF属于神经营养因子家族,在神经的生成、发展和功能维持中起着至关重要的作用[28]。大量研究表明,BDNF与抑郁症的病理生理学和抗抑郁疗效有关[29]。研究发现,抑郁症动物和患者以及抑郁症受试者的尸检样本中,大脑BDNF水平降低[28, 30]。此外,给予LPS或促炎细胞因子可显著降低海马和大脑皮层的BDNF水平[31]。这表明炎症会影响BDNF的表达。抗抑郁药物治疗可以有效改善抑郁症引起的BDNF含量的降低,进一步促进神经发生,增强神经可塑性,并起到抗抑郁的作用[32]。研究发现,BDNF的释放以及与TrkB的结合能够触发多种下游信号级联,包括RAS/MAPK通路和PI3K/AKT通路,这些信号通路与抑郁症的发生发展密切相关[33]。慢性应激可抑制ERK信号的传递,抗抑郁治疗则可逆转这种抑制[34],表明ERK信号阻断会导致抑郁和焦虑行为。这与抑郁症患者的尸检报告一致[35]。此外,慢性应激还会导致内侧前额叶皮层锥体神经元的树突形态发生变化,具体表现为树突回缩和树突棘丢失[36]。而抗抑郁治疗可以通过AKT/mTOR途径逆转这一现象,并有效改善小鼠的抑郁样症状[37]。上述研究表明,BDNF与TrkB结合,进而通过ERK和AKT/mTOR信号通路引发的信号级联反应可能是抗抑郁药物发挥治疗作用的关键分子机制。本研究结果显示,百合知母汤能显著促进抑郁症小鼠海马BDNF和TrkB的表达水平,表明百合知母汤能上调BDNF/TrkB信号通路。同时,百合知母汤能显著促进RK、AKT和mTOR的磷酸化水平。表明百合知母汤能同时激活下游的ERK/AKT/mTOR信号通路。而采用NLRP1激活剂MDP活化NLRP1炎症小体后,百合知母汤对BDNF/TrkB信号通路和ERK/AKT/mTOR信号通路上调作用被显著逆转,表明百合知母汤通过抑制NLRP1炎症小体活化,激活BDNF/TrkB信号通路和ERK/AKT/mTOR信号通路。
综上所述,百合知母汤通过抑制NLRP1炎症小体活化,抑制CUMS抑郁症小鼠海马的神经炎症反应,进而激活BDNF/TrkB信号通路和ERK/AKT/mTOR信号通路来改善CUMS小鼠的抑郁样行为。
-
[1] YUAN D P, LONG J, LU Y, et al. The forecast of anticancer targets of cryptotanshinone based on reverse pharmacophore-based screening technology[J]. Chin J Nat Med,2014,12(6):443-448. [2] CHEN L, ZHENG S Z, SUN Z G, et al. Cryptotanshinone has diverse effects on cell cycle events in melanoma cell lines with different metastatic capacity[J]. Cancer Chemother Pharmacol,2011,68(1):17-27. doi: 10.1007/s00280-010-1440-8 [3] PARK I J, YANG W K, NAM S H, et al. Cryptotanshinone induces G1 cell cycle arrest and autophagic cell death by activating the AMP-activated protein kinase signal pathway in HepG2 hepatoma[J]. Apoptosis,2014,19(4):615-628. doi: 10.1007/s10495-013-0929-0 [4] JI Y B, LIU Y C, XUE N N, et al. Cryptotanshinone inhibits esophageal squamous-cell carcinoma in vitro and in vivo through the suppression of STAT3 activation[J]. Onco Targets Ther,2019,12:883-896. doi: 10.2147/OTT.S187777 [5] WU Y H, WU Y R, LI B, et al. Cryptotanshinone: a review of its pharmacology activities and molecular mechanisms[J]. Fitoterapia,2020,145:104633. doi: 10.1016/j.fitote.2020.104633 [6] LI H Y, GAO C D, LIU C, et al. A review of the biological activity and pharmacology of cryptotanshinone, an important active constituent in Danshen[J]. Biomed Pharmacother,2021,137:111332. doi: 10.1016/j.biopha.2021.111332 [7] JIANG G Q, LIU J, REN B Y, et al. Anti-tumor and chemosensitization effects of Cryptotanshinone extracted from Salvia miltiorrhiza Bge. on ovarian cancer cells in vitro[J]. J Ethnopharmacol,2017,205:33-40. doi: 10.1016/j.jep.2017.04.026 [8] MAN Y H, YANG L, ZHANG D X, et al. Cryptotanshinone inhibits lung tumor growth by increasing CD4+ T cell cytotoxicity through activation of the JAK2/STAT4 pathway[J]. Oncol Lett,2016,12(5):4094-4098. doi: 10.3892/ol.2016.5123 [9] LIU S, HAN Z, TRIVETT A L, et al. Cryptotanshinone has curative dual anti-proliferative and immunotherapeutic effects on mouse Lewis lung carcinoma[J]. Cancer Immunol Immunother,2019,68(7):1059-1071. doi: 10.1007/s00262-019-02326-8 [10] HAN Z, LIU S, LIN H S, et al. Inhibition of murine hepatoma tumor growth by cryptotanshinone involves TLR7-dependent activation of macrophages and induction of adaptive antitumor immune defenses[J]. Cancer Immunol Immunother,2019,68(7):1073-1085. doi: 10.1007/s00262-019-02338-4 [11] DONG B W, LIANG Z R, CHEN Z R, et al. Cryptotanshinone suppresses key onco-proliferative and drug-resistant pathways of chronic myeloid leukemia by targeting STAT5 and STAT3 phosphorylation[J]. Sci China Life Sci,2018,61(9):999-1009. doi: 10.1007/s11427-018-9324-y [12] XIA C, BAI X P, HOU X Y, et al. Cryptotanshinone reverses cisplatin resistance of human lung carcinoma A549 cells through down-regulating Nrf2 pathway[J]. Cell Physiol Biochem,2015,37(2):816-824. doi: 10.1159/000430398 [13] HU T, TO K K, WANG L, et al. Reversal of P-glycoprotein (P-gp) mediated multidrug resistance in colon cancer cells by cryptotanshinone and dihydrotanshinone of Salvia miltior-rhiza[J]. Phytomedicine,2014,21(11):1264-1272. doi: 10.1016/j.phymed.2014.06.013 [14] WANG Y, LU H L, LIU Y D, et al. Cryptotanshinone sensitizes antitumor effect of paclitaxel on tongue squamous cell carcinoma growth by inhibiting the JAK/STAT3 signaling pathway[J]. Biomed Pharmacother,2017,95:1388-1396. doi: 10.1016/j.biopha.2017.09.062 [15] XU Z Y, JIANG H, ZHU Y H, et al. Cryptotanshinone induces ROS-dependent autophagy in multidrug-resistant colon cancer cells[J]. Chem Biol Interact,2017,273:48-55. doi: 10.1016/j.cbi.2017.06.003 [16] HAO W H, ZHANG X N, ZHAO W W, et al. Cryptotanshinone induces pro-death autophagy through JNK signaling mediated by reactive oxygen species generation in lung cancer cells[J]. Anticancer Agents Med Chem,2016,16(5):593-600. doi: 10.2174/1871520615666150907093036 [17] ZOU S L, TONG Q Y, LIU B W, et al. Targeting STAT3 in cancer immunotherapy[J]. Mol Cancer,2020,19(1):145. doi: 10.1186/s12943-020-01258-7 [18] SHIN D S, KIM H N, SHIN K D, et al. Cryptotanshinone inhibits constitutive signal transducer and activator of transcription 3 function through blocking the dimerization in DU145 prostate cancer cells[J]. Cancer Res,2009,69(1):193-202. doi: 10.1158/0008-5472.CAN-08-2575 [19] CHEN L D, LV D Y, CHEN X F, et al. Biosensor-based active ingredients recognition system for screening STAT3 ligands from medical herbs[J]. Anal Chem,2018,90(15):8936-8945. doi: 10.1021/acs.analchem.8b01103 [20] BLASIUS R, REUTER S, HENRY E, et al. Curcumin regulates signal transducer and activator of transcription (STAT) expression in K562 cells[J]. Biochem Pharmacol,2006,72(11):1547-1554. doi: 10.1016/j.bcp.2006.07.029 [21] GE Y Q, YANG B, CHEN Z, et al. Cryptotanshinone suppresses the proliferation and induces the apoptosis of pancreatic cancer cells via the STAT3 signaling pathway[J]. Mol Med Rep,2015,12(5):7782-7788. doi: 10.3892/mmr.2015.4379 [22] YANG Y F, CAO Y, CHEN L H, et al. Cryptotanshinone suppresses cell proliferation and glucose metabolism via STAT3/SIRT3 signaling pathway in ovarian cancer cells[J]. Cancer Med,2018,7(9):4610-4618. doi: 10.1002/cam4.1691 [23] YUAN X R, BU H, ZHOU J P, et al. Recent advances of SHP2 inhibitors in cancer therapy: current development and clinical application[J]. J Med Chem,2020,63(20):11368-11396. doi: 10.1021/acs.jmedchem.0c00249 [24] YU B, LIU W, YU W M, et al. Targeting protein tyrosine phosphatase SHP2 for the treatment of PTPN11-associated malignancies[J]. Mol Cancer Ther,2013,12(9):1738-1748. doi: 10.1158/1535-7163.MCT-13-0049-T [25] LIU W, YU B, XU G, et al. Identification of cryptotanshinone as an inhibitor of oncogenic protein tyrosine phosphatase SHP2 (PTPN11)[J]. J Med Chem,2013,56(18):7212-7221. doi: 10.1021/jm400474r [26] LU L, ZHANG S L, LI C X, et al. Cryptotanshinone inhibits human glioma cell proliferation in vitro and in vivo through SHP-2-dependent inhibition of STAT3 activation[J]. Cell Death Dis,2017,8(5):e2767. doi: 10.1038/cddis.2017.174 [27] HECK M M, EARNSHAW W C. Topoisomerase II: a specific marker for cell proliferation[J]. J Cell Biol,1986,103(6):2569-2581. doi: 10.1083/jcb.103.6.2569 [28] KIM E J, KIM S Y, KIM S M, et al. A novel topoisomerase 2a inhibitor, cryptotanshinone, suppresses the growth of PC3 cells without apparent cytotoxicity[J]. Toxicol Appl Pharmacol,2017,330:84-92. doi: 10.1016/j.taap.2017.07.007 [29] MOLONEY J N, COTTER T G. ROS signalling in the biology of cancer[J]. Semin Cell Dev Biol,2018,80:50-64. doi: 10.1016/j.semcdb.2017.05.023 [30] LIU C, SUN H N, LUO Y H, et al. Cryptotanshinone induces ROS-mediated apoptosis in human gastric cancer cells[J]. Oncotarget,2017,8(70):115398-115412. doi: 10.18632/oncotarget.23267 [31] YE T H, ZHU S R, ZHU Y X, et al. Cryptotanshinone induces melanoma cancer cells apoptosis via ROS-mitochondrial apoptotic pathway and impairs cell migration and invasion[J]. Biomed Pharmacother,2016,82:319-326. doi: 10.1016/j.biopha.2016.05.015 [32] CHEN W X, LIU L, LUO Y, et al. Cryptotanshinone activates p38/JNK and inhibits Erk1/2 leading to caspase-independent cell death in tumor cells[J]. Cancer Prev Res (Phila),2012,5(5):778-787. doi: 10.1158/1940-6207.CAPR-11-0551 [33] PARK I J, KIM M J, PARK O J, et al. Cryptotanshinone induces ER stress-mediated apoptosis in HepG2 and MCF7 cells[J]. Apoptosis,2012,17(3):248-257. doi: 10.1007/s10495-011-0680-3 [34] WU C Y, HSIEH C Y, HUANG K E, et al. Cryptotanshinone down-regulates androgen receptor signaling by modulating lysine-specific demethylase 1 function[J]. Int J Cancer,2012,131(6):1423-1434. doi: 10.1002/ijc.27343 [35] XU D F, LIN T H, LI S S, et al. Cryptotanshinone suppresses androgen receptor-mediated growth in androgen dependent and castration resistant prostate cancer cells[J]. Cancer Lett,2012,316(1):11-22. doi: 10.1016/j.canlet.2011.10.006 [36] PAN Y H, SHI J F, NI W T, et al. Cryptotanshinone inhibition of mammalian target of rapamycin pathway is dependent on oestrogen receptor alpha in breast cancer[J]. J Cell Mol Med,2017,21(9):2129-2139. doi: 10.1111/jcmm.13135 [37] LI S H, WANG H T, HONG L, et al. Cryptotanshinone inhibits breast cancer cell growth by suppressing estrogen receptor signaling[J]. Cancer Biol Ther,2015,16(1):176-184. doi: 10.4161/15384047.2014.962960 [38] KIM S A, KANG O H, KWON D Y. Cryptotanshinone induces cell cycle arrest and apoptosis of NSCLC cells through the PI3K/Akt/GSK-3β pathway[J]. Int J Mol Sci,2018,19(9):2739. doi: 10.3390/ijms19092739 [39] YE Y T, ZHONG W, SUN P, et al. Apoptosis induced by the methanol extract of Salvia miltiorrhiza Bunge in non-small cell lung cancer through PTEN-mediated inhibition of PI3K/Akt pathway[J]. J Ethnopharmacol,2017,200:107-116. doi: 10.1016/j.jep.2016.12.051 [40] ZHANG J T, WEN G L, SUN L H, et al. Cryptotanshinone inhibits cellular proliferation of human lung cancer cells through downregulation ofIGF-1R/PI3K/Akt signaling pathway[J]. Oncol Rep,2018,40(5):2926-2934. [41] ZHANG L, CHEN C, DUANMU J X, et a. Cryptotanshinone inhibits the growth and invasion of colon cancer by suppressing inflammation and tumor angiogenesis through modulating MMP/TIMP system, PI3K/Akt/mTOR signaling and HIF-1α nuclear translocation[J]. Int Immunopharmacol,2018,65:429-437. doi: 10.1016/j.intimp.2018.10.035 [42] KE F Y, WANG Z, SONG X L, et al. Cryptotanshinone induces cell cycle arrest and apoptosis through the JAK2/STAT3 and PI3K/Akt/NFκB pathways in cholangiocarcinoma cells[J]. Drug Des Devel Ther,2017,11:1753-1766. doi: 10.2147/DDDT.S132488 [43] ZHANG J, HUANG M, GUAN S, et al. A mechanistic study of the intestinal absorption of cryptotanshinone, the major active constituent of Salvia miltiorrhiza[J]. J Pharmacol Exp Ther,2006,317(3):1285-1294. doi: 10.1124/jpet.105.100701 [44] 刘航. 隐丹参酮衍生物的设计, 合成及其对STAT3转录活性的影响[D]. 福州: 福建中医药大学, 2021. [45] WANG H, LIU Z, GUAN L N, et al. LYW-6, a novel cryptotanshinone derived STAT3 targeting inhibitor, suppres-ses colorectal cancer growth and metastasis[J]. Pharmacol Res,2020,153:104661. doi: 10.1016/j.phrs.2020.104661 [46] XU D F, LIN T H, ZHANG C X, et al. The selective inhibitory effect of a synthetic tanshinone derivative on prostate cancer cells[J]. Prostate,2012,72(7):803-816. doi: 10.1002/pros.21474 -

 点击查看大图
点击查看大图
计量
- 文章访问数: 5447
- HTML全文浏览量: 3201
- PDF下载量: 29
- 被引次数: 0




 下载:
下载:

 下载:
下载:
