-
盐酸阿霉素是一种基于蒽环类的广谱抗肿瘤药物,能够通过多种机制达到抗肿瘤活性。他能与S期DNA相互作用,抑制核酸合成。此外,作为DNA拓扑异构酶Ⅱ抑制剂,盐酸阿霉素可引起DNA链的断裂[1-5];但由于盐酸阿霉素严重的心脏毒性和肿瘤细胞耐药性阻碍了其在临床实践中的广泛应用。小分子化疗增敏剂能够改善肿瘤的多药耐药,提高化疗药物的疗效。氯尼达明在调节热疗、放射疗法、光动力疗法的活性方面具有潜力[6-7]。氯尼达明作为己糖激酶Ⅱ(HK-Ⅱ)抑制剂,能够抑制肿瘤细胞有氧糖酵解、减少肿瘤细胞的能量供应[8-9]。此外,氯尼达明可以通过破坏跨膜电位而有效地触发线粒体凋亡途径。但它作为单一药物,其抗肿瘤活性有限[10],因此经常与其他抗肿瘤药物联合用作化学增敏剂。有研究报道指出,氯尼达明与盐酸阿霉素的共递送,在体外能够显著增强细胞毒性并降低抗肿瘤药物的给药剂量[11-14],二者在协同治疗肝癌、卵巢癌、乳腺癌等领域已取得显著进展。通过大量的文献调研,我们发现氯尼达明与盐酸阿霉素的最佳协同比例为1∶6,但并未有人专门构建氯尼达明与盐酸阿霉素混合溶液的含量分析方法[13]。因此,本研究采用HPLC法建立针对氯尼达明与盐酸阿霉素联合用药的含量分析测定方法,为二者联合用药的含量检测提供参考。
-
Agilent-1260 Infinity Ⅱ高效液相色谱仪、紫外可见分光光度计[安捷伦科技(中国)有限公司];SECURA125-1CN型十万分之一电子天平、Arium@mini超纯水机(德国赛多利斯)。
-
盐酸阿霉素对照品(99%)、甲醇(色谱纯)、三氟乙酸(TFA,色谱纯)均购自sigma-Aldrich Company;氯尼达明对照品(99%,上海毕得医药科技有限公司);纯净水(杭州娃哈哈集团有限公司)。
-
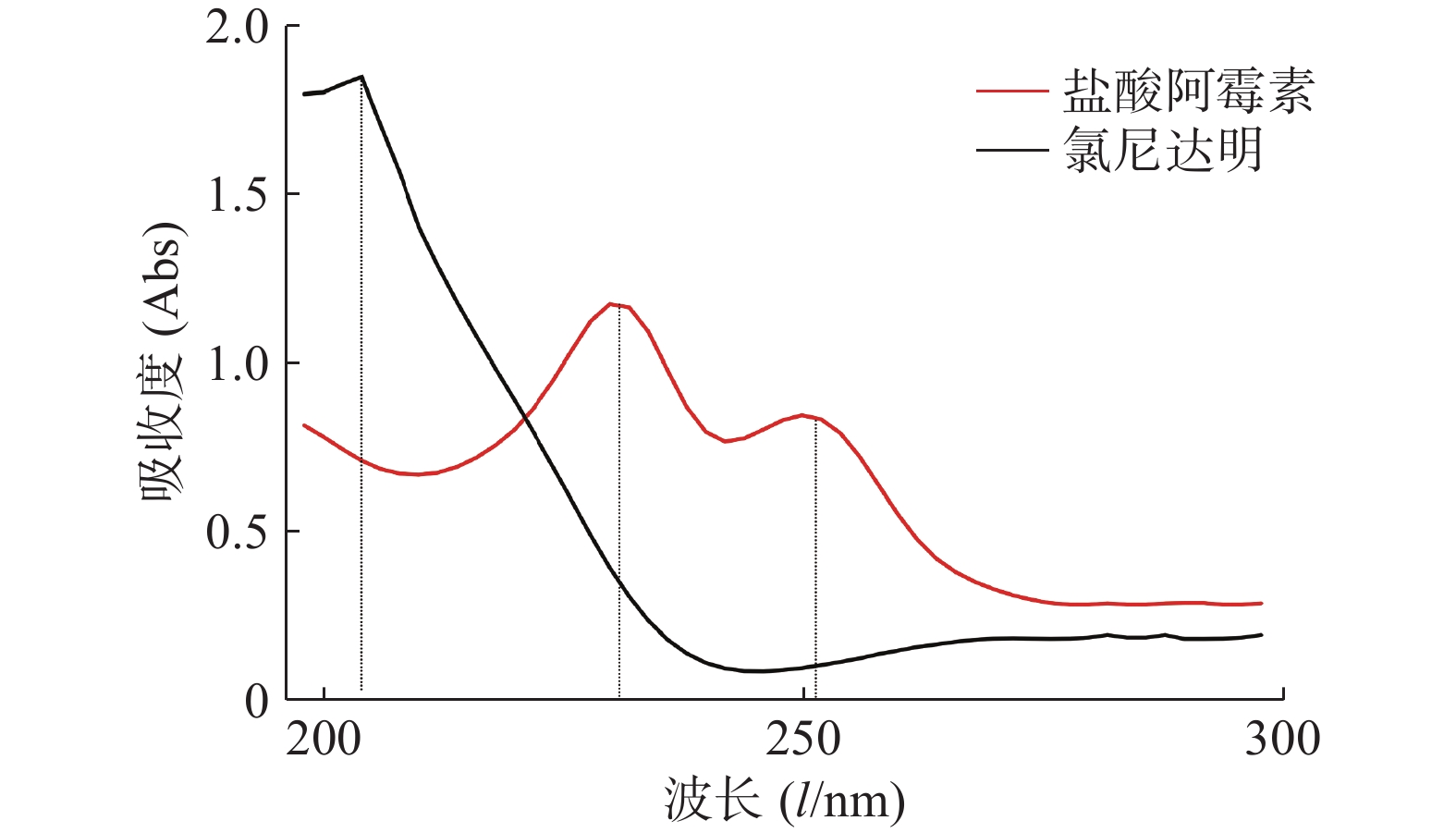
精密称取氯尼达明和盐酸阿霉素对照品适量,分别用甲醇水溶液(50%)溶解制成20 µg/ml的对照品溶液,在190~400 nm波长内进行扫描,盐酸阿霉素的最大吸收波长为228、253 nm,氯尼达明的最大吸收波长为205 nm。故分别选择253、205 nm作为检测波长,见图1。
-
色谱柱:Agilent 5 HC-C18(2)(4.6 mm×250 mm,5 µm);流动相:甲醇(A)-0.1% TFA水溶液(B);检测波长:205、253 nm;流速: 1.0 ml/min;柱温:35℃;进样量:10 µl;梯度洗脱程序如表1所示。
表 1 梯度洗脱程序
时间(t/ min) 流动相A(%) 流动相B(%) 0 65 35 3 65 35 7 90 10 13 90 10 15 65 35 20 65 35 -
精密称取12 mg 氯尼达明加入50%甲醇水溶液,涡旋震荡并超声溶解后定容至10 ml量瓶中,即得1.2 mg/ml氯尼达明溶液;精密称取10 mg盐酸阿霉素加入50%甲醇水溶液,涡旋震荡溶解后定容至50 ml量瓶中,即得0.2 mg/ml盐酸阿霉素溶液。
-
将“2.3.1”项中的溶液等体积混合后,量取一定体积的50%甲醇水溶液稀释2.5倍,定容于10 ml容量瓶中,即得氯尼达明与盐酸阿霉素质量浓度分别为240 µg/ml和40 µg/ml的混合溶液。
-
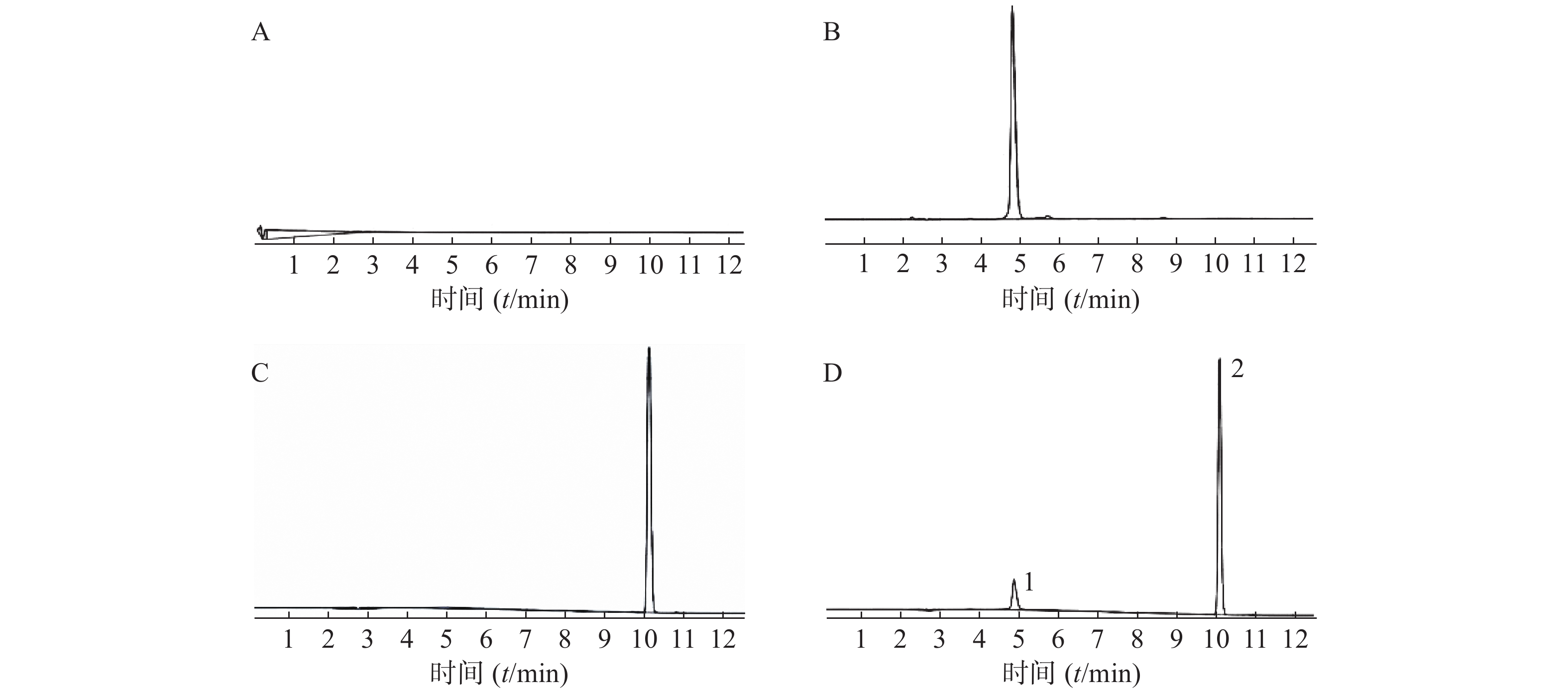
按照“2.3.1”项及“2.3.2”项条件,配制以下样品。按照“2.2”项下方法进样检测,考察方法的专属性。如图2所示,实验结果表明,该方法专属性良好,氯尼达明与盐酸阿霉素的色谱峰完全分离。
-
精密量取不同体积“2.3.2”项下制备的混合对照品溶液,置于5 ml量瓶中,加溶剂稀释并定容,最终得到质量浓度为240、180、120、60、30、12、6 µg/ml的氯尼达明溶液,此条件下,盐酸阿霉素的质量浓度分别为40、30、20、10、5、2、1 µg/ml。
按上述“2.2”项下色谱条件进样,以对照品的峰面积(Y)对质量浓度(X)进行线性回归,得氯尼达明回归方程: Y=51.439X+111.46,r=0.9999,证明在本方法下,氯尼达明在6~240 µg/ml 浓度范围内线性良好。得盐酸阿霉素回归方程:Y= 25.142X + 2.1863,r=0.9999,证明在本方法下,盐酸阿霉素在1~40 µg/ml浓度范围内线性良好。
-
取氯尼达明质量浓度为30、60、240 µg/ml的混合对照品溶液,按照“2.2”项下的色谱条件进行日内精密度及日间精密度考察。日内精密度测定方法为样品测定5次,计算日内相对偏差;日间精密度测定方法为样品连续测定5 d,计算日间相对偏差。如表2、表3所示,3种不同浓度的氯尼达明和盐酸阿霉素的日内、日间精密度的RSD值均小于2.0 %,符合精密度要求。
表 2 盐酸阿霉素精密度试验(n=5)
浓度(ρB/µg·ml−1) 日内RSD(%) 日间RSD(%) 5 1.40 1.48 10 0.38 0.92 40 0.11 0.06 表 3 氯尼达明精密度试验(n=5)
浓度(ρB/µg·ml−1) 日内RSD(%) 日间RSD(%) 30 0.03 0.19 60 0.13 0.06 240 0.11 0.07 -
根据上述方法配制质量浓度分别为60、10 µg/ml 的氯尼达明、盐酸阿霉素混合溶液,分别在第0、2、4、8、12、24 h时进样,按照“2.2”项下色谱条件,进行含量测定,结果如表4、表5所示,表明氯尼达明与盐酸阿霉素的混合溶液在8 h内稳定。
表 4 氯尼达明在不同时间下的稳定性考察
时间(t/h) RSD(%) 0 0.20 2 0.07 4 0.05 8 0.13 12 0.12 24 0.02 表 5 盐酸阿霉素在不同时间下的稳定性考察
时间(t/h) RSD(%) 0 0.32 2 0.38 4 0.14 8 0.49 12 0.62 24 0.58 -
精密称取6份12 mg 氯尼达明和10 mg 盐酸阿霉素,加入50%甲醇水溶液,分别定容于10 ml和50 ml容量瓶中,即得1.2 mg/ml 氯尼达明溶液和0.2 mg/ml 盐酸阿霉素溶液。
将上述溶液等体积混合后,量取一定体积的50%甲醇水溶液稀释2.5倍,定容于10 ml容量瓶后,即得6份氯尼达明与盐酸阿霉素质量浓度分别为240 µg/ml和40 µg/ml的混合溶液,按“2.2”项下色谱条件进行测定,带入回归方程计算氯尼达明和盐酸阿霉素的含量、回收率和RSD值。结果如表6所示。说明此方法回收率符合要求。
表 6 回收率实验结果(n=6)
成分 原有量
(m/mg)测得量
(m/mg)回收率
(%)平均回收率
(%)RSD
(%)氯尼达明 12.0 11.8 98.3 99.2 2.9 12.1 11.9 98.3 11.9 11.8 99.2 12.4 12.8 98.4 11.8 11.8 100.0 12.1 12.8 105.8 盐酸阿霉素 10.1 9.8 97.0 100.8 1.9 10.1 9.8 97.0 10.0 9.8 98.0 9.9 10.0 101.0 10.1 10.0 99.0 10.1 10.2 101.0 -
氯尼达明极性小,有机相比例的改变对其出峰时间影响较大。对于流动相的选择,本实验曾尝试以乙腈(0.1% TFA)-水(0.1%TFA)、乙腈:水(0.1% 三乙胺,磷酸调pH=3.0)、乙腈:水(0.1%甲酸)作为流动相[15-17],但氯尼达明出峰时间过长且峰对称性差。以甲醇-水(0.1% TFA)作为流动相时,分离效果及峰形较好[18],故分别考察了甲醇与水分别为90∶10、80∶20、70∶30、65∶35等比例下两种化合物的保留时间。结果表明,有机相甲醇比例低于70% 时,氯尼达明出峰时间过长。在溶剂的选择上,本实验尝试以甲醇、甲醇水溶液作为溶剂,当溶剂为甲醇水溶液时,盐酸阿霉素及氯尼达明两组不存在前沿及拖尾现象,且基线较平稳,分离度较好。故在此基础上,为缩短氯尼达明的出峰时间,我们尝试在4~15 min内改变有机相比例,利用梯度洗脱以保证两种化合物出峰完整且保留时间适中。本实验结果表明,选用该梯度洗脱方法同时测定氯尼达明和盐酸阿霉素,在一定浓度范围内线性良好,专属性高,且精密度、回收率、稳定性均符合方法学要求,可以作为同时测定氯尼达明和盐酸阿霉素含量的测定方法。
Content measurement of doxorubicin hydrochloride and lonidamine by HPLC
-
摘要:
目的 建立同时测定盐酸阿霉素(DOX·HCl)与氯尼达明(LND)含量的测定方法。 方法 采用HPLC法,色谱柱为Agilent 5 HC-C18(2)(4.6 mm×250 mm ,5 µm),流动相为甲醇-0.1%TFA水溶液,梯度洗脱,甲醇比例随时间变化为:0~3 min, 65%甲醇;3~7 min, 65%→90%甲醇;7~13 min,90%甲醇;13~15 min,90%→65%甲醇;15~20 min、65%甲醇。采集时间20 min,平衡时间3 min,紫外检测波长205 nm及253 nm,流速1.0 ml/min,柱温35 ℃,进样量:10 µl。 结果 该方法专属性好,盐酸阿霉素在1~40 µg/ml 的浓度范围内线性良好,氯尼达明在6~240 µg/ml的浓度范围内线性良好。该方法之下,两种化合物的精密度、稳定性、回收率均符合要求。 结论 建立了同时检测盐酸阿霉素与氯尼达明含量的液相分析方法,该方法专属性强,准确可靠。 Abstract:Objective To establish a method for the simultaneous determination of DOX·HCl and LND. Methods HPLC was performed on Agilent 5 HC-C18(2) (4.6 mm × 250 mm, 5 µm) column. The mobile phase was methanol-0.1% TFA aqueous solution, and the gradient elution procedure were: 0 to 3 min, 65% methanol; 3 to 7 min, 65%→90% methanol; 7 to 13 min, 90% methanol; 13 to 15 min, 90%→65% methanol; 15 to 20 min, 65% methanol. The collection time was 20 min, the balance time was 3 min, the UV detection wavelengths were 205 nm and 253 nm. The flow rate was 1.0 ml/min and the column temperature was 35℃. The amount of inlet was 10 µl. Results The method was highly specific, and both DOX·HCl and LND exhibited good linearity in the concentration range of 1-40 µg/ml and 6-240 µg/ml, respectively. The two compounds’ precision, stability, and recovery satisfied the requirements of the method. Conclusion This study established a HPLC method that was suitable for the simultaneous detection of DOX·HCl and LND. This method’s high level of specificity, accuracy, and reliability . -
Key words:
- lonidamine /
- doxorubicin hydrochloride /
- HPLC /
- drug combination /
- gradient elution
-
盐酸阿霉素是一种基于蒽环类的广谱抗肿瘤药物,能够通过多种机制达到抗肿瘤活性。他能与S期DNA相互作用,抑制核酸合成。此外,作为DNA拓扑异构酶Ⅱ抑制剂,盐酸阿霉素可引起DNA链的断裂[1-5];但由于盐酸阿霉素严重的心脏毒性和肿瘤细胞耐药性阻碍了其在临床实践中的广泛应用。小分子化疗增敏剂能够改善肿瘤的多药耐药,提高化疗药物的疗效。氯尼达明在调节热疗、放射疗法、光动力疗法的活性方面具有潜力[6-7]。氯尼达明作为己糖激酶Ⅱ(HK-Ⅱ)抑制剂,能够抑制肿瘤细胞有氧糖酵解、减少肿瘤细胞的能量供应[8-9]。此外,氯尼达明可以通过破坏跨膜电位而有效地触发线粒体凋亡途径。但它作为单一药物,其抗肿瘤活性有限[10],因此经常与其他抗肿瘤药物联合用作化学增敏剂。有研究报道指出,氯尼达明与盐酸阿霉素的共递送,在体外能够显著增强细胞毒性并降低抗肿瘤药物的给药剂量[11-14],二者在协同治疗肝癌、卵巢癌、乳腺癌等领域已取得显著进展。通过大量的文献调研,我们发现氯尼达明与盐酸阿霉素的最佳协同比例为1∶6,但并未有人专门构建氯尼达明与盐酸阿霉素混合溶液的含量分析方法[13]。因此,本研究采用HPLC法建立针对氯尼达明与盐酸阿霉素联合用药的含量分析测定方法,为二者联合用药的含量检测提供参考。
1. 仪器与试药
1.1 仪器
Agilent-1260 Infinity Ⅱ高效液相色谱仪、紫外可见分光光度计[安捷伦科技(中国)有限公司];SECURA125-1CN型十万分之一电子天平、Arium@mini超纯水机(德国赛多利斯)。
1.2 药品与试剂
盐酸阿霉素对照品(99%)、甲醇(色谱纯)、三氟乙酸(TFA,色谱纯)均购自sigma-Aldrich Company;氯尼达明对照品(99%,上海毕得医药科技有限公司);纯净水(杭州娃哈哈集团有限公司)。
2. 方法与结果
2.1 波长的选择
精密称取氯尼达明和盐酸阿霉素对照品适量,分别用甲醇水溶液(50%)溶解制成20 µg/ml的对照品溶液,在190~400 nm波长内进行扫描,盐酸阿霉素的最大吸收波长为228、253 nm,氯尼达明的最大吸收波长为205 nm。故分别选择253、205 nm作为检测波长,见图1。
2.2 色谱条件
色谱柱:Agilent 5 HC-C18(2)(4.6 mm×250 mm,5 µm);流动相:甲醇(A)-0.1% TFA水溶液(B);检测波长:205、253 nm;流速: 1.0 ml/min;柱温:35℃;进样量:10 µl;梯度洗脱程序如表1所示。
表 1 梯度洗脱程序时间(t/ min) 流动相A(%) 流动相B(%) 0 65 35 3 65 35 7 90 10 13 90 10 15 65 35 20 65 35 2.3 溶液的制备
2.3.1 对照品储备液的制备
精密称取12 mg 氯尼达明加入50%甲醇水溶液,涡旋震荡并超声溶解后定容至10 ml量瓶中,即得1.2 mg/ml氯尼达明溶液;精密称取10 mg盐酸阿霉素加入50%甲醇水溶液,涡旋震荡溶解后定容至50 ml量瓶中,即得0.2 mg/ml盐酸阿霉素溶液。
2.3.2 混合对照品溶液的制备
将“2.3.1”项中的溶液等体积混合后,量取一定体积的50%甲醇水溶液稀释2.5倍,定容于10 ml容量瓶中,即得氯尼达明与盐酸阿霉素质量浓度分别为240 µg/ml和40 µg/ml的混合溶液。
2.4 系统适用性考察
按照“2.3.1”项及“2.3.2”项条件,配制以下样品。按照“2.2”项下方法进样检测,考察方法的专属性。如图2所示,实验结果表明,该方法专属性良好,氯尼达明与盐酸阿霉素的色谱峰完全分离。
2.5 线性关系考察
精密量取不同体积“2.3.2”项下制备的混合对照品溶液,置于5 ml量瓶中,加溶剂稀释并定容,最终得到质量浓度为240、180、120、60、30、12、6 µg/ml的氯尼达明溶液,此条件下,盐酸阿霉素的质量浓度分别为40、30、20、10、5、2、1 µg/ml。
按上述“2.2”项下色谱条件进样,以对照品的峰面积(Y)对质量浓度(X)进行线性回归,得氯尼达明回归方程: Y=51.439X+111.46,r=0.9999,证明在本方法下,氯尼达明在6~240 µg/ml 浓度范围内线性良好。得盐酸阿霉素回归方程:Y= 25.142X + 2.1863,r=0.9999,证明在本方法下,盐酸阿霉素在1~40 µg/ml浓度范围内线性良好。
2.6 精密度试验
取氯尼达明质量浓度为30、60、240 µg/ml的混合对照品溶液,按照“2.2”项下的色谱条件进行日内精密度及日间精密度考察。日内精密度测定方法为样品测定5次,计算日内相对偏差;日间精密度测定方法为样品连续测定5 d,计算日间相对偏差。如表2、表3所示,3种不同浓度的氯尼达明和盐酸阿霉素的日内、日间精密度的RSD值均小于2.0 %,符合精密度要求。
表 2 盐酸阿霉素精密度试验(n=5)浓度(ρB/µg·ml−1) 日内RSD(%) 日间RSD(%) 5 1.40 1.48 10 0.38 0.92 40 0.11 0.06 表 3 氯尼达明精密度试验(n=5)浓度(ρB/µg·ml−1) 日内RSD(%) 日间RSD(%) 30 0.03 0.19 60 0.13 0.06 240 0.11 0.07 2.7 稳定性试验
根据上述方法配制质量浓度分别为60、10 µg/ml 的氯尼达明、盐酸阿霉素混合溶液,分别在第0、2、4、8、12、24 h时进样,按照“2.2”项下色谱条件,进行含量测定,结果如表4、表5所示,表明氯尼达明与盐酸阿霉素的混合溶液在8 h内稳定。
表 4 氯尼达明在不同时间下的稳定性考察时间(t/h) RSD(%) 0 0.20 2 0.07 4 0.05 8 0.13 12 0.12 24 0.02 表 5 盐酸阿霉素在不同时间下的稳定性考察时间(t/h) RSD(%) 0 0.32 2 0.38 4 0.14 8 0.49 12 0.62 24 0.58 2.8 回收率试验
精密称取6份12 mg 氯尼达明和10 mg 盐酸阿霉素,加入50%甲醇水溶液,分别定容于10 ml和50 ml容量瓶中,即得1.2 mg/ml 氯尼达明溶液和0.2 mg/ml 盐酸阿霉素溶液。
将上述溶液等体积混合后,量取一定体积的50%甲醇水溶液稀释2.5倍,定容于10 ml容量瓶后,即得6份氯尼达明与盐酸阿霉素质量浓度分别为240 µg/ml和40 µg/ml的混合溶液,按“2.2”项下色谱条件进行测定,带入回归方程计算氯尼达明和盐酸阿霉素的含量、回收率和RSD值。结果如表6所示。说明此方法回收率符合要求。
表 6 回收率实验结果(n=6)成分 原有量
(m/mg)测得量
(m/mg)回收率
(%)平均回收率
(%)RSD
(%)氯尼达明 12.0 11.8 98.3 99.2 2.9 12.1 11.9 98.3 11.9 11.8 99.2 12.4 12.8 98.4 11.8 11.8 100.0 12.1 12.8 105.8 盐酸阿霉素 10.1 9.8 97.0 100.8 1.9 10.1 9.8 97.0 10.0 9.8 98.0 9.9 10.0 101.0 10.1 10.0 99.0 10.1 10.2 101.0 3. 讨论
氯尼达明极性小,有机相比例的改变对其出峰时间影响较大。对于流动相的选择,本实验曾尝试以乙腈(0.1% TFA)-水(0.1%TFA)、乙腈:水(0.1% 三乙胺,磷酸调pH=3.0)、乙腈:水(0.1%甲酸)作为流动相[15-17],但氯尼达明出峰时间过长且峰对称性差。以甲醇-水(0.1% TFA)作为流动相时,分离效果及峰形较好[18],故分别考察了甲醇与水分别为90∶10、80∶20、70∶30、65∶35等比例下两种化合物的保留时间。结果表明,有机相甲醇比例低于70% 时,氯尼达明出峰时间过长。在溶剂的选择上,本实验尝试以甲醇、甲醇水溶液作为溶剂,当溶剂为甲醇水溶液时,盐酸阿霉素及氯尼达明两组不存在前沿及拖尾现象,且基线较平稳,分离度较好。故在此基础上,为缩短氯尼达明的出峰时间,我们尝试在4~15 min内改变有机相比例,利用梯度洗脱以保证两种化合物出峰完整且保留时间适中。本实验结果表明,选用该梯度洗脱方法同时测定氯尼达明和盐酸阿霉素,在一定浓度范围内线性良好,专属性高,且精密度、回收率、稳定性均符合方法学要求,可以作为同时测定氯尼达明和盐酸阿霉素含量的测定方法。
-
表 1 梯度洗脱程序
时间(t/ min) 流动相A(%) 流动相B(%) 0 65 35 3 65 35 7 90 10 13 90 10 15 65 35 20 65 35 表 2 盐酸阿霉素精密度试验(n=5)
浓度(ρB/µg·ml−1) 日内RSD(%) 日间RSD(%) 5 1.40 1.48 10 0.38 0.92 40 0.11 0.06 表 3 氯尼达明精密度试验(n=5)
浓度(ρB/µg·ml−1) 日内RSD(%) 日间RSD(%) 30 0.03 0.19 60 0.13 0.06 240 0.11 0.07 表 4 氯尼达明在不同时间下的稳定性考察
时间(t/h) RSD(%) 0 0.20 2 0.07 4 0.05 8 0.13 12 0.12 24 0.02 表 5 盐酸阿霉素在不同时间下的稳定性考察
时间(t/h) RSD(%) 0 0.32 2 0.38 4 0.14 8 0.49 12 0.62 24 0.58 表 6 回收率实验结果(n=6)
成分 原有量
(m/mg)测得量
(m/mg)回收率
(%)平均回收率
(%)RSD
(%)氯尼达明 12.0 11.8 98.3 99.2 2.9 12.1 11.9 98.3 11.9 11.8 99.2 12.4 12.8 98.4 11.8 11.8 100.0 12.1 12.8 105.8 盐酸阿霉素 10.1 9.8 97.0 100.8 1.9 10.1 9.8 97.0 10.0 9.8 98.0 9.9 10.0 101.0 10.1 10.0 99.0 10.1 10.2 101.0 -
[1] LU J Q, LI R, MU B S, et al. Multiple targeted doxorubicin-lonidamine liposomes modified with p-hydroxybenzoic acid and triphenylphosphonium to synergistically treat glioma[J]. Eur J Med Chem, 2022, 230:114093. doi: 10.1016/j.ejmech.2021.114093 [2] SCHIRONE L, D’AMBROSIO L, FORTE M, et al. Mitochondria and doxorubicin-induced cardiomyopathy: a complex interplay[J]. Cells, 2022, 11(13):2000. doi: 10.3390/cells11132000 [3] KITAKATA H, ENDO J, IKURA H, et al. Therapeutic targets for DOX-induced cardiomyopathy: role of apoptosis vs. ferroptosis[J]. Int J Mol Sci, 2022, 23(3):1414. doi: 10.3390/ijms23031414 [4] WANG J, TANG W, YANG M, et al. Inflammatory tumor microenvironment responsive neutrophil exosomes-based drug delivery system for targeted glioma therapy[J]. Biomaterials, 2021, 273:120784. doi: 10.1016/j.biomaterials.2021.120784 [5] TIAN W, XIE X J, CAO P L. Magnoflorine improves sensitivity to doxorubicin (DOX) of breast cancer cells via inducing apoptosis and autophagy through AKT/mTOR and p38 signaling pathways[J]. Biomed Pharmacother, 2020, 121:109139. doi: 10.1016/j.biopha.2019.109139 [6] HUANG Y X, SUN G H, SUN X D, et al. The potential of lonidamine in combination with chemotherapy and physical therapy in cancer treatment[J]. Cancers, 2020, 12(11):3332. doi: 10.3390/cancers12113332 [7] SHUTKOV I A, OKULOVA Y N, TYURIN V Y, et al. Ru(Ⅲ) complexes with lonidamine-modified ligands[J]. Int J Mol Sci, 2021, 22(24):13468. doi: 10.3390/ijms222413468 [8] CHENG G, ZHANG Q, PAN J, et al. Targeting lonidamine to mitochondria mitigates lung tumorigenesis and brain metastasis[J]. Nat Commun, 2019, 10(1):2205. doi: 10.1038/s41467-019-10042-1 [9] NATH K, GUO L L, NANCOLAS B, et al. Mechanism of antineoplastic activity of lonidamine[J]. Biochim Biophys Acta BBA Rev Cancer, 2016, 1866(2):151-162. doi: 10.1016/j.bbcan.2016.08.001 [10] COHEN-EREZ I, ISSACSON C, LAVI Y, et al. Antitumor effect of lonidamine-polypeptide-peptide nanoparticles in breast cancer models[J]. ACS Appl Mater Interfaces, 2019, 11(36):32670-32678. doi: 10.1021/acsami.9b09886 [11] PENG Y, LU J Q, LI R, et al. Glucose and triphenylphosphonium co-modified redox-sensitive liposomes to synergistically treat glioma with doxorubicin and lonidamine[J]. ACS Appl Mater Interfaces, 2021, 13(23):26682-26693. doi: 10.1021/acsami.1c02404 [12] ZHAO Y, PENG Y, YANG Z Z, et al. pH-redox responsive cascade-targeted liposomes to intelligently deliver doxorubicin prodrugs and lonidamine for glioma[J]. Eur J Med Chem, 2022, 235:114281. doi: 10.1016/j.ejmech.2022.114281 [13] LI H Z, XU W, LI F, et al. Amplification of anticancer efficacy by co-delivery of doxorubicin and lonidamine with extracellular vesicles[J]. Drug Deliv, 2022, 29(1):192-202. doi: 10.1080/10717544.2021.2023697 [14] LIU Y Q, ZHANG X J, ZHOU M J, et al. Mitochondrial-targeting lonidamine-doxorubicin nanoparticles for synergistic chemotherapy to conquer drug resistance[J]. ACS Appl Mater Interfaces, 2017, 9(50):43498-43507. doi: 10.1021/acsami.7b14577 [15] GRIPPA E, GATTO M T, LEONE M G, et al. Analysis of lonidamine in rat serum and testis by high performance liquid chromatography[J]. Biomed Chromatogr, 2001, 15(1):1-8. doi: 10.1002/bmc.14 [16] 杨学礼, 张红蕾, 杨瑜涛, 等. HPLC法测定DNA纳米运输系统载药阿霉素的含量[J]. 药物分析杂志, 2019, 39(7):1239-1243. doi: 10.16155/j.0254-1793.2019.07.10 [17] 朱站站, 王绍仙, 王亚伦, 等. 载阿霉素PEG-PLGA纳米粒的制备及优化[J]. 广州化工, 2022, 50(7):85-87. doi: 10.3969/j.issn.1001-9677.2022.07.026 [18] 陈希, 黄佳, 葛雨欣, 等. 甲醇-水为流动相的HPLC法检测抗肿瘤药物盐酸阿霉素[J]. 嘉兴学院学报, 2021, 33(6):90-93. doi: 10.3969/j.issn.1671-3079.2021.06.016 -





 下载:
下载:
 下载:
下载:


