-
万古霉素是广泛应用于临床的三环糖肽类抗生素,临床上主要用于耐甲氧西林金黄色葡萄球菌所致感染,也常用于腹膜透析相关性腹膜炎覆盖G+菌的经验性治疗。最常见的药物不良反应(ADR)是过敏反应、肝肾毒性、耳毒性和血液系统ADR[1],近年来,万古霉素致中性粒细胞减少、血小板减少的文献报道不断增多[2-4],但其致全血细胞减少的个案报道仅4篇[5-8]。笔者对临床工作中发现的1例万古霉素引起腹膜透析患者全血细胞减少的病例进行分析,以期引起临床工作人员对这一不良反应的关注,提高对万古霉素用药安全性的警惕。
-
患者,男,78岁,体重65 kg,维持性腹透5年余,因腹痛、腹泻3 d,腹透液浑浊,现为腹膜评估收住入院。入院诊断:腹膜透析相关性腹膜炎、慢性肾脏病5期、维持性腹膜透析。目前腹透方案:连续不卧床腹膜透析(continuous ambulatory peritoneal dialysis,CAPD),具体为15%低钙腹膜透析液(PD4)2 L×3袋+25% PD4×2袋,夜间留腹,每天超滤400~500 ml。2019年11月19日,入院查体:T38.8 ℃,血压100/58 mmHg,神清,精神可,HR 78次/min;血常规:白细胞7.8×109/L,红细胞3.05×1012/L,血红蛋白93 g/L,血小板计数134×109/L,C反应蛋白(CRP)75.72 mg/L,降钙素原(PCT)3.05 ng/ml;血清肌酐(SCr)612 μmol/L;腹水常规:腹透液淡黄、混浊;李凡他试验:阳性;细胞总数:3 420×106/L,有核细胞计数:1 715×106/L;嗜中性分叶核细胞98%,腹透相关性腹膜炎诊断明确。根据腹膜炎治疗经验,暂给予注射用盐酸万古霉素1 g加入腹透液中(留腹大于6 h),q3d;注射用头孢他啶1 g qd,加夜间腹透液;注射用美罗培南1 g+氯化钠注射液100 ml qd,静脉滴注抗感染治疗,患者住院期间使用的主要治疗药物详见表1,待腹透液细菌培养结果和药敏结果回报后进一步调整抗菌药物。考虑患者本身肾功能不全,以及万古霉素安全范围窄且不良反应大,临床药师建议用药过程中进行万古霉素的血药浓度监测,密切关注ADR,定期复查血常规及肝、肾功能。
表 1 患者住院期间的主要治疗药物
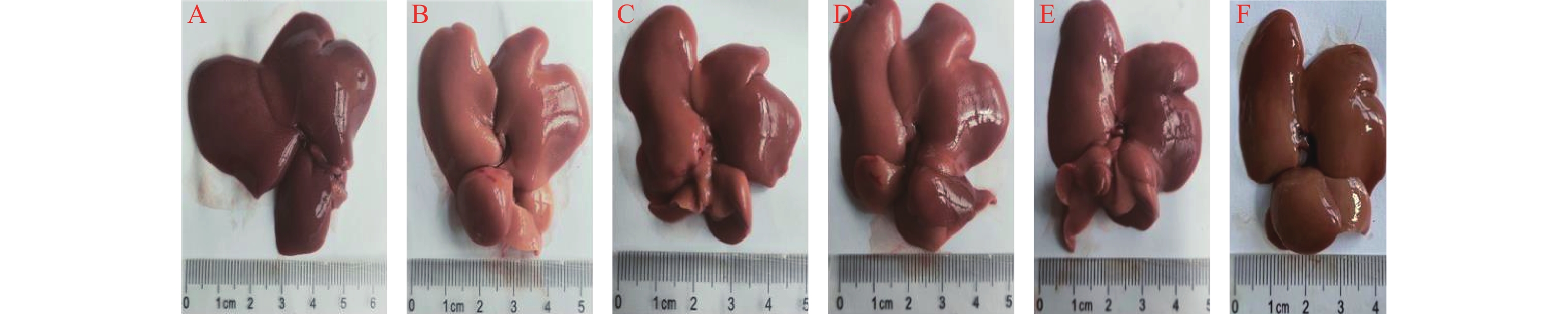
开始用药 药品名称及用法用量 停止用药 2019-11-19 注射用盐酸万古霉素1 g,留腹时间>6 h 注射用头孢他啶1 g qd,加夜间腹透液 2019-11-23 注射用美罗培南1 g+氯化钠注射液100 ml qd 静脉滴注 2019-11-23 2019-11-22 注射用盐酸万古霉素1 g加入头孢他啶留腹的腹透液中 2019-11-25 注射用盐酸万古霉素1 g加入腹透液中 重组人促红素注射液5000 U,皮下注射 2019-11-28 注射用盐酸万古霉素1 g加入腹透液中 2019-12-03 注射用盐酸万古霉素1 g加入腹透液中 11月23日,患者腹痛、腹泻症状较前明显好转,无发热,腹软,上腹轻压痛,无反跳痛,腹透液细菌培养:非解乳链球菌,药敏结果示:万古霉素敏感,故予停用美罗培南、头孢他啶,继续万古霉素1 g q3d,腹膜透析用抗感染治疗。患者全血细胞减少(图1),临床药师分析认为因感染所致或抗菌药物不良反应,目前已停用美罗培南、头孢他啶,根据病情仍需使用万古霉素,密切关注患者血常规变化。
11月25日,患者无明显腹痛、腹泻症状,感染症状明显好转,继续使用万古霉素抗感染治疗,足疗程2周治疗。患者血红蛋白73 g/L,目前仍有贫血,给予重组人促红素注射液5 000 U,皮下注射纠正贫血。11月28日,患者无腹痛、腹泻,腹软,无压痛,无反跳痛,腹透液正常,凝血功能:凝血酶原时间(PT)12.6 s,部分活化凝血酶原时间(APTT)26.6 s,国际标准比率(INR)1.07,血小板66×109/L,血小板进行性下降。据文献报道万古霉素可致血小板减少[4],临床药师分析可能为万古霉素引起的不良反应,仔细询问并对患者进行查体,患者无牙龈出血、咯血、呕血、黑便,全身未见瘀点、瘀斑等出血倾向,感染仍为其主要矛盾,临床药师告知患者:若出现出血现象,及时告知医生和护士,密切复查血常规,若血小板低于30×109/L,可给予重组人白介素-11或重组人血小板生成素注射液,必要时给予输注血小板。
11月30日,患者腹透液澄清透明、无腹泻、无发热等症状,精神状态良好。腹透液检查结果详见表2,测得万古霉素血药浓度:15.4 μg/ml,继续维持万古霉素腹腔灌注治疗。患者本身肾功能不全,加之万古霉素的肾毒性,监测其肾功能是首要任务之一,肾功能主要指标详见表3;观察血细胞是否还是处于持续下降状态(图1)。12月4日,患者腹透液澄清透明、中性细胞数正常,无腹泻、无发热等症状,精神状态良好,病情稳定,予以出院,嘱患者1周后复查血常规。12月12日,复查血常规:白细胞7.4×109/L,红细胞3.47×1012/L,血红蛋白108 g/L,血小板114×109/L,基本恢复正常。
表 2 腹透液主要指标检查结果
日期 腹透液透明度 李凡他试验 细胞总数(×106/L) 有核细胞计数(×106/L) 2019-11-19 浑浊 阳性 3 420 1715 2019-11-20 微浑 阴性 546 402 2019-11-21 透明 阴性 45 20 2019-11-22 透明 阴性 8 4 2019-11-24 透明 阴性 12 0 2019-11-26 透明 阴性 5 2 2019-11-28 透明 阴性 7 6 2019-11-30 透明 阴性 7 2 2019-12-02 透明 阴性 3 1 表 3 肾功能主要指标检查结果
日期 血肌酐(μmol/L) 2019-11-19 612↑ 2019-11-23 566↑ 2019-11-26 629↑ 2019-12-03 698↑ -
《腹膜透析相关感染的防治指南(2018)》[9](简称《指南》)指出:出现典型腹膜炎表现的患者,在留取透析液标本和更换连接短管后,应尽早开始经验性抗生素治疗,无需等待腹水常规及培养结果。经验性抗生素的抗菌谱须同时覆盖G+菌和G−菌。根据《2016版国际腹膜透析学会(ISPD)指南》[10]:推荐使用万古霉素或第1代头孢菌素治疗G+菌感染,使用第3代头孢菌素(如头孢他啶)或氨基糖苷类抗生素治疗G−菌感染。推荐腹透液中加入抗生素留腹治疗,间断给药留腹治疗需持续至少6 h[9]。对于CAPD患者,腹腔内抗生素推荐剂量如下[10]:万古霉素15~30 mg/kg,每5~7 d加入腹透液中;头孢他啶1 000~1 500 mg qd,腹膜透析用。ISPD指南的推荐剂量和频次变异程度较大,给临床用药带来一定的困难。万古霉素经腹膜透析清除率的大小主要依据:患者残存肾功能、腹膜的渗透率以及透析时间。结合患者实际情况,临床药师认为每3 d给药一次的方案为好,并建议进行血药浓度监测,根据监测结果调整治疗方案。该患者体重65 kg,万古霉素使用1 g q3d 加入腹透液;头孢他啶使用1 g qd加夜间腹透液。患者入院体温38.8 ℃,CRP、PCT均升高,属于严重腹膜炎,腹膜透析相关感染的防治指南(2018)》指出:严重腹膜炎患者合并发热(体温超过38.5℃),建议联合静脉抗生素治疗[9],细菌性腹膜炎的病原菌主要为G−菌,其中,大肠杆菌为主要致病菌,其次为G+菌,其中以凝固酶阴性葡萄球菌为主,故联合使用了广谱抗菌药物美罗培南静脉滴注抗感染治疗。美罗培南为广谱碳青霉烯类抗生素,对厌氧菌、G+菌与G−菌抗菌活性更强,对大多数β-内酰胺酶(包括G+菌与G−菌所产生的青霉素酶和头孢菌素酶,金属β-内酰胺酶除外)的水解作用具有较强的稳定性;根据《抗菌药物药代动力学/药效学理论临床应用专家共识》[11]:对于肌酐清除率<10 ml/min的患者,美罗培南推荐剂量为0.5 g qd。该患者肌酐清除率为8.08 ml/min,美罗培南使用1 g qd,剂量偏大,临床药师建议:美罗培南给药剂量调整为0.5 g qd。
入院第5天,腹透液培养结果为非解乳链球菌。腹透液细菌培养结果显示患者对万古霉素敏感,故停用头孢他啶和美罗培南,继续万古霉素1 g q3d加入腹透液抗感染治疗。入院第12天,患者腹膜炎明显好转,但全血细胞数下降,血小板进行性降低,患者已使用万古霉素灌腹4次,根据《万古霉素临床应用剂量中国专家共识》[12]:万古霉素血药谷浓度是指导剂量调整最关键和最实用的方法,应在第5次给药前,测定万古霉素血药浓度,故临床药师建议抽血测血药浓度。在透析患者中,由于存在血药浓度的反弹,治疗药物监测(TDM)宜在透析结束后6 h进行[13]。正确的采血时间是血药浓度监测结果指导个体化用药的前提,为了保证测得的血药浓度的准确性,临床药师与临床医师、护士提前做好沟通工作,在他们的帮助下完成透析结束后6 h的采血,测得万古霉素血药浓度为15.4 μg/ml。近年来国际上的指南和共识均建议万古霉素血药谷浓度应保持在15 mg/L以上[9-10],该患者使用万古霉素第5剂给药前监测万古霉素谷浓度,此时患者体内万古霉素血药浓度已达稳态,测得血药浓度值为15.4 mg/L,符合指南推荐的目标血药浓度范围。此治疗方案合理。临床药师建议按疗程继续维持万古霉素灌腹治疗。
-
该老年患者血清肌酐(SCr)612 μmol/L,根据肌酐-肾小球滤过率(EPI)公式得肾小球滤过率(eGFR)为7.75 ml/(min·1.73m2),属于慢性肾脏病5期,无尿,腹透液交换是万古霉素最主要的排泄途径,需密切监测肾功能的变化。《成人万古霉素治疗与监测实践指南》中推荐万古霉素治疗数日后,多次(至少2~3次)监测血清肌酐浓度增高(比基线值增高5 mg/L或超过基础水平50%以上)且没有其他原因解释,则可视为发生了万古霉素肾毒性。该患者用药3 d后SCr 566 μmol/L,用药6 d后SCr 629 μmol/L,用药13 d后SCr 698 μmol/L,SCr较前有所升高但幅度不大,临床药师认为是腹膜炎导致腹膜功能下降从而引起SCr升高,判断其未发生肾毒性。对于一般非重度耐甲氧西林金黄色葡萄球菌(MRSA)感染或预防感染的患者,推荐目标谷浓度为10~15 μg/ml,对于严重MRSA感染的成人患者,建议目标谷浓度维持在15~20 μg/ml,以提高抗感染治疗成功率,但应注意监测患者的肾功能[14]。近年来国际上的指南和共识均建议万古霉素血药谷浓度应保持在15 μg/ml以上[9-10]。该患者的万古霉素血药浓度为15.4 μg/ml,在安全范围内。然而,在入院第5天,患者全血细胞数较前减少;做了几次血常规检验发现,患者血小板进行性下降,引起临床药师的关注。
-
不良反应的发生是否由药物引起的,根据国家药品不良反应评价中心制定的不良反应关联性评价标准,评价标准如下:①用药与不良反应/事件的出现有无合理的时间关系;②反应是否符合该药已知的不良反应类型;③停药或减量后,反应是否消失或减轻;④再次使用可疑药品是否再次出现同样反应/事件;⑤反应/事件是否可用合并用药的作用、患者病情的进展、其他治疗的影响来解释。并将ADR关联性评价分为肯定、很可能、可能、可能无关、待评价、无法评价共6级。患者入院后初始用药给予头孢他啶、万古霉素加入腹透液,美罗培南静滴抗感染。在入院第5天,血常规检验结果显示全血细胞较入院时下降,此时刚停用头孢他啶和美罗培南,未采取相应措施,观察血细胞指标。之后2次检验结果大致同前。入院第12天,患者腹膜炎明显好转,但全血细胞数仍较正常水平下降,血小板进行性降低(图1),从用药时间上全血细胞的减少与万古霉素的使用存在合理的时间关系。万古霉素说明书中介绍其多种血细胞减少发生率小于0.1%,血小板减少频率不明。国内外有万古霉素引起全血细胞减少的相关文献报道[5-8]。万古霉素致全血细胞减少的反应与其已知的不良反应类型相吻合。患者出院后第8天(12月12日)至门诊随访,全血细胞计数较出院时回升(图1),未出现牙龈出血、咯血、呕血、黑便、全身未见瘀点瘀斑等现象与头晕等贫血症状。该患者未再次使用万古霉素。患者疾病因素与该不良反应可能无关,因为感染所致的全血细胞减少多伴有发热,多数患者随着疾病进展会出现血象进行性下降导致全血细胞减少,随着疾病好转血象逐渐恢复正常,外周血表现多为中性粒细胞比例或绝对值的增高等,而该患者使用万古霉素抗感染后,病情逐渐好转,但是白细胞、红细胞、血红蛋白和血小板较前降低,血小板进行性下降,无法用疾病来解释出现全血细胞减少的原因。根据不良反应判断标准,患者符合上述5条标准中的①、②、③、⑤4条内容,所以判定全血细胞减少很可能是万古霉素所致。
-
抗菌药物所致血细胞减少症主要分为两种类型:一是骨髓被药物毒性作用抑制所致,如氯霉素类、磺胺类药物等,临床表现的严重程度与用药剂量相关,一旦发现减少,及时停药多可恢复。二是药物通过免疫机制破坏骨髓造血系统,发病率较高的药物如磺胺类、抗结核类药物,而许多药物所致的血细胞减少是双重机制引起。目前万古霉素引起全血细胞减少的机制尚不清楚,一些学者在做患者的骨髓活检时发现了粒细胞的增多或减少,故而认为万古霉素引起全血细胞减少的机制可能是骨髓抑制[6]。《临床用药须知(2005年版)》中提到万古霉索可偶见粒细胞减少、血小板减少,可能与免疫机制有关[15]。目前多数研究认为,万古霉素致血小板减少和粒细胞减少是通过免疫机制介导的[16-17],主要机制是由万古霉素刺激机体产生的特异性万古霉素依赖性抗血小板抗体,与相应抗原血小板膜上的血小板膜糖蛋白GP Ⅱ b 和(或)GP Ⅲa 结合成免疫复合物,从而引起血小板结构的破坏和功能的丧失,进而引起血小板计数的降低和血液系统的凝血功能障碍。总之,万古霉素相关全血细胞减少的原因可能是单一机制,也可能是多种因素共同作用的结果,具体原因有待进一步研究探讨。
-
腹膜透析相关性腹膜炎是腹膜透析最常见的并发症,也是导致患者退出腹膜透析的常见原因之一。万古霉素腹腔灌注是《指南》推荐的治疗措施,该患者腹透液培养结果为非解乳链球菌,腹透液细菌培养结果显示对万古霉素敏感,经万古霉素腹腔灌注后腹膜炎症状明显好转,腹透液生化明显改善。万古霉素最常见的不良反应是耳、肾毒性,临床药师对其不良反应进行了监护,治疗过程中未发生耳、肾毒性;但患者出现了全血细胞减少,临床药师通过查找文献分析可能与使用万古霉素有关,根据不良反应判断标准,患者全血细胞减少的原因很可能是万古霉素所致。临床药师建议在万古霉素达稳态后对该药进行血药浓度监测,根据监测结果调整用药方案。告知医师与护士有关万古霉素采血的时机与有效血药浓度范围的事宜。经监测万古霉素血药浓度为15.4 μg/ml,处于我国和ISPD指南推荐的血药浓度范围内,考虑到该患者的治疗方案有效,且患者未发生严重血细胞减少与其他严重不良反应,故临床药师建议继续当前用药方案的抗感染治疗,但需在用药期间密切监测患者血常规。
以血药浓度监测为指导的个体化治疗为临床药师参与临床治疗提供了新思路。对于本文患者,在应用万古霉素期间患者出现的全血细胞减少,并未盲目地停药或更改用药方案,而是进行了万古霉素血药谷浓度的监测,同时密切关注其血常规变化,并对万古霉素的耳、肾毒性进行用药监护。血药浓度监测结果提示药物浓度在相关指南推荐范围内,万古霉素用药方案合理;用药监护中患者未发生耳、肾毒性及血细胞减少等严重不良反应,所以临床药师建议继续当前用药方案抗感染治疗,并加强对患者的血细胞监测,获得医师采纳。最终患者的感染得到了有效控制,在万古霉素停药后血细胞指标有所好转。
临床上发现万古霉素引起全血细胞减少的病例较少,尽管可逆,但是万古霉素可诱导机体产生相应的抗体,产生的抗体除引起血小板破坏之外,还会引起红细胞和白细胞的破坏,严重者可发生出血和免疫抑制。临床药师应注意当发现有使用万古霉素并出现全血细胞减少的患者,应提高警惕,定期监测血常规,密切关注血小板计数及观察有无出血现象,加强万古霉素的用药监护,提高使用万古霉素的安全性。
Medication evaluation and adverse reaction monitoring in patient on peritoneal dialysis with pancytopenia induced by vancomycin
-
摘要:
目的 为临床药师参与腹膜透析相关性腹膜炎患者的抗感染治疗和个体化药学服务实践提供参考。 方法 临床药师通过对1例腹膜透析患者万古霉素血药谷浓度的监测,根据腹透液细菌培养与药敏结果评价以调整抗感染治疗方案,并对万古霉素所致的全血细胞减少进行了不良反应监护。 结果 有效控制了该腹膜透析患者的感染,全血细胞减少的相关指标有所好转。 结论 通过对1例万古霉素致腹膜透析患者全血细胞减少的病例分析,以期引起临床工作人员对这一不良反应的关注,提高使用万古霉素的用药安全性。 Abstract:Objective To provide reference for anti-infection treatment and individual pharmaceutical care in patient on peritoneal dialysis. Methods The plasma concentration of vancomycin in patient on peritoneal dialysis was monitored by clinical pharmacists. The anti-infection treatment plan was evaluated and adjusted according to the bacterial culture and drug sensitivity results of the abdominal dialysis fluid. The adverse reactions of pancytopenia induced by vancomycin were documented. Results Infection in the patient on peritoneal dialysis was effectively controlled. The related indicators of pancytopenia were improved. Conclusion A case of pancytopenia induced by vancomycin in the patient on peritoneal dialysis was analyzed to get clinical staff's attention to this adverse reaction and improve the safety of vancomycin administration. -
非酒精性脂肪性肝病(NAFLD)是临床常见的肝脏疾病之一,其中,非酒精性脂肪性肝炎(NASH)是非酒精性脂肪肝(NAFL)向非酒精性脂肪性肝硬化转化过程中一个非常重要的环节[1]。非酒精性脂肪性肝炎发展到晚期将导致肝硬化的发生,最终进展为肝细胞癌(HCC),从而影响整体肝功能。因此,NASH的防治具有重要意义。七味脂肝方由垂盆草、豨莶草、牡蛎等七味药组成,处方源于岐黄学者、中医临床肝病专家季光教授临床经验的总结,长期临床应用显示对NASH具有很好的效果。本研究参考常用的NASH动物模型[2-4],选用蛋氨酸和胆碱缺乏(MCD)饮食诱导以及胆碱缺乏的高脂高胆固醇饮食(CDAHFHC)诱导的2个经典NASH的动物模型,研究七味脂肝方对NASH的药效作用,为临床用药提供科学的理论依据。
1. 材料与仪器
1.1 药物与试剂
七味脂肝方供试品(江苏康缘药业股份有限公司提供,批号:Z201001),根据项目组前期制定的提取工艺,将七味脂肝方制备成每1 g含6.19 g生药的浸膏粉;维生素E(VE)软胶囊(上海信谊延安药业有限公司,国药准字H31020237,批号:03210202);罗格列酮片(成都恒瑞制药有限公司,国药准字H20030569,批号:210601);丙氨酸氨基转移酶(ALT)、门冬氨酸氨基转移酶(AST)、碱性磷酸酶(ALP)、甘油三酯(TG)、胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)测定试剂盒(上海惠中生物科技有限公司,批号:01ALT210107、01AST210329、01ALP210222、02TG210330、01CHOL210226、01HDL210525、01LDL210302);乳酸脱氢酶(LDH)测定试剂盒(上海执诚生物科技有限公司,批号:ZCJULT019);游离脂肪酸(FFA)、总胆红素(TBIL)测定试剂盒(美康生物科技股份有限公司,批号:210609101、190731101);苏木素、伊红染色液(珠海贝索生物技术有限公司,批号:719041、719033);F4/80抗体,(Abcam,批号:1004577-2)。
1.2 仪器
全自动生化分析仪(日本东芝,型号:TBA-40R);全自动样品快速研磨仪(上海净信,型号:Tissuelyser-24);轮转式石蜡切片机、冷冻切片机、组织包埋机(徕卡显微系统(上海)贸易有限公司,型号:RM2235、CM1950、Histocore Amber);正置显微镜(日本OLYMPUS,型号:CX31RTSF)。
1.3 实验动物
Sprague-Dawley大鼠(SD大鼠),雄性,6周龄,体重200~250 g,48只,购自上海市计划生育科学研究所实验动物经营部,生产许可证号:SCXK(沪)2018-0006。C57BL/J小鼠,雌雄各半,6周龄,体重(24±2)g,96只,购置于上海吉辉实验动物饲养有限公司,生产许可证号:SCXK(沪)2017-0012。通过上海中医药大学实验动物中心实验动物伦理(伦理号:PZSHUTCM210625020)审查,实验动物使用许可证号:SYXK(沪)2018-0006,SPF级环境饲养。
2. 方法
2.1 造模与分组
2.1.1 MCD诱导的大鼠NASH模型
48只雄性SD大鼠,饲养于上海中医药大学实验动物中心,正常饮食,自由食水,观察7 d。第8天,根据动物体重按随机数字法随机分为对照组和模型组,除对照组外,其余动物饲料梯度替换为MCD饲料(正常饲料喂养;25%MCD饲料喂养2 d;50%MCD饲料喂养2 d;75%MCD饲料喂养2 d;100%MCD饲料喂养2周),自由食水。造模2周后,对模型组动物根据体重随机分组,分为模型组、七味脂肝方低剂量组(2.8 g/kg生药)、七味脂肝方中剂量组(5.6 g/kg生药)、七味脂肝方高剂量组(11.2 g/kg生药)、阳性对照VE组(40 mg/kg),每组8只。各给药组每天灌胃1次,连续28 d,对照组及模型组灌胃等量的生理盐水。
2.1.2 CDAHFHC诱导的小鼠NASH模型
96只C57BL/J小鼠,雌雄各半,饲养于上海中医药大学实验动物中心,正常饮食,自由食水,观察7 d。第8天,根据动物体重按随机数字法随机分为对照组和模型组,除对照组外,其余动物饲料梯度替换为CDAHFHD饲料(正常饲料喂养;25%CDAHFHC饲料喂养2 d;50%CDAHFHC饲料喂养2 d;75%CDAHFHC饲料喂养2 d;100%CDAHFHC饲料喂养2周),自由食水。造模2周后,对模型组动物根据体重随机分组,分为模型组、七味脂肝方低剂量组(4 g /kg生药)、七味脂肝方中剂量组(8 g/kg生药)、七味脂肝方高剂量组(16 g/kg生药)、阳性对照罗格列酮组(RSG,1.14 mg/kg),每组16只。各给药组每天灌胃1次,连续28 d,对照组及模型组灌胃等量的生理盐水。
2.2 检测方法
2.2.1 血清肝功能和血脂生化指标检测
使用全自动生化分析仪测定ALT、AST、ALP、LDH、TG、TC、HDL-C、LDL-C、TBIL、FFA在血清中的水平。
2.2.2 肝组织脂质水平检测
取新鲜肝脏组织样本,加入1∶9(质量体积比)的匀浆介质(乙醇∶丙酮=1∶1),冰浴条件下匀浆,置于冰箱4 ℃过夜,4 000 r/min离心15 min,收集上清液样本,使用全自动生化分析仪测定TG、TC、HDL-C、LDL-C在肝脏组织中的水平。
2.2.3 肝脏组织病理学评价
肝脏左叶样本固定后,经组织脱水,石蜡包埋,将其切成4 μm的石蜡切片。
(1)HE染色
取肝脏石蜡切片样本,经HE染色,用正置显微镜拍照并评价肝脏病理变化。NASH病理诊断标准采用NAFLD活动度积分(NAS)进行评估(具体评判标准见表1)。
表 1 NAFLD活动度积分(NAS)组织学评分判断标准评分 肝细胞脂肪变(%) 小叶内炎症 肝细胞气球样变 0 <5 无病灶 无 1 5~33 <2 少量气球样细胞 2 34~66 2~4 较多/显著气球样变 3 >66 >4 注:NAS≥5分可明确NASH的诊断;NAS<3分则可排除NASH;两者之间者为NASH可能。 (2)Masson染色
取肝脏石蜡切片样本,经Masson三色染色,通过正置显微镜观察并拍照记录,评价肝组织纤维化程度。Masson染色纤维化诊断评分参照以下评分标准(表2)。
表 2 肝纤维化分期评分判断标准评分 纤维化程度 0 无 1 窦周或汇管区纤维化 2 窦周和汇管区周围纤维化 3 桥接纤维化 4 肝硬化 (3)免疫组织化学染色
取肝脏石蜡切片样本,经F4/80抗体免疫组织化学染色,通过正置显微镜观察并拍照记录,评价肝组织中Kupffer细胞的活化程度。
2.3 统计方法
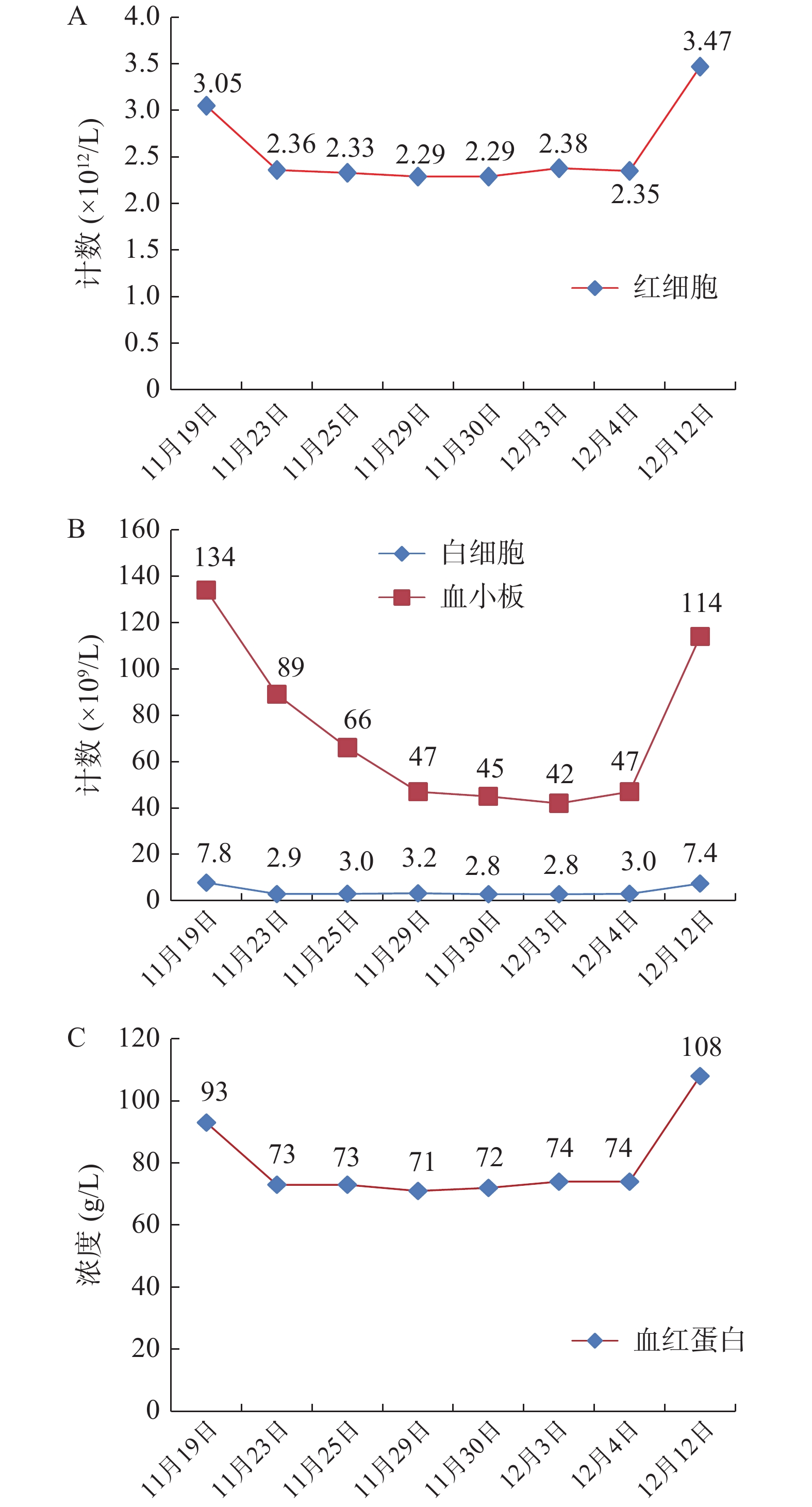
所有计量资料采用平均值±标准偏差(
$ \bar{x}\pm s $ )表示。计量资料采用单因素方差分析(one-sample Kolmogorov-Smirnov test)进行数据分布判断,正态分布时采用参数检验的单因素方差分析(ANOVA),偏态分布时采用非参数检验(Mann-Whitney test)。所有数据均使用GraphPad Prism 8软件进行统计并进行图表制作。3. 结果
3.1 对肝脏形态、肝重及肝脏指数的影响
3.1.1 MCD诱导的大鼠NASH模型实验结果
对照组肝脏表面光滑,色深红,质地软,有弹性,肝叶边缘锐利。与对照组相比,模型组肝脏体积增大,颜色变浅;与模型组相比,七味脂肝方各剂量组和阳性对照VE组可以观察到肝脏颜色稍红,各组均可一定程度改善肝脏形态,结果见图1和表3。
表 3 大鼠体重、肝脏重量及肝脏指数($ \bar{{x}}\pm {s} $ )组别 动物数(n) 体重(m/g) 肝重(m/g) 肝指数(%) 对照组 8 397.28±31.15 10.46±1.15 2.63±0.14 模型组 8 202.19±15.56## 6.91±1.10## 3.41±0.42## 七味脂肝方低剂量组 8 202.75±14.72 7.31±1.08 3.59±0.34 七味脂肝方中剂量组 8 202.98±17.39 7.90±1.54 3.88±0.57 七味脂肝方高剂量组 8 201.83±16.04 7.82±0.90 3.88±0.43* 阳性对照VE组 8 201.83±11.16 7.22±0.57 3.59±0.34 *P<0.05,与模型组比较; ##P<0.01,与对照组比较。 3.1.2 CDAHFHC诱导的小鼠NASH模型实验结果
对照组肝脏表面光滑,色深红,质地软,有弹性,肝叶边缘锐利;与对照组相比,模型组肝脏体积增大,颜色变浅;与模型组相比,七味脂肝方各剂量组和阳性对照RSG组可以观察到肝脏颜色稍红,各组均可一定程度改善肝脏形态,结果见图2。
与对照组相比,模型组肝脏重量、肝脏指数显著升高(P<0.01);与模型组相比,七味脂肝方的各剂量组和阳性对照RSG组均能显著降低肝脏重量(P<0.05或P<0.01),七味脂肝方的中、高剂量组和阳性对照RSG组能显著降低肝脏指数(P<0.01),结果见表4。
表 4 小鼠体重、肝脏重量及肝脏指数($ \bar{x}\pm {s} $ )组别 动物数(n) 体重(m/g) 肝重(m/g) 肝指数(%) 对照组 16 22.12±2.00 0.91±0.16 4.11±0.47 模型组 16 18.91±1.36## 1.69±0.15## 8.96±0.62## 七味脂肝方低剂量组 16 18.59±1.01 1.56±0.20* 8.41±1.06 七味脂肝方中剂量组 16 18.48±1.08 1.51±0.18** 8.17±0.72** 七味脂肝方高剂量组 16 18.32±1.03 1.54±0.13** 8.38±0.53** 阳性对照RSG组 16 19.14±1.34 1.56±0.18* 8.16±0.68** *P<0.05,**P<0.01,与模型组比较; ##P<0.01,与对照组比较。 3.2 对血清肝功能、血脂水平的影响
3.2.1 MCD诱导的大鼠NASH模型实验结果
与对照组相比,模型组血清ALT水平显著升高(P<0.01);与模型组相比,七味脂肝方中剂量组血清ALT水平显著降低(P<0.05),七味脂肝方中、高剂量组可改善血清ALP、LDH、HDL水平,结果见表5、表6。
表 5 大鼠血清肝功能数据($ \bar{x}\pm {s}$ )组别 动物数(n) ALT(U/L) AST(U/L) ALP(U/L) LDH(U/L) 对照组 8 45.50±3.38 165.38±24.80 88.50±15.73 1547.50 ±243.04模型组 8 107.25±32.84## 187.50±24.36 93.75±32.65 1250.00 ±235.02#七味脂肝方低剂量组 8 107.00±37.80 195.88±25.90 87.25±24.54 1263.00 ±451.90七味脂肝方中剂量组 8 69.38±16.33* 171.25±19.91 63.13±18.76* 886.88±304.48* 七味脂肝方高剂量组 8 114.13±51.86 177.88±44.05 89.75±34.65 855.88±375.75* 阳性对照VE组 8 111.00±15.76 165.75±16.61 128.50±58.52 1219.63 ±368.75*P<0.05,与模型组比较;#P<0.05,##P<0.01,与对照组比较。 表 6 大鼠血脂4项数据($ \bar{x}\pm {s} $ )组别 动物数(n) TG(mmol/L) TC(mmol/L) HDL(mmol/L) LDL(mmol/L) 对照组 8 0.32±0.10 1.12±0.22 0.28±0.03 0.15±0.02 模型组 8 0.23±0.05# 0.83±0.18# 0.32±0.06 0.14±0.04 七味脂肝方低剂量组 8 0.29±0.07 0.93±0.12 0.38±0.07 0.15±0.03 七味脂肝方中剂量组 8 0.32±0.19 1.25±0.51* 0.49±0.19* 0.21±0.08 七味脂肝方高剂量组 8 0.23±0.06 1.20±0.26** 0.48±0.10** 0.21±0.08 阳性对照VE组 8 0.23±0.05 0.84±0.23 0.33±0.12 0.15±0.04 *P<0.05,**P<0.01,与模型组比较;#P<0.05,与对照组比较。 3.2.2 CDAHFHC诱导的小鼠NASH模型结果
与对照组相比,模型组血清ALT、AST、ALP、LDH、TG、TC、LDL水平显著升高(P<0.01),HDL水平显著降低(P<0.01);与模型组相比,七味脂肝方低剂量组血清ALP、TG水平显著降低(P<0.05或P<0.01),七味脂肝方中剂量组血清LDH、TG水平显著降低(P<0.05),七味脂肝方高剂量组血清ALT、AST、ALP、LDH、TG水平显著降低(P<0.05或P<0.01),阳性对照RSG组血清ALT水平显著降低(P<0.05),结果见表7和表8。
表 7 小鼠血清肝功能数据($\bar{x}\pm {s}$ )组别 动物数(n) ALT(U/L) AST(U/L) ALP(U/L) LDH(U/L) 对照组 16 35.13±6.08 146.06±43.63 88.31±9.41 653.94±145.10 模型组 16 606.06±111.12## 486.31±69.39## 216.19±28.30## 1390.25 ±128.14##七味脂肝方低剂量组 16 561.44±98.43 440.69±67.29 179.06±46.80* 1347.19 ±150.78七味脂肝方中剂量组 16 553.00±116.35 442.94±72.95 198.06±32.64 1261.69 ±122.55*七味脂肝方高剂量组 16 486.63±88.90** 406.25±75.39** 189.94±34.09* 1161.00 ±134.22**阳性对照RSG组 16 513.56±91.17* 441.81±70.00 273.94±43.98** 1328.75 ±160.91*P<0.05,**P<0.01,与模型组比较;##P<0.01,与对照组比较。 表 8 小鼠血脂4项数据($\bar{x}\pm {s}$ )组别 动物数(n) TG(mmol/L) TC(mmol/L) HDL(mmol/L) LDL(mmol/L) 对照组 16 0.82±0.39 2.70±0.42 1.64±0.35 0.18±0.03 模型组 16 1.27±0.26## 3.45±0.55## 0.93±0.29## 0.57±0.17## 七味脂肝方低剂量组 16 1.01±0.25** 3.29±0.61 0.91±0.19 0.55±0.18 七味脂肝方中剂量组 16 1.01±0.31* 3.46±0.52 0.99±0.26 0.59±0.13 七味脂肝方高剂量组 16 1.01±0.29* 3.37±0.34 0.99±0.13 0.57±0.10 阳性对照RSG组 16 1.10±0.28 3.33±0.79 0.94±0.32 0.56±0.15 *P<0.05,**P<0.01,与模型组比较; ##P<0.01,与对照组比较。 与对照组相比,模型组血清TBIL、FFA水平显著升高(P<0.01);与模型组相比,七味脂肝方高剂量组和阳性对照RSG组血清TBIL水平显著降低(P<0.05)。结果见表9。
表 9 小鼠血清TBIL、FFA数据($\bar{x}\pm {s}$ )组别 动物数(n) TBIL(μmol/L) FFA(mmol/L) 对照组 16 3.59±0.55 1.41±0.31 模型组 16 7.77±1.52## 2.16±0.46## 七味脂肝方低剂量组 16 6.95±1.78 2.01±0.43 七味脂肝方中剂量组 16 7.79±3.97 1.98±0.49 七味脂肝方高剂量组 16 6.37±1.72* 2.16±0.49 阳性对照RSG组 16 9.09±1.69* 2.20±0.55 *P<0.05,与模型组比较; ##P<0.01,与对照组比较。 3.3 对肝脏脂质水平的影响
3.3.1 MCD诱导的大鼠NASH模型实验结果
与对照组相比,模型组肝脏TG水平显著升高(P<0.01),HDL水平显著降低(P<0.01);与模型组相比,阳性对照VE组肝脏HDL水平显著升高(P<0.01),结果见表10。
表 10 大鼠肝脏脂质水平($\bar{x}\pm {s}$ )组别 动物数(n) TG(mmol/g) TC(mmol/g) HDL(mmol/g) LDL(mmol/g) 对照组 8 3.93±0.56 1.49±0.16 0.11±0.03 0.67±0.08 模型组 8 5.97±0.53## 1.14±0.13## 0.03±0.02## 0.25±0.13## 七味脂肝方低剂量组 8 5.73±0.82 1.03±0.12 0.02±0.02 0.27±0.10 七味脂肝方中剂量组 8 5.57±0.93 1.14±0.12 0.03±0.03 0.31±0.07 七味脂肝方高剂量组 8 5.93±0.81 1.10±0.14 0.02±0.01 0.27±0.08 阳性对照VE组 8 7.25±1.40* 1.21±0.15 0.08±0.02** 0.34±0.09 *P<0.05,**P<0.01,与模型组比较; ##P<0.01,与对照组比较。 3.3.2 CDAHFHC诱导的小鼠NASH模型实验结果
与对照组相比,模型组肝脏TG、TC水平显著升高(P<0.01);与模型组相比,七味脂肝方高剂量组肝脏TG水平显著降低(P<0.01),结果见表11。
表 11 小鼠肝脏脂质水平($\bar{x}\pm {s}$ )组别 动物数(n) TG(mmol/g) TC(mmol/g) HDL(mmol/g) LDL(mmol/g) 对照组 16 3.54±1.98 1.04±0.15 0.20±0.07 0.35±0.11 模型组 16 8.78±0.89## 2.29±0.21## 0.47±0.13## 0.42±0.21 七味脂肝方低剂量组 16 8.54±1.04 2.20±0.20 0.47±0.08 0.36±0.16 七味脂肝方中剂量组 16 8.69±1.54 2.28±0.31 0.49±0.09 0.43±0.17 七味脂肝方高剂量组 16 7.85±0.79** 2.12±0.39 0.45±0.14 0.39±0.24 阳性对照RSG组 16 8.44±0.97 2.12±0.26 0.47±0.09 0.36±0.16 **P<0.01,与模型组比较; ##P<0.01,与对照组比较。 3.4 对肝脏病理NAS评分的影响
3.4.1 MCD诱导的大鼠NASH模型HE染色实验结果
对照组大鼠肝小叶结构完整,肝细胞排列整齐,肝板以中央静脉为中心呈放射状排列,未见明显病理性改变。
模型组镜下可见广泛的肝细胞空泡变性,中央静脉及汇管区周围可见肝细胞坏死,小叶间炎症细胞浸润,肝小叶结构被破坏。与对照组相比,模型组脂肪变性、小叶内炎症及NAS评分显著升高(P<0.01)。
与模型组相比,七味脂肝方的各给药组和阳性对照VE组可明显减轻小叶内炎症程度。与模型组相比,七味脂肝方低、中、高剂量组和阳性对照VE组小叶内炎症评分显著降低(P<0.05或P<0.01),七味脂肝方的中剂量组和阳性对照VE组NAS评分显著降低,结果见表12。
表 12 大鼠肝脏NAS评分($\bar{x}\pm {s}$ )组别 动物数(n) 脂肪变性 小叶内炎症 气球样变 NAS 对照组 8 0.00±0.00 0.00±0.00 0.00±0.00 0.00±0.00 模型组 8 2.88±0.35## 1.63±0.52## 0.00±0.00 4.50±0.76## 七味脂肝方低剂量组 8 3.00±0.00 1.00±0.00* 0.38±0.52 4.38±0.52 七味脂肝方中剂量组 8 3.00±0.00 0.88±0.35* 0.00±0.00 3.88±0.35* 七味脂肝方高剂量组 7 3.00±0.00 0.86±0.38* 0.00±0.00 3.86±0.38 阳性对照VE组 8 3.00±0.00 0.63±0.52** 0.00±0.00 3.63±0.52* *P<0.05,**P<0.01,与模型组比较; ##P<0.01,与对照组比较。 3.4.2 CDAHFHC诱导的小鼠NASH模型HE染色实验结果
对照组肝小叶结构完整,肝细胞排列整齐,肝板以中央静脉为中心呈放射状排列,未见明显病理性改变。
模型组镜下可见广泛的肝细胞空泡变性,中央静脉及汇管区周围可见肝细胞点状或灶状坏死,小叶间炎性细胞浸润,肝小叶结构被破坏,较多个肝细胞呈气球样变。与对照组相比,模型组脂肪变性、小叶内炎症、气球样变及NAS评分显著升高。
与模型组相比,七味脂肝方中、高剂量组可有效减轻炎性灶数量和肝细胞气球样变,显著降低小叶内炎症程度评分、气球样变评分及NAS评分(P<0.01),阳性对照RSG组可减轻小叶内炎症程度,显著降低小叶内炎症程度评分及NAS评分(P<0.01),结果见表13。
表 13 小鼠肝脏NAS评分($\bar{x}\pm {s}$ )组别 动物数(n) 脂肪变性 小叶内炎症 气球样变 NAS 对照组 16 0.00±0.00 0.00±0.00 0.00±0.00 0.00±0.00 模型组 16 3.00±0.00## 2.81±0.40## 1.88±0.34## 7.69±0.48## 七味脂肝方低剂量组 16 3.00±0.00 2.56±0.51 1.69±0.48 7.25±0.86 七味脂肝方中剂量组 16 3.00±0.00 2.13±0.34** 1.38±0.50** 6.50±0.73** 七味脂肝方高剂量组 16 3.00±0.00 1.88±0.34** 1.31±0.48** 6.19±0.66** 阳性对照VE组 16 3.00±0.00 2.19±0.40** 1.56±0.51 6.75±0.68** **P<0.01,与模型组比较; ##P<0.01,与对照组比较。 3.5 对肝脏Masson染色及纤维化评分的影响
CDAHFHC诱导的小鼠NASH模型Masson染色结果显示,对照组肝小叶结构完整,肝细胞排列整齐,汇管区结构清晰,被染成蓝色的纤维结缔组织分布在肝小叶间血管和胆管周围,汇管区周围的纤维结缔组织呈围管状包绕血管及胆管分支。
模型组可见肝细胞点状或灶状坏死,炎症细胞浸润,镜下多个视野可见小叶内和汇管区周围被染成蓝色的胶原纤维增生。与对照组相比,模型组纤维化评分显著升高(P<0.01)。
与模型组相比,七味脂肝方的中、高剂量组可观察到肝小叶内和汇管区周围胶原纤维增生情况明显减轻,并呈现一定程度的剂量梯度效应;阳性对照RSG组在肝小叶和汇管区周围的胶原纤维增生情况也可得到一定程度的改善。与模型组相比,七味脂肝方的高剂量组纤维化评分显著降低(P<0.05),结果见表14。
表 14 小鼠肝脏纤维化分期评分($\bar{x}\pm {s}$ )组别 动物数(n) 纤维化分期评分 对照组 16 0.00±0.00 模型组 16 1.56±0.51## 七味脂肝方低剂量组 16 1.75±0.45 七味脂肝方中剂量组 16 1.44±0.51 七味脂肝方高剂量组 16 1.19±0.40* 阳性对照RSG组 16 1.25±0.45 *P<0.05,与模型组比较; ##P<0.01,与对照组比较。 3.6 对肝脏Kupffer细胞的影响
MCD诱导的大鼠和CDAHFHC诱导的小鼠NASH模型F4/80免疫组织化学染色结果显示,对照组大鼠肝脏Kupffer细胞处于静息状态,为不规则或树枝状分布。
模型组可观察到在肝小叶炎性灶及汇管区周围大量的被激活的Kupffer细胞,呈现花冠状分布,被F4/80标记的阳性细胞数明显增加。
与模型组相比,七味脂肝方的中、高剂量组显示被F4/80标记的阳性细胞数密度降低,Kupffer细胞活化程度明显减弱,花冠状分布程度明显减轻,呈一定程度的浓度依赖;阳性对照VE组和RSG组同样可减轻Kupffer细胞活化程度,与文献报道一致,结果见图3、图4。
4. 讨论
NASH是在非酒精性肝脂肪变基础上形成的,出现血清生化酶学超过正常值上限,肝穿刺病理组织学显示肝细胞脂肪变>5%,伴有炎症及肝细胞损伤(如气球样变),并除外导致肝脂肪变的其他原因,如大量饮酒、长期应用促脂肪形成药物或单基因遗传紊乱等的疾病[1]。近年来,关于NASH发病机制的研究已取得很大进展,但目前治疗选择非常有限[5-6],FDA、SFDA尚未批准针对该疾病的有效药物。权威指南中推荐使用的药物有维生素E、吡格列酮等,但这些药物的有效性和安全性存在争议[7-8]。目前,防治NASH的主要方法以生活方式干预为主,其他方法包括降糖、降脂和保肝的间接对症治疗,降低导致NASH的高危因素的相关疾病,使患者间接获益。
中医药因具有多因子、多靶点和多环节的协同药理效应,在治疗该类疾病具有独特的优势,在治NASH方面取得了一定进展[9-11]。非酒精性脂肪性肝炎并无确切中医学病名[12],根据其临床表现可归属于“肝癖”、“胁痛”、“黄疸”等范畴。病位主要涉及肝脾,病久及肾。由于过食肥甘厚味,运化失职,使谷精不能尽化气血而凝为膏脂,导致肝失疏泄、脾失健运,痰浊淤积于肝;脾胃为气机升降之枢,湿浊困脾,脾气不升,一身气机运化失常,加剧肝气郁结和肝络失养。
七味脂肝方中酒豨莶草、垂盆草清热解毒、利湿退黄,二药合为君药;煅牡蛎软坚散结,《珍珠囊》谓其可“软痞积”,《本草纲目》谓“化痰软坚,清热除湿”,山楂消食积,散淤血,《本草纲目》认为其可“化饮食,消肉积,癥瘕,痰饮痞满吞酸,滞血痛胀”,海藻消痰软坚散结,利水消肿,三药共为臣药;虎杖协同加强解毒、化瘀、退黄之功效,为佐药;醋五味子收敛固涩、益气生津、补肾宁心,可补五脏气,为使药。全方七味药物相辅相成,达到湿、痰、瘀、毒兼顾,利湿解毒,消痰散结,用于NASH湿热痰瘀互结证。现代药理学表明,方中垂盆草中的槲皮素[13]、虎杖中的虎杖苷等成分均对NASH有一定治疗作用[14-15]。
NASH是一种更严重的NAFLD病理类型,NASH的特征是存在肝细胞损伤、肝脂肪变性、炎症和纤维化,进而发生肝硬化并增加肝细胞癌的风险[16]。在NASH发展过程中,肝脏内脂肪合成量不断上升,代谢功能逐渐下降,肝脏对脂质的摄取和代谢能力随之减弱,导致脂质代谢过程中TC、TG和LDL-c含量升高,同时受损的肝细胞还会释放AST、ALT活力到血液中,导致AST、ALT活力升高,这些指标的异常变化可作为NASH的标志[17]。肝内过量的脂质沉积可导致炎症反应,促使单纯性脂肪肝向NASH的病理进展[18]。肝纤维化是肝细胞外基质的弥漫性过度沉积与异常分布,是肝脏对慢性损伤的病理性修复反应。目前,肝组织病理学检查仍是肝纤维化诊断的“金标准”。目前的科学研究普遍认为,Kupffer细胞对NAFLD的发生和发展至关重要,如果它们被适度激活,可以发挥防御作用,但如果它们被过度激活,将释放大量的促炎细胞因子,这对肝组织和其他细胞会造成一定程度的损伤。已有文献表明,活化的肝脏巨噬细胞可以促进NASH的进展[19]。
本研究在MCD诱导的大鼠和CDAHFD诱导的小鼠两个经典NASH模型的实验结果显示,经过2周的诱导后,模型组的肝脏质量以及ALT、AST、ALP、LDH、TG、TC、LDL、TBIL及FFA水平显著高于对照组,HE、Masson及免疫组化染色显示,肝脏组织炎症和肝细胞脂肪变性严重,NAS评分显著增加,肝小叶内和汇管区周围胶原纤维增生及Kupffer细胞活化程度加重,说明建立NASH模型成功。经4周的给药后,七味脂肝方能显著降低上述指标,此外,HE、Masson及免疫组化染色显示,七味脂肝方能显著减轻肝脏组织炎症程度,降低肝脏组织病理NAS评分,减轻肝纤维化及Kupffer细胞活化程度。说明七味脂肝方能有效降低血脂、调节肝脏脂质代谢紊乱,改善NASH小鼠肝脏炎症损伤向肝纤维化发展的趋势,改善肝脏组织病理损伤,从而有效减缓并改善NASH的进展程度。
NASH的发病机制尚未完全阐明,目前公认的是“多重打击”理论,其认为胰岛素抵抗、脂肪毒性、炎症、氧化应激等多种致病因素共同导致了NASH的发生发展,而炎症在NASH的恶化过程中扮演着至关重要的角色[18]。肝脏具有密集的吞噬细胞网络,在非炎症条件下维持耐受性,并快速感知肝细胞损伤和氧化应激信号,导致促炎级联反应的激活。在损伤后,白细胞迅速渗入肝实质,通过产生可溶性介质激活其他免疫细胞和非实质细胞群,从而促进炎症和纤维化的发生。炎症介质可以激活肝星状细胞(HSCs),HSCs是肝纤维化形成过程中的主要效应细胞,导致细胞外基质过度沉积,形成创伤愈合或瘢痕反应,进一步促进纤维化发展。活化的HSCs产生促炎介质,进而使肝脏炎症持续存在,导致炎症的慢性循环和瘢痕组织的形成,最终导致器官衰竭[20]。因此,抑制炎症对于NASH的预防和治疗具有重要意义,深入理解NASH相关的炎症信号通路(NF-κB和MAPK等),并找到能够有效靶向特定炎症的靶点,将为治疗NASH提供更多的思路和新的策略。已有多次报道NF-κB信号通路参与NASH中炎症反应,损伤相关分子模式(DAMPs)激活Kupffer细胞,诱导细胞内的NF-κB信号激活[21]。本研究病理染色结果证明,七味脂肝方可减少炎性浸润,减轻肝纤维化程度,改善NASH动物肝脏的病理表现,后续将继续探究七味脂肝方药效物质基础作用的炎症通路,进一步阐明其治疗NASH的机制。
本研究结果初步提示,七味脂肝方可能是通过改善NASH肝脏炎症损伤,继而阻碍其向肝纤维化发展的趋势来发挥药效,为其后续机制探究提供研究方向。针对目前的NASH临床需求,七味脂肝方具有较好的临床价值。
-
表 1 患者住院期间的主要治疗药物
开始用药 药品名称及用法用量 停止用药 2019-11-19 注射用盐酸万古霉素1 g,留腹时间>6 h 注射用头孢他啶1 g qd,加夜间腹透液 2019-11-23 注射用美罗培南1 g+氯化钠注射液100 ml qd 静脉滴注 2019-11-23 2019-11-22 注射用盐酸万古霉素1 g加入头孢他啶留腹的腹透液中 2019-11-25 注射用盐酸万古霉素1 g加入腹透液中 重组人促红素注射液5000 U,皮下注射 2019-11-28 注射用盐酸万古霉素1 g加入腹透液中 2019-12-03 注射用盐酸万古霉素1 g加入腹透液中 表 2 腹透液主要指标检查结果
日期 腹透液透明度 李凡他试验 细胞总数(×106/L) 有核细胞计数(×106/L) 2019-11-19 浑浊 阳性 3 420 1715 2019-11-20 微浑 阴性 546 402 2019-11-21 透明 阴性 45 20 2019-11-22 透明 阴性 8 4 2019-11-24 透明 阴性 12 0 2019-11-26 透明 阴性 5 2 2019-11-28 透明 阴性 7 6 2019-11-30 透明 阴性 7 2 2019-12-02 透明 阴性 3 1 表 3 肾功能主要指标检查结果
日期 血肌酐(μmol/L) 2019-11-19 612↑ 2019-11-23 566↑ 2019-11-26 629↑ 2019-12-03 698↑ -
[1] BRUNIERA F R, FERREIRA F M, SAVIOLLI L R, et al. The use of vancomycin with its therapeutic and adverse effects: a review[J]. Eur Rev Med Pharmacol Sci,2015,19(4):694-700. [2] BLACK E, LAU T T, ENSOM M H. Vancomycin-induced neutropenia: is it dose- or duration-related? Ann Pharmacother,2011,45(5):629-638. doi: 10.1345/aph.1P583 [3] SHAHAR A, BERNER Y, LEVI S. Fever, rash, and pancytopenia following vancomycin rechallenge in the presence of ceftazidime[J]. Ann Pharmacother,2000,34(2):263-264. doi: 10.1345/aph.19051 [4] 张金红, 房德敏, 高颖, 等. 万古霉素致血小板减少症的国内外文献系统回顾性分析[J]. 中国药学杂志, 2017, 52(21):1953-1960. [5] CARMICHAEL A J, AL-ZAHAWI M F. Drug points: Pancytopenia associated with vancomycin[J]. BMJ,1986,293(6554):1103. [6] ROCHA J L, KONDO W, BAPTISTA M I, et al. Uncommon vancomycin-induced side effects[J]. Braz J Infect Dis,2002,6(4):196-200. doi: 10.1590/S1413-86702002000400007 [7] GUPTA S, SHARMA S, MENON N, et al. Case report of vancomycin-induced pancytopenia[J]. Rev Soc Bras Med Trop,2016,49(2):258-259. doi: 10.1590/0037-8682-0263-2015 [8] LENG B, YAN G, LI T, et al. Vancomycin-induced reversible pancytopenia and rash in a 16-month-old boy with osteomyelitis: a case report? Int J Clin Pharmacol Ther,2020,58(4):242-246. doi: 10.5414/CP203619 [9] 中国腹膜透析相关感染防治专家组. 腹膜透析相关感染的防治指南[J]. 中华肾脏病杂志, 2018, 34(2):139-148. doi: 10.3760/cma.j.issn.1001-7097.2018.02.010 [10] LI PK, SZETO CC, PIRAINO B, et al. ISPD peritonitis recommendations: 2016 update on prevention and treatment[J]. Perit Dial Int,2018,38(4):313. doi: 10.3747/pdi.2018.00030 [11] 中国医药教育协会感染疾病专业委员会. 抗菌药物药代动力学/药效学理论临床应用专家共识[J]. 中华结核和呼吸杂志, 2018, 41(6):409-446. doi: 10.3760/cma.j.issn.1001-0939.2018.06.004 [12] 万古霉素临床应用剂量专家组. 万古霉素临床应用剂量中国专家共识[J]. 中华传染病杂志, 2012, 30(11):641-646. doi: 10.3760/cma.j.issn.1000-6680.2012.11.001 [13] 万古霉素临床应用中国专家共识(2011版)[J]. 万古霉素临床应用中国专家共识(2011版)[J]. 中国新药与临床杂志, 2011, 30(8):561-573. [14] 翟所迪, 贺蓓, 王睿, 等. 《中国万古霉素治疗药物监测指南》解读[J]. 中国临床药理学杂志, 2016, 32(17):1633-1636. [15] 国家药典委员会. 中华人民共和国药典: 临床用药须知(中药卷)(2005年版)[M]. 北京: 人民卫生出版社, 2005. [16] VON DRYGALSKI A, CURTIS B R, BOUGIE D W, et al. Vancomycin-induced immune thrombocytopenia[J]. N Engl J Med,2007,356(9):904-910. doi: 10.1056/NEJMoa065066 [17] SCHWARTZ M D. Vancomycin-induced neutropenia in a patient positive for an antineutrophil antibody[J]. Pharmacother: J Hum Pharmacol Drug Ther,2002,22(6):783-788. doi: 10.1592/phco.22.9.783.34059 -





 下载:
下载:
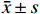















 下载:
下载:


