-
胃食管反流病(Gastroesophageal reflux disease,GERD)是指胃内容物反流至食管、口腔(包括咽喉)和/或肺导致的一系列症状[1],发病机制包括反流物的攻击、食管黏膜防御作用减弱、一过性食管下括约肌松弛(transient lower esophageal sphincter relaxations,TLESR)、食管裂孔疝、食管清除能力降低等[2]。反流性食管炎(reflux esophagitis, RE)是GERD的临床表现之一,是指胃和(或)十二指肠内容物反流入食管引起食管黏膜的炎症反应,主要表现为吞咽困难、反酸、烧心等。药物治疗主要以对症治疗为主,抑酸药能够降低胃酸分泌,迅速缓解反酸症状和降低反流对食管黏膜的进一步损伤,其中标准剂量的质子泵离子抑制剂(PPI)被推荐作为反流性食管炎的一线用药[3]。艾司奥美拉唑为目前常用的PPI,其表现出了显著的抑酸效果,但是经过CYP2C19 和CYP3A4酶代谢[4],尽管在临床上的应用非常普及,其代谢特点使其存在个体差异,并且在联合用药方面存在局限性。研究表明,药物并不会降低严重胃食管反流病患者胃酸反流的频率或提高反流物的清除率,控制胃酸重要的是减少食管接触酸的持续时间[5],因此需要寻找长效持久的PPI,以提高治疗反流性食管炎的疗效。
艾普拉唑是一种新型质子泵离子抑制剂,为苯并咪唑类,与奥美拉唑等化学结构相似,但在苯并咪唑上用吡咯环取代了氢,在吡啶环上用氢取代了甲基,这一特殊的分子结构使其能更有效地降低胃酸分泌,减少食管的酸暴露时间[6]。艾普拉唑受到CYPC2C19基因影响小,消除半衰期长,能够发挥持久的抑酸效果[7],这一药动学优势使其在联合用药方面具有很大的应用空间。艾普拉唑肠溶片最初上市批准的适应证仅限于十二指肠溃疡,后于2017年被批准用于治疗反流性食管炎[8],作为新一代的 PPI,具有一定的综合评价需求。近期一篇网状meta分析比较了所有PPI用于十二指肠溃疡4周疗程后的治疗效果,结果显示各PPI间的疗效相似,差异无统计学意义[9]。目前艾普拉唑用于治疗RE的研究越来越多,但尚未有文献对艾普拉唑治疗RE的有效性和安全性进行总结,本文通过 Meta 分析方法,对比10 mg艾普拉唑肠溶片与40 mg艾司奥美拉唑肠溶片在RE治疗中的有效性和安全性,以期为临床用药提供参考。
-
公开发表的RCT、研究内容为艾普拉唑肠溶片用于RE治疗的疗效研究,语种不限。
-
有典型的反酸、烧心、胸骨后疼痛等症状,并经内镜检查确诊为 RE 的患者。
-
试验组:给予艾普拉唑肠溶片(10 mg,1次 /d,口服);对照组:给予艾司奥美拉唑肠溶片(40 mg,1 次 /d,口服)
-
①内镜下有效率(治疗时间≥4周),其中内镜检查参照洛杉矶分级标准[10]:
无发现:黏膜无破损;A级:食管黏膜存在1个或1个以上破损,最大直径≤5 mm;B级:食管黏膜存在1个或1个以上破损,最大直径>5 mm,破损的黏膜无融合;C级:食管黏膜存在1个或1个以上破损,且有融合,<食管直径的75%;D级:食管黏膜存在1个或1个以上破损,且有融合,≥食管直径的75%;②症状缓解率;③不良反应发生率。
-
①未提供原始数据或者数据缺失,联系原作者也无法获得的文献;②重复发表的文献(同一作者及团队的一系列研究选用数据最完整的研究);③综述、动物实验、会议论文、毕业论文、个案报道。
-
采用主题词和自由词相结合的方式检索文献,中文检索词包括:艾普拉唑、反流性食管炎、糜烂性食管炎;英文检索词包括:Ilaprazole、IY 81149、Reflux Esophagitis、Esophagitides, Peptic、Reflux Esophagitides等,检索中国知网(CNKI)、维普网(VIP)、万方数据知识服务平台及PubMed、Web of Science、EMBase、The Cochrane Library,检索时间从建库截至2021年4月,无语言限制。
-
由2名研究者独立筛选文献、提取资料并交叉核对。如有分歧,则通过讨论或与第三方协商解决。文献筛选时首先阅读文章标题,在排除明显不相关的文献后,再进一步阅读摘要和全文以确定是否纳入。必要时通过邮件联系研究作者获取相关信息。资料提取内容包括:①纳入研究的基本信息。包括研究题目、作者、研究对象的临床基线资料、发表时间等;②干预措施;③偏倚风险评价的关键因素;④所关注的结局指标和结果。
-
采用Cochrane手册5.1.0版提供的RCT偏倚风险评价纳入研究的方法学质量。
-
使用 Cochrane 协作网提供的RevMan 5.4软件进行分析,二分类变量采用相对危险度(RR)及其95%CI为效应分析统计量,计量资料采用均数差(MD)及其95%CI为效应分析统计量。绘制森林图并进行异质性检验与发表偏倚检测。各研究间的异质性检验采用 Q 检验与 I2 值,P>0.10且 I2≤50% 时提示各研究间无统计学异质性,采用固定效应模型进行Meta分析;如果各研究间存在统计学异质性(P≤0.10 或 I2≥50%),应先分析异质性来源,若无明显临床异质性且无法找到确定的统计学异质性来源则采用随机效应模式进行 Meta 分析。以 P<0.05 为差异有统计学意义。明显的临床异质性采用亚组分析或敏感性分析等方法进行处理。
-
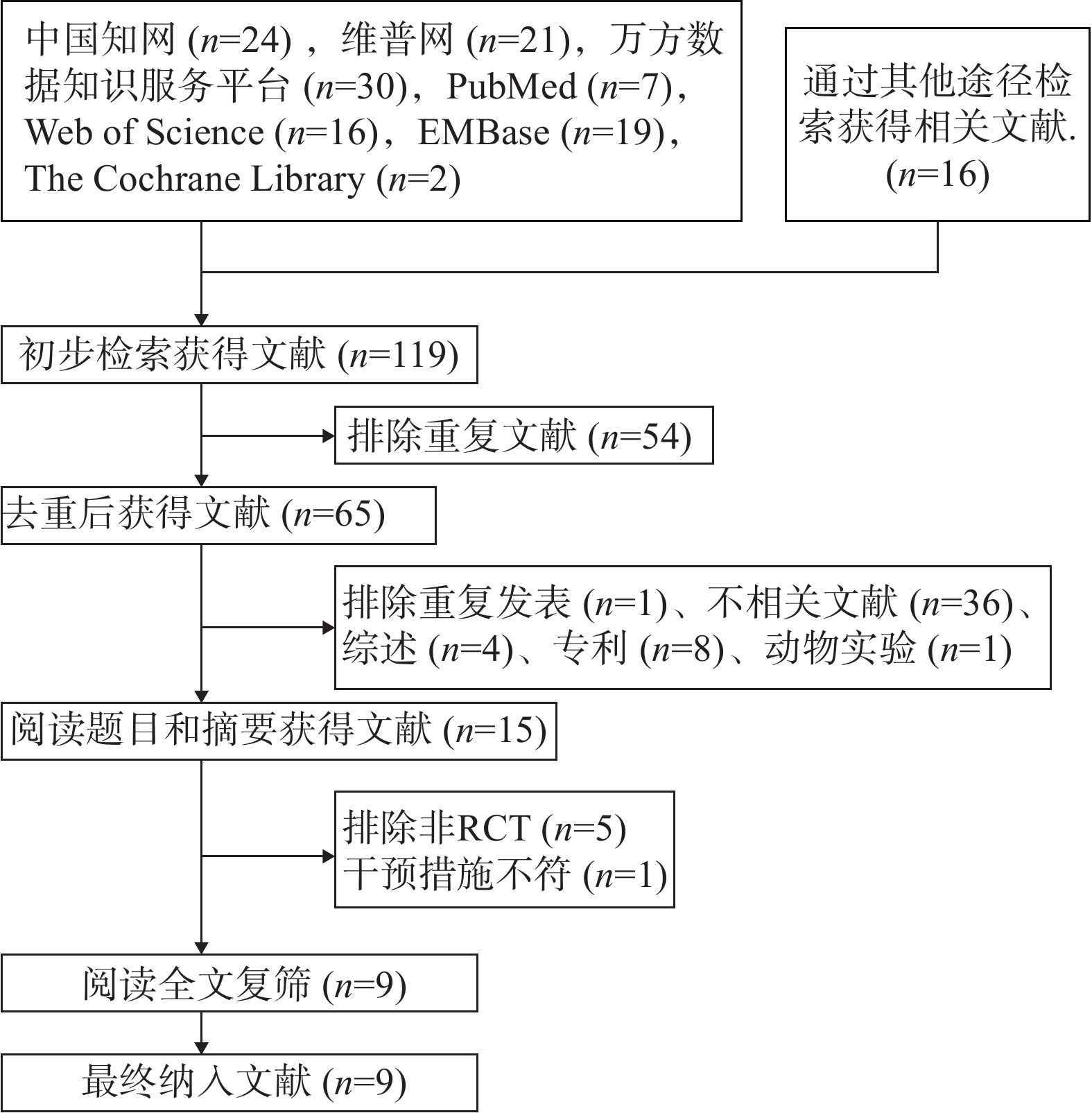
文献筛选流程见图1,初步检索到有关文献119篇,包括中文文献 71 篇,英文文献 48 篇,经过文献摘要及全文的阅读、排除重复文献及不符合纳入标准的研究后,最终有9 篇文献纳入研究,共涉及 1115 例患者。所有研究均采用随机分组设计。纳入文献的基本特征见表1。
表 1 纳入文献的基本特征表
纳入研究 例数 临床诊断 干预措施 疗程(周) 结局指标 试验组 对照组 试验组 对照组 范学峰2019[11] 45 45 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ① Xue2016[12] 290 181 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ①③ 胡爱萍2016[13] 43 43 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ②③ 霍结容2015[14] 50 50 RE A:10 mg,1 次/d B:40 mg,1 次/d 4 ②③ 牛省利2013[15] 143 137 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ② 艾冬华2013[16] 40 40 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ①② 宋芳2012[17] 60 60 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ①②③ 郭永谊2012[18] 35 34 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ②③ 李东复2011[19] 43 35 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ②③ RE:反流性食管炎;A 代表艾普拉唑肠溶片; B 代表艾司奥美拉唑肠溶片;①内镜下有效率;②临床症状缓解率;③不良反应 -
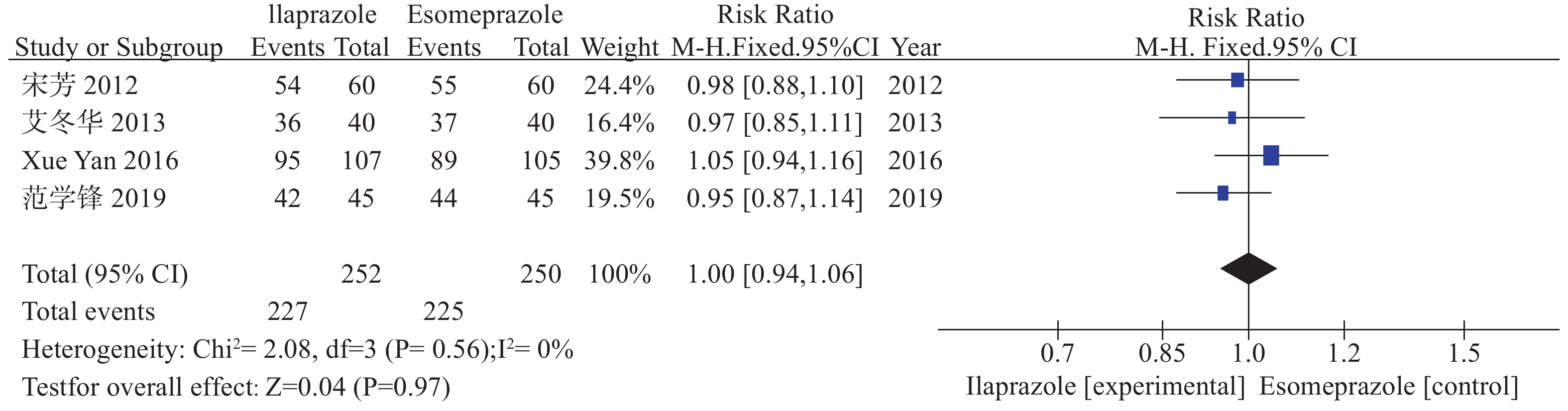
共 4篇文献[11-12, 16-17]分析了治疗8周内镜下有效率。异质性检验结果显示,各研究间无统计学异质性(I2=0%,P=0.56),采用固定效应模型进行 Meta 分析。结果显示,纳入艾普拉唑治疗组的患者内镜下有效率为 90.08%(227例/252例),纳入艾司奥美拉唑治疗组的患者内镜下有效率为90.00%(225例/250例),差异无统计学意义[RR=1.00,95%CI(0.94,1.06),P=0.97],见图2。
-
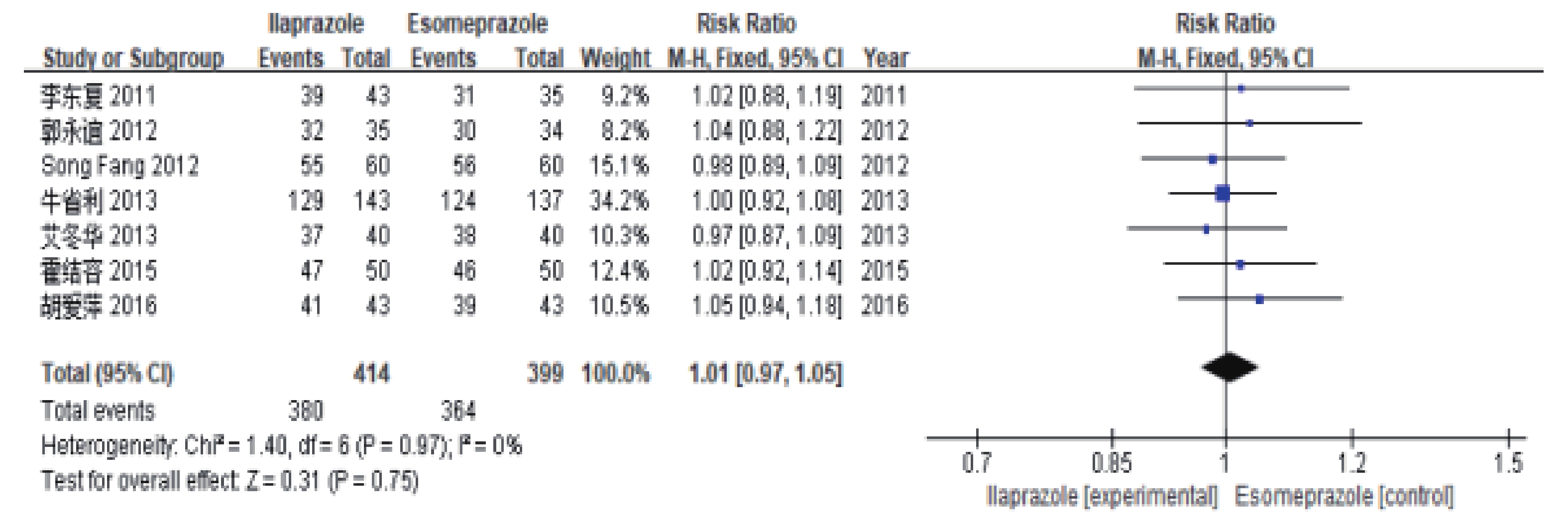
共7篇文献[13-19]分析了症状缓解率,其中1篇文献治疗周期为4周,其余6篇治疗周期为8周。异质性检验结果显示,各研究间无统计学异质性(I2=0%,P=0.97),采用固定效应模型进行 Meta 分析。结果显示,纳入艾普拉唑治疗组的患者症状缓解率为 91.79%(380例/414例),纳入艾司奥美拉唑治疗组的患者症状缓解率为91.23%(364例/399例),差异无统计学意义[RR=1.01,95%CI(0.97,1.05),P=0.75],见图3。
-
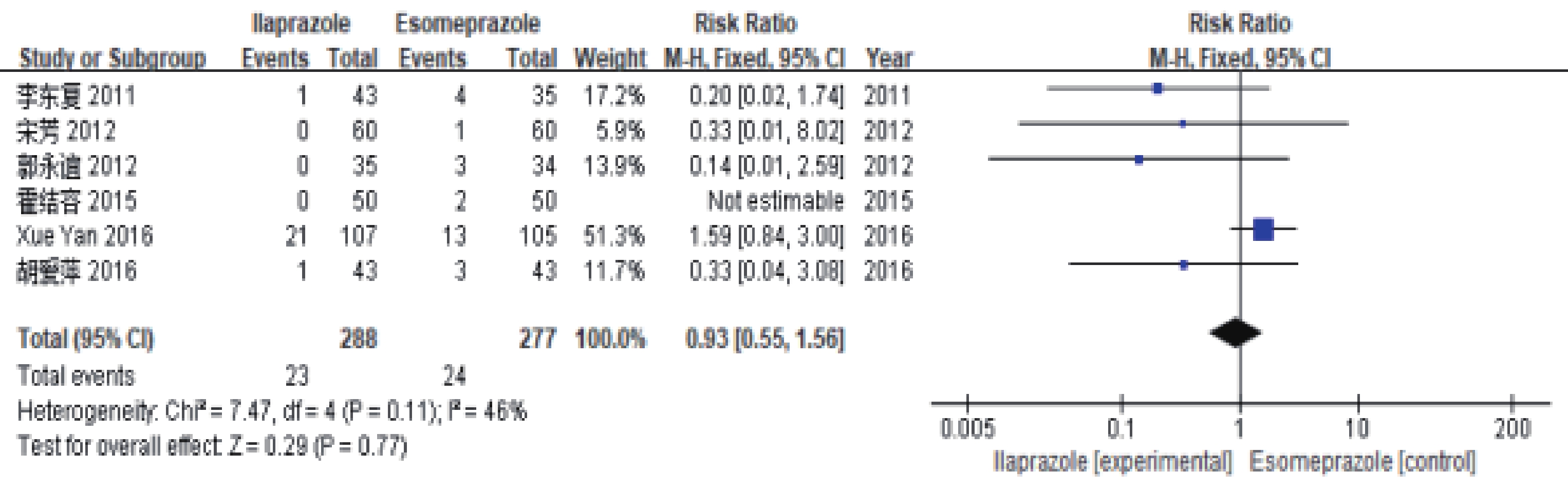
共6篇文献[12-14, 17-19]分析了不良反应发生率。异质性检验结果显示,各研究间无统计学异质性(I2=46%,P=0.11),采用固定效应模型进行 Meta 分析。结果显示,纳入艾普拉唑治疗组的患者不良反应发生率为 7.99%(23例/288例),纳入艾司奥美拉唑治疗组的患者不良反应发生率为8.66%(24例/277例),差异无统计学意义 [RR=0.93,95%CI(0.55,1.56),P=0.77],见图4。
-
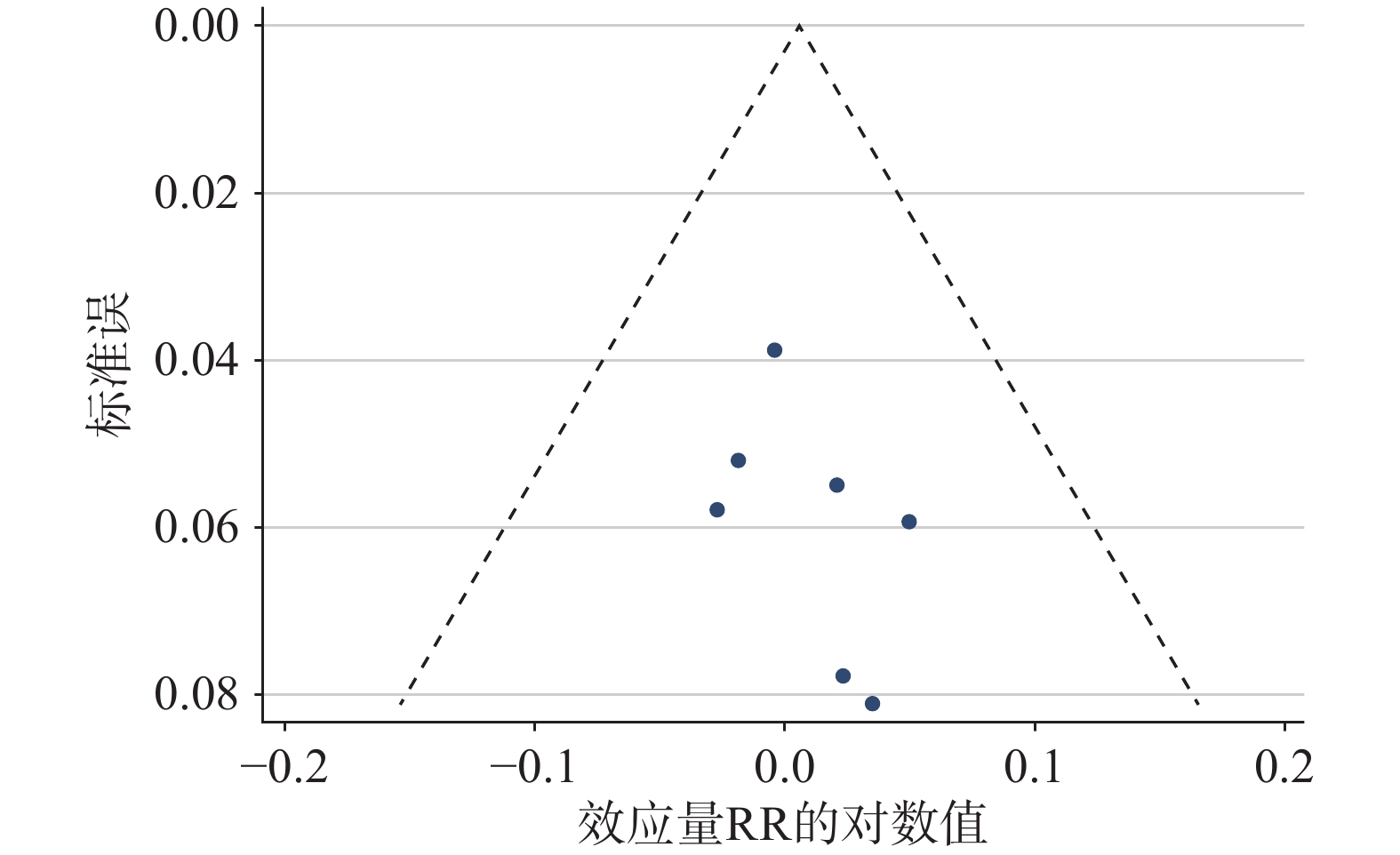
对纳入以艾普拉唑组和艾司奥美拉唑组的症状缓解率为结局指标的研究,以效应量的标准误(log RR的对数)作为纵坐标,以各研究的效应量RR的对数值作为横坐标绘制漏斗图,详见图5。由图可见,漏斗图基本对称,提示纳入文献的发表偏倚较小。Egger检验结果提示:P=0.368,表明本研究不存在明显的偏倚。
-
临床研究表明,RE是反流物对食管黏膜的攻击和抗反流防御机制下降的综合结果[20],PPI能够抑制胃酸分泌,迅速缓解反酸症状和降低反流对食管黏膜的进一步损伤。临床上常应用艾普拉唑治疗RE,相关的RCT研究也说明了艾普拉唑的疗效与安全性,因此有必要应用Meta分析对已有研究进行综合讨论。本文对9篇文献,1115名RE患者的治疗情况进行了统计分析,结果显示,艾普拉唑肠溶片10 mg/d的治疗方案与艾司奥美拉唑肠溶片40 mg/d的治疗方案相比,内镜下有效率和症状缓解率相似,差异无统计学意义。但从用药剂量上看,艾普拉唑的每日剂量为10 mg,艾司奥美拉唑的每日剂量为40 mg,提示应用更少剂量的艾普拉唑能达到与艾司奥美拉唑相似的治疗效果,这也是艾普拉唑肠溶片的一大优势。研究表明艾普拉唑预防RE、抑制胃酸分泌和预防脂质过氧化的效果与奥美拉唑相当,且不会诱导胃泌素的分泌,对幽门螺杆菌的杀菌作用比奥美拉唑强2 ~ 4倍[21]。本文同时统计了艾普拉唑出现的腹泻、口干等不良反应,但其不良反应发生率与艾司奥美拉唑治疗组相当,且无严重不良反应发生,提示艾普拉唑安全性良好。
本Meta分析尚存在一定的局限性,本研究严格限定了筛选条件,因此将部分国外研究筛除在外,致本研究纳入文献数量较少,且均为国内RCT试验。国外研究如Periclou的RCT试验表明艾普拉唑与奥美拉唑相比,对GERD表现出了更强更持久的抑酸效果[22];而Song的非RCT试验表明艾普拉唑能使非RE病因的GERD导致的胃灼热症状得到改善,以上研究均证明艾普拉唑对GERD表现出较好的治疗效果[23]。本Meta分析的对照药局限于艾司奥美拉唑,而缺乏其他PPI作为对照来进一步证实其疗效及安全性的优越性,纳入的部分试验在治疗RE时设计的临床试验诊断标准和疗效评价可能没有按照国际公认的标准进行,致系统评价的推荐等级和证据强度有所降低。
本研究中艾普拉唑肠溶片的用法用量均为10 mg/d,使用的最长疗程为8周,尚没有足够的临床试验说明艾普拉唑用于RE作为长期维持治疗用药的最佳剂量、用药周期和复发率,并且患者的年龄均在18 ~ 75岁之间,排除了存在严重合并症(如心、肝、肾功能不全)的患者,因此未来仍需要更多的临床试验探讨艾普拉唑用于儿童、老年人、肝肾功能不全患者等特殊人群的疗效及安全性。
PPI的有效性和安全性使其得到广泛的应用,但是一部分患者并不能获得完全的治疗效果[24]。研究表明吸烟、喝浓茶、暴饮暴食等生活方式和发病密切相关[25],社会心理因素也会增加烧灼的感觉和食道疼痛[26],因此在抑酸疗效不佳时有必要采取联合用药的方式提高治疗效果,或者通过改变生活方式减少诱发RE的危险因素[27]。例如Yu等的研究中,PPI与氟哌噻吨美利曲辛片联用,疗效优于PPI单药治疗[28],Yoshida等的研究则表明瑞巴派特与兰索拉唑联用有利于预防GERD长期维持治疗期间症状的复发[29]。目前存在艾普拉唑与抗酸药、胃黏膜保护剂、促胃动力药等药物联用的研究报道,但是报道数量有限,不足以为循证医学提供充分的数据支持,因此仍需更多临床试验来分析艾普拉唑联合用药的具体情况。
综上所述,用于治疗RE时,无论在症状改善方面,或内镜下食管愈合方面,艾普拉唑的疗效和安全性与艾司奥美拉唑相当,值得临床推广应用。鉴于纳入Meta 分析的文献数量及样本量的局限性,今后仍需要开展更多高质量、大样本的随机对照试验加以验证。
Meta-analysis of the efficacy and safety of Ilaprazole Enteric-Coated Tablets on reflux esophagitis
-
摘要:
目的 系统评估艾普拉唑肠溶片治疗反流性食管炎的有效性和安全性。 方法 检索CNKI、VIP、万方数据知识服务平台及PubMed、Web of Science、EMBase、The Cochrane Library数据库,搜集2021年4月之前公开发表的应用艾普拉唑肠溶片治疗RE的随机对照试验(RCT)。纳入符合标准的文献,经数据提取和质量评价后,采用RevMan 5.4软件对内镜下有效率、症状缓解率和不良反应发生率进行统计分析。 结果 共纳入9个RCT,包括1115名RE患者。Meta分析结果显示,有效性方面,10 mg艾普拉唑肠溶片与40 mg艾司奥美拉唑肠溶片相比,内镜下有效率 (90.08% vs. 90.00%,P>0.05) 和症状缓解率 (91.79% vs. 91.23%,P>0.05) 相当;安全性方面,艾普拉唑肠溶片与艾司奥美拉唑肠溶片相比,不良反应发生率较低 (7.99% vs. 8.66%,P>0.05),但差异无统计学意义。 结论 艾普拉唑肠溶片应用更少的剂量能达到与艾司奥美拉唑肠溶片相似的治疗效果,能有效治疗RE且安全性良好。 Abstract:Objective To evaluate the efficacy and safety of Ilaprazole Enteric-Coated Tablets in the treatment of RE. Methods The databases of CNKI, VIP, Wanfang Data, PubMed, Embase, and The Cochrane Library were searched to collect all the randomized controlled trials (RCTs) of Ilaprazole in the treatment of RE published before April 2021. After data extraction and quality evaluation, the RCTs meeting the inclusion criteria were performed, and the meta-analysis was conducted by RevMan 5.4. Results Nine RCTs were included, with a total of 1115 patients of RE. The results of the meta-analysis showed that Ilaprazole Enteric-Coated Tablets were comparable to Esomeprazole Enteric-Coated Tablets in both endoscopic efficiency (90.08% vs. 90.00%, P > 0.05) and symptom relief rates (91.79% vs. 91.23%, P > 0.05), and there was no statistically significant difference in the incidence of adverse reactions (7.99% vs. 8.66%, P > 0.05). Conclusion Ilaprazole Enteric-Coated Tablets with lower doses were comparable to Esomeprazole Enteric-Coated Tablets which showed good efficacy and safety in the treatment of reflux esophagitis. -
Key words:
- Reflux esophagitis /
- Ilaprazole Enteric-Coated Tablets /
- Meta-analysis
-
山楂为蔷薇科植物山里红Crataegus pinnatifida Bge. var. major N. E. Br. 或山楂 Crataegus pinnati- fida Bge. 的干燥成熟果实,焦山楂为其炒制品[1]。现代药理研究证明,焦山楂抑菌作用强于生山楂,而某些特定菌群与消化功能密切相关[2]。而山楂炒焦后产生新的物质—类黑素,类黑素是在食品热处理过程中形成的。目前,类黑素的抗菌活性已得到证实。大多数类黑素对微生物作用的研究都是在特定的微生物生长培养基中进行的,这些研究表明类黑素可以刺激微生物生长[3],也可以抑制微生物生长[4-5]。肠道菌群与人体健康密切相关,药物和功能食品可能通过调节肠道微生物来改善胃肠功能,帮助消化[6-7]。双歧杆菌和大肠杆菌是典型的有益菌和有害菌,双歧杆菌常被加入酸奶饮品中帮助消化。乙酸是双歧杆菌的主要代谢物质,随着乙酸的增多,pH值降低从而抑制大肠杆菌的生长繁殖。本实验通过研究山楂,焦山楂以及焦山楂炒制过程中产生的类黑素对大肠杆菌、双歧杆菌以及其代谢物乙酸的影响,探究“山楂炒焦长于消食导滞”的作用机制。
1. 材料与方法
1.1 材料
1.1.1 实验仪器
低温培养箱(美墨尔特有限公司,德国),生物安全柜(赛默飞世尔科技公司,美国),高压灭菌锅(三洋公司,日本),纯水机(密理博公司,美国),厌氧罐(北京陆桥技术股份有限公司,北京);紫外可见分光光度计(上海佑科仪器仪表有限公司,上海);7890B型气相色谱仪(安捷伦科技有限公司,美国);HP-FFAP型毛细管柱(货号:19091F-413,安捷伦科技有限公司,美国);GM900型非接触红外测温仪(深圳聚茂源科技有限公司,深圳)。
1.1.2 实验试剂
MRS固体培养基、PYG液体培养基、厌氧产气袋和厌氧指示剂(北京陆桥技术股份有限公司);蛋白胨、酵母粉(英国OXOID公司);乙酸(98.85%,国药集团化学试剂有限公司,中国);其余试剂均为分析纯。
1.1.3 山楂和实验菌株
净山楂饮片(四川同善堂中药饮片有限责任公司,批号:180501);双歧杆菌(GDMCC1.1258)、大肠杆菌(ATCC25922)(中国科学院微生物研究所)。
1.2 方法
1.2.1 焦山楂的炮制
参照2015版《中国药典》一部山楂项下制备焦山楂。取生山楂150 g,中火(380~420)℃炒制10 min,至药材表面呈焦黄或焦褐色,内部颜色加深,并具有焦香气味,取出,常温封存,即得。
1.2.2 生山楂,焦山楂和类黑素浸膏的制备
(1)生山楂和焦山楂浸膏的制备
取生山楂和焦山楂各100 g进行水浸提,料液比为1:15,浸提8 h,浸提2次。生山楂和焦山楂浸提液分别在4 ℃下以3 600 r/min离心10 min,取上层清液各1 000 ml。将500 ml上层清液进行蒸发浓缩至胶状,停止加热,余温使其自然干燥,得生山楂浸膏13.75 g,焦山楂浸膏14.02 g。
(2)焦山楂中类黑素的提取
取焦山楂100 g,按照“1.2.2”项中⑴的方法提取得到1 000 ml上层清液。取500 ml上层清液蒸发浓缩得棕褐色浓缩液50 ml,进行大孔树脂吸附,室温吸附流速1.5 ml/min,60%乙醇作为洗脱剂,洗脱至色谱柱上无棕色为止,收集洗脱液500 ml。洗脱液蒸发浓缩至胶状,停止加热,余温使其自然干燥,得焦山楂类黑素浸膏13.12 g。
(3)类黑素的紫外检测
取类黑素浸膏1 g,蒸馏水溶解定容至100 ml,取10 ml溶液,分别定容至50 ml;因波长420 nm处是类黑素的特征吸收波长,测其特征吸收下的吸光度值,焦山楂类黑素浸膏吸光度值为0.492,说明焦山楂中类黑素提取成功。
1.2.3 山楂炮制品及类黑素对肠道菌群生长繁殖的影响
(1)双歧杆菌测试菌菌液的制备
以接种环自双歧杆菌标准菌种管挑取菌种,划线接种至MRS固体培养基,36 ℃厌氧培养48 h,挑取单菌落接种至PYG液体培养基,36 ℃厌氧培养48 h,以生理盐水调整浓度至1.0麦氏浓度,作为受试菌初始菌液,按10:1浓度加入试验体系。
(2)大肠杆菌测试菌液的制备
以接种环自大肠杆菌标准菌种管挑取菌种,划线接种至LB固体培养基(配方:蛋白胨10 g,酵母粉5 g,氯化钠10 g,琼脂粉15 g,加入1 L蒸馏水,以5 mol/L氢氧化钠调节pH至7.0,121 ℃高压灭菌15 min备用),36 ℃有氧培养24 h,挑取单菌落接种至LB液体培养基(配方:蛋白胨10 g,酵母粉5 g,氯化钠10 g,加入1 L蒸馏水,以5 mol/L氢氧化钠调节pH至7.0,121 ℃高压灭菌15 min备用),36 ℃有氧培养6 h,以生理盐水调整浓度至0.5麦氏浓度,作为受试菌初始菌液,按10:1浓度加入试验体系。
(3)样本药液的处理
准确称取生山楂,焦山楂和类黑素浸膏各10 g,加入100 ml去离子水,超声振荡处理,期间手动震摇数次,直至样本完全溶解,配制10%母液,并经115 ℃高压灭菌处理15 min后4 ℃保存备用。
(4)乙酸含量测定
①样本前处理:将经过微生物培养的溶液1 ml,经过高速离心机4 000 r/min离心,之后再过0.2 µm有机相滤头于进样瓶,样品量大于0.5 ml,或者使用内插管,上机测定。
②标准溶液及标准曲线:称取60.05 g乙酸于100 ml容量瓶,用一级水定容至刻度,摇匀,作为储备标准溶液,浓度为101.33 mmol/L。将标准储备溶液依次稀释1、3、10、20、100、200倍得标准工作溶液。
③色谱条件:洗针液为甲醇,进样量0.5 µl,进样口温度240 ℃;压力6.1219 psi;分流比10:1,流量为1.0 ml;升温程序:初始温度:100 ℃,保持0 min;梯度一:以5 ℃/min升到120 ℃,保持0 min;梯度二:以20 ℃/min升到200 ℃,保持10 min;总运行时间:18 min;检测器(FID)温度:240 ℃;空气流量:300 ml/min;氢气流量:33 ml/min;尾吹氮气流量:20 ml/min;数据采集频率/峰宽:20 Hz/0.01 min。
1.3 统计学方法
使用SPSS 22.0进行独立样本t检验,数据以平均数±标准差(
$\bar x \pm s$ )表示,P<0.05认为存在显著性差异。2. 结果
2.1 乙酸标准曲线的建立
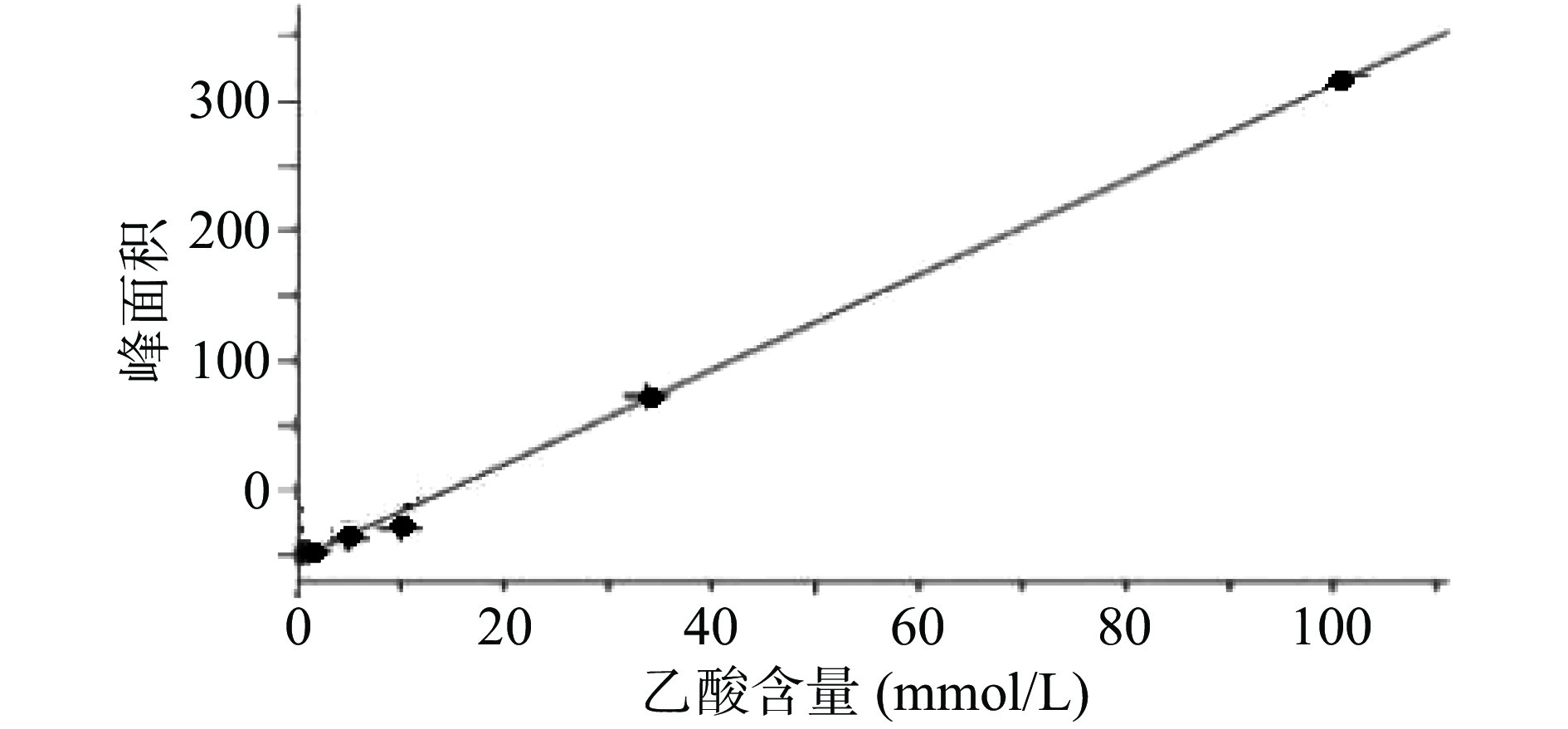
乙酸浓度在0.51~101.33 mmol/L线性关系良好。以乙酸峰面积(Y)为纵坐标,乙酸含量(X)为横坐标,绘制标准曲线,得到线性回归方程为Y=3.670 5X−4.300 8,r=0.999 0,残留标准误差为6.644 2,如图1所示。
2.2 山楂饮片及类黑素对双歧杆菌体外生长的影响
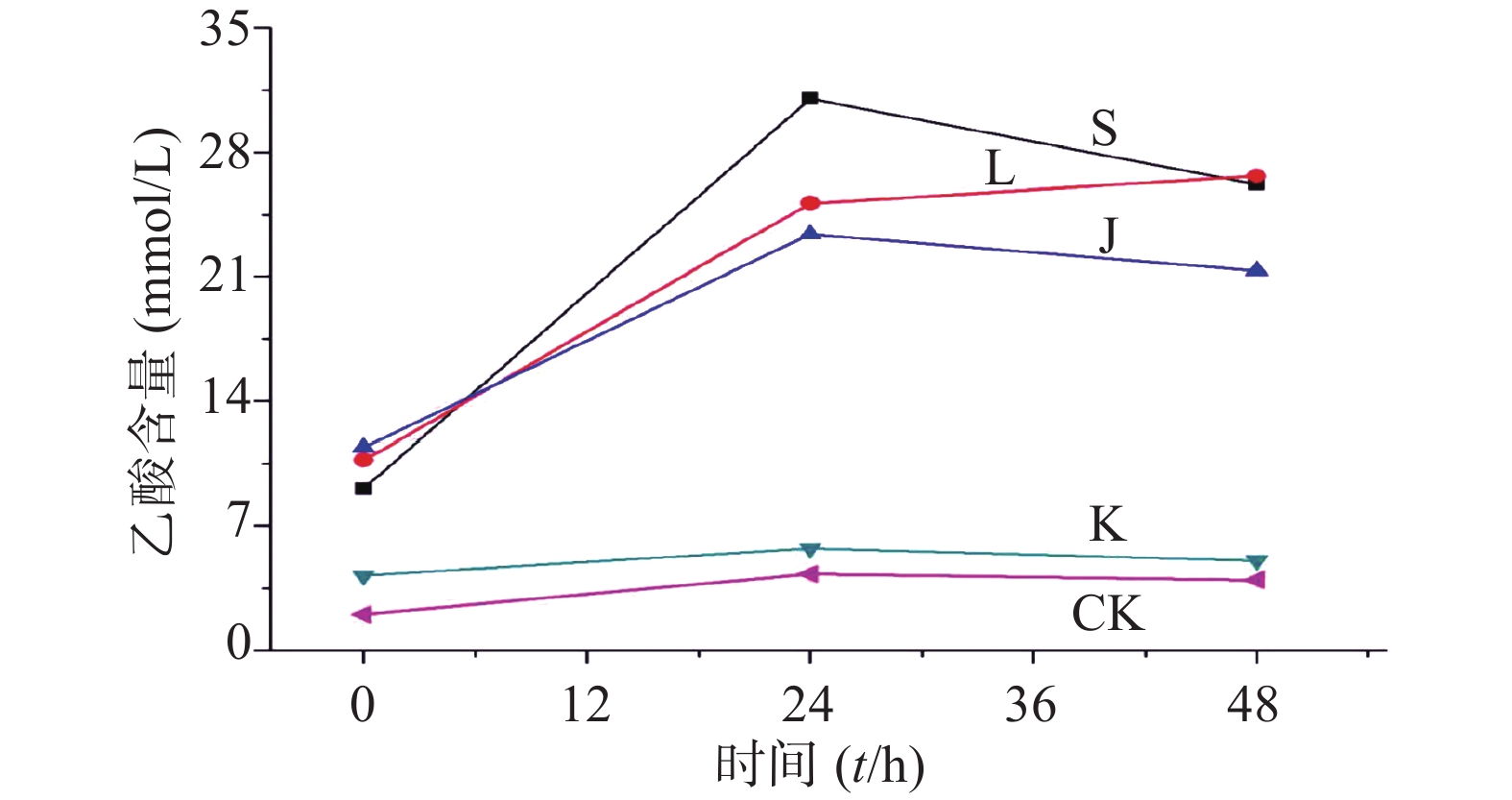
生山楂和焦山楂加速生长期双歧杆菌的生长繁殖,达稳定期后,由于生山楂中多种物质被分解,菌群产生大量代谢废物,于衰亡期加速双歧杆菌的衰亡;由于焦山楂中多种物质被分解,菌群产生大量代谢废物,于衰亡期加速双歧杆菌的衰亡;但因焦山楂中存在类黑素且其他物质较少,衰亡速率慢于生山楂组;类黑素加速生长期双歧杆菌的生长繁殖,但由于无其他物质,其生长速率慢于生山楂组,但在衰亡期中明显改变双歧杆菌生长规律,使生长期延长(生长速率变缓),双歧杆菌衰亡延后,如图2。
2.3 山楂饮片及类黑素对大肠杆菌体外生长的影响
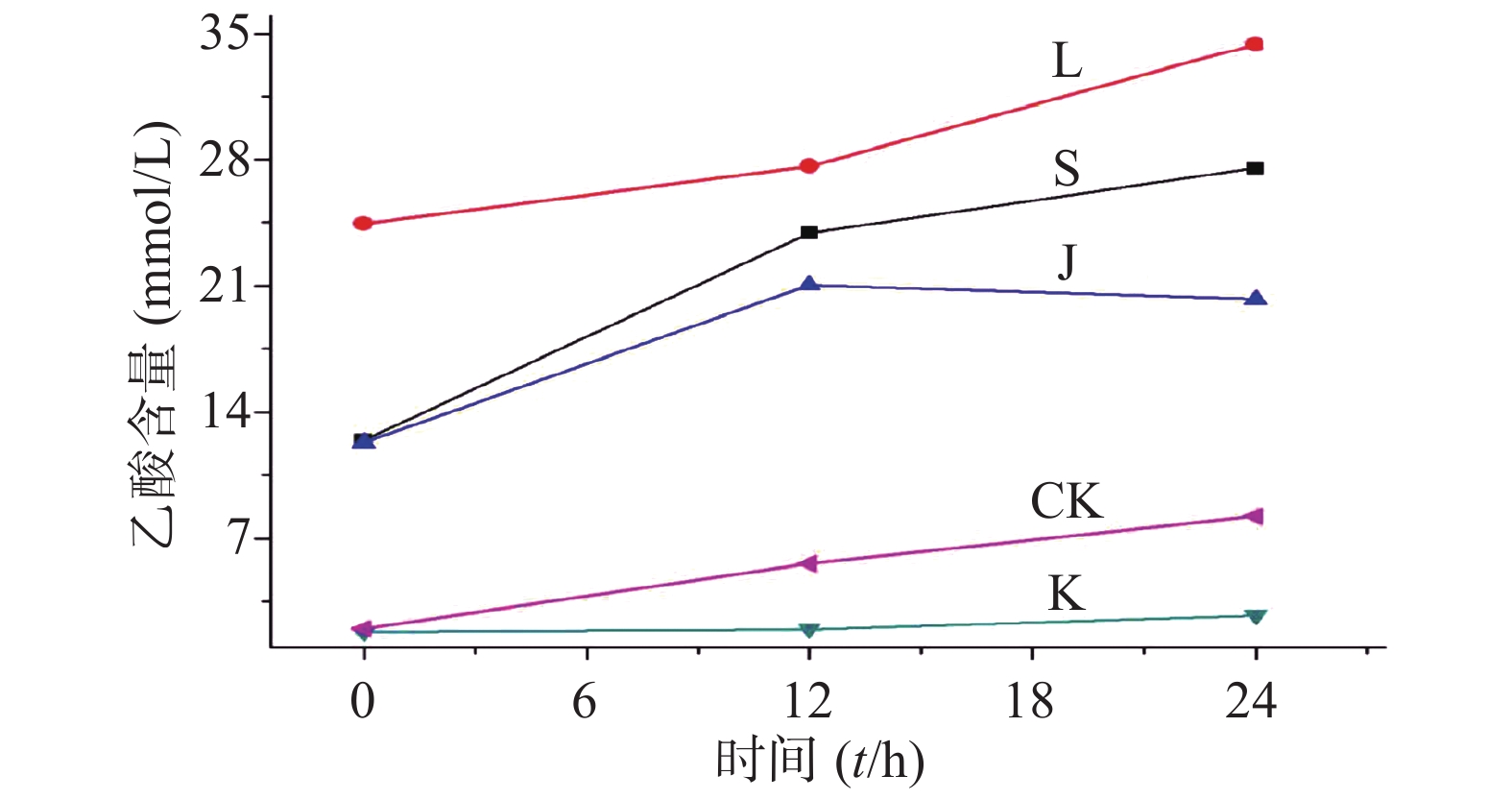
生山楂促进大肠杆菌生长期前期的生长繁殖,但由于代谢废物的逐渐增加,乙酸堆积,使生长速率逐渐变缓;焦山楂促进大肠杆菌生长期前期的生长繁殖,但由于类黑素及代谢废物的影响使生长期变短,稳定期提前;类黑素对大肠杆菌生长期前期无明显影响,但生长期后期明显促进大肠杆菌的生长繁殖,如图3所示。
3. 讨论
3.1 焦山楂炮制工艺研究
《中国药典》一部中对焦山楂炮制方法为:取净山楂,中火条件下炒至药材表面焦褐色,内部焦黄色,并具有焦香气味。因无可控工艺参数,焦山楂炮制过程中易出现饮片表面以及内部颜色不均一,山楂炒制成品质量不稳定等情况。结合课题组前期实验,采用分别100、150、200和250 g净山楂为炮制对象,中火条件为(340~380)℃、(380~420)℃和(420~460)℃,炮制时间为8、10、12和14 min;不同质量同一批号的净山楂在不同的中火条件下炮制不同的时间,采用非接触式红外测温仪检测炒制温度,并以炒锅初温和山楂药材炒制末温辅助控温。实验筛选出150 g净山楂中火条件(380~420)℃下炒制10 min,可得到质量稳定,颜色均一的焦山楂。
3.2 焦山楂类黑素提取工艺研究
类黑素的提取方法主要是水浸提法,Borrelli等[8]在90 ℃条件下,采用1:6料液比,对咖啡中的类黑素进行水提;Langner等[9]在室温条件下采用1:12料液比,水浸提1 h,提取到土豆类黑素粗制品。类黑素成分复杂,提纯困难。目前,主要的纯化方法有大孔树脂、超滤和凝胶层析等方法。何健[10]等发现X-5大孔树脂是曲霉型豆豉类黑素的最佳吸附树脂。秦礼康等[11]利用S-8树脂分离得到豆豉两个类黑素组分。本实验在水浸提法的基础上进行改良,最终获得最优提取工艺。结果显示类黑色素在420 nm处有较强吸收[12]。
3.3 气相色谱条件的筛选
实验采用气相色谱法检测菌群代谢物乙酸的含量。参照文献[13-14],结果显示其色谱条件对于本样品分析效果不佳;在柱温选择中,恒温法对乙酸检测效果不理想,峰形不稳定,因此实验采取梯度升温。经反复试验,最终获得正文中的检测参数,分离效果好,可作为本实验乙酸检测条件。
-
表 1 纳入文献的基本特征表
纳入研究 例数 临床诊断 干预措施 疗程(周) 结局指标 试验组 对照组 试验组 对照组 范学峰2019[11] 45 45 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ① Xue2016[12] 290 181 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ①③ 胡爱萍2016[13] 43 43 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ②③ 霍结容2015[14] 50 50 RE A:10 mg,1 次/d B:40 mg,1 次/d 4 ②③ 牛省利2013[15] 143 137 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ② 艾冬华2013[16] 40 40 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ①② 宋芳2012[17] 60 60 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ①②③ 郭永谊2012[18] 35 34 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ②③ 李东复2011[19] 43 35 RE A:10 mg,1 次/d B:40 mg,1 次/d 8 ②③ RE:反流性食管炎;A 代表艾普拉唑肠溶片; B 代表艾司奥美拉唑肠溶片;①内镜下有效率;②临床症状缓解率;③不良反应 -
[1] KATZ P O, GERSON L B, VELA M F. Guidelines for the diagnosis and management of gastroesophageal reflux disease[J]. Am J Gastroenterol,2013,108(3):308-328. doi: 10.1038/ajg.2012.444 [2] ZACHARIAH R A, GOO T, LEE R H. Mechanism and pathophysiology of gastroesophageal reflux disease[J]. Gastrointest Endosc Clin N Am,2020,30(2):209-226. doi: 10.1016/j.giec.2019.12.001 [3] Iwakiri K, Kinoshita Y, Habu Y, et al. Evidence-based clinical practice guidelines for gastroesophageal reflux disease 2015[J]. J Gastroenterol,2016,51(8):751-767. doi: 10.1007/s00535-016-1227-8 [4] EL ROUBY N, LIMA J J, JOHNSON J A. Proton pump inhibitors: from CYP2C19 pharmacogenetics to precision medicine[J]. Expert Opin Drug Metab Toxicol,2018,14(4):447-460. doi: 10.1080/17425255.2018.1461835 [5] IWAKIRI K. Treatment strategy for standard-dose proton pump inhibitor-resistant reflux esophagitis[J]. J Nippon Med Sch,2017,84(5):209-214. doi: 10.1272/jnms.84.209 [6] 刘腾, 徐春敏, 赵志刚. 新型质子泵抑制剂艾普拉唑的综合评价与临床应用进展[J]. 药品评价, 2016, 13(22):8-12. doi: 10.3969/j.issn.1672-2809.2016.22.002 [7] DE BORTOLI N, MARTINUCCI I, GIACCHINO M, et al. The pharmacokinetics of ilaprazole for gastro-esophageal reflux treatment[J]. Expert Opin Drug Metab Toxicol,2013,9(10):1361-1369. doi: 10.1517/17425255.2013.813018 [8] 李婷, 赵紫楠, 胡欣, 等. 艾普拉唑肠溶片治疗十二指肠溃疡的快速卫生技术评估[J]. 中国药学杂志, 2020, 55(13):1111-1116. [9] ZHANG J X, GE L, HILL M, et al. Standard-dose proton pump inhibitors in the initial non-eradication treatment of duodenal ulcer: systematic review, network meta-analysis, and cost-effectiveness analysis[J]. Front Pharmacol,2019,9:1512. doi: 10.3389/fphar.2018.01512 [10] LUNDELL L R, DENT J, BENNETT J R, et al. Endoscopic assessment of oesophagitis: clinical and functional correlates and further validation of the Los Angeles classification[J]. Gut,1999,45(2):172-180. doi: 10.1136/gut.45.2.172 [11] 范学锋. 艾普拉唑对反流性食管炎临床治疗价值分析[J]. 人人健康, 2019(22):225. [12] XUE Y, QIN X H, ZHOU L Y, et al. A randomized, double-blind, active-controlled, multi-center study of ilaprazole in the treatment of reflux esophagitis[J]. Clin Drug Investig,2016,36(12):985-992. doi: 10.1007/s40261-016-0446-3 [13] 胡爱萍, 李娜. 艾普拉唑治疗反流性食管炎的疗效与药物经济学分析[J]. 蛇志, 2016, 28(1):47-48. doi: 10.3969/j.issn.1001-5639.2016.01.023 [14] 霍结容. 艾普拉唑治疗反流性食管炎临床效果观察及药物经济学研究[J]. 广东微量元素科学, 2015, 22(6):56-59. doi: 10.16755/j.cnki.issn.1006-446x.2015.06.008 [15] 牛省利. 艾普拉唑治疗反流性食管炎的疗效观察[J]. 中国实用医药, 2013, 8(19):186-187. doi: 10.3969/j.issn.1673-7555.2013.19.134 [16] 艾冬华. 艾普拉唑治疗反流性食管炎临床效果观察及药物经济学分析[J]. 中国基层医药, 2013, 20(19):2902-2904. doi: 10.3760/cma.j.issn.1008-6706.2013.19.010 [17] 宋芳, 何辉, 沈磊, 等. 艾普拉唑治疗反流性食管炎180例的疗效及安全性[J]. 中国新药杂志, 2012, 21(8):905-907. [18] 郭永谊, 祁真, 苟新敏, 等. 艾普拉唑治疗反流性食管炎的药物经济学评价[J]. 中国药物评价, 2012, 29(3):235-236. doi: 10.3969/j.issn.2095-3593.2012.03.015 [19] 李东复, 陈永胜, 马静婷, 等. 艾普拉唑治疗反流性食管炎的临床研究[J]. 中华消化杂志, 2011, 31(4):264-265. doi: 10.3760/cma.j.issn.0254-1432.2011.04.012 [20] HERREGODS T V K, BREDENOORD A J, SMOUT A J P M. Pathophysiology of gastroesophageal reflux disease: new understanding in a new era[J]. Neurogastroenterol Motil,2015,27(9):1202-1213. doi: 10.1111/nmo.12611 [21] KIL B J, KIM I W, SHIN C Y, et al. Comparison of IY81149 with omeprazole in rat reflux oesophagitis[J]. J Auton Pharmacol,2000,20(5-6):291-296. doi: 10.1046/j.1365-2680.2000.00192.x [22] PERICLOU A P, GOLDWATER R, LEE S M, et al. A comparative pharmacodynamic study of IY-81149 versus omeprazole in patients with gastroesophageal reflux disease[J]. Clin Pharmacol Ther,2000,68(3):304-311. doi: 10.1067/mcp.2000.109155 [23] SONG I J, KIM H K, LEE N K, et al. Prospective single arm study on the effect of ilaprazole in patients with heartburn but no reflux esophagitis[J]. Yonsei Med J,2018,59(8):951-959. doi: 10.3349/ymj.2018.59.8.951 [24] HIGUCHI K, JOH T, NAKADA K, et al. Is proton pump inhibitor therapy for reflux esophagitis sufficient?: a large real-world survey of Japanese patients[J]. Intern Med,2013,52(13):1447-1454. doi: 10.2169/internalmedicine.52.0349 [25] WANG R X, WANG J, HU S Q. Study on the relationship of depression, anxiety, lifestyle and eating habits with the severity of reflux esophagitis[J]. BMC Gastroenterol,2021,21(1):127. doi: 10.1186/s12876-021-01717-5 [26] HUNGIN A P S, MOLLOY-BLAND M, SCARPIGNATO C. Revisiting Montreal: new insights into symptoms and their causes, and implications for the future of GERD[J]. Am J Gastroenterol,2019,114(3):414-421. doi: 10.1038/s41395-018-0287-1 [27] JAVADI S A H S, SHAFIKHANI A A. Anxiety and depression in patients with gastroesophageal reflux disorder[J]. Electron Physician,2017,9(8):5107-5112. doi: 10.19082/5107 [28] YU Y, FANG D, FAN L, et al. Efficacy and safety of esomeprazole with flupentixol/melitracen in treating[J]. J Gastroenterol Hepatol,2014,29(6):1200-1206. doi: 10.1111/jgh.12552 [29] YOSHIDA N, KAMADA K, TOMATSURI N, et al. Management of recurrence of symptoms of gastroesophageal reflux disease: synergistic effect of rebamipide with 15mg lansoprazole[J]. Dig Dis Sci,2010,55(12):3393-3398. doi: 10.1007/s10620-010-1166-9 -





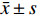
 下载:
下载:
 下载:
下载: