-
心脑血管疾病是心脏血管和脑血管疾病的统称,泛指由于高脂血症、血液黏稠、动脉粥样硬化、高血压等所导致的心脏、大脑及全身组织发生的缺血性或出血性疾病。心脑血管疾病是一种严重威胁人类健康的常见病,具有高患病率、高致残率和高死亡率的特点。这种疾病也对我国人民的健康和医疗卫生事业的发展带来了巨大的挑战。而在心脑血管疾病中,又以缺血性心脏病和缺血性脑卒中最为常见[1-3]。
黄酮类化合物(flavonoids)是一类广泛存在于自然界植物中的次生代谢产物。是一种以黄酮(2-苯基色原酮)为母核而衍生的一类黄色色素,其中包括黄酮的同分异构体及其氢化和还原产物[4]。它在植物的生长、发育、开花、结果以及抗菌防病等方面起着重要的作用。本文将对目前黄酮类化合物抗心脑血管疾病的作用研究进展作一综述。
-
早在1938年,Szent-Gyorgyi等研究发现来自于柠檬的黄酮类化合物橘皮苷具有强化毛细血管的作用,该项功能将有助于改善心脏微循环的水平,从而产生保护作用[5]。此后,一项名为Zutphen Elderly Study的流行病学研究探讨了膳食类黄酮摄取量与冠心病风险之间的相关性。该研究对65岁至84岁的老年男性黄酮类摄取量进行了统计,结果显示膳食类黄酮摄取量与冠心病引起的死亡之间呈明显负相关,同时与心梗发病率之间也呈弱负相关 [6]。在欧洲,荷兰科学家对黄酮醇类和黄酮类摄入量与冠心病死亡率和中风发生率之间做了分析,结果显示摄入量大于30 mg/d者两种疾病的发病风险仅为摄入量最低者的三分之一,且该项调查已排除了高胆固醇、高血压、饮酒、吸烟等心脑血管疾病常见危险因素的影响。而另一项针对饮茶人群的研究表明茶叶中富含的茶叶类黄酮可以很好地预防缺血性心脏病的发生 [7]。这些研究均提示我们黄酮类物质可能发挥较强的抗氧化作用,从而降低冠心病的发病率和死亡率。
-
与心肌缺血类似,缺血性脑卒中同样严重威胁人类的生命健康。而与心肌缺血不同的是,损伤部位是人类神经行为的中枢—脑组织,因此,临床表现更为复杂。黄酮类化合物作为一种常见且重要的中药成分被较多的实验证明其具有抗缺血性脑卒中的作用。
研究表明从中药灯盏细辛中提取出来的黄酮类活性成分灯盏花素可以起到抗脑缺血的作用,其作用主要通过改善血液流变学、缩小脑组织梗死面积以及减少脑海马区域细胞凋亡数来实现[8-9]。此外,本课题组从传统中药中提取出来的黄酮类活性成分菸花苷,在实验中被证明同样具有确切的保护脑缺血损伤的作用。实验中急性脑缺血的大鼠在注射菸花苷后其生存率较对照组有大幅提升,同时缺血梗死面积显著缩小[10-11],在各个时间点对给药组和对照组进行神经行为学评价如mNSS评分、提尾实验等,发现注射菸花苷的大鼠其行为学得分逐渐降低,提示神经功能逐渐趋向好转。此外,该实验还对各组大鼠脑电图和脑组织含水量进行了测定,结果表明,给予菸花苷治疗的大鼠脑电图消失的时间显著延长,同时其脑组织含水量显著降低,改善了脑水肿情况 [12]。证实了菸花苷对动物的实验性脑梗塞及缺血后再灌注引起的组织损伤有明显的预防和治疗作用。
-
研究发现,缺血性心脏病和缺血性脑卒中的病理机制类似,可以归纳为氧化性损伤、钙超载、炎症反应、细胞凋亡及血小板凝集、自噬等。这几种因素之间相互作用,相互影响,形成多个复杂的调控网络,从而造成一系列病理级联反应。而黄酮类化合物可以通过对上述各因素的抑制作用来保护损伤的心肌组织和脑组织。
-
现代医学研究表明,在心肌缺血发生时,人体内会产生较多的氧自由基,同时机体清除氧自由基的能力下降,使得堆积的氧自由基在心肌细胞中发生过氧化反应,从而破坏心肌细胞的结构和功能,导致心肌缺血进一步加重[13]。研究发现,超氧化物酶(SOD)作为生物体内清除自由基的首要物质,可减弱氧自由基对细胞造成的损伤,同时还具有修复受损细胞的功能,其活性高低可反映机体清除自由基能力的大小[14];丙二醛(MDA)则作为脂质过氧化物反应的产物,常被用于评价机体氧化应激损伤的严重程度[15];一氧化氮(NO)是我们熟知的生物体内反应极强的自由基,在机体发生心肌缺血时,该物质在血清中的水平明显下降。实验表明,葡萄籽中富含的原花色素可以有效地清除自由基,从而稳定心肌细胞膜,对心肌产生保护作用[16-17]。另一项研究以异丙肾上腺素作为诱导的急性心肌缺血大鼠为模型,探索了布渣叶总黄酮对心肌缺血的作用,结果显示,布渣叶总黄酮可明显降低大鼠血清中乳酸脱氢酶(LDH)、肌酸激酶(CK)以及心肌组织中MDA的含量,同时心肌组织中SOD和NO的活性也得到提高[18]。揭示了黄酮类化合物通过抗氧化作用来产生保护心肌组织的作用。
近年来,氧化应激学说同样也在脑缺血性疾病中被广泛研究。该机制不仅可以直接造成细胞破坏,使脑细胞坏死,还可以通过介导线粒体途径,神经细胞膜结构以及DNA修复酶和转录因子等间接地导致脑细胞凋亡。研究发现,注射天然黄酮类化合物木犀草素的脑缺血大鼠SOD、过氧化氢酶(CAT)活性相较于对照组明显提升,而MDA的含量则显著降低,该结果提示我们木犀草素可以加强机体清除氧自由基的能力,从而产生脑保护作用[19]。而在另一项体外研究中,中药黄芩中的黄酮类化合物黄芩苷可以抑制外源性和内源性过氧亚硝基阴离子诱导的神经毒性作用,保护人源神经母细胞瘤细胞(SH-SY5Y)神经细胞系[20]。同时,从传统中药红花中提取出来的黄酮类成分菸花苷,也在此前的实验中被证实可以显著降低脑组织中MDA的含量,提高SOD活性[12]。以上结果表明,黄酮类化合物发挥抗心肌缺血及脑缺血的作用与提高机体抗氧化应激的能力有密切的关系。
-
炎症反应广泛地存在于各种疾病的病理机制中,其主要通过致炎因子和炎性介质来介导一系列的链式反应。当炎症反应发生在缺血的心肌细胞时,会进一步加剧细胞的缺血和缺氧 [21]。在炎症反应中,具有代表性的重要炎症因子有白介素家族,如IL-1β、IL-6以及肿瘤坏死因子(TNF-α)等,这些炎症因子多出现在炎症反应通路的下游,直接影响并加剧炎症反应的发生和发展。而另一种重要的转录因子Kappa-B(NF-κB),作为一种氧化还原敏感因子在炎症反应中同样扮演了重要的角色,其介导的一系列炎症因子如上述的白介素家族、趋化因子、炎性小体等在心肌细胞缺血损伤中起到重要的作用[22-24]。以往的研究表明,香青兰总黄酮可以抑制心肌缺血大鼠心肌组织中的炎症因子白介素IL-1、IL-6和TNF-α的水平,使炎症因子减少释放,从而降低心肌组织中中性粒细胞的浸润,以达到保护心肌的作用[25]。另一项研究也发现,银杏黄酮同样可以抑制心肌组织中中性粒细胞的浸润,其作用主要通过下调NF-κB和细胞间黏附因子-1(ICAM-1)的表达来实现[26]。
与此类似,在机体发生缺血性脑卒中的时候,各类炎症因子依然扮演了重要的角色。研究发现,灯盏细辛在治疗脑梗死时可以显著降低TNF-α、IL-6的含量,从而减轻炎症反应[27]。在另一项对黄酮类化合物山奈酚的研究中发现,其抗炎作用已在细胞层面得到了证实。它可降低促炎因子的产生和mRNA表达,如胸腺基质淋巴细胞生成素(TSLP)、IL-8等[28],此外,在以PC12细胞作为研究对象的体外实验中,人们发现加入山奈酚处理后,该组细胞的炎性相关蛋白环氧化酶(COX2),诱导型一氧化氮合酶(iNOS)以及核因子NF-κB水平明显下调,且细胞活力随着的山奈酚的浓度增加而逐步增长;进一步的检测发现,对照组的磷酸化P38丝裂原活化蛋白激酶(P38-MAPK)表达升高,而山奈酚组表达降低,而当加入P38-MAPK抑制剂后发现对照组的炎性相关蛋白水平降低[29],该结果提示我们黄酮类化合物山奈酚可以通过抑制P38-MAPK信号通路来对抗机体病理性炎症反应[30],进而产生脑细胞保护作用。由此可见,黄酮类化合物主要通过影响炎症因子的表达和释放来发挥抗炎的作用。
-
细胞凋亡又称为程序性细胞死亡,是机体为了维持内环境稳定,通过基因控制的细胞自主而有序的死亡,涉及了一系列的基因激活、表达以及调控作用,与各种信号通路、免疫应答以及上述提到的炎症反应有着密不可分的联系。细胞凋亡是心肌缺血再灌注损伤的重要病理机制之一。目前与细胞凋亡相关的基因有Bcl-2家族,Caspase家族等,相关通路有NF-κB信号通路、丝裂原活化蛋白激酶MAPK信号通路、磷脂酰肌醇-3激酶/蛋白激酶B(PI3K/AKT)信号通路等。这些基因同时参与了细胞凋亡的诱发和抑制。在一项研究中发现,我国瑶族传统草药成分铜钻总黄酮可以明显降低已形成心肌缺血再灌注损伤的大鼠心肌组织中Bax蛋白的表达,该蛋白可以促进细胞凋亡,同时实验还发现铜钻总黄酮还可以升高抗凋亡的Bcl-2蛋白的表达,从而抑制细胞凋亡,避免心肌缺血再灌注损伤的进一步加重[31]。在另一项研究中,科研人员发现来源于印度崖豆的黄酮类化合物不仅可以降低Bax蛋白的表达,升高Bcl-2蛋白的表达,还可以提升心肌组织中结构氮氧化合成酶(cNOS)的活性,同时抑制诱生型一氧化氮合酶(iNOS)活性,从而显著改善心肌缺血再灌注大鼠的心肌组织病理学形态,其实验组的心肌细胞形态、结构和排列较之对照组更为完整和规律[32]。同时在MAPK信号通路中c-Jun氨基末端激酶(JNK)和P38蛋白激酶可促进细胞的凋亡。研究发现玫瑰中黄酮类化合物可显著下调大鼠心肌组织中磷酸化JNK和P38的表达,从而抑制心肌细胞的凋亡 [33]。而另一条重要的信号转导通路PI3K/AKT在细胞的增殖、凋亡、代谢中也发挥了重要的生物学作用,其可抑制细胞凋亡的进程[34]。其中活化的AKT进入细胞质与细胞核后,可以调节Caspase家族中Caspase-3的表达,同时还可以调节内皮型一氧化氮(eNOS)以及抗凋亡因子Bcl-2和促凋亡因子Bax的表达[35-36]。实验发现,玉郎伞查尔酮可以激活PI3K/AKT信号通路,抑制大鼠心肌细胞的凋亡,从而产生抗心肌缺血的作用[37]。此外,有研究表明黄芩茎叶总黄酮可以降低发生心肌缺血再灌注损伤的大鼠心肌细胞的凋亡率,其作用可能与降低Caspase-3基因mRNA和蛋白表达有关[38-39]。
细胞凋亡同时也是缺血性脑卒中发生发展的一个重要病理机制。临床研究发现,认知障碍是缺血性脑卒中发病后的一项重要并发症,它严重影响患者的预后和生活质量。因此,大脑中负责学习记忆和认知的海马区成为了科学家们重点关注的对象。其中CA1区的神经元对脑缺血缺氧较为敏感,容易受到损伤,而CA3区及DG区的神经元则相对耐受[40]。尼氏体是神经元胞体和树突内的嗜碱性颗粒或小斑块,由游离的核糖体和粗面内质网构成,对缺血变化非常敏锐[41]。课题组在对黄酮类化合物菸花苷的一项研究中发现,缺血再灌注的大鼠海马区神经元大小不一,胞质不规则淡染,胞核皱缩变形,部分细胞脱失明显,CA1区锥体细胞和 DG区的颗粒细胞排列松散,CA3区锥体细胞排列散乱,表明大鼠发生急性脑缺血再灌注损伤后神经细胞受损严重,与之相比,使用菸花苷处理的MCAO大鼠神经元虽也出现了细胞淡染,大小不均,部分胞体肿胀,CA1区及DG区排列稍显混乱,但整体的形态接近正常,病理损伤明显减轻。同时,在尼氏体方面,模型组整体淡染,皮层的尼氏体大大减少,海马区尼氏体极少,表明造模后神经元功能受到损伤。与模型组相比,菸花苷组皮层尼氏体数目更多,个体更大,染色较均匀,海马区尼氏体虽多为颗粒状,个体稍小,但数目明显增多,说明神经元蛋白合成有所增加,较为活跃[42]。因此,我们可以得出结论,菸花苷通过促进神经元蛋白的合成,抑制神经细胞的凋亡,保持神经元的活性来提高机体抗脑缺血的功能。同样,黄芩苷在用于脑缺血动物模型时,也可以明显改善实验动物的认识记忆能力[43],还通过下调促凋亡基因Bax的表达,下调Bax/Bcl-2的比值,降低COX-2的表达来抑制神经细胞凋亡[44]。以上研究表明,黄酮类化合物通过抑制细胞凋亡来进一步保护心脑组织免受缺血再灌注的损伤。
-
研究发现,当心肌发生缺血时,心肌细胞线粒体中Na+/K+-ATP酶和Ca2+-ATP酶活性下降,使线粒体对钙离子的摄入减少,同时包浆内的钠离子含量升高,造成Na+ -Ca2+交换增加,从而发生钙超载 ,加重心肌缺血的临床症状[45]。研究发现,玉郎伞黄酮能够提高心肌组织中的Na+/K+-ATP酶和Ca2+-ATP酶活性,减轻细胞内钙离子超载的程度,改善缺血再灌注造成的心肌损伤[46];从传统中药香青兰中提取的香青兰总黄酮也可以提高心肌组织中的ATP酶含量,保持线粒体的活性和结构完整性,使其功能得到发挥,从而抑制钙超载的发生[47]。
-
在正常的生理状态下,血栓素花生四烯酸(TXA2)与环前列腺素(PGI2)处于一种相对平衡的状态。而在心肌受到缺血再灌注损伤后,该平衡即被打破。此时,心肌内皮细胞受损,导致PGI2合成减少而TXA2作用增强,进一步引起血小板大量聚集,从而加重心肌缺血的程度。研究表明,黄酮类化合物可以发挥抗血小板聚集的作用。如从黄顶茜草中分离出的硫酸黄酮能够阻断TXA2受体而发挥抗血小板凝集的作用 [48]。同样的,白桂芦苇中的黄酮类化合物也可以抑制血小板的聚集,从而起到保护心肌的作用[49]。上述现象的发生机制可能与黄酮类化合物抑制环氧合酶,提高血小板环磷酸腺苷(cAMP)合成,阻断TXA2受体,提高PGI2水平有着直接的联系。
-
自噬是近几年科学界的一个研究热点,其因开启细胞循环自身物质的新纪元而备受全世界的关注 [50-52]。自噬根据发生过程分为三类:巨自噬,微自噬,分子伴侣介导的自噬。目前研究一般集中于巨自噬,其一般过程为:自噬前体的形成,自噬前体延长包裹底物形成自噬小体,自噬小体与溶酶体融合形成自噬溶酶体最终降解[53-55]。在脑卒中的发生过程中,自噬起到了关键的保护作用。课题组在MCAO大鼠模型中发现菸花苷可以增加大鼠脑缺血再灌注后缺血半暗带的自噬小体数目,增强LC3的表达,提高活性形式 LC3-II 在LC3表达中所占的比例,增强参与吞噬泡形成的重要相关蛋白 BECN1 蛋白的表达,降低参与自噬溶酶体降解的重要蛋白 SQSTM1 蛋白的表达,降低自噬相关通路雷帕霉素靶蛋白依赖性途径中关键蛋白 phospho-mTOR 的表达,上调 BECN1、Atg7 mRNA 的表达,下调SQSTM1mRNA的表达。由此可知,菸花苷对大鼠脑缺血再灌注后缺血半暗带的自噬水平有促进作用。同时在体外,在人源神经母细胞瘤细胞(SH-SY5Y)细胞株上建立模拟体内缺血再灌注的缺复氧模型,结果显示,菸花苷同样可以增加SH-SY5Y细胞内自噬小体的生成,增加LC3的表达,提高自噬体膜标志性蛋白LC3-II表达含量,增强BECN1蛋白的表达,降低SQSTM1蛋白的表达,增强促进细胞内自噬流的进程[42, 56]。由此可知,黄酮类化合物菸花苷可通过自噬来发挥神经保护作用。
-
黄酮类化合物作为一种常见的天然化合物,存在于自然界的许多植物以及传统中药中。随着科学技术的进步,人们发现这类化合物具有诸多的生物活性,而其强大的药理作用也屡见报道。如降低血管的脆性,改善血管的通透性、降低血脂和胆固醇,防治老年高血压、脑溢血、冠心病、心绞痛、扩张冠状血管,增加冠脉流量等。在这些药理作用中,其抗心脑缺血的作用对于临床上治疗和预防相关疾病显得尤为重要。在上文中,我们列举了许多不同种类的黄酮类化合物在心脑血管疾病中的作用,这些活性成分有的可以直接通过改善血管通透性、缩小梗死组织面积来保护心脑血管组织,有的则通过分子信号通路来产生保护作用。随着研究的推进,它们的作用机制也进一步地得到阐释。可以肯定的是,黄酮类化合物能够为人类治疗和预防心脑血管疾病提供新的治疗思路。当然目前很多实验仅涉及到分子机制中的某个环节,而对于完整的调控过程,精准的作用靶点还有待研究发现。只有通过这一系列系统科学的研究,才能够更好地为心脑血管疾病的治疗提供理论依据,从而进一步在临床得到广泛的应用。
Research progress of the effect of flavonoids on cardiovascular and cerebrovascular ischemic diseases
-
摘要: 黄酮类化合物是一种广泛存在于传统中药中的次生代谢产物,拥有许多生物活性和药理作用。近年来,研究发现黄酮类化合物可以通过多种途径在缺血性脑卒中和缺血性心脏病的治疗中发挥有效的保护作用,同时对于其保护作用的机制也有了较为详细系统的阐释。比如黄酮类化合物可以在抗氧化、抑制炎症反应、细胞凋亡和自噬等病理生理机制中发挥有效作用。本文通过查阅国内外的相关文献,对黄酮类化合物抗心脑血管缺血性疾病的保护作用及其机制进行综述。旨在为抗心脑血管疾病药物的研究开发提供参考。Abstract: Flavonoids are secondary metabolites that widely existing in traditional Chinese medicine. They have many biological activities and pharmacological effects. In recent years, studies have found that flavonoids can play an effective protective role in the treatments of ischemic stroke and ischemic heart disease through various ways. The mechanisms of their protective effects have been systematically explained in detail. For example, flavonoids can affect pathophysiological mechanisms such as antioxidant, inhibition of inflammatory response, apoptosis and autophagy pathway. This paper reviews the protective effect and mechanisms of the treatments of flavonoids on cardiovascular and cerebrovascular ischemic diseases by referring to relevant literatures. The purpose is to provide reference for future research and development of drugs for the treatments of cardiovascular and cerebrovascular diseases.
-
Key words:
- flavonoids /
- ischemic heart disease /
- ischemic stroke /
- protective effect /
- mechanism of action
-
免疫介导的炎性眼前段疾病(immune-mediated inflammatory anterior ocular diseases,IIAODs)如春季结膜炎、前葡萄膜炎等是临床上较常见的眼科疾病。局部或全身性使用类固醇是控制这类疾病炎症的主要手段。然而,长期使用类固醇可能会导致白内障、青光眼等,从而存在失明的可能。因此,眼科临床越来越频繁地局部使用免疫抑制剂来治疗这类疾病。
他克莫司(tacrolimus,FK506)作为第二代免疫抑制剂代表性药物,是治疗IIAODs的主要方式之一[1-3]。目前国内上市的FK506眼用制剂为日本千寿药业生产的Talymus®,其药效容易受到泪液冲刷的影响而降低。因此,本研究研制了他克莫司阳离子微乳凝胶(FK506-loaded cationic nanoemulsion-based in-situ gel, FK506 CNE GEL),旨在利用该剂型的特性,延长药物在眼部的滞留时间,提高生物利用度,减少给药频次。本文通过HE染色处理的兔眼组织病理切片观察FK506 CNE GEL的眼部刺激性,并通过建立HPLC-MS测定兔眼房水药物浓度的方法,考察其房水药动学。
1. 材料
1.1 仪器
Agilent 1100型高效液相色谱系统(美国安捷伦公司);AL204 电子天平(梅特勒托利多仪器有限公司);DF-101S集热式恒温加热磁力搅拌器(上海精密试验设备有限公司);NS1001L型高压均质机(意大利Niro Soavi公司);85-1型磁力搅拌器(上海志成电器有限公司);CX31光学显微镜(Olympus Corporation);JY92-2D超声波细胞粉碎机(宁波新芝生物科技股份有限公司);H1850R型台式高速冷冻离心机(湖南湘仪实验室仪器开发有限公司);SCIEX QTRAP® 5500 型高压快速液相色谱-三重串联四级杆质谱联用仪(美国AB SCIEX公司)。
1.2 药物与试剂
他克莫司对照品(含量99.3%,福建科瑞药业有限公司);子囊霉素对照品(含量99.5%,上海齐奥化工有限公司);蓖麻油(湖南宏康制药股份有限公司);中链脂肪酸甘油酯(铁岭北亚药用油有限公司);吐温-80(四川金山制药有限公司);泊洛沙姆407、泊洛沙姆188(德国BASF提供);西他氯胺(Sigma-Aldrich);甘油(湖南尔康制药有限公司);注射用水(明澈D24UV);甲醇(上海科丰实业有限公司);他克莫司滴眼液(Talymus®,日本千寿制药株式会社);0.9%氯化钠注射液(国药集团化学试剂有限公司);戊巴比妥钠(Merck 分装);盐酸丙美卡因滴眼液(爱尔凯因®,美国爱尔康眼药厂比利时分厂);其他药品和试剂均为药用规格或分析纯。
1.3 动物
新西兰白兔,雌雄兼用,2.5~3.0 kg,上海斯莱克实验动物有限公司。实验前24 h自由进食、饮水,进行眼部检查以确保无任何眼病。
2. 方法与结果
2.1 FK506 CNE GEL的配制
根据本研究前期报道制备FK506 CNE GEL[4]。首先以蓖麻油(4 %,W/V)、中链脂肪酸甘油酯(6 %,W/V)作为混合油相,西他氯胺(0.02 %,W/V)作为阳离子表面活性剂,吐温−80(1 %,W/V)、泊洛沙姆188(0.1 %,W/V)作为非离子表面活性剂,甘油(2.2 %,W/V)作为渗透压调节剂,通过高压均质制得FK506 CNE(0.1 %,W/V)。而后以26 %泊洛沙姆407和12 %泊洛沙姆188共同作为凝胶基质,将FK506 CNE进一步制备成FK506 CNE GEL(0.1 %,W/V)。
2.2 FK506 CNE GEL的眼部刺激性考察[5-6]
2.2.1 分组给药设计
取实验兔8只,随机分为A、B两组。采用动物同体左右侧自身对比法,A组实验兔左眼滴入FK506 CNEGEL 50 μl,右眼滴入生理盐水50 μl作为对照。B组实验兔左眼滴入市售Talymus® 50 μl,右眼滴入生理盐水50 μl作为对照。给药后使兔眼被动闭合10 s,使药液与局部有充分接触。每日给药3次,连续给药2周。
2.2.2 眼球组织病理切片
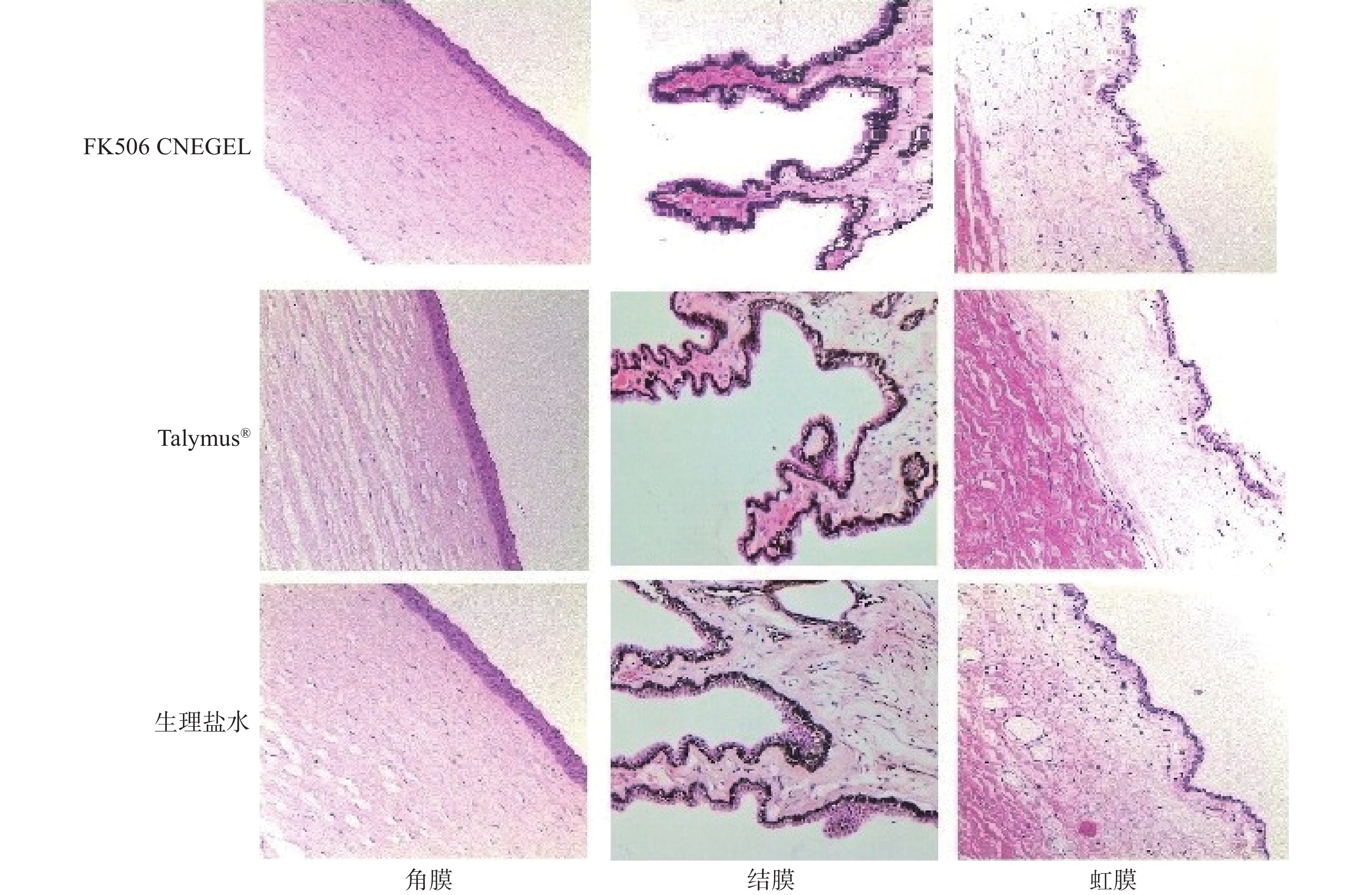
通过耳缘静脉注入空气处死实验兔后取出眼球,进行病理组织切片,详细步骤如下:① 10 %中性福尔马林固定;② 流水冲洗;③ 组织修切平面;④ 组织脱水、石蜡包埋;⑤ 石蜡组织切片;⑥ 二甲苯-无水乙醇脱蜡;⑦ 苏木素-伊红染色;⑧ 小浓度氨水返蓝;⑨ 脱水、复染、洗涤;⑩ 继续脱水后封片。光学显微镜下观察兔眼角膜,虹膜,结膜并拍照,试验结果见图1。
一般情况下,兔眼较人眼对刺激反应更为敏感。图1为显微镜下滴入FK506 CNE GEL、Talymus®及生理盐水后的兔眼角膜、虹膜及结膜结构。对比可见,滴入FK506 CNE GEL后兔眼角膜组织排列规则有序、纹理清晰;虹膜各层组织结构清晰,无明显异常;结膜组织清晰可见,未见坏死及炎性细胞浸润,与生理盐水组及Talymus®组对比无明显差异。结果表明,FK506 CNE GEL对兔眼角膜、虹膜及结膜均无明显刺激性。
2.3 FK506 CNE GEL房水药动学研究[7-10]
2.3.1 色谱条件
采用Agilent 1100型高效液相色谱仪,色谱柱为Agilent Poroshell 120 EC-C18 (2.1 mm×50 mm, 2.7 μm),流动相为甲醇-水(2 mmol/L醋酸铵)(90∶10, v/v),柱温为40 ℃,流速为0.3 ml/min,进样量为1 μl。
2.3.2 质谱条件
采用SCIEX QTRAP® 5500 型高压快速液相色谱-三重串联四级杆质谱联用仪以ESI正离子电离方式检测,扫描方式为多反应监测(MRM),扫描时间为100 ms,离子源电离电压为5 500 V,离子源温度为550 ℃,雾化气流流速为7 L/min。以上述质谱条件对FK506及子囊霉素(ascomycin ,FK520)进行离子扫描,结果如表1所示。根据扫描结果,选择m/z 821.5→768.4 作为 FK506 定量分析离子对,m/z 821.5→576.3 作为其定性分析离子对;选择m/z 809.5→756.5作为FK520定量分析离子对,m/z 809.5→564.3 作为其定性分析离子对。
表 1 FK506和FK520的质谱行为分析参数 FK506 FK520 分子量 804.2 792.4 定性分析的离子反应(m/z) 821.5→576.3 809.5→564.3 碎裂能量(CE, V) 31.2 29.0 定量分析的离子反应(m/z) 821.5→768.4 809.5→756.5 碎裂能量(CE, V) 28.0 26.1 解簇电压(DP, V) 120 45 2.3.3 房水样品的制备
精密移取房水样品30 μl置于2 ml离心管中,加入50 μl FK520内标液(100 ng/ml)及120 μl甲醇,涡旋混合,12 000 r/min离心15 min,取上清液进样分析。
2.3.4 方法专属性考察
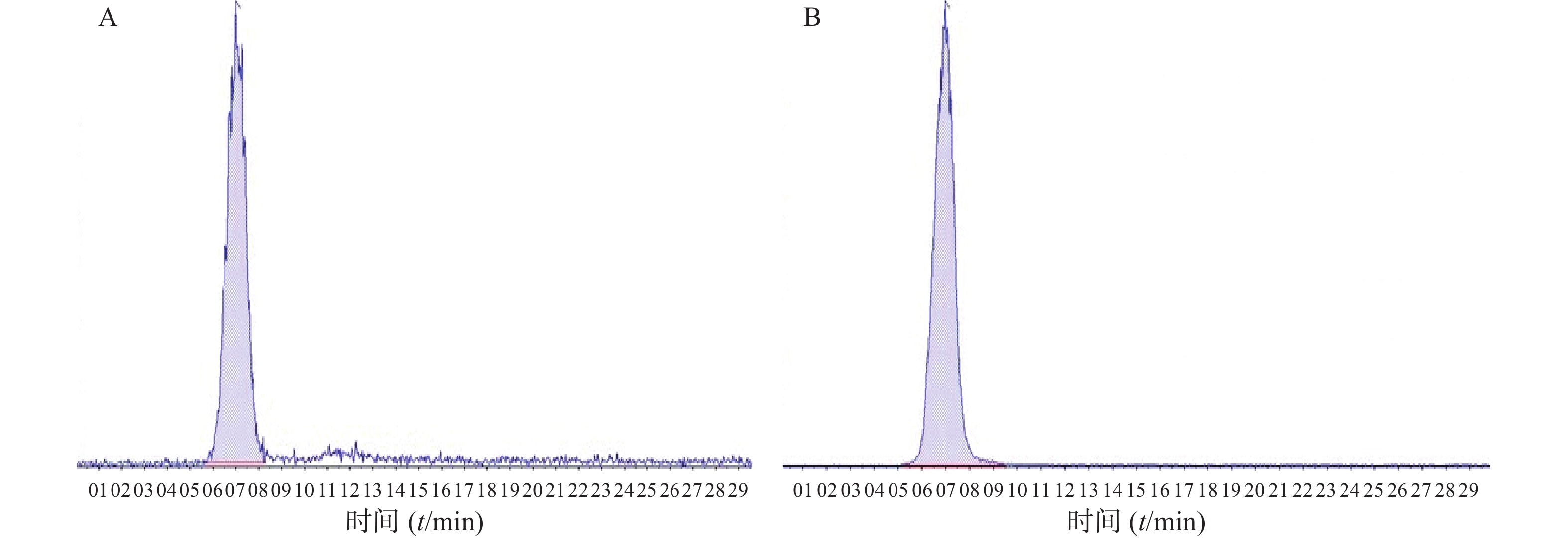
取空白房水30 μl,将一定浓度的FK506和FK520标准溶液分别加入空白房水中,按照“2.3.3”项下方法处理,记录谱图。结果如图2所示,表明房水中内源性物质对FK506的测定无干扰,方法专属性良好。
2.3.5 标准曲线和定量限
精密移取空白房水 30 μl置于2 ml离心管中,加入不同量的100 ng/ml FK506标准溶液及50 μl FK520内标液(100 ng/ml),加入甲醇使总量达200 μl制成系列浓度50、25、10、5、2.5、1、0.5 ng/ml的FK506溶液,12 000 r/min离心15 min,液质联用仪进样分析,记录对应图谱。以FK506峰面积Ai与FK520峰面积As的比值Ai/As作为纵坐标,以FK506浓度C(ng/ml)为横坐标进行线性回归,得线性回归方程:A=0.324 75C+0.05577,r=0.999 96。结果表明FK506在0.5~50 ng/ml浓度范围内线性关系良好,定量限为0.5 ng/ml。
2.3.6 方法精密度考察
配制浓度为1、10、30 ng/ml的FK506样品,按照“2.3.3”项下方法处理,于1 d内重复测定5次,连续测定5 d,考察方法的日内、日间精密度。根据测得浓度与理论浓度比值计算方法回收率,结果见表2。结果表明,日内、日间精密度RSD<2%,精密度良好。
表 2 方法精密度试验结果时间 浓度
(ng/ml)序号 平均值 RSD
(%)1 2 3 4 5 日内 1 1.00 0.97 0.98 0.98 0.96 0.98 1.52 10 9.91 9.98 9.92 9.97 9.94 9.94 0.31 30 29.96 29.95 29.96 29.87 29.98 29.94 0.09 日间 1 0.99 0.98 1.97 0.96 1.01 1.18 0.37 10 9.96 9.98 9.95 9.97 9.98 9.97 0.13 30 29.98 29.96 29.96 30.01 29.95 29.97 0.05 2.3.7 方法重复性考察
配制浓度为1、10、30 ng/ml的房水样品各3份,按照“2.3.3”项下方法处理,1 d内测定。结果见表3,表明3个样品浓度RSD<2%,重复性良好。
表 3 方法重复性试验结果浓度
(ng/ml)序号 平均值 RSD
(%)1 2 3 1 0.98 0.96 0.97 0.97 1.03 10 9.97 9.93 9.96 9.95 0.21 30 29.93 29.98 29.92 29.94 0.06 2.3.8 回收率试验
取FK506浓度为1、10、30 ng/ml样品各3份,按照“2.3.3”项下方法处理并测定,记录FK506峰面积为A1;取空白房水同法萃取,于分离的上清液中加入对应浓度等量的FK506和FK520,测定并记录FK506峰面积A2。按提取回收率公式(A1/A2)×100 %算得FK506的提取回收率。结果表明,FK506在各个浓度的提取回收率分别为(78.14±4.21)%、(78.32±4.55)%、(76.56±4.35)%,符合体内药动学研究的相关指标。
2.3.9 分组给药设计
将实验兔随机分成A、B两组,每组6只,共12只。A组实验兔(A1~A6)左眼给予Talymus®,右眼给予自制FK506 CNE;B组实验兔(B1~B6)左眼给予FK506 CNE GEL,右眼给予FK506 CNE。实验前24 h自由进食、饮水,并进行眼部检查,以确保无任何疾病。于给药点用开睑器撑开实验兔眼睑,使用移液枪往实验兔左、右眼分别滴入等量药液50 μl,按压实验兔眼睑使之被动闭合约10 s使药物分布均匀。
2.3.10 统计学分析
采用SPSS统计软件进行独立样本t检验分析,当P<0.05时,统计学有显著性差异。实验数据均以(
$ \bar x \pm s $ )表示。2.3.11 样品采集
提前给予实验兔1 %戊巴比妥钠(0.6 ml/kg)进行耳缘静脉麻醉,并于采样前使用盐酸丙美卡因滴眼液进行局麻。接着,用镊子固定眼球后采用角膜穿刺术抽取房水,分别于给药后0.5、1、1.5、2、2.5、3、4、6、8、10 h时间点采样。A1~A3实验兔于给药后0.5、1.5、2.5、4、8 h各抽取房水30 μl,A4~A6实验兔于给药后1、2、3、6、10 h各抽取房水30 μl。B1~B3实验兔于给药后0.5、1.5、2.5、4、8 h各抽取房水30 μl,B4~B6实验兔于给药后1、2、3、6、10 h各抽取房水30 μl。
2.3.12 数据处理分析
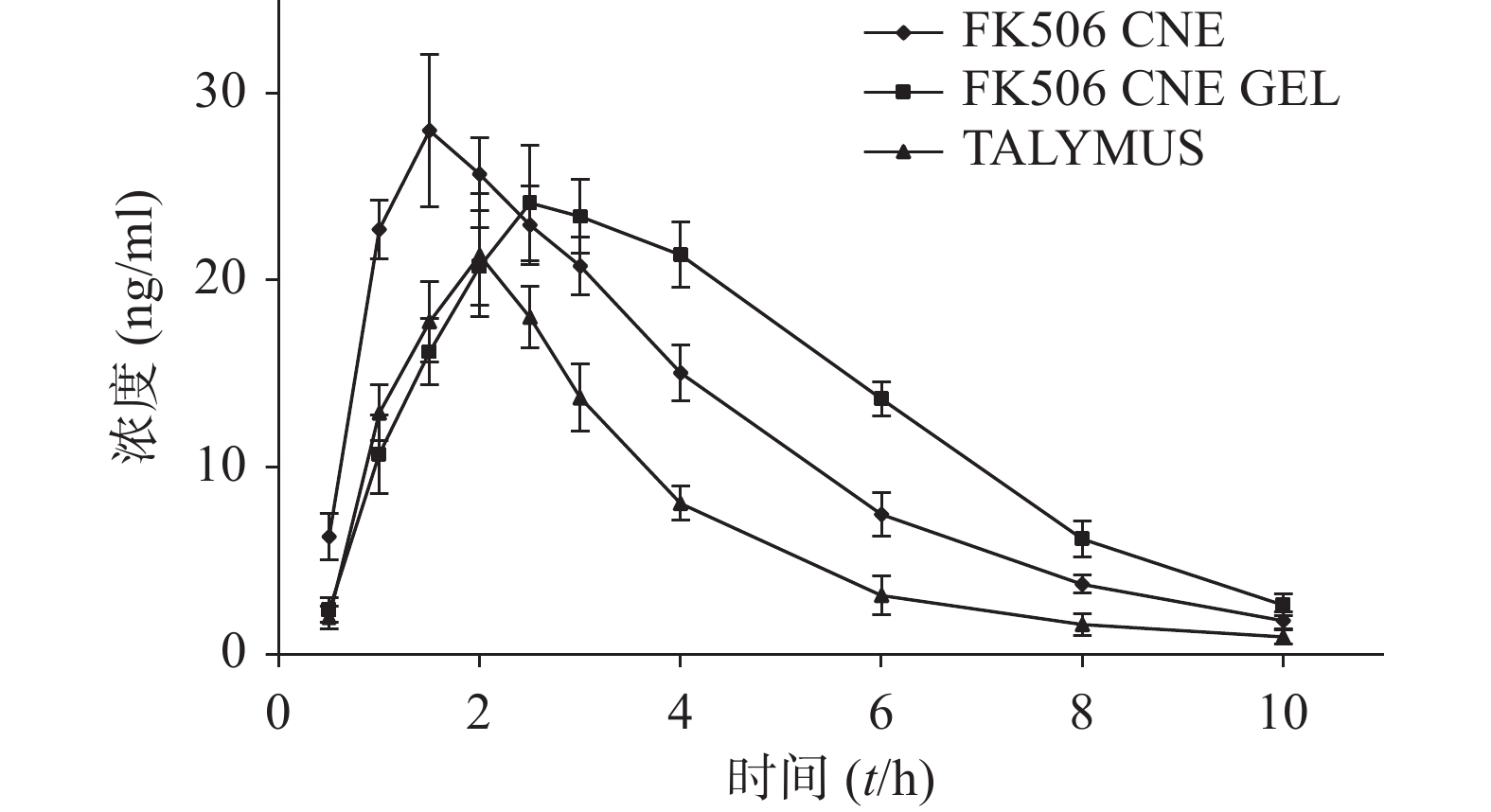
以房水样品中FK506浓度C(ng/ml)为纵坐标,以时间T(h)为横坐标作图,得药-时曲线图3及对应药动学参数表4。
表 4 给予FK506三种制剂后的房水药动学参数(n=3)药动学参数 FK506 CNE Talymus® FK506 CNE GEL AUC(ng·h /ml) 113.61±12.36* 68.25±10.82 128.34±13.09*# c max (ng/ml) 28.02±4.07 21.34±3.31 24.14±3.10 t max (t/h) 1.50±0.20* 2.00±0.17 2.50±0.25*# ka (h-1) 2.16±0.51* 1.14±0.90 0.94±0.08*# ke (h-1) 0.34±0.02* 0.41±0.05 0.32±0.02*# MRT (t/h) 3.46±0.28* 3.23±0.24 4.23±0.34*# *P<0.05,与Talymus®比较;#P<0.05,与FK 506 CNE比较 由表4可见,MRT(CNE GEL)>MRT(CNE)>MRT(Talymus®),即FK506 CNE GEL的平均滞留时间最长,表明FK506 CNE GEL在角膜的滞留时间最长。此外,AUC(Talymus®)为(68.25±10.82) ng·h /ml,AUC(CNE)为(113.61±12.36)ng·h /ml,AUC(CNE GEL)为(128.34±13.09)ng·h /ml。三者对比得AUC(CNE GEL)是AUC(CNE)的1.13倍,是AUC(Talymus®)的1.88倍,说明FK506 CNE GEL的生物利用度较高。
3. 讨论
3.1 FK506 CNE GEL的辅料
FK506 CNE GEL所采用的辅料都是安全、无刺激的,例如采用的阳离子材料为阳离子表面活性剂西他氯胺(CKC)。CKC作为眼药水中常用的防腐剂苯扎氯胺的一个组分,其安全性已得到保证,且CKC在市售产品空白阳离子纳米乳Cationorm®和口腔软膏Bonjela®中广泛使用,其临床安全性得到进一步证实。此外,采用的凝胶基质为P407/P188。由于非离子型表面活性剂泊洛沙姆无毒、无刺激,不仅可以通过空间位阻效应稳定纳米乳而且具有模拟黏膜的性质,是温敏型原位凝胶最常用的凝胶基质,同样安全性也能得到保证。其他辅料如蓖麻油、MCT、吐温-80和甘油均是常用的眼用制剂辅料之一。
3.2 FK506 CNE GEL的药动学参数
药动学参数t max (CNE GEL)>t max (Talymus®)>t max (CNE),说明FK506 CNE GEL的达峰时间最长。这是因为FK506 CNE GEL在角膜表面形成一层凝胶且其所带正电荷能与带负电荷的角膜发生静电吸引作用,从而延长其在眼部的滞留时间,缓慢而持续地释放药物,使药物作用时间延长,达峰时间延迟。而ka (CNE)>ka (Talymus®)>ka (CNE GEL)同样证实了这一点,由于FK506 CNE和Talymus®是水溶性滴眼液,相较于FK506 CNE GEL,释放药物透过角膜被吸收的速度相对较快,故FK506 CNE GEL被吸收的速度最慢。而Talymus®的粒径(1671.5±66.3)nm较FK506 CNE的粒径(178.8±2.7)nm大,故FK506 CNE相较而言吸收快、达峰时间短。
由于泪液冲刷及鼻泪管排泄,房水药物浓度随时间延长而降低。由药时曲线可见,在给药后2~4 h,Talymus®的消除曲线下降趋势最为陡峭,FK506 CNE次之,而FK506 CNE GEL的消除曲线最为平缓。ke (Talymus®)>ke (CNE)>ke (CNE GEL)同样说明FK506 CNE GEL在眼部被消除的速度最慢,相较另外两种制剂而言,明显延缓了药物从前房的消除。
综上所述,FK506 CNE GEL对兔眼无明显刺激性,给药后能黏附于黏膜表面,延长药物作用时间,提高药物生物利用度,减少给药频次。有望成为一种眼部安全性高、滞留时间长的FK506眼用制剂,其研发成功将为眼科临床提供更多选择,为IIAODs患者的临床治疗提供帮助。
-
[1] LI Z X, CHEN H L, LV J L, et al. The application and neuroprotective mechanisms of cerebral ischemic post-conditioning: a review[J]. Brain Res Bull,2017,131:39-46. doi: 10.1016/j.brainresbull.2017.03.002 [2] 陈伟伟, 隋辉, 马丽媛. 中国心脑血管病流行现况及防治进展[J]. 心脑血管病防治, 2016, 16(2):79-83. doi: 10.3969/j.issn.1009-816X.2016.02.001 [3] 李英华, 聂雪琼, 杨宠, 等. 我国6省市5类职业人群心脑血管疾病及影响因素研究[J]. 中国健康教育, 2012, 28(1):3-7. [4] 张甘良, 汪钊, 鄢洪德. 生物类黄酮化合物的结构与生物活性的关系[J]. 生物学杂志, 2005, 22(1):4-7. doi: 10.3969/j.issn.2095-1736.2005.01.002 [5] 唐传核, 彭志英. 类黄酮的最新研究进展(Ⅱ): 生理功能[J]. 中国食品添加剂, 2002(1):5-10,14. doi: 10.3969/j.issn.1006-2513.2002.01.002 [6] HERTOG M G, FESKENS E J, HOLLMAN P C, et al. Dietary flavonoids and cancer risk in the Zutphen Elderly Study[J]. Nutr Cancer,1994,22(2):175-184. doi: 10.1080/01635589409514342 [7] QI Y Y, YANG C J, JIANG Z, et al. Epicatechin-3-gallate signaling and protection against cardiac ischemia/reperfusion injury[J]. J Pharmacol Exp Ther,2019,371(3):663-674. doi: 10.1124/jpet.119.260117 [8] 韦佳, 黄罗生, 窦昌贵. 灯盏花素脂质体注射液对大鼠脑缺血再灌注损伤的保护作用[J]. 中药药理与临床, 2005, 21(4):20-22. doi: 10.3969/j.issn.1001-859X.2005.04.010 [9] ZHANG H F, HU X M, WANG L X, et al. Protective effects of scutellarin against cerebral ischemia in rats: evidence for inhibition of the apoptosis-inducing factor pathway[J]. Planta Med,2009,75(2):121-126. doi: 10.1055/s-0028-1088368 [10] Li, R. , M. Guo, G. Zhang, et al., Neuroprotection of nicotiflorin in permanent focal cerebral ischemia and in neuronal cultures[J]. Biol Pharm Bull,2006,29(9):1868-1872. doi: 10.1248/bpb.29.1868 [11] LI R P, GUO M L, ZHANG G, et al. Nicotiflorin reduces cerebral ischemic damage and upregulates endothelial nitric oxide synthase in primarily cultured rat cerebral blood vessel endothelial cells[J]. J Ethnopharmacol,2006,107(1):143-150. doi: 10.1016/j.jep.2006.04.024 [12] 王业晴, 夏玉叶, 唐颖, 等. 菸花苷对全脑缺血再灌注模型大鼠的脑保护作用[J]. 药学服务与研究, 2017, 17(2):109-113. [13] 窦锦明, 荆汉卫. 黄芩总黄酮对大鼠心肌缺血再灌注损伤的保护作用[J]. 山东中医药大学学报, 2013, 37(1):50-52. [14] DUBOIS-DERUY E, PEUGNET V, TURKIEH A, et al. Oxidative stress in cardiovascular diseases[J]. Antioxidants (Basel),2020,9(9):864. doi: 10.3390/antiox9090864 [15] CHEN D T, LIANG M H, JIN C, et al. Expression of inflammatory factors and oxidative stress markers in serum of patients with coronary heart disease and correlation with coronary artery calcium score[J]. Exp Ther Med,2020,20(3):2127-2133. [16] ZHAO G X, GAO H Q, QIU J, et al. The molecular mechanism of protective effects of grape seed proanthocyanidin extract on reperfusion arrhythmias in rats in vivo[J]. Biol Pharm Bull,2010,33(5):759-767. doi: 10.1248/bpb.33.759 [17] GULER A, SAHIN M A, YUCEL O, et al. Proanthocyanidin prevents myocardial ischemic injury in adult rats[J]. Med Sci Monit,2011,17(11):BR326-BR331. [18] 陈艳芬, 杨超燕, 李坤平, 等. 布渣叶总黄酮对大鼠急性心肌缺血的保护作用及其机制[J]. 中草药, 2013, 44(8):1003-1007. [19] 乔会敏. 木犀草素对实验性脑缺血大鼠的脑保护作用及机制研究[D]. 石家庄: 河北医科大学, 2012. [20] XU M J, CHEN X M, GU Y, et al. Baicalin can scavenge peroxynitrite and ameliorate endogenous peroxynitrite-mediated neurotoxicity in cerebral ischemia-reperfusion injury[J]. J Ethnopharmacol,2013,150(1):116-124. doi: 10.1016/j.jep.2013.08.020 [21] 赵喜娟, 许霞, 张厚霞. 灯盏花素联合预适应对心肌缺血-再灌注损伤兔心肌组织炎症因子的影响[J]. 西北药学杂志, 2016, 31(4):389-391. doi: 10.3969/j.issn.1004-2407.2016.04.019 [22] BARTEKOVA M, RADOSINSKA J, JELEMENSKY M, et al. Role of cytokines and inflammation in heart function during health and disease[J]. Heart Fail Rev,2018,23(5):733-758. doi: 10.1007/s10741-018-9716-x [23] ABBATE A, TOLDO S, MARCHETTI C, et al. Interleukin-1 and the inflammasome as therapeutic targets in cardiovascular disease[J]. Circ Res,2020,126(9):1260-1280. doi: 10.1161/CIRCRESAHA.120.315937 [24] 樊鑫梅, 曹文疆, 邢建国, 等. 香青兰总黄酮对大鼠心肌缺血再灌注损伤保护作用的研究[J]. 中成药, 2013, 35(8):1625-1629. doi: 10.3969/j.issn.1001-1528.2013.08.008 [25] 赵艳荣, 张国斌, 邴飞虹. 银杏黄酮对心肌缺血再灌注损伤大鼠的心肌保护作用及其作用机制研究[J]. 实用心脑肺血管病杂志, 2016, 24(3):38-42. doi: 10.3969/j.issn.1008-5971.2016.03.011 [26] 王金良, 顾卫, 谭峰. 灯盏细辛注射液对急性脑梗塞患者血小板CD62p及TNF-α、IL-6的影响[J]. 中国中西医结合杂志, 2005, 25(4):324-326. doi: 10.3321/j.issn:1003-5370.2005.04.009 [27] NAM S Y, JEONG H J, KIM H M. Kaempferol impedes IL-32-induced monocyte-macrophage differentiation[J]. Chem Biol Interact,2017,274:107-115. doi: 10.1016/j.cbi.2017.07.010 [28] 蔡美云, 庄文欣, 吕娥, 等. 山奈酚通过抑制p38 MAPK通路减轻6-羟多巴胺(6-OHDA)诱导的PC12细胞炎症[J]. 细胞与分子免疫学杂志, 2020, 36(7):583-589. [29] D'MELLO S R. When good kinases go rogue: GSK3, p38 MAPK and CDKs as therapeutic targets for Alzheimer's and Huntington's disease[J]. Int J Mol Sci,2021,22(11):5911. doi: 10.3390/ijms22115911 [30] 路倩, 朱开梅, 齐俊斌, 等. 瑶族药铜钻总黄酮对大鼠心肌缺血再灌注损伤的保护作用[J]. 中国实验方剂学杂志, 2016, 22(10):128-132. [31] HUANG J C, ZHANG X D, QIN F Z, et al. Protective effects of Millettia pulchra flavonoids on myocardial ischemia in vitro and in vivo[J]. Cell Physiol Biochem,2015,35(2):516-528. doi: 10.1159/000369716 [32] ZHANG X H, WANG Y H, SHEN W L, et al. Rosa rugosa flavonoids alleviate myocardial ischemia reperfusion injury in mice by suppressing JNK and p38 MAPK[J]. Microcirculation,2017,24(7):e12385. doi: 10.1111/micc.12385 [33] 李佳. PI3K/AKT/GSK3-b信号转导通路在红景天苷保护大鼠心肌缺血再灌注损伤中的作用机制[J]. 中西医结合心脑血管病杂志, 2016, 14(22):2621-2624. doi: 10.3969/j.issn.1672-1349.2016.22.009 [34] YU Z H, CAI M, XIANG J, et al. PI3K/Akt pathway contributes to neuroprotective effect of Tongxinluo against focal cerebral ischemia and reperfusion injury in rats[J]. J Ethnopharmacol,2016,181:8-19. doi: 10.1016/j.jep.2016.01.028 [35] YU H J, ZHANG H S, ZHAO W H, et al. Gypenoside protects against myocardial ischemia-reperfusion injury by inhibiting cardiomyocytes apoptosis via inhibition of CHOP pathway and activation of PI3K/Akt pathway in vivo and in vitro[J]. Cell Physiol Biochem,2016,39(1):123-136. doi: 10.1159/000445611 [36] 禤霏霏, 黄建春, 唐静芝, 等. 玉郎伞查尔酮调控PI3K/Akt信号通路抗心肌缺血/再灌注损伤的作用及机制研究[J]. 中国药理学通报, 2015, 31(12):1730-1735. doi: 10.3969/j.issn.1001-1978.2015.12.020 [37] 于晓敏, 郝祥俊, 龚明玉. 黄芩茎叶总黄酮对大鼠心肌缺血再灌注细胞凋亡的保护作用及机制[J]. 中国老年学杂志, 2013, 33(13):3132-3134. doi: 10.3969/j.issn.1005-9202.2013.13.062 [38] 刘永平, 龚明玉, 周晓慧, 等. 黄芩茎叶总黄酮抑制大鼠心肌缺血再灌注时细胞凋亡的研究[J]. 中国实验方剂学杂志, 2010, 16(12):146-149. doi: 10.3969/j.issn.1005-9903.2010.12.049 [39] ALKADHI K A. Cellular and molecular differences between area CA1 and the dentate gyrus of the Hippocampus[J]. Mol Neurobiol,2019,56(9):6566-6580. doi: 10.1007/s12035-019-1541-2 [40] HU H H, LI S J, WANG P, et al. An L-type calcium channel agonist, bay K8644, extends the window of intervention against ischemic neuronal injury[J]. Mol Neurobiol,2013,47(1):280-289. doi: 10.1007/s12035-012-8362-x [41] 王业晴. 蜂斗菜总内酯对急性高原缺氧的保护作用以及菸花苷抗缺血性脑卒中的作用机制研究[D]. 上海: 第二军医大学, 2017 [42] 李园园, 杨晖, 廖桂凤, 等. 黄芩苷抗脑缺血小鼠学习记忆功能损伤的保护作用[J]. 昆明医学院学报, 2011, 32(5):13-16. [43] CHENG O M, LI Z H, HAN Y, et al. Baicalin improved the spatial learning ability of global ischemia/reperfusion rats by reducing hippocampal apoptosis[J]. Brain Res,2012,1470:111-118. doi: 10.1016/j.brainres.2012.06.026 [44] DUONG Q V, HOFFMAN A, ZHONG K T, et al. Calcium overload decreases net free radical emission in cardiac mitochondria[J]. Mitochondrion,2020,51:126-139. doi: 10.1016/j.mito.2020.01.005 [45] 吕纪华, 贺敏, 黄建春, 等. 玉郎伞黄酮对心肌缺血再灌注损伤心肌组织ATP酶和凋亡蛋白的影响[J]. 中国实验方剂学杂志, 2010, 16(13):162-166. doi: 10.3969/j.issn.1005-9903.2010.13.049 [46] 姚佳茗, 曹文疆, 袁勇, 等. 香青兰总黄酮对心肌缺血-再灌注损伤线粒体保护作用的研究[J]. 石河子大学学报(自然科学版), 2015, 33(5):599-603. [47] GUGLIELMONE H A, AGNESE A M, NÚÑEZ MONTOYA S C, et al. Inhibitory effects of sulphated flavonoids isolated from Flaveria bidentis on platelet aggregation[J]. Thromb Res,2005,115(6):495-502. doi: 10.1016/j.thromres.2004.11.019 [48] WENG J R, CHAN S C, LU Y H, et al. Antiplatelet prenylflavonoids from Artocarpus communis[J]. Phytochemistry,2006,67(8):824-829. doi: 10.1016/j.phytochem.2006.01.030 [49] CARLONI S, BUONOCORE G, BALDUINI W. Protective role of autophagy in neonatal hypoxia-ischemia induced brain injury[J]. Neurobiol Dis,2008,32(3):329-339. doi: 10.1016/j.nbd.2008.07.022 [50] NAKKA V P, GUSAIN A, MEHTA S L, et al. Molecular mechanisms of apoptosis in cerebral ischemia: multiple neuroprotective opportunities[J]. Mol Neurobiol,2008,37(1):7-38. doi: 10.1007/s12035-007-8013-9 [51] ADHAMI F, LIAO G H, MOROZOV Y M, et al. Cerebral ischemia-hypoxia induces intravascular coagulation and autophagy[J]. Am J Pathol,2006,169(2):566-583. doi: 10.2353/ajpath.2006.051066 [52] LEVINE B, KLIONSKY D J. Development by self-digestion: molecular mechanisms and biological functions of autopha-gy[J]. Dev Cell,2004,6(4):463-477. doi: 10.1016/S1534-5807(04)00099-1 [53] MIZUSHIMA N. Autophagy: process and function[J]. Genes Dev,2007,21(22):2861-2873. doi: 10.1101/gad.1599207 [54] LEVINE B, KROEMER G. Autophagy in the pathogenesis of disease[J]. Cell,2008,132(1):27-42. doi: 10.1016/j.cell.2007.12.018 [55] WANG Y Q, ZHANG S S, NI H L, et al. Autophagy is involved in the neuroprotective effect of nicotiflorin[J]. J Ethnopharmacol,2021,278:114279. doi: 10.1016/j.jep.2021.114279 -

 点击查看大图
点击查看大图
计量
- 文章访问数: 8488
- HTML全文浏览量: 2740
- PDF下载量: 51
- 被引次数: 0




 下载:
下载:
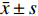

 下载:
下载:
