-
2型糖尿病(T2DM)是一种以高血糖为特征的慢性代谢性疾病,主要是由于胰岛素分泌不足而导致的空腹血糖升高[1]。冠状动脉粥样硬化性心脏病(CHD,简称冠心病)是一种常见的心血管疾病,主要是由于冠状动脉的粥样性硬化引起的血管阻塞或管腔狭窄,从而导致心肌缺血或缺氧性坏死,进而影响心脏功能[2]。近年来,T2DM的患病人数不断增加。据相关不完全统计,预计到2045年,全球T2DM患病人数将增加至7.83亿,已成为全球关注的重要人类问题之一[3]。目前,我国60岁以上的老年人中T2DM患病率超过20%,其中心血管疾病是最常见的并发症,而CHD则是T2DM患者最常见的致残或致死原因[4, 5]。有研究表明,T2DM患者发生心血管疾病的概率是非T2DM人群的2~4倍,葡萄糖耐受量受损是影响CHD进展的重要因素[6]。由此可见,T2DM与CHD相互影响,相互促进。
中药复方制剂麝香保心丸源于宋代《太平惠民和剂局方》中治疗“寒闭证”的经典名方苏合香丸,由戴瑞鸿教授在1972年改良而来。麝香保心丸已在临床应用40余年,方中麝香通窍温阳、活血化瘀为君药;苏合香辟秽通窍、人参扶正益气为臣药;牛黄开窍醒神、肉桂助阳通脉、蟾酥开窍止痛为佐药;冰片开窍醒神为使药。全方寒温并用、通补兼施、益气强心,主要用于治疗气滞血瘀所致的胸痹,症见心前区疼痛固定不移,心肌缺血所致的心绞痛、心肌梗死等[7-9]。目前临床上将麝香保心丸与基础西药中的降糖药联合应用,表现出比单用降糖药更好的血糖调节效果[10],还可以降低患者血清胆固醇水平[11],显著降低心血管事件发生率[12]。但目前关于麝香保心丸“异病同治”T2DM和CHD共同作用机制的研究相对不足。本研究旨在通过运用网络药理学方法,探索麝香保心丸“异病同治”T2DM和CHD的共同作用机制,为今后的研究和应用提供理论依据。
-
运用中药系统药理学数据库与分析平台(TCMSP)、中药成分数据库(TCMID)、中医药百科全书数据库(ETCM)和BATMAN-TCM数据库,以“人工麝香、人参提取物、人工牛黄、苏合香、蟾酥、肉桂、冰片”为关键词,检索麝香保心丸的化学成分。将口服生物利用度(OB)≥20%、类药性(DL)≥0.1,同时文献报道具有确切活性的化合物,以及本课题组前期研究鉴定的入血成分,均视为麝香保心丸的活性化合物。取BATMAN-TCM中score≥48、TCMID中score≥400、ETCM中score≥0.8的靶点,同时将仅有1个成分对应的靶点去除,筛选得到麝香保心丸的潜在作用靶点,然后通过Uniprot数据库规范靶点蛋白的基因名。
-
在DisGeNET数据库和GeneCards数据库中以“type 2 diabetes mellitus”和“coronary heart disease”为关键词筛选出T2DM和CHD的相关靶点,为获得与疾病相关度更高的靶点,将GeneCards数据库中score≤10的靶点去除。
-
绘制麝香保心丸组方中筛选出的化合物靶点、T2DM相关靶点和CHD相关靶点的Venn图,取三者交集,得到麝香保心丸同时治疗T2DM和CHD的潜在作用靶点。
-
运用Cytoscape 3.8.2软件构建麝香保心丸发挥“异病同治”作用的“药物-成分-靶点”网络图,运用“Network Analyzer”功能进行分析,其中节点代表药物、成分、靶点,边代表药物与成分、成分与靶点之间的关系。
-
运用STRING数据库,导入“药物-疾病”交集靶点,物种限制为“人”,构建PPI网络图,然后将STRING数据库得到的数据导入Cytoscape 3.8.2软件进行网络分析,依据度值筛选出核心靶点。
-
运用DAVID在线数据库导入交集靶点进行GO功能富集分析和KEGG通路富集分析,研究麝香保心丸治疗T2DM和CHD可能靶点的潜在关键生物学过程和相关通路。
-
通过TCMSP、TCMID、ETCM和BATMAN-TCM数据库共检索得到2 535个化学成分,以OB≥20%、DL≥0.1,文献报道具有确切活性的化合物,以及本课题组前期研究鉴定的入血成分,并以BATMAN-TCM中取score≥48;TCMID中取score≥400;ETCM中取score≥0.8,同时将仅有1个成分对应的潜在靶点去除为标准,共筛选出七味中药的108个活性成分,对应451个靶点。
-
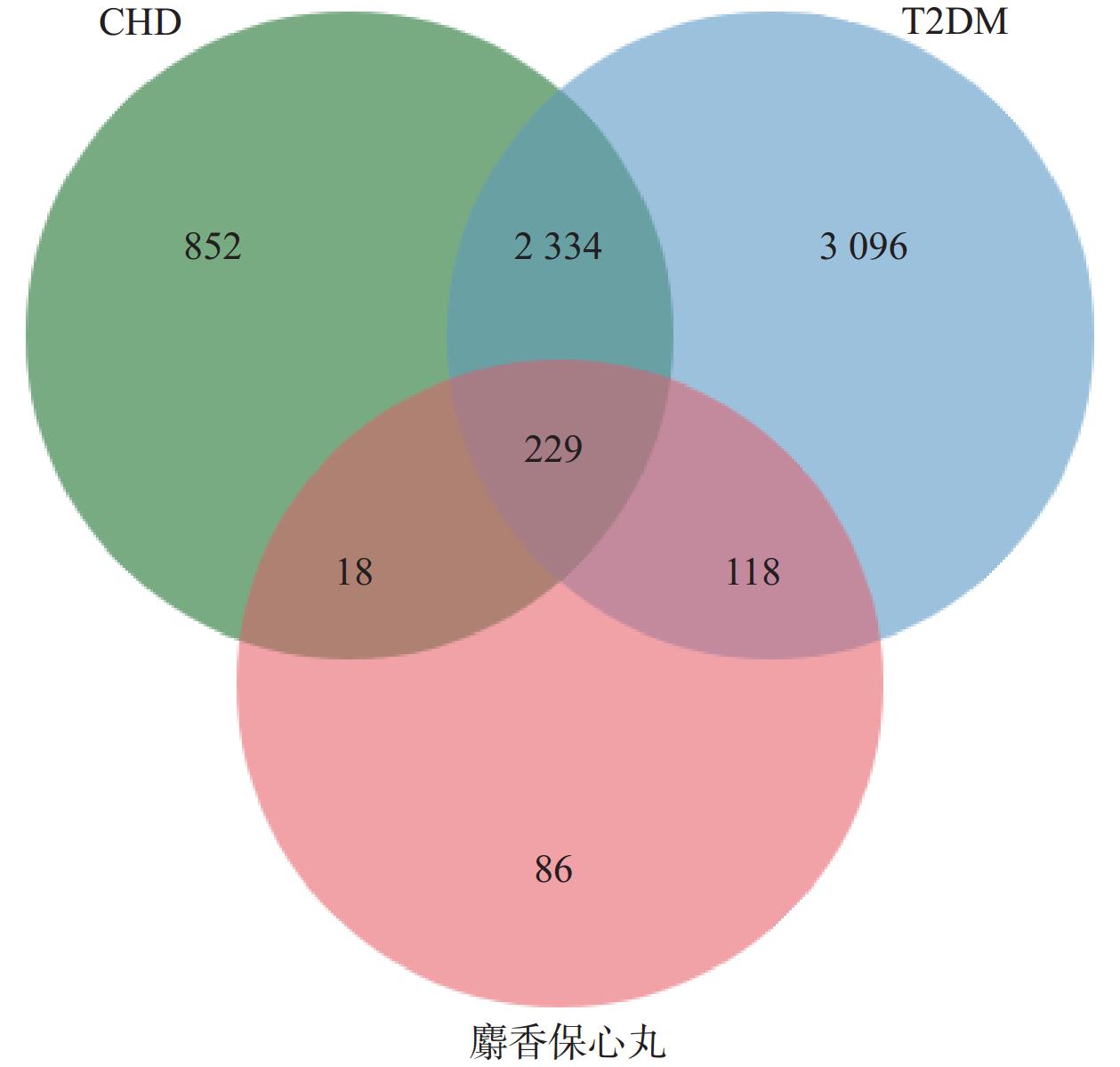
在DisGeNET和GeneCards数据库中共检索筛选得到T2DM相关靶点5 777个,CHD相关靶点3 433个。利用Venn图将麝香保心丸预测筛选出的活性成分潜在靶点与疾病靶点作交集,得到麝香保心丸作用于T2DM和CHD的潜在共同靶点229个(图1)。
-
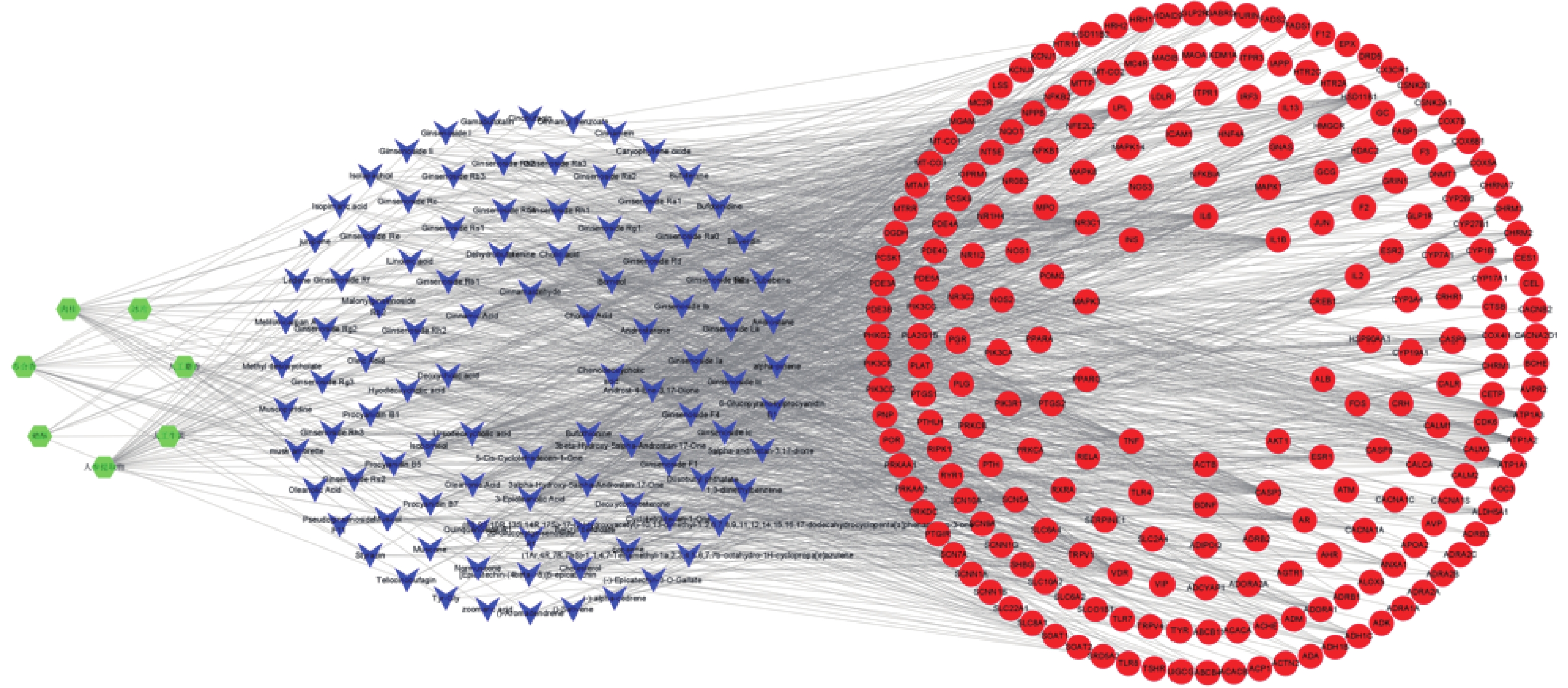
运用Cytoscape 3.8.2软件构建“药物-成分-靶点”网络图,网络中共有337个节点,其中药物7个、活性成分101个、靶点229个。其中绿色代表麝香保心丸组方中的7味中药,蓝色代表活性成分,红色代表作用于疾病的靶点。根据度值大小筛选贡献较大的活性成分,其中鹅去氧胆酸、熊去氧胆酸、肉桂醛、胆汁酸、人参皂苷Rh2、人参皂苷Rb1、肉桂酸等活性成分排名靠前,可能是麝香保心丸发挥治疗T2DM和CHD作用的主要贡献成分(图2)。
-
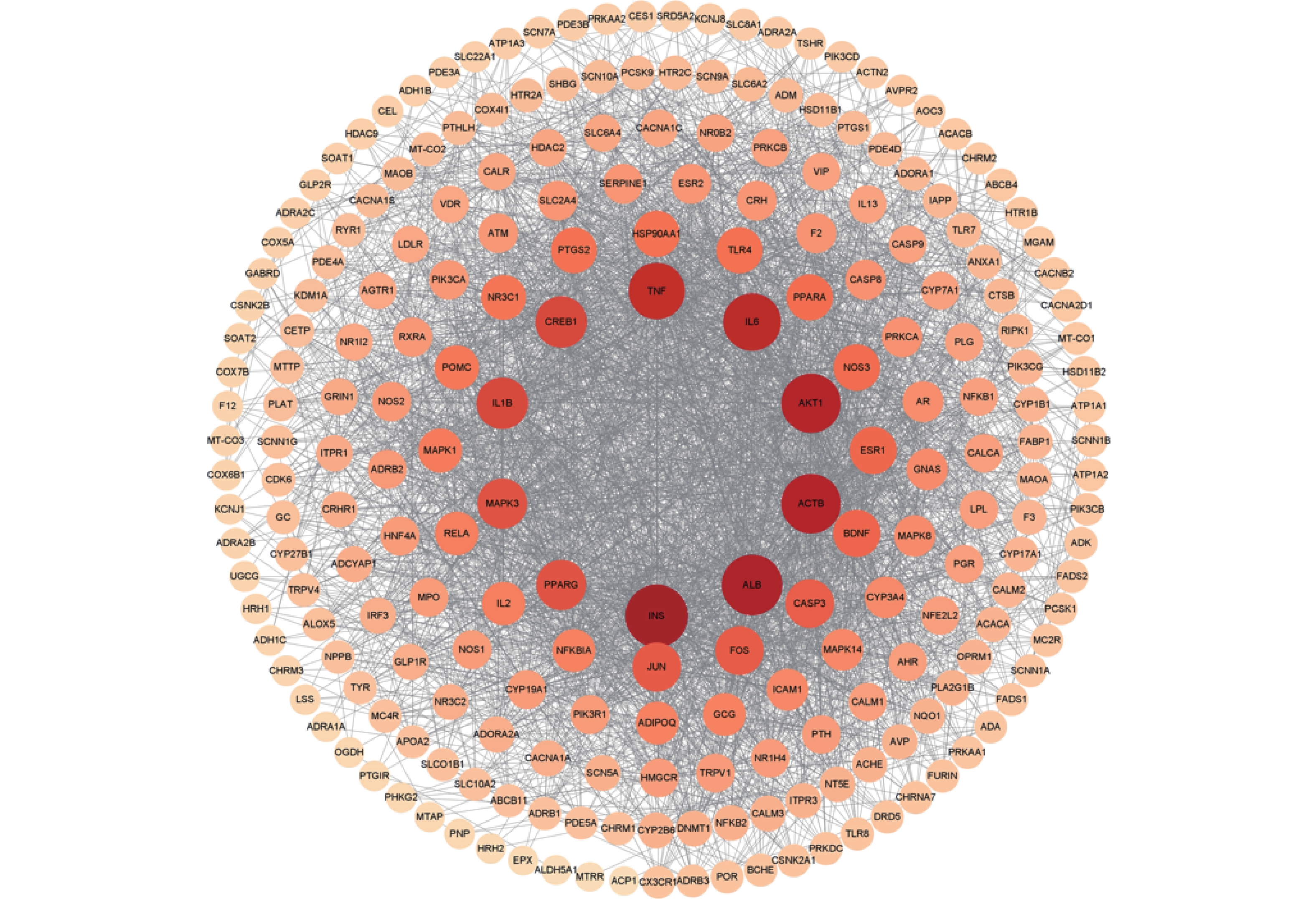
将麝香保心丸229个交集靶点导入STRING数据库中,并利用Cytoscape 3.8.2软件对PPI图进行可视化分析(图3)。根据度值由大到小对节点进行筛选,选取排名前10的潜在核心靶点,分别是胰岛素(INS)、白蛋白(ALB)、蛋白激酶B(Akt1)、白介素-6(IL-6)、肿瘤坏死因子(TNF)、环腺苷酸反应元件结合蛋白1(CREB1)、白细胞介素-1(IL-1β)、丝裂原活化蛋白激酶3(MAPK3)、过氧化物酶体增生激活受体γ(PPARG),这些靶点可能是麝香保心丸治疗T2DM和CHD的关键核心靶点。
-
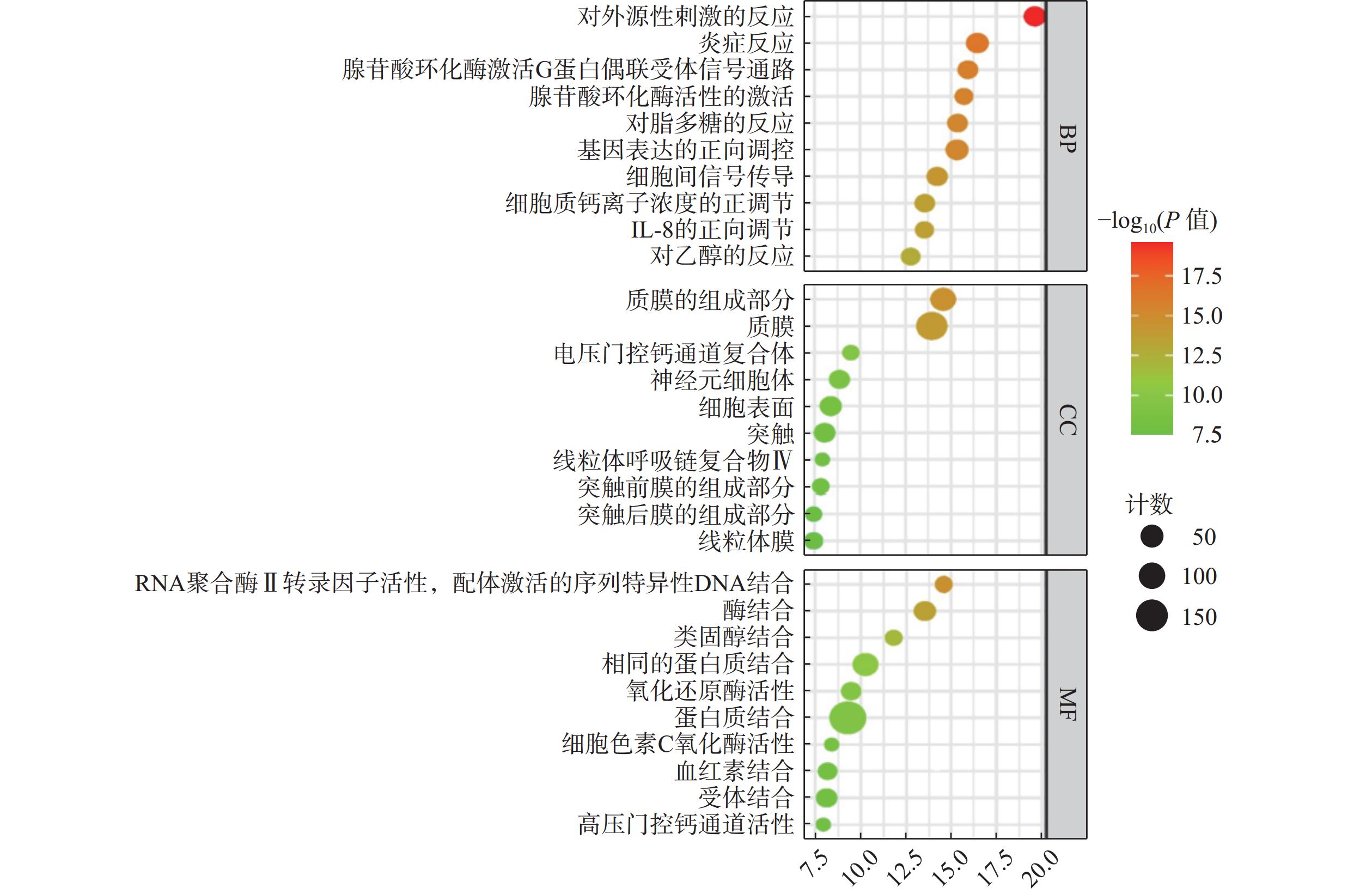
将麝香保心丸229个交集靶点导入DAVID在线数据库进行GO功能富集分析,以P≤0.05为筛选标准,共筛选出生物过程(BP)724条、细胞成分(CC)112条、分子功能(MF)208条,分别选取前10条绘制气泡图(图4)。BP主要涉及对外源性刺激的反应、炎症反应、基因表达的正调控等过程;CC主要涉及质膜、电压门控钙通道复合物、神经元细胞体等过程;MF主要涉及RNA聚合酶Ⅱ转录因子活性、配体激活序列特异性DNA结合、类固醇结合、氧化还原酶活性等过程。
-
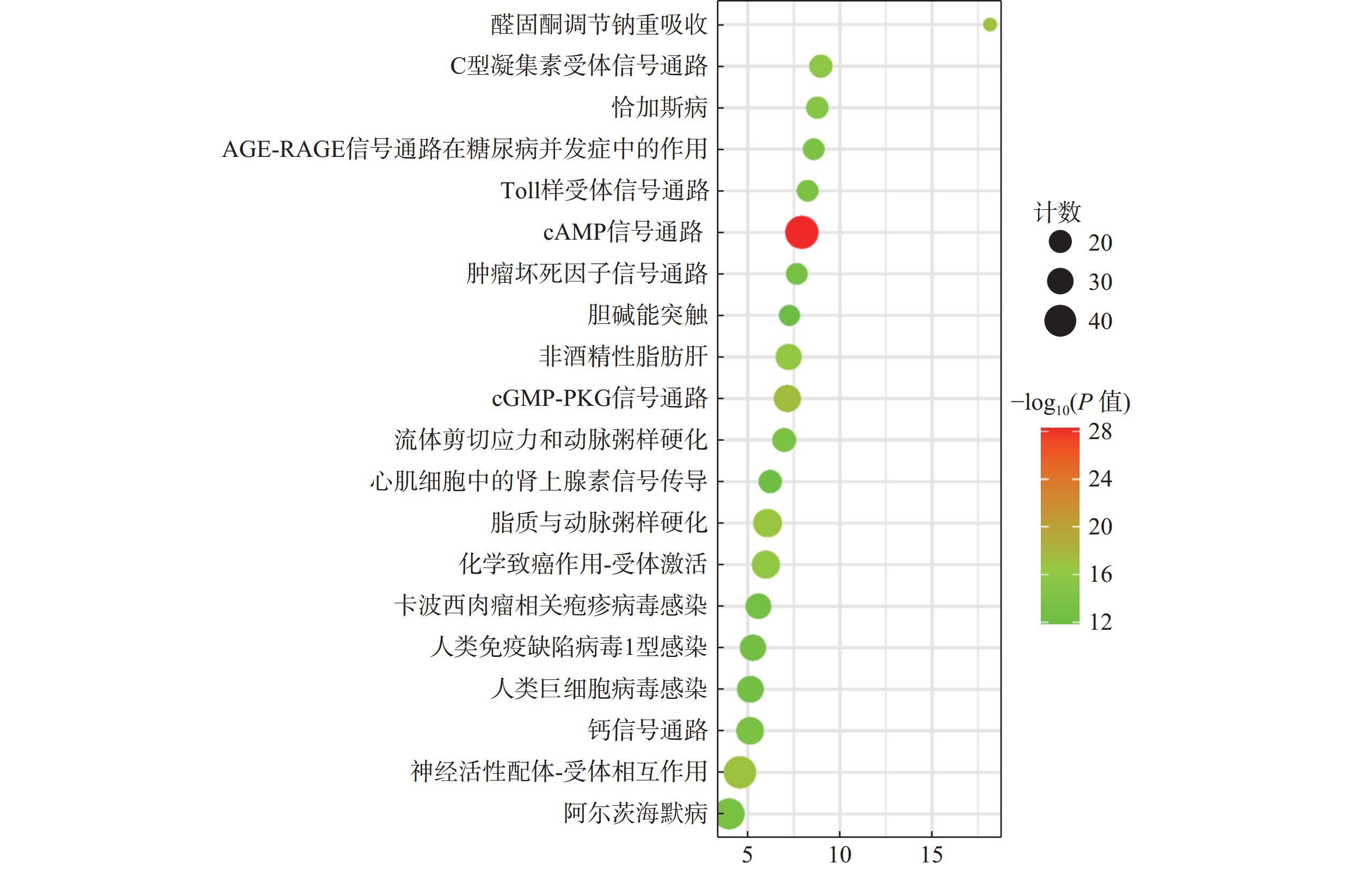
通过KEGG通路富集分析229个交集靶点,以P≤0.05为筛选标准,共得到麝香保心丸治疗T2DM和CHD的188条信号通路,选取排名前20的绘制气泡图(图5)。cAMP信号通路、cGMP-PKG信号通路、糖尿病并发症中的AGE-RAGE信号通路、Toll样受体信号通路、TNF信号通路、钙信号传导通路等可能在麝香保心丸治疗T2DM和CHD中发挥重要作用。
-
中医将以多饮、多食、多尿、身体消瘦为主要特征的T2DM归结为“消渴症”范畴,以气阴两虚和阴虚内热为主要病机[13]。CHD以气虚血瘀为主要病机,虚证多以阳虚、气虚、气阴两虚为主,实证多以气滞血瘀、痰凝寒浊为主[14]。中药复方制剂麝香保心丸作为中医经典名方“苏合香丸”的发展延续,是我国目前最常用的芳香温通类药物,为益气活血剂,临床上广泛应用于治疗心血管疾病[15]。由于T2DM与CHD均有“气阴两虚”表型,故现临床上将麝香保心丸用于治疗T2DM比单用西药进行基础治疗表现出更好的控制血糖、促进心功能恢复、改善糖尿病患者微循环障碍、降低血液粘度等作用[15, 16]。虽然麝香保心丸在治疗T2DM和CHD方面具有良好的临床疗效,但其“异病同治”的作用机制尚不明确。本研究主要运用网络药理学方法,探讨麝香保心丸“异病同治”T2DM和CHD的潜在作用机制。
本研究运用网络药理学分析方法共筛选得到麝香保心丸的101个活性成分和“异病同治”T2DM和CHD的共同靶点229个。其中人参总皂苷提取物是麝香保心丸的臣药,文献报道其具有抑制IL-1β等炎性因子的表达[17],调节线粒体能量代谢和糖脂代谢,改善胰岛素抵抗、抑制心肌细胞凋亡[18]的作用,人参皂苷Rg1、Rb1可通过抑制IL-6、IL-1β、TNF-α等炎症因子的表达,减轻肝脏损伤和胰岛素抵抗[19] ,缓解心肌损伤[20]。已有研究表明,肉桂提取物可以减少氧化应激,保护胰岛β细胞,增加胰岛素分泌[21],改善血脂异常[22],减轻糖尿病心肌并发症症状。肉桂中的有效成分肉桂醛[23]可通过自噬途径减轻缺氧复氧导致的H9C2心肌细胞的损伤,抑制自噬水平,增强心肌细胞活力。肉桂酸[24]则能通过激活PI3K/Akt/FoxO1信号通路,降低db/db小鼠空腹血糖水平、调节血脂、改善胰岛素抵抗。牛黄中的有效成分熊去氧胆酸可增加肝脏能量消耗、改善线粒体功能和胆汁酸代谢,减少甘油三酯(TG)和FFA,改善糖脂代谢[25]。由此可见,麝香保心丸治疗T2DM和CHD可能是其多个活性成分共同发挥作用的结果。
绘制PPI网络图,根据度值分析得到排名前10的核心靶点,INS、ALB、Akt1、IL-6、TNF、CREB1、IL-1β、MAPK3、PPAGR、ACTB是麝香保心丸“异病同治”T2DM和CHD的潜在核心靶点。研究表明,促炎细胞因子和炎症相关核转录因子与胰岛素分泌受损有关,可能会诱导T2DM的发生[26],例如,IL-6被认为可能与胰岛素抵抗和β细胞功能障碍有关[27]。此外,有研究表明,在血管生物学中,IL-6还可能与动脉粥样硬化形成相关的成纤维细胞和内皮细胞分泌有关[28]。因此,抑制IL-6炎症因子的激活能有效改善胰岛素抵抗,缓解动脉粥样硬化。有研究表明,PPARG(即PPARγ)是一种过氧化物酶体增殖受体,是配体激活受体,参与能量稳态调节,其在脂肪组织、脾脏和大肠中的表达最高,主要表现为调节脂肪生成、脂质和葡萄糖代谢以及炎症途径,因此,激活PPARG受体不仅可以改善胰岛素敏感性,还可以调节血管生成[29]。ACTB是一种β-肌动蛋白,是重要的细胞骨架蛋白,可以通过调节内皮NO合酶活性改变NO产生,从而导致内皮功能障碍,这被认为可能是导致CHD的潜在作用机制[30]。同时有研究表明,ACTB是与T2DM风险有关的一种可靠的基因蛋白[31]。由此可见,麝香保心丸通过作用于多个靶点发挥“异病同治”T2DM和CHD的治疗作用。
GO生物功能分析发现,麝香保心丸“异病同治”T2DM和CHD的潜在调控生物过程,主要涉及炎症反应、基因表达的正调控、对脂多糖的反应、酶结合、蛋白质结合、受体结合、电压门控钙通道复合物等生物过程。KEGG通路富集分析发现,麝香保心丸治疗T2DM和CHD的通路主要富集在脂质与动脉粥样硬化、糖尿病并发症中的AGE-RAGE信号通路、TNF信号通路、Toll样受体信号通路、cGMP-PKG信号通路等信号通路。晚期糖基化终产物(AGEs)是游离还原性糖和蛋白质、脂质、核酸之间非酶促糖化反应的结果,主要发生于持续高血糖状态的患者体内,属于有害分子,AGEs会与其晚期糖基化终产物受体(RAGE)发生非特异性作用[32],产生氧化应激,导致促炎细胞因子产生和炎症反应,从而干扰细胞内信号,导致胰岛素抵抗[33]。有研究表明,AGE水平升高与动脉壁硬度增加、冠状动脉疾病等心血管风险有关,与T2DM患者冠状动脉粥样硬化的严重程度和心血管事件的发生有关,这主要是因为AGE诱导的血管和心肌蛋白交联会降低血管弹性和心肌灵活性,导致血管壁柔韧性降低,血管和心肌僵硬以及影响细胞内皮功能,最终导致CHD[34]。Toll样受体(TLRs)属于炎症小体,主要有2个亚型:①在其外域中具有多个半胱氨酸簇的TLR(mccTLRs);②在其外域中具有单个半胱氨酸簇的TLR(sccTLRs)[35]。动脉粥样硬化主要是由慢性炎症引起的血管壁结构和功能异常,TLR信号通路的激活参与动脉粥样硬化的炎症过程,其中TLR2和TLR4在动脉硬化过程中上调使CHD进一步加剧[36]。胰岛素抵抗是T2DM的主要症状之一,起因之一是肥胖,脂肪组织分泌各种激素和细胞因子,在代谢应激的作用下,TLR4信号传导的激活会引起免疫细胞释放促炎因子,使脂肪组织中的巨噬细胞聚集极化为M1和M2亚型,导致慢性低度炎症,干扰代谢组织中的胰岛素信号传导,进而发展成T2DM[37]。cAMP是一种单磷酸腺苷,由腺嘌呤、核糖以及磷酸基团组成,是细胞内的第二信使分子。cAMP信号通路主要包括cAMP合成环化酶、降解磷酸二酯酶(PDE)和cAMP效应,主要来源是细胞质膜上的跨膜腺苷酸环化酶(tmACs)和细胞内的可溶性腺苷酸环化酶(sAC),负责激素诱导的肝糖原分解[38],可刺激胰岛素分泌,是胰岛素依赖性cAMP信号通路[39]。蛋白激酶A(PKA)是主要的cAMP效应靶标,cAMP水平升高和PKA激活可调节内皮屏障稳态,促进血管舒张[40]。上述分析结果表明,麝香保心丸发挥治疗T2DM和CHD的作用是方中的多种化学成分作用于多个信号通路的结果,主要涉及氧化应激和炎症反应。
-
“异病同治”治疗思想是中医对《黄帝内经》“同病异治”传统理论的继承与发展,目前临床应用广泛,但相关作用机制尚不明确[41]。本文运用网络药理学方法研究发现,麝香保心丸“异病同治”T2DM和CHD的靶点和信号通路主要涉及炎症反应和氧化应激,与目前关于T2DM和CHD的相关作用机制研究相符,证实麝香保心丸通过多成分、多靶点、多通路发挥治疗T2DM和CHD的共同作用。研究结果为麝香保心丸的临床应用及进一步实验验证研究提供了理论依据。
Mechanisms of Shexiang Baoxin Pill in homo-therapy for heteropathy in type 2 diabetes mellitus and coronary heart disease based on network pharmacology
-
摘要:
目的 基于网络药理学方法研究麝香保心丸“异病同治”2型糖尿病(T2DM)和冠心病(CHD)的作用机制。 方法 运用中药系统药理学数据库与分析平台(TCMSP)、中药成分数据库(TCMID)、中医药百科全书数据库(ETCM)和BATMAN-TCM数据库筛选麝香保心丸中七味中药的化学成分和作用靶点,利用DisGeNET和GeneCards数据库获取与CHD和T2DM相关的疾病靶点。运用Cytoscape3.8.2软件构建“药物-成分-靶点”网络图,利用STRING数据库构建蛋白互作(PPI)网络图,利用DAVID在线数据库对麝香保心丸治疗T2DM和CHD的共同作用靶点进行GO生物过程分析和KEGG通路富集分析。 结果 共筛选出麝香保心丸治疗T2DM和CHD的潜在活性成分101个,对应229个靶点。网络分析结果表明,麝香保心丸治疗T2DM和CHD的共同主要成分可能是鹅去氧胆酸、熊去氧胆酸、肉桂醛、胆汁酸、肉桂酸及人参皂苷类成分。通路富集分析结果显示,麝香保心丸“异病同治”T2DM和CHD的作用机制可能与抑制炎症反应和氧化应激有关。 结论 麝香保心丸可通过多成分、多靶点、多途径发挥“异病同治”T2DM和CHD的作用,为麝香保心丸的临床应用及进一步研究提供理论基础。 Abstract:Objective To probe into the mechanism of Shexiang Baoxin Pill in homo-therapy for heteropathy for type 2 diabetes mellitus (T2DM) and coronary heart disease (CHD) based on network pharmacology. Methods All chemical components and action targets of these seven traditional Chinese medical in Shexiang Baoxin Pill were screened by Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform (TCMSP), Traditional Chinese Medicines Integrated Database (TCMID), The Encyclopedia of Traditional Chinese Medicine (ETCM) and BATMAN-TCM platform, and the DisGeNET and GeneCards databases were used to obtain CHD and T2DM-related Disease targets. The “drug-component-target” network map was constructed by Cytoscape 3.8.2 software, the protein-protein interaction (PPI) network map was constructed by STRING database, and the GO biological process analysis and KEGG pathway enrichment analysis were performed on the common targets of Shexiang Baoxin Pill for T2DM and CHD using DAVID online database. Results A total of 101 potential active ingredients for the treatment of T2DM and CHD in Shexiang Baoxin Pill were screened out, corresponding to 229 targets. Network analysis results showed that the common main active ingredients in Shexiang Baoxin Pill for treating T2DM and CHD might be chenodeoxycholic acid, ursodeoxycholic acid, cinnamic aldehyde, bile acids, cinnamic acid, and ginsenosides. The results of pathway enrichment analysis showed that the mechanism of action of Shexiang Baoxin Pill in the treatment of type 2 diabetes and coronary heart disease in treating T2DM and CHD might be related to the inhibition of inflammatory response and oxidative stress. Conclusion Shexiang Baoxin Pill could play a role in treating CHD and T2DM through multiple components, multiple targets and multiple pathways, which provided a certain theoretical basis for the clinical application and further research of Shexiang Baoxin Pill. -
光动力治疗(PDT)基于光辐照聚集光敏剂的肿瘤组织,由光敏剂诱发光动力反应形成单线态氧(1O2)等活性氧(ROS),通过对肿瘤细胞和肿瘤血管的直接杀伤及激活机体系统免疫反应等多种机制发挥抗肿瘤作用[1-3]。二氢卟吩及菌绿素类光敏剂是PDT新药研究的热点[4-8]。其中,已获批上市的代表药物有他拉泊芬(talaporfin)和帕利泊芬(padeliporfin)等[9, 10]。
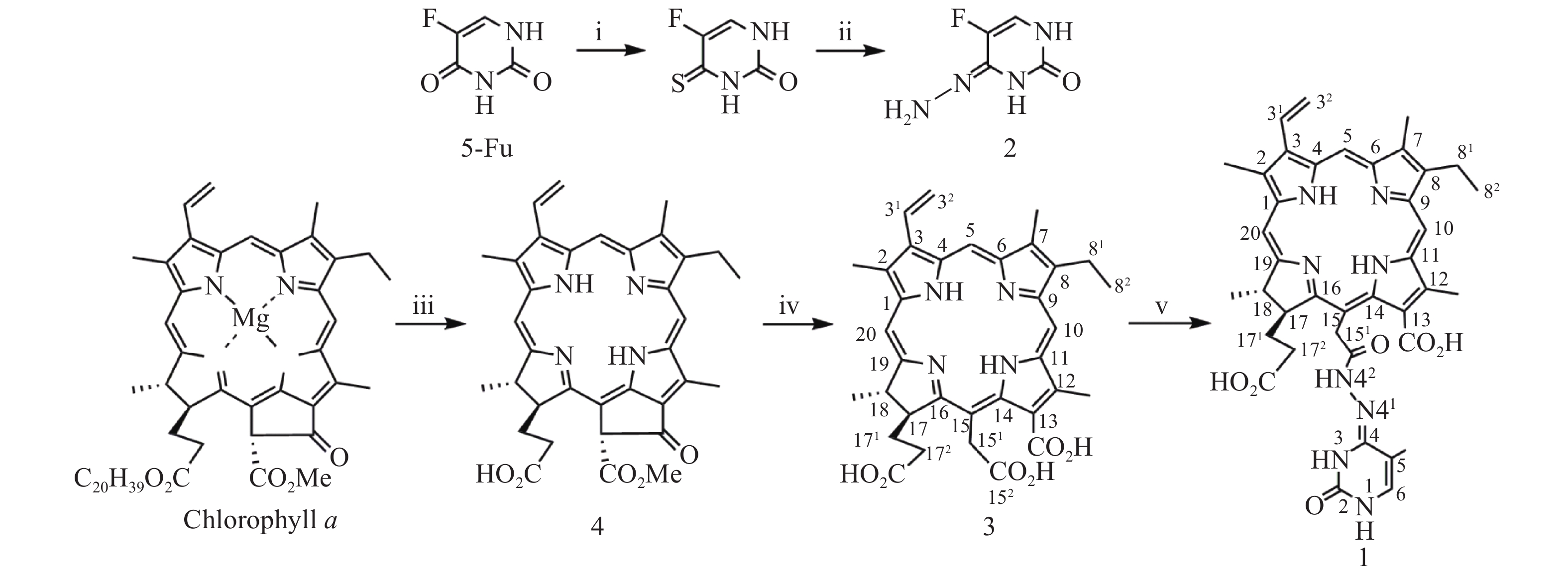
光敏剂作为结构非特异性药物,存在缺乏肿瘤靶向性摄入和明确的作用药靶等缺陷。此外,PDT受制于局部治疗,对浸润较深的肿瘤组织,及已发生转移的肿瘤疗效有限。目前,PDT和化疗联用是克服上述缺陷,提高PDT疗效最为普遍和有效的策略之一。研究表明,抗代谢化疗药物氟尿嘧啶(5-Fu)与PDT联用具有协同抗肿瘤作用[11-13]。据此,我们设想利用在肿瘤微环境下能响应性断裂的连接基团(linker)将光敏剂与化疗药物偶联,希望实现二者在肿瘤组织的靶向释放,从而发挥其PDT和化疗协同抗肿瘤作用。酰腙键是酸敏感化学键,常被用来连接载体,以药物制备智能药物载体。这种药物载体到达肿瘤细胞的内涵体或溶酶体中时,会发生酸性水解将药物有效释放出来。因此,本文针对肿瘤微环境呈弱酸性的特点,采用药物化学最经典的前药设计策略,以脱镁叶绿素a(Phephorbide a)粗提物经酸碱降解制得的二氢卟吩e6(3)[14]为先导光敏剂,通过其152-羧基与抗肿瘤药物5-Fu以酸敏感酰腙键连接,设计合成pH响应型光化疗协同抗肿瘤光敏剂二氢卟吩e6-偕氟尿嘧啶(1),并考察其体外PDT抗肿瘤活性和pH响应性5-Fu释放,及其对黑色素瘤B16-F10和肝癌HepG2细胞的光动力抗癌活性及其作用机制,以期获得高效、低毒的PDT治癌药物候选药物,合成路线见图1。
1. 化学合成
1.1 仪器与试剂
用Bruker MSL-600型核磁共振仪测定1H NMR,CD3OD为溶剂;用API-3000 LC-MS型电喷雾质谱仪测定质谱(ESI-MS);用岛津UV-160型紫外分光光度计测定UV吸收谱;用日立F-7000荧光分光光度计测定荧光发射谱;用Shimazu LC-20AD HPLC仪测定化合物1的相对纯度及其5-Fu的体外释放。色谱柱型号为Waters Xterra C18柱,流动相:乙腈-0.3%乙酸水溶液(80 : 20);流速:1.0 ml/min;检测波长:400 nm(化合物1的相对纯度)或254 nm(5-Fu释放);柱温:30 ℃;进样量:20 μl。柱色谱分离用TELEDYNE ISCO的快速制备色谱Combi Flash@Rf+仪,硅胶H作为固定相。PDT抗癌活性测试使用BWT半导体激光仪(北京凯普林,波长为660 nm);用流式细胞仪(BD Accuri C6,美国)(激发波长:488 nm,发射波长:525 nm)检测受试肿瘤细胞样品的ROS水平、细胞凋亡率和细胞周期阻滞。
二氢卟吩e6(3)按照文献[14]的方法制备;其它实验用材料和化学试剂均为市售商品。
1.2 42-N-(二氢卟吩 e6-152-酰基)-5-氟尿嘧啶-4-腙(1)的合成
取氟尿嘧啶(0.2 g,1.563 mmol)溶于无水吡啶(10 ml),加入五硫化二磷(0.298 g,1.563 mmol),加热回流12 h。反应完毕,减压回收溶剂,残物加乙酸乙酯溶解(100 ml),用0.1 mol/L HCl洗涤(50 ml×2),无水Na2SO4干燥,减压除去溶剂得4-硫代-5-氟尿嘧啶粗品。上述4-硫代-5-氟尿嘧啶粗品加甲醇(10 ml)溶解,于0 ℃下滴加N2H4·H2O(0.316 g,6.252 mmol),室温继续搅拌2 h。反应完毕,减压抽滤,P2O5真空干燥得固体化合物5-氟尿嘧啶-4-腙(2)中间体,直接用于下步反应。取二氢卟吩e6(0.1 g,0.168 mmol)溶于无水DMF(10 ml),加1-乙基-(3-二甲氨基丙基)碳二亚胺盐酸盐(EDC·HCl)(0.035 g,0.183 mmol),室温搅拌反应6 h后再加入中间体2(0.031 g,0.218 mmol),继续搅拌36 h。反应完毕,反应液加入10倍体积量乙酸乙酯,饱和NaCl水溶液洗涤(50 ml×3),无水Na2SO4干燥,减压回收溶剂所得固体经快速制备色谱梯度洗脱分离纯化(流动相为二氯甲烷/甲醇/甲酸=15∶1∶0.1~8∶1∶0.1)得黑色固体1纯品0.048 g,产率39.6%。UV-vis λmax (MeOH, nm) (ε, M−1cm−1):660 (3.15×104), 510 (0.82×104), 402 (8.13×104)。1H-NMR (600 MHz, CD3OD, δ, ppm): 9.79 (s, 1H, 10-CH), 9.73 (s, 1H, 5-CH), 9.07 (s, 1H, 20-CH), 8.19 (dd, J = 18.0, 12.0 Hz, 1H, 31-CH), 7.29 (s, 1H, 5-Fu的6-CH), 6.38 (d, J = 18.0 Hz, 1H, 32-CHB), 6.15 (d, J = 12.0 Hz, 1H, 32-CHA), 5.35 (s, 2H, 151-CH2), 4.65 (m, 2H, 17-CH和18-CH), 3.84 (q, J = 7.5 Hz, 2H, 81-CH2), 3.63 (s, 3H, 12-CH3), 3.53 (s, 3H, 2-CH3), 3.30 (s, 3H, 7-CH3), 2.3~2.0 (m,4H , 171-CH2 和172-CH2), 1.76 (m, 6H¸ 18-CH3和82-CH3)。MS (ESI+) m/z: 723.63 (M+H)+ (100%)。元素分析(C38H39N8O6F,%)计算值:C 63.16, H 5.40, N 15.48;实测值:C 63.34, H 5.38, N 15.43。HPLC测定纯度:95.2%。
2. 体外光理化性质和光生物活性
2.1 化合物1的紫外吸收谱和荧光发射谱
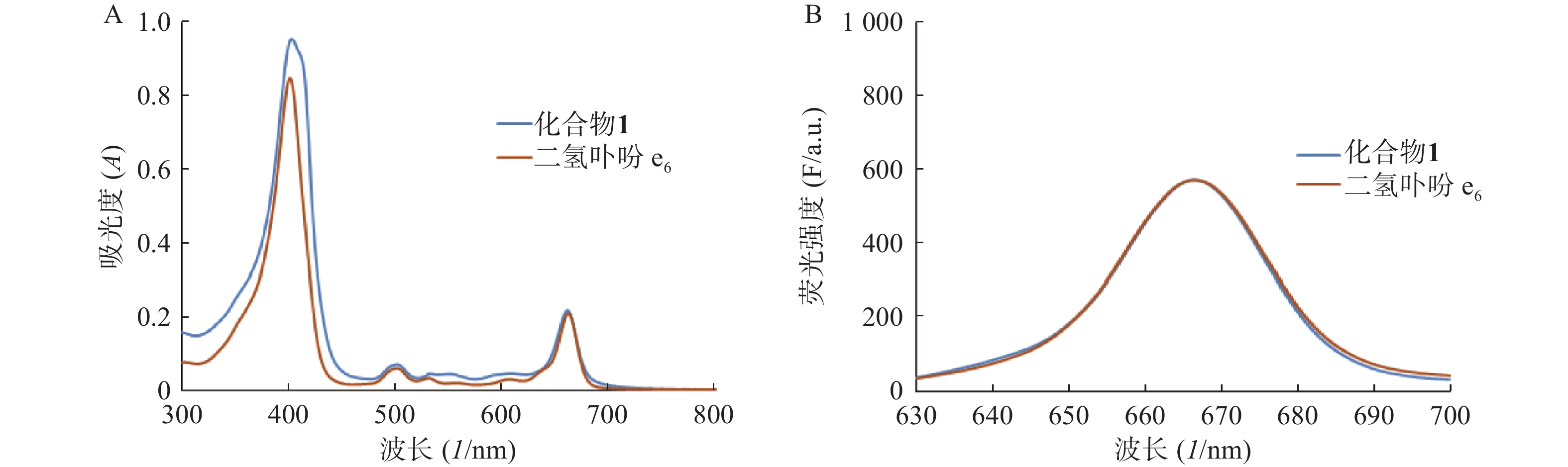
分别测定目标化合物1及其先导化合物二氢卟吩e6(3)的甲醇溶液(10 μmol/L)在300~800 nm处的紫外吸收谱和激发波长为400 nm的荧光发射光谱,结果见图2。
2.2 化合物1的体外pH响应性5-Fu释放
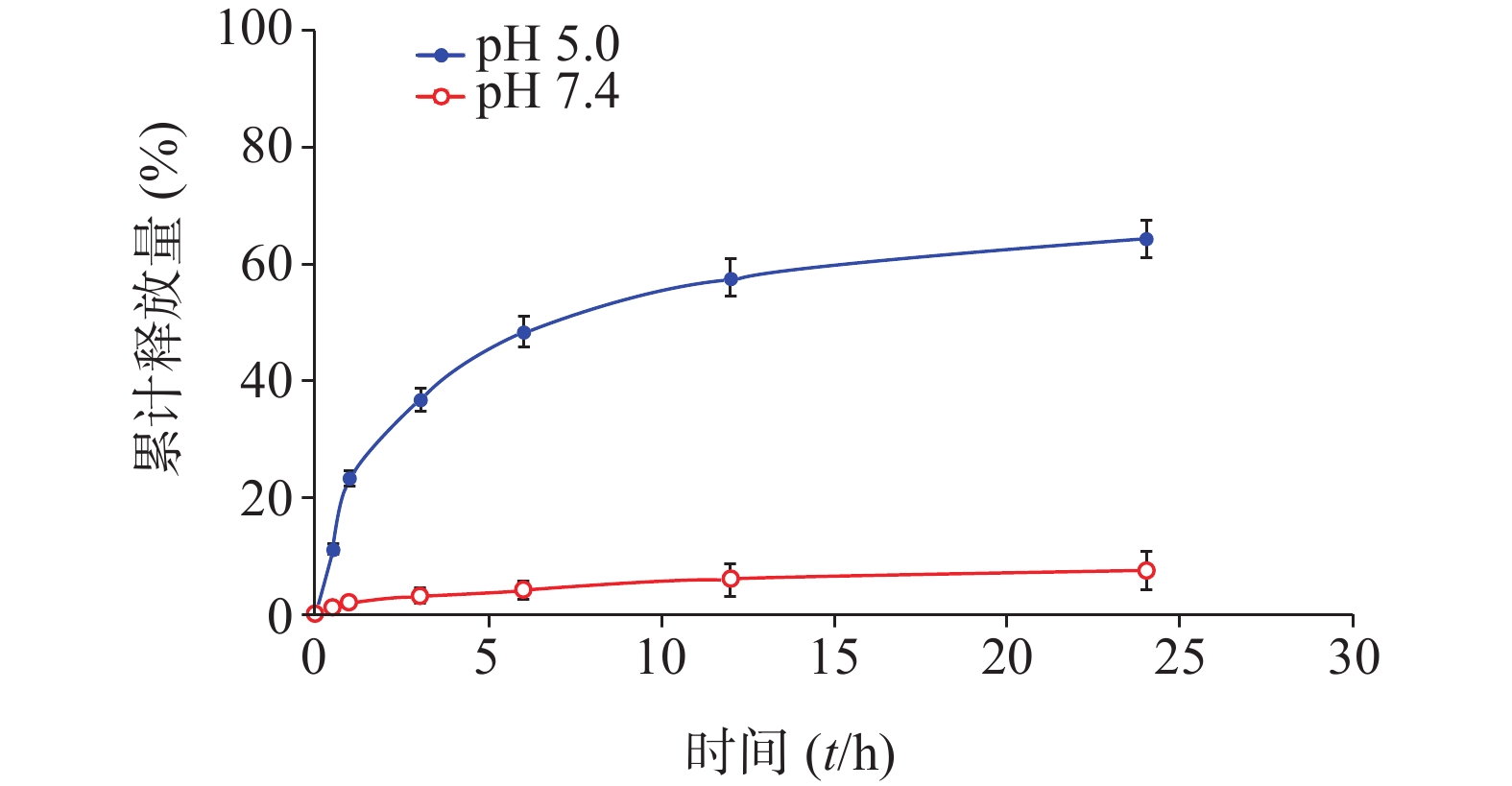
分别配制浓度为50 μmol/L的化合物1的HOAc-NaOAc缓冲液(pH 5.0)和PBS溶液(10 ml),并于0.5、1.0、3.0、6.0、12、24 h时分别取样(500 μl)。其中,HOAc-NaOAc缓冲液(pH 5.0)组取样液用0.1 mol/L氢氧化钠水溶液迅速调节pH值至7.4。每份取样液加PBS稀释至原溶液1/3浓度,微孔滤膜(孔径0.22 μm)过滤,HPLC进样检测;实验重复3次。根据5-Fu的HPLC峰面积-浓度标准曲线分析计算,绘制目标化合物1于弱酸(pH 5.0)中的5-Fu体外释放量-时间曲线,结果见图3。
2.3 化合物1的体外光动力抗癌活性
2.3.1 细胞孵育
2.3.2 细胞暗毒性测试
参照文献[6-8]的方法,每孔5×103个B16-F10细胞或HepG2细胞悬液(100 μl)接种于96孔板上,加入等体积上述细胞培养液孵育24 h;更换含不同浓度待测物的培养液(DMSO浓度小于1%,100 μl),继续避光孵育48 h;再更换含10%(V/V)CCK-8(Beyotime,中国)的RPMI 1640基础培养基(100 μl),继续培养1.5 h,然后用Varioskan Flash全波长酶标仪(Thermo)于波长450 nm处测定每孔的吸光度值,计算各浓度对应的细胞存活率,并拟合得到待测物的肿瘤细胞半数抑制浓度即IC50值。
2.3.3 细胞光毒性测试
每孔5×103个B16-F10细胞或HepG2细胞悬液(100 μl)接种于96孔板上,加入等体积细胞培养液孵育24 h;更换含不同浓度待测物的细胞培养液(DMSO浓度小于1%,100 μl),继续避光孵育24 h;再更换新鲜培养液(100 μl),以波长为660 nm的激光辐照受试细胞样品(光照剂量为10 J/cm2),继续孵育24 h。最后按“2.3.2”项下CCK-8法测定各待测物的肿瘤细胞IC50值。
2.3.4 实验结果
以临床光敏药物他拉泊芬为阳性对照,化合物1及其先导化合物3对肿瘤细胞株的体外PDT抗癌活性结果见表1。
表 1 目标化合物1的体外光动力抗癌活性(IC50,μmol/L)化合物 B16-F10细胞 暗毒/光毒比 HepG2细胞 暗毒/光毒比 暗毒性 光毒性 暗毒性 光毒性 化合物 1 46.84±8.46*, ΔΔΔ 0.73±0.16**, ΔΔΔ 64.2 50.80±6.45**, #, ΔΔΔ 0.90±0.22**, ΔΔΔ 56.4 二氢卟吩e6 69.72±4.69 3.36±0.59 20.8 70.38±10.9 2.75±0.41 25.6 他拉泊芬 254.8±18.8 11.31±3.88 22.5 176.4±28.4 15.47±5.07 11.4 5-Fu 35.80±6.68 NTa − 39.16±2.7 NTa − NTa:未测定;*P < 0.05,**P < 0.01,与二氢卟吩 e6组比较;#P < 0.05,与5-Fu组比较;ΔΔΔP < 0.001,与他拉泊芬组比较。 2.4 化合物1介导的PDT对肿瘤细胞内ROS水平的影响
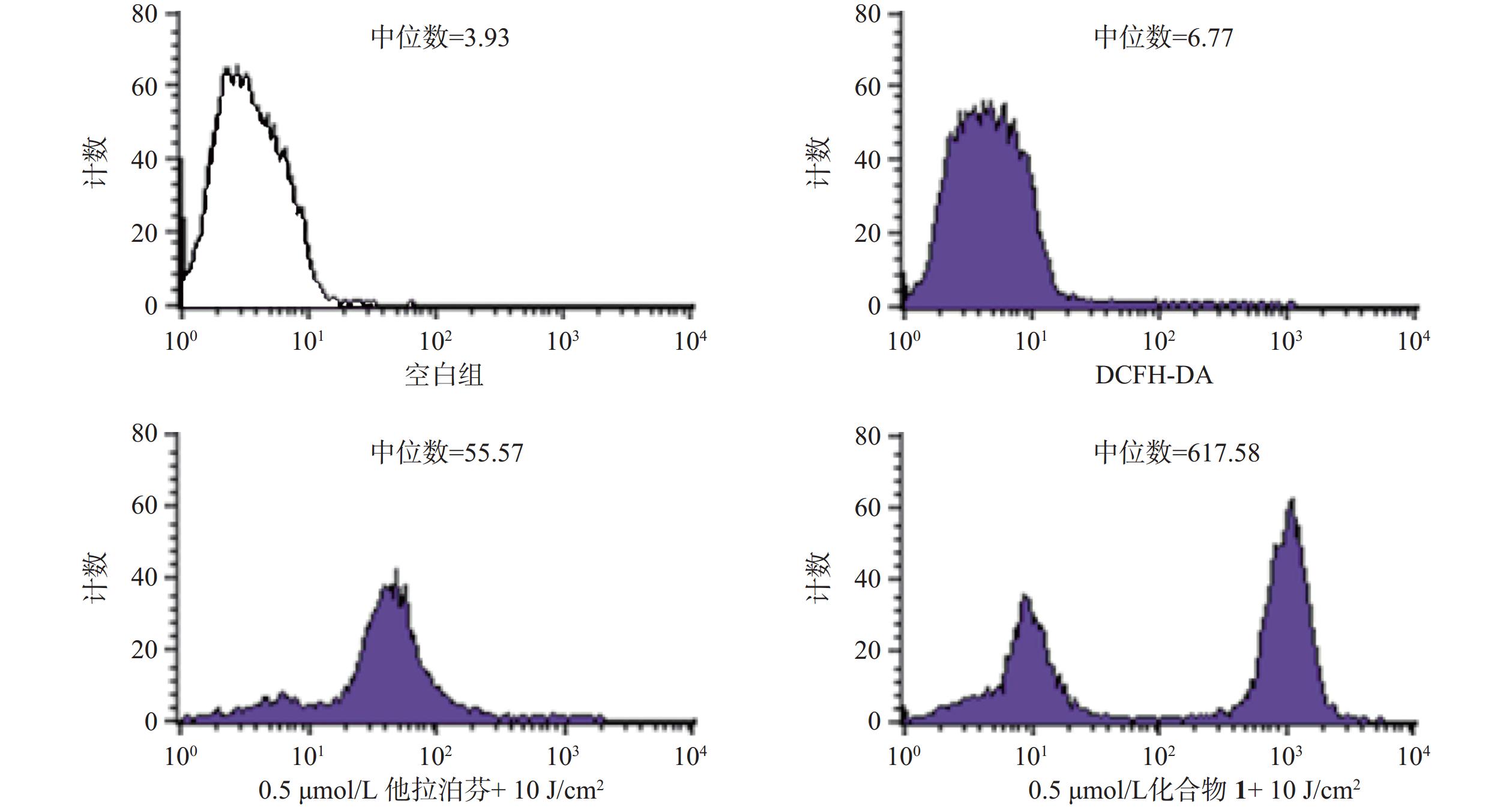
操作步骤如下:a. 每孔3 × 105个B16-F10细胞悬液(2 ml)接种6孔板上,按“2.3.1”项条件避光孵育24 h;b. 分别更换含一定浓度化合物1或他拉泊芬的新鲜培养液(DMSO浓度小于1%,2 ml),继续避光孵育24 h;c. 加入10 mmol/L DCFH-DAROS荧光检测探针(Beyotime,1.5 μl),吹打混匀,继续避光孵育20 min;d. PBS洗涤3次,再加新鲜培养液(2 ml),以660 nm波长的激光辐照(光剂量10 J/cm2)细胞样品,继续避光孵育20 min;e. 收集每孔细胞样品,用流式细胞仪检测各孔细胞ROS水平,结果见图4。
2.5 化合物1介导的PDT对肿瘤细胞凋亡的影响
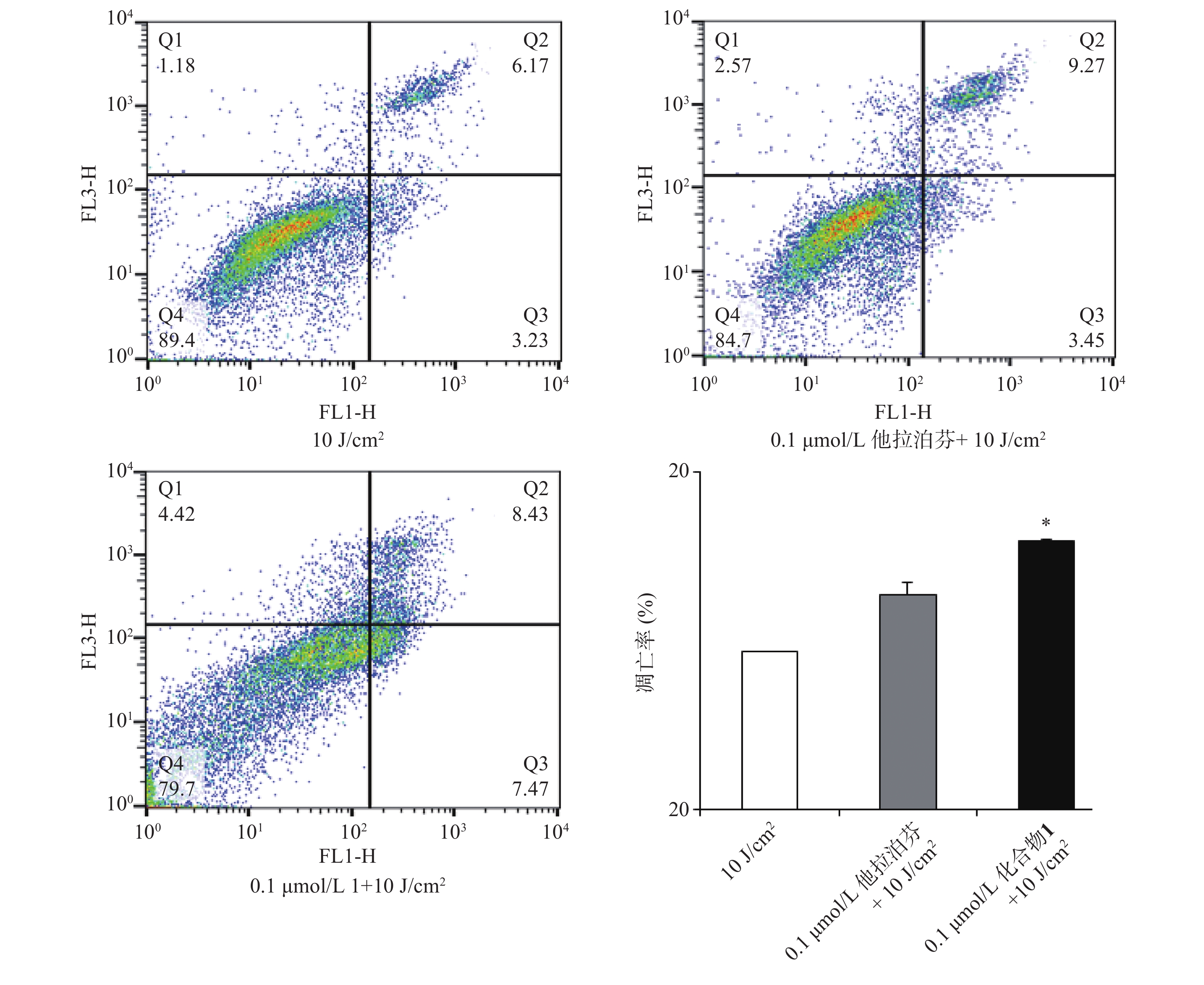
按“2.4”项下操作方法,仅从步骤c开始,更换新鲜培养液(2 ml),用660 nm波长的激光辐照(光剂量10 J/cm2)细胞样品,继续避光孵育20 min;d. 以1 500 r/min离心(5 min)细胞样品,PBS洗涤,再以1 000 r/min离心(5 min)后获取细胞样品;e. 按Annexin V-FITC细胞凋亡检测试剂盒(Beyotime)操作流程操作,结果见图5。
2.6 化合物1介导的PDT对肿瘤细胞周期的阻滞作用
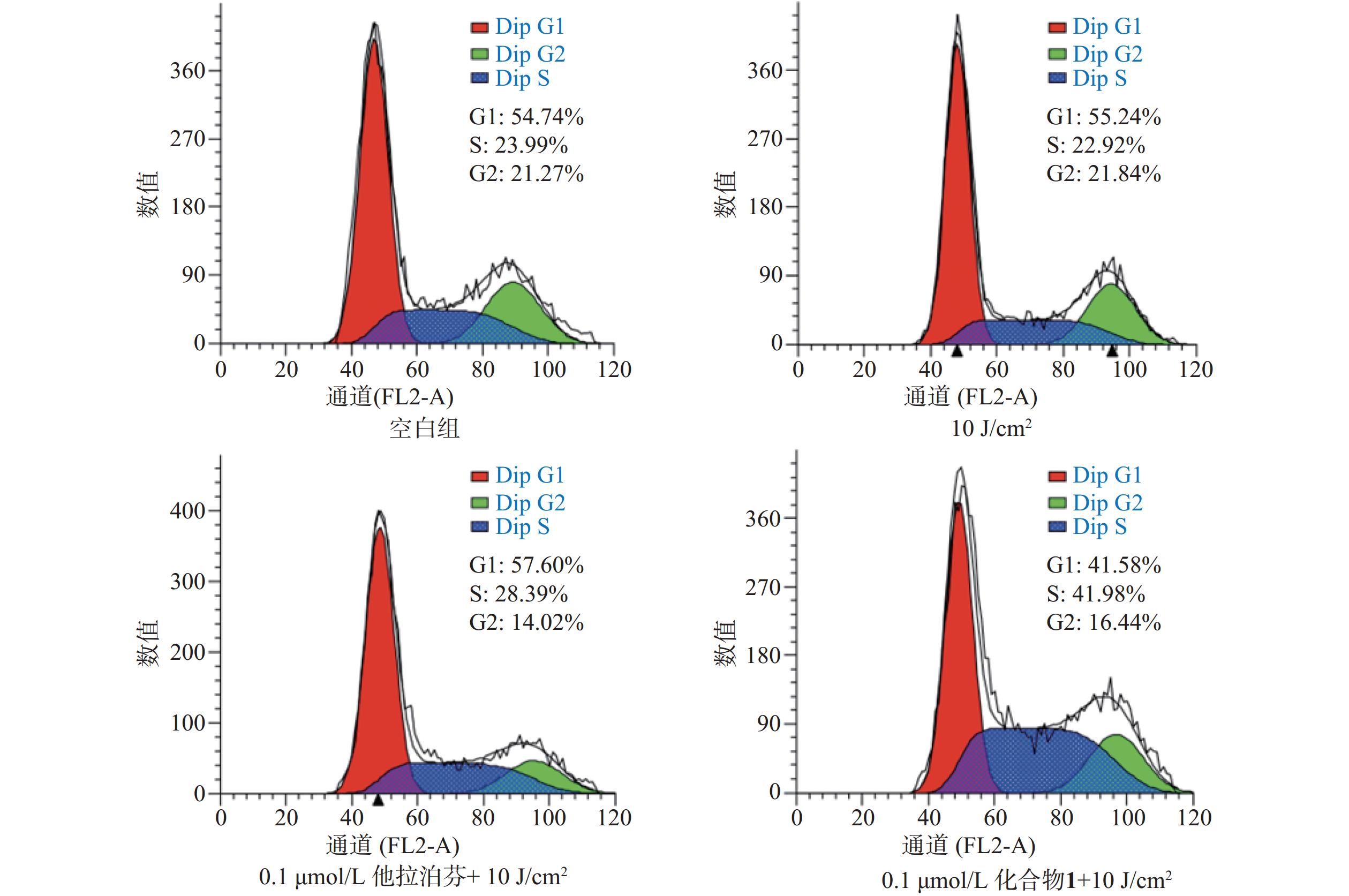
按“2.5”项下操作方法,仅在e步骤中,换以细胞周期阻滞检测试剂盒(Beyotime)的操作流程,每份细胞样品中分别加入染色缓冲液(300 µl)、RNase A(6 µl)和碘化丙啶染色液(15 µl),轻轻混匀,避光孵育20 min后,用流式细胞仪进行细胞周期阻滞检测,结果见图6。
3. 结果与讨论
按文献[14]方法制得的二氢卟吩e6(3)为先导化合物,经1-乙基-(3-二甲氨基丙基)碳二亚胺盐酸盐(EDC·HCl)于无水DMF中催化分子内脱水缩合制得二氢卟吩e6-131,152-酸酐活泼中间体[15],然后直接与中间体2发生酰化反应成功合成得到了光化疗双模抗肿瘤光敏剂二氢卟吩e6-偕氟尿嘧啶(1),反应收率达39.6%,其结构经UV、ESI-MS、1H NMR及元素分析确证。
化合物1在甲醇中最大紫外吸收波长和荧光发射波长(激发波长:400 nm)分别为660 nm和670 nm,与先导物3相一致,表明先导物3以酰腙键偶联5-Fu后,并没有改变其作为光敏剂特有的紫外吸收和荧光发射光谱等光物理特性。此外,化合物1在弱酸(pH 5.0)条件下,能有效释放5-Fu,24 h内累积释放率可达60.3%;但在pH 7.4的条件下较为稳定,24 h内5-Fu累积释放率仅为5%。
体外PDT抗癌活性测试结果显示,化合物1对B16-F10和HepG2细胞株的光毒活性和暗毒/光毒比(治疗指数)均显著优于先导物二氢卟吩e6(3)(P<0.005)和他拉卟吩(P<0.001),其IC50值分别达0.73 μmol/L和0.90 μmol/L。
体外PDT抗癌机制研究提示,化合物1介导的PDT能显著提升B16-F10细胞内ROS水平和诱导B16-F10细胞凋亡,并阻滞肿瘤细胞周期于S期。
总之,二氢卟吩e6-偕氟尿嘧啶(1)具有PDT抗癌活性强、治疗指数(暗毒/光毒比)高且可在肿瘤弱酸环境中有效释放5-Fu等优点,从而实现“单分子”光化疗协同抗肿瘤作用,值得进一步开发研究。
-
[1] SATIN L S, SOLEIMANPOUR S A, WALKER E M. New aspects of diabetes research and therapeutic development[J]. Pharmacol Rev, 2021, 73(3):1001-1015. doi: 10.1124/pharmrev.120.000160 [2] HUANG X Y, CHU Y, REN H, et al. Antioxidation function of EGCG by activating Nrf2/HO-1 pathway in mice with coronary heart disease[J]. Contrast Med Mol Imaging, 2022, 2022:1-8. [3] SUN H, SAEEDI P, KARURANGA S, et al. IDF Diabetes Atlas: Global, regional and country-level diabetes prevalence estimates for 2021 and projections for 2045[J]. Diabetes Res Clin Pract, 2022, 183:109119. doi: 10.1016/j.diabres.2021.109119 [4] TIAN X, GAO Y, ZHONG M, et al. The association between serum Sestrin2 and the risk of coronary heart disease in patients with type 2 diabetes mellitus[J]. BMC Cardiovas Disord, 2022, 22(1):1-8. doi: 10.1186/s12872-021-02434-3 [5] CAI X L, SHEN J, YE B Q, et al. Characteristics, treatment patterns, and glycemic control of older type 2 diabetes mellitus patients in China[J]. Chin Med J, 2021, 134(23):2893-2895. doi: 10.1097/CM9.0000000000001674 [6] KATSIKI N, BANACH M, MIKHAILIDIS D P. Is type 2 diabetes mellitus a coronary heart disease equivalent or not? Do not just enjoy the debate and forget the patient![J]. Arch Med Sci, 2019, 15(6):1357-1364. doi: 10.5114/aoms.2019.89449 [7] 钟钰灵. 基于网络药理学的麝香保心丸治疗冠状动脉微循环疾病的机制研究[D]. 桂林: 桂林医学院, 2022. [8] 叶健, 李凌燕, 席鑫, 等. 麝香保心丸基于miR-144-3p/SLC7A11通路减轻心肌细胞铁死亡的机制研究[J]. 中国中西医结合杂志, 2022, 42(11):1335-1340. [9] 李芃琪, 信琪琪, 袁蓉, 等. 麝香保心丸调控冠心病血管新生的研究进展[J]. 中国实验方剂学杂志, 2022, 28(14):242-253. [10] 侯志杰. 麝香保心丸治疗冠心病合并2型糖尿病患者55例临床观察[J]. 医学理论与实践, 2014, 27(20):2701-2702. [11] 费震宇, 徐玫, 陈宇明, 等. 麝香保心丸对2型糖尿病患者尿微量白蛋白/肌酐比值的影响[J]. 上海医药, 2020, 41(10):23-25. [12] 李勇萍, 杜从云, 刘桃喜. 麝香保心丸对冠心病伴糖尿病患者发生心血管临床事件的影响分析[J]. 中西医结合心血管病电子杂志, 2018, 6(18): 163, 166. [13] 华姞安, 孟靓, 孟智睿, 等. 中成药治疗2型糖尿病用药规律及作用靶点分析[J]. 世界中医药, 2023, 18(5):692-698,703. doi: 10.3969/j.issn.1673-7202.2023.05.019 [14] 卢李娜, 郑娴. 从气虚血瘀论治冠心病的研究进展[J]. 实用中医内科杂志, 2023, 37(4):38-41. [15] 中国医师协会中西医结合医师分会心血管病专业委员会, 国家中医心血管病临床医学研究中心. 麝香保心丸治疗冠心病专家共识[J]. 中国中西医结合杂志, 2022, 42(7):782-790. [16] 李桂梅, 谢秀峰. 麝香保心丸配合强化抗血小板治疗对急性心肌梗死合并糖尿病患者疗效研究[J]. 创伤与急危重病医学, 2020, 8(6):426-430. [17] 郭施勉, 楚英杰. 人参皂苷Rg1对冠心病大鼠心肌细胞凋亡的影响及机制研究[J]. 中西医结合心脑血管病杂志, 2021, 19(23):4054-4059. doi: 10.12102/j.issn.1672-1349.2021.23.008 [18] ZHOU P, XIE W J, HE S B, et al. Ginsenoside Rb1 as an anti-diabetic agent and its underlying mechanism analysis[J]. Cells, 2019, 8(3):204. doi: 10.3390/cells8030204 [19] FAN X, ZHANG C, NIU S, et al. Ginsenoside Rg1 attenuates hepatic insulin resistance induced by high-fat and high-sugar by inhibiting inflammation[J]. Eur J Pharmacol, 2019, 854:247-255. doi: 10.1016/j.ejphar.2019.04.027 [20] CHANG X, ZHANG T, ZHANG W, et al. Natural drugs as a treatment strategy for cardiovascular disease through the regulation of oxidative stress[J]. Oxidative Med Cell Longevity, 2020, 2020:5430407. [21] LI W, QIAO J, LIN K, et al. Ethyl-acetate fraction from a cinnamon-cortex extract protects pancreatic β-cells from oxidative stress damage[J]. Front Pharmacol, 2023, 14:1111860. doi: 10.3389/fphar.2023.1111860 [22] NAIR A, PREETHA RANI M R, SALIN RAJ P, et al. Cinnamic acid is beneficial to diabetic cardiomyopathy via its cardioprotective, anti-inflammatory, anti-dyslipidemia, and antidiabetic properties[J]. J Biochemi Molecular Toxicol, 2022, 36(12):e23215. doi: 10.1002/jbt.23215 [23] 王笑, 张恒, 李媛媛, 等. 肉桂醛预处理对H9C2心肌细胞缺氧复氧损伤后自噬的影响[J]. 中药药理与临床, 2021, 37(3):30-34. [24] 赵丹, 王明慧, 张程斐, 等. 肉桂酸对db/db小鼠肝脏PI3K/AKT/FoxO1信号通路的影响[J]. 世界科学技术(中医药现代化), 2021, 23(10):3613-3620. [25] CHEN Y S, LIU H M, LEE T Y. Ursodeoxycholic acid regulates hepatic energy homeostasis and white adipose tissue macrophages polarization in leptin-deficiency obese mice [J]. Cells, 2019, 8(3):253. [26] LI D D, ZHONG J X, ZHANG Q R, et al. Effects of anti-inflammatory therapies on glycemic control in type 2 diabetes mellitus[J]. Front Immunol, 2023, 14:1125116. doi: 10.3389/fimmu.2023.1125116 [27] AKBARI M, HASSAN-ZADEH V. IL-6 signalling pathways and the development of type 2 diabetes[J]. Inflammopharmacol, 2018, 26(3):685-698. doi: 10.1007/s10787-018-0458-0 [28] RIDKER P M, RANE M. Interleukin-6 signaling and anti-interleukin-6 therapeutics in cardiovascular disease[J]. Circ Res, 2021, 128(11):1728-1746. doi: 10.1161/CIRCRESAHA.121.319077 [29] WAGNER N, WAGNER K D. Pharmacological utility of PPAR modulation for angiogenesis in cardiovascular disease[J]. Int Mol Sci, 2023, 24(3):2345. doi: 10.3390/ijms24032345 [30] JIN J L, ZHU C, WANG J X, et al. The association between ACTB methylation in peripheral blood and coronary heart disease in a case-control study[J]. Front Cardiovasc Med, 2022, 9:972566. doi: 10.3389/fcvm.2022.972566 [31] BOUTCHUENG-DJIDJOU M, BELLEAU P, BILODEAU N, et al. A type 2 diabetes disease module with a high collective influence for Cdk2 and PTPLAD1 is localized in endosomes[J]. PLoS One, 2018, 13(10):e0205180. doi: 10.1371/journal.pone.0205180 [32] WAGHELA B N, VAIDYA F U, RANJAN K, et al. AGE-RAGE synergy influences programmed cell death signaling to promote cancer[J]. Mol Cell Biochem, 2021, 476(2):585-598. doi: 10.1007/s11010-020-03928-y [33] SHEN C Y, LU C H, WU C H, et al. The development of Maillard reaction, and advanced glycation end product (AGE)-receptor for AGE (RAGE) signaling inhibitors as novel therapeutic strategies for patients with AGE-related diseases[J]. Mol, 2020, 25(23):5591. doi: 10.3390/molecules25235591 [34] KOSMOPOULOS M, DREKOLIAS D, ZAVRAS P D, et al. Impact of advanced glycation end products (AGEs) signaling in coronary artery disease[J]. Biochim Biophys Acta BBA Mol Basis Dis, 2019, 1865(3):611-619. doi: 10.1016/j.bbadis.2019.01.006 [35] BRENNAN J J, GILMORE T D. Evolutionary origins of toll-like receptor signaling[J]. Mol Biol Evol, 2018, 35(7):1576-1587. doi: 10.1093/molbev/msy050 [36] KOUSHKI K, SHAHBAZ S K, MASHAYEKHI K, et al. Anti-inflammatory action of statins in cardiovascular disease: the role of inflammasome and toll-like receptor pathways[J]. Clinic Rev Allerg Immunol, 2021, 60(2):175-199. doi: 10.1007/s12016-020-08791-9 [37] AAMIR K, KHAN H U, SETHI G, et al. Wnt signaling mediates TLR pathway and promote unrestrained adipogenesis and metaflammation: therapeutic targets for obesity and type 2 diabetes[J]. Pharmacol Res, 2020, 152:104602. doi: 10.1016/j.phrs.2019.104602 [38] ZACCOLO M, ZERIO A, LOBO M J. Subcellular organization of the cAMP signaling pathway[J]. Pharmacol Rev, 2021, 73(1):278-309. doi: 10.1124/pharmrev.120.000086 [39] WANG Y N, LIU Q, KANG S G, et al. Dietary bioactive ingredients modulating the cAMP signaling in diabetes treatment[J]. Nutrients, 2021, 13(9):3038. doi: 10.3390/nu13093038 [40] SADEK M S, CACHORRO E, EL-ARMOUCHE A, et al. Therapeutic implications for PDE2 and cGMP/cAMP mediated crosstalk in cardiovascular diseases[J]. Int J Mol Sci, 2020, 21(20):7462. [41] 张晓囡, 孙长鑫, 陈纪烨, 等. 基于“异病同治”理论探讨四妙勇安汤在心血管疾病中的应用[J]. 中西医结合心脑血管病杂志, 2023, 21(5):946-949. doi: 10.12102/j.issn.1672-1349.2023.05.040 -





 下载:
下载:
 下载:
下载: