-
头癣、体癣、手癣等皮肤病多由浅部真菌感染引起,发病率高,可达全部皮肤病的25%左右。常用的市售制剂存在多个问题,首先,药效不全面。浅部真菌感染常合并有细菌感染[1-2],因此单纯给予抗真菌药物无法根治疾病。其次,耐药性。市售复方酮康唑乳膏虽然结合了抗真菌和抗细菌药物,但选用的硫酸新霉素易导致细菌产生耐药性。最后,皮肤安全性。为产生抗过敏作用,市售复方酮康唑乳膏中添加了丙酸氯倍他索,但易导致皮肤烧灼感、瘙痒刺痛和皮肤萎缩,长期大面积用药可导致高血糖、尿糖等不良反应[3]。对此,前期研究制备并优化了新型复方酮康唑软膏,含有酮康唑、莫匹罗星和糠酸莫米松[4]。其中,莫匹罗星是新型抗菌药物,通过结合细菌异亮氨酸转RNA合成酶,阻断异亮氨酸的供给,导致细菌死亡,具有广谱、高效、不易发生过敏、不易发生交叉耐药和多重耐药等优势[5-6]。糠酸莫米松属于强效糖皮质激素,皮肤不良反应极为少见。
在此基础上,本课题重点研究自制的复方酮康唑软膏的体外抑菌作用,并对其皮肤刺激性和变态反应进行考察,从而证明自制制剂的有效性和安全性,并说明选择3种药物的合理性。
-
生物安全柜(HFsafe1200型,上海力申科学仪器有限公司);隔水式恒温培养箱(303-6B型,南通科学仪器厂);霉菌培养箱(MJ-160型,上海跃进医疗器械厂);LDZX-40KBS立式压力蒸汽灭菌器(上海申安医疗器械厂)。
-
自制复方酮康唑软膏(第九〇〇医院药学科制备,含酮康唑,莫匹罗星,糠酸莫米松,批号20171220);复方酮康唑乳膏(含酮康唑,丙酸氯倍他索,硫酸新霉素,批号1408028,上海宝龙药业有限公司);莫匹罗星软膏(含莫匹罗星,批号20161006,人福医药有限公司);酮康唑乳膏(含酮康唑,批号150302,福建太平洋制药有限公司)。
-
红色毛癣菌CMCC(F)T1a、须癣毛癣菌CMCC(F)T5a、断发毛癣菌CMCC(F)T4b、犬小孢子菌CMCC(F)M3d、石膏样小孢子菌CMCC(F)M2c、裴氏着色真菌CMCC(F)M2c,均购自中国医学科学院皮肤病研究所。
-
参考前期研究制备软膏[4],酮康唑、莫匹罗星和糠酸莫米松的含量依次为2%、2%和0.1%。同时,制备缺酮康唑的阴性对照软膏、缺莫匹罗星的阴性对照软膏分别用于抗真菌试验、抗细菌试验。
-
取直径9 cm的培养皿,加入20 ml培养液,制成培养基平板。细菌用营养琼脂培养基,37 ℃培养1~3 d;真菌用沙堡弱培养基,28 ℃培养5~7 d。菌落形成后,挑取一定量的菌落,加入1 ml灭菌蒸馏水,充分混合均匀。采用紫外分光光度计调整菌悬液浊度为0.5,相当于5×10 CFU/ml。用无菌棉签蘸取菌悬液,均匀涂布于实验用培养基平皿表面。
采用定性滤纸制成直径7 mm的圆形纸片、经灭菌,尔后分别浸入空白软膏(不含药)、自制复方酮康唑软膏、以及市售的复方酮康唑乳膏、酮康唑乳膏和莫匹罗星软膏的甲醇溶液中,待药液完全浸润纸片后,取出纸片放置于已涂布菌悬液的培养基表面。细菌置隔水式恒温培养箱37 ℃培养3 d,真菌置霉菌培养箱28 ℃培养7 d。观察各药敏纸片周围抑菌圈,并测定其直径值(长径与短径的平均值, mm),每株菌同时做3个平板。
-
实验计量数据用平均值±标准差(
${{\overline x}}\pm s$ )表示,采用SPSS 19.0统计软件对数据进行单因素方差分析(两两间比较用LSD法),以P<0.05表示有统计学差异[7-9]。 -
实验结果表明,莫匹罗星软膏和空白软膏的纸片均被真菌包围,而其余3种制剂的纸片均产生了明显的抑菌圈。自制软膏、市售的酮康唑乳膏和复方酮康唑乳膏的抑菌圈直径相当(P>0.05),对不同真菌的抑菌圈直径大小为:断发毛癣菌>石膏样小孢子菌>裴氏着色真菌>须癣毛癣菌>犬小孢子菌>红色毛癣菌。由此可知,各制剂的抑菌圈直径大小顺序为:自制复方酮康唑软膏=复方酮康唑乳膏=酮康唑乳膏>莫匹罗星软膏=阴性对照软膏。提示自制复方酮康唑软膏对真菌的抑菌活性与市售单成分酮康唑乳膏、复方成分的复方酮康唑乳膏相当,结果见表1。
表 1 自制与市售制剂对几种皮肤真菌抑菌试验结果(抑菌圈直径/mm)
真菌 自制制剂复方酮康唑软膏 市售制剂 缺酮康唑阴性对照软膏 酮康唑乳膏 复方酮康唑乳膏 莫匹罗星软膏 须癣毛癣菌 32.14±0.74 32.34±0.42 32.55±0.38 7.00±0.00 7.00±0.00 红色毛癣菌 17.15±0.15 17.11±0.18 16.99±0.03 7.00±0.00 7.00±0.00 断发毛癣菌 48.02±0.04 48.23±0.17 48.16±0.14 7.00±0.00 7.00±0.00 犬小孢子菌 30.06±0.05 30.03±0.06 29.97±0.19 7.00±0.00 7.00±0.00 石膏样小孢子菌 38.10±0.07 38.05±0.15 38.08±0.09 7.00±0.00 7.00±0.00 裴氏着色真菌 34.07±0.35 33.84±0.57 34.04±0.10 7.00±0.00 7.00±0.00 -
在2种细菌的培养皿中,各组对铜绿假单胞菌均未产生抑菌圈;对金黄色葡萄球菌,空白软膏和市售的酮康唑乳膏未产生抑菌圈,其余制剂产生了明显的抑菌圈。自制软膏与市售莫匹罗星软膏的抑菌圈直径均为20 mm左右(P>0.05),且均显著大于复方酮康唑乳膏(P<0.01)。由此可知,各制剂的抑菌圈直径大小顺序为:自制酮康唑软膏=莫匹罗星软膏>复方酮康唑乳膏>酮康唑乳膏=阴性对照组软膏,结果见表2。
表 2 自制与市售制剂对两种细菌的抑菌试验结果(抑菌圈直径/mm)
细菌 自制制剂复方酮康唑软膏 市售制剂 缺莫匹罗星阴性对照软膏 酮康唑乳膏 复方酮康唑乳膏 莫匹罗星软膏 金黄色葡萄球菌 20.76±0.14 7.02±0.01 13.19±0.08 20.74±0.09 7.01±0.01 铜绿假单胞菌 7.00±0.00 7.01±0.02 7.01±0.01 7.00±0.01 7.01±0.01 -
取雌雄各半的健康家兔4只,于试验前24 h,在家兔背部脊柱两侧对称划定左、右各3 cm×3 cm的相同区域。用电剪刀剔除兔毛后,用硫化钠溶液进行脱毛处理,并于脱毛24 h后,检查去毛处皮肤是否损伤,排除损伤皮肤。采用同体左右侧自身对比法,设给药组(自制复方酮康唑软膏)与对照组(空白软膏)。家兔背部左侧皮肤涂布空白软膏,右侧皮肤涂布0.5 g复方酮康唑软膏,然后用一层玻璃纸和二层纱布覆盖,再用胶布和绷带加以固定。
采用封闭实验,贴敷时间为4 h。实验结束后除去受试药品并用温水清洁给药部位,在自然光线下观察皮肤反应。于清洗后的1、24、48、72 h观察涂抹部位皮肤反应,按表3进行皮肤刺激反应评分,并计算受试动物积分的平均值,按表4判断皮肤刺激强度。
表 3 皮肤刺激反应评分
皮肤反应 具体表现 分值 红斑和
焦痂无 0 非常轻的红斑,勉强可见 1 明显的红斑 2 中度至重度的红斑 3 重度红斑(鲜红色)至轻度焦痂形成(深层损伤) 4 水肿 无 0 非常轻度的水肿,勉强可见 1 轻度水肿(边缘清晰) 2 中度水肿(皮肤隆起约1 mm) 3 重度水肿(皮肤隆起大于1 mm,超过涂抹区域) 4 表 4 皮肤刺激强度分级
积分均值 强度 0~<0.5 无刺激性 0.5~<2.0 轻刺激性 2.0~<6.0 中刺激性 6.0~8.0 强刺激性 观察发现,实验组仅有1只家兔出现勉强可见的轻微红斑,其余均未出现红斑、充血、水肿等刺激症状。根据表3评分,对照组皮肤刺激反应平均积分值为0,而实验组的分值小于0.5(表5),根据表4可认为复方酮康唑软膏单次给药对皮肤无刺激性。
表 5 自制复方酮康唑软膏皮肤单次刺激性试验评分结果
时间 (h) 对照组 实验组 No.1 No.2 No.3 No.4 总积分 平均分 No.1 No.2 No.3 No.4 总积分 平均分 1 0 0 0 0 0 0 0 0 0 0 0 0 24 0 0 0 0 0 0 0 0 1 0 1 0.25 48 0 0 0 0 0 0 0 0 1 0 1 0.25 72 0 0 0 0 0 0 0 0 1 0 1 0.25 -
多次刺激性试验中家兔的处理方法和初次给药方法与“2.3.1”项下相同,不同的是,对照组和给药组每天涂抹1次,给药时间持续涂抹14 d。从第2天开始,每次涂抹前修剪毛,用温水清除残留受试物1 h后观察,按表3评分。最后按公式每天每只动物平均积分=红斑和水肿积分总和/(受试动物×14),计算平均积分,以表4判断皮肤刺激强度分级。
多次给药后定期观察发现,对照组的家兔在各时间均未出现红斑、充血和水肿等皮肤刺激。实验组有2只家兔在8、12、13和14 d时出现极轻微的红斑,平均分值为0.25,在其余时间所有家兔无红斑、充血等刺激症状(表6),根据表4可认为复方酮康唑软膏多次给药对皮肤无刺激性。
表 6 自制复方酮康唑软膏皮肤多次刺激性试验评分结果
时间(d) 左侧 右侧 No.1 No.2 No.3 No.4 总积分 平均分 No.1 No.2 No.3 No.4 总积分 平均分 1 0 0 0 0 0 0 0 0 0 0 0 0 2 0 0 0 0 0 0 0 0 0 0 0 0 3 0 0 0 0 0 0 0 0 0 0 0 0 4 0 0 0 0 0 0 0 0 0 0 0 0 5 0 0 0 0 0 0 0 0 0 0 0 0 6 0 0 0 0 0 0 0 0 0 0 0 0 7 0 0 0 0 0 0 0 0 0 0 0 0 8 0 0 0 0 0 0 0 0 0 1 1 0.25 9 0 0 0 0 0 0 0 0 0 0 0 0 10 0 0 0 0 0 0 0 0 0 0 0 0 11 0 0 0 0 0 0 0 0 0 0 0 0 12 0 0 0 0 0 0 0 0 0 1 1 0.25 13 0 0 0 0 0 0 0 1 0 0 1 0.25 14 0 0 0 0 0 0 0 1 0 0 1 0.25 -
采用豚鼠为试验动物,试验前约24 h,将豚鼠背部左侧2 cm×2 cm区域的毛剔短后,用硫化钠溶液进行脱毛处理。脱毛后24 h,检查去毛处皮肤是否损伤,有损伤的皮肤不宜进行试验。
试验分为2个阶段,首先在诱导接触阶段,将约0.5 g样品涂于豚鼠皮肤上,用一层玻璃纸和二层纱布覆盖,再以胶布封闭固定6 h;第7天和14天同法重复一次。在激发接触阶段,于末次诱导接触后14~28 d,将约0.2 g的样品涂于豚鼠背部右侧2 cm×2 cm去毛区(接触前24 h脱毛),然后用一层玻璃纸和二层纱布覆盖,再以无刺激胶布固定6 h。激发接触后24 h和48 h观察皮肤反应,按表3评分,当受试组动物出现皮肤反应积分≥2时,认为该动物出现皮肤变态反应(阳性),按表7判定受试物的致敏强度。
表 7 致敏强度分级
致敏率(%) 分级 过敏反应强度 0~8 Ⅰ 弱致敏 9~28 Ⅱ 轻度致敏 29~64 Ⅲ 中度致敏 65~80 Ⅳ 强致敏 81~100 Ⅴ 极强致敏 将豚鼠随机分为3组,实验组和阳性对照组均含20只豚鼠,阴性对照组含10只豚鼠。实验组采用上述的复方酮康唑软膏,阳性对照组和阴性对照组的处理方法与实验组基本相同,但阳性对照组采用2,4-二硝基氯代苯为样品,而阴性对照组在诱导接触时不给予任何样品,在激发接触时给予自制复方酮康唑软膏。实验结果如表8所示,自制复方酮康唑软膏致敏率为0,无皮肤变态反应。
表 8 自制复方酮康唑软膏对豚鼠皮肤变态反应试验结果
组别 动物数(只) 观察时间(h) 皮肤反应强度评分 阳性动物数(只) 致敏率(%) 0 1 2 3 4 阴性对照 10 24 10 0 0 0 0 0 0 48 10 0 0 0 0 0 0 给药组 20 24 20 0 0 0 0 0 0 48 20 0 0 0 0 0 0 阳性对照 20 24 3 3 11 3 0 14 70 48 2 4 13 1 0 14 70 -
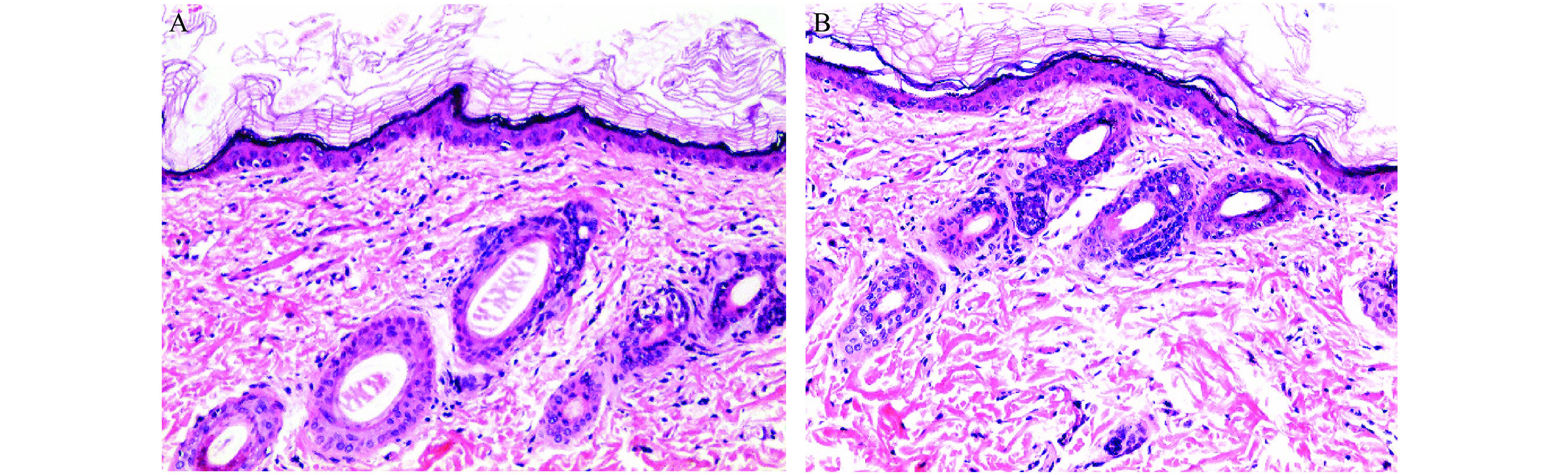
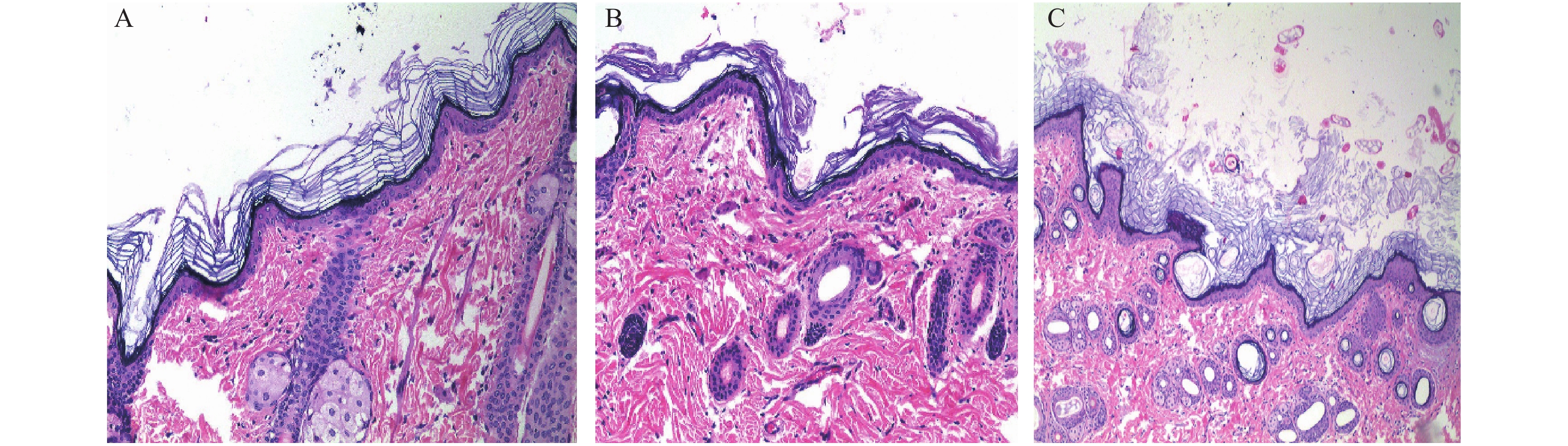
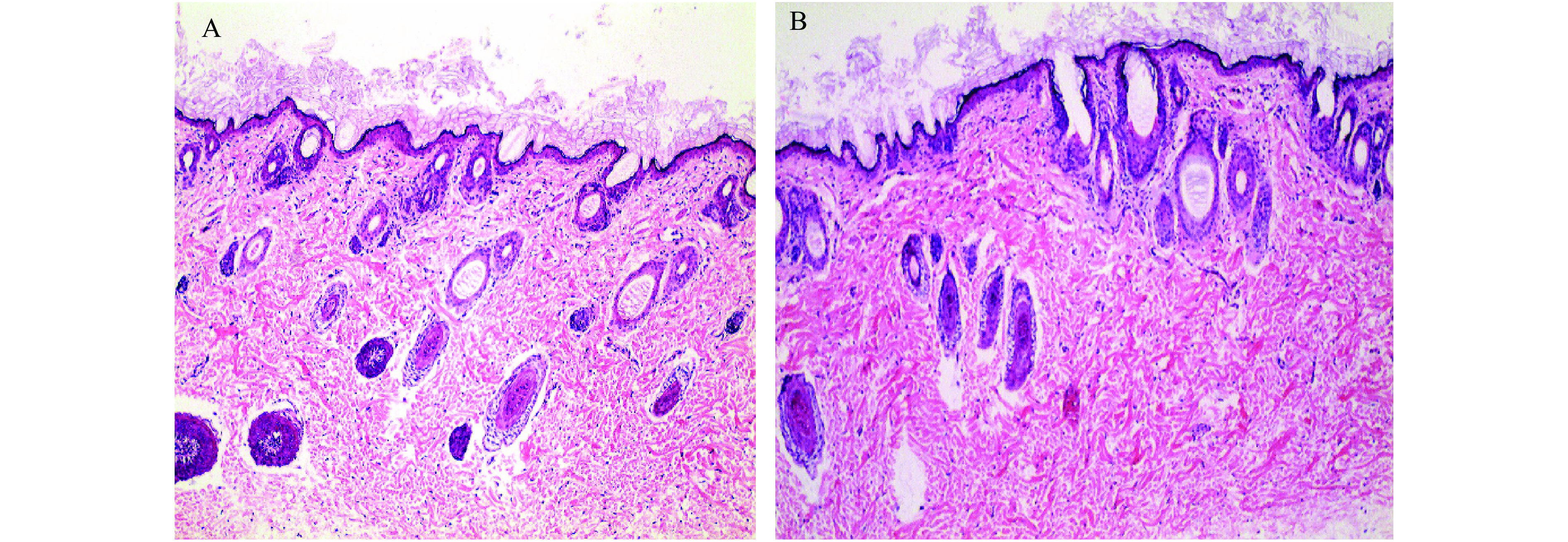
在单次、多次刺激性试验和皮肤变态反应试验之后,将试验动物处死,并取左右侧皮肤,经4%多聚甲醛固定、脱水、透明、浸蜡、包埋及切片后,进行HE染色,最后在倒置相差显微镜下观察皮肤。如图1、2、3所示,在单次、多次刺激性试验和皮肤变态反应试验中,给予自制软膏后,皮肤的各层结构完整,与对照组的正常皮肤组织基本一致。
-
浅部真菌病主要由毛癣菌属、小孢子菌属和表皮癣菌属引起[13-14],其中红色毛癣菌和须癣毛癣菌是手、足癣中最常见的真菌,70%以上的病例中均可检出[15],本研究中抗真菌实验选择的菌种均为皮肤癣菌病的最常见的致病菌。酮康唑是抑制真菌的常用药物,本实验显示,自制软膏抗真菌活性与市售制剂相当,特别是在断发毛癣菌、须癣毛癣菌、石膏样小孢子菌方面表现出较强的杀菌活性。
在抗细菌方面,常见浅表局限性皮肤及软组织感染,其引起的病原菌相对简单和明确,主要是金葡菌和化脓性链球菌[16]。限于实验室条件,本实验仅选取现有的金黄色葡萄球菌和铜绿假单胞菌两种细菌为试验菌种。实验显示,铜绿假单胞菌不在莫匹罗星抗菌谱中;而含有莫匹罗星的自制软膏在抗金黄色葡萄球菌活性上大大优于市售酮康唑类产品,说明莫匹罗星是本处方较为理想的选择。
浅部真菌感染经治疗后极易复发的重要原因之一是合并细菌感染。有报道称将市售的复方酮康唑乳膏与莫匹罗星软膏交替使用,可对真菌性皮肤溃疡患者有更好的治疗作用[17]。本研究表明自制复方酮康唑软膏兼具显著的抗真菌和细菌作用,优于多数市售制剂,且单次给药和多次给药的刺激性试验和皮肤变态反应试验表明,自制软膏具有良好的安全性。
自制复方酮康唑软膏的药物组成为浅部真菌感染提供了一种更加简便、有效的治疗手段。综合药效结果和安全性结果,自制软膏有望成为在皮肤浅部真菌感染疾病中,替代市售制剂成为更加优越的选择。
Study on pharmacodynamics and safety of self-made compound ketoconazole ointment
-
摘要:
目的 评价自制复方酮康唑软膏的药效学和安全性。 方法 采用纸片扩散法,选取6种真菌和2种细菌,考察自制软膏及3种市售制剂对抑菌圈直径的影响。另外,采用单次和多次给药的皮肤刺激性,及皮肤变态反应,评价自制软膏的安全性。 结果 自制软膏与含酮康唑的市售制剂类似,均对6种真菌产生了显著的抑菌圈。对铜绿假单胞菌,各制剂均未产生抑菌圈;对金黄色葡萄球菌,自制软膏与市售莫匹罗星软膏的抑菌圈相似,且显著大于其他市售制剂。给予自制软膏后,皮肤刺激反应评分均小于0.5,致敏率为0,组织结构与正常皮肤无差异。 结论 自制的复方酮康唑软膏的抑菌性能优于多数市售制剂,且具有良好的皮肤安全性,有望用于皮肤浅部真菌感染的治疗。 Abstract:Objective To evaluate the pharmacodynamics and safety of the self-made compound ketoconazole ointment. Methods Using the disk diffusion test, 6 kinds of fungi and 2 kinds of bacteria were selected to investigate the effect of the self-made ointment and 3 commercial products on the diameter of the bacteriostatic circle. In addition, the skin irritation and skin allergies of the single and multiple applications were used to evaluate the safety of the self-made ointment. Results The self-made ointment was similar to the commercial products containing ketoconazole. They all showed remarkable bacteriostatic circle against the 6 kinds of fungi. For pseudomonas aeruginosa, none of the preparations contributed to visible bacteriostatic circle. For staphylococcus aureus, the bacteriostatic circle of the self-made ointment was similar to that of commercial mupirocin ointment and was significantly larger than other commercial products. After the treatment with the self-made ointment, the score of the skin irritation was below 0.5 and the sensitization rate was 0. There was no difference in tissue structure between treated and normal skin. Conclusion The self-made compound ketoconazole ointment has better safety and better antibacterial property than the commercial products. It is expected to be used for the treatment of superficial skin fugle infections. -
Key words:
- ketoconazole /
- mupirocin /
- mometasone furoate /
- ointment /
- antibacterial property /
- safety
-
疲劳的定义为机体生理过程不能维持其机能在一特定水平上,或不能维持预定的运动强度[1]。由于疲劳的分子机制并不清楚,目前并无真正官方认可的抗疲劳药物。一些天然产物,如人参、红景天、大蒜等,以及营养补充剂,如维生素、矿物质和肌酸等,报道有抵抗肌肉疲劳、提高运动成绩的效应,但是效果缓慢而不显著[2];苯丙胺、莫达非尼、咖啡因等药物虽能快速改善疲劳,但实质为中枢兴奋药,存在成瘾、耐受、改变生物节律等问题[3]。因此,抗疲劳药物的进一步研发,对改善生活质量、提升运动成绩、提高军事作业能力有重要意义。
组织糖原含量与疲劳的发生密切相关[4]。本课题组通过大规模化合物合成和筛选,获得了一个全新小分子化合物HMS-01,可以通过促进肝脏和肌肉组织糖原的储存,改善疲劳后组织损伤,显著增加肌肉耐力,发挥抗疲劳的作用。为了进一步了解HMS-01的药动学特点以及在组织中的分布,本课题组采用液相色谱-串联质谱(LC-MS/MS)技术[5-6],研究建立灵敏、特异的测定血浆等生物样品中HMS-01浓度的分析方法,并开展HMS-01在大鼠体内的药动学研究,为后续药物研发提供理论依据。
1. 仪器与试药
1.1 仪器
Agilent 1290 InfinityⅡ液相色谱仪(Agilent Technologies,美国)、4000 Q-Trap型串联质谱仪(AB Sciex,美国);低温高速离心机(Thermo,德国);XW 80A型涡旋混合器(医大仪器,上海);Mettler AE240十万分之一电子天平(梅特勒-托利多,瑞士);Millipore-Q超纯去离子水净化仪(Millipore,美国)。
1.2 试药
HMS-01(西安秦申嘉合药物研究有限公司,批号HMS-1-1010-3);罗红霉素(Sigma,CAS:2058-46-0);乙腈(色谱纯,Fisher Chemical);甲酸(色谱纯,Fisher Chemical);其他试剂为市售分析纯。
2. 方法与结果
2.1 色谱条件
色谱柱为Gemini C18(50 mm×2.0 mm, 5 μm),流动相:含5 mmol甲酸铵及1 mmol甲酸的水溶液(A)-含1 mmol甲酸的乙腈(B),梯度洗脱,洗脱程序如下:0~2 min,90% A;2~6 min,5% A;6~8 min,90% A。流速:0.35 ml/min,柱温:25 ℃,进样量5μl,运行时间8 min。
2.2 质谱条件
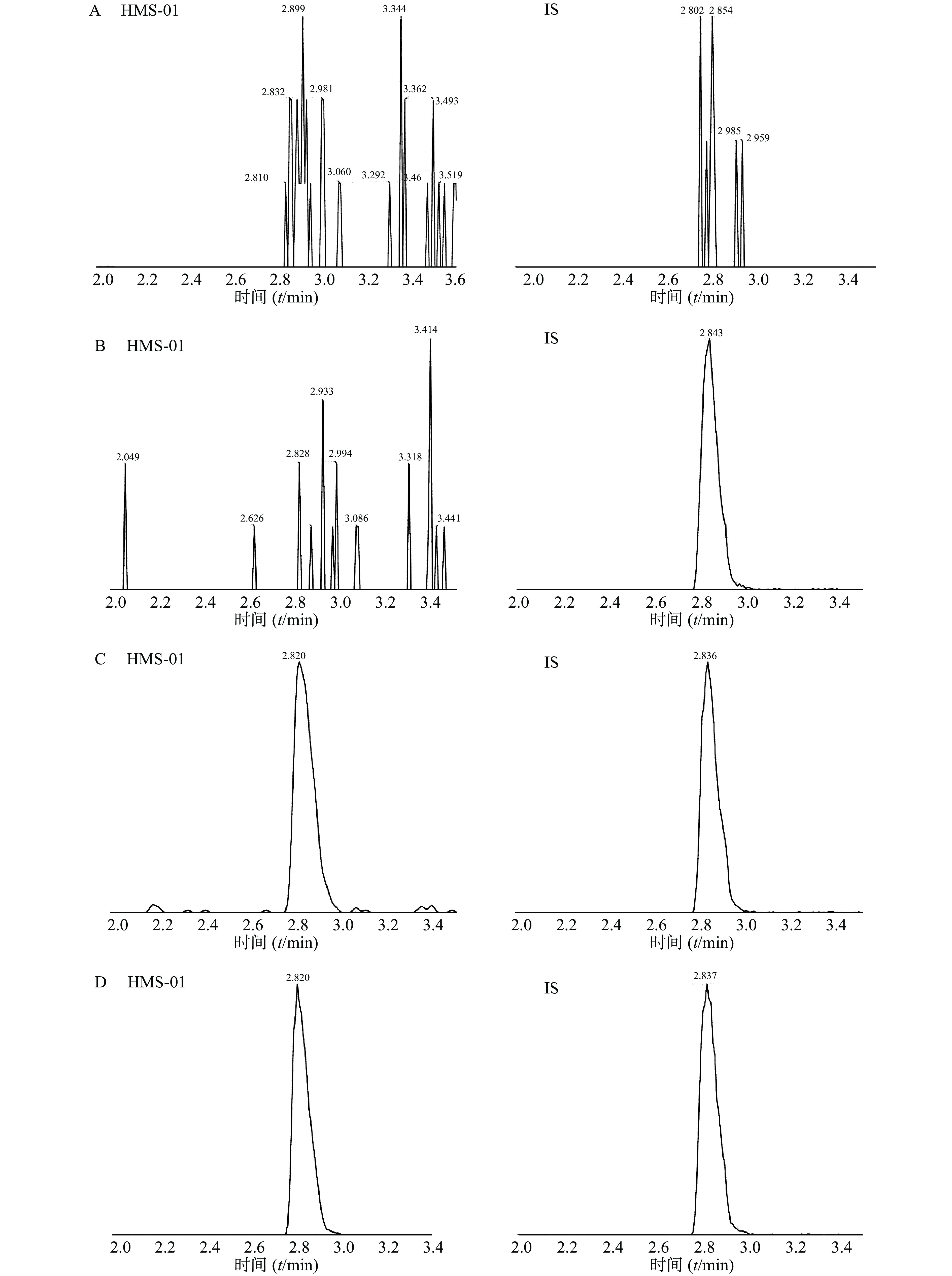
采用ESI正离子模式,多反应离子监测模式(MRM)进行二级扫描;动态反应监测的离子对参数:HMS-01 772.5→614.5;罗红霉素(IS)837.5→158.1。离子源参数设置:干燥气温度350 ℃;干燥气流速10 L/min;雾化器压力40 psi;鞘气温度400 ℃;鞘气流速11 L/min;毛细管电压4 000 V;喷嘴电压500 V。HMS-01保留时间为2.834 min,罗红霉素保留时间为2.839 min,色谱图如图1所示。
2.3 标准曲线溶液的配制和质控样品的制备
精密称取HMS-01对照品772.5 mg,置于10 ml容量瓶中,加甲醇溶解并稀释至刻度,摇匀,得质量浓度为77.25 mg/ml对照品储备液。再采用逐级稀释法配置质量浓度为772.5、386.25、193.125、96.563、48.281、24.141、12.070、6.035、3.018、1.509、0.754 ng/ml的系列含对照品血浆溶液;随行质控样品中HMS-01的低、中、高质量浓度分别为3.09、30.9、618 ng/ml。以上溶液置于4 ℃冰箱备用。
2.4 血浆样品前处理方法
取50 μl血浆样品于离心管中,加入200 μl(含41.875 ng/ml的IS内标)乙腈溶液,涡旋60 s,4 ℃条件下3 000×g离心10 min,取上清液进样。
2.5 线性关系考察
按“2.3”项和“2.4”项中的方法制备标准曲线,平行操作5份,按上述LC-MS/MS条件,连续进样分析,以对照品浓度(X)为横坐标,HMS-01的峰面积与内标的峰面积比值(Y)为纵坐标,进行线性回归,得线性方程:
Y=0.009 3 X+0.005 08, r = 0.999 3,
线性范围为0.976~1 000 ng/ml,以信噪比为3或5时测得HMS-01的最低定量限均为976 pg/ml。
2.6 精密度试验
按“2.3”项和“2.4”项中的方法制备低、中、高3种浓度的质控样品,平行操作5份,连续3 d,计算实测浓度。如表1所示,精密度用相对标准偏差(RSD)表示,结果日内精密度RSD≤12%,日间精密度RSD≤9%;准确度以相对回收率表示,实测浓度与理论加入浓度的比值即为相对回收率。结果表明日内、日间结果准确度范围在87%~106%。
表 1 HMS-01在大鼠血浆中的精密度和准确度(n=5)浓度(ng/ml) 日内 日间 实测浓度(ng/ml) 精密度(%) 准确度(%) 实测浓度(ng/ml) 精密度(%) 准确度(%) 3.09 2.71±0.27 7.7 87.9 2.71±0.27 7.5 87.9 30.9 31.4±4.8 11.8 102 32.6±3.6 8.4 106 618 618±46 5.8 100 618±46 5.4 98.4 2.7 基质效应和提取回收率
按“2.3”项和“2.4”项中的方法制备低、高2种浓度含药血浆,平行操作6份;取空白血浆按“2.4”项下处理,甲醇代替内标溶液,取处理好的空白血浆样品加入相应浓度对照品溶液,使之浓度与待测物的峰面积理论浓度一致,分别制备6份;将待测化合物标准溶液用甲醇稀释,使之与待测物的峰面积理论浓度一致,进样6次。基质效应等于(含基质样品的峰面积)/(80%乙腈溶液的峰面积),提取回收率等于(待测物的峰面积)/(含基质样品的峰面积),考察内标的基质效应和提取回收率操作步骤同上。低、高两种浓度待测物及内标提取回收率均在60%~75%之间,基质效应均在5.6%~6.1%之间,具体结果见表2。
表 2 待测物基质效应和提取回收率(n=6)待测物 浓度(ng/ml) 提取回收率(%) 基质效应(%) HMS-01 3.09 68±3 6.1 618 63±4 5.7 内标 3.35 73±2 6.1 670 73±2 5.6 2.8 稳定性试验
按“2.3”项和“2.4”项中的方法制备低、高2种浓度含药血浆,分别考察样品前处理后室温放置24 h,3次冻融循环以及-70 ℃保存30 d的稳定性,测定样品浓度,计算平均值,并计算RSD(%)及相对偏差RE(%),计算公式:RE%=(实测值−真实值)/真实值×100%。结果见表3。测定结果的RE范围为2%~17%,RSD均小于7%,表明样本稳定性良好。
表 3 样品稳定性(n =3)条件 浓度(ng/ml) RSD(%) RE(%) 室温24 h 3.09 3.7 16.5 618 1.0 2.6 3次冻融循环 3.09 6.7 4.5 618 0.6 5.9 –70 ℃保存30 d 3.06 6.8 8.7 6.18 0.6 10.1 2.9 HMS-01药动学研究
SD大鼠12只,分成2组,每组6只,雌雄各半。给药前禁食12 h,自由饮水。按30 mg/kg的剂量单次灌胃、1 mg /kg的剂量单次静注给药。灌胃给药的,于给药前和给药后5、10、20、30 min和1、1.5、2、4、6、8、10、12、24 h分别眼眶采血约100 µl;静注给药的,于给药前和给药后3、8、15、30 min和1、2、3、4、6、8、10、12、24 h分别眼眶采血约100 µl。血液用1%肝素抗凝,8 000×g离心5 min,分离血浆。–70 ℃保存待测。采血过程冰浴避光,以防止光对药物稳定性产生影响。
大鼠单次静注给予1 mg/kg HMS-01后的药动学参数(非房室模型)总结于表4。大鼠静脉注射1 mg/kg HMS-01后,雄、雌大鼠药动学参数血浆浓度-时间曲线下面积(AUC)、平均清除率(CL)显示有极显著性差异(P<0.01),药动学参数血浆消除半衰期(t1/2)、表观分布容积(V)均呈显著性差异(P<0.05)。雄性大鼠AUC0-t为221 ng·h/ml,CL为4.53 L/h·kg,为大鼠肝脏血流量(约3.3 L/h·kg)的137%,体内清除快, t1/2约为0.786 h,V为5.13 L/kg;雌性大鼠AUC0-t为409 ng·h/ml,CL为2.41 L/h·kg,为大鼠肝脏血流量的73%,体内清除较快, t1/2约为1.27 h,V为3.82 L/kg。
表 4 大鼠静注1 mg/kg HMS-01后血浆药动学参数($ \bar { x}\pm { s}$ ,n=6)性别 AUC0-t (ng·h/ml) AUC0-∞ (ng·h/ml) MRT0-∞ (t/h) t1/2z (t/h) CLz (L/h·kg) Vz (L/kg) cmax (ng/ml) 雄性 221±12.6 221±12.4 0.776±0.022 0.786±0.039 4.53±0.252 5.13±0.388 491±112 雌性 409±23.3** 416±21.0** 1.270±0.115 1.090±0.141* 2.41±0.120** 3.82±0.666* 571±55.1 合计 315±105 319±108 1.030±0.282 0.940±0.193 3.47±1.17 4.47±0.871 531±90.3 大鼠单次灌胃给予30 mg/kg HMS-01后的药动学参数(非房室模型)总结见表5。灌胃给予30 mg/kg HMS-01后,雄、雌大鼠药动学参数AUC显示有极显著性差异(P<0.01),药动学参数CL、F显示有显著性差异(P<0.05)。在大鼠体内血浆浓度达峰时间tmax为1.17 h,达峰浓度cmax为1 243 ng/ml,消除半衰期t1/2为2.00 h。雄、雌大鼠AUC0-t分别为2 271和8 529 ng·h/ml,生物利用度分别为34.3%和69.5%。
表 5 大鼠灌胃30 mg/kg HMS-01后血浆药代动力学参数($\bar { x}\pm { s}$ ,n=6)性别 AUC0-t (ng·h/ml) AUC0-∞ (ng·h/ml) MRT0-∞ (t/h) t1/2z (t/h) tmax (t/h) CLz/F (L/h·kg) Vz/F (L/kg) cmax (ng/ml) F(%) 雄性 2 271±666 2 279±667 2.58±0.156 1.43±0.130 1.17±0.289 14.00±4.31 28.5±7.04 729±263 34.3±10.1 雌性 8 529±1 920** 9 071±1 529** 4.79±1.39 2.58±1.060 1.17±0.289 3.38±0.629* 13.1±7.78 1757±584 69.5±15.6* 合计 5 400±3 661 5 675±3 867 3.68±1.50 2.00±0.924 1.17±0.258 8.69±6.44 20.8±10.7 1 243±694 51.9±22.6 3. 讨论
HMS-01在大鼠体内的药动学过程存在显著的性别差异。口服吸收的比较,雌性大鼠的生物利用度远高于雄性,体内的清除速率方面,雌性比雄性慢,与此同时,HMS-01在雌性体内的半衰期也更长。存在性别差异的原因有待进一步深入研究。本实验采用的分析方法的特异性、灵敏性、准确性、精密度及稳定性均满足定量分析的要求。鉴于HMS-01在大鼠血浆中不稳定的情况,在做动物实验时,课题组将采取以下措施:全血采集后立刻在4 ℃下离心2 min获取血浆,随即立刻取50 µl血浆样品加入至200 µl含内标的乙腈中,从而阻断血浆中的水解酶对化合物进行水解。
-
表 1 自制与市售制剂对几种皮肤真菌抑菌试验结果(抑菌圈直径/mm)
真菌 自制制剂复方酮康唑软膏 市售制剂 缺酮康唑阴性对照软膏 酮康唑乳膏 复方酮康唑乳膏 莫匹罗星软膏 须癣毛癣菌 32.14±0.74 32.34±0.42 32.55±0.38 7.00±0.00 7.00±0.00 红色毛癣菌 17.15±0.15 17.11±0.18 16.99±0.03 7.00±0.00 7.00±0.00 断发毛癣菌 48.02±0.04 48.23±0.17 48.16±0.14 7.00±0.00 7.00±0.00 犬小孢子菌 30.06±0.05 30.03±0.06 29.97±0.19 7.00±0.00 7.00±0.00 石膏样小孢子菌 38.10±0.07 38.05±0.15 38.08±0.09 7.00±0.00 7.00±0.00 裴氏着色真菌 34.07±0.35 33.84±0.57 34.04±0.10 7.00±0.00 7.00±0.00 表 2 自制与市售制剂对两种细菌的抑菌试验结果(抑菌圈直径/mm)
细菌 自制制剂复方酮康唑软膏 市售制剂 缺莫匹罗星阴性对照软膏 酮康唑乳膏 复方酮康唑乳膏 莫匹罗星软膏 金黄色葡萄球菌 20.76±0.14 7.02±0.01 13.19±0.08 20.74±0.09 7.01±0.01 铜绿假单胞菌 7.00±0.00 7.01±0.02 7.01±0.01 7.00±0.01 7.01±0.01 表 3 皮肤刺激反应评分
皮肤反应 具体表现 分值 红斑和
焦痂无 0 非常轻的红斑,勉强可见 1 明显的红斑 2 中度至重度的红斑 3 重度红斑(鲜红色)至轻度焦痂形成(深层损伤) 4 水肿 无 0 非常轻度的水肿,勉强可见 1 轻度水肿(边缘清晰) 2 中度水肿(皮肤隆起约1 mm) 3 重度水肿(皮肤隆起大于1 mm,超过涂抹区域) 4 表 4 皮肤刺激强度分级
积分均值 强度 0~<0.5 无刺激性 0.5~<2.0 轻刺激性 2.0~<6.0 中刺激性 6.0~8.0 强刺激性 表 5 自制复方酮康唑软膏皮肤单次刺激性试验评分结果
时间 (h) 对照组 实验组 No.1 No.2 No.3 No.4 总积分 平均分 No.1 No.2 No.3 No.4 总积分 平均分 1 0 0 0 0 0 0 0 0 0 0 0 0 24 0 0 0 0 0 0 0 0 1 0 1 0.25 48 0 0 0 0 0 0 0 0 1 0 1 0.25 72 0 0 0 0 0 0 0 0 1 0 1 0.25 表 6 自制复方酮康唑软膏皮肤多次刺激性试验评分结果
时间(d) 左侧 右侧 No.1 No.2 No.3 No.4 总积分 平均分 No.1 No.2 No.3 No.4 总积分 平均分 1 0 0 0 0 0 0 0 0 0 0 0 0 2 0 0 0 0 0 0 0 0 0 0 0 0 3 0 0 0 0 0 0 0 0 0 0 0 0 4 0 0 0 0 0 0 0 0 0 0 0 0 5 0 0 0 0 0 0 0 0 0 0 0 0 6 0 0 0 0 0 0 0 0 0 0 0 0 7 0 0 0 0 0 0 0 0 0 0 0 0 8 0 0 0 0 0 0 0 0 0 1 1 0.25 9 0 0 0 0 0 0 0 0 0 0 0 0 10 0 0 0 0 0 0 0 0 0 0 0 0 11 0 0 0 0 0 0 0 0 0 0 0 0 12 0 0 0 0 0 0 0 0 0 1 1 0.25 13 0 0 0 0 0 0 0 1 0 0 1 0.25 14 0 0 0 0 0 0 0 1 0 0 1 0.25 表 7 致敏强度分级
致敏率(%) 分级 过敏反应强度 0~8 Ⅰ 弱致敏 9~28 Ⅱ 轻度致敏 29~64 Ⅲ 中度致敏 65~80 Ⅳ 强致敏 81~100 Ⅴ 极强致敏 表 8 自制复方酮康唑软膏对豚鼠皮肤变态反应试验结果
组别 动物数(只) 观察时间(h) 皮肤反应强度评分 阳性动物数(只) 致敏率(%) 0 1 2 3 4 阴性对照 10 24 10 0 0 0 0 0 0 48 10 0 0 0 0 0 0 给药组 20 24 20 0 0 0 0 0 0 48 20 0 0 0 0 0 0 阳性对照 20 24 3 3 11 3 0 14 70 48 2 4 13 1 0 14 70 -
[1] 闫慧敏, 姜薇. 人类皮肤微生物群和皮肤疾病[J]. 中国皮肤性病学杂志, 2015, 29(12):1292-1294. [2] 黄梦雅, 赵明丹, 王晋蜀, 等. 135例足癣患者微生物学调查及药敏分析[J]. 中国真菌学杂志, 2018, 13(5):290-293. doi: 10.3969/j.issn.1673-3827.2018.05.008 [3] 刘淮, 刘景桢. 外用糖皮质激素的适应症与副作用[J]. 皮肤病与性病, 2016, 38(1):19-20. doi: 10.3969/j.issn.1002-1310.2016.01.007 [4] 陶春, 吴博, 黄爱文, 等. 复方酮康唑软膏的制备与稳定性考察[J]. 药学实践杂志, 2017, 35(6):535-538, 550. doi: 10.3969/j.issn.1006-0111.2017.06.013 [5] 姜吉波, 张瑞环. 针对皮肤金葡菌感染应用抗感染药的临床调查分析[J]. 临床医药文献电子杂志, 2019, 6(17):186, 195. [6] 陈舒影, 林纯婵, 刘欢乐, 等. 莫匹罗星对金黄色葡萄球菌临床分离株体外敏感性分析[J]. 中华医院感染学杂志, 2016, 26(1):23-25. [7] 赵前思, 赵超莉, 吴金虎, 等. 烧伤搽剂体外抑菌作用研究[J]. 医药导报, 2013, 32(11):1418-1421. doi: 10.3870/yydb.2013.11.007 [8] KOGA H, TSUJI Y, INOUE K, et al. In vitro antifungal activity of luliconazole against clinical isolates from patients with dermatomycoses[J]. J Infect Chemother,2006,12(3):163-165. doi: 10.1007/s10156-006-0440-4 [9] UCHIDA K, NISHIYAMA Y, TANAKA T, et al. In vitro activity of novel imidazole antifungal agent NND-502 against Malassezia species[J]. Int J Antimicrob Agents,2003,21(3):234-238. doi: 10.1016/S0924-8579(02)00362-X [10] 房盛楠. 盐酸普萘洛尔立方液晶凝胶的制备与评价[D]. 福州: 福建医科大学, 2017. [11] 庄珊珊. 痤疮治疗用盐酸氨酮戊酸原位凝胶的制备与评价[D]. 福州: 福建医科大学, 2015. [12] 王天宇. 防水型液体创可贴的研究[D]. 厦门: 厦门大学, 2017. [13] MONICA G K, KIM E H, BRUCE S K. Intertrigo and secondary skin infections[J]. Am Fam Physician,2014,89(7):569-573. [14] JEU L, PIACENTI F J, LYAKHOVETESKIY A G, et al. Voriconazole[J]. Clin Ther,2013,25(15):1321-1381. [15] 王美华. 手足癣常见病原性真菌及其检验结果分析[J]. 基层医学论坛, 2019, 23(19):2764-2766. [16] 马琳, 刘盈. 皮肤金黄色葡萄球菌感染的抗菌药物选择[J]. 中国皮肤性病学杂志, 2013, 27(3):225-227. [17] 陆雪华, 陆艳萍, 覃美玲等. 复方酮康唑、莫匹罗星联合治疗真菌性皮肤溃疡疗效观察[J]. 中外医学研究, 2017, 15(27):3-4. -





 下载:
下载:
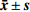
 下载:
下载: