-
自2013年起,我国已成为全球糖尿病患者最多的国家,患病人数高达1.2亿,患病率也以远超欧美国家的速度逐年增长[1]。皮肤溃疡是糖尿病常见的并发症之一,也是导致糖尿病患者截肢的首要原因,糖尿病导致的皮肤溃疡住院患者的人数,在我国各种体表难愈性溃疡住院总人数中居首位[2] ,具有高致残率和死亡率的特征,给家庭和社会造成沉重负担。据统计,糖尿病溃疡患者在5年内的病死率是无溃疡糖尿病患者的2.5倍[3] 。因此,积极预防和管理体表慢性溃疡,是降低糖尿病患者致残率和死亡率的首要任务。
糖尿病溃疡形成原因复杂,确切机制仍不清楚,成为阻碍精准医疗和新药研发的重要原因[4] 。西医治疗目前缺乏特效药物,临床上普遍以局部使用生长因子制剂和抗生素为主[5-6] ,价格高昂,但疗效有限,且存在致癌风险和抗生素耐药等副作用。中医药是中华民族的瑰宝,中草药作为中医天然药物资源的重要组成部分,其疗效经长期实践,得到普遍认可,受到国内外研究者的广泛关注。与合成药物不同,中草药一般含有多种活性成分,可以同时作用于多个靶点,产生协同效应。多项研究表明[7-8],中草药治疗难愈性皮肤溃疡疗效确切,可以显著降低因糖尿病溃疡而导致的截肢风险。因此,在中医愈创理论指导下,积极挖掘中草药中活性成分群,对于丰富现有治疗方案、延长患者寿命、提高患者生存质量具有重要意义。
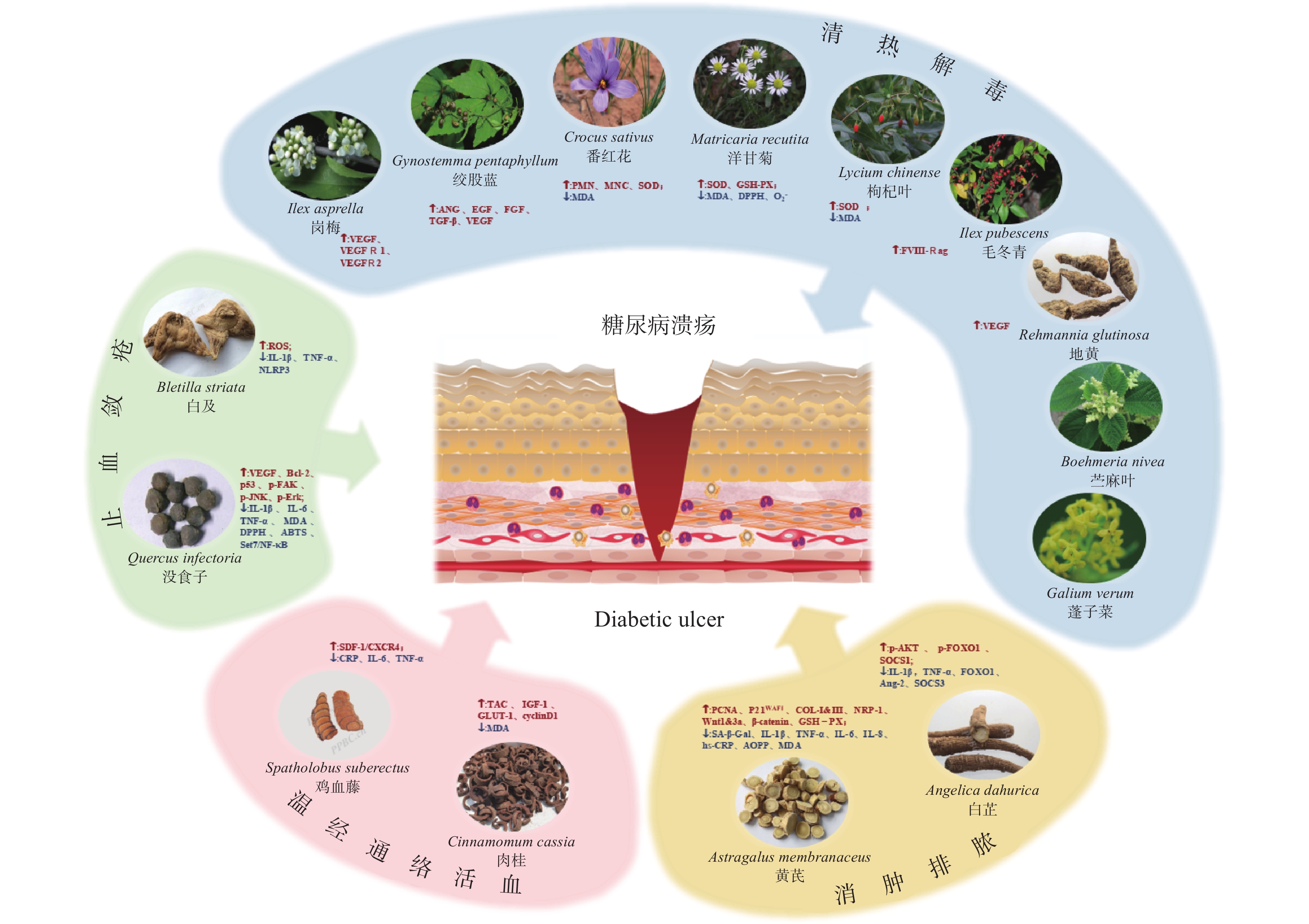
近年来,多种中草药活性成分对糖尿病溃疡创面愈合的影响已被报道,但缺乏较为系统的评价。故本综述总结了番红花、肉桂、黄芪、地黄等15种中草药的提取物对糖尿病创面愈合作用模式的相关研究(图1),并基于传统中医药理论进行分类讨论,以期为糖尿病溃疡的中草药精准治疗及新药研发提供参考。
-
绞股蓝提取物[9]含有豆甾醇、山柰酚和槲皮素等化合物。局部应用在糖尿病小鼠伤口皮肤上可以加速伤口愈合促进血管生成并诱导血管生成素(ANG)、表皮生长因子(EGF)、成纤维细胞生长因子(FGF)、转化生长因子-β(TGF-β)和血管内皮生长因子(VEGF)的表达。体外实验证明,绞股蓝提取物可以促进体外伤口愈合并增强在糖尿病条件下培养的人内皮细胞、成纤维细胞、角质形成细胞和肥大细胞的迁移和/或增殖,分别增加了1倍、3倍、12倍和10倍。
洋甘菊提取物(CT)[10]具有良好的降血糖作用和较强的抗氧化能力。CT灌胃可以显著降低糖尿病小鼠空腹血糖值,改善糖耐量,升高血清超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-PX)含量,降低丙二醛(MDA)含量。在体外实验发现,1.0 mg/ml的 CT对DPPH和超氧阴离子(O2−)自由基有一定的清除能力,但羟基自由基清除作用不明显,其抗氧化作用可能与其总黄酮成分有关。
岗梅提取物(LCE)[11]促进糖尿病溃疡的愈合,其机制与抗高糖诱导血管内皮细胞损伤、促进溃疡面的血管生成以及胶原合成有关。岗梅提取物药膏外用治疗组与空白对照组比较,可以使糖尿病大鼠胶原合成量增多,创面愈合速度增快,且10%剂量组较5%剂量组创面愈合效果更佳。免疫组化染色的结果显示,10% LCE软膏组血管的内皮细胞膜CD31的阳性表达量明显高于莫匹罗星治疗组。体外对人脐静脉血管内皮(HUVECs)细胞实验[12]显示,经50~100 mg/L LCE处理HUVECs的VEGF表达明显高于高糖对照组,25~100 mg/L处理的细胞VEGF R1及 VEGF R2基因表达显著高于高糖对照组。
苎麻叶提取物[13]主要存在酚类和黄酮类化合物。与对照组相比,提取物组第7d、第14d的炎症浸润评估,第7d的成纤维细胞定量,第14d、第21d的血管生成量显著增加,对糖尿病大鼠的组织修复和炎症细胞减少明显有效。
地黄提取物(RR)[14]治疗组与空白对照组相比,第4d起开始有显著的VEGF表达,第8d伤口面积出现了显著差异,有更完整的疤痕、更连续的表皮和更多的毛细血管形成。此外,RR提取物还显著缓解了角叉菜胶引起的炎症。
不同浓度蓬子菜溶液[15]在治疗糖尿病大鼠溃疡面过程中,在同一时间点的创面面积均明显小于贝复济治疗组,其中3mg/ml浓度蓬子菜治疗组的创面缩小最为明显,创面愈合修复最好。
毛冬青浸膏[16]外用对糖尿病小鼠溃疡具有较显著的修复作用,其作用可能与上调创面组织中增殖细胞核抗原第八因子相关抗原(FⅧ-RAg)的表达有关,从而促进表皮细胞增殖和新生血管的形成。
慢性难愈性溃疡常伴有多重耐药菌感染,而据报道中药具有逆转抗生素耐药的作用[17]。研究显示[18]番红花叶提取物可以增加耐甲氧西林金黄色葡萄球菌对甲氧西林的敏感度,对耐甲氧西林金黄色葡萄球菌感染伤口有显著疗效。番红花叶提取物通过抑制菌落数量,增加多形核(PMN)和单核(MNC)细胞浸润,促进胶原蛋白沉积、成纤维细胞增殖和血管新生,避免急性出血、充血、水肿,减少肉芽组织的成熟时间,增强再上皮化,加速创面愈合,提高创面愈合质量。同时,提取物治疗组的SOD水平显著增高,MDA、羰基蛋白显著降低,提示番红花叶提取物还有抗氧化作用,可以保护组织免受氧化损伤,通过减轻组织应激,为组织愈合提供有利的环境。枸杞叶提取物[19]也显示出类似的功效,此外枸杞叶提取物还可以增加胶原蛋白的交联促进成熟,提高修复过程中细胞和结缔组织在超微结构水平上的适应性,缩短创面愈合时间。
清热解毒药药性多为苦寒。中医认为,苦寒之品,能直折火势,清泻血热。其中,枸杞叶、绞股蓝、岗梅、地黄兼具甘味,故亦有清热滋阴养血之效。现代药理学研究发现,清热解毒单味药物提取成分促愈的主要机制为保护组织避免氧化损伤,并促进表皮、成纤维、血管上皮细胞增殖迁移。
-
肉桂提取物[20]中肉桂醛(11.26%)和2-羟基肉桂醛(6.7%)为主要成分。研究表明,肉桂提取物治疗组在伤口形成后第7 d和第14 d表现出较低的水肿评分和较少的炎症细胞浸润,在第7天有更好的血管形成和良好的肉芽组织,K-6染色显示角蛋白的合成显著增加,第14 d观察到完全的上皮再形成。10%浓度的肉桂提取物较5%浓度的治疗效果更显著。肉桂的抗氧化特性被认为是促进伤口愈合的关键因素,伤口产生后第3d和第7d,组织的总抗氧化能力(TAC)增加,MDA水平降低,防止细胞DNA、RNA和蛋白质损伤。此外,肉桂提取物增强了胰岛素样生长因子(IGF-1)、葡萄糖转运蛋白-1(GLUT-1)和cyclinD1 mRNA的表达。IGF-1和GLUT-1表达上调,加速葡萄糖转入细胞,并随之加快肉芽形成、重新上皮化和角蛋白的生物合成。cyclinD1通过推进细胞增殖期间的G1期来加速成纤维细胞和上皮细胞增殖,促进细胞迁移和血管生成。
鸡血藤提取物[21]可以促进糖尿病足大鼠溃疡愈合,显著降低C反应蛋白(CRP)、白介素-6(IL-6)及α-肿瘤坏死因子(TNF-α)水平,其促愈机制可能与抗炎作用有关。鸡血藤提取物的促愈合作用还可能与激活基质细胞衍生因子(SDF-1)/趋化因子受体4(CXCR4)轴有关。实验发现鸡血藤提取物可以提升大鼠外周血白细胞数量和骨髓、外周血中骨髓间充质干细胞(BMSCs)数量、造血干细胞(HSCs)数量和创面HSCs数量,促进血清中SDF-1和粒细胞集落刺激因子(G-CSF)的分泌,通过激活SDF-1/CXCR4轴,促进骨髓干细胞增殖、趋化迁移至皮肤创面而实现促进创面修复。体外实验亦证明鸡血藤提取物能够激活SDF-1/CXCR4信号轴,保护氧化损伤BMSCs的增殖活性,提升氧化应激状态下BMSCs的迁移和趋化能力[22]。
温经通络活血药味多辛、苦,性多偏温。辛能散行,苦能通降,温能通畅血行,可使血脉温通,瘀滞消散。研究亦发现肉桂、鸡血藤可以有效减轻炎症反应,降低血糖,促进血管生成,激发干细胞迁移,进而促进糖尿病溃疡愈合。
-
黄芪注射液可以通过缩短细胞倍增时间、降低G1期阻滞、上调增殖细胞核抗原(PCNA)及细胞周期检查点控制基因 P21WAF1 mRNA的表达,使变大的细胞体积逐渐缩小,扁平的细胞形态逐步恢复成梭形、放射状、旋涡状走形,帮助溃疡面成纤维细胞恢复至正常形态并促进细胞增殖[23];上调成纤维细胞透明质酸合成酶的浓度,从而增加伤口透明质酸的浓度[24];增加成纤维细胞Ⅰ型和Ⅲ型胶原蛋白的合成和分泌量[25],改善伤口愈合条件。研究还发现,黄芪注射液的促愈作用可能与活化Wnt/β-catenin信号通路有关,通过上调Wnt1、Wnt3a、β-catenin的表达,启动通路下游靶基因C-myc、CyclinD1的转录,提高C-myc、CyclinD1的表达,调节Wnt/β-catenin信号通路,而起到促进创面肉芽组织增生,促进表皮干细胞的增殖分化,加快创面上皮化的进程的作用[26]。另有临床血检发现,使用黄芪注射液的患者炎症细胞因子TNF-α、IL-6、白介素-8(IL-8)、超敏C反应蛋白(hs-CRP),氧化应激反应相关因子隐性氧化蛋白产物(AOPP)、MDA明显低于空白对照组,而GSH-PX水平明显高于空白对照组[27-28],提示加速炎症因子吸收,抑制氧化应激反应也是APS重要的促愈机制。翁鹤[29]研究发现,黄芪的水提取液可以促进人角质细胞形成细胞(HaCaT)增殖,上调HaCaT细胞NRP-1 mRNA表达水平及NRP-1蛋白表达水平,浓度在5 mg/ml作用最佳。进一步探究黄芪作用成分发现,黄芪提取物中的主要作用成分多糖(APS)可以通过调控表皮干细胞的分化、角质形成细胞和成纤维细胞的增殖、胶原蛋白的合成分泌等方式,促进糖尿病溃疡的愈合。在体外实验中发现,10~160 μg/ml剂量的APS呈量效、时效依赖性地促进糖尿病溃疡成纤维细胞增殖、增加胶原合成,但过高浓度(> 640 μg/ml)会出现抑制作用[30-31];降低白介素-1β(IL-1β)的浓度和具有水解细胞外基质和基底膜蛋白的基质金属蛋白酶MMP-2和MMP-9的活性及蛋白表达,以减少对成纤维细胞的增殖抑制作用和破坏[32];降低β-半乳糖苷酶,延缓并抑制成纤维细胞的衰老和凋亡[33] 。
白芷提取物[34]能在2型糖尿病小鼠创面愈合多个时期发挥积极作用,在早期可减轻创面炎症细胞数量,下调创面组织炎症因子 IL-1β,TNF-α 表达,其机制可能与调节细胞因子信号传导抑制分子1(SOCS1)/细胞因子信号传导抑制分子 3(SOCS3)表达,抑制糖尿病小鼠创面巨噬细胞向M1过度极化有关。在增殖阶段,白芷能提高2型糖尿病小鼠创面及体外高糖缺氧下内皮细胞对周细胞的趋化募集作用,促进内皮细胞-周细胞管状结构形成,促进创面血管新生及成熟,其相关机制可能与上调p-AKT促进叉头蛋白叉头转录因子1(FOXO1)磷酸化,抑制FOXO1激活,降低血管生成素-2(Ang-2)表达有关。
黄芪、白芷善消肿排脓,其中黄芪性甘温,温中补气,托毒排脓,消肿生肌,其提取物可帮助溃疡面细胞恢复正常形态、促进增殖、延缓衰老和凋亡,并加速炎症因子吸收,抑制氧化应激反应。白芷辛温解表,消肿排脓,其提取物可以抑制局部创面炎症,趋化募集周细胞至创面,促进创面愈合。
-
白及提取物(BSP)[35]外用治疗的糖尿病小鼠溃疡创面愈合加速,巨噬细胞浸润减少,血管生成增加,溃疡区IL-1β和TNF-α含量减少,并能抑制局部NLRP3炎症小体过度活化,提高溃疡区胰岛素敏感性。离体细胞实验结果表明,BSP干预处理可缓解高糖刺激导致的骨髓来源巨噬细胞(BMDMs)内活性氧(ROS)水平上升、NLRP3炎症小体过度活化和IL-1β释放量增多以及心肌微血管内皮细胞(CMECs)活力下降及胞内胰岛素信号传导受损;BMDMs-CMECs共培养实验结果提示BSP干预对两种细胞的上述异常情况均有保护作用,而加入IL-1β可抑制BSP的上述作用。
没食子含有高含量的单宁(50%~70%)以及没食子酸、鞣花酸和丁香酸等化合物。没食子提取物中总酚类化合物含量较高(954.07 mgGAE/100g),接近标准没食子酸(960.85 mgGAE/100g)[36]。没食子提取物外用治疗可显著缩小糖尿病小鼠伤口面积,降低IL-1β、IL-6和TNF-α浓度,降低了MDA浓度并增加了总抗氧化能力[37],对自由基DPPH和ABTS的抑制率分别为97.40%和98.70%[36],这可能是通过抑制Set7/NF-κB信号通路[38]。没食子提取物治疗组的肉芽组织发育丰富,含有大量成纤维细胞、胶原蛋白、毛细血管[36],每平方毫米伤口组织的成纤维细胞分布、胶原沉积、快速上皮再形成增加,且角质形成细胞分化更为规则,并上调VEGF、Bcl-2和p53等相关mRNA的表达[37],这可能与激活粘着斑激酶(FAK)、c-Jun N 末端激酶(JNK) 和细胞外信号调节激酶 (Erk)在内的几条伤口愈合信号通路来加速细胞迁移有关[39]。临床观察51例糖尿病溃疡患者[40]发现,没食子提物处理的慢性创面愈合迅速,伤口尺寸减少率比对照组高15%,治疗第8周,完全愈合率高达65.38%,而对照组仅为8%,且观察组未发生感染、皮疹、发红、过敏等不良反应。
止血敛疮药药性苦、涩,主燥湿收敛,善止血收湿敛疮。白及、没食子主要通过抑制创面炎症,改善创面愈合环境,进而促进并丰富肉芽组织发育,起到促进愈合的效果,见表1。
表 1 15种中草药提取物促进糖尿病创面愈合的作用机制
作用 中草药 靶点、作用机制 实验水平 给药途径、剂量 清热解毒 绞股蓝 ↑:ANG、EGF、FGF、TGF-β、VEGF 动物(小鼠)
细胞(HUVECs、HaCaT、HF21)0.5% 药膏外用
50、100 μg/ml[9]洋甘菊 ↑:SOD、GSH-PX;
↓:MDA、DPPH、O2-动物(小鼠) 971、485、243 mg/kg灌胃[10] 岗梅 无 动物(大鼠) 5%、10%软膏外用[11] ↑:VEGF、VEGF R1、VEGF R2 细胞(HUVECs) 12.5、25、50、100 mg/L培养[12] 苎麻叶 无 动物(大鼠) 2%粗提物外用[13] 地黄 ↑:VEGF 动物(大鼠) 1.85 g/kg管饲[14] 蓬子菜 无 动物(大鼠) 30、3、0.3 mg/ml制剂外用[15] 毛冬青 ↑:FⅧ-Rag 动物(小鼠) 0.25、0.5、1.0 ml药膏外用[16] 番红花叶 ↑:PMN、MNC、SOD;
↓:MDA动物(大鼠) 2 g/100g药膏外用[18] 枸杞叶 ↑:SOD;
↓:MDA动物(大鼠) 1、2、4 g/100g药膏外用[19] 温经通脉活血 肉桂 ↑:TAC、IGF-1、GLUT-1、cyclinD1 动物(小鼠) 5%、10%软膏外用[20] ↓:MDA 鸡血藤 ↓:CRP、IL-6、TNF-α 动物(大鼠) 2.0、1.0、0.5 g/ml药膏外用[21] ↑:SDF-1/CXCR4 动物(大鼠) 1 ml/100g灌服[22] 消肿排脓 黄芪 ↑:PCNA、P21WAF1 细胞(Fb) 20 g/L培养[23] 无 细胞(Fb) 20 g/L培养[24] ↑:COL-Ⅰ、COL-Ⅲ 细胞(Fb) 20 g/L培养[25] ↑:Wnt1、Wnt3a、β-catenin 动物(大鼠) 0.675 ml、1.39 ml、2.7 ml灌胃[26] ↓:TNF-α、IL-6、IL-8、hs-CRP、AOPP、MDA;
↑:GSH-PX糖尿病溃疡患者 30 ml配以250 ml生理盐水静脉滴注[27, 28] ↑:NRP-1 细胞(HaCaT) 0、0.1、0.5、1、5、10、20、50、100 mg/ml培养[29] 无 细胞(Fb) 10、40、160、640 μg/ml培养[30] 无 细胞(Fb) 10、40、160、640 μg/ml培养[31] ↓:IL-1β、MMP-2、MMP-9 细胞(Fb) 100 mg/L培养[32] ↓:SA-β-Gal 细胞(Fb) 10、40、160、640 μg/ml培养[33] 白芷 ↓:IL-1β,TNF-α、FOXO1、Ang-2、SOCS3
↑:p-AKT、p-FOXO1、SOCS1动物(小鼠) 1.8、3.6、7.2 g/kg·d灌胃[34] 止血敛疮 白及 ↓:IL-1β、TNF-α、NLRP3
↑:ROS动物(小鼠) 50 μL5%制剂外用[35] 没食子 ↓:DPPH、ABTS 动物(大鼠) 30%局部外用[36] ↓:IL-1β、IL-6、TNF-α、MDA;
↑:VEGF、Bcl-2、p53动物(小鼠) 5%、10%软膏外用[37] ↓:Set7/NF-κB 动物(小鼠) 30%药物制剂局部外用[38] ↑:p-FAK、p-JNK、p-Erk 细胞(HaCaT、MEF、HF21) 10、20、50、100和200 μM培养[39] 无 糖尿病溃疡患者 30%药物制剂局部外用[40] 注:MEF.小鼠胚胎成纤维细胞;HF21.人成纤维细胞;Fb.成纤维细胞;COL-Ⅰ.Ⅰ型胶原蛋白;COL-Ⅲ.Ⅲ型胶原蛋白;“↑”表示增加,“↓”表示减少。 -
糖尿病溃疡具有病机复杂、病程较长等特点,常迁延难愈,并伴随多重耐药菌感染,临床治疗颇为棘手。中医认为,糖尿病溃疡的主要病机为血脉瘀阻,一为肝肾亏虚,阴虚燥热,热盛伤阴致血脉涩滞;二为气血不足,血行无力致血脉瘀阻;三为脾肾阳虚,阳不通,血不行致血脉瘀阻。故而治疗原则应以清热解毒、滋阴养血、温经通络、活血化瘀为主。现代医学认为,伤口愈合主要涉及3个阶段:炎症反应、细胞增殖和组织重塑[41]。近年研究发现,不同的中草药提取物可以调节Set7/NF-κB、Wnt/β-catenin、SDF-1/CXCR4等信号通路,从而减少炎症浸润、逆转抗生素耐药性、促进表皮细胞增殖、恢复原有上皮结构、抑制瘢痕形成(表1)。其中,清热解毒药提取物的作用主要表现为保护组织避免氧化损伤,促进表皮、成纤维、血管上皮细胞增殖迁移;温经通络活血药提取物主要表现为减轻炎症反应、降低血糖、促进血管生成、激发干细胞迁移;消肿排脓药提取物主要表现为抑制局部创面炎症,趋化募集周细胞至创面,帮助溃疡面细胞恢复正常形态、促进增殖、延缓衰老和凋亡;止血敛疮药提取物主要表现为抑制创面炎症,改善创面愈合环境,进而促进并丰富肉芽组织发育。上述研究初步展现出中医药传统概念中清热解毒、温经通络活血、消肿排脓、止血敛疮药物对糖尿病溃疡愈合的不同阶段均有较好的疗效,显示出中草药多靶点的作用优势,富有临床应用前景,但其促进创面愈合的关键环节和作用机制仍有待进一步阐明。同时,中医治疗主张根据病因和症状的不同辨证论治,而现有的糖尿病溃疡模型较为单一,无法体现在不同证型条件下,不同特性中草药的差异、偏颇与优势,有待在将来的研究中进一步设立完善。未来,期待通过更多高质量的临床研究和真实世界数据来客观评价中草药治疗糖尿病溃疡的疗效和安全性。
Advances in the treatment of diabetic ulcers by Chinese herbal extracts
-
摘要: 皮肤溃疡是糖尿病最常见的并发症,糖尿病溃疡患者死亡率远高于无溃疡糖尿病患者。近年来,中草药因具有多成分、多靶点、多通路协同的治疗效应而受到广泛关注。临床实践证明,中草药能有效促进糖尿病创面愈合,并展现出良好的安全性。为系统评价中草药对糖尿病溃疡的治疗效应,笔者通过检索文献,回顾和总结了15种中草药提取物促进糖尿病创面愈合的作用机制,并基于传统中医药理论进行分类讨论,以期为糖尿病溃疡的精准治疗及新药研发提供参考。Abstract: Skin ulcers are the most prevalent consequence of diabetes mellitus, and people with diabetic ulcers have a substantially greater death risk than those who do not have ulcers. Herbal medications have gained wide concern in recent years due to their multi-component, multi-target, and multi-pathway synergistic therapeutic effects. Clinical trials have demonstrated the safety and efficacy of herbal treatments in diabetic refractory ulcers. To systematically evaluate the healing effect of herbs on diabetic wounds, a literature search was conducted, the mechanism of action of 15 herbal extracts in promoting diabetic wound healing were reviewed, and the classification based on traditional Chinese medicine theory was discussed, which could provide a reference for the precise treatment and exploitation of herbal medicines for diabetic ulcers.
-
Key words:
- Chinese herbal medicine /
- extracts /
- diabetic ulcers /
- mechanism of action
-
肺型氧中毒是长期吸入高浓度氧气导致的肺部损伤,表现为肺组织充血、水肿、炎性浸润等,其中以多型核白细胞为主[1]。活化的多型核白细胞可以激活氧化酶,进而产生和释放大量的炎症介质和氧自由基,进一步介导级联式扩大的炎症反应对肺部造成损伤[2]。在饱和潜水或重型减压病患者进行加压治疗时,肺型氧中毒已成为最常见的并发症[3]。然而,目前关于高压氧(HBO)诱导的肺型氧中毒发生机制缺乏深入的探讨。
山莨菪碱(ANI)是一种毒蕈碱(M)受体阻滞剂,新斯的明(NEO)是一种临床常见的胆碱酯酶抑制剂。我们课题组前期研究发现ANI和NEO以500∶1的比例组成复方,简称新斯莨菪碱,能协同地激活α7nAChR,并减轻二者联用所致的不良反应。研究表明激活α7nAChR受体在感染性休克[4]、类风湿关节炎[5]、挤压综合征[6]、脑卒中[7]等动物模型上均发挥保护作用。然而,在HBO诱导的肺型氧中毒的发生、发展过程中,新斯莨菪碱是否可以用于肺型氧中毒的治疗?其治疗作用的病理生理机制是什么?这些都尚未阐明。
铁死亡是一种以细胞内铁依懒性的活性氧(ROS)异常增高,导致细胞内ROS的生成和降解失衡为特征的细胞死亡方式[8]。高浓度氧暴露条件下生成的大量ROS,一方面可直接对肺细胞产生损害,另一方面可参与炎症反应,促进炎症细胞渗透聚集,使各种致炎因子的表达增多,进一步加重肺的急性炎症反应[9]。
本文探究了新斯莨菪碱对HBO诱导的肺型氧中毒是否具有保护效应,并在此基础上,阐明铁死亡在新斯莨菪碱治疗HBO诱导的肺型氧中毒中的作用,以期为肺型氧中毒的临床防治提供新的理论指导和思路。
1. 材料和方法
1.1 实验动物
雄性C57BL/6小鼠,6~8周龄,小鼠购自上海斯莱克公司。所有小鼠均饲养于22℃,昼夜循环12 h的独立饲养系统中。小鼠自由饮食、自由饮水。所有实验均经海军军医大学实验动物伦理委员会批准并按照指南进行。
1.2 仪器和试剂
小型实验动物氧舱(RDC150-300-6,海军军医大学);台式高速冷冻离心(SCILOGEX);7500RT-PCR 仪器(Applied Biosystems 公司);激光共聚焦显微镜(日本Olympus公司);酶标仪(瑞士Tacan 公司);高速组织研磨仪(上海净信实业发展有限公司);Trizol、BCA 法蛋白定量试剂盒(美国GLPBIO公司);苏木精-伊红(上海Sangon Biotech公司);戊巴比妥(上海国药集团化学试剂公司);RT-PCR试剂盒(日本Takara公司);组织铁检测试剂盒(北京Solarbiog公司);伊文思蓝(美国Sigma-Aldrich公司);MDA、GSH检测试剂盒(上海Beyotime公司);Perls stain、抗谷胱甘肽过氧化物酶4(GPX4)抗体、抗β-actin抗体(英国Abcam公司);驴抗兔/驴抗鼠二抗、Odyssey 扫膜仪(LI-COR公司)。
1.3 实验方法
1.3.1 肺型氧中毒模型的制备
将小鼠置于动物加压舱内,先用纯氧冲洗舱5 min,然后将压力在5 min内调至舱内为100% O2、2.5 ATA,维持6 h,在暴露过程中保持 0.5 L/min的连续氧流量,每1~2 h调整气阀进行快速通气,同时舱内放置碱石灰以避免呼吸产生的CO2在舱内蓄积。动物实验分组如下:①正常组:腹腔注射给予生理盐水10 ml/kg,常压饲养;②模型组:HBO暴露前30 min给予生理盐水10 ml/kg,2.5 ATA暴露6 h;③新斯莨菪碱组:HBO暴露前30 min给予ANI(25 mg/kg)+NEO(50 μg/kg),2.5 ATA 暴露6 h。
1.3.2 HE染色
使用戊巴比妥钠麻醉并处死小鼠,解剖取小鼠左肺组织于4%多聚甲醛中固定,然后用石蜡包埋并切成5 μm的薄片。在 200倍光学显微镜下观察组织炎症、水肿或其他损伤。组织学评分:0分为正常组织学;1分代表轻度白细胞浸润和毛细血管充血;2分代表轻度白细胞浸润、血管周围水肿、肺结构部分破坏和出血;3分代表强烈的白细胞浸润和肺结构破坏。
1.3.3 伊文思蓝染色
HBO暴露6 h后,将小鼠固定,尾静脉注射1%伊文思蓝(50 mg/kg)后放回笼中自由活动,约30 min处死动物,用PBS灌流后取肺组织,用滤纸擦干肺组织表面水分并对肺组织进行拍照。每100 mg肺组织加入2 ml甲酰胺,55℃孵育18 h,反应结束后10 000×g 离心30 min后取上清液,并在630、740 nm处测量吸光度。
1.3.4 肺组织湿干比
将小鼠麻醉处死后,取新鲜左肺组织,滤纸擦干表面血迹后称重记为湿重,随后将肺组织置于60℃干燥箱中,每日测量肺组织重量,直至肺组织重量不再变化,此时肺组织重量为干重。肺含水量(%)=(湿重−干重)/湿重×100%。
1.3.5 肺泡灌洗液蛋白含量测定
用1 ml预冷PBS经气管插管灌洗肺3次,收集混合的支气管肺泡灌洗液(BALF),将收集到的BALF以1 500 r/min 离心10 min获得其上清液,BCA法测定试剂盒定量BALF中总蛋白。
1.3.6 非血红素铁含量测定
30 mg肺组织在冷PBS中清洗,在冰上用匀浆器在铁测定缓冲液中匀浆,在4℃以16 000×g离心10 min,收集上清液用铁检测试剂盒进行组织铁含量测定。
1.3.7 普鲁士蓝染色
戊巴比妥钠麻醉处死小鼠,取新鲜肺组织于4%多聚甲醛中固定,固定48 h后进行梯度脱水,二甲苯置换,浸蜡;包埋、切片(厚度为5 μm)。将石蜡切片脱蜡后用Prussian Blue Stain(等体积的亚铁氰化钾溶液和盐酸溶液混合,制成铁染色工作液)染色15 min,洗涤,然后用核固红溶液染色5 min,洗涤,封片后在Olympus光学显微镜下观察染色切片。
1.3.8 丙二醛(MDA)的测定
取100 μg肺组织于300 μl PBS溶液中,匀浆机研磨后,以12 000 r/min离心10 min后取上清液待测。所有试剂盒均按照制造商的说明书使用,按检测工作液与上清2∶1配好检测体系后100℃水浴15 min,冷却后于532 nm处测吸光度。
1.3.9 谷胱甘肽(GSH)的测定
取100 μg肺组织,与700 μl蛋白去除试剂S溶液混匀,匀浆机研磨后以12 000 r/min,离心10 min后取上清液进行总谷胱甘肽测定。所有试剂盒均按照制造商的说明书使用,25℃反应60 min即可测得氧化性谷胱甘肽(GSSG)含量,还原GSH含量=总谷胱甘肽含量−GSSG×2 。
1.3.10 实时定量PCR
动物出舱后,解剖取肺组织,使用TRIzol试剂提取组织总RNA并逆转录成cDNA,进行PCR扩增,采用2–ΔΔCT分析目的基因的相对表达量,引物序列见表1。
表 1 实时定量PCR引物序列引物名称 引物序列(5′—3′) IL-6(F) CCAGAAACCGCTATGAAGTTCC IL-6(R) GTTGGGAGTGGTATCCTCTGTGA IL-1β(F) GTTCCCATTAGACAACTGCACTACAG IL-1β(R) GTCGTTGCTTGGTTCTCCTTGTA TNF-α(F) CCCCAAAGGGATGAGAAGTTC TNF-α(R) CCTCCACTTGGTGGTTTGCT GAPDH(F) GTATGACTCCACTCACGGCAAA GAPDH(R) GGTCTCGCTCCTGGAAGATG 注:F: 正向引物; R: 反向引物。 1.3.11 Western blot
提取肺组织蛋白,BCA法测定蛋白浓度。十二烷基硫酸钠-聚丙烯酰胺凝胶(SDS-PAGE)电泳分离蛋白质,然后转移到硝酸纤维素膜上,与GPX4、β-肌动蛋白共孵育。最后,根据情况将膜与驴抗兔或驴抗鼠二抗孵育,使用Odyssey 扫膜仪获取图像,通过Image J 软件对条带进行定量分析。
1.4 统计学处理
实验数据的分析以及数据处理均使用GraphPad Prism 8.0 软件进行。所有值以(
$ \bar{x}\pm s $ )表示,多组间比较用单因素方差分析(ANOVA)并 Bonferroni 检验,P<0.05 视为差异具有统计学意义。2. 结果
2.1 新斯莨菪碱保护了 HBO暴露引起的肺组织损伤
首先,探究HBO暴露后对肺组织的病理损伤情况以及新斯莨菪碱对HBO诱导的肺损伤的作用。将C57BL/6小鼠置于2.5 ATA的高压氧舱中暴露6 h建立肺型氧中毒模型,然后通过HE染色观察肺组织结构变化,如图1所示。正常组小鼠肺泡肺泡壁结构完整,间隔无增厚,肺泡腔内无渗出物;HBO暴露后,肺泡间隔出现水肿、增厚,肺泡腔内可见红细胞渗出,肺间质见大量炎性细胞浸润(图1B);给予新斯莨菪碱治疗后,肺水肿明显减轻,肺泡内炎性细胞浸润以及红细胞渗出减少,肺组织病理损伤减轻(图1C~D)。以上结果表明新斯莨菪碱治疗能减轻肺型氧中毒后肺组织的病理损伤。
2.2 新斯莨菪碱改善肺组织渗透性
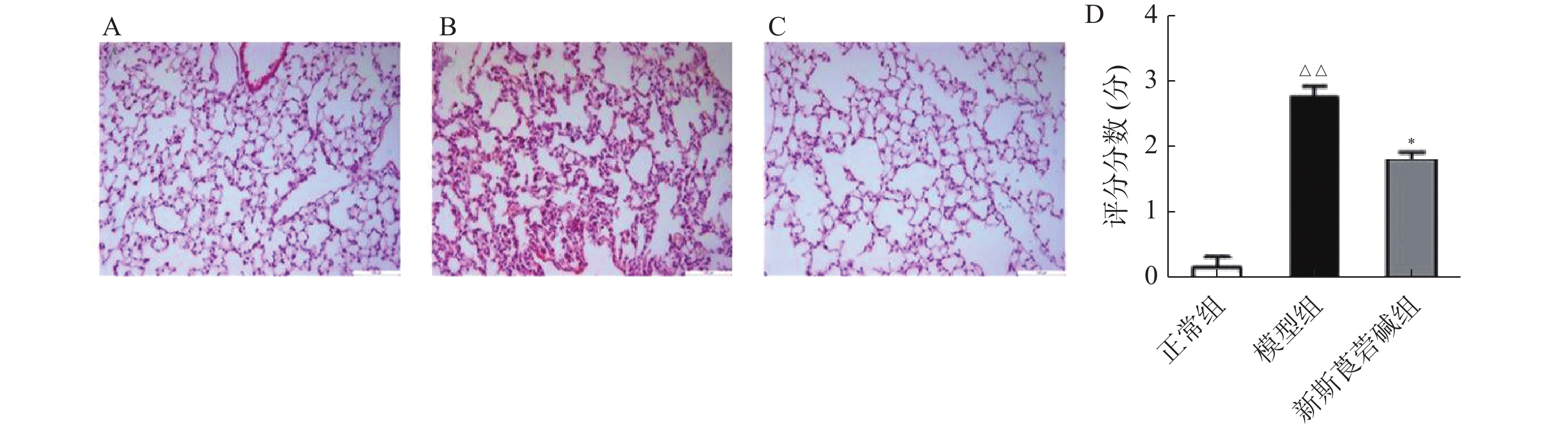
从图2可以看出,模型组伊文思蓝染色加深,表明HBO暴露后肺渗透性增加,而新斯莨菪碱治疗后上述情况明显改善(图2A~B)。与正常组相比,模型组肺组织湿干比重明显增加,而新斯莨菪碱治疗后能够显著降低肺湿干比(图2C)。此外,HBO暴露后肺泡灌洗液中蛋白含量升高,新斯莨菪碱治疗能够有效减少肺泡灌洗液中蛋白的渗出(图2D)。这些结果表明,新斯莨菪碱治疗能够有效改善肺型氧中毒后的肺水肿及肺组织渗出。
2.3 新斯莨菪碱抗炎、抗氧化应激作用
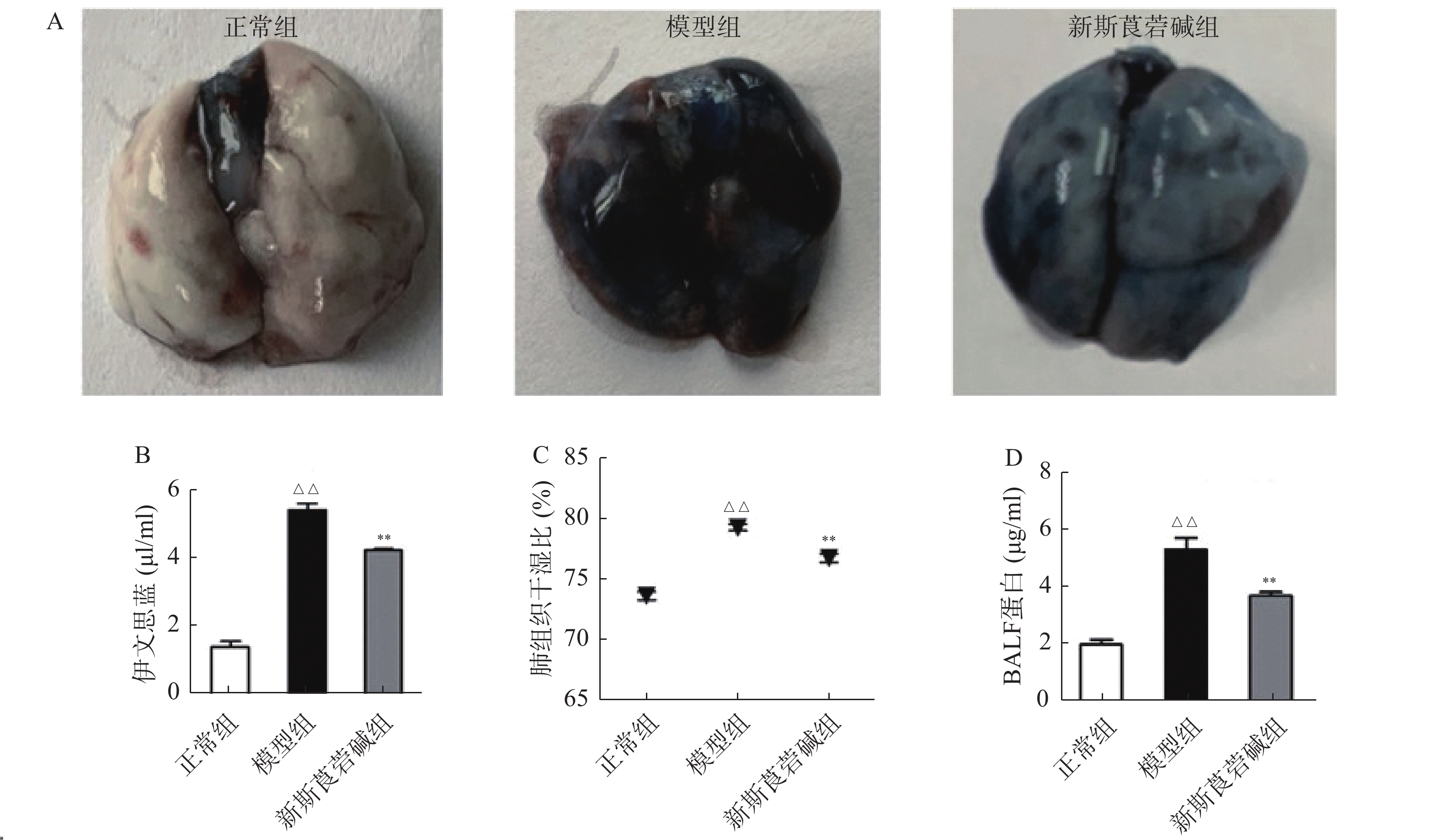
从图3中可以看出,HBO暴露后,肺组织中促细胞因子,如TNF-α、IL-1β、IL-6和IFN-γ的mRNA显著增高,抗炎因子IL-4及TGF-β则显著降低,而新斯莨菪碱能显著降低促炎因子的表达,同时提高抗炎因子的水平(图3A~F)。HBO暴露后肺组织氧化指标MDA升高,而抗氧化指标GSH降低,给予新斯莨菪碱治疗后,能明显逆转上述变化(图3G~H)。由此说明,新斯莨菪碱能降低HBO诱导的肺型氧中毒引起的炎症反应及氧化应激水平。
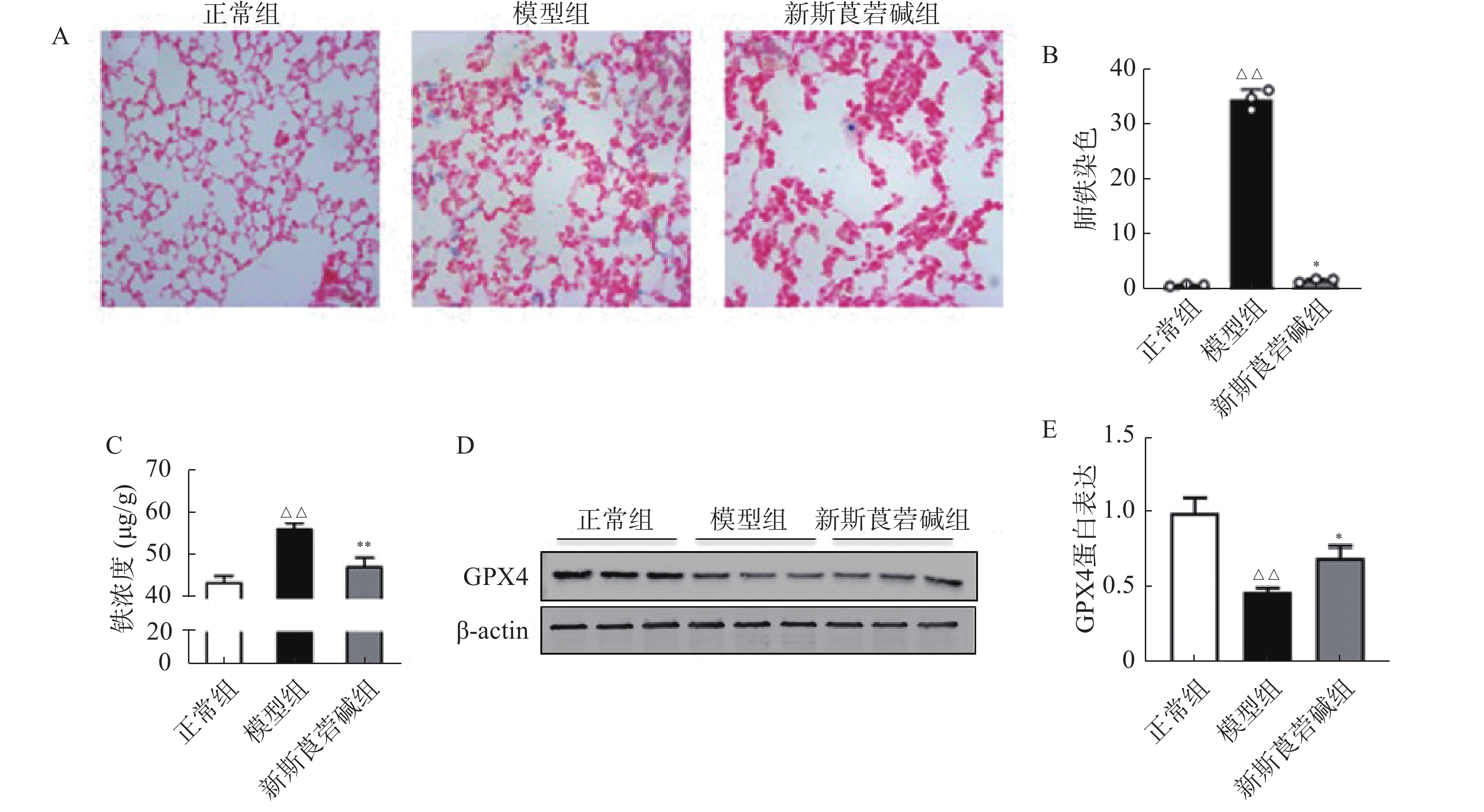
2.4 新斯莨菪碱减轻铁死亡
铁元素是维持正常生理活动所必需的,但过量的铁会产生对细胞有害的自由基。在病理状态下,铁蛋白的破坏导致细胞内游离铁的增高,脂质过氧化反应和游离铁的增高会导致细胞的铁死亡。如图4所示,HBO暴露后普鲁士蓝染色可见肺组织中铁含量增高,对肺组织铁离子含量进行检测得到了同样的结果(图4A~C)。GPX4是一种重要的抗氧化酶,HBO暴露后GPX4的表达降低(图4D~E),导致机体抗氧化应激能力减弱,对细胞有害的自由基无法被有效清除。而新斯莨菪碱治疗后可以改善GPX4的表达,降低肺组织铁含量,从而减少细胞铁死亡的发生,对肺组织起到保护作用。
3. 讨论
HBO已被广泛用于多种疾病的治疗以及潜水作业中,并发挥了难以替代的作用[10]。然而,在饱和潜水或重型减压病患者加压治疗以及临床上用于治疗新生儿呼吸窘迫时,HBO诱导的肺损伤已成为最常见的并发症[11]。研究发现,当HBO环境持续存在时,将出现小气道功能障碍,表现为肺活量降低、气体扩散功能减弱和肺顺应性降低[12]。与之前的报道一致,本研究结果表明,与正常组相比,模型组的肺组织损伤显著加重;伊文思蓝染色显示HBO暴露后染色加深,肺湿/干比增加,同时肺泡灌洗液中的蛋白含量也显著增加,新斯莨菪碱治疗后这些变化被显著抑制,这些结果初步表明新斯莨菪碱与HBO诱导的肺型氧中毒的发生密切相关。
ANI属于传出自主神经M受体阻断剂,阻断M受体引起交感神经优势。NEO是一种可逆性胆碱酯酶抑制剂,可有效延长乙酰胆碱的作用时间,同时激活胆碱能抗炎通路[11]。Sun等[4]研究证实,两药物联合使用,不仅可以加强胆碱能抗炎通路的炎症抑制作用,还可降低NEO的不良反应,达到协同增强作用。本课题组前期的研究发现ANI和NEO联合使用,能够通过阻断巨噬细胞上的毒蕈碱型受体,使更多的乙酰胆碱作用于α7尼古丁乙酰胆碱受体,进而对胆碱能抗炎通路起到双向活化调节作用,进一步加强了对炎症反应的抑制作用[7]。本研究发现新斯莨菪碱能够显著降低肺组织中促炎因子TNF-α、IL-1β、IL-6和IFN-γ的表达。由此说明,新斯莨菪碱可减轻HBO导致的肺部炎症反应。
肺型氧中毒包括高压力损伤和高浓度氧损伤,目前认为ROS 及其代谢产物介导的生化紊乱是导致肺型氧中毒发生发展的主要因素。HBO环境下会产生大量氧自由基,可能导致细胞因子释放和炎症反应的增加,而异常的炎症反应可加剧肺损伤[13]。研究发现,HBO 暴露后肺组织中氧化指标MDA 显著升高、抗氧化指标 GSH 则显著降低,而给新斯莨菪碱治疗能明显改善肺组织氧化损伤情况。
铁死亡作为一种新发现的细胞死亡方式,其释放出内源性损伤相关分子(DAMPs)与炎症和氧化应激之间存在着诸多途径的交互作用。GPX4作为铁死亡的核心调控因子,近年来受到广泛关注。研究表明GPX4的缺乏或功能丧失会加剧铁死亡的发生,并促使细胞进一步受到氧化应激的影响[14]。Kang等[15]的研究发现在LPS诱导的脓毒症模型中,敲除GPX4导致脂质过氧化的加剧并进一步促进铁死亡的发生。本研究发现,HBO暴露后肺组织中铁含量增高、GPX4的表达量降低,而新斯莨菪碱治疗后可以逆转这些变化。
综上所述,新斯莨菪碱可能通过激活胆碱能抗炎通路,从而抑制炎症的和氧化应激的发生,进而减少了肺组织中游离铁的含量,最终抑制细胞铁死亡。下一步我们将通过体外实验,进一步验证在HBO诱导的肺型氧中毒模型中,新斯莨菪碱是否通过抑制铁死亡的产生从而减轻肺组织的损伤情况,以期为防治HBO诱导的肺型氧中毒提供新的策略。
-
表 1 15种中草药提取物促进糖尿病创面愈合的作用机制
作用 中草药 靶点、作用机制 实验水平 给药途径、剂量 清热解毒 绞股蓝 ↑:ANG、EGF、FGF、TGF-β、VEGF 动物(小鼠)
细胞(HUVECs、HaCaT、HF21)0.5% 药膏外用
50、100 μg/ml[9]洋甘菊 ↑:SOD、GSH-PX;
↓:MDA、DPPH、O2-动物(小鼠) 971、485、243 mg/kg灌胃[10] 岗梅 无 动物(大鼠) 5%、10%软膏外用[11] ↑:VEGF、VEGF R1、VEGF R2 细胞(HUVECs) 12.5、25、50、100 mg/L培养[12] 苎麻叶 无 动物(大鼠) 2%粗提物外用[13] 地黄 ↑:VEGF 动物(大鼠) 1.85 g/kg管饲[14] 蓬子菜 无 动物(大鼠) 30、3、0.3 mg/ml制剂外用[15] 毛冬青 ↑:FⅧ-Rag 动物(小鼠) 0.25、0.5、1.0 ml药膏外用[16] 番红花叶 ↑:PMN、MNC、SOD;
↓:MDA动物(大鼠) 2 g/100g药膏外用[18] 枸杞叶 ↑:SOD;
↓:MDA动物(大鼠) 1、2、4 g/100g药膏外用[19] 温经通脉活血 肉桂 ↑:TAC、IGF-1、GLUT-1、cyclinD1 动物(小鼠) 5%、10%软膏外用[20] ↓:MDA 鸡血藤 ↓:CRP、IL-6、TNF-α 动物(大鼠) 2.0、1.0、0.5 g/ml药膏外用[21] ↑:SDF-1/CXCR4 动物(大鼠) 1 ml/100g灌服[22] 消肿排脓 黄芪 ↑:PCNA、P21WAF1 细胞(Fb) 20 g/L培养[23] 无 细胞(Fb) 20 g/L培养[24] ↑:COL-Ⅰ、COL-Ⅲ 细胞(Fb) 20 g/L培养[25] ↑:Wnt1、Wnt3a、β-catenin 动物(大鼠) 0.675 ml、1.39 ml、2.7 ml灌胃[26] ↓:TNF-α、IL-6、IL-8、hs-CRP、AOPP、MDA;
↑:GSH-PX糖尿病溃疡患者 30 ml配以250 ml生理盐水静脉滴注[27, 28] ↑:NRP-1 细胞(HaCaT) 0、0.1、0.5、1、5、10、20、50、100 mg/ml培养[29] 无 细胞(Fb) 10、40、160、640 μg/ml培养[30] 无 细胞(Fb) 10、40、160、640 μg/ml培养[31] ↓:IL-1β、MMP-2、MMP-9 细胞(Fb) 100 mg/L培养[32] ↓:SA-β-Gal 细胞(Fb) 10、40、160、640 μg/ml培养[33] 白芷 ↓:IL-1β,TNF-α、FOXO1、Ang-2、SOCS3
↑:p-AKT、p-FOXO1、SOCS1动物(小鼠) 1.8、3.6、7.2 g/kg·d灌胃[34] 止血敛疮 白及 ↓:IL-1β、TNF-α、NLRP3
↑:ROS动物(小鼠) 50 μL5%制剂外用[35] 没食子 ↓:DPPH、ABTS 动物(大鼠) 30%局部外用[36] ↓:IL-1β、IL-6、TNF-α、MDA;
↑:VEGF、Bcl-2、p53动物(小鼠) 5%、10%软膏外用[37] ↓:Set7/NF-κB 动物(小鼠) 30%药物制剂局部外用[38] ↑:p-FAK、p-JNK、p-Erk 细胞(HaCaT、MEF、HF21) 10、20、50、100和200 μM培养[39] 无 糖尿病溃疡患者 30%药物制剂局部外用[40] 注:MEF.小鼠胚胎成纤维细胞;HF21.人成纤维细胞;Fb.成纤维细胞;COL-Ⅰ.Ⅰ型胶原蛋白;COL-Ⅲ.Ⅲ型胶原蛋白;“↑”表示增加,“↓”表示减少。 -
[1] OGURTSOVA K, DA ROCHA FERNANDES J D, HUANG Y, et al IDF Diabetes Atlas: Global estimates for the prevalence of diabetes for 2015 and 2040 [J]. Diabetes Res Clin Pract2017 128 40 50 .[2] JIANG Y, HUANG S, FU X, et al Epidemiology of chronic cutaneous wounds in China [J]. Wound Repair Regen2011 19 2 181 188 .[3] CHENG B, JIANG Y, FU X, et al Epidemiological characteristics and clinical analyses of chronic cutaneous wounds of inpatients in China: Prevention and control [J]. Wound repair and regeneration : official publication of the Wound Healing Society [and] the European Tissue Repair Society,2020 28 5 623 630 .[4] AL-WAHBI A M Impact of a diabetic foot care education program on lower limb amputation rate [J]. Vasc Health Risk Manag2010 6 923 934 .[5] YAZDANPANAH L, NASIRI M, ADARVISHI S Literature review on the management of diabetic foot ulcer [J]. World J Diabetes2015 6 1 37 53 .[6] SINWAR P D The diabetic foot management - recent advance [J]. Int J Surg2015 15 27 30 .[7] KUAI L, ZHANG J T, DENG Y, et al Sheng-ji Hua-yu formula promotes diabetic wound healing of re-epithelization via Activin/Follistatin regulation [J]. BMC Complement Altern Med2018 18 1 32 .[8] 黄仁燕, 柳国斌 中医特色外治方案治疗Wagner2~4级糖尿病足溃疡临床观察 [J]. 中华中医药杂志2019 34 05 2117 2120 .[9] SUTTHAMMIKORN N, SUPAJATURA V, YUE H, et al Topical Gynura procumbens as a Novel Therapeutic Improves Wound Healing in Diabetic Mice [J]. Plants (Basel)2021 10 6 1122 .[10] 马红梅, 王莹, 兰卫 洋甘菊提取物对2型糖尿病小鼠血糖的影响及其抗氧化作用研究 [J]. 上海中医药杂志2020 54 08 77 82 .[11] 周洁, 严鹏程, 魏克民 岗梅提取物对糖尿病大鼠溃疡愈合的促进作用及其胶原、CD_(31)表达的影响 [J]. 中国中医药科技2015 22 02 156 158 .[12] 周洁, 杨钦钦, 倪茂巍, 等 岗梅提取物对高糖损伤血管内皮细胞VEGF及其受体表达影响的研究 [J]. 中国中医药科技2017 24 02 177 179 .[13] CORREA A C L, OLIVEIRA A K M, DOURADO D M, et al Pouteria ramiflora leaf extract on emulgel in wound healing activity in diabetic rats [J]. Braz J Biol2021 82 e239378 .[14] LAU T W, LAM F F, LAU K M, et al Pharmacological investigation on the wound healing effects of Radix Rehmanniae in an animal model of diabetic foot ulcer [J]. J Ethnopharmacol2009 123 1 155 162 .[15] 苑海刚, 赵钢, 贾振, 等 蓬子菜水溶液治疗糖尿病性大鼠慢性皮肤溃疡的效果及其最佳治疗浓度研究 [J]. 中国医药导报2019 16 31 26 29 .[16] 罗骞, 涂星, 廖小红 毛冬青浸膏对糖尿病溃疡模型小鼠创面修复作用及机制研究 [J]. 今日药学2016 26 10 698 702 .[17] LIU Q Q, HAN J, ZUO G Y, et al Potentiation activity of multiple antibacterial agents by Salvianolate from the Chinese medicine Danshen against methicillin-resistant Staphylococcus aureus (MRSA) [J]. J Pharmacol Sci2016 131 1 13 17 .[18] ASHJA ZADEH M A, EBRAHIMI M, SALARIAN A A, et al Evaluation of Beneficial Influence of Local Application of Crocus Pallasii Subsp. Haussknechtii Boiss. Extract on Healing of Full Thickness Excisional Infected Wounds in Diabetic Rats [J]. Bull Emerg Trauma2020 8 3 169 178 .[19] NAJI S, ZAREI L, POURJABALI M, et al The Extract of Lycium depressum Stocks Enhances Wound Healing in Streptozotocin-Induced Diabetic Rats [J]. Int J Low Extrem Wounds2017 16 2 85 93 .[20] DAEMI A, LOTFI M, FARAHPOUR M R, et al Topical application of Cinnamomum hydroethanolic extract improves wound healing by enhancing re-epithelialization and keratin biosynthesis in streptozotocin-induced diabetic mice [J]. Pharm Biol2019 57 1 799 806 .[21] 梁田, 郝文立, 甘永康, 等 鸡血藤水提物对糖尿病足模型大鼠炎症因子的影响 [J]. 天津药学2020 32 01 1 3 .[22] 刘青武. 回阳生肌汤和鸡血藤对慢性皮肤溃疡愈合过程中MSCs趋化和迁移功能的调节作用研究 [D].北京: 北京中医药大学, 2021. [23] 邓家德, 李杨, 肖正华, 等 黄芪对糖尿病足溃疡处成纤维细胞增殖作用的研究 [J]. 江西医学检验2005 05 389 392 .[24] 罗开军, 邓家德 黄芪对糖尿病足溃疡处成纤维细胞透明质酸合成酶mRNA及透明质酸的影响 [J]. 中国民族民间医药杂志2007 02 110 -112+124.[25] 邓家德, 肖正华, 凌艳英, 等 黄芪对糖尿病足溃疡处成纤维细胞合成Ⅰ、Ⅲ型胶原的影响 [J]. 海南医学2007 04 128 129 .[26] 仇莲胤. 黄芪注射液介导Wnt/β-Catenin信号通路调控表皮干细胞增殖分化促进糖尿病溃疡愈合的机制研究 [D].上海: 上海中医药大学, 2019. [27] 赵玉阳, 勾宝晶 黄芪注射液对糖尿病下肢皮肤溃疡患者血清炎症指标及氧化应激物水平的影响 [J]. 中国烧伤创疡杂志2017 29 02 109 112 .[28] 姑丽斯坦·阿不都热西提, 阿斯亚·麦麦吐逊, 阿依姆妮萨·阿卜杜热合曼 黄芪注射液对糖尿病下肢皮肤溃疡患者血清炎症指标及氧化应激指标的影响 [J]. 现代中西医结合杂志2020 29 30 3393 3396 .[29] 翁鹤. 黄芪提取液促HaCaT细胞增殖的实验研究 [D].杭州: 浙江中医药大学, 2013. [30] 周倩, 肖正华, 陈定宇, 等 糖尿病足截肢患者成纤维细胞生物学特性改变及黄芪多糖的影响 [J]. 中国糖尿病杂志2012 20 03 185 188 .[31] 周倩, 王燕, 肖正华, 等 黄芪多糖对糖尿病足溃疡成纤维细胞胶原合成的影响 [J]. 解剖学研究2011 33 02 135 137 .[32] 张正军, 肖正华, 陈定宇, 等 黄芪多糖对糖尿病足溃疡渗出液成纤维细胞MMP-2、MMP-9表达的影响 [J]. 中国糖尿病杂志2007 04 202 203 .[33] 周倩, 肖正华, 陈定宇 黄芪多糖对糖尿病足溃疡成纤维细胞β-半乳糖苷酶的影响 [J]. 实用糖尿病杂志2010 6 05 33 35 .[34] 雷思思, 胡志波, 郭俊, 等 白芷提取物促糖尿病溃疡新生血管成熟作用及机制研究 [J]. 中草药2020 51 12 3223 3233 .[35] 韩振琦, 董敬蓉, 丁文斌 白及提取物及其复方制剂的现代治疗应用 [J]. 中国农村卫生2016 20 9 10 .[36] CHOKPAISARN J, CHUSRI S, AMNUAIKIT T, et al Potential wound healing activity of Quercus infectoria formulation in diabetic rats [J]. PeerJ2017 5 e3608 .[37] DARDMAH F, FARAHPOUR M R Quercus infectoria gall extract aids wound healing in a streptozocin-induced diabetic mouse model [J]. J Wound Care2021 30 8 618 625 .[38] CHOKPAISARN J, URAO N, VORAVUTHIKUNCHAI S P, et al Quercus infectoria inhibits Set7/NF-kappaB inflammatory pathway in macrophages exposed to a diabetic environment [J]. Cytokine2017 94 29 36 .[39] YANG D J, MOH S H, SON D H, et al Gallic Acid Promotes Wound Healing in Normal and Hyperglucidic Conditions [J]. Molecules2016 21 7 899 .[40] CHOKPAISARN J, CHUSRI S, VORAVUTHIKUNCHAI S P Clinical randomized trial of topical Quercus infectoria ethanolic extract for the treatment of chronic diabetic ulcers [J]. Journal of Herbal Medicine2020 21 100301 .[41] BARMAN P K, KOH T J Macrophage Dysregulation and Impaired Skin Wound Healing in Diabetes [J]. Front Cell Dev Biol2020 8 528 . -





 下载:
下载:
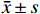
 下载:
下载:


